文档内容
湖南省名校联盟 2024-2025 学年高一下学期开学质量检测
化学
本试卷共6页。全卷满分100分,考试时间75分钟。
注意事项:
1.答题前,考生务必将自己的姓名、准考证号填写在本试卷和答题卡上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡上对应的答案标号涂黑,如有改动,
用橡皮擦干净后,再选涂其他答案;回答非选择题时,将答案写在答题卡上,写在本试卷上
无效。
3.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Na-23 Al-27 S-32 Cl-35.5 Fe-56
Cu-64 Ag-108 Ba-137
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一
项是符合题目要求的。
1. 化学品在食品加工领域用途广泛。下列说法错误的是
A. 利用维生素C的氧化性将食物中的Fe3+转化为Fe2+
B. 苏打和小苏打的水溶液均显碱性,是重要的食用碱
C. 袋装还原性铁粉可作为脱氧剂,防止富脂食品变质
D. ClO 消毒能力较强,且不会生成有害的有机氯化物,是传统液氯消毒剂的重要替代品
2
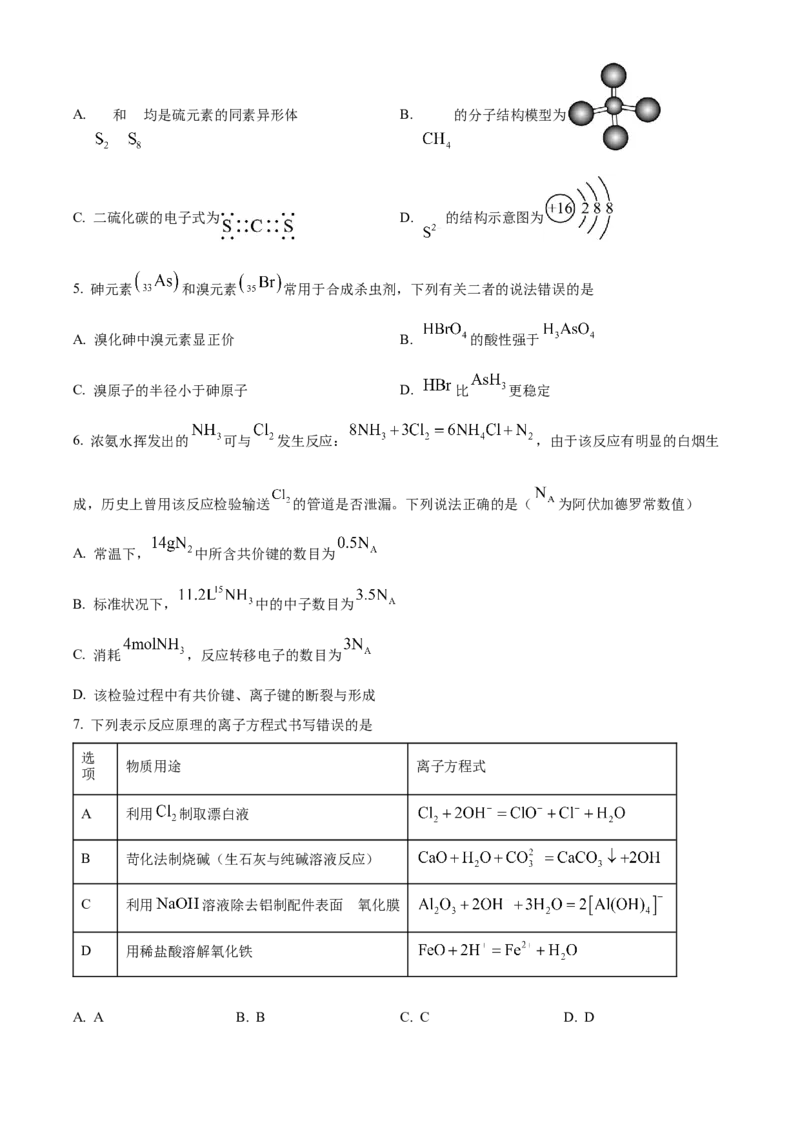
2. 下图是某科技文献上提供的螺旋形元素周期表,下列说法正确的是A. 处于图中斜线区域( ) 元素均为金属元素
的
B. 元素位于元素周期表的第四周期第IVA族
C. 元素所在族的元素统称为碱金属元素
D. 相同条件下, 比 更容易被还原
3. 海底存在丰富的固态甲烷水合物(xCH·yHO),某科研小组提出利用CO 置换甲烷水合物中的CH,实现
4 2 2 4
甲烷水合物的安全开采,其原理如图所示下列说法正确的是
A. CO 中存在非极性共价键
2
.
B HO分子通过化学键形成笼a和笼b
2
C. 甲烷水合物中的CH 无法全部被置换
4
D. 置换过程中xCH·yHO断裂极性键
4 2
4. 二硫化碳 是制作人造棉的重要原料,我国主要利用天然气生产 ,其反应为
。下列说法错误的是A. 和 均是硫元素的同素异形体 B. 的分子结构模型为
C. 二硫化碳的电子式为 D. 的结构示意图为
5. 砷元素 和溴元素 常用于合成杀虫剂,下列有关二者的说法错误的是
A. 溴化砷中溴元素显正价 B. 的酸性强于
C. 溴原子的半径小于砷原子 D. 比 更稳定
6. 浓氨水挥发出的 可与 发生反应: ,由于该反应有明显的白烟生
成,历史上曾用该反应检验输送 的管道是否泄漏。下列说法正确的是( 为阿伏加德罗常数值)
A. 常温下, 中所含共价键的数目为
B. 标准状况下, 中的中子数目为
C. 消耗 ,反应转移电子的数目为
D. 该检验过程中有共价键、离子键的断裂与形成
7. 下列表示反应原理的离子方程式书写错误的是
选
物质用途 离子方程式
项
A 利用 制取漂白液
B 苛化法制烧碱(生石灰与纯碱溶液反应)
C 利用 溶液除去铝制配件表面 的氧化膜
D 用稀盐酸溶解氧化铁
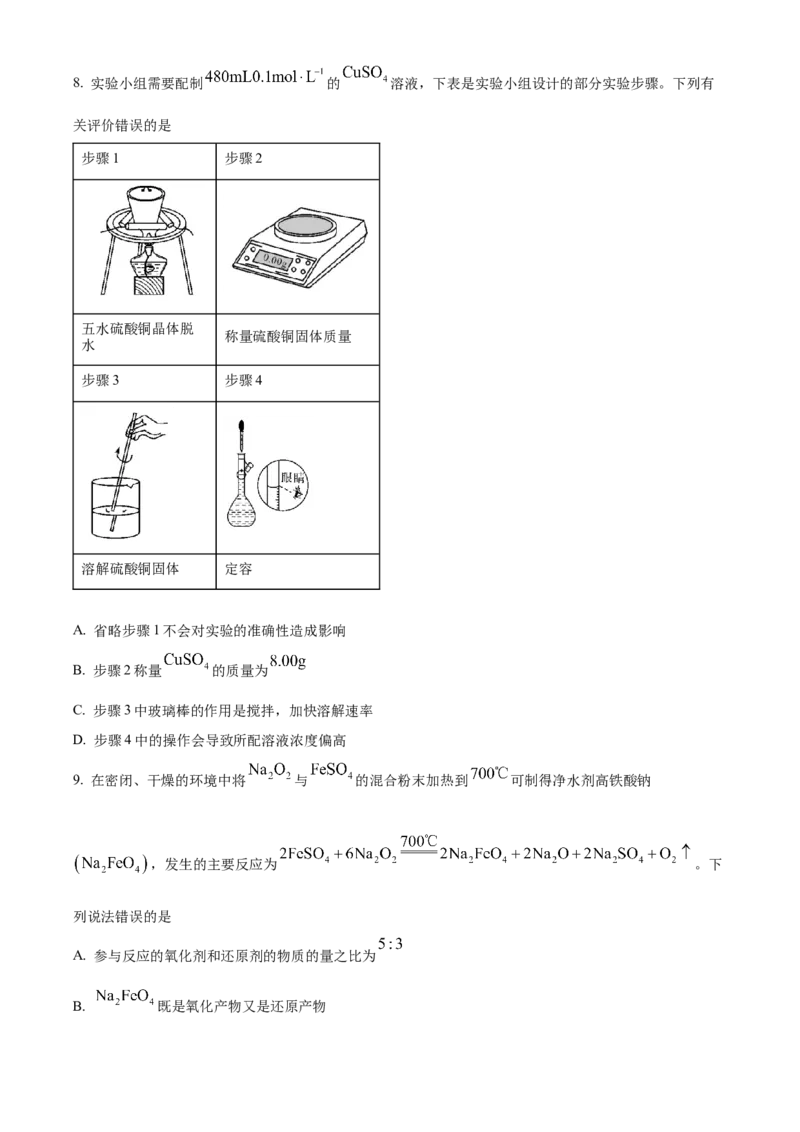
A. A B. B C. C D. D8. 实验小组需要配制 的 溶液,下表是实验小组设计的部分实验步骤。下列有
关评价错误的是
步骤1 步骤2
五水硫酸铜晶体脱
称量硫酸铜固体质量
水
步骤3 步骤4
溶解硫酸铜固体 定容
A. 省略步骤1不会对实验的准确性造成影响
B. 步骤2称量 的质量为
C. 步骤3中玻璃棒的作用是搅拌,加快溶解速率
D. 步骤4中的操作会导致所配溶液浓度偏高
9. 在密闭、干燥的环境中将 与 的混合粉末加热到 可制得净水剂高铁酸钠
,发生的主要反应为 。下
列说法错误的是
A. 参与反应的氧化剂和还原剂的物质的量之比为
B. 既是氧化产物又是还原产物C. 作氧化剂时,参与反应的 为
D. 每生成标准状况下 ,有 被氧化
10. 下列实验方案能够达到实验目的的是
选
实验目的 实验方案
项
A 制备 胶体 向 溶液中逐滴加入 饱和溶液,继续煮沸后停止加热
确定纯碱样品(含 取一定质量的纯碱样品与足量的盐酸反应,用碱石灰吸收产生的气体,
B
)的纯度 测定碱石灰的增重
将稀盐酸滴在大理石粉末表面,将产生的气体通入澄清石灰水中,观察
C 验证非金属性:
澄清石灰水是否变浑浊
取少量溶液于试管中,滴加几滴 溶液,再加入几滴淀粉溶液,观
检验 溶液中是否存
D
在 察溶液是否变蓝(已知淀粉遇 变蓝)
A. A B. B C. C D. D
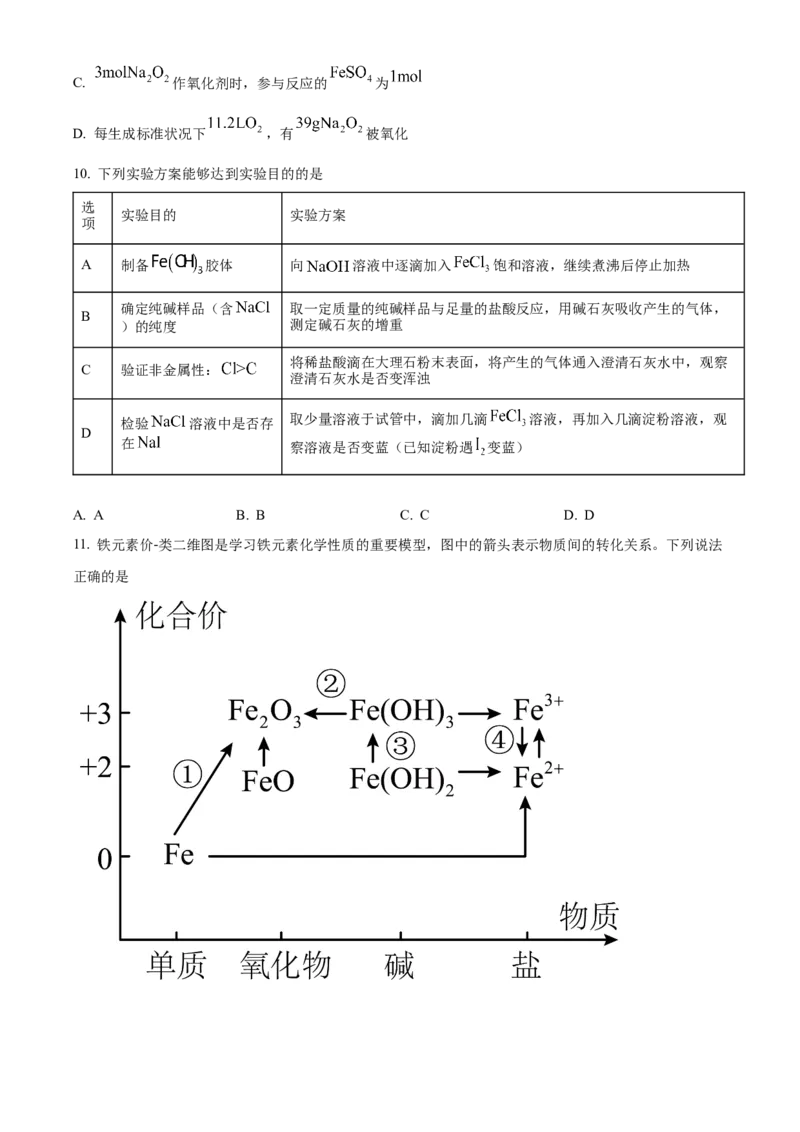
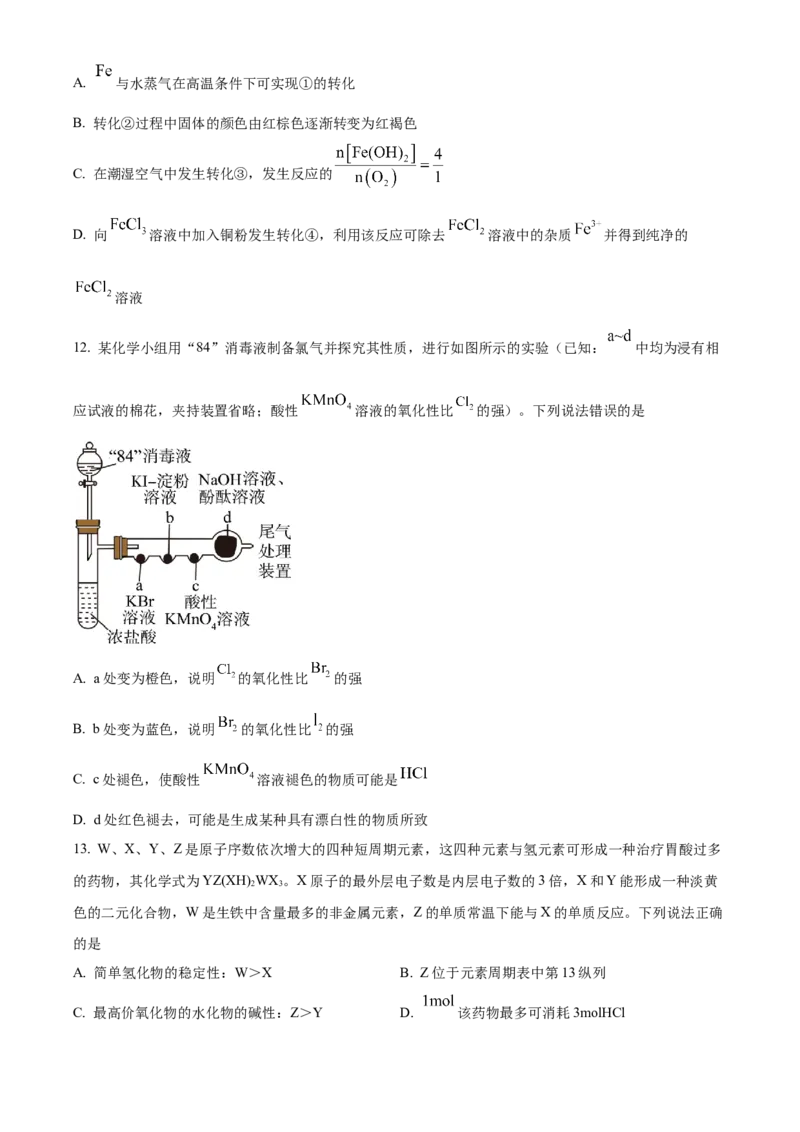
11. 铁元素价-类二维图是学习铁元素化学性质的重要模型,图中的箭头表示物质间的转化关系。下列说法
正确的是A. 与水蒸气在高温条件下可实现①的转化
B. 转化②过程中固体的颜色由红棕色逐渐转变为红褐色
C. 在潮湿空气中发生转化③,发生反应的
D. 向 溶液中加入铜粉发生转化④,利用该反应可除去 溶液中的杂质 并得到纯净的
溶液
12. 某化学小组用“84”消毒液制备氯气并探究其性质,进行如图所示的实验(已知: 中均为浸有相
应试液的棉花,夹持装置省略;酸性 溶液的氧化性比 的强)。下列说法错误的是
A. a处变为橙色,说明 的氧化性比 的强
B. b处变为蓝色,说明 的氧化性比 的强
C. c处褪色,使酸性 溶液褪色的物质可能是
D. d处红色褪去,可能是生成某种具有漂白性的物质所致
13. W、X、Y、Z是原子序数依次增大的四种短周期元素,这四种元素与氢元素可形成一种治疗胃酸过多
的药物,其化学式为YZ(XH) WX。X原子的最外层电子数是内层电子数的3倍,X和Y能形成一种淡黄
2 3
色的二元化合物,W是生铁中含量最多的非金属元素,Z的单质常温下能与X的单质反应。下列说法正确
的是
A. 简单氢化物的稳定性:W>X B. Z位于元素周期表中第13纵列
C. 最高价氧化物的水化物的碱性:Z>Y D. 该药物最多可消耗3molHCl14. 铝粉和氧化铁粉形成的混合物被称为铝热剂,常用于焊接钢轨。某实验小组设计如下实验对铝热剂的
组成进行探究。
步骤1:称取 铝热剂,并分成两等份。
步骤2:向其中的一份中加入 的 溶液,加热并搅拌,充分反应后,过滤,得滤液
中 的浓度为 (忽略溶液体积的变化),滤渣经洗涤、干燥、称量,得质量为 。
步骤3:将另一份点燃,恰好完全反应,待产物冷却后向其中加入 的盐酸,充分搅拌
至固体完全溶解,经检测溶液中的阳离子只有 ,其中 的浓度为 (忽略溶液
体积的变化)。
下列说法错误的是
A. 步骤2中生成铝盐的物质的量为 B. 步骤2中所得滤渣的质量为
C. 步骤3溶液中 D. 步骤1称取铝热剂的质量为
二、非选择题:本题共4小题,共58分。
15. 物质的分类、转化在化学中占有重要地位。现有下列几种物质:①铜;②干冰;③稀硫酸;④液态氯
化氢;⑤蔗糖;⑥ 固体;⑦氢氧化铁胶体。回答下列问题:
(1)属于分散系的是___________(填序号,下同);能够导电的纯净物是__________;属于电解质的是
__________。
(2)⑦区别于溶液和浊液的本质特征为__________,利用__________可区分胶体和溶液。
(3) 某金属氯化物 含有 氯离子,则金属M的摩尔质量为___________。
(4)实验室需要配制 的稀硫酸 ,需量取质量分数为98%、密度为 的浓硫酸
__________ (保留2位有效数字),配制过程中所需玻璃仪器除烧杯、量筒、玻璃棒、胶头滴管外,
还需要的玻璃仪器有__________。
(5)可用酸性高锰酸钾溶液处理 固体( 显 价),补全发生反应的离子方程式_________:□
☐ ☐_________☐ ☐ ☐ □_________。
16. X、Y、Z、M、Q、W为原子序数依次增大的五种短周期主族元素,元素的性质或原子结构的相关叙述如表所示,回答下列问题:
元素编
元素性质或原子结构的相关叙述
号
X 原子L层比K层多2个电子
Y 可形成空间结构呈V形的10电子氢化物
Z 短周期主族元素中原子半径最大
M 原子最外层电子数是最内层电子数的1.5倍
Q 原子L层电子数等于K、M层电子数之和
W 最高正化合价与最低负化合价代数和为6
(1)X在元素周期表中的位置是____________;它的一种核素可测定文物年代,这种核素是
____________(填核素符号)。
(2)Y、Q、W的简单离子半径依次增大的顺序为____________(用离子符号表示)。
(3)X的最高价氧化物与Z的某种氧化物反应可以生成Y的一种单质,该化学方程式为___________。Z
的这种氧化物中含有的化学键类型是____________。
(4)Q的最高价氧化物对应的水化物的水溶液与M的最高价氧化物对应的水化物反应的离子方程式为
__________。
(5)上述元素形成的最高价氧化物对应的水化物中,酸性最强的是____________(填化学式)。用电子
式表示Q的钾盐(二元化合物)的形成过程:____________。
(6)元素Z与元素M相比,金属性较强的是____________(填元素符号)。下列表述正确且能证明这一
事实的是____________(填字母)。
A.对应单质与酸反应时,每个M原子比Z原子失去的电子多
B.对应单质与水反应时,M不如Z反应剧烈
C.Z的单质可将M从其盐溶液中置换出来,反之M的单质无法将Z从其盐溶液中置换出来
D.M的最高价氧化物的熔点比Z的最高价氧化物的熔点高
17. 某工厂的工业废水中含有大量 和较多的 ,为减少污染并促进废物利用,工厂计划
从该废液中回收 和金属铜并制得明矾,请根据以下流程图,回答下列问题:已知: (过量) 。
(1)流程中的①、②物质分别是____________、____________。
(2)将明矾溶于水后再加入过量的 溶液,反应的离子方程式为____________。
(3)鉴别滤液D中的金属阳离子,下列滴加试剂顺序正确的是____________(填字母)。写出鉴别过程
中属于氧化还原反应的离子方程式:___________。
A.先滴加 溶液,后滴加新制氯水
B.先滴加新制氯水,后滴加 溶液
(4)取 滤液D于试管中,滴加足量 溶液,观察到的现象是_____________。
(5)绿矾在空气中容易被部分氧化[转化为 ,不考虑其他反应],为确定绿矾未被全部氧化,可
选择的最佳试剂是____________(填字母)。现取被部分氧化的绿矾晶体溶于稀盐酸后,加入足量的
溶液,过滤得沉淀 ,再通入 (标准状况)氯气恰好将其中的 完全氧化。计算该晶
体中 ____________。
A. 溶液 B. 溶液 C. 溶液 D.酸性 溶液
(6)某些工业废水中还含有剧毒的 ,常用绿矾在酸性条件下作还原剂来处理( 变为
),反应的离子方程式为____________。
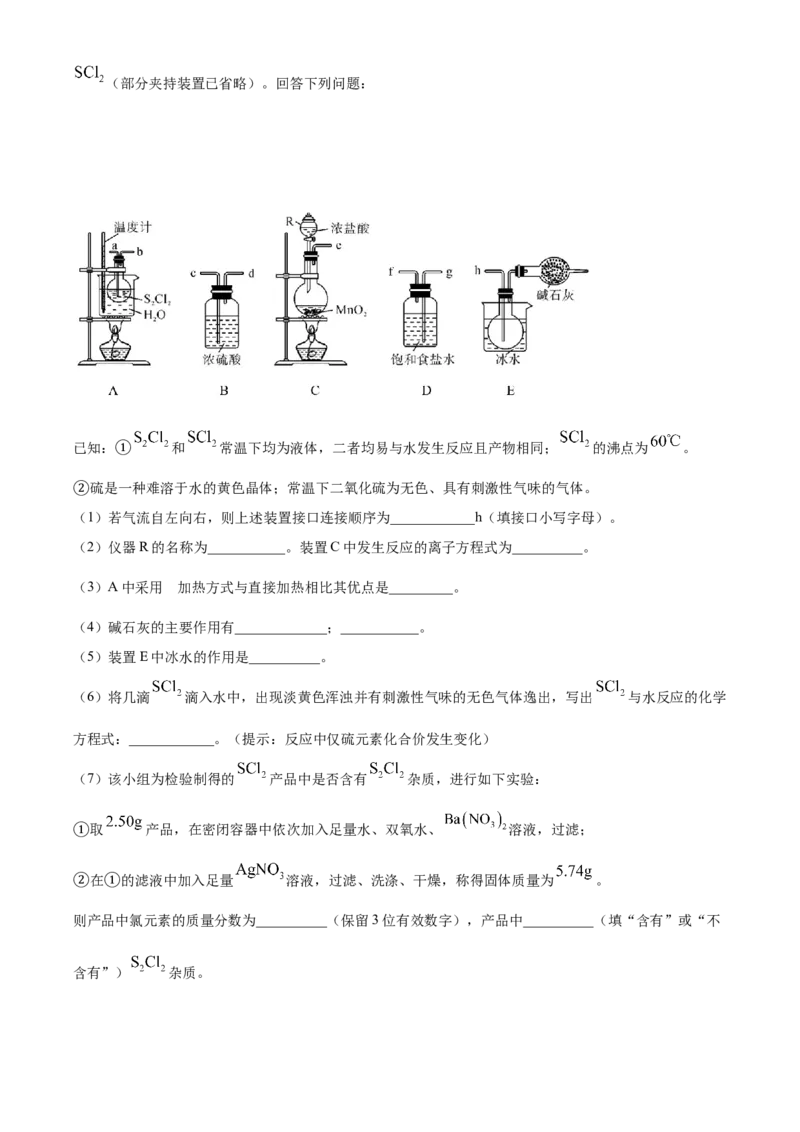
18. 将 通入 中,保持反应温度为 左右可制备 ,某实验小组利用下列装置制取少量(部分夹持装置已省略)。回答下列问题:
已知: 和 常温下均为液体,二者均易与水发生反应且产物相同; 的沸点为 。
①
硫是一种难溶于水的黄色晶体;常温下二氧化硫为无色、具有刺激性气味的气体。
②(1)若气流自左向右,则上述装置接口连接顺序为____________h(填接口小写字母)。
(2)仪器R的名称为___________。装置C中发生反应的离子方程式为__________。
的
(3)A中采用 加热方式与直接加热相比其优点是_________。
(4)碱石灰的主要作用有_____________;___________。
(5)装置E中冰水的作用是__________。
(6)将几滴 滴入水中,出现淡黄色浑浊并有刺激性气味的无色气体逸出,写出 与水反应的化学
方程式:____________。(提示:反应中仅硫元素化合价发生变化)
(7)该小组为检验制得的 产品中是否含有 杂质,进行如下实验:
取 产品,在密闭容器中依次加入足量水、双氧水、 溶液,过滤;
①
在 的滤液中加入足量 溶液,过滤、洗涤、干燥,称得固体质量为 。
② ①
则产品中氯元素的质量分数为__________(保留3位有效数字),产品中__________(填“含有”或“不
含有”) 杂质。湖南省名校联盟 2024-2025 学年高一下学期开学质量检测
化学 答案
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一
项是符合题目要求的。
【1题答案】
【答案】A
【2题答案】
【答案】A
【3题答案】
【答案】C
【4题答案】
【答案】B
【5题答案】
【答案】A
【6题答案】
【答案】C
【7题答案】
【答案】D
【8题答案】
【答案】D
【9题答案】
【答案】C
【10题答案】
【答案】D
【11题答案】
【答案】C
【12题答案】
【答案】B
【13题答案】
【答案】B
【14题答案】
【答案】D二、非选择题:本题共4小题,共58分。
【15题答案】
【答案】(1) ①. ③⑦ ②. ① ③. ④⑥
(2) ①. 分散质粒子的直径在 之间 ②. 丁达尔效应
(3)
.
(4) ① 5.4 ②. 容量瓶
(5)8 5 44 10 5 8 22
【16题答案】
【答案】(1) ①. 第二周期第 族 ②.
(2)
(3) ①. ②. 离子键、非极性(共价)键(或离子键、共价
键)
(4)
(5) ①. ②.
(6) ①. ②. B
【17题答案】
【答案】(1) ①. ②. 粉(或铁粉)
(2)
(3) ①. A ②.
(4)先生成白色沉淀,然后沉淀迅速变为灰绿色,最后变为红褐色(答案合理即可)
(5) ①. D ②.(6)
【18题答案】
【答案】(1)egfcdab
(2) ①. 分液漏斗 ②.
(3)受热均匀,便于控制温度
(4) ①. 吸收多余的 ,防止污染环境 ②. 防止空气中的水蒸气进入装置E的烧瓶中与 发
生反应
(5)使 冷凝为液体,减少挥发
(6)
(7) ①. 56.8% ②. 含有