文档内容
鲁科版(2019)必修第一册第三章第1节 铁的多样性课时
训练一
学校:___________姓名:___________班级:___________考号:___________
一、单选题
1.在给定条件下,下列物质间的转化均能实现的有
①
②
③
④
⑤
⑥
⑦
A.2个 B.3个 C.4个 D.5个
2.为了探究铁、铜及其化合物的性质,某同学设计并进行了下列实验。下列说法中错
误的是
A.乙装置中的反应为:3Fe+4H O(g) Fe O+4H
2 3 4 2
B.虚线框处宜选择的装置是丙
C.实验后,可用铝粉在高温下还原玻璃管中的固体获得铁单质
D.实验时将螺旋状铜丝加热,变黑后再趁热迅速伸入试管中,可观察到铜丝由黑色
变为红色
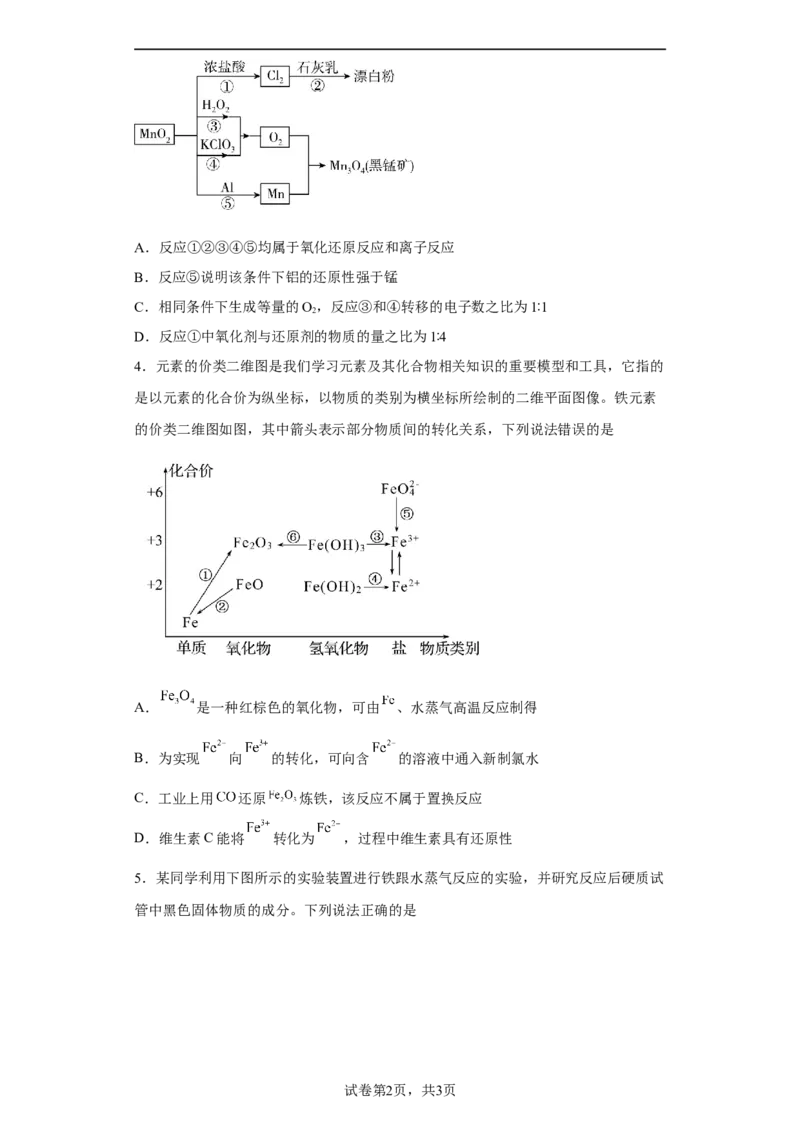
3.根据如图所示的转化关系(反应条件已略去)判断,下列说法正确的是A.反应①②③④⑤均属于氧化还原反应和离子反应
B.反应⑤说明该条件下铝的还原性强于锰
C.相同条件下生成等量的O,反应③和④转移的电子数之比为1∶1
2
D.反应①中氧化剂与还原剂的物质的量之比为1∶4
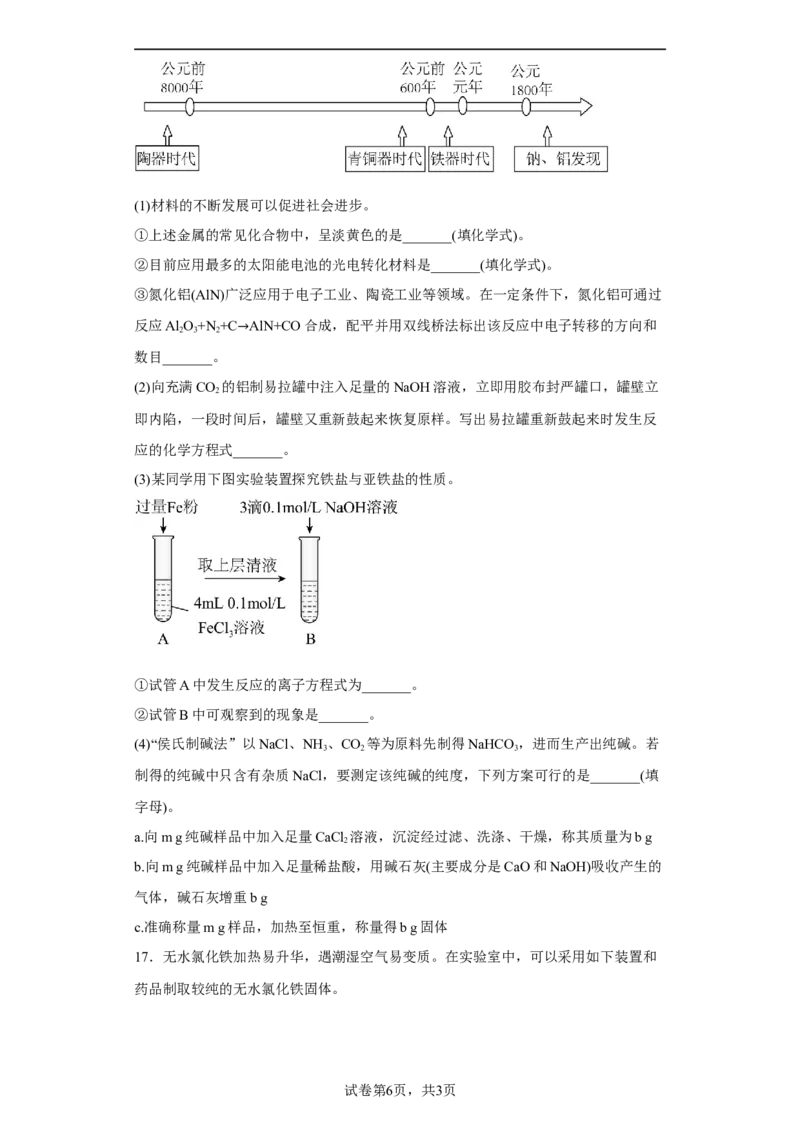
4.元素的价类二维图是我们学习元素及其化合物相关知识的重要模型和工具,它指的
是以元素的化合价为纵坐标,以物质的类别为横坐标所绘制的二维平面图像。铁元素
的价类二维图如图,其中箭头表示部分物质间的转化关系,下列说法错误的是
A. 是一种红棕色的氧化物,可由 、水蒸气高温反应制得
B.为实现 向 的转化,可向含 的溶液中通入新制氯水
C.工业上用 还原 炼铁,该反应不属于置换反应
D.维生素C能将 转化为 ,过程中维生素具有还原性
5.某同学利用下图所示的实验装置进行铁跟水蒸气反应的实验,并研究反应后硬质试
管中黑色固体物质的成分。下列说法正确的是
试卷第2页,共3页A.观察到肥皂水中产生气泡说明该反应中已经有氢气生成
B.向反应后的固体加入稀硫酸使其完全溶解,若滴加KSCN溶液后不变红色,说明
没有生成
C.向反应后的固体加入稀硫酸使其完全溶解,若滴加铁氰化钾溶液后出现蓝色沉淀,
说明铁粉未完全反应
D.排除氧气干扰的条件下,将反应后的固体用稀硫酸溶解,若滴加KSCN溶液后变
红色,说明黑色固体中可能有
6.下列说法不正确的是
A.铁在一定条件下与纯氧气或水蒸气反应的共同产物可能是
B.铁是人体必需微量元素中含量最多的一种
C.铁的化学性质活泼,所以铁在自然界中全部以化合态存在
D.铁在高温下与水蒸气发生的反应是置换反应
7.纯净铁的物理性质有
①光亮的银白色 ②黑色 ③在潮湿的空气中易被腐蚀 ④有延展性 ⑤能导电导热
⑥硬而脆 ⑦能被磁铁吸,引易被磁化
A.①③④⑤⑦ B.①④⑤⑦ C.①③⑤⑦ D.全部
8.用 代表阿伏加德罗常数的数值,下列说法正确的是
A.3mol单质Fe与足量水蒸气在高温下完全反应,失去9 个电子
B.2g氘化锂( )中含中子数为
C.2.24L 与足量的 充分反应,转移电子数为0.1D.56g Fe与足量硫粉充分反应转移电子数为3
9.类比的思维方法常用于预测物质的结构与性质,下列类比分析结果正确的是
A.Mg条能在CO 中剧烈燃烧,则Na也能与CO 反应
2 2
B.Fe丝在Cl 中燃烧生成FeCl ,则Fe粉和硫粉反应的产物为Fe S
2 3 2 3
C.Fe O 为碱性氧化物,则Al O 也为碱性氧化物
2 3 2 3
D.Cl 与Fe加热生成FeCl ,则I 与Fe加热生成FeI
2 3 2 3
10.下列方程式与所给事实相符的是
A.用食醋除水垢:
B.向 中滴加 至 沉淀完全:
C.向稀硝酸中加入过量铁粉:
D.乙酸、乙醇和浓硫酸共热,产生有香味的油状液体:
11.将过量的金属铁投入灼热的浓硫酸中,下列判断正确的是
A.会立即生成
B.会立即生成 ,且只生成
C.除了 外,还会有 产生
D.金属铁表面因生成致密氧化膜而使反应不能继续进行
12.某稀硫酸和稀硝酸的混合溶液200mL,平均分成两等份。向其中一份中逐渐加入
铜粉,最多能溶解19.2g(已知硝酸只被还原为NO气体)。向另一份中逐渐加入铁粉,
产生气体的量随铁粉质量增加的变化如图所示。下列分析或结果不正确的是
A.OA段产生的是NO,AB段发生的反应为Fe+2Fe3+=3Fe2+,BC段产生氢气
试卷第4页,共3页B.原混合酸中NO 物质的量为0.4mol
C.反应结束后,第一份溶液中的溶质为CuSO 和HSO
4 2 4
D.取20mL原混合酸加水稀释至1L,溶液中c(H+)=0.1mol/L
13.下列离子方程式中不正确的是
A.将稀硫酸滴在铁片上:
B.将氧化铝加入稀盐酸中:
C.向硫酸亚铁溶液加入铁粉防止其氧化:
D.将铜片插入硝酸银溶液中:
14.将 镁铁合金加入 稀盐酸中恰好完全反应,得到标准状况下氢气 。
下列有关说法正确的是
A.该合金中镁、铁的物质的量之比为
B.反应中转移电子
C.该盐酸的物质的量浓度为
D.将标准状况下 气体溶于 水中即可配制成该盐酸
15.下列解释事实的方程式不正确的是
A.氯气与氯化亚铁溶液发生反应:
B.加热碳酸氢钠固体质量减轻:
C.碳酸钙沉淀溶于稀硝酸:
D.红热的铁与水蒸气发生反应:
二、实验题
16.如图是部分金属和非金属材料发现和使用的时间简轴。(1)材料的不断发展可以促进社会进步。
①上述金属的常见化合物中,呈淡黄色的是_______(填化学式)。
②目前应用最多的太阳能电池的光电转化材料是_______(填化学式)。
③氮化铝(AlN)广泛应用于电子工业、陶瓷工业等领域。在一定条件下,氮化铝可通过
反应Al O+N +C AlN+CO合成,配平并用双线桥法标出该反应中电子转移的方向和
2 3 2
数目_______。 →
(2)向充满CO 的铝制易拉罐中注入足量的NaOH溶液,立即用胶布封严罐口,罐壁立
2
即内陷,一段时间后,罐壁又重新鼓起来恢复原样。写出易拉罐重新鼓起来时发生反
应的化学方程式_______。
(3)某同学用下图实验装置探究铁盐与亚铁盐的性质。
①试管A中发生反应的离子方程式为_______。
②试管B中可观察到的现象是_______。
(4)“侯氏制碱法”以NaCl、NH 、CO 等为原料先制得NaHCO ,进而生产出纯碱。若
3 2 3
制得的纯碱中只含有杂质NaCl,要测定该纯碱的纯度,下列方案可行的是_______(填
字母)。
a.向m g纯碱样品中加入足量CaCl 溶液,沉淀经过滤、洗涤、干燥,称其质量为b g
2
b.向m g纯碱样品中加入足量稀盐酸,用碱石灰(主要成分是CaO和NaOH)吸收产生的
气体,碱石灰增重b g
c.准确称量m g样品,加热至恒重,称量得b g固体
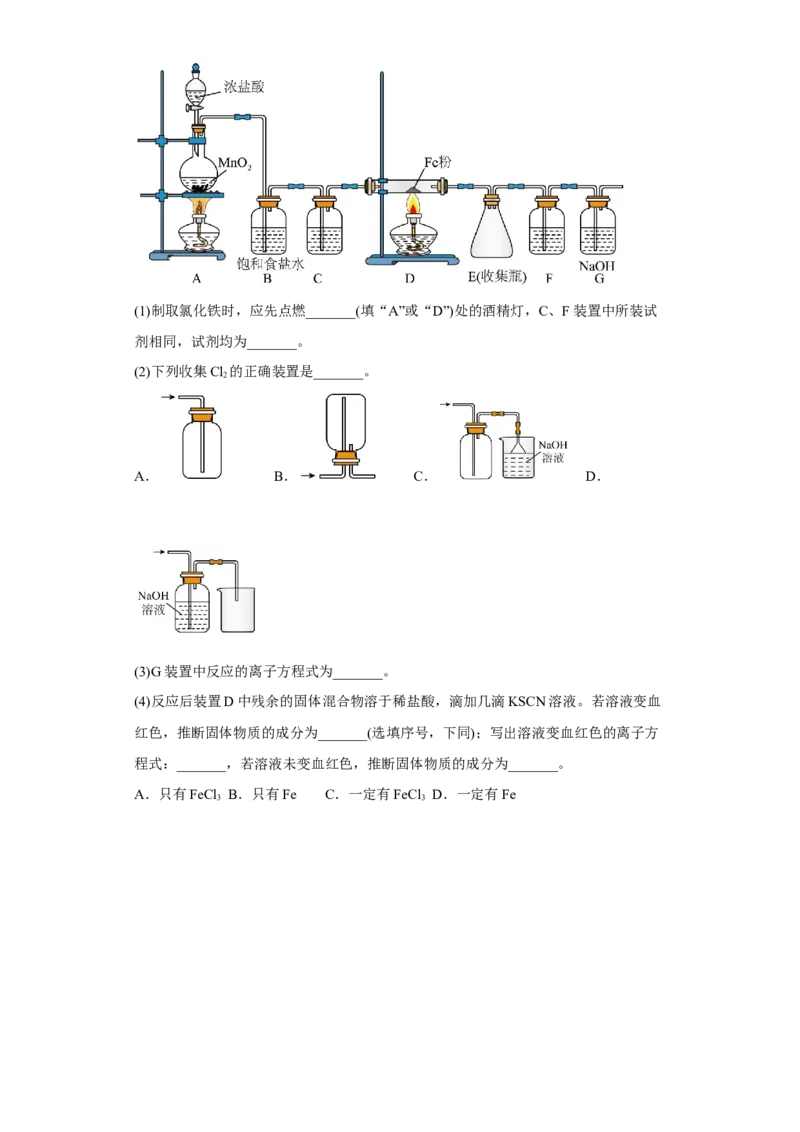
17.无水氯化铁加热易升华,遇潮湿空气易变质。在实验室中,可以采用如下装置和
药品制取较纯的无水氯化铁固体。
试卷第6页,共3页(1)制取氯化铁时,应先点燃_______(填“A”或“D”)处的酒精灯,C、F装置中所装试
剂相同,试剂均为_______。
(2)下列收集Cl 的正确装置是_______。
2
A. B. C. D.
(3)G装置中反应的离子方程式为_______。
(4)反应后装置D中残余的固体混合物溶于稀盐酸,滴加几滴KSCN溶液。若溶液变血
红色,推断固体物质的成分为_______(选填序号,下同);写出溶液变血红色的离子方
程式:_______,若溶液未变血红色,推断固体物质的成分为_______。
A.只有FeCl B.只有Fe C.一定有FeCl D.一定有Fe
3 3参考答案:
1.C
【详解】①NaHCO 受热分解成NaCO、CO 和HO,NaCO 与饱和石灰水反应生成
3 2 3 2 2 2 3
CaCO 和NaOH,两步反应均能实现,故①正确;
3
②Al与NaOH溶液反应生成NaAlO 和H,NaAlO 与过量盐酸反应生成NaCl、AlCl 和
2 2 2 3
HO,第二步反应不能实现,故②错误;
2
③钠与氧气点燃生成过氧化钠,过氧化钠与水反应生成氢氧化钠和氧气,两步反应均能实
现,故③正确;
④Al与Fe O 高温发生铝热反应生成Al O 和Fe,Fe与HCl反应生成FeCl 和H,第二步反
2 3 2 3 2 2
应不能实现,故④错误;
⑤硫与氧气点燃生成二氧化硫,二氧化硫与氯化钡溶液不反应,第二步反应不能实现,故
⑤错误;
⑥氯化镁与石灰乳转化为更难溶的氢氧化镁,Mg(OH) 不稳定,加热分解为 MgO ,故两
2
步都可以实现,故⑥正确;
⑦铝与四氧化三铁高温条件反应生成氧化铝和铁,氧化铝与氢氧化钠溶液反应生成偏铝酸
钠和水,两步反应均能实现,故⑦正确;
①③⑥⑦正确,故选C。
2.B
【详解】A.甲装置提供水蒸气,乙装置是铁和水蒸气反应,其反应的方程式为:
3Fe+4H O(g) Fe O+4H ,故A正确;
2 3 4 2
B.生成的氢气的密度比空气的密度小,用向下排空气法收集氢气,因此选丁装置,故B
错误;
C.实验后,玻璃管中的固体主要是四氧化三铁,铝粉与四氧化三铁发生铝热反应,因此
可用铝粉在高温下还原玻璃管中的固体获得铁单质,故C正确;
D.实验时将螺旋状铜丝加热,变黑后再趁热迅速伸入试管中,变色的物质为氧化铜,氧
化铜和氢气加热条件下反应生成铜和水,因此可观察到铜丝由黑色变为红色,故D正确。
综上所述,答案为B。
3.B
【分析】①为二氧化锰与浓盐酸反应生成氯气、氯化锰、水;②为氯气与石灰乳反应生成氯化钙、次氯酸钙、水;
③为过氧化氢分解生成水和氧气;
④为氯酸钾分解生成氯化钾和氧气;
⑤为铝和二氧化锰反应铝热反应生成Mn和氧化铝,均存在元素的化合价变化;据此分析。
【详解】A.由上述分析可知,①②③④⑤均属于氧化还原反应,但⑤不是离子反应,A
错误;
B.⑤为铝热反应,Al 失去电子,为还原剂,Mn为还原产物,则还原性:Al>Mn,B正确;
C.由关系式: ,可知,生成等量的O,反应③和
2
④转移的电子数之比为1∶2,C错误;
D.MnO +4HCl(浓) MnCl +Cl↑+2H O,锰元素的化合价降低,氯元素的化合价升高,
2 2 2 2
4molHCl中只有2mol HCl作还原剂,则氧化剂与还原剂的物质的量之比为1∶2,D错误;
故本题选B。
4.A
【详解】A. 是一种黑色的氧化物,可由 、水蒸气高温反应制得,A错误;
B.Fe2+转化成Fe3+,铁元素的化合价升高,需要加入新制氯水等氧化剂才能实现转化,B
正确;
C.置换反应是一种单质和一种化合物反应生成新的单质和化合物的反应,工业上用 还
原 炼铁,该反应不属于置换反应,C正确;
D.维生素C能将 还原为 ,过程中维生素表现还原性,D正确;
故选A。
5.D
【详解】A.在导管末端会产生大量的肥皂泡,用燃着的火柴靠近肥皂泡,有爆鸣声才能
说明是氢气,故A错误;
B.若滴加KSCN溶液后不变红色,说明不含三价铁离子,但由于铁粉能把三价铁离子还
原成二价铁离子,不能确定黑色粉末是否含有Fe O,故B错误;
3 4
C.若滴加铁氰化钾溶液后出现蓝色沉淀,说明含有二价铁离子,不能确定二价铁离子来
自铁粉还是Fe O,故C错误;
3 4
D.若滴加KSCN溶液后变红色,说明含三价铁离子,说明黑色固体中可能有 ,故D
答案第2页,共2页正确;
故选D。
6.C
【详解】A.铁与纯氧气反应生成四氧化三铁,在高温条件下Fe粉和水蒸气可以反应,生
成产物为Fe O 和H,故A正确;
3 4 2
B.铁是人体必需微量元素中含量最多的一种,故B正确;
C.陨铁是单质铁,在自然界中以游离态存在的铁,故C错误;
D.Fe粉在高温下和水蒸气可以反应生成Fe O 和H,特征为单质和化合物反应生成另一
3 4 2
种单质和另一种化合物,属于置换反应,故D正确;
故选:C。
7.B
【详解】纯净的铁为银白色固体,具有很强的抗腐蚀能力,具有延展性,能导电导热,能
被磁铁吸,引易被磁化;只有①④⑤⑦符合题意,故答案选B。
8.B
【详解】A.3mol单质Fe与足量水蒸气在高温下完全反应生成四氧化三铁,失去8 个电
子,A错误;
B.2g氘化锂( )中含中子数为 ,B正确;
C.标准状况下,2.24L 与足量的 充分反应,转移电子数为0.1 ,题中没有标
准状况,无法就算,C错误;
D.56g Fe与足量硫粉充分反应生成FeS,转移电子数为2 ,D错误;
故答案选B。
9.A
【详解】A.金属性:Na>Mg,Na比Mg的化学性质活泼,Mg条能在CO 中剧烈燃烧,则
2
Na也能与CO 反应,故A正确;
2
B.S和Fe反应生成低价金属,即只生成FeS,故B错误;
C.Al O 既能和酸反应也能和碱反应,属于两性氢氧化物,故C错误;
2 3
D.I 的氧化性较弱,与Fe加热生成FeI,故D错误;
2 2
故选A。10.B
【详解】A.食醋中的主要成分是弱酸醋酸,不能拆,A错误;
B.硫酸根将钡离子完成沉淀时引入了等物质的量的氢离子,只能中和等物质的量的氢氧
根,方程式为: ,B正确;
C.过量的铁粉会将三价铁离子还原成二价的亚铁,C错误;
D.酯化反应的断键机理是酸脱羟基醇脱氢,故水分子中的氧元素来自酸未标记,D错误;
故选B。
11.C
【分析】将过量的金属铁投入灼热的浓硫酸中,首先发生反应:
,由于氧化性:铁离子大于氢离子,然
后发生反应:Fe+Fe (SO )=3FeSO,最后发生:Fe+H SO =FeSO+H ↑。
2 4 3 4 2 4 4 2
【详解】A.根据分析可知,会立即生成SO ,最后生成H,A错误;
2 2
B.根据分析可知,会立即生成SO ,最后生成H,B错误;
2 2
C.根据分析可知,会立即生成SO ,最后生成H,C正确;
2 2
D.金属铁与冷的浓硫酸会发生钝化现象,加热时会继续反应,D错误;
故答案选C。
12.D
【分析】由图象可以知道,因为铁过量,OA段发生反应为Fe+NO +4H+=Fe3+
+NO↑+2HO,AB段发生反应为Fe+2Fe3+=3Fe2+,BC段发生反应为Fe+2H+=Fe2++H ↑,据此
2 2
分析解答。
【详解】A.由图象可以知道,因为铁过量,OA段发生反应为Fe+NO +4H+=Fe3+
+NO↑+2HO,AB段发生反应为Fe+2Fe3+=3Fe2+,BC段发生反应为Fe+2H+=Fe2++H ↑,A正
2 2
确;
B.OA段发生反应为Fe+NO +4H+=Fe3+ +NO↑+2HO,硝酸全部起氧化剂作用,所以
2
n(NO )= 2n(Fe)= 2× ,B正确;
答案第4页,共2页C.硝酸全部被还原,没有显酸性的硝酸,因为溶液中有硫酸根,并且铁单质全部转化为
亚铁离子,所以溶液中最终溶质为FeSO ,C正确;
4
D.反应消耗22.4g铁,其物质的量 ,所有的铁都在硫酸亚铁中,根据硫
酸根守恒每份含硫酸0.4mol,200mL原溶液中含有0.8mol硫酸、0.4molHNO ,原混合液中
3
含有氢离子的总物质的量= 0.8mol×2 + 0.4mol= 2mol,取出20mL溶液中含有氢离子的物质
的量为0.2mol,稀释过程中氢离子的物质的量不变,则稀释至1 L后溶液c(H+)= =
0.2mol·L-1,D错误;
故答案选D。
13.C
【详解】A.将稀硫酸滴在铁片上,发生置换反应,生成硫酸亚铁和氢气:
,A正确;
B.将氧化铝加入稀盐酸中,发生复分解反应,生成氯化铝和水:
,B正确;
C.硫酸亚铁溶液露置在空气中,若Fe2+被氧化为Fe3+,铁粉能将Fe3+还原为Fe2+,从而防
止其被氧化: ,C不正确;
D.将铜片插入硝酸银溶液中,发生置换反应,生成硝酸铜和银: ,
D正确;
故选C。
14.C
【分析】将8.0g镁铁合金加入500mL稀盐酸中恰好完全反应,得到标准状况下氢气
4.48L,发生的反应为:Mg+2HCl=MgCl +H↑、Fe+2HCl=FeCl +H↑,设镁、铁的物
2 2 2 2质的量分别为xmol和ymol,则 ,解得x=y=0.1,据
此分析解题。
【详解】A.该合金中镁、铁的物质的量之比为0.1mol:0.1mol=1:1,故A错误;
B.反应中,生成0.2mol氢气,转移电子为0.4mol,故B错误;
C.n(HCl)=2n(金属)=2×(0.1mol+0.1mol)=0.4mol,则盐酸的物质的量浓度为
,故C正确;
D.将标准状况下8.96L HCl气体溶于500mL水中,形成的盐酸的体积不知道,因为溶液
的体积不等于水的体积,所以无法计算溶液的物质的量浓度,故D错误;
故答案选选C。
【点睛】本题考查了有关方程式的计算、混合物的计算,把握发生反应方程式、物质的量
的计算、物质的量浓度的计算是解题的关键。
15.C
【详解】A.氯气与氯化亚铁溶液发生反应生成氯化铁:2Fe2++Cl=2Fe3++2Cl−,故A正确;
2
B.加热碳酸氢钠固体质量减轻,因为碳酸氢钠固体受热分解产生二氧化碳和水:
,故B正确;
C.碳酸钙沉淀溶于稀硝酸,碳酸钙难溶于水,不可拆:
,故C错误;
D.红热的铁与水蒸气发生反应:3Fe+4H O(g) Fe O+4H ,故D正确;
2 3 4 2
故选C。
16.(1) Na O Si
2 2
(2)2Al+2NaOH+2H O=2NaAlO +3H ↑
2 2 2
答案第6页,共2页(3) 2Fe3++Fe=3Fe2+ 有白色沉淀产生,沉淀迅速变为灰绿色,最终变为红褐色
(4)a
【分析】FeCl 溶液呈棕黄色,加入过量Fe粉后,Fe3+被还原为Fe2+,此时溶液变为浅绿色;
3
往溶液中加入NaOH溶液,起初生成Fe(OH) 白色沉淀,随后有一部分Fe(OH) 被溶解的空
2 2
气中的氧气氧化为Fe(OH) ,此时沉淀变为灰绿色,最终固体变为红褐色。
3
【详解】(1)①上述金属的常见化合物中,只有钠燃烧生成的过氧化钠呈淡黄色,所以呈
淡黄色的是NaO。
2 2
②硅是良好的半导体材料,能发生光电效应,可用于生产太阳能电池,目前应用最多的太
阳能电池的光电转化材料是Si。
③在一定条件下,生产氮化铝的反应为Al O+N +3C=2AlN+3CO,用双线桥法标出该反应
2 3 2
中电子转移的方向和数目为 。答案为:NaO;
2 2
Si; ;
(2)向充满CO 的铝制易拉罐中注入足量的NaOH溶液,起初NaOH吸收CO 气体,使罐
2 2
内压强减小,罐壁内陷;随后,铝与氢氧化钠溶液反应生成氢气等,一段时间后,罐壁又
重新鼓起来恢复原样,此时发生反应的化学方程式为2Al+2NaOH+2H O=2NaAlO +3H ↑。
2 2 2
答案为:2Al+2NaOH+2H O=2NaAlO +3H ↑;
2 2 2
(3)①试管A中,铁还原氯化铁生成氯化亚铁,反应的离子方程式为2Fe3++Fe=3Fe2+。
②由分析可知,先生成Fe(OH) ,然后发生部分变质,最后发生完全变质,则试管B中可
2
观察到的现象是:有白色沉淀产生,沉淀迅速变为灰绿色,最终变为红褐色。答案为:
2Fe3++Fe=3Fe2+;有白色沉淀产生,沉淀迅速变为灰绿色,最终变为红褐色;
(4)a.向m g纯碱样品中加入足量CaCl 溶液,由CaCO 的质量为b g,可求出NaCO 的
2 3 2 3质量,从而求出纯碱样品的纯度,a可行;
b.向m g纯碱样品中加入足量稀盐酸,碱石灰吸收CO 和水蒸气共b g,由于二者组成不确
2
定,无法求出CO 的物质的量,也就无法求出NaCO 的质量,从而无法求出纯碱的纯度,
2 2 3
b不可行;
c.准确称量m g样品,加热至恒重,由于样品中碳酸钠、氯化钠都不分解,b g固体仍为碳
酸钠、氯化钠混合物的质量,所以无法求出NaCO 的质量,最终无法求出纯碱的纯度,c
2 3
不可行;
故选a。答案为:a。
【点睛】在铝与氢氧化钠溶液的反应中,氢氧化钠只表现出碱性,不表现出氧化性。
17.(1) A 浓硫酸
(2)C
(3)Cl +2OH—=Cl—+ClO—+H O
2 2
(4) C Fe3++3SCN—=Fe (SCN) D
3
【分析】由实验装置图可知,装置A中二氧化锰与浓盐酸共热反应制备氯气,浓盐酸具有
挥发性,制得的氯气中混有氯化氢和水蒸气,装置B中盛有的饱和食盐水用于除去氯化氢
气体,装置C中盛有的浓硫酸用于干燥氯气,装置D中铁与氯气共热反应制备氯化铁,装
置E为氯化铁冷凝收集装置,装置F中盛有的浓硫酸用于吸收水蒸气,防止水蒸气进入装
置E中,装置G盛有的氢氧化钠溶液用于吸收未反应的氯气,防止污染空气。
【详解】(1)为防止铁与装置中空气中的氧气反应,制取氯化铁时,应先点燃A处酒精
灯,利用反应生成的氯气排尽装置中的氧气后,再点燃D处的酒精灯;由分析可知,装置
C中盛有的浓硫酸用于干燥氯气,装置F中盛有的浓硫酸用于吸收水蒸气,防止水蒸气进
入装置E中,目的是防止氯化铁遇潮湿空气易变质,故答案为:浓硫酸;
(2)A.收集气体时,集气瓶不能用橡胶塞堵住,应用双孔橡胶塞有利于空气排出,故A
错误;
B.氯气密度大于空气,应用向上排空气法收集氯气,且氯气有毒不能直接排放,应有尾
气吸收装置,故B错误;
C.氯气密度大于空气,收集装置可用于收集比空气密度大的氯气,盛有氢氧化钠溶液的
烧杯可用于吸收氯气,防止污染空气,故C正确;
D.氯气能与氢氧化钠溶液反应,将氯气先通入氯气无法收集得到氯气,故D错误;
故选C;
答案第8页,共2页(3)由分析可知,装置G盛有的氢氧化钠溶液用于吸收未反应的氯气,防止污染空气,
反应的离子方程式为Cl+2OH—=Cl—+ClO—+H O,故答案为:Cl+2OH—=Cl—+ClO—+H O;
2 2 2 2
(4)反应后装置D中残余的固体混合物溶于稀盐酸,滴加几滴硫氰化钾溶液,若溶液变
血红色说明固体中含有氯化铁,氯化铁溶液与硫氰化钾溶液反应生成硫氰化铁和氯化钾,
反应的离子方程式为Fe3++3SCN—=Fe (SCN) ,若溶液未变血红色说明铁粉未完全反应,固
3
体中含有氯化铁和铁,铁与溶液中的铁离子反应生成亚铁离子,故答案为:C;Fe3++3SCN
—=Fe (SCN) ;D。
3答案第10页,共2页