文档内容
必修第一册 第二章 第二节 氯及其化合物 测试题
榆次一中 李金虎
一、选择题(每小题只有一个正确选项,每小题4分,共40分)
1. 下列说法正确的是( )
A.Cl 的性质活泼,与H 混合后立即发生爆炸
2 2
B.实验室制取Cl 时,为了防止环境污染,多余的Cl 可以用NaOH溶液吸收
2 2
C.检验HCl气体中是否混有Cl,方法是将气体通入AgNO 溶液中
2 3
D.除去HCl气体中的Cl,可将气体通入饱和食盐水中
2
2. 用自来水养金鱼时,通常先将自来水晒一段时间再注入鱼缸,目的是( )
A.提高水温 B.增加水中氧气的含量
C.除去水中少量的次氯酸 D.用紫外线杀死水中的细菌
3. 在探究新制氯水成分及性质的实验中,依据下列方法和现象,不能得出相应结论的是( )
选项 方法 现象 结论
A 观察氯水颜色 氯水呈浅黄绿色 氯水中含Cl
2
B 向饱和NaHCO 溶液中加入足量氯水 有无色气体产生 氯水中含HClO
3
C 向红色纸条上滴加氯水 红色纸条褪色 氯水具有漂白性
D 向FeCl 溶液中滴加氯水 溶液变成棕黄色 氯水具有氧化性
2
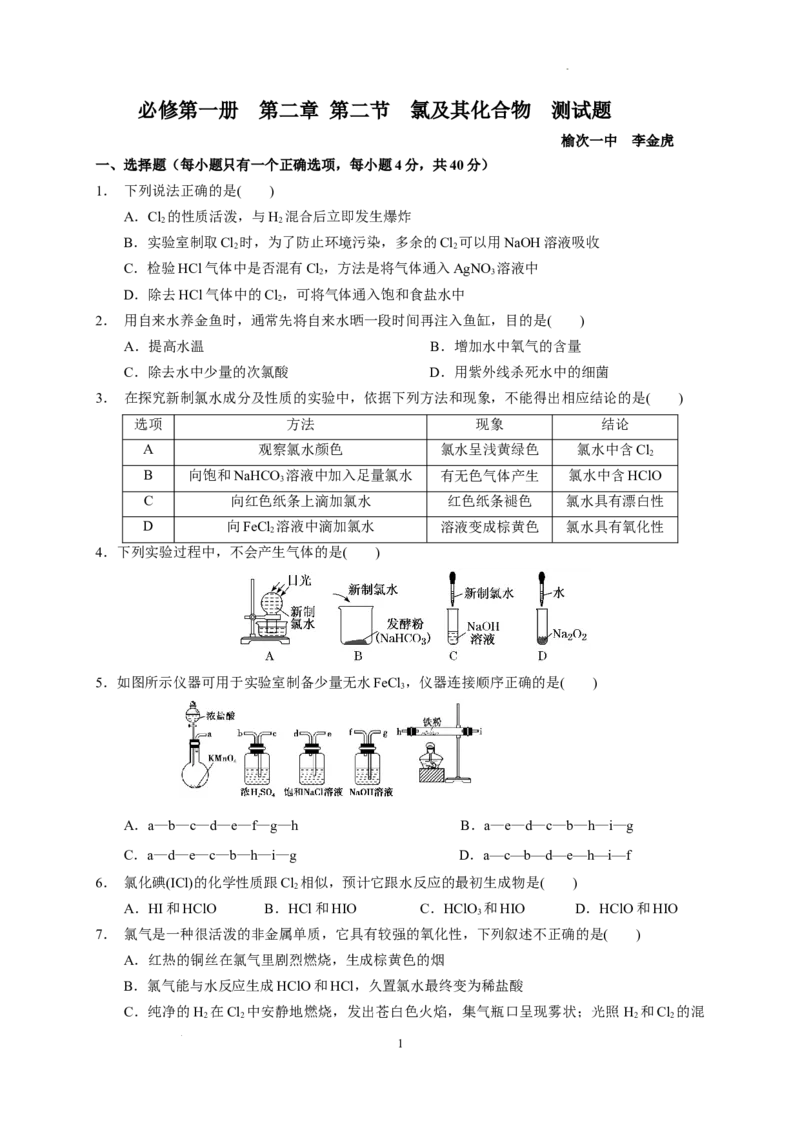
4.下列实验过程中,不会产生气体的是( )
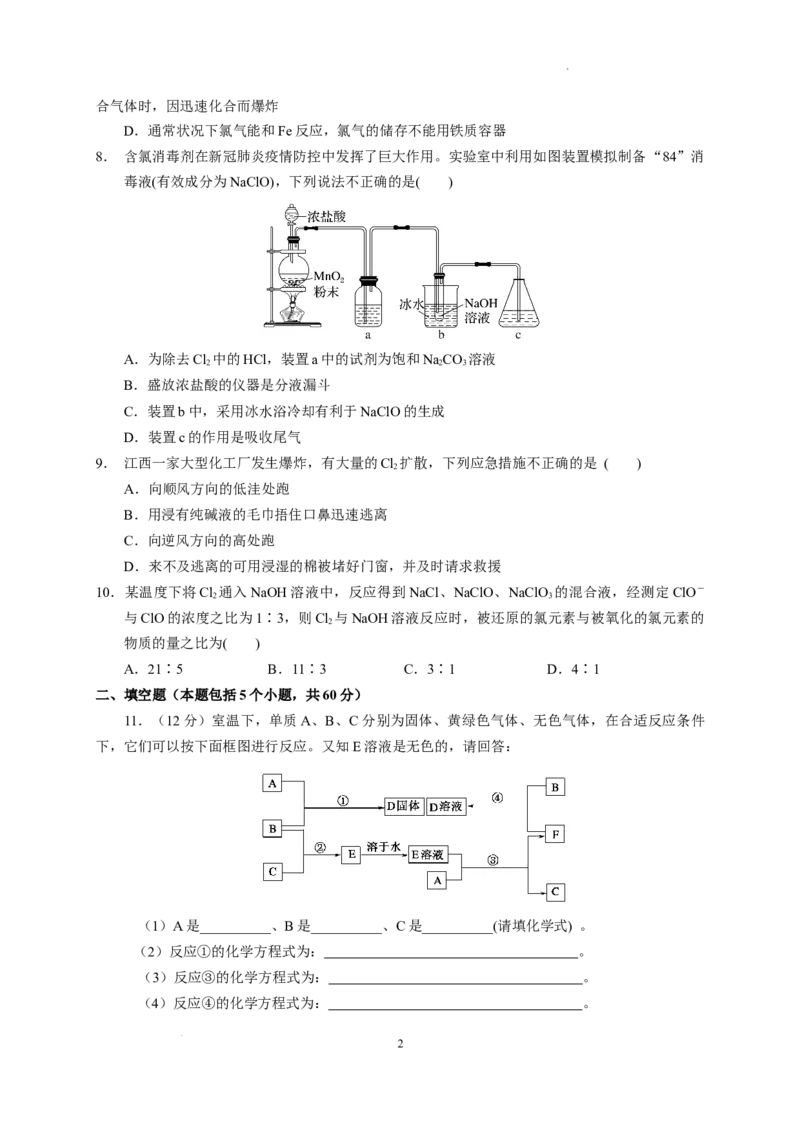
5.如图所示仪器可用于实验室制备少量无水FeCl ,仪器连接顺序正确的是( )
3
A.a—b—c—d—e—f—g—h B.a—e—d—c—b—h—i—g
C.a—d—e—c—b—h—i—g D.a—c—b—d—e—h—i—f
6. 氯化碘(ICl)的化学性质跟Cl 相似,预计它跟水反应的最初生成物是( )
2
A.HI和HClO B.HCl和HIO C.HClO 和HIO D.HClO和HIO
3
7. 氯气是一种很活泼的非金属单质,它具有较强的氧化性,下列叙述不正确的是( )
A.红热的铜丝在氯气里剧烈燃烧,生成棕黄色的烟
B.氯气能与水反应生成HClO和HCl,久置氯水最终变为稀盐酸
C.纯净的H 在Cl 中安静地燃烧,发出苍白色火焰,集气瓶口呈现雾状;光照 H 和Cl 的混
2 2 2 2
1
学科网(北京)股份有限公司合气体时,因迅速化合而爆炸
D.通常状况下氯气能和Fe反应,氯气的储存不能用铁质容器
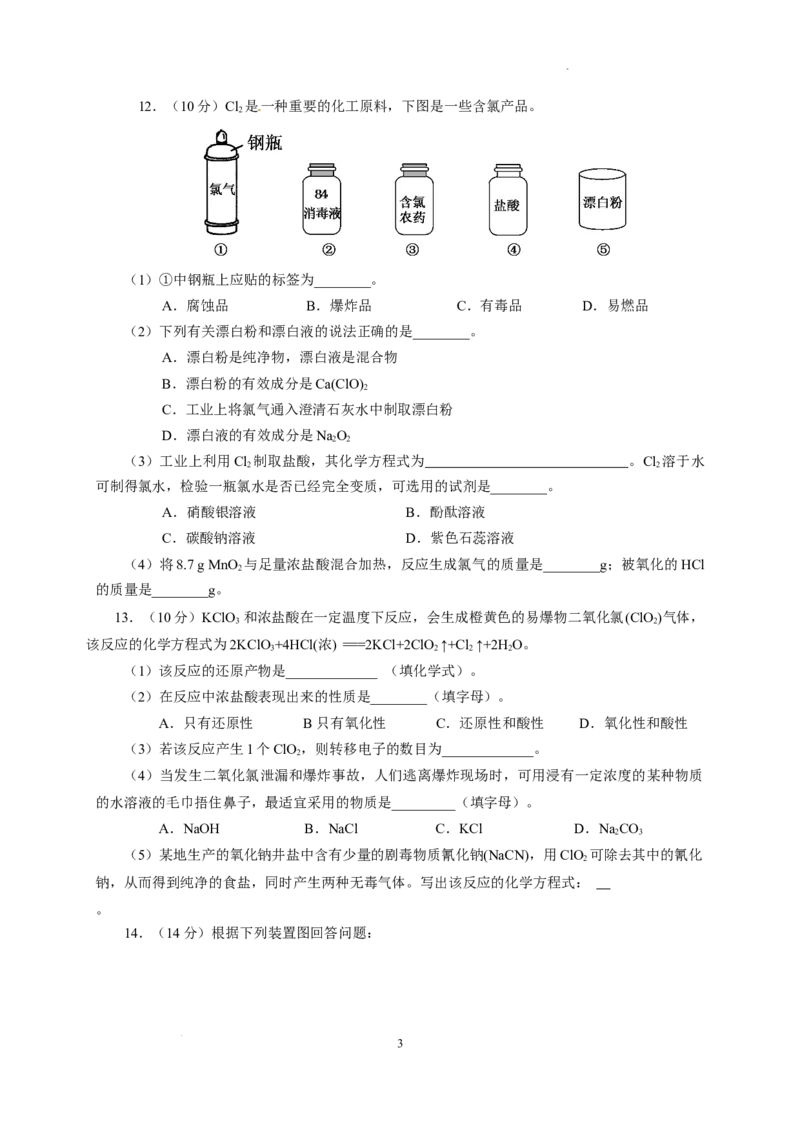
8. 含氯消毒剂在新冠肺炎疫情防控中发挥了巨大作用。实验室中利用如图装置模拟制备“84”消
毒液(有效成分为NaClO),下列说法不正确的是( )
A.为除去Cl 中的HCl,装置a中的试剂为饱和NaCO 溶液
2 2 3
B.盛放浓盐酸的仪器是分液漏斗
C.装置b中,采用冰水浴冷却有利于NaClO的生成
D.装置c的作用是吸收尾气
9. 江西一家大型化工厂发生爆炸,有大量的Cl 扩散,下列应急措施不正确的是 ( )
2
A.向顺风方向的低洼处跑
B.用浸有纯碱液的毛巾捂住口鼻迅速逃离
C.向逆风方向的高处跑
D.来不及逃离的可用浸湿的棉被堵好门窗,并及时请求救援
10.某温度下将Cl 通入NaOH溶液中,反应得到NaCl、NaClO、NaClO 的混合液,经测定ClO-
2 3
与ClO的浓度之比为1∶3,则Cl 与NaOH溶液反应时,被还原的氯元素与被氧化的氯元素的
2
物质的量之比为( )
A.21∶5 B.11∶3 C.3∶1 D.4∶1
二、填空题(本题包括5个小题,共60分)
11.(12分)室温下,单质A、B、C分别为固体、黄绿色气体、无色气体,在合适反应条件
下,它们可以按下面框图进行反应。又知E溶液是无色的,请回答:
(1)A是__________、B是__________、C是__________(请填化学式) 。
(2)反应①的化学方程式为: 。
(3)反应③的化学方程式为: 。
(4)反应④的化学方程式为: 。
2
学科网(北京)股份有限公司12.(10分)Cl 是一种重要的化工原料,下图是一些含氯产品。
2
(1)①中钢瓶上应贴的标签为________。
A.腐蚀品 B.爆炸品 C.有毒品 D.易燃品
(2)下列有关漂白粉和漂白液的说法正确的是________。
A.漂白粉是纯净物,漂白液是混合物
B.漂白粉的有效成分是Ca(ClO)
2
C.工业上将氯气通入澄清石灰水中制取漂白粉
D.漂白液的有效成分是NaO
2 2
(3)工业上利用Cl 制取盐酸,其化学方程式为 。Cl 溶于水
2 2
可制得氯水,检验一瓶氯水是否已经完全变质,可选用的试剂是________。
A.硝酸银溶液 B.酚酞溶液
C.碳酸钠溶液 D.紫色石蕊溶液
(4)将8.7 g MnO 与足量浓盐酸混合加热,反应生成氯气的质量是________g;被氧化的HCl
2
的质量是________g。
13.(10分)KClO 和浓盐酸在一定温度下反应,会生成橙黄色的易爆物二氧化氯(ClO )气体,
3 2
该反应的化学方程式为2KClO+4HCl(浓) ===2KCl+2ClO ↑+Cl ↑+2H O。
3 2 2 2
(1)该反应的还原产物是_____________ (填化学式)。
(2)在反应中浓盐酸表现出来的性质是________(填字母)。
A.只有还原性 B 只有氧化性 C.还原性和酸性 D.氧化性和酸性
(3)若该反应产生1个ClO ,则转移电子的数目为_____________。
2
(4)当发生二氧化氯泄漏和爆炸事故,人们逃离爆炸现场时,可用浸有一定浓度的某种物质
的水溶液的毛巾捂住鼻子,最适宜采用的物质是_________(填字母)。
A.NaOH B.NaCl C.KCl D.NaCO
2 3
(5)某地生产的氧化钠井盐中含有少量的剧毒物质氰化钠(NaCN),用ClO 可除去其中的氰化
2
钠,从而得到纯净的食盐,同时产生两种无毒气体。写出该反应的化学方程式:
。
14.(14分)根据下列装置图回答问题:
3
学科网(北京)股份有限公司(1)装置A、B通入干燥的Cl 后,观察到的现象是___________________________________
2
______________________________________________________,根据现象可得出的结论是
______________________________________________________________________________。
(2)装置B中发生反应的离子方程式是_____________________________________________。
(3)实验开始后,观察装置C中的现象是___________________________________________。
(4)通入Cl 时装置D中发生反应的离子方程式是____________________________________。
2
(5)装置E中发生反应的离子方程式是______________________________________________。
(6)装置F的作用是_______________________________________________________________。
15.(14分)消毒剂在生产、生活中有极其重要的作用,开发具有广谱、高效、低毒的杀菌
剂和消毒剂是今后发展的趋势。
(1)Cl 、HO 、ClO (还原产物为Cl-)、O(1个 O 转化为1个 O 和1个 HO)等物质常被用
2 2 2 2 3 3 2 2
作消毒剂。等物质的量的上述物质消毒效率最高的是________(填字母)。
A.Cl B.HO C.ClO D.O
2 2 2 2 3
(2)HO 有时可作为矿业废液消毒剂,有“绿色氧化剂”的美称。如消除采矿业胶液中的氰
2 2
化物(如KCN),经以下反应实现:KCN+HO+HO===A+NH ↑,则生成物A的化学式为
2 2 2 3
________,HO 被称为“绿色氧化剂”的理由是___________________________________________。
2 2
(3)漂白剂亚氯酸钠(NaClO)在常温与黑暗处可保存一年。亚氯酸不稳定可分解,反应的离
2
子方程式为HClO→ClO ↑+H++Cl-+HO(未配平)。在该反应中,当有1个 ClO 生成时转移的电
2 2 2 2
子数约为________。
(4)“84”消毒液(主要成分是 NaClO)和洁厕剂(主要成分是浓盐酸)不能混用,原因是
____________________________________________(用离子方程式表示)。利用氯碱工业的产物可以
生产“84”消毒液,写出有关反应的化学方程式:_______________________________。
【解析】
1.答案 B
解析:Cl 与H 混合,达到爆炸极限时,在点燃或光照的条件下能发生爆炸,A错误;实验室中通
2 2
4
学科网(北京)股份有限公司常用NaOH溶液吸收多余的Cl ,B正确; HCl气体与AgNO 溶液反应可产生AgCl沉淀,C错误;
2 3
将混合气体通入饱和食盐水中,除去的是HCl气体,而不是Cl,⑤错误,D错误。
2
2.答案 C
解析:自来水中常通入0.002 g/L氯气作消毒剂,因此水中含有微量的次氯酸,对金鱼的喂养有害,
须经日晒,除去水中少量的次氯酸。
3.答案 B
解析:氯气为黄绿色气体,氯水呈浅黄绿色,是因为溶解了氯气,A正确;向饱和NaHCO 溶液中
3
加入足量氯水,有无色气体产生,是因为HCO与氯水中的H+发生反应生成水和二氧化碳,B错误;
红色纸条褪色,说明氯水具有漂白性,C正确;向FeCl 溶液中滴加氯水,溶液变成棕黄色,是因
2
为发生反应:2FeCl +Cl===2FeCl ,说明氯水具有氧化性,D正确。
2 2 3
4.答案 C
解析:新制氯水中含有次氯酸,光照条件下次氯酸分解生成氧气,A不符合题意;新制氯水呈酸性,
NaHCO 与氯水反应生成二氧化碳气体,B不符合题意;氯水与NaOH溶液反应生成NaCl、NaClO
3
和水,不会生成气体,C符合题意;NaO 与水反应生成氧气,D不符合题意。
2 2
5.答案 B
解析:按制气→除HCl→除HO→制备FeCl →吸收Cl 顺序连接。
2 3 2
6.答案 B
解析:Cl 跟HO反应生成含-1价氯的无氧酸和含+1价氯的含氧酸:Cl+HO HCl+
2 2 2 2
HClO;ICl跟HO反应也应生成类似于HCl和HClO的两种酸。在Cl 中氯元素的化合价是0价,
2 2
在ICl中氯元素的化合价是-1价,碘元素的化合价是+1价。因此,ICl跟HO反应后,Cl生成
2
HCl,I生成HIO。
7.答案 D
解析:A项,红热的铜丝在氯气里剧烈燃烧生成氯化铜,生成棕黄色的烟,正确;B项,氯气与水
反应生成盐酸和次氯酸,次氯酸不稳定,受热分解生成氧气和氯化氢,所以久置氯水最终变为稀盐
酸,正确;C项,纯净的H 在Cl 中安静地燃烧生成氯化氢,发出苍白色火焰,氯化氢结合水蒸气
2 2
产生盐酸小液滴,所以集气瓶口呈现雾状,光照H 和Cl 的混合气体时,因迅速化合而爆炸,正确;
2 2
D项,通常状况下氯气和Fe不反应,氯气的储存能用铁质容器,错误。
8.答案 A
解析:A项,为除去Cl 中的HCl,装置a中的试剂为饱和NaCl溶液,错误;B项,盛放浓盐酸的
2
仪器是分液漏斗,错误;C项,装置b中,采用冰水浴冷却有利于NaClO的生成,防止温度高时产
生副产品NaClO,正确;D项,装置c的作用是吸收尾气,防止污染空气,正确。
3
9.答案 A
解析:氯气是一种比空气密度大的有毒气体,故应向逆风方向的高处跑;氯气能溶于水和碱性溶液,
故可用浸水或碱液织物临时阻挡Cl2进入口鼻或室内。
10.答案 D
5
学科网(北京)股份有限公司解析:氧化产物为ClO-和ClO,还原产物为Cl-,设ClO-和ClO物质的量分别为x、3x,Cl-物质
的量为y,据电子守恒,有x+5×3x=y,y=16x,则被还原的氯元素与被氧化的氯元素的物质的量
之比为16x∶4x=4∶1。
11.答案: (1)Fe Cl H
2 2
(2)2Fe+3Cl=====2FeCl
2 3
(3)2HCl+Fe===FeCl +H↑
2 2
(4)2FeCl +Cl===2FeCl
2 2 3
12.答案: (1)C (2)B (3)H+Cl=====2HCl D
2 2
(4)7.1 7.3
13.答案: (1)ClO (2)C (3)l
2
(4)D (5)2ClO +2NaCN===2CO +N +2NaCl
2 2 2
14.答案: (1)干燥的红色(或装置A中)布条不褪色,湿润的红色(或装置B中)布条褪色 Cl
2
无漂白性,Cl 与水反应生成的HClO有漂白性
2
(2)Cl+HO===H++Cl-+HClO
2 2
(3)溶液先变为红色,后褪色
(4)HO+SO+Cl===2H++SO+2Cl-
2 2
(5)2Fe2++Cl===2Fe3++2Cl-
2
(6)吸收氯气,防止污染环境
15.答案: (1)C
(2)KHCO HO 是氧化剂,其还原产物是HO,没有污染
3 2 2 2
(3) 1
(4)ClO-+Cl-+2H+===Cl↑+HO Cl+2NaOH===NaClO+NaCl+HO
2 2 2 2
解析:(1)1个Cl 、HO 、ClO 、O 分别消毒时,转移电子的物质的量依次为2、2、5、2,等
2 2 2 2 3
数目的上述物质反应,ClO 转移的电子数最多,消毒效率最高,C正确。
2
(2)根据质量守恒,可知反应 KCN+HO +HO===A+NH ↑中的A为KHCO 。在反应中,
2 2 2 3 3
HO 是氧化剂,其还原产物没有污染,所以HO 被称为“绿色氧化剂”。
2 2 2 2
(3)该反应是歧化反应,HClO 中+3价的氯元素一部分升高到ClO 中的+4价,一部分降低到
2 2
-1价,当有1个ClO 生成时,反应中转移1个电子。
2
(4)ClO-与浓盐酸中的Cl-会发生反应生成有毒的Cl ,离子方程式为ClO-+Cl-+2H+===Cl↑
2 2
+HO,氯碱工业的产物是NaOH、H 和Cl ,NaOH溶液和Cl 反应可以得到含有NaClO的溶液,
2 2 2 2
化学方程式为Cl+2NaOH===NaClO+NaCl+HO。
2 2
6
学科网(北京)股份有限公司7
学科网(北京)股份有限公司