文档内容
A. A B. B C. C D. D
2024-2025 学年高三第一次质量检测考试
6. 澳大利亚科学家发现了纯碳新材料“碳纳米泡沫”,每个泡沫含有约 4 000 个碳原子,直径约 6~9
化学试卷 nm,在 低于-183 ℃时,泡沫具有永久磁性,下列叙述正确的是( )
A .“碳纳米泡沫”与石墨互为同位素
(考试时间:75 命题人: )
B .把“碳纳米泡沫”分散到适当的溶剂中,能产生丁达尔效
注意事项: 应 C .“碳纳米泡沫”是一种新型的碳化合物
1.答卷前,考生务必将自己的姓名、准考证号填写在答题卡上。
D .“碳纳米泡沫”和金刚石的性质相同
2.回答选择题时,选出每小题答案后,用 2B 铅笔把答题卡上对应题目的答案标号框涂黑。如需改动,用橡
皮擦干净后,再选涂其它答案标号框。回答非选择题时,将答案写在答题卡上。写在本试卷上无效。 7.能正确表示下列反应的离子方程式为( )
3.考试结束后,将本试卷和答题卡一并交回。 A .硫化钠溶液和硝酸混合:S2-+2H+===H S↑
2
可能用到的相对原子质量:H-1 ,D-2 ,C-12 ,N-14
- +
一、选择题:(本题共 14 小题,每小题 3 分,共 42 分。在每小题给出的四个选项中,只有一 B .明矾溶液与过量氨水混合:Al3++4NH 3 +2H 2 O===AlO2+4NH4
项是符合题目要求的)。 - -
C .硅酸钠溶液中通入二氧化碳:SiO -+CO +H O===HSiO3+HCO3
2 2
1. 下列文物的材质属于天然有机高分子的是( )
D .将等物质的量浓度的 Ba (OH) 和 NH HSO 溶液以体积比 1 ∶ 2 混合: Ba2+ +2OH- +
8. 下列实验操作、现象和结论相对应的2 是( 4 4
2H+ + SO -===BaSO ↓+2H O
4 2
实验操作、现象 结论
A 用蓝色石蕊试纸检验某无色溶液,试纸变红 该溶液是酸溶液
B 用酒精灯灼烧织物产生类似烧焦羽毛的气味 该织物含蛋白质
A .铜奔马 B .汉竹简 C .莲花形玻璃托盏 D.垂鳞纹秦公铜鼎
A. A B. B C. C D. D C 乙醇和浓硫酸加热,产生的气体使溴水褪色 该气体是乙烯
2. 生活中处处有化学,下列叙述错误的是( )
D 氯化镁溶液中滴入氢氧化钠溶液,生成沉淀 氢氧化钠的碱性比氢氧化镁强
A. 合理施用化肥农药可以实现农作物增产 B. 豆腐制作过程中可使用氯化镁作凝固剂
C. 聚四氟乙烯可用作不粘锅内侧涂层材料 D. 制白砂糖时用活性炭脱色属于化学变化 9 .下列各组离子在指定的环境中一定能大量共存的是 ( )
3. 下列物质间的转化需要通过氧化还原反应才能实现的是( ) A .滴加石蕊试液显红色的溶液:Fe3+ 、NH + 4 、Cl- 、SCN-
A. CO2→NaHCO3 B .Fe(OH) 2→Fe
B .含有大量 HCO
-
3的溶液:NH
+
4 、Ca2+ 、Mg2+ 、I-
4. N A 为阿伏加德罗常数的值,下列叙述正确的是( )
(OH)
3 C .加入铝粉能产生 H 的溶液:NH + 4 、Fe2+ 、SO - 、NO - 3
2
A. 常温常压下, 12g 金刚石含有 4N 个共价键
A D .含有大量 ClO- 的溶液:H+ 、Mg2+ 、I- 、SO -
B. pH = 1的乙酸和盐酸混合溶液含 0.1N 个
A
H+ C. 标准状态下, 20g ND 含有的质子数为 10. 焦性没食子酸是一种优良的除氧剂。下列关于该物质的说法错误的是( )
3
10N D. 电解水生成 2g 氢气,外电路通过 1N A. 有酸性,是一种羧酸 B. 有酚羟基,能溶解于 NaOH 水溶液
A A
个电子 C. 可以与 Fe3+ 反应制备特种墨水 D. 可以与甲醛反应生成树脂
5. 下列实验操作对应的装置不正确的是( )
A B C D 11.工业制备高纯硅的主要过程如下:
焦 炭
灼烧海带制海带灰 准确量取15.00mL 稀盐配制一定浓度的NaCl溶液使用电石和饱和食盐水制备C 2 H 2 石英砂――― 1~ 800 ― 2 ― 000 ― ℃ → 粗 硅 300 ℃ S iH C l 3 ― 1 100 → ℃ 高纯硅 ,下列说法错误的是( )
酸
A .制备粗硅的反应方程式为 SiO +2C Si+2CO↑ B .1 mol Si 含 Si—Si 的数目约为
2
4×6.02×1023
C .原料气 HCl 和 H 应充分去除水和氧气 D .生成 SiHCl 的反应为熵减过程
2 3
-
12 .下列操作中,不会影响溶液中 K+ 、Al3+ 、Fe3+ 、Ba2+ 、Cl- 、NO 3等离子大量共存的是( )
A .加入 ZnSO B .加入 Fe 粉 C .通入 NH D .通入 CO
4 3 2
13.已知反应:①SO +2Fe3++2H O===SO -+2Fe2++W;②Cr O -+aFe2++bH+ℵ→Cr3++Fe3++H O
2 2 2 2
(未 配平)下列有关说法正确的是( )
高三化学试卷 ·第 1页(共 3页)C .a =6 ,b =7 D .反应 Cr O -+3SO +2H+===2Cr3++3SO -+H O 不能发生 高铁酸钾的溶解度。
2 2 2
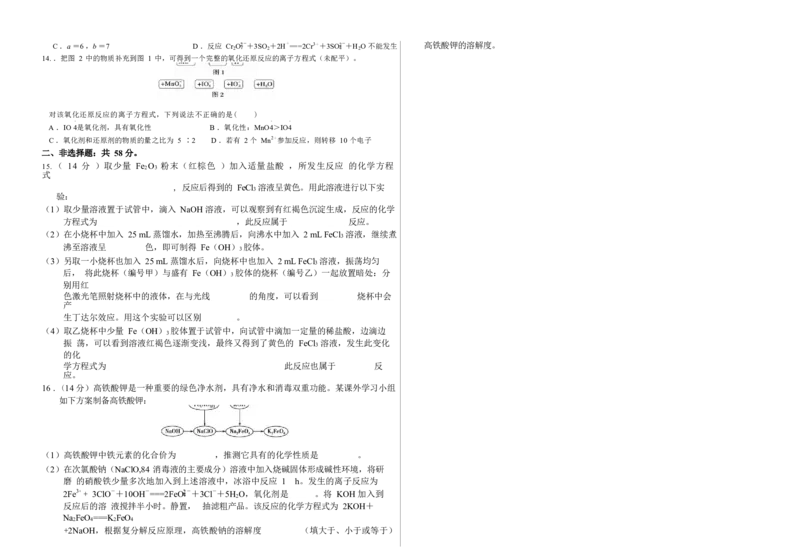
14. .把图 2 中的物质补充到图 1 中,可得到一个完整的氧化还原反应的离子方程式(未配平)。
对该氧化还原反应的离子方程式,下列说法不正确的是( )
- - -
A .IO 4是氧化剂,具有氧化性 B .氧化性:MnO4>IO4
C .氧化剂和还原剂的物质的量之比为 5 ∶2 D .若有 2 个 Mn2+参加反应,则转移 10 个电子
二、非选择题:共 58 分。
15. ( 14 分 )取少量 Fe 2 O 3 粉末(红棕色 )加入适量盐酸 ,所发生反应 的化学方程
式
, 反应后得到的 FeCl 溶液呈黄色。用此溶液进行以下实
3
验:
(1)取少量溶液置于试管中,滴入 NaOH 溶液,可以观察到有红褐色沉淀生成,反应的化学
方程式为 ,此反应属于 反应。
(2)在小烧杯中加入 25 mL 蒸馏水,加热至沸腾后,向沸水中加入 2 mL FeCl 溶液,继续煮
3
沸至溶液呈 色,即可制得 Fe(OH) 胶体。
3
(3)另取一小烧杯也加入 25 mL 蒸馏水后,向烧杯中也加入 2 mL FeCl 溶液,振荡均匀
3
后, 将此烧杯(编号甲)与盛有 Fe(OH) 胶体的烧杯(编号乙)一起放置暗处:分
3
别用红
色激光笔照射烧杯中的液体,在与光线 的角度,可以看到 烧杯中会
产
生丁达尔效应。用这个实验可以区别 。
(4)取乙烧杯中少量 Fe(OH) 胶体置于试管中,向试管中滴加一定量的稀盐酸,边滴边
3
振 荡,可以看到溶液红褐色逐渐变浅,最终又得到了黄色的 FeCl 溶液,发生此变化
3
的化
学方程式为 此反应也属于 反
应。
16 .(14 分)高铁酸钾是一种重要的绿色净水剂,具有净水和消毒双重功能。某课外学习小组
如下方案制备高铁酸钾:
(1)高铁酸钾中铁元素的化合价为 ,推测它具有的化学性质是 。
(2)在次氯酸钠(NaClO,84 消毒液的主要成分)溶液中加入烧碱固体形成碱性环境,将研
磨 的硝酸铁少量多次地加入到上述溶液中,冰浴中反应 1 h。发生的离子反应为
2Fe3+ + 3ClO-+10OH-===2FeO -+3Cl-+5H O,氧化剂是 。将 KOH 加入到
2
反应后的溶 液搅拌半小时。静置, 抽滤粗产品。该反应的化学方程式为 2KOH+
Na FeO ===K FeO
2 4 2 4
+2NaOH,根据复分解反应原理,高铁酸钠的溶解度 (填大于、小于或等于)酸化过程发生反应的化学方程式: 。
(3)在强碱性溶液中,高铁酸钾能将亚铬酸钾(KCrO )氧化为铬酸钾(K CrO ),生成的
2 2 4
(3)工业上用 Al O 与 C 、Cl 在高温条件下反应制取 AlCl ,理论上每消耗 6.0 g 碳单质,
铬 酸盐溶解酸化后,得到的重铬酸钾(K Cr O )用(NH ) Fe(SO ) 的标准溶液 2 3 2 3
2 2 7 4 2 4 2 转
滴定, 以二苯胺磺酸钠为指示剂。到达滴定终点时,溶液由紫色变为淡绿色(+6 价
移 1 mol 电子,则反应的化学方程式为 。
铬转化成
(4)某同学推测铝与氧化铁发生铝热反应得到的熔融物中还含有 Fe2O3,设计了如下方案
+3 价铬),有关离子方程式为 ;
来 验证:取一块该熔融物投入少量稀硫酸中,反应一段时间后,向反应后的混合液中
(4)明矾、硫酸铁、高铁酸钾都能净水,简述高铁酸钾净水原理: 。
滴加 物质甲的溶液,观察溶液颜色的变化,即可证明熔融物中是否含有 Fe2O3。
17(15 分).铝是一种重要的金属,在生产、生活中具有许多重要的用途,
则物质甲是 (填化学式),请判断该同学设计的实验方案的合理性 (填
“合理”或“不合理”)。原因是 (若合理,则不用填
写)。
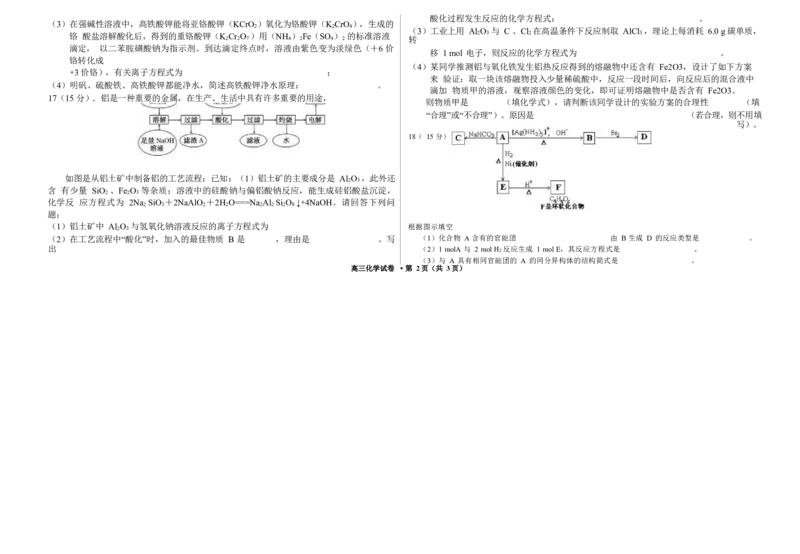
18( 15 分)
.
如图是从铝土矿中制备铝的工艺流程:已知:(1)铝土矿的主要成分是 Al O ,此外还
2 3
含 有少量 SiO 、Fe O 等杂质;溶液中的硅酸钠与偏铝酸钠反应,能生成硅铝酸盐沉淀,
2 2 3
化学反 应方程式为 2Na SiO +2NaAlO +2H O===Na Al Si O ↓+4NaOH。请回答下列问
2 3 2 2 2 2 2 8
题:
(1)铝土矿中 Al O 与氢氧化钠溶液反应的离子方程式为 根据图示填空
2 3
(2)在工艺流程中“酸化”时,加入的最佳物质 B 是 ,理由是 。写 (1)化合物 A 含有的官能团 由 B 生成 D 的反应类型是 。
出 (2)1 molA 与 2 mol H 反应生成 1 mol E,其反应方程式是 。
2
(3)与 A 具有相同官能团的 A 的同分异构体的结构简式是 。
高三化学试卷 ·第 2页(共 3页)(4)B 在酸性条件下与 Br 2 反应得到 D ,D 的结构简式是 s 。
(5)F 的结构简式是 。由 E 生成 F 的反应类型是 。
高三化学试卷 ·第 3页(共 3页)