文档内容
机密★启用前 〔考试时间:2024年7月4日上午9∶00—10∶15〕
乐山市高中 2025届教学质量检测
化 学
本试卷共两大题,共6页,满分100分,考试时间75分钟。考生作答时,须将答案正确填涂
在答题卡上,在本试题卷、草稿纸上答题无效。考试结束后,请将答题卡交回,试卷自行保存。
注意事项:
1.答题前,考生务必将自己的姓名、准考证号在答题卷上填写清楚。
2.选择题必须使用2B铅笔将答案填涂在答题卡对应题目标号的位置上。
3.考试结束后,请监考人员将答题卡回收并装袋。
可能用到的相对原子质量:H1 C12 N14 O16 Mg24 Fe56 Cu64
一、选择题(共14小题,每小题3分,共42分,每小题只有一个正确选项)
1.化学与生活、科研紧密相关,下列说法正确的是
A.日常装修溶解油漆一般用有机溶剂(如乙酸乙酯等)而不用水
B.苯酚有消毒作用,含苯酚的废水可以直接排放
C.圆形容器中结出的冰是圆形的,体现了晶体的自范性
D.利用红外光谱可以获得键长、键角等分子结构信息
2.下列描述对应的模型正确的是
A.SO 的空间结构: B.Cu(NH)2+中的配位键:
3 3 4
C.某晶体的晶胞: D.顺-2-丁烯的球棍模型:
3.四川三星堆青铜文明的独特魅力彰显了古老中华文明的绚丽多彩。下列有关说法正确的是
A.青铜的熔点和硬度均大于铜
B.基态Cu原子的价电子排布式为3d94s2
C.铜晶体中原子间以离子键相互结合
D.青铜和铜都属于金属晶体
高二化学试题 第 1页(共6页)
{#{QQABIYAEggCoAJBAAQgCUQG6CgKQkAGAASgOAEAMsAAAwANABAA=}#}
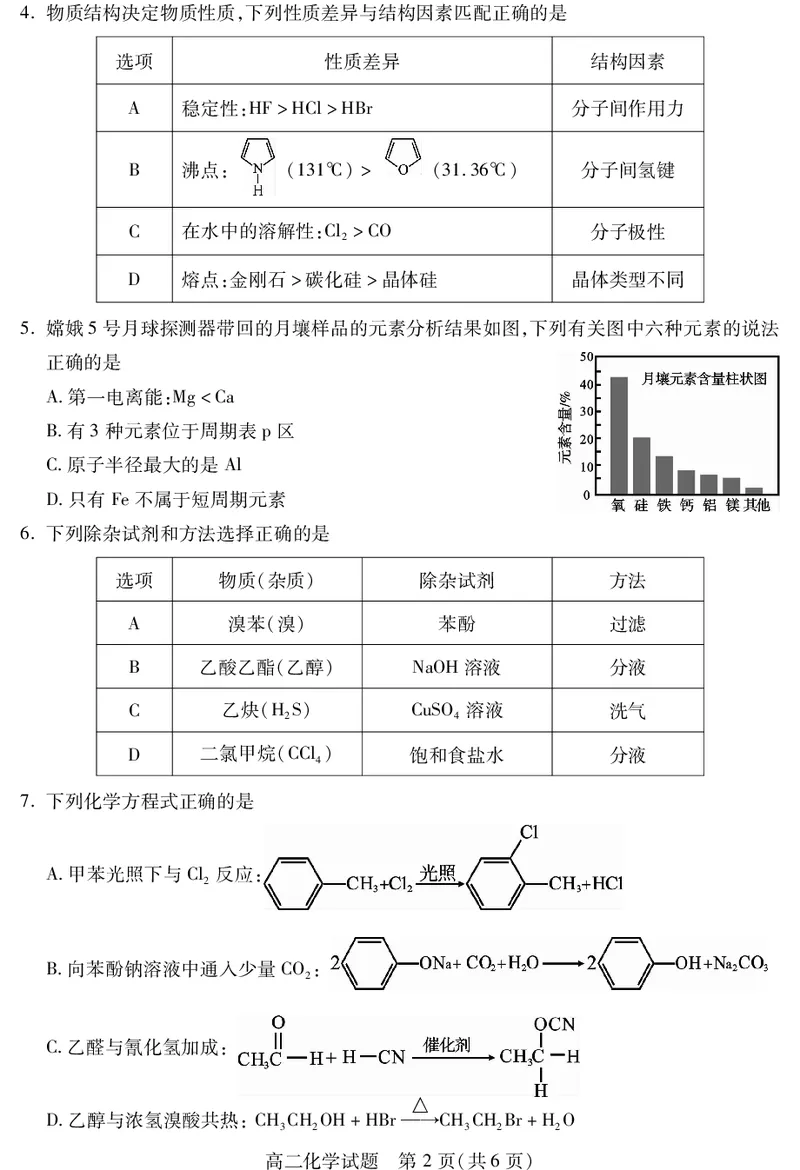
书书书4.物质结构决定物质性质,下列性质差异与结构因素匹配正确的是
选项 性质差异 结构因素
A 稳定性:HF>HCl>HBr 分子间作用力
B 沸点: (131℃)> (31.36℃) 分子间氢键
C 在水中的溶解性:Cl>CO 分子极性
2
D 熔点:金刚石>碳化硅>晶体硅 晶体类型不同
5.嫦娥5号月球探测器带回的月壤样品的元素分析结果如图,下列有关图中六种元素的说法
正确的是
A.第一电离能:Mg<Ca
B.有3种元素位于周期表p区
C.原子半径最大的是Al
D.只有Fe不属于短周期元素
6.下列除杂试剂和方法选择正确的是
选项 物质(杂质) 除杂试剂 方法
A 溴苯(溴) 苯酚 过滤
B 乙酸乙酯(乙醇) NaOH溶液 分液
C 乙炔(HS) CuSO 溶液 洗气
2 4
D 二氯甲烷(CCl) 饱和食盐水 分液
4
7.下列化学方程式正确的是
A.甲苯光照下与Cl反应:
2
B.向苯酚钠溶液中通入少量CO:
2
C.乙醛与氰化氢加成:
△
D.乙醇与浓氢溴酸共热:CHCHOH+HBr→CHCHBr+HO
3 2 3 2 2
高二化学试题 第 2页(共6页)
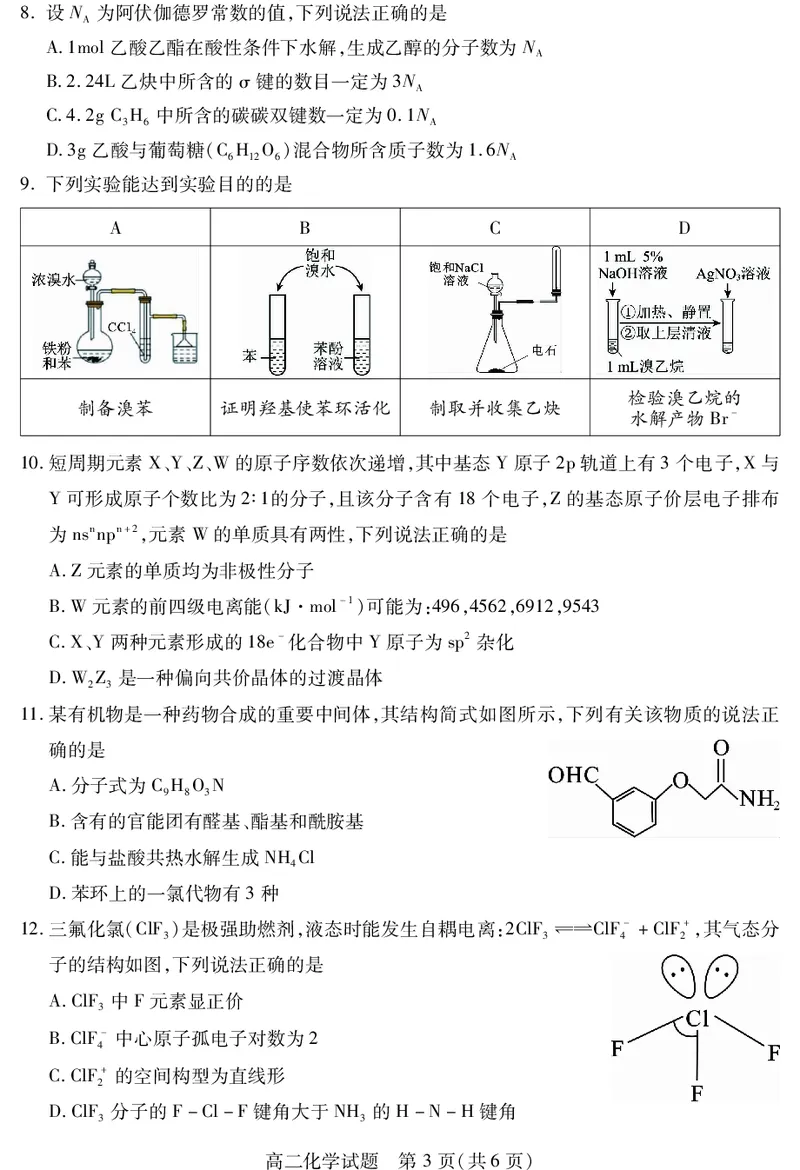
{#{QQABIYAEggCoAJBAAQgCUQG6CgKQkAGAASgOAEAMsAAAwANABAA=}#}8.设N 为阿伏伽德罗常数的值,下列说法正确的是
A
A.1mol乙酸乙酯在酸性条件下水解,生成乙醇的分子数为N
A
B.2.24L乙炔中所含的σ键的数目一定为3N
A
C.4.2gCH 中所含的碳碳双键数一定为0.1N
3 6 A
D.3g乙酸与葡萄糖(CH O)混合物所含质子数为1.6N
6 12 6 A
9.下列实验能达到实验目的的是
A B C D
检验溴乙烷的
制备溴苯 证明羟基使苯环活化 制取并收集乙炔
水解产物Br-
10.短周期元素X、Y、Z、W的原子序数依次递增,其中基态Y原子2p轨道上有3个电子,X与
Y可形成原子个数比为2∶1的分子,且该分子含有18个电子,Z的基态原子价层电子排布
为nsnnpn+2,元素W的单质具有两性,下列说法正确的是
A.Z元素的单质均为非极性分子
B.W元素的前四级电离能(kJ·mol-1)可能为:496,4562,6912,9543
C.X、Y两种元素形成的18e-化合物中Y原子为sp2杂化
D.W Z是一种偏向共价晶体的过渡晶体
2 3
11.某有机物是一种药物合成的重要中间体,其结构简式如图所示,下列有关该物质的说法正
确的是
A.分子式为CHON
9 8 3
B.含有的官能团有醛基、酯基和酰胺基
C.能与盐酸共热水解生成NHCl
4
D.苯环上的一氯代物有3种
12.三氟化氯(ClF)是极强助燃剂,液态时能发生自耦电离:2ClF幑幐ClF-+ClF+,其气态分
3 3 4 2
子的结构如图,下列说法正确的是
A.ClF中F元素显正价
3
B.ClF-中心原子孤电子对数为2
4
C.ClF+的空间构型为直线形
2
D.ClF分子的F-Cl-F键角大于NH 的H-N-H键角
3 3
高二化学试题 第 3页(共6页)
{#{QQABIYAEggCoAJBAAQgCUQG6CgKQkAGAASgOAEAMsAAAwANABAA=}#}13.有机物戊是制备降压药美托拉宗的一种中间体,其合成路线如图所示。下列说法错误的是
A.甲中含有的官能团为苯环、碳氯键和氨基
B.乙中所有碳原子可能共面
C.“甲→乙”的目的是保护-NH
2
D.“丙→丁”属于氧化反应
14.铁和氨气在640℃发生反应得到有磁性的FeN,其中一种晶胞结构如图甲所示,晶胞边长
x y
为anm。一定条件下Cu可以完全替代该晶体中面心或顶点位置的 Fe,替代后晶胞参数和
晶体能量均会发生变化,已知FeN 转化为两种Cu替代型产物的能量变化如图乙所示,下
x y
列说法正确的是
A.FeN晶胞中与Fe等距且最近的Fe有12个
x y
B.N填充在Fe围成的正六面体空隙
C.FeCuN比FeCuN稳定
3 3
56×3+64+14
D.Cu替代顶点位置后晶体的密度为: g·cm-3
N(a×10-7)3
A
二、非选择题(共4小题,共58分)
15.(13分)碱式碳酸镁[4MgCO·Mg(OH)·4HO]是一种新型阻燃剂,也常用作橡胶制品
3 2 2
的优良填充剂。
回答下列问题:
(1)下列Mg原子的核外电子排布式中,能量最高的是 (选填编号,下同),能量最低
的是 。
A.1s22s22p43s23p13p1 B.1s22s22p43s23p2
x y x
C.1s22s22p63s13p1 D.1s22s22p63s2
x
(2)在元素周期表中,Mg与Na和Al相邻,三种元素的第一电离能由大到小的顺序为 。
(3)碱式碳酸镁中,CO2-的中心原子的杂化类型是 ,OH-的电子式为 。
3
(4)由对角线规则可知锂、镁的性质有相似性,则单质 Li在氧气中燃烧生成的氧化物的化
学式为 。
高二化学试题 第 4页(共6页)
{#{QQABIYAEggCoAJBAAQgCUQG6CgKQkAGAASgOAEAMsAAAwANABAA=}#}(5)碱式碳酸镁受热能生成MgO,其晶胞结构如图所示。
①半径r(Mg2+)<r(O2-)的原因为 。
②每个Mg2+周围等距且最近的O2-的数目为 ,设晶胞参
数为apm,阿伏伽德罗常数的值为 N,则 MgO晶体的密度
A
为 g·cm-3(列出计算式)。
(6)试分析碱式碳酸镁能够阻燃的原因 (写一条即可)。
16.(15分)有机物A可能含有碳、氢、氧三种元素,为研究其组成与结构,进行了如下实验,回
答下列问题。
实验步骤 解释或实验结论
(1)物质A的质谱与核磁共振氢谱
①A的相对分子量为 。
②A分子中含有 种不同化
学环境的氢原子,个数比为
。
(质谱) (核磁共振氢谱)
(2)取14.8gA在足量纯氧中充分燃烧,并使其燃烧产物
依次缓缓通过浓硫酸、碱石灰,发现两者增重分别为 A的分子式为 。
10.8g和26.4g。
(3)另取14.8gA与足量Na反应产生0.1moH;将少量物质
2
A中含有的官能团的名称为 。
A与新制Cu(OH)悬浊液共热,有砖红色沉淀产生。
2
(4)综上:
①物质A的结构简式为 ,其化学名称为 。
②写出物质A与新制Cu(OH)悬浊液共热发生反应的化学方程式 。
2
③A有多种同分异构体,写出其中属于酯的同分异构体的结构简式 。
17.(15分)氧、硫等元素形成的单质或化合物在科学研究中有广泛的用途。
回答下列问题:
(1)硫元素的基态原子价电子的轨道表示式为 。
(2)冰有多种晶体,其中一种晶体的晶胞如图所示,晶体中水分子间的
作用力有 ,已知该冰晶体的密度为0.9g·cm-3,N 为阿伏伽德罗常数的值,则
A
晶胞的体积为 cm3。
(3)HO的结构如图所示,由图可知HO是一种 (填“极性”
2 2 2 2
或“非极性”)分子。HO的两个H原子被磺酸基(-SOH)取代
2 2 3
后的产物为过二硫酸,是一种常用强氧化剂,过二硫酸的分子式为
,分子中硫元素的化合价为 。
高二化学试题 第 5页(共6页)
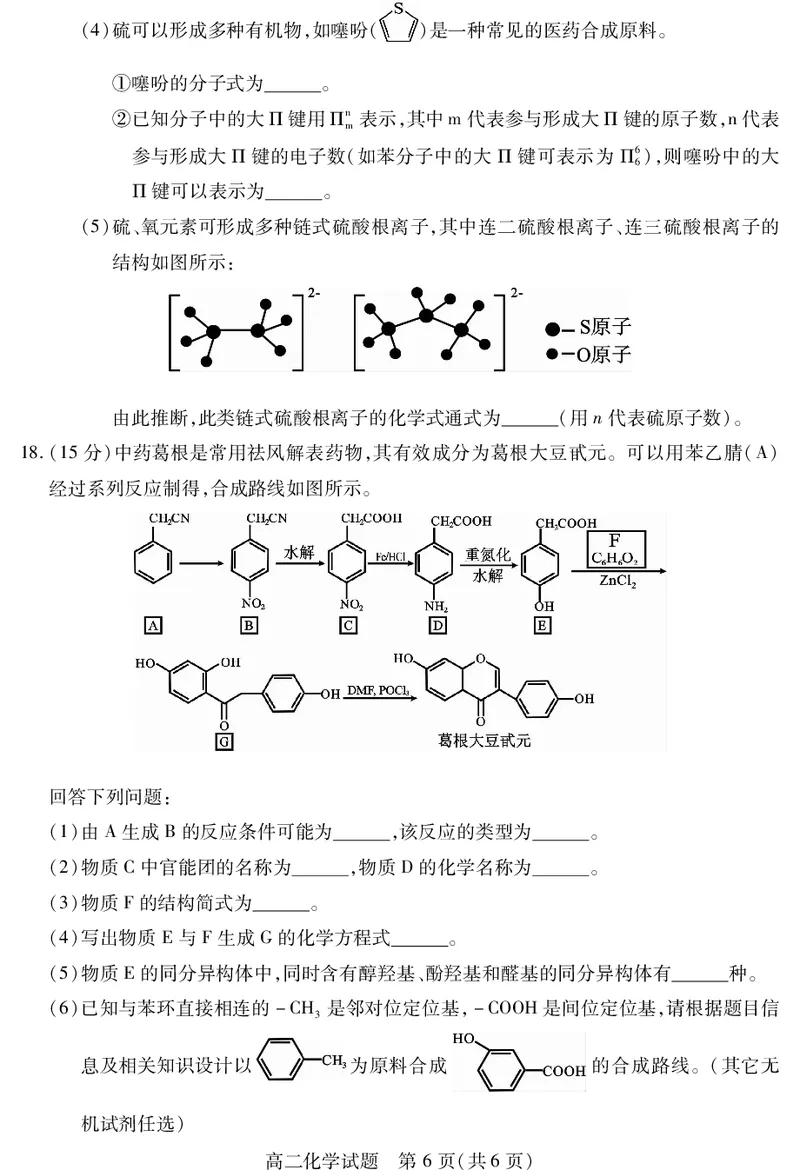
{#{QQABIYAEggCoAJBAAQgCUQG6CgKQkAGAASgOAEAMsAAAwANABAA=}#}(4)硫可以形成多种有机物,如噻吩( )是一种常见的医药合成原料。
①噻吩的分子式为 。
②已知分子中的大Π键用Πn表示,其中m代表参与形成大Π键的原子数,n代表
m
参与形成大Π键的电子数(如苯分子中的大 Π键可表示为 Π6),则噻吩中的大
6
Π键可以表示为 。
(5)硫、氧元素可形成多种链式硫酸根离子,其中连二硫酸根离子、连三硫酸根离子的
结构如图所示:
由此推断,此类链式硫酸根离子的化学式通式为 (用n代表硫原子数)。
18.(15分)中药葛根是常用祛风解表药物,其有效成分为葛根大豆甙元。可以用苯乙腈(A)
经过系列反应制得,合成路线如图所示。
回答下列问题:
(1)由A生成B的反应条件可能为 ,该反应的类型为 。
(2)物质C中官能团的名称为 ,物质D的化学名称为 。
(3)物质F的结构简式为 。
(4)写出物质E与F生成G的化学方程式 。
(5)物质E的同分异构体中,同时含有醇羟基、酚羟基和醛基的同分异构体有 种。
(6)已知与苯环直接相连的-CH 是邻对位定位基,-COOH是间位定位基,请根据题目信
3
息及相关知识设计以 为原料合成 的合成路线。(其它无
机试剂任选)
高二化学试题 第 6页(共6页)
{#{QQABIYAEggCoAJBAAQgCUQG6CgKQkAGAASgOAEAMsAAAwANABAA=}#}