文档内容
成都外国语学校 2025—2026 学年度上期十月月考
高二化学试卷
注意事项:
1、本试卷分Ⅰ卷(选择题)和Ⅱ卷(非选择题)两部分。
2、本堂考试75分钟,满分100分。
3、答题前,考生务必先将自己的姓名、学号填写在答卷上,并使用2B铅笔填涂。
4、考试结束后,将答题卡交回。
第Ⅰ卷
(选择题,共 42 分)
一、选择题(本题包括14小题,每小题3分,共42分。每小题只有一个选项符合题意)
1.“能源”是人们生活中不可或缺的一部分。下列属于将化学能转化为热能的是( )
A.自热火锅发热包 B.太阳能热水器烧水
C.风力发电机 D.新能源汽车电池
2.我们往往在化学反应和实验操作中采取一些加快速率的操作,下列说法正确的是( )
A.用Cl 制备84消毒液的过程中加热 B.实验室制取氢气时采用粗锌而非纯锌
2
C.过滤时用玻璃棒不断搅拌 D.用98%浓硫酸代替稀硫酸与铁反应制备氢气
3.下列事实不能用勒夏特列原理解释的是( )
A.在制备乙酸乙酯中,加入过量的乙醇 B.夏天,打开冰镇啤酒瓶盖产生大量泡沫
C.Fe(SCN) 溶液中加入铁粉后溶液颜色变浅 D.工业合成氨反应中采用400~500℃的高温
3
4.下列关于电解质的说法正确的是( )
A.由于BaSO 难溶于水,所以是弱电解质。
4
B.有机物溶于水均不导电,所以有机物均是非电解质
C.CO 为非电解质但是溶于水形成的溶液能导电,是因为CO 与H O反应产生了H CO
2 2 2 2 3
D.强电解质的水溶液导电能力一定比弱电解质的水溶液导电能力强
5.下列各组离子在给定溶液中能大量共存的是( )
A.在强酸性溶液中:Fe2、 K、Cl、MnO
4
B.含有大量CH
3
COO-的溶液: K、H、Cl、SO2
4
C.无色透明的溶液中:Fe3、 K、Cl、I D.滴加酚酞变红的溶液:Na、Ba2、NO、Cl
3
6.下列事实能证明HA是弱酸的是( )
0.1molL1HA溶液中通入HCl气体,c
A
减小
①
高二化学 1/8
{#{QQABZQEkwgqQkJbACS4qAQEgC0kYkIMgJOgEAUAQOAwLQBFIBIA=}#}常温下,0.1molL1HA溶液中:c H 0.1molL1
② 0.1molL1HA溶液可以使石蕊溶液变红
③
相同温度下,0.1molL1HA溶液的导电能力比0.1molL1HCl溶液弱
A. B. C. D.
④
7.丙烷
①
脱
②
氢制丙烯的一种机
①
理
③
如图所示(图中TS① 表示
②
过
④
渡态,*表示吸附
②
态 ③)。
④
下列说法错误的是( )
A.使用高效催化剂,可改变反应历程和焓变 B.提高反应温度,可提高丙烯的平衡产率
C.生成过渡态TS3的过程是总反应的决速步骤 D.C
3
H*
8
C
3
H*
7
H*的活化能:E
a正
E
a逆
8.下列有关热化学方程式的叙述中,正确的是( )
A.在一定条件下,将0.5molN 和1.5molH 置于密闭容器中充分反应生成NH 放热19.3kJ,则其热化学
2 2 3
方程式为:N g3H g 2NH g H38.6kJmol1
2 2 3
B.根据2H gO g2H Ol △H=-483.6kJ·mol-1,可知H 的燃烧热为241.8kJ·mol-1
2 2 2 2
C.根据C(石墨,s)C(金刚石,s)ΔH 0,可知金刚石比石墨稳定
1
D.由CsO gCO g ΔH 和Cs O gCOg ΔH ,可知ΔH ΔH
2 2 1 2 2 2 1 2
9.下列各实验装置、目的或结论全都正确的是( )
A.①可用于测定锌与稀硫酸反应生成氢气的速率
B.②可用于探究 Fe3、Cu2对H
2
O
2
分解速率的影响
C.③可通过出现浑浊的快慢比较温度对化学反应速率的影响
D.④中密封注射器活塞从Ⅰ处拉到Ⅱ处,颜色先变浅后变深可证明平衡移动
高二化学 2/8
{#{QQABZQEkwgqQkJbACS4qAQEgC0kYkIMgJOgEAUAQOAwLQBFIBIA=}#}10.CH COOH的电离方程式为CH COOHH++CH COO-,25℃时,0.1mol·L-1CH COOH溶液的K =1.8×10-5。
3 3 3 3 a
下列说法正确的是( )
A.升高温度,c(H+)增大,K 变大
a
B.向该溶液中加少量CH COONa固体,平衡正向移动
3
C.向该溶液中滴加几滴浓盐酸,平衡逆向移动,c(H+)减小
D.该温度下0.01mol·L-1CH COOH溶液的K <1.8×10-5
3 a
11.由下列实验事实所得出的结论正确的是( )
选项 实验事实 结论
密闭容器中发生反应H (g)I (g)2HI(g),压
A 2 2 增大压强,平衡向逆反应方向移动
缩容器体积,气体颜色变深
在恒温恒容下发生反应
B 该反应达到了平衡状态
2SO (g)+O (g)2SO (g),气体密度不再变化
2 2 3
CuH O2 aq,蓝色 +4Cl-aq
加热盛有CuCl 溶液的试管,溶液变为黄色,冰 2 4
2
C
水冷却后变为蓝色 CuCl 2- aq,黄色 +4H O1 ΔH>0
4 2
浓度相同的盐酸和醋酸分别与等质量的形状相同 金属与酸的反应中,酸的浓度对反应速率
D
的锌粒反应,前者反应速率快 无影响
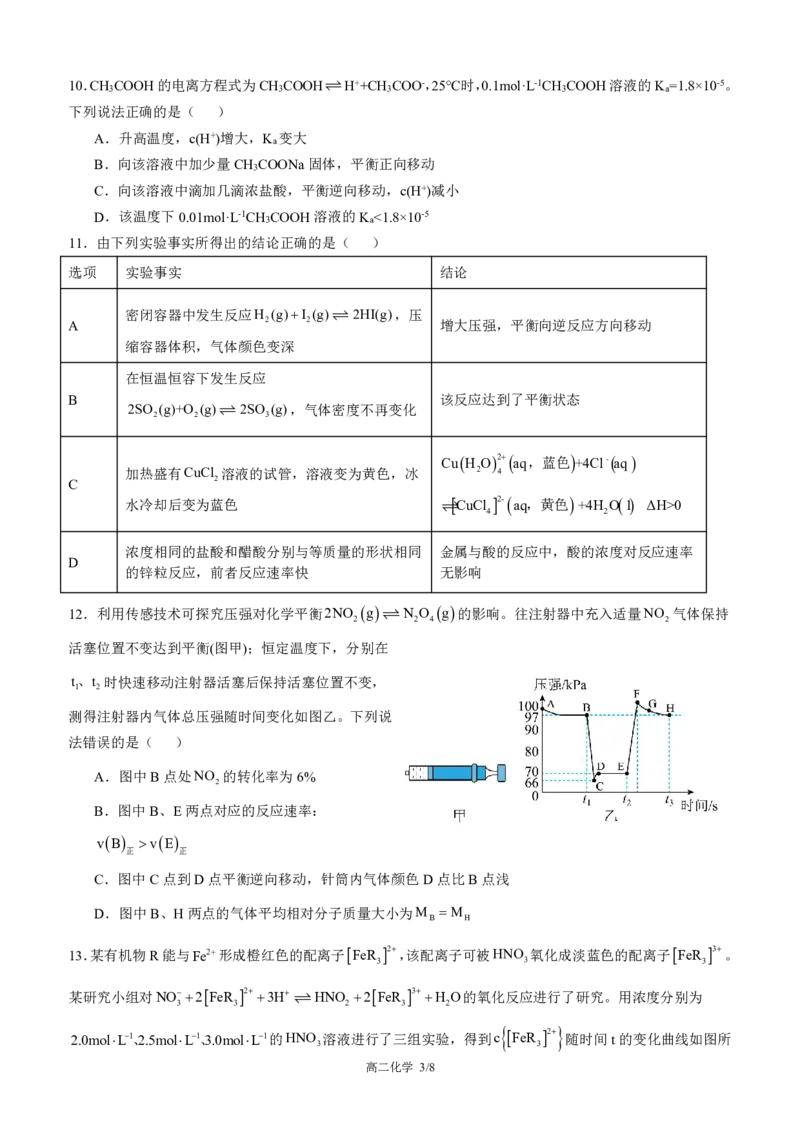
12.利用传感技术可探究压强对化学平衡2NO g N O g的影响。往注射器中充入适量NO 气体保持
2 2 4 2
活塞位置不变达到平衡(图甲);恒定温度下,分别在
t、t 时快速移动注射器活塞后保持活塞位置不变,
1 2
测得注射器内气体总压强随时间变化如图乙。下列说
法错误的是( )
A.图中B点处NO 的转化率为6%
2
B.图中B、E两点对应的反应速率:
vB vE
正 正
C.图中C点到D点平衡逆向移动,针筒内气体颜色D点比B点浅
D.图中B、H两点的气体平均相对分子质量大小为M M
B H
13.某有机物R能与Fe2形成橙红色的配离子
FeR
2,该配离子可被HNO 氧化成淡蓝色的配离子
FeR
3。
3 3 3
某研究小组对NO2 FeR 23H HNO 2 FeR 3H O的氧化反应进行了研究。用浓度分别为
3 3 2 3 2
2.0molL1、2.5molL1、3.0molL1的HNO 溶液进行了三组实验,得到c
FeR
2
随时间t的变化曲线如图所
3 3
高二化学 3/8
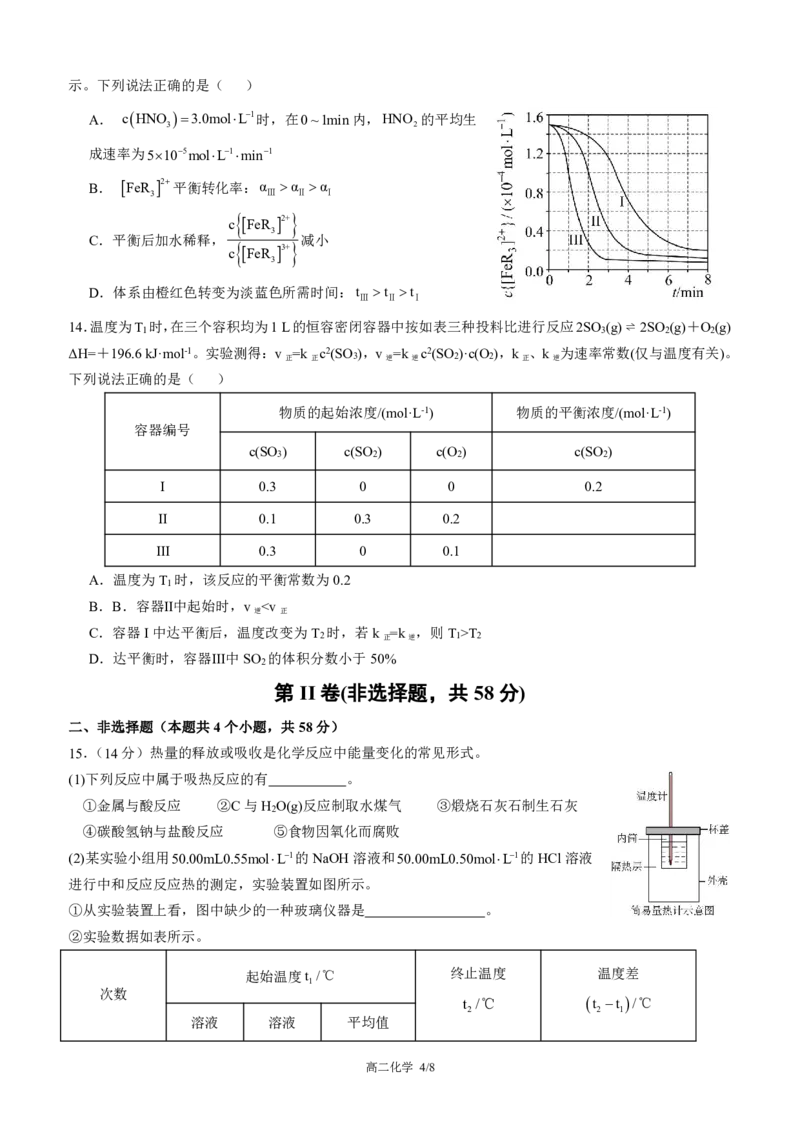
{#{QQABZQEkwgqQkJbACS4qAQEgC0kYkIMgJOgEAUAQOAwLQBFIBIA=}#}示。下列说法正确的是( )
A. cHNO 3.0molL1时,在0~1min内,HNO 的平均生
3 2
成速率为5105molL1min1
B. FeR 2平衡转化率:α α α
3 Ⅲ Ⅱ Ⅰ
2+
c FeR
3
C.平衡后加水稀释,
减小
3+
c FeR
3
D.体系由橙红色转变为淡蓝色所需时间:t t t
Ⅲ Ⅱ Ⅰ
14.温度为T 时,在三个容积均为1L的恒容密闭容器中按如表三种投料比进行反应2SO (g)⇌ 2SO (g)+O (g)
1 3 2 2
ΔH=+196.6kJ·mol-1。实验测得:v =k c2(SO ),v =k c2(SO )·c(O ),k 、k 为速率常数(仅与温度有关)。
正 正 3 逆 逆 2 2 正 逆
下列说法正确的是( )
物质的起始浓度/(mol·L-1) 物质的平衡浓度/(mol·L-1)
容器编号
c(SO ) c(SO ) c(O ) c(SO )
3 2 2 2
I 0.3 0 0 0.2
Ⅱ 0.1 0.3 0.2
Ⅲ 0.3 0 0.1
A.温度为T 时,该反应的平衡常数为0.2
1
B.B.容器Ⅱ中起始时,v T
2 正 逆 1 2
D.达平衡时,容器Ⅲ中SO 的体积分数小于50%
2
第 II 卷(非选择题,共 58 分)
二、非选择题(本题共4个小题,共58分)
15.(14分)热量的释放或吸收是化学反应中能量变化的常见形式。
(1)下列反应中属于吸热反应的有 。
①金属与酸反应 ②C与H O(g)反应制取水煤气 ③煅烧石灰石制生石灰
2
④碳酸氢钠与盐酸反应 ⑤食物因氧化而腐败
(2)某实验小组用50.00mL0.55molL1的NaOH溶液和50.00mL0.50molL1的HCl溶液
进行中和反应反应热的测定,实验装置如图所示。
①从实验装置上看,图中缺少的一种玻璃仪器是 。
②实验数据如表所示。
起始温度t /℃ 终止温度 温度差
1
次数
t /℃ t t /℃
2 2 1
溶液 溶液 平均值
高二化学 4/8
{#{QQABZQEkwgqQkJbACS4qAQEgC0kYkIMgJOgEAUAQOAwLQBFIBIA=}#}1 26.2 26.0 26.1 30.1 4.0
2 27.0 27.4 27.2 30.7 3.5
3 25.9 25.9 25.9 29.2 3.3
4 26.4 26.2 26.3 29.7 3.4
近似认为0.55molL1的NaOH溶液和0.50molL1的HCl溶液的密度都是1g/cm3,中和后生成溶液的比
热容c4.18J/g℃。测得的H+(aq)+OH-(aq)=H O(l)的ΔH 。(小数点后一位)
2
③上述实验结果与ΔH57.3kJ/mol有偏差,产生这种偏差的原因可能是 (填序号)。
a.实验装置保温,隔热效果差 b.实验室环境温度较高
c.用温度计测定NaOH溶液起始温度后未洗涤,直接测定盐酸的温度
(3)通常把拆开1mol某化学键吸收的能量看作是该化学键的键能。下表是常见的键能数据,已知合成氨反应,
N g3H g 2NH g ΔH92kJmol1则a为 。
2 2 3
化学键 NH NN HH
键能(kJ/mol) 386 946 a
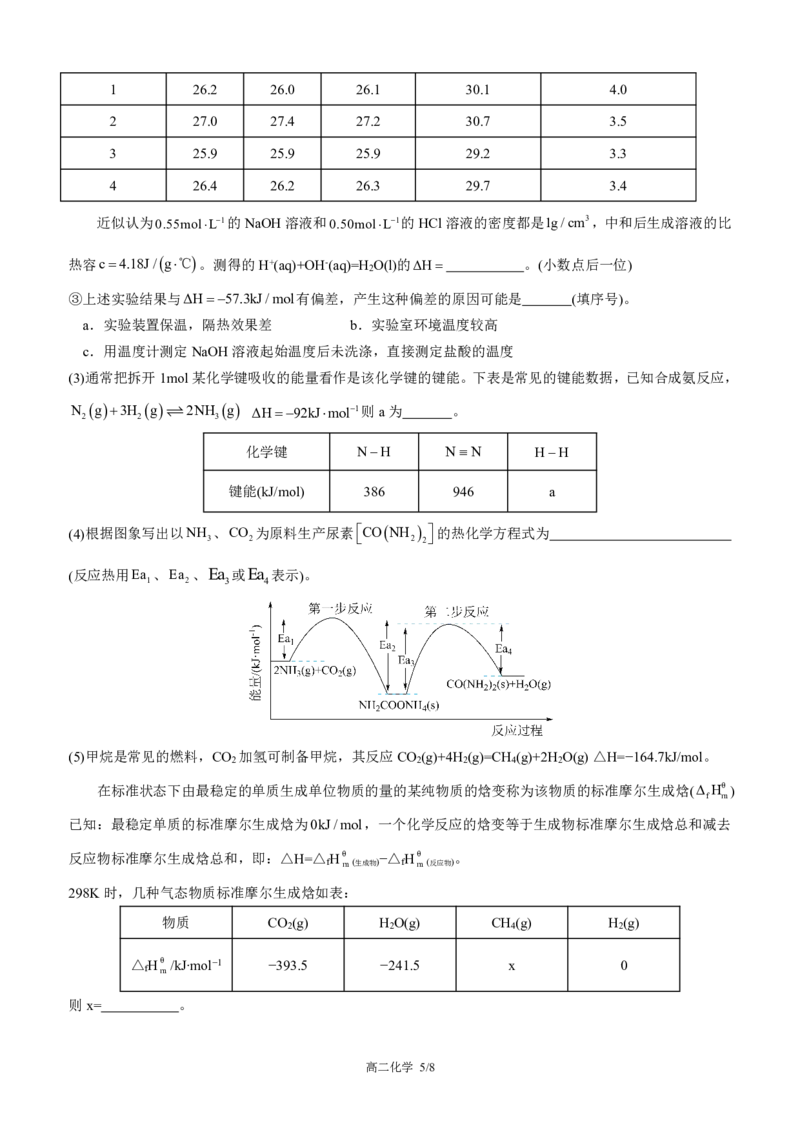
(4)根据图象写出以NH
3
、CO
2
为原料生产尿素
CONH
2
2
的热化学方程式为
(反应热用Ea 、Ea 、Ea 或Ea 表示)。
1 2 3 4
(5)甲烷是常见的燃料,CO 加氢可制备甲烷,其反应CO (g)+4H (g)=CH (g)+2H O(g)△H=−164.7kJ/mol。
2 2 2 4 2
在标准状态下由最稳定的单质生成单位物质的量的某纯物质的焓变称为该物质的标准摩尔生成焓( Hθ )
f m
已知:最稳定单质的标准摩尔生成焓为0kJ/mol,一个化学反应的焓变等于生成物标准摩尔生成焓总和减去
反应物标准摩尔生成焓总和,即:△H=△Hθ −△Hθ 。
f m(生成物) f m(反应物)
298K时,几种气态物质标准摩尔生成焓如表:
物质 CO (g) H O(g) CH (g) H (g)
2 2 4 2
△Hθ /kJ∙mol−1 −393.5 −241.5 x 0
f m
则x= 。
高二化学 5/8
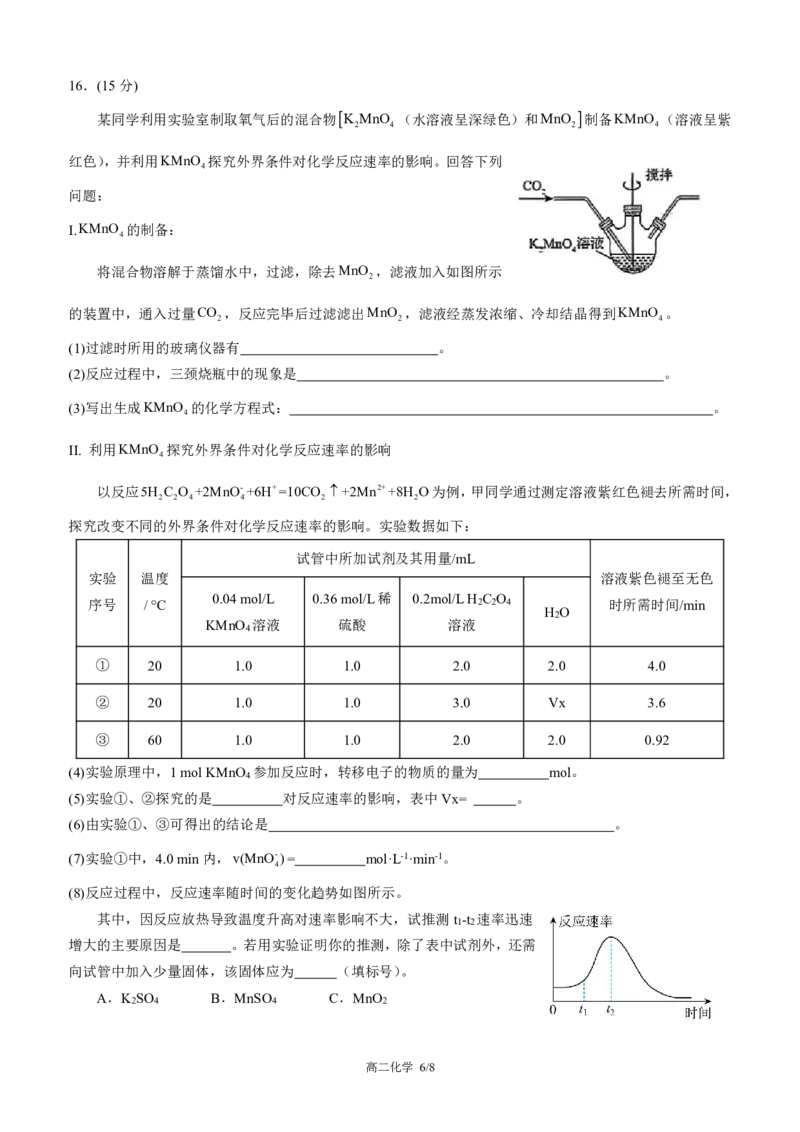
{#{QQABZQEkwgqQkJbACS4qAQEgC0kYkIMgJOgEAUAQOAwLQBFIBIA=}#}16.(15分)
某同学利用实验室制取氧气后的混合物 K MnO (水溶液呈深绿色)和MnO 制备KMnO (溶液呈紫
2 4 2 4
红色),并利用KMnO 探究外界条件对化学反应速率的影响。回答下列
4
问题:
I.KMnO 的制备:
4
将混合物溶解于蒸馏水中,过滤,除去MnO ,滤液加入如图所示
2
的装置中,通入过量CO ,反应完毕后过滤滤出MnO ,滤液经蒸发浓缩、冷却结晶得到KMnO 。
2 2 4
(1)过滤时所用的玻璃仪器有 。
(2)反应过程中,三颈烧瓶中的现象是 。
(3)写出生成KMnO 的化学方程式: 。
4
II. 利用KMnO 探究外界条件对化学反应速率的影响
4
以反应5H C O +2MnO-+6H+=10CO +2Mn2++8H O为例,甲同学通过测定溶液紫红色褪去所需时间,
2 2 4 4 2 2
探究改变不同的外界条件对化学反应速率的影响。实验数据如下:
试管中所加试剂及其用量/mL
实验 温度 溶液紫色褪至无色
序号 /°C 0.04mol/L 0.36mol/L稀 0.2mol/LH 2 C 2 O 4 时所需时间/min
H O
2
KMnO 溶液 硫酸 溶液
4
① 20 1.0 1.0 2.0 2.0 4.0
② 20 1.0 1.0 3.0 Vx 3.6
③ 60 1.0 1.0 2.0 2.0 0.92
(4)实验原理中,1molKMnO 参加反应时,转移电子的物质的量为 mol。
4
(5)实验①、②探究的是 对反应速率的影响,表中Vx= 。
(6)由实验①、③可得出的结论是 。
(7)实验①中,4.0min内,v(MnO-)= mol·L-1·min-1。
4
(8)反应过程中,反应速率随时间的变化趋势如图所示。
其中,因反应放热导致温度升高对速率影响不大,试推测t -t 速率迅速
1 2
增大的主要原因是 。若用实验证明你的推测,除了表中试剂外,还需
向试管中加入少量固体,该固体应为 (填标号)。
A.K SO B.MnSO C.MnO
2 4 4 2
高二化学 6/8
{#{QQABZQEkwgqQkJbACS4qAQEgC0kYkIMgJOgEAUAQOAwLQBFIBIA=}#}17.(15分)
CaCO 的热分解与Ni P 催化的CH 重整结合,可生产高纯度合成气(H 和CO),实现碳资源的二次利用。
3 x y 4 2
主要反应如下:
反应Ⅰ:CaCO s CaOsCO g ΔH 178kJ·mol-1
3 2 1
反应Ⅱ:CH gCO g 2COg2H g ΔH 247kJ·mol-1
4 2 2 2
反应Ⅲ:H gCO g COgH Og ΔH 41kJ·mol-1
2 2 2 3
回答下列问题:
(1)CaO的电子式为 。
(2)反应Ⅳ:CH gH Og COg3H g ΔH kJ·mol-1,该反应自发进行的条件为
4 2 2 4
(填“低温”“高温”或“任何温度”)。
(3)恒压条件下,加入CH 进行重整反应可以促进CaCO 分解,原因为 。
4 3
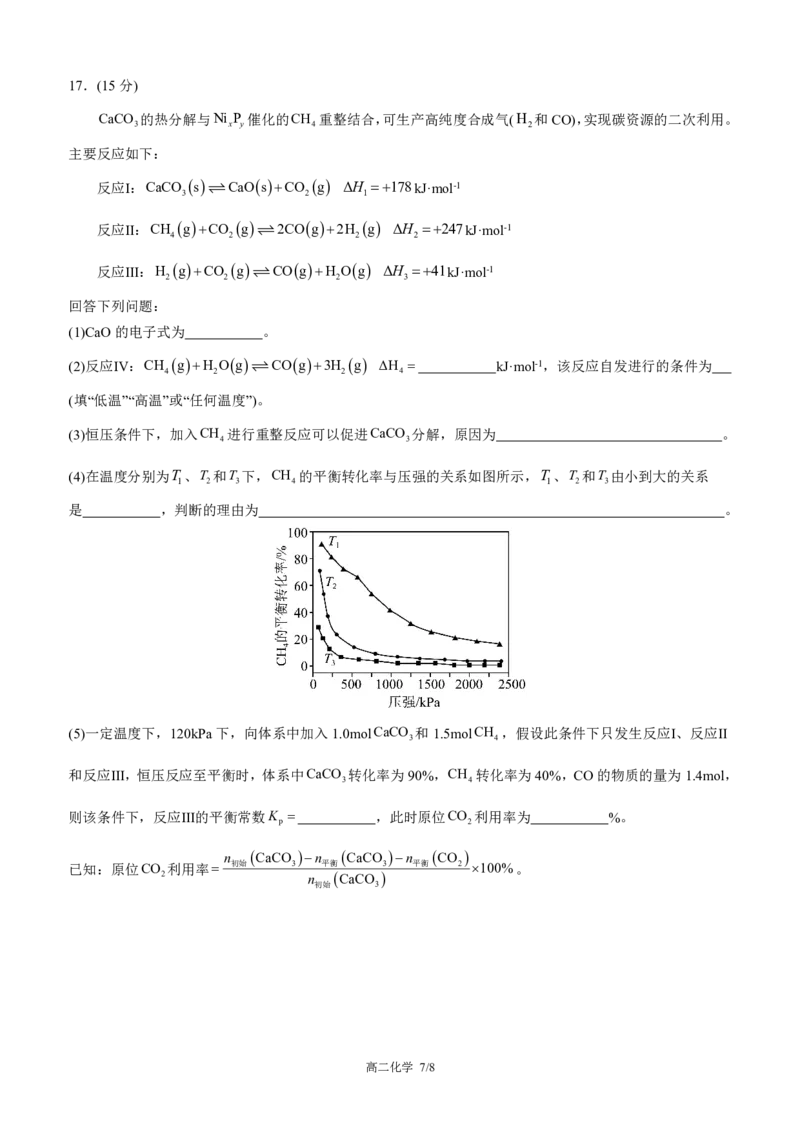
(4)在温度分别为T 、T 和T 下,CH 的平衡转化率与压强的关系如图所示,T 、T 和T 由小到大的关系
1 2 3 4 1 2 3
是 ,判断的理由为 。
(5)一定温度下,120kPa下,向体系中加入1.0molCaCO 和1.5molCH ,假设此条件下只发生反应Ⅰ、反应Ⅱ
3 4
和反应Ⅲ,恒压反应至平衡时,体系中CaCO 转化率为90%,CH 转化率为40%,CO的物质的量为1.4mol,
3 4
则该条件下,反应Ⅲ的平衡常数K ,此时原位CO 利用率为 %。
p 2
n CaCO n CaCO n CO
已知:原位CO 利用率 初始 3 平衡 3 平衡 2 100%。
2 n CaCO
初始 3
高二化学 7/8
{#{QQABZQEkwgqQkJbACS4qAQEgC0kYkIMgJOgEAUAQOAwLQBFIBIA=}#}18.(14分)磷酸铁锂(LFP)是目前应用广泛的动力电池材料,回收磷酸铁锂具有重要意义。一种从废旧磷酸铁
锂正极片(含LiFePO 、导电石墨、铝箔)中回收锂的工艺流程如下:
4
已知:①不同温度下,碳酸锂在水中的溶解度如下表所示。
T/℃ 0 10 20 30 50 60 80 100
溶解度/g 1.64 1.53 1.48 1.17 1.05 1.01 0.85 0.72
②Li CO 在水中煮沸时发生水解。
2 3
回答下列问题:(1)在“碱浸”时,为加快浸出速率,可采用的措施为 (任写一种)。
(2)“氧化浸出”时,虽然控制较低温度,但仍需要加入过量H O ,可能的原因是 。
2 2
“氧化浸出”时生成了难溶的FePO ,该反应的离子方程式为 。
4
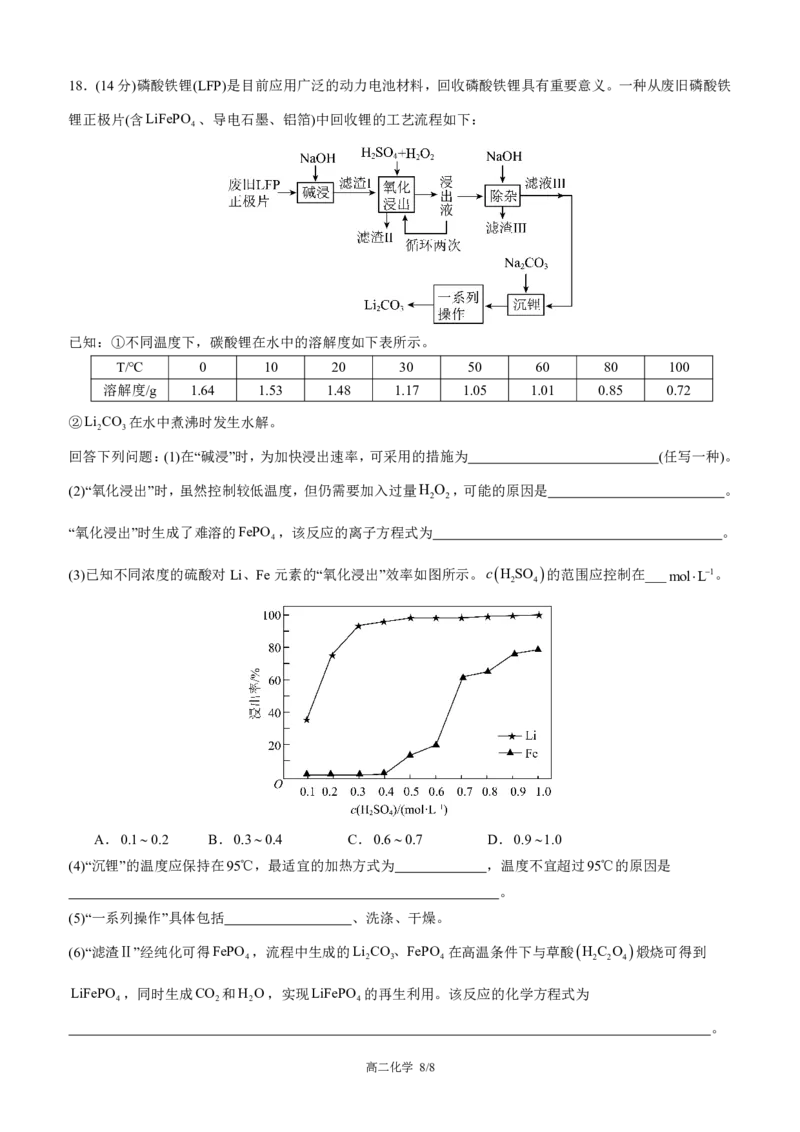
(3)已知不同浓度的硫酸对Li、Fe元素的“氧化浸出”效率如图所示。cH SO 的范围应控制在___molL1。
2 4
A.0.10.2 B.0.30.4 C.0.60.7 D.0.91.0
(4)“沉锂”的温度应保持在95℃,最适宜的加热方式为 ,温度不宜超过95℃的原因是
。
(5)“一系列操作”具体包括 、洗涤、干燥。
(6)“滤渣Ⅱ”经纯化可得FePO ,流程中生成的Li CO、FePO 在高温条件下与草酸H C O 煅烧可得到
4 2 3 4 2 2 4
LiFePO ,同时生成CO 和H O,实现LiFePO 的再生利用。该反应的化学方程式为
4 2 2 4
。
高二化学 8/8
{#{QQABZQEkwgqQkJbACS4qAQEgC0kYkIMgJOgEAUAQOAwLQBFIBIA=}#}