文档内容
4. 下列说法正确的是
四川省万源中学高 2026 届第二次月考试题(高二.下)
化 学
A. 属于苯的同系物,其一氯代物有 6 种
满分 100 分,考试时间 75 分钟。 B.分子式为 C 4 H 9 Br 属于卤代烃的同分异构体有 4 种
C.(CH ) CCH C(CH ) 有 3 种沸点不同的一氯代物
3 3 2 3 3
可能用到的相对原子质量:H 1 C 12 O 16 Si 28 S 32 Mg 24 Cu 64
D.(CH ) C=CHCH CH CH 分子存在顺反异构体
3 2 2 2 3
第Ⅰ卷 选择题
5.下列说法中正确的是
一、单选题(共15个小题,每小题3分,共 45分,每小题只有一个选项符合题意)
①HF 液化和溶于水两个变化过程中都破坏相同的作用力
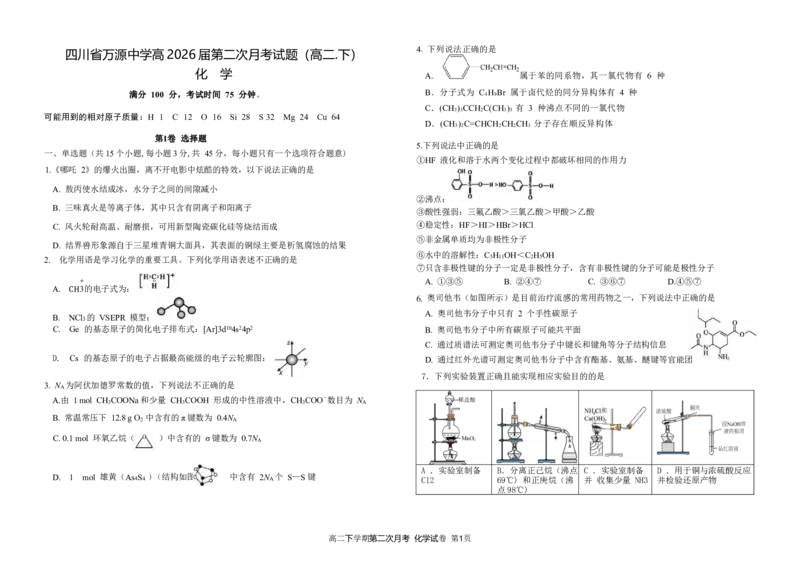
1.《哪吒 2》的爆火出圈,离不开电影中炫酷的特效,以下说法正确的是
A. 敖丙使水结成冰,水分子之间的间隙减小
②沸点:
B. 三味真火是等离子体,其中只含有阴离子和阳离子
③酸性强弱:三氟乙酸>三氯乙酸>甲酸>乙酸
C. 风火轮耐高温、耐磨损,可用新型陶瓷碳化硅等烧结而成 ④稳定性:HF>HI>HBr>HCl
⑤非金属单质均为非极性分子
D. 结界兽形象源自于三星堆青铜大面具,其表面的铜绿主要是析氢腐蚀的结果
⑥水中的溶解性:C H OH<C H OH
2. 化学用语是学习化学的重要工具。下列化学用语表述不正确的是 5 11 2 5
⑦只含非极性键的分子一定是非极性分子,含有非极性键的分子可能是极性分子
A. ①③⑤ B. ②④⑦ C. ③⑥⑦ D.④⑤⑦
A. 3的电子式为:
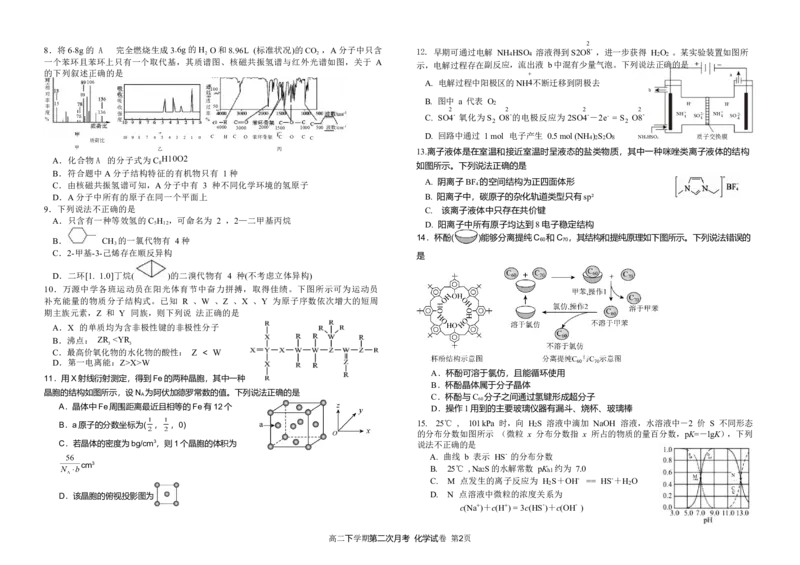
+ 6. 奥司他韦(如图所示)是目前治疗流感的常用药物之一,下列说法中正确的是
CH
A. 奥司他韦分子中只有 2 个手性碳原子
B. NCl 的 VSEPR 模型:
3
C. Ge 的基态原子的简化电子排布式:[Ar]3d104s24p2 B. 奥司他韦分子中所有碳原子可能共平面
C. 通过质谱法可测定奥司他韦分子中键长和键角等分子结构信息
D. Cs 的基态原子的电子占据最高能级的电子云轮廓图: D. 通过红外光谱可测定奥司他韦分子中含有酯基、氨基、醚键等官能团
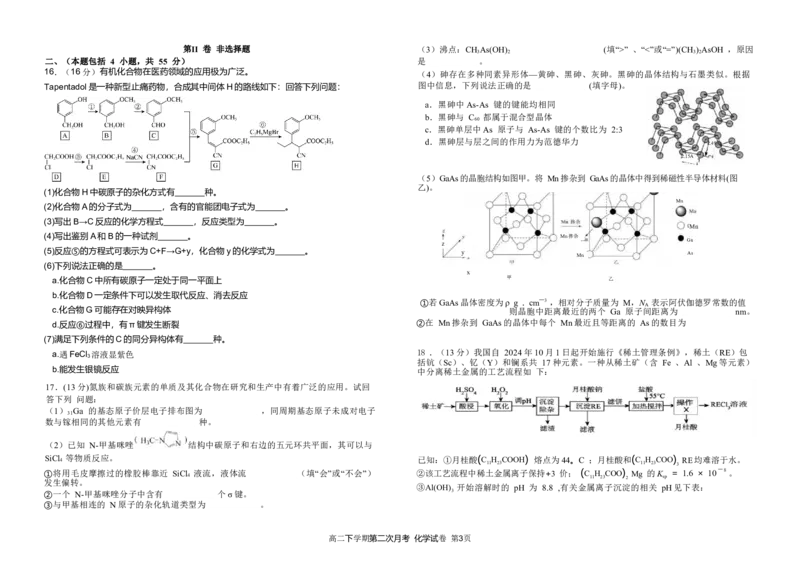
7.下列实验装置正确且能实现相应实验目的的是
3. N 为阿伏加德罗常数的值,下列说法不正确的是
A
A.由 1 mol CH COONa和少量 CH COOH 形成的中性溶液中,CH COO-数目为 N
3 3 3 A
B. 常温常压下 12.8 g O 中含有的π键数为 0.4N
2 A
C. 0.1 mol 环氧乙烷( )中含有的 σ键数为 0.7N
A
A .实验室制备 B.分离正己烷(沸点 C .实验室制备 D .用于铜与浓硫酸反应
D. 1 mol 雄黄(As4S
4
)(结构如图 中含有 2N
A
个 S—S键
Cl2 69℃) 和正庚烷(沸 并 收集少量 NH3 并检验还原产物
点98℃)
高二下学期第二次月考 化学试卷 第1页2
8.将6.8g的 A 完全燃烧生成3.6g的H 2 O和8.96L (标准状况)的CO 2 ,A分子中只含 12. 早期可通过电解 NH 4 HSO 4 溶液得到S2O8 ,进一步获得 H 2 O 2 。某实验装置如图所
一个苯环且苯环上只有一个取代基,其质谱图、核磁共振氢谱与红外光谱如图,关于 A 示,电解过程存在副反应,流出液 b中混有少量- 气泡。下列说法正确的是
的下列叙述正确的是 + a
106 A. 电解过程中阳极区的NH4不断迁移到阴极去
相 100 b
对 89
率 丰 15 吸 收 透 过50 B. 图中 2 a 代表 O 2 2 2 2 H+ H+
度 % 78 136 强 度 率 % 0 C. SO4 氧化为S 2 O8 的电极反应为2SO4 -2e- = S 2 O8 NH+ 4 SO2 4 - NH+ 4 SO2 4 -
4000 3000 2000 1500 1000 500 波数/cm-1 - - - -
质荷比
10 9 8 7 6 5 4 3 2 1 0 C H C O 苯环骨架 C O C C D. 回路中通过 1 mol 电子产生 0.5 mol (NH 4 ) 2 S 2 O 8 NH4HSO4 质子交换膜
甲 乙 丙 13.离子液体是在室温和接近室温时呈液态的盐类物质,其中一种咪唑类离子液体的结构
A.化合物A 的分子式为C H10O2
8 如图所示。下列说法正确的是
B.符合题中A分子结构特征的有机物只有 1种
A. 阴离子BF -的空间结构为正四面体形
C.由核磁共振氢谱可知,A分子中有 3 种不同化学环境的氢原子 4
D.A分子中所有的原子在同一个平面上 B. 阳离子中,碳原子的杂化轨道类型只有sp²
9.下列说法不正确的是 C. 该离子液体中只存在共价键
A.只含有一种等效氢的C H ,可命名为 2 ,2—二甲基丙烷
5 12 D. 阳离子中所有原子均达到8电子稳定结构
14.杯酚( )能够分离提纯C 和C ,其结构和提纯原理如下图所示。下列说法错误的
B. CH 的一氯代物有 4种 60 70
3
C.2-甲基-3-己烯存在顺反异构
是
D.二环[1. 1.0]丁烷( )的二溴代物有 4 种(不考虑立体异构)
10.万源中学各班运动员在阳光体育节中奋力拼搏,取得佳绩。下图所示可为运动员
补充能量的物质分子结构式。已知 R 、W 、Z 、X 、Y 为原子序数依次增大的短周
期主族元素,Z 和 Y 同族,则下列说 法正确的是
A.X 的单质均为含非极性键的非极性分子
B.沸点: ZR X>W
A.杯酚可溶于氯仿,且能循环使用
11.用X射线衍射测定,得到Fe的两种晶胞,其中一种
B.杯酚晶体属于分子晶体
晶胞的结构如图所示,设N 为阿伏加德罗常数的值。下列说法正确的是
A C.杯酚与C 分子之间通过氢键形成超分子
60
A.晶体中Fe周围距离最近且相等的Fe有12个 D.操作1用到的主要玻璃仪器有漏斗、烧杯、玻璃棒
B.a原子的分数坐标为( , ,0) 15. 25℃ , 101 kPa 时,向 H 2 S 溶液中滴加 NaOH 溶液,水溶液中-2 价 S 不同形态
的分布分数如图所示 (微粒 x 分布分数指 x 所占的物质的量百分数,pK=-lgK),下列
C.若晶体的密度为bg/cm3,则1个晶胞的体积为 说法不正确的是
A. 曲线 b 表示 HS 的分布分数 a b
cm3
B. 25℃ ,Na2S的水- 解常数 pK
h1
约为 7.0
M N
C. M 点发生的离子反应为 H S+OH == HS+H O
2 2
C
D.该晶胞的俯视投影图为 D. N 点溶液中微粒的浓度关系为 - -
c(Na+)+c(H+) = 3c(HS)+c(OH )
- -
高二下学期第二次月考 化学试卷 第2页第Ⅱ 卷 非选择题 (3)沸点:CH As(OH) (填“>” 、“<”或“=”)(CH ) AsOH ,原因
3 2 3 2
二、(本题包括 4 小题,共 55 分) 是 。
16.(16分)有机化合物在医药领域的应用极为广泛。
(4)砷存在多种同素异形体—黄砷、黑砷、灰砷。黑砷的晶体结构与石墨类似。根据
Tapentadol是一种新型止痛药物,合成其中间体H的路线如下:回答下列问题: 图中信息,下列说法正确的是 (填字母)。
a.黑砷中As-As 键的键能均相同
b.黑砷与 C 都属于混合型晶体
60
c.黑砷单层中As 原子与 As-As 键的个数比为 2:3
d.黑砷层与层之间的作用力为范德华力
2.49A
2.15A
(5)GaAs的晶胞结构如图甲。将 Mn掺杂到 GaAs的晶体中得到稀磁性半导体材料(图
乙)。
(1)化合物H中碳原子的杂化方式有 种。
Mn
(2)化合物A的分子式为 ,含有的官能团电子式为 。
(3)写出B→C反应的化学方程式 ,反应类型为 。
Mn
(4)写出鉴别A和B的一种试剂 。 Mn掺杂
Ga
z
(5)反应⑤的方程式可表示为C+F→G+y,化合物y的化学式为 。 y Mn As
(6)下列说法正确的是 。
x
a.化合物C中所有碳原子一定处于同一平面上 甲 乙
b.化合物D一定条件下可以发生取代反应、消去反应
①若GaAs晶体密度为ρ g . cm—3 ,相对分子质量为 M,N 表示阿伏伽德罗常数的值
A
c.化合物G可能存在对映异构体 则晶胞中距离最近的两个 Ga 原子间距离为 nm。
d.反应⑥过程中,有π键发生断裂
②在 Mn掺杂到 GaAs的晶体中每个 Mn最近且等距离的 As的数目为
(7)满足下列条件的C的同分异构体有 种。
a.遇FeCl 溶液显紫色 18 .(13分)我国自 2024年10月1日起开始施行《稀土管理条例》,稀土(RE)包
3
括钪(Sc)、钇(Y)和镧系共 17种元素。一种从稀土矿(含 Fe 、Al 、Mg等元素)
b.能发生银镜反应 中分离稀土金属的工艺流程如 下:
17.(13分)氮族和碳族元素的单质及其化合物在研究和生产中有着广泛的应用。试回
答下列 问题:
(1) Ga 的基态原子价层电子排布图为 ,同周期基态原子未成对电子
31
数与镓相同的其他元素有 种。
(2)已知 N-甲基咪唑 结构中碳原子和右边的五元环共平面,其可以与
SiCl 4 等物质反应。 已知:①月桂酸(C H COOH) 熔点为44。C ;月桂酸和(C H COO) RE均难溶于水。
11 23 11 23 3
①将用毛皮摩擦过的橡胶棒靠近 SiCl 液流,液体流 (填“会”或“不会”) ②该工艺流程中稀土金属离子保持+3 价; (C H COO) Mg 的K = 1.6 × 10一8 。
4 11 23 2 sp
发生偏转。
③Al(OH) 开始溶解时的 pH 为 8.8 ,有关金属离子沉淀的相关 pH见下表:
②一个 N-甲基咪唑分子中含有 个σ键。 3
③与甲基相连的 N原子的杂化轨道类型为 。
高二下学期第二次月考 化学试卷 第3页冰醋酸,继续蒸发母液,又可得部分蓝绿色醋酸铜晶体。
离子 Mg2+ Fe3+ Al3+ RE3+
(1)装置b的名称是 ,装置c的作用是 。
(2)步骤2中,温度需要控制在 左右的原因是 。
开始沉淀时的 pH 8.8 1.5 3.6 6.2∼7.4 (3)步骤3中,减压抽滤的目的是 。
(4)步骤3中,加热蒸发时补加冰醋酸的原因是 。
沉淀完全时的 pH / 3.2 4.7 /
实验Ⅱ.间接碘量法测定碱式碳酸铜 中x与y的比
(1) “氧化 ”步骤的主要目的是转化Fe2+ ,发生反应的离子方程式为 。
(2) “沉淀除杂 ”前调 pH 的适宜范围是 ,滤渣的成分有 。
已知: 能与 反应生成CuI,CuI不溶于水。
(3) “沉淀 RE ”后,滤液中Mg2+ 浓度为2.4g / L 。为确保滤饼中检测不到
步骤1:准确称取 碱式碳酸铜样品于烧杯中,加入适量 稀硫酸使固体完全溶解;将
Mg元素,滤液中 c (C H COO-) 应低于 mol / L 。
11 23
(4) ①“加热搅拌 ”有利于加快RE3+ 溶出、提高产率,其原因是 。 得到的溶液完全转移至 容量瓶中,洗涤转移并定容至刻度线。
②“操作 X ”的过程为:先 ,再固液分离。 步骤2:用移液管移取25 ml配好的溶液至250 ml锥形瓶。
(5)稀土元素钇(Y)可用于制备高活性的合金类催化剂Pt Y ,还原YCl 和PtCl 熔融盐
3 3 4 步骤3:加入5 ml pH为4.0的CH 3 COOH-CH 3 COONa缓冲溶液,再加入过量碘化钾溶
制备Pt Y (稀土离子保持+3 价不变) ,生成1molPt Y转移 mol电子
3 3
19.(13分)醋酸铜可作色谱分析试剂和有机合成催化剂等,可以用碱式碳酸铜[
液,振荡摇匀;用已标定的 溶液滴至浅黄色,再加入 淀粉溶液,
]为原料制备。
实验I.用碱式碳酸铜制备醋酸铜晶体 继续滴定至终点。已知:( )
步骤4:平行滴定3次,平均消耗 溶液 。
(5)滴定至终点时,溶液的颜色变化为 。
(6)加入碘化钾后 发生的离子反应方程式为 。
(7)x与y的比为 (用 表示)。
步骤1:称取 碱式碳酸铜于装置a中,加入 水,搅拌得蓝绿色悬浊液。
步骤2:水浴加热a至 ,然后向该装置b中加入 的冰醋酸,缓慢滴入到装置a中,此时
逸出大量气泡。继续在 下混合搅拌 左右,至基本无气泡逸出即可。
1
步骤3:趁热迅速减压抽滤,将滤液倒入蒸发皿中,加热蒸发至溶液体积为原来的 ,
3
补加 冰醋酸,搅拌、冷却、结晶、抽滤,得到蓝绿色醋酸铜晶体;再向剩余母液中补加
高二下学期第二次月考 化学试卷 第4页