文档内容
2024—2025 学年(上)期末考试
高 2026 届化学试题
考试说明:
1.考试时间 90分钟
2.试题总分 100分
3.试卷页数 10页
可能用到的相对原子质量:H 1 C 12 O 16 S 32 Cl 35.5 Cu 64
第Ⅰ卷(选择题,共48分)
一、选择题(共16小题,每小题3分,每小题只有一个符合题意的答案)
1. 化学与社会、生产、生活皆有密切关系。下列有关说法不正确的是
苏打水 水垢
中国“天宫”空间站 碳酸饮料
A. 天然苏打水呈碱性,其中的苏打是指碳酸钠
B. 为了除去锅炉水垢中的 ,可先用 溶液处理,然后用盐酸除去
C. 中国空间站使用的高纯硅太阳能电池可将太阳能转化为电能
D. 打开碳酸饮料瓶盖时有大量气泡逸出,可用勒夏特列原理解释
【答案】A
【解析】
【详解】A.天然苏打水呈碱性,苏打水的苏打是指碳酸氢钠,A错误;B.CaSO 不溶于酸,溶度积常数大于CaCO ,除去锅炉水垢中的 ,可先用 溶液处理,使
4 3
CaSO 转化为CaCO ,然后用盐酸除去,B正确;
4 3
C.高纯硅太阳能电池的能量转化方式为将太阳能转化为电能,C正确;
D.汽水中存在CO(g) CO(aq),打开汽水瓶,压强减小,平衡左移,有大量气泡冒出,能用勒夏特列
2 2
原理解释,D正确;
答案选A。
2. 常温下,下列各组离子在指定溶液中能大量共存的是
A. 醋酸中: 、 、 、
B. 小苏打溶液中: 、 、 、
C. 明矾溶液中: 、 、 、
D. 溶液中: 、 、 、
【答案】B
【解析】
【详解】A.在醋酸溶液中, 离子不能存在,与醋酸反应生成二氧化碳气体和醋酸根离子,A不符合
题意;
B.小苏打是碳酸氢钠的俗称,小苏打溶液中, 、 、 、 各离子不反应,可以大量共存
于溶液中,B符合题意;
C.明矾溶液中含 , 与 发生双水解反应生成氢氧化铝沉淀,不能共存,C不符合题
意;
D. 溶液电离出的 和 都具有还原性;酸性条件下, 和 具有氧化性, 能氧化 ,
能氧化 和 ,不能大量共存,D不符合题意;
故选B。
3. 硫酸铅难溶于水,但可溶于醋酸铵溶液,形成无色溶液,其化学方程式为:。下列有关说法中不正确的是
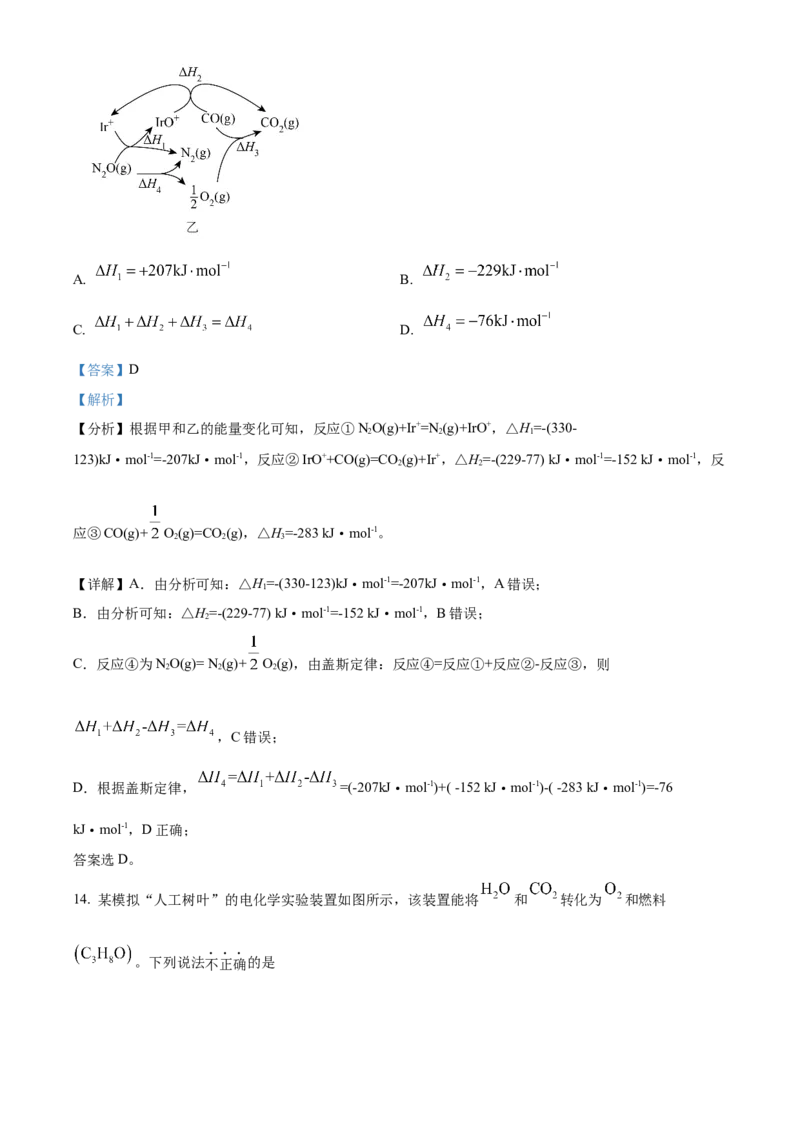
A. 元素的电负性: B. 元素的第一电离能:
.
C 离子半径: D. 基态原子中未成对电子数:
【答案】D
【解析】
【详解】A.同周期元素从左到右电负性逐渐增大,则元素的电负性: ,A正确;
B.同周期元素从左到右第一电离能呈增大趋势,但第 、 族元素的第一电离能大于相邻元素,则元
素的第一电离能,B正确;
C. 无电子,半径最小,C正确;
D.碳原子的基态电子排布为 ,碳有 个未成对电子;硫原子的基态电子排布为
,硫有 个未成对电子,D错误;
故选D。
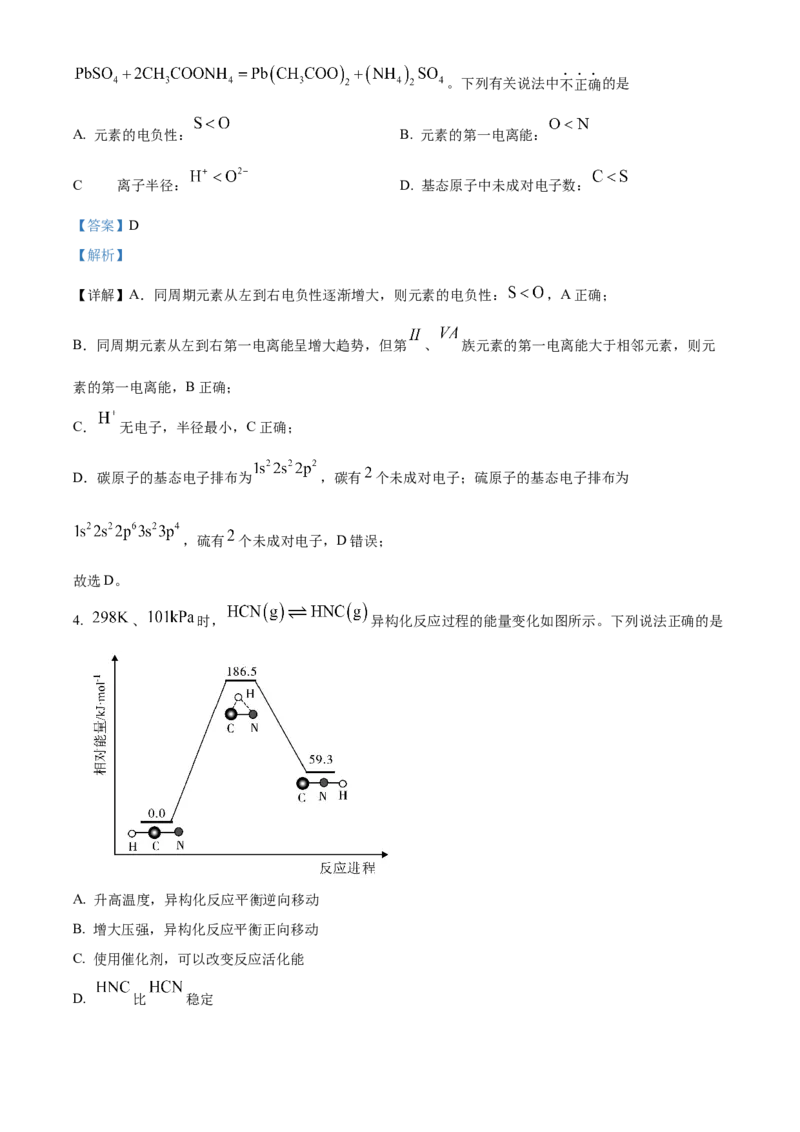
4. 、 时, 异构化反应过程的能量变化如图所示。下列说法正确的是
A. 升高温度,异构化反应平衡逆向移动
B. 增大压强,异构化反应平衡正向移动
C. 使用催化剂,可以改变反应活化能
D. 比 稳定【答案】C
【解析】
【详解】A.由图可知,该反应是吸热反应,升高温度,异构化反应平衡正向移动,A错误;
B.反应 是气体体积不变的反应,增大压强,异构化反应平衡不移动,B错误;
C.使用催化剂,可以降低反应活化能,从而加快反应速率,C正确;
D.能量越低越稳定, 比 能量高,HCN更稳定,D错误;
答案选C。
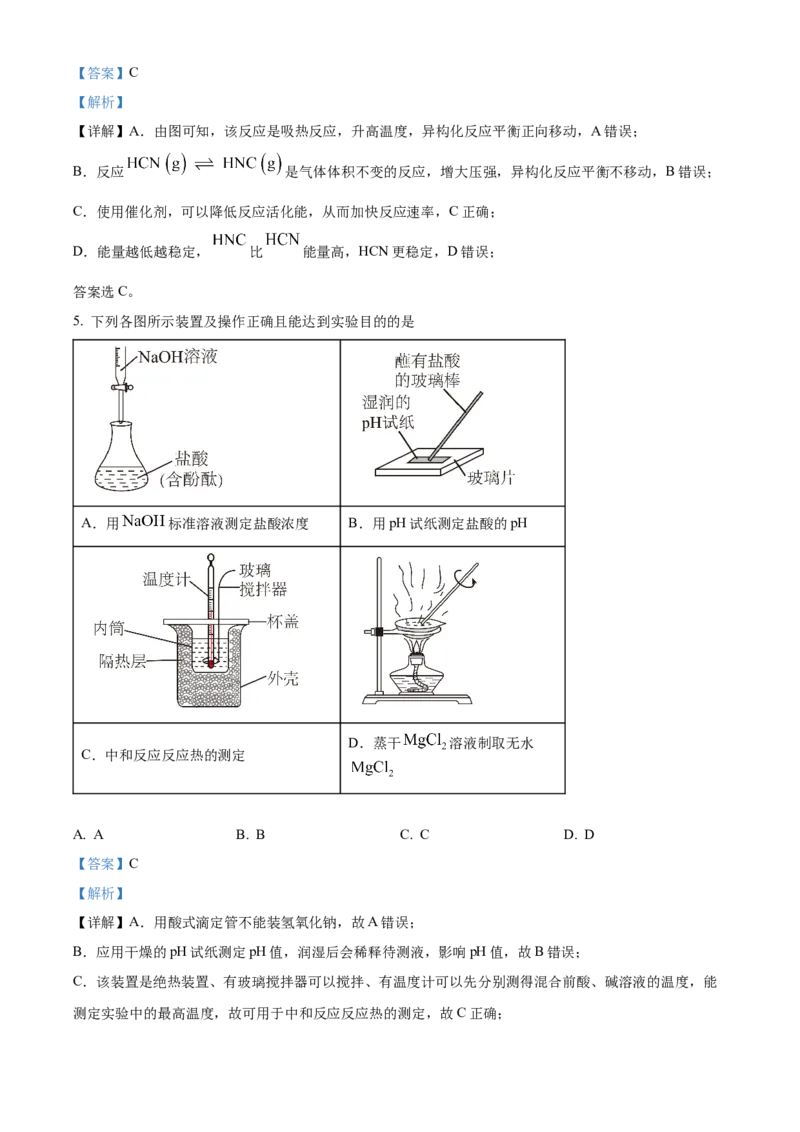
5. 下列各图所示装置及操作正确且能达到实验目的的是
A.用 标准溶液测定盐酸浓度 B.用pH试纸测定盐酸的pH
D.蒸干 溶液制取无水
C.中和反应反应热的测定
A. A B. B C. C D. D
【答案】C
【解析】
【详解】A.用酸式滴定管不能装氢氧化钠,故A错误;
B.应用干燥的pH试纸测定pH值,润湿后会稀释待测液,影响pH值,故B错误;
C.该装置是绝热装置、有玻璃搅拌器可以搅拌、有温度计可以先分别测得混合前酸、碱溶液的温度,能
测定实验中的最高温度,故可用于中和反应反应热的测定,故C正确;D.直接蒸干氯化镁溶液会使其水解,最终蒸干产物为氢氧化镁,应在HCl气氛中蒸干水分,故D错误;
故选:C。
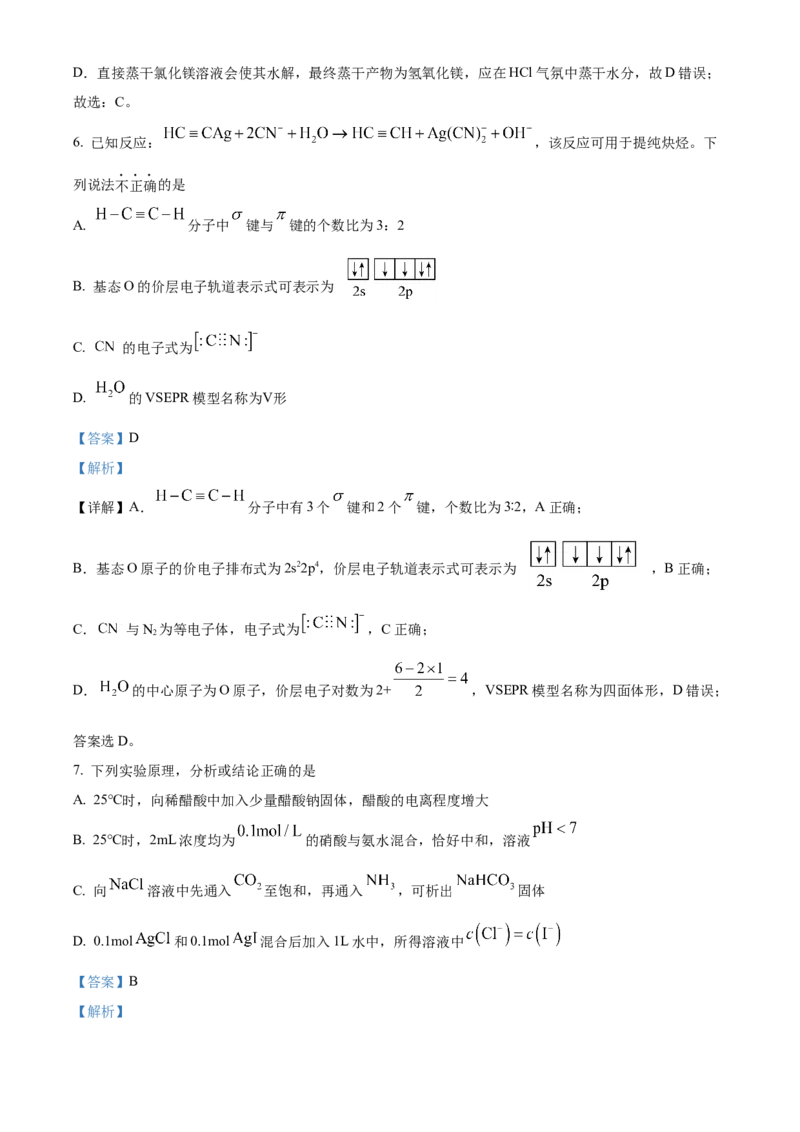
6. 已知反应: ,该反应可用于提纯炔烃。下
列说法不正确的是
A. 分子中 键与 键的个数比为3:2
B. 基态O的价层电子轨道表示式可表示为
C. 的电子式为
D. 的VSEPR模型名称为Ⅴ形
【答案】D
【解析】
【详解】A. 分子中有3个 键和2个 键,个数比为3∶2,A正确;
B.基态O原子的价电子排布式为2s22p4,价层电子轨道表示式可表示为 ,B正确;
C. 与N 为等电子体,电子式为 ,C正确;
2
D. 的中心原子为O原子,价层电子对数为2+ ,VSEPR模型名称为四面体形,D错误;
答案选D。
7. 下列实验原理,分析或结论正确的是
A. 25℃时,向稀醋酸中加入少量醋酸钠固体,醋酸的电离程度增大
B. 25℃时,2mL浓度均为 的硝酸与氨水混合,恰好中和,溶液
C. 向 溶液中先通入 至饱和,再通入 ,可析出 固体
D. 0.1mol 和0.1mol 混合后加入1L水中,所得溶液中
【答案】B
【解析】【详解】A.醋酸是弱电解质,存在电离平衡:CHCOOH CHOO-+H+,加入少量醋酸钠固体,增大了
3 3
醋酸根离子浓度,电离平衡逆向移动,醋酸的电离程度减小,A错误;
B.25℃时,2mL浓度均为 的硝酸与氨水混合,恰好中和生成NH NO ,NH NO 属于强酸弱碱
4 3 4 3
盐,水解显酸性,溶液 ,B正确;
C.NH 的溶解度大于CO,且氨气的水溶液呈碱性、能吸收更多的二氧化碳,制取NaHCO 固体,向
3 2 3
溶液中先通入 至饱和,再通入 ,可析出 固体,C错误;
D.由于K (AgCl))>K (AgI),故等物质的量混合溶液中氯离子和碘离子的浓度不相等、且氯离子浓度大于
sp sp
碘离子浓度,D错误;
答案选B。
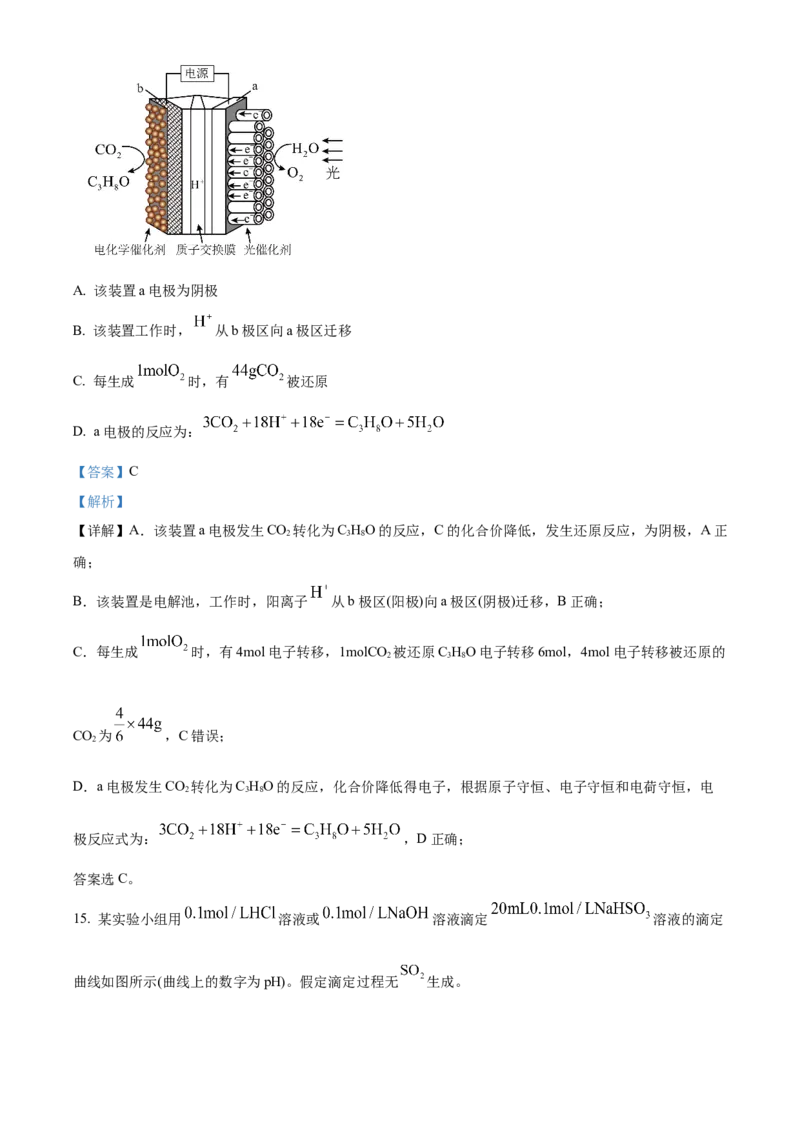
8. 以熔融盐为电解液,以含 、 和Si的铝合金废料为阳极进行电解,实现 的再生。该过程中
A. 阳极上 被氧化
B. 阴极发生的反应为
C. 在电解槽底部产生的阳极泥只含
D. 阳极和阴极的质量变化相等
【答案】A
【解析】
【分析】根据电解原理可知,电解池中阳极发生失电子的氧化反应,阴极发生得电子的还原反应,该题中
以熔融盐为电解液,含 、 和Si等的铝合金废料为阳极进行电解,通过控制一定的条件,从而可使
阳极区Mg和Al发生失电子的氧化反应,分别生成Mg2+和Al3+,Cu和Si不参与反应,阴极区Al3+得电子
生成Al单质,从而实现Al的再生,据此分析解答。
【详解】A.阳极上发生氧化反应, 失去电子生成Al3+被氧化,A正确;
B.阴极发生还原反应,电极反应为 ,B错误;
C.在电解槽底部产生的阳极泥有 和Si,C错误;
D.因为阳极除了铝参与电子转移,镁也参与了电子转移,且还会形成阳极泥,而阴极只有铝离子得电子生成铝单质,根据电子转移数守恒及元素守恒可知,阳极与阴极的质量变化不相等,D错误;
答案选A。
9. 羰基硫( )可作为一种粮食熏蒸剂,能防止某些昆虫,线虫和真菌的危害。在恒容密闭绝热容器中,
一定温度下将10molCO和a 混合使之发生如下反应: ,
经tmin达到平衡,CO物质的量为 , 。下列说法正确的是
A. 升高温度, 浓度增加,表明该反应是吸热反应
B. 当容器内气体压强不再变化时,反应达到平衡状态
C.
D. CO的平衡转化率为
【答案】B
【解析】
【分析】三段式分析如下: ,K=
= ,解得:a=12,据此分析解题。
【详解】A.升高温度, 浓度增加,说明化学平衡逆向移动,故该反应正反应是放热反应, A错误;
B.在绝热容器中反应时,容器内气体温度、压强会随着反应而变化,当容器内气体压强不再变化时,则
温度不变,反应达到平衡状态,B正确;
C. 据分析, ,C错误;
D.CO的平衡转化率为 ,D错误;
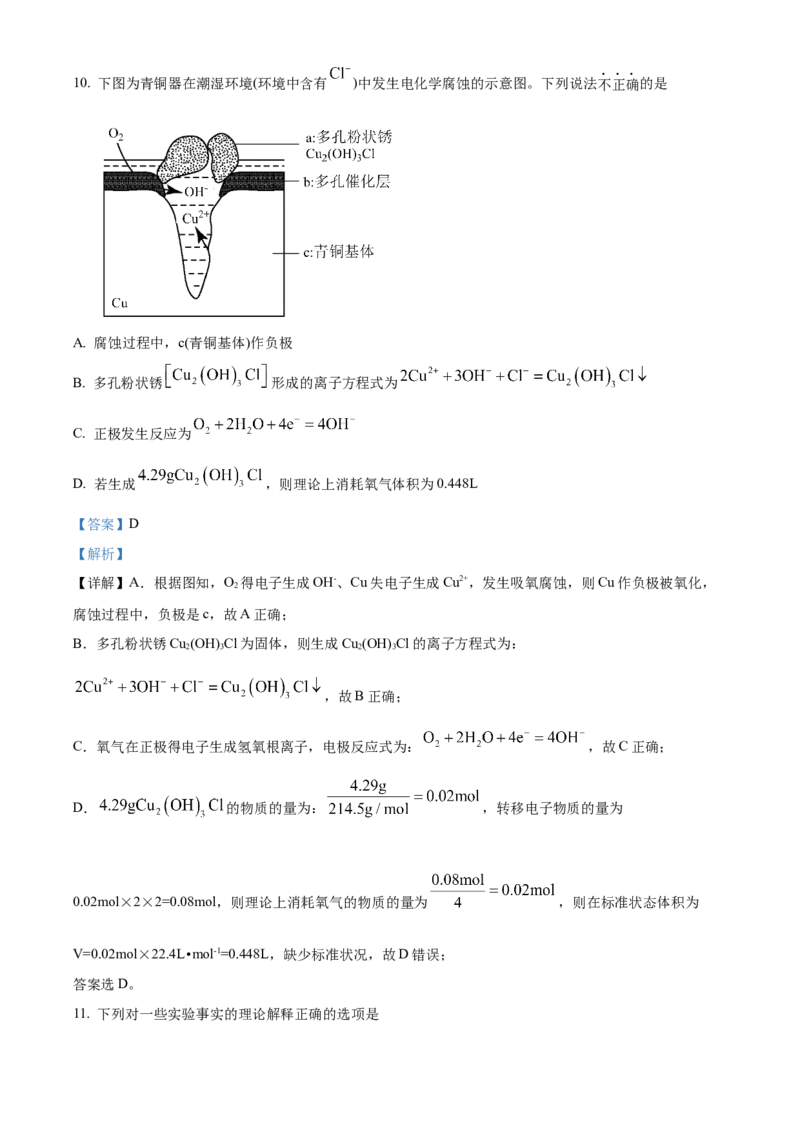
故答案为:B。10. 下图为青铜器在潮湿环境(环境中含有 )中发生电化学腐蚀的示意图。下列说法不正确的是
A. 腐蚀过程中,c(青铜基体)作负极
B. 多孔粉状锈 形成的离子方程式为
C. 正极发生反应为
D. 若生成 ,则理论上消耗氧气体积为0.448L
【答案】D
【解析】
【详解】A.根据图知,O 得电子生成OH-、Cu失电子生成Cu2+,发生吸氧腐蚀,则Cu作负极被氧化,
2
腐蚀过程中,负极是c,故A正确;
B.多孔粉状锈Cu (OH) Cl为固体,则生成Cu (OH) Cl的离子方程式为:
2 3 2 3
,故B正确;
C.氧气在正极得电子生成氢氧根离子,电极反应式为: ,故C正确;
D. 的物质的量为: ,转移电子物质的量为
0.02mol×2×2=0.08mol,则理论上消耗氧气的物质的量为 ,则在标准状态体积为
V=0.02mol×22.4L•mol-1=0.448L,缺少标准状况,故D错误;
答案选D。
11. 下列对一些实验事实的理论解释正确的选项是选项 实验事实 理论解释
元素的第一电离能( ): N的2p能级半充满,较稳定;而O的2p能级为
A
,较易失去一个电子变为半充满
B 为直线形分子 分子中氧碳氧原子之间的夹角为180°
C 水分子很稳定 水分子之间含有大量氢键
D HF的沸点高于 HF的相对分子质量小于
A. A B. B C. C D. D
【答案】A
【解析】
【详解】A.N的电子排布式为:1s22s22p3,2p能级半充满、较稳定,而O的2p能级为 ,较易失去一
个电子变为半充满,第一电离能N大于O,A正确;
B. 的中心原子为C原子,价层电子对为2+ ,C的杂化方式为sp杂化,分子的构型为直
线形,氧碳氧夹角为180°,B错误;
C.水分子很稳定原因是 O-H键键能较大,稳定性与氢键无关,C错误;
D.HF的沸点高于 的原因是HF分子间有氢键,分子间作用力大,沸点高,D错误;
答案选A。
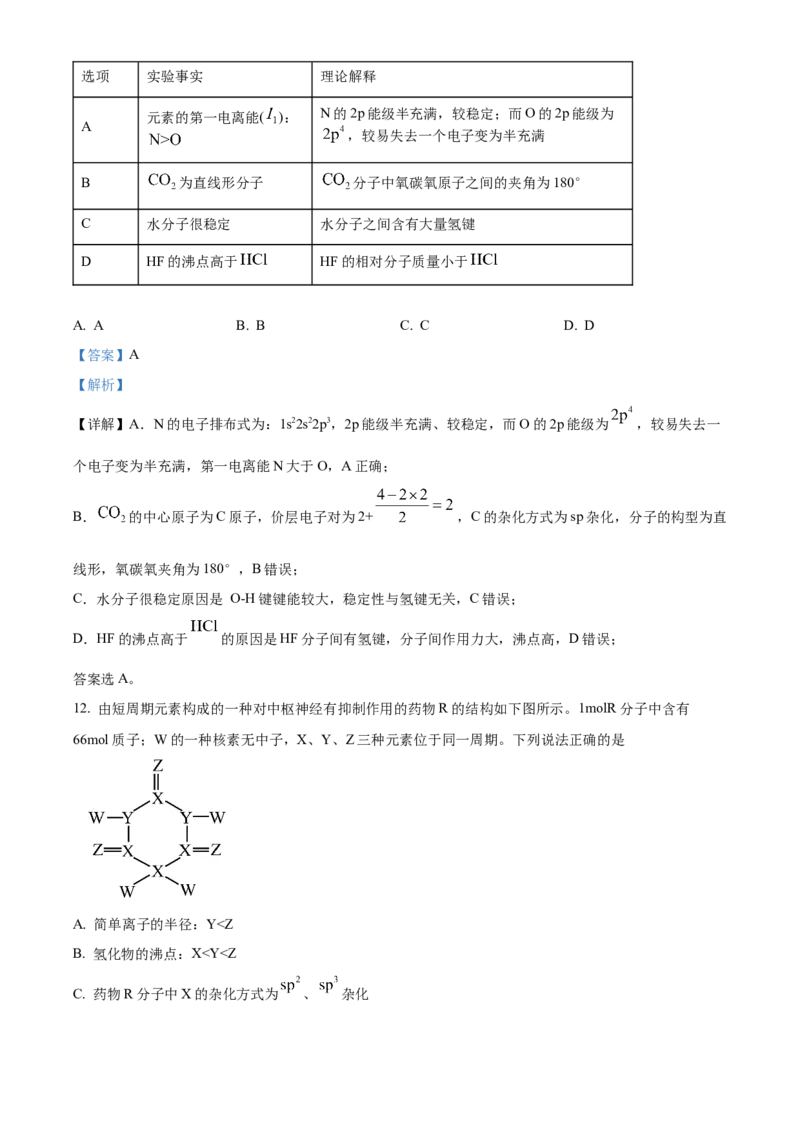
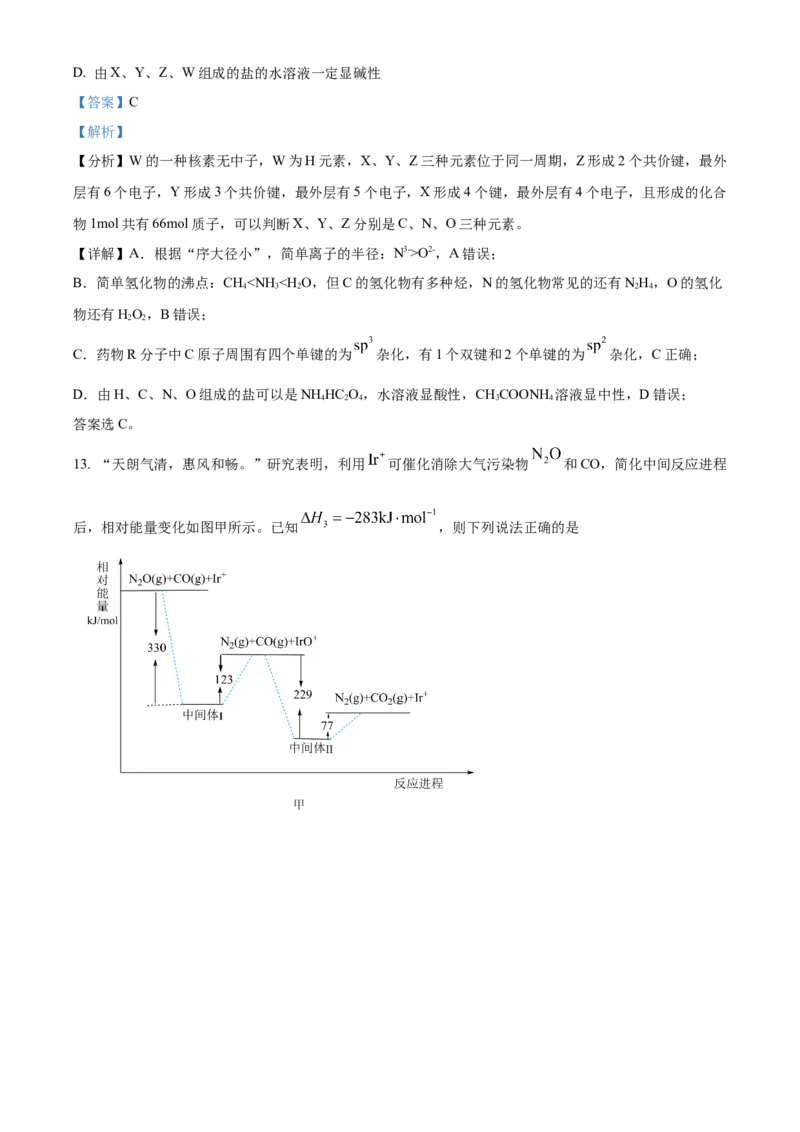
12. 由短周期元素构成的一种对中枢神经有抑制作用的药物R的结构如下图所示。1molR分子中含有
66mol质子;W的一种核素无中子,X、Y、Z三种元素位于同一周期。下列说法正确的是
A. 简单离子的半径:YO2-,A错误;
B.简单氢化物的沸点:CHK,平衡逆向移动,D正确;
答案选D。
第Ⅱ卷(非选择题,共52分)
二、非选择题(共4小题,52分)
17. 氨硼烷( )含氢量高、热稳定性好,是一种具有潜力的固体储氢材料。回答下列问题:
(1)H、B、N中,基态原子轨道上未成对电子最多的是___________;电负性最大的是___________;B
的2s轨道形状为___________。
(2) 分子中只有 键,B原子的杂化轨道类型为___________。 在一定条件下分解产
生 , 分子空间形状为___________。
(3) 分子中,与N原子相连的3个H呈正电性 ,与B原子相连的3个H呈负电性 ,
为由___________键(填“极性”或“非极性”)构成的___________(填“极性”或“非极性”)分
子;与 原子总数相等,电子总数相等的等电子体是 ,其熔点比
___________(填“高”或“低”),原因是在 分子之间,存在___________,也称“双氢键”。
【答案】(1) ①. N ②. N ③. 球形
(2) ①. ②. 三角锥形
(3) ①. 极性 ②. 极性 ③. 低 ④. 与 的静电引力
【解析】
【小问1详解】
H 的未成对电子数为1,B的电子排布式为1s22s1,未成对电子数为1,N的电子排布式为1s22s22p3,未成
对电子数为3,基态原子轨道上未成对电子最多的是N;
非金属性越强,电负性越大,H、B、N中非金属性最强的是N,电负性最大的是N;B的2s轨道的形状为球形;
【小问2详解】
分子中只有 键,结构式为: ,B原子价层电子对数为4,杂化轨道类型为
sp3杂化;NH 分子中的中心原子为N,价层电子对数为3+ ,有1对孤电子对,空间构型为三
3
角锥形;
【
小问3详解】
中的N-H键和B-H键都是极性键, 分子不对称,正负电中心不重合,属于极性键构成
的极性分子;由题目信息可知: 中有呈正电性 和呈负电性 , 和 之间
有静电引力,使得分子间作用力大,沸点高于CHCH。
3 3
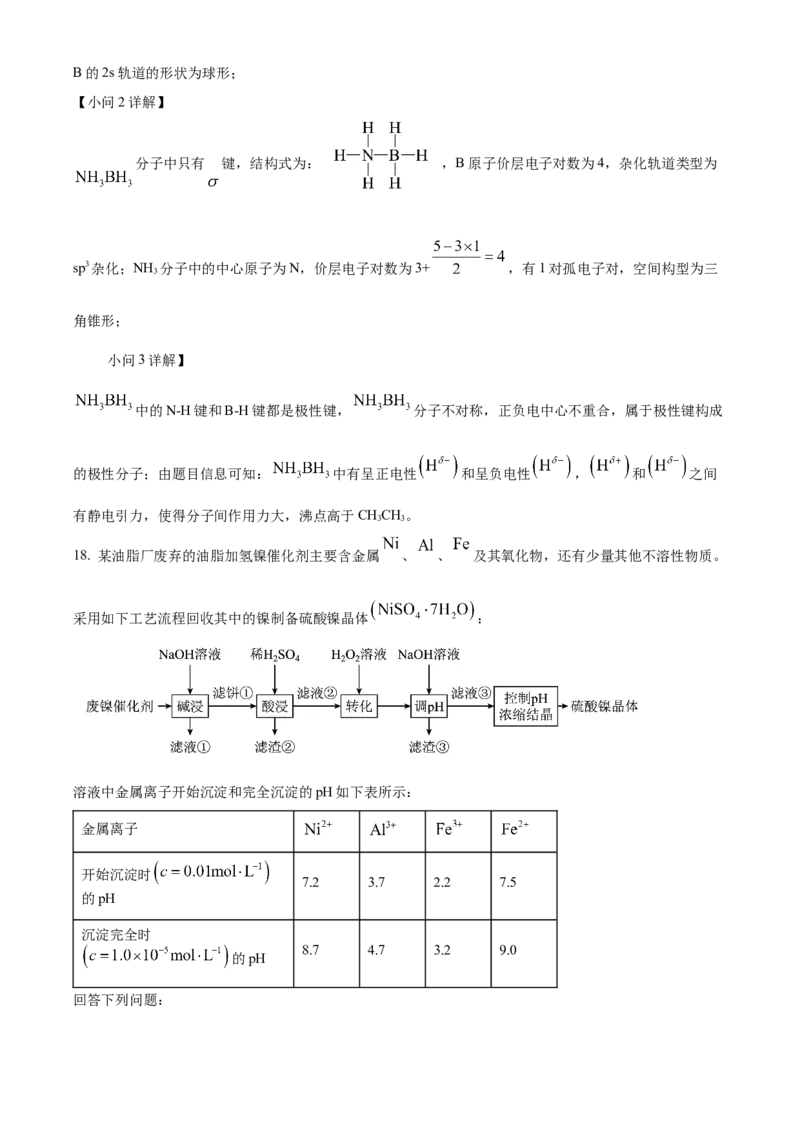
18. 某油脂厂废弃的油脂加氢镍催化剂主要含金属 、 、 及其氧化物,还有少量其他不溶性物质。
采用如下工艺流程回收其中的镍制备硫酸镍晶体 :
溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
金属离子
开始沉淀时
7.2 3.7 2.2 7.5
的pH
沉淀完全时
8.7 4.7 3.2 9.0
的pH
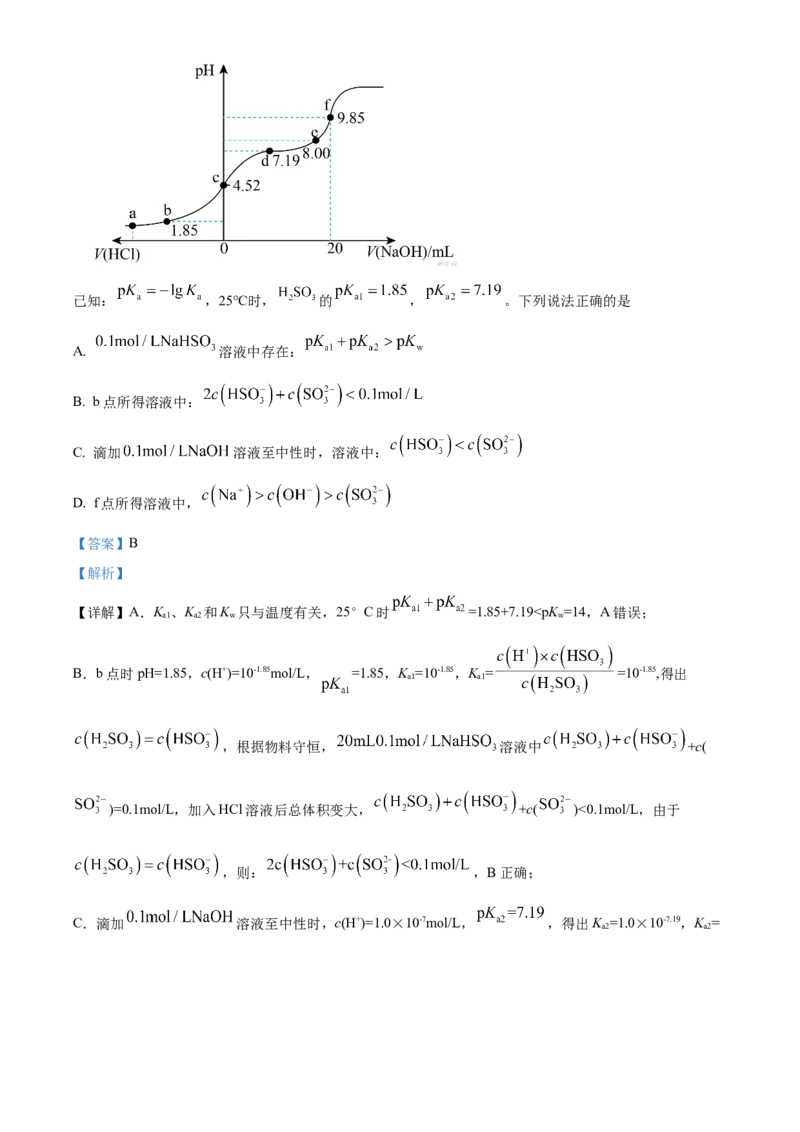
回答下列问题:(1) 、 、 三种元素位于周期表中___________区, 中镍离子的简化电子排布式
为___________。
(2)“碱浸”中 的作用:①除去油脂:②___________(用化学方程式表示)。
(3)向“滤液②”中加KSCN溶液,溶液变红,表明滤液②中含___________。
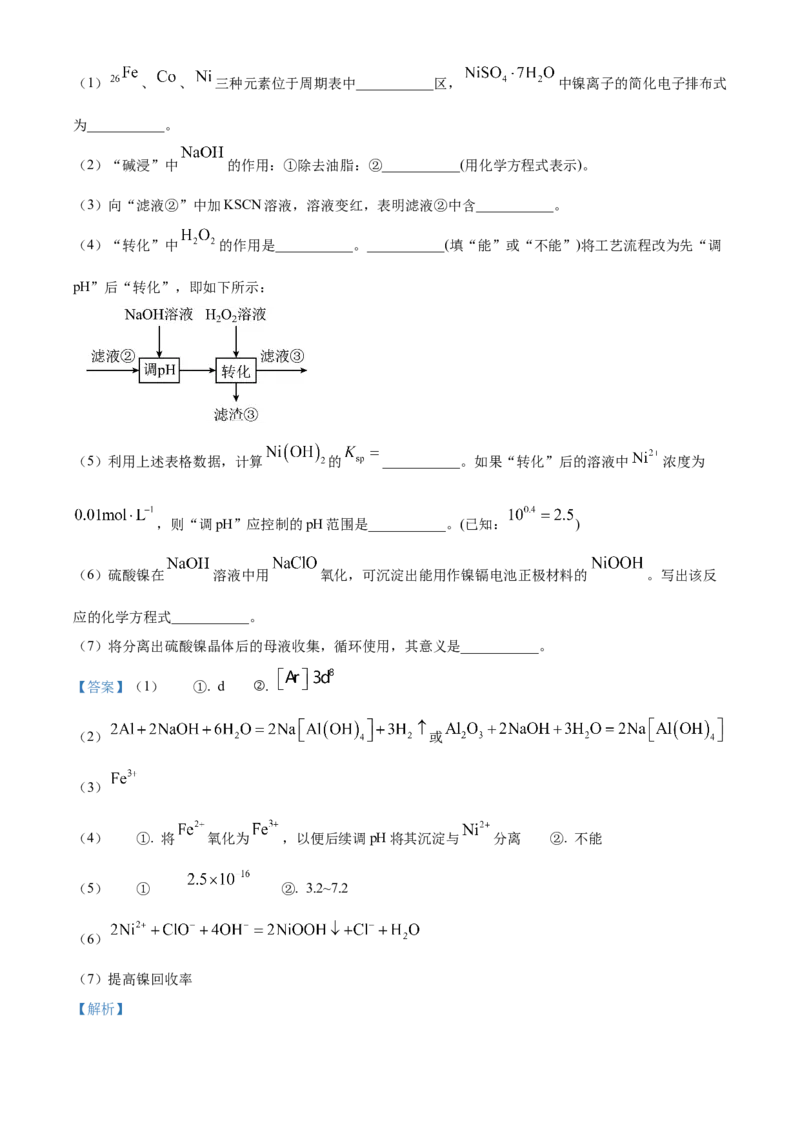
(4)“转化”中 的作用是___________。___________(填“能”或“不能”)将工艺流程改为先“调
pH”后“转化”,即如下所示:
(5)利用上述表格数据,计算 的 ___________。如果“转化”后的溶液中 浓度为
,则“调pH”应控制的pH范围是___________。(已知: )
(6)硫酸镍在 溶液中用 氧化,可沉淀出能用作镍镉电池正极材料的 。写出该反
应的化学方程式___________。
(7)将分离出硫酸镍晶体后的母液收集,循环使用,其意义是___________。
【答案】(1) ①. d ②.
(2) 或
(3)
(4) ①. 将 氧化为 ,以便后续调pH将其沉淀与 分离 ②. 不能
.
(5) ① ②. 3.2~7.2
(6)
(7)提高镍回收率
【解析】【分析】由工艺流程分析可得,向废镍催化剂中加入NaOH溶液进行碱浸,可除去油脂,Al和Al O 均能
2 3
与NaOH溶液反应生成Na[Al(OH)],将Al及其氧化物溶解,得到的滤液①含有Na[Al(OH)],滤饼①为
4 4
Ni、Fe及其氧化物和少量其他不溶性杂质,加稀HSO 酸浸后得到含有Ni2+、Fe2+、Fe3+的滤液②,Fe2+经
2 4
HO 氧化为Fe3+后,加入NaOH调节pH使Fe3+转化为Fe(OH) 沉淀除去,再控制pH浓缩结晶得到硫酸镍
2 2 3
的晶体,据此分析解答问题。
【小问1详解】
Fe、Co、Ni属于第四周期第VIII族,属于d区;Ni是28号元素,Ni2+的简化的电子排布式为: ;
【小问2详解】
根据分析,“碱浸”中 的作用:除去油脂、溶解Al和Al O,化学方程式为:
2 3
或 ;
【小问3详解】
Fe3+遇到KSCN溶液显示红色,向“滤液②”中加KSCN溶液,溶液变红,表明滤液②中含Fe3+;
【小问4详解】
“转化”中 的作用是:将 氧化为 ,以便后续调pH将其沉淀与 分离;
不能将工艺流程改为先“调pH”后“转化”,若先“调pH”Fe2+和Ni2+均会沉淀,不能将Fe2+和Ni2+分离;
【小问5详解】
根据Ni2+沉淀完全时,c(Ni2+)=1.0×10-5mol/L,对应的pH=8.7,c(OH-)=1.0×10-5.3mol/L,则K =
sp
c(Ni2+)×c2(OH-)=1.0×10-5×(1.0×10-5.3)2=10-15.6=2.5×10-16;
浓度为 ,根据K = c(Ni2+)×c2(OH-),Ni2+开始沉淀时的c2(OH-)= =2.5×10-
sp
14,c(OH-)=1.0×10-6.8mol/L,c(H+)=1.0×10-7.2mol/L,pH=7.2,Fe3+完全沉淀的pH为3.2,则“调pH”应控制
的pH范围为3.2-7.2;
【小问6详解】
Ni2+与ClO-在碱性溶液中反应生成NiOOH沉淀,反应的离子方程式为:
;
【小问7详解】
将分离出硫酸镍晶体后的母液收集,循环使用,其意义是:提高镍回收率。19. 草酸 是一种重要的化学试剂。
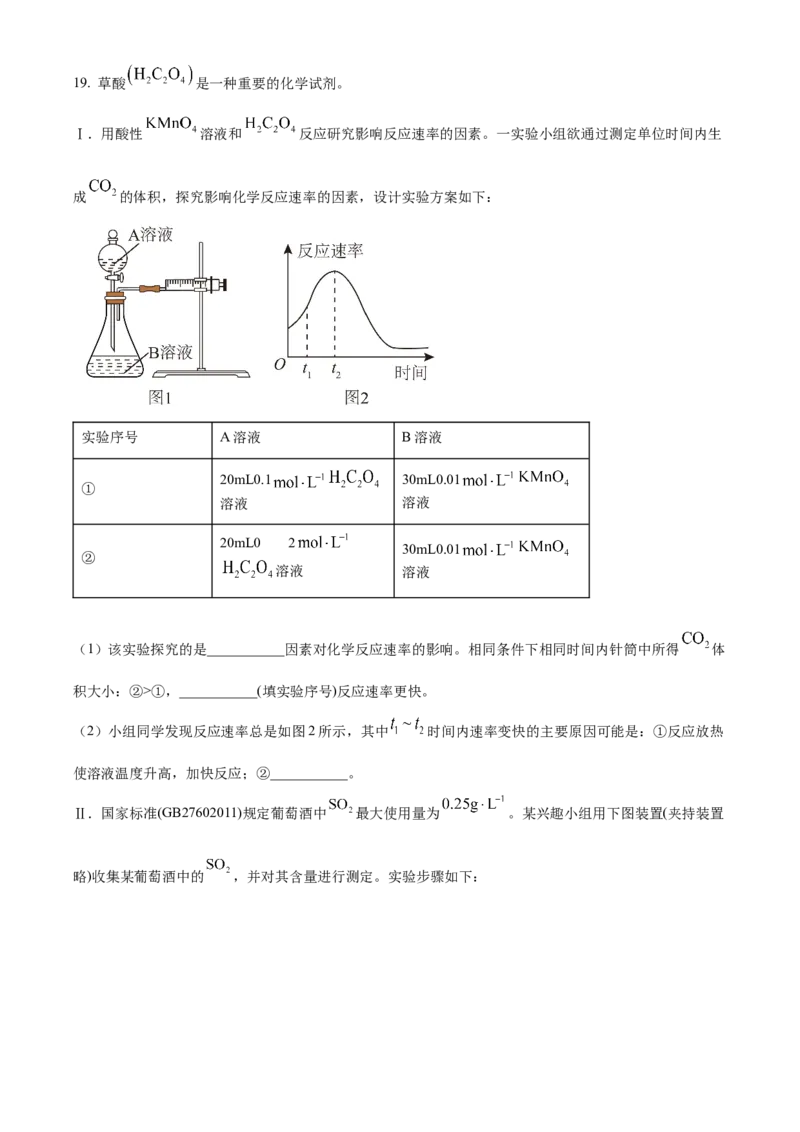
Ⅰ.用酸性 溶液和 反应研究影响反应速率的因素。一实验小组欲通过测定单位时间内生
成 的体积,探究影响化学反应速率的因素,设计实验方案如下:
实验序号 A溶液 B溶液
20mL0.1 30mL0.01
①
溶液 溶液
.
20mL0 2
30mL0.01
②
溶液 溶液
(1)该实验探究的是___________因素对化学反应速率的影响。相同条件下相同时间内针筒中所得 体
积大小:②>①,___________(填实验序号)反应速率更快。
(2)小组同学发现反应速率总是如图2所示,其中 时间内速率变快的主要原因可能是:①反应放热
使溶液温度升高,加快反应;②___________。
Ⅱ.国家标准(GB27602011)规定葡萄酒中 最大使用量为 。某兴趣小组用下图装置(夹持装置
略)收集某葡萄酒中的 ,并对其含量进行测定。实验步骤如下:a.向B中加入300.00mL葡萄酒和适量稀硫酸,加热,促使 全部逸出,并全部进入C中的
的酸性 溶液中,充分反应后,再将C中得到的吸收液(紫红色)稀释至
500mL。
b.取25.00mL稀释后的吸收液于一只洁净的锥形瓶中,用 标准液滴定吸收液中残
余的 。
c.数据处理:
标准溶液的体积/mL
吸收液的体
滴定次数
积/mL 消耗标准溶液体
滴定前刻度 滴定后刻度
积
1 25.00 0.10 6.60 6.50
2 25.00 7.60 14.00 6.40
3 25.00 0.20 6.80 6.60
已知:酸性 溶液可以氧化乙醇。
回答下列问题:
(3)该滴定实验不会用到下图中___________(填标号)滴定管。(4)写出步骤b中发生的离子反应___________。
(5)滴定终点的现象为___________。
(6)根据表格中的数据计算该葡萄酒中 含量为___________ (保留2位小数)。
(7)下列操作会导致所测葡萄酒中 含量偏低的是___________(填标号)。
a.滴定管装标准液前未润洗
b.用滴定管量取稀释后的吸收液时,未用吸收液润洗
c.达到滴定终点时,仰视读数
d.装标准溶液的滴定管尖嘴部分在滴定前无气泡,滴定终点时发现气泡
(8)该兴趣小组同学做实验测得 含量总是偏高,可能原因是___________。
【答案】(1) ①. 浓度 ②. ②
(2)反应生成的 具有催化作用,随着 的增多,反应明显加快
(3)乙 (4)
(5)溶液由浅紫色恰好变为无色,且30s不复原
(6)0.26 (7)ac
(8)加热蒸出的 中含有酒精蒸汽,酒精会消耗酸性 溶液(其它合理答案也给分)
【解析】
【小问1详解】
实验①、②的变量是草酸的浓度,该实验探究的是草酸浓度对化学反应速率的影响。相同条件下相同时间
内针筒中所得 体积大小:②>①,说明实验②反应速率更快。【小问2详解】
根据影响反应速率的因素, 时间内速率变快的主要原因可能是:①反应放热使溶液温度升高,加快
反应;②反应生成的 具有催化作用,随着 的增多,反应明显加快。
【小问3详解】
酸性高锰酸钾溶液用酸式滴定管量取,草酸溶液应盛放在酸式滴定管中,该滴定实验不会用到碱式滴定管,
选乙。
【小问4详解】
步骤b中高锰酸钾把草酸氧化为二氧化碳,发生反应的离子方程式为
;
【小问5详解】
滴定终点时,高锰酸钾恰好完全反应,滴定终点的现象为溶液由浅紫色恰好变为无色,且30s不复原。
【小问6详解】
25mL稀释后吸收液消耗6.50mL标准草酸溶液,根据
,草酸消耗高锰酸钾的物质的量为
;二氧化硫消耗高锰酸钾的物质的量为
,二氧化硫和高锰酸钾反应的离子方程式为
,则该葡萄酒中二氧化硫的物质的量为
,该葡萄酒中 含量为 。
【小问7详解】
a.滴定管装标准液前未润洗,消耗标准液体积偏大,则所测葡萄酒中 含量偏低,故选a;b.用滴定管量取稀释后的吸收液时,未用吸收液润洗,吸收液浓度偏小,消耗标准液体积偏小,则所测
葡萄酒中 含量偏高,故不选b;
c.达到滴定终点时,仰视读数,消耗标准液体积偏大,则所测葡萄酒中 含量偏低,故选c;
d.装标准溶液的滴定管尖嘴部分在滴定前无气泡,滴定终点时发现气泡,消耗标准液体积偏小,则所测
葡萄酒中 含量偏高,故不选d;
选ac。
【小问8详解】
酸性 溶液可以氧化乙醇,加热蒸出的 中含有酒精蒸汽,酒精会消耗酸性 溶液,所以
测得 含量总是偏高。
20. 甲烷,甲醇 ,甲醛 等含有一个碳原子的物质称为“一碳”化合物,广泛应用于化
工,医药,能源等方面。研究“一碳”化合物的化学称为“一碳”化学。
(1)已知:ⅰ.
ⅱ.
反应ⅲ. 的反应热 ___________ 。
(2)我国科学家制备了一种 催化剂(下图为分子筛膜催化反应器,反应器中发生反应ⅰ和ⅲ),
实现 高选择性合成 。实现 高选择性合成 的可能原因是:
a.催化剂的选择性;
b.在反应器中适宜的条件下,合成 的反应限度大;
c.生成的部分 及时透过分子筛及多孔载体被 吹扫出去,___________。
(3)已知反应ⅳ ,
①在温度和体积不变的密闭容器中充入一定量的 发生反应ⅳ,经过5分钟,压力传感器显示容器
内的压强由akPa(初始压强)升高到bkPa;这段时间内该反应的平均化学反应速率 ___________
min。
②该反应的速率方程式为 , , 、 表示速率常
数,与温度、活化能有关。升高温度, 的增大程度___________ 的增大程度(填“>”“<”或“=”),
平衡时,容器内压强升高至 , ___________kPa。( 为气体压强平衡常数)
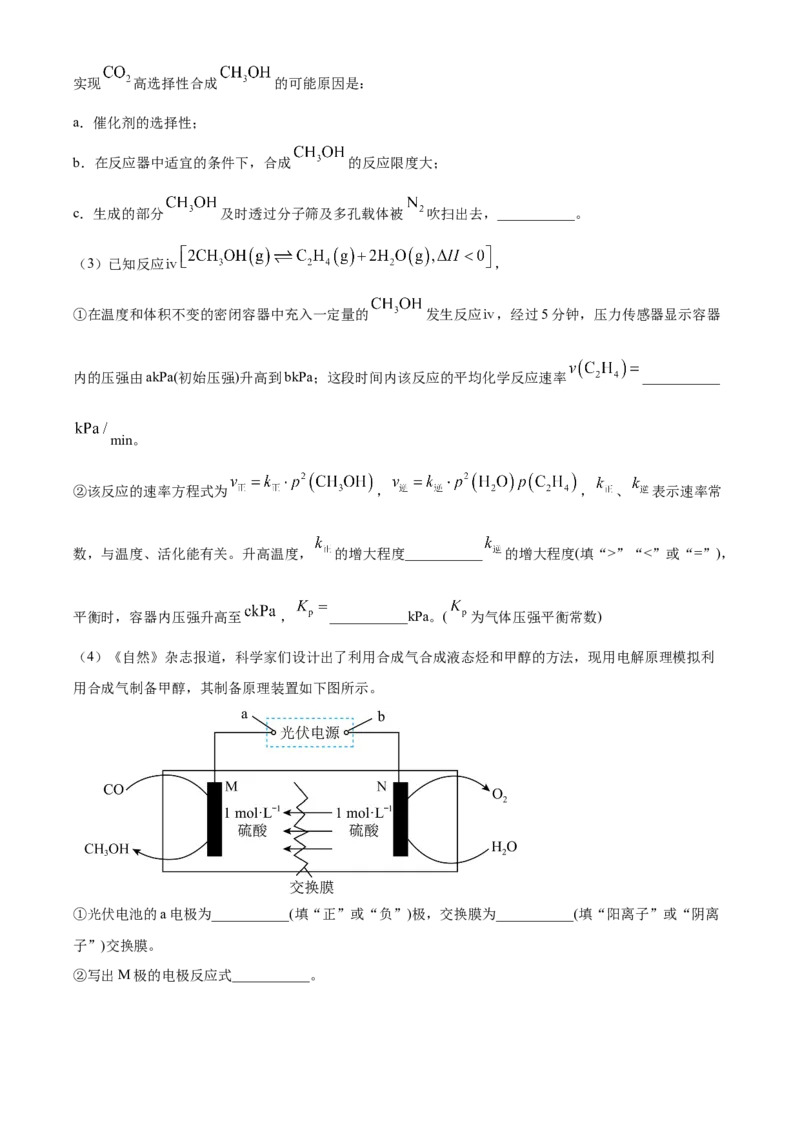
(4)《自然》杂志报道,科学家们设计出了利用合成气合成液态烃和甲醇的方法,现用电解原理模拟利
用合成气制备甲醇,其制备原理装置如下图所示。
①光伏电池的a电极为___________(填“正”或“负”)极,交换膜为___________(填“阳离子”或“阴离
子”)交换膜。
②写出M极的电极反应式___________。③光伏电池工作一段时间,测得N极生成 (标准状况下),M极生成甲醇0.008mol,则M极生成
甲醇的法拉第效率(FE%)=___________。(提示:法拉第效率(FE%)=
×100%)
【答案】(1)-49.5
(2)合成 的反应平衡因体系中 的浓度降低向正反应方向移动,进而提高合成
的选择性
(3) ①. ②. < ③.
(4) ①. 负 ②. 阳离子 ③. ④. 80%
【解析】
【小问1详解】
根据盖斯定律:ⅰ.
ⅱ. ,反应i+反应ii=反应iii,
反应ⅲ. △H=△H+△H=+40.9kJ/mol-90.4
1 2
kJ/mol=-49.5kJ/mol;
【小问2详解】
高选择性合成 的反应中,生成的部分 及时透过分子筛及多孔载体被 吹扫出去,
使 的浓度降低向正反应方向移动,进而提高合成 的选择性;
【小问3详解】
根据三段式:a-2x+x+2x=b,x=b-a, min;
反应 为放热反应,升高温度,平衡逆向移动,升高温度,
的增大程度< 的增大程度;
根据三段式:
a-2y+y+2y=c,y=c-a,p(CHOH)=a-2(c-a)kPa=(3a-2c) kPa,p(C H)=(c-a)kPa,p(H O)= 2(c-a)kPa,K =
3 2 4 2 p
= ;
【小问4详解】
①M极发生CO转化为CHOH,C的化合价降低,发生还原反应,M为阴极,a为负极,N极上HO失去
3 2
电子生成O,发生氧化反应,为阳极,b为正极;交换膜允许H+通过,为阳离子交换膜;
2
②M极上发生CO转化为CHOH的反应,C的化合价降低,发生还原反应,电极反应式为:
3
;