文档内容
西南大学附中 2023-2024 学年度下期期末考试
高二化学试题
(满分:100分;考试时间:75分钟)
一、选择题:本大题共14个小题,每小题3分,共42分。每小题只有一个选项符合题目要求。
1.下列物质属于纯净物的是( )
A.纯碱 B.出炉煤气 C.聚乙烯 D.碱石灰
2.下列说法不正确的是( )
A.乙炔可用于制备导电高分子 B.蚕丝的主要成分为纤维素
C.环状聚烯烃属于有机高分子材料 D.核酸属于生物大分子
3.下列化学用语表示正确的是( )
A.CHCl 的球棍模型: B.N 的电子式:
3 2
C. 的名称:2,3-二乙基丁烷 D.乙醇的分子式:C H O
2 6
4.下列说法正确的是( )
A.利用质谱法可以确定分子中所含的官能团
B.苯酚可与甲醛发生缩聚反应生成酚醛树脂
C.向蛋白质溶液中加入饱和Na SO 溶液可使其变性
2 4
D.银氨溶液的配制:向1mL 2%的氨水中逐滴加入AgNO 溶液至沉淀恰好溶解
3
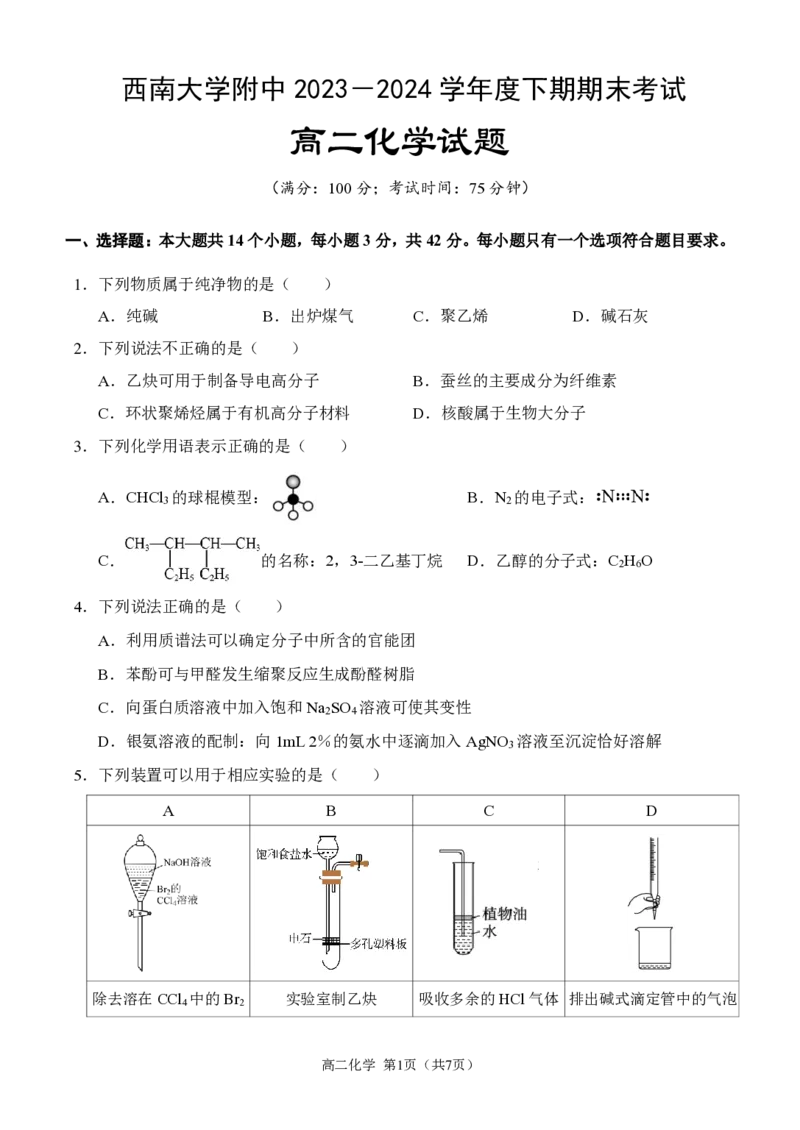
5.下列装置可以用于相应实验的是( )
A B C D
除去溶在CCl 中的Br 实验室制乙炔 吸收多余的HCl气体 排出碱式滴定管中的气泡
4 2
高二化学 第1页(共7页)
{#{QQABDYCAggAgAJBAAAhCQQHKCkMQkAEACYgOgEAIoAAAwANABAA=}#}6.车叶草苷酸是传统药材闭花耳草的活性成分之一,结构简式如图所示。下列关于该物质说
法错误的是( )
A.光照下与氯气反应,可形成C-Cl键
B.该分子中含氧官能团有4种
C.催化剂存在下与足量氢气反应,π键均可断裂
D.在浓硫酸存在条件下加热,可形成π键
7.克拉维酸钾是一种β-内酰胺类抗生素,下列说法错误的是( )
A.克拉维酸钾存在顺反异构
B.克拉维酸分子含有两个手性碳原子
C.上述转化中的二者均能使酸性KMnO 溶液褪色
4
D.在一定条件下,1 mol克拉维酸可加入足量KOH溶液实现上述转化
8.利用如图所示装置可将电解原理广泛应用于工业生产,当X、Y选用不同材料时,下列说
法中正确的是( )
A.氯碱工业中,X、Y均为石墨,X附近能得到氢氧化钠
B.电镀工业中,X是待镀金属,Y是镀层金属
C.铜的精炼中,X是纯铜,Y是粗铜,Z是CuSO
4
D.外加电流保护法中,X是惰性阳极,Y是被保护的金属
9.铅磷青铜具有很高的耐腐蚀+性和耐磨性,常用于制作耐磨零件和滑动轴承。如图为铅磷青
铜的一种晶胞结构,已知A点为坐标原点(0,0,0)。下列说法错误的是( )
A.该晶胞的化学式为PbCu P
3
B.基态磷原子的核外电子共有9种运动状态
C.与P等距且最近的Cu有6个
D.C点原子的分数坐标为( , ,0)
高二化学 第2页(共7页)
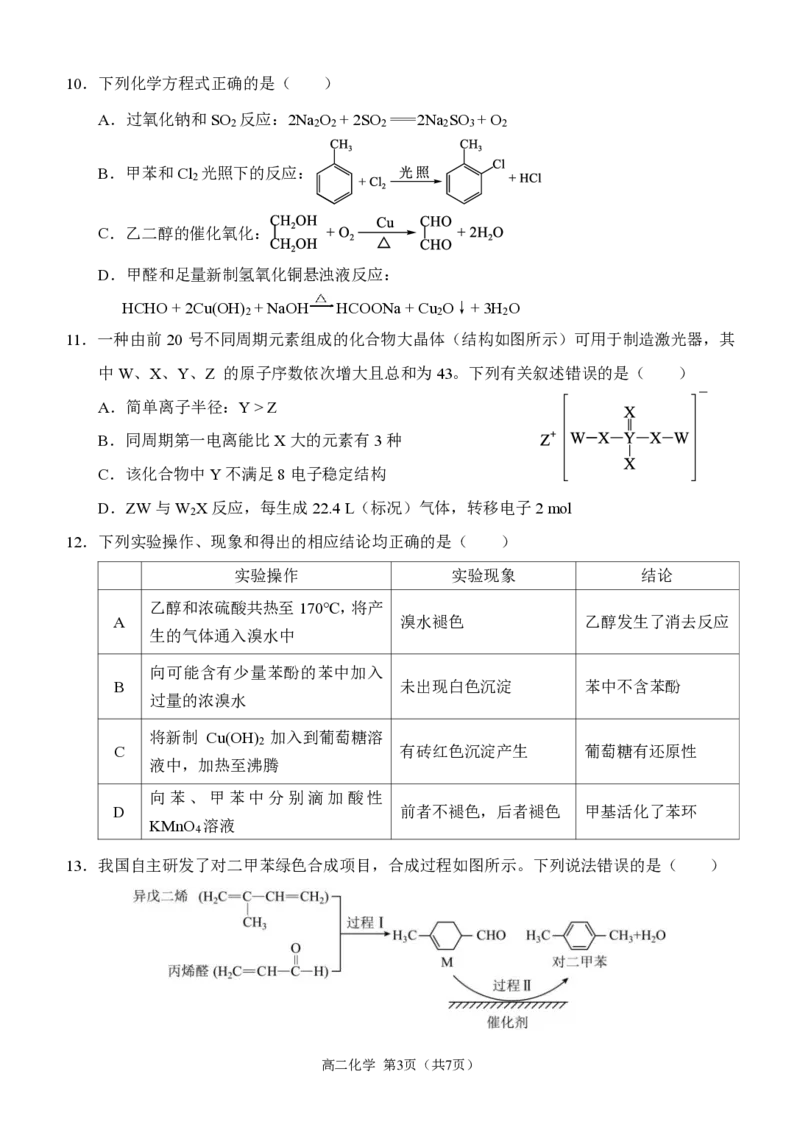
{#{QQABDYCAggAgAJBAAAhCQQHKCkMQkAEACYgOgEAIoAAAwANABAA=}#}10.下列化学方程式正确的是( )
A.过氧化钠和SO 反应:2Na O + 2SO =2Na SO + O
2 2 2 2 2 3 2
B.甲苯和Cl 光照下的反应:
2
C.乙二醇的催化氧化:
D.甲醛和足量新制氢氧化铜悬浊液反应:
HCHO + 2Cu(OH) + NaOH HCOONa + Cu O↓+ 3H O
2 2 2
11.一种由前 20 号不同周期元素组成的化合物大晶体(结构如图所示)可用于制造激光器,其
中W、X、Y、Z 的原子序数依次增大且总和为43。下列有关叙述错误的是( )
A.简单离子半径:Y > Z
B.同周期第一电离能比X大的元素有3种
C.该化合物中Y不满足8电子稳定结构
D.ZW与W X反应,每生成22.4 L(标况)气体,转移电子2 mol
2
12.下列实验操作、现象和得出的相应结论均正确的是( )
实验操作 实验现象 结论
乙醇和浓硫酸共热至170℃,将产
A 溴水褪色 乙醇发生了消去反应
生的气体通入溴水中
向可能含有少量苯酚的苯中加入
B 未出现白色沉淀 苯中不含苯酚
过量的浓溴水
将新制 Cu(OH) 加入到葡萄糖溶
2
C 有砖红色沉淀产生 葡萄糖有还原性
液中,加热至沸腾
向苯、甲苯中分别滴加酸性
D 前者不褪色,后者褪色 甲基活化了苯环
KMnO 溶液
4
13.我国自主研发了对二甲苯绿色合成项目,合成过程如图所示。下列说法错误的是( )
高二化学 第3页(共7页)
{#{QQABDYCAggAgAJBAAAhCQQHKCkMQkAEACYgOgEAIoAAAwANABAA=}#}A.异戊二烯可发生氧化、取代、加聚反应 B.对二甲苯有6种二氯代物
C.该反应的副产物可能有间二甲苯 D.可用溴水鉴别M和对二甲苯
14.向绝热恒容密闭容器中通入一定量SO 与NO 的混合气体,在一定条件下发生反应:SO (g)
2 2 2
+ NO (g) SO (g) + NO(g)其正反应速率 v 随时间 t 变化的曲线如下,不考虑副反应的影
2 3 正
响,下列说法正确的是( )
A.该反应的∆H > 0
B.BC段v 逐渐减小
逆
C.从A点到C点,NO的分压先增大后减小
D.其他条件不变时,若在恒温条件下发生此反应,则
SO 的平衡转化率增大 2
二、非选择题:本大题共4个小题,共58分,考生根据要求作答。
15.(14分) 有机物的种类繁多,请回答下列有关问题:
(1) 请写出下列物质的名称或者结构简式:
①CH CH=C(CH ) :________________;
3 3 2
②HOOCCH CH COOH:________________;
2 2
③聚苯乙烯:________________。
(2) 为检验1-溴丙烷中的溴元素,下列实验操作正确的顺序是_____________(填序号)。
①加入硝酸银溶液 ②加热煮沸 ③加入足量稀硝酸酸化
④取少量1-溴丙烷 ⑤冷却 ⑥加入氢氧化钠溶液
(3) 分子式为 C H 的芳香烃,苯环上的一溴取代物只有一种,写出该芳香烃的结构简式
8 10
______________。
(4) 某含氧有机化合物A的燃烧产物只有CO 和H O,完全燃烧1.08 g该物质,生成1.568
2 2
L CO (标况)。该物质的蒸气密度是相同条件下氢气的54倍。
2
①该有机化合物的分子式为______________;
②实验证实:该有机物与三氯化铁溶液显紫色且核磁共振氢谱上峰面积之比为
3∶2∶2∶1。请写出该有机化合物A的结构简式______________;
③请写出将足量的A加入Na CO 溶液的化学方程式____________________________。
2 3
高二化学 第4页(共7页)
v
正
A
a
B
b c
C
t
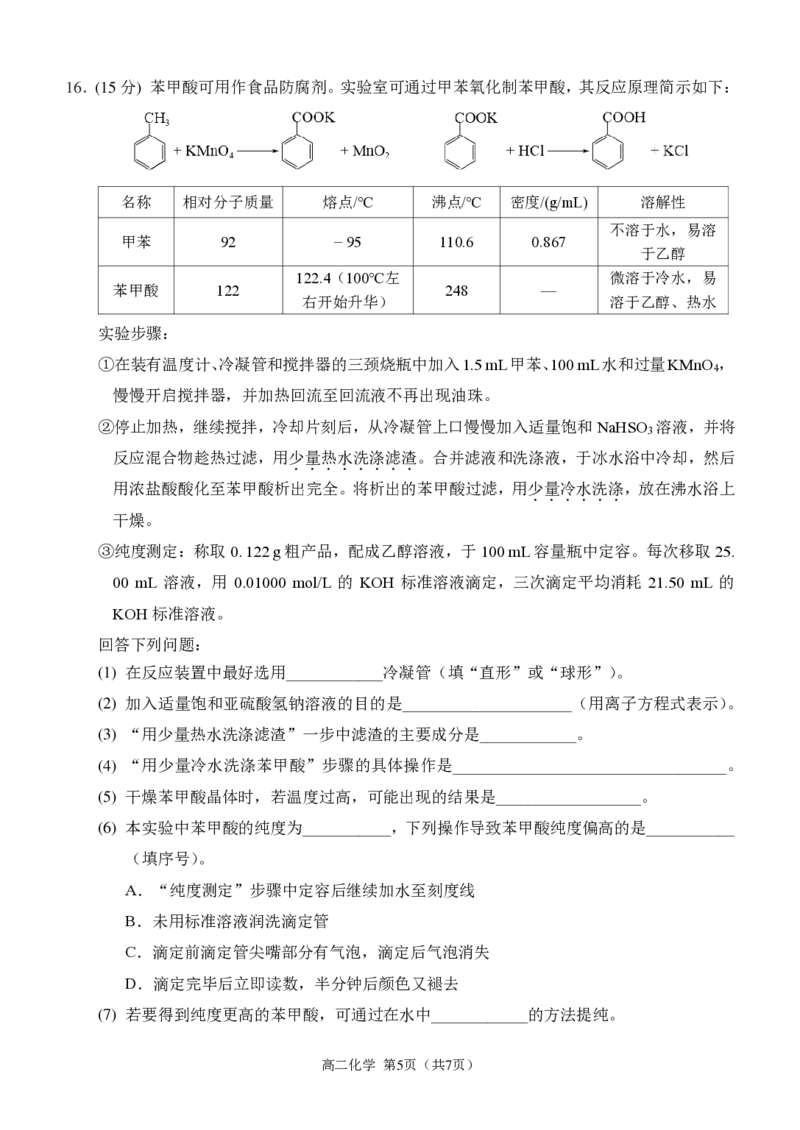
{#{QQABDYCAggAgAJBAAAhCQQHKCkMQkAEACYgOgEAIoAAAwANABAA=}#}16.(15分) 苯甲酸可用作食品防腐剂。实验室可通过甲苯氧化制苯甲酸,其反应原理简示如下:
名称 相对分子质量 熔点/℃ 沸点/℃ 密度/(g/mL) 溶解性
不溶于水,易溶
甲苯 92 − 95 110.6 0.867
于乙醇
122.4(100℃左 微溶于冷水,易
苯甲酸 122 248 —
右开始升华) 溶于乙醇、热水
实验步骤:
①在装有温度计、冷凝管和搅拌器的三颈烧瓶中加入1.5 mL甲苯、100 mL水和过量KMnO ,
4
慢慢开启搅拌器,并加热回流至回流液不再出现油珠。
②停止加热,继续搅拌,冷却片刻后,从冷凝管上口慢慢加入适量饱和NaHSO 溶液,并将
3
反应混合物趁热过滤,用少量热水洗涤滤渣。合并滤液和洗涤液,于冰水浴中冷却,然后
........
用浓盐酸酸化至苯甲酸析出完全。将析出的苯甲酸过滤,用少量冷水洗涤,放在沸水浴上
......
干燥。
③纯度测定:称取0. 122 g粗产品,配成乙醇溶液,于100 mL容量瓶中定容。每次移取25.
00 mL 溶液,用 0.01000 mol/L 的 KOH 标准溶液滴定,三次滴定平均消耗 21.50 mL 的
KOH标准溶液。
回答下列问题:
(1) 在反应装置中最好选用____________冷凝管(填“直形”或“球形”)。
(2) 加入适量饱和亚硫酸氢钠溶液的目的是_____________________(用离子方程式表示)。
(3) “用少量热水洗涤滤渣”一步中滤渣的主要成分是____________。
(4) “用少量冷水洗涤苯甲酸”步骤的具体操作是__________________________________。
(5) 干燥苯甲酸晶体时,若温度过高,可能出现的结果是__________________。
(6) 本实验中苯甲酸的纯度为___________,下列操作导致苯甲酸纯度偏高的是___________
(填序号)。
A.“纯度测定”步骤中定容后继续加水至刻度线
B.未用标准溶液润洗滴定管
C.滴定前滴定管尖嘴部分有气泡,滴定后气泡消失
D.滴定完毕后立即读数,半分钟后颜色又褪去
(7) 若要得到纯度更高的苯甲酸,可通过在水中____________的方法提纯。
高二化学 第5页(共7页)
{#{QQABDYCAggAgAJBAAAhCQQHKCkMQkAEACYgOgEAIoAAAwANABAA=}#}17.(14分) 羰基硫(COS)是一种粮食熏蒸剂,工业上用于合成除草剂、杀草丹等。工业上一
般通过CO 或者CO与H S反应制取COS,发生的相关反应如下:
2 2
反应1:CO(g) + H S(g) COS(g) + H (g) ∆H = – 38 kJ/mol
2 2 1
反应2:CO (g) + H S(g) COS(g) + H O(g) ∆H = +22 kJ/mol
2 2 2 2
(1) 计算反应CO (g) + H (g) CO(g) + H O(g)的∆H = ____________kJ/mol。
2 2 2
(2) 在一定温度下,将2 mol CO与2 mol H S通入恒容密闭容器中发生上述反应1。
2
①能证明上述反应达到平衡的标志是____________(填字母)。
A.混合气体的密度不变
B.CO的体积分数不变
C.2 mol S-H键断裂同时断裂1 mol H-H
D.CO与 H S的物质的量之比不变
2
②上述反应达到平衡后,COS所占的体积分数为25%,则该反应的平衡常数为_________。
若此时再向体系中加入1 mol CO与1 mol H ,平衡将____________(填“向正反应方
2
向”、“向逆反应方向”、“不”)移动;理由是____________________________。
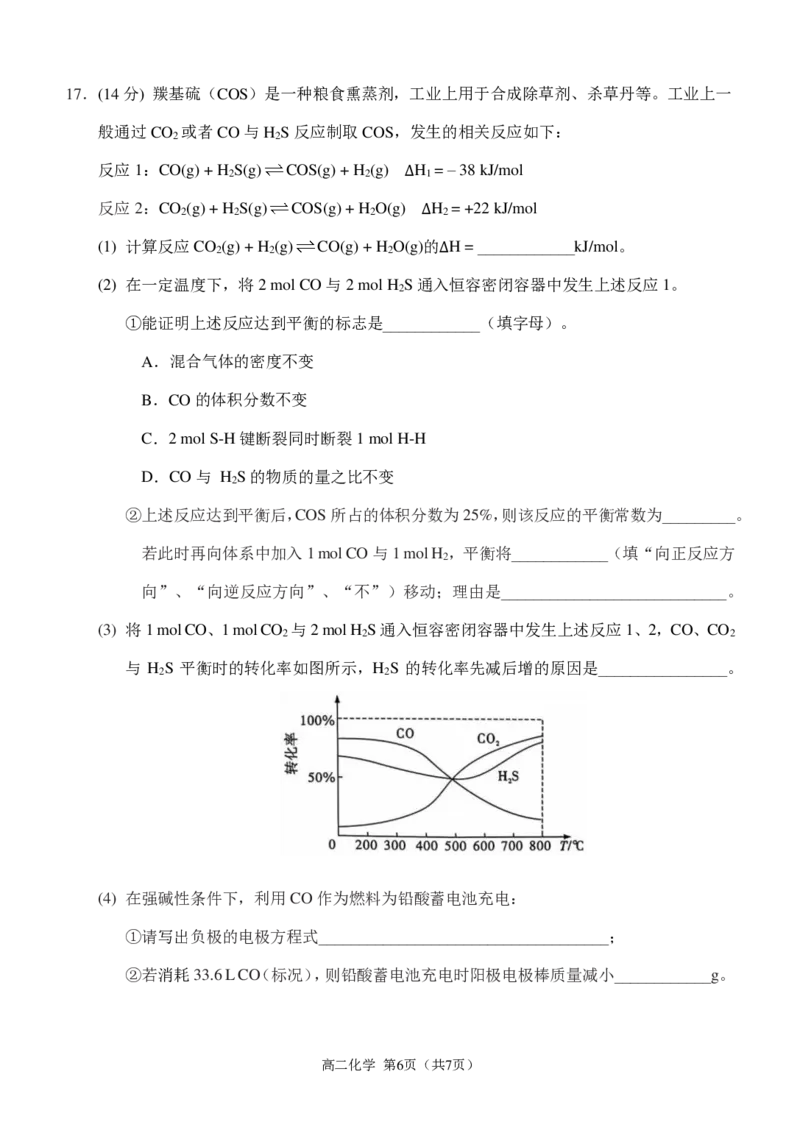
(3) 将1 mol CO、1 mol CO 与2 mol H S通入恒容密闭容器中发生上述反应1、2,CO、CO
2 2 2
与 H S 平衡时的转化率如图所示,H S 的转化率先减后增的原因是________________。
2 2
(4) 在强碱性条件下,利用CO作为燃料为铅酸蓄电池充电:
①请写出负极的电极方程式____________________________________;
②若消耗33.6 L CO(标况),则铅酸蓄电池充电时阳极电极棒质量减小____________g。
高二化学 第6页(共7页)
{#{QQABDYCAggAgAJBAAAhCQQHKCkMQkAEACYgOgEAIoAAAwANABAA=}#}18.(15分) 化合物G是合成某黄酮类抗菌消炎药物的中间体,其合成路线如下:
已知:① ;
② RCl RCN
③ (R 、R 、R 、R 为烃
1 2 3 4
基或H)
回答下列问题:
(1) A的化学名称是____________(系统命名法),C中所含官能团的名称是____________。
(2) 由A生成B的反应类型为____________,F的结构简式为____________。
(3) 由D生成E的化学方程式为____________________________________。
(4) 芳香化合物W是C的同分异构体,能同时发生银镜反应与水解反应的W有_______种。
其中核磁共振氢谱有四组峰,且峰面积之比为 6∶2∶1∶1 的结构简式为____________
(任写一种)。
(5) 设计由甲苯和乙醛制备肉桂醛( )的合成路线(无机试剂任选)
__________________________________________________________________________ 。
高二化学 第7页(共7页)
{#{QQABDYCAggAgAJBAAAhCQQHKCkMQkAEACYgOgEAIoAAAwANABAA=}#}