文档内容
扬州市 2023 年初中毕业、升学统一考试化学试题
说明:
1.本试卷共6页,包含单项选择题(第1题~第20题,共20题)、非选择题(第21题~第
25题,共5题)两部分。本卷满分100分,考试时间为100分钟。考试结束后,请将本试卷
和答题卡一并交回。
2.答题前,考生务必将本人的姓名、准考证号填写在答题卡相应的位置上,同时务必在试卷
的装订线内将本人的姓名、准考证号、毕业学校填写好,在试卷第一面的右下角填写好座位
号。
3.所有的试题都必须在专用的“答题卡”上作答,单项选择题用 2B铅笔作答、非选择题在
指定位置用0.5毫米黑色墨水签字笔作答。如有作图需要,用 2B铅笔作答,并请加黑加粗,
描写清楚。在试卷或草稿纸上答题无效。
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Na-23 S-32 Cl-35.5 Ca-40
一、单项选择题:共20题,每题2分,共40分。每题只有一个选项最符合题意。
1. 下列是我国“国家最高科学技术奖”几位获得者及其部分研究领域,其中研究领域主要涉及具有优良性
能导电材料开发的是
A. 闵恩泽,石油化工催化剂研究 B. 师昌绪,材料腐蚀研究
C. 赵忠贤,高温超导材料研究 D. 张存浩,高能化学激光研究
2. 保存珍贵文物可用空气中含量最多的气体,该气体的化学式为
A. N B. O C. CO D. HO
2 2 2 2
3. 绿色植物通过光合作用将气体X与HO转化为葡萄糖与O,气体X是
2 2
A. N B. Ar C. CO D. SO
2 2 2
4. 用手触摸生活中的碱性溶液时常有滑腻感。下列溶液显碱性的是
A. 食盐水 B. 肥皂水 C. 蔗糖溶液 D. 食醋
5. 重氢可应用于光导纤维制备。重氢和氢都属于氢元素,是因为它们的原子具有相同的
A. 质子数 B. 中子数 C. 体积 D. 相对原子质量
6. 关于某可再生能源的描述如下:该能源储量巨大,但阴雨天等因素会影响其使用。如图为该能源在生活
中的运用。该能源是
第1页/共9页
学科网(北京)股份有限公司A. 地热能 B. 太阳能 C. 水能 D. 化石燃料
的
7. 下列属于分解反应 是
A. B.
C. D.
8. Y是生活中常见的物质,完全燃烧的化学方程式为 。Y的化学式为
A. CHO B. C H C. C H D. C HO
4 2 4 3 8 2 6
9. 化学肥料中通常含有N、P、K等元素。下列属于复合肥料的是
A. KH PO B. KSO C. NH HCO D. CO(NH )
2 4 2 4 4 3 2 2
10. 《天工开物》记载“泥瓦罐载铜十斤,继入炉甘石六斤……,即成黄铜”。炉甘石的主要成分为
ZnCO ,ZnCO 属于
3 3
A. 氧化物 B. 酸 C. 碱 D. 盐
11. 构成物质的微粒有分子、原子、离子等。下列物质由离子构成的是
A. 氧气 B. 水
C. 氯化钠 D. 金刚石
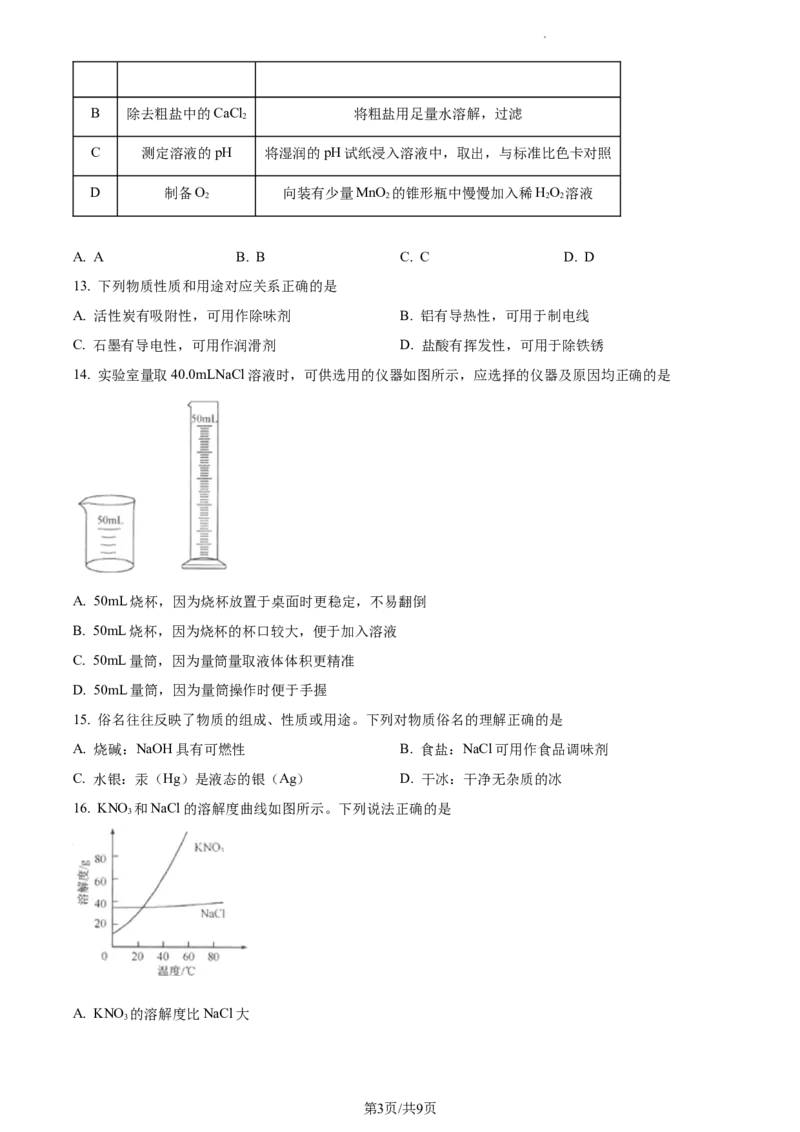
12. 在实验室中进行下列实验,其中实验方案设计正确且能达到实验目的的是
选
实验目的 实验方案
项
A 鉴别CO和O 将两种气体分别通入澄清石灰水
2
第2页/共9页
学科网(北京)股份有限公司B 除去粗盐中的CaCl 将粗盐用足量水溶解,过滤
2
C 测定溶液的pH 将湿润的pH试纸浸入溶液中,取出,与标准比色卡对照
D 制备O 向装有少量MnO 的锥形瓶中慢慢加入稀HO 溶液
2 2 2 2
A. A B. B C. C D. D
13. 下列物质性质和用途对应关系正确的是
A. 活性炭有吸附性,可用作除味剂 B. 铝有导热性,可用于制电线
C. 石墨有导电性,可用作润滑剂 D. 盐酸有挥发性,可用于除铁锈
14. 实验室量取40.0mLNaCl溶液时,可供选用的仪器如图所示,应选择的仪器及原因均正确的是
A. 50mL烧杯,因为烧杯放置于桌面时更稳定,不易翻倒
B. 50mL烧杯,因为烧杯的杯口较大,便于加入溶液
C. 50mL量筒,因为量筒量取液体体积更精准
D. 50mL量筒,因为量筒操作时便于手握
15. 俗名往往反映了物质的组成、性质或用途。下列对物质俗名的理解正确的是
A. 烧碱:NaOH具有可燃性 B. 食盐:NaCl可用作食品调味剂
C. 水银:汞(Hg)是液态的银(Ag) D. 干冰:干净无杂质的冰
16. KNO 和NaCl的溶解度曲线如图所示。下列说法正确的是
3
A. KNO 的溶解度比NaCl大
3
第3页/共9页
学科网(北京)股份有限公司B. 将室温下KNO 的饱和溶液升高温度,溶液仍饱和
3
C. KNO 和NaCl均属于难溶物质
3
D. 除去KNO 中少量NaCl可用冷却热饱和溶液结晶的方法
3
17. 下列对实验现象的解释不正确的是
选
实验现象 解释
项
A 将50mL水和50mL酒精混合,总体积小于100mL 分子之间有空隙
B 向锌粒中加入稀硫酸,产生气泡 金属均能与酸反应产生H
2
C 将黄铜片和铜片相互刻画,铜片表面有明显划痕 合金的硬度往往比其成分金属大
D 铁丝在空气中不能燃烧,在氧气中可以燃烧 氧气的浓度对物质的燃烧有影响
A. A B. B C. C D. D
18. Ca(OH) 与HO 溶液反应可制备CaO 。反应过程包括:
2 2 2 2
步骤—: ,其中O代表氧原子;
步骤二:主要发生 ,少量发生 。
下列说法不正确的是
A. 为增大反应混合物中Ca(OH) 的含量,应使用石灰乳而非石灰水
2
B. 生成CaO 的总反应为
2
C. 增加Ca(OH) 的用量,可以消耗更多O,减少O 的生成
2 2
D. 制备时反应每生成72gCaO,同时生成32gO
2 2
阅读下列材料,完成下面小题。
有机物DMF是一种水污染物,在疏松多孔Al O 的催化下,O 先将其转化为小分子化合物,最终降解为
2 3 3
CO 而去除。制备O 时,将O 通过臭氧发生器,O 部分转化为O,得到O 与O 的混合气体。为研究
2 3 2 2 3 3 2
Al O 和O 对DMF的去除效果,取四份DMF溶液,控制其他条件相同,分别进行四个实验:①向溶液中
2 3 3
通入O 与O 的混合气体并加入Al O;②向溶液中通入O 与O 的混合气体;③向溶液中加入Al O;④向
3 2 2 3 3 2 2 3
溶液中通入O 并加入Al O。
2 2 3
19. O 通过臭氧发生器转化为O,反应前后发生变化的是
2 3
A. 原子总数 B. 分子种类
C. 元素种类 D. 物质的总质量
第4页/共9页
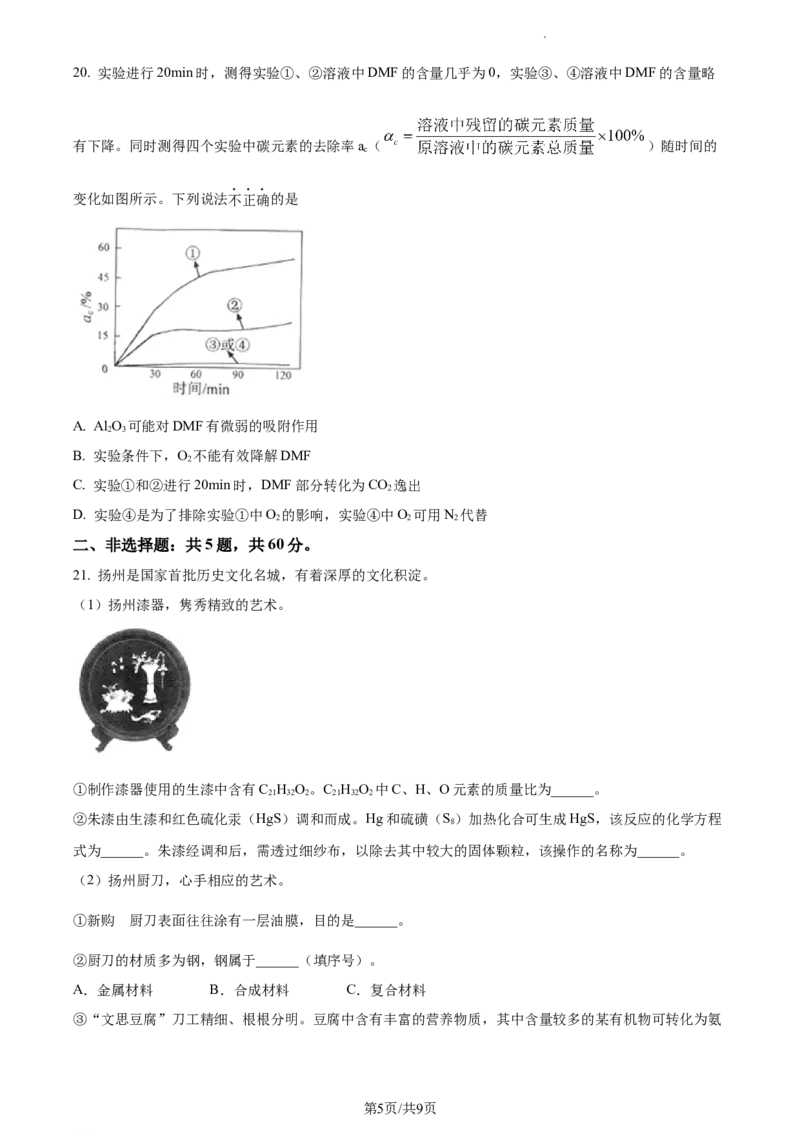
学科网(北京)股份有限公司20. 实验进行20min时,测得实验①、②溶液中DMF的含量几乎为0,实验③、④溶液中DMF的含量略
有下降。同时测得四个实验中碳元素的去除率a( )随时间的
c
变化如图所示。下列说法不正确的是
A. Al O 可能对DMF有微弱的吸附作用
2 3
B. 实验条件下,O 不能有效降解DMF
2
C. 实验①和②进行20min时,DMF部分转化为CO 逸出
2
D. 实验④是为了排除实验①中O 的影响,实验④中O 可用N 代替
2 2 2
二、非选择题:共5题,共60分。
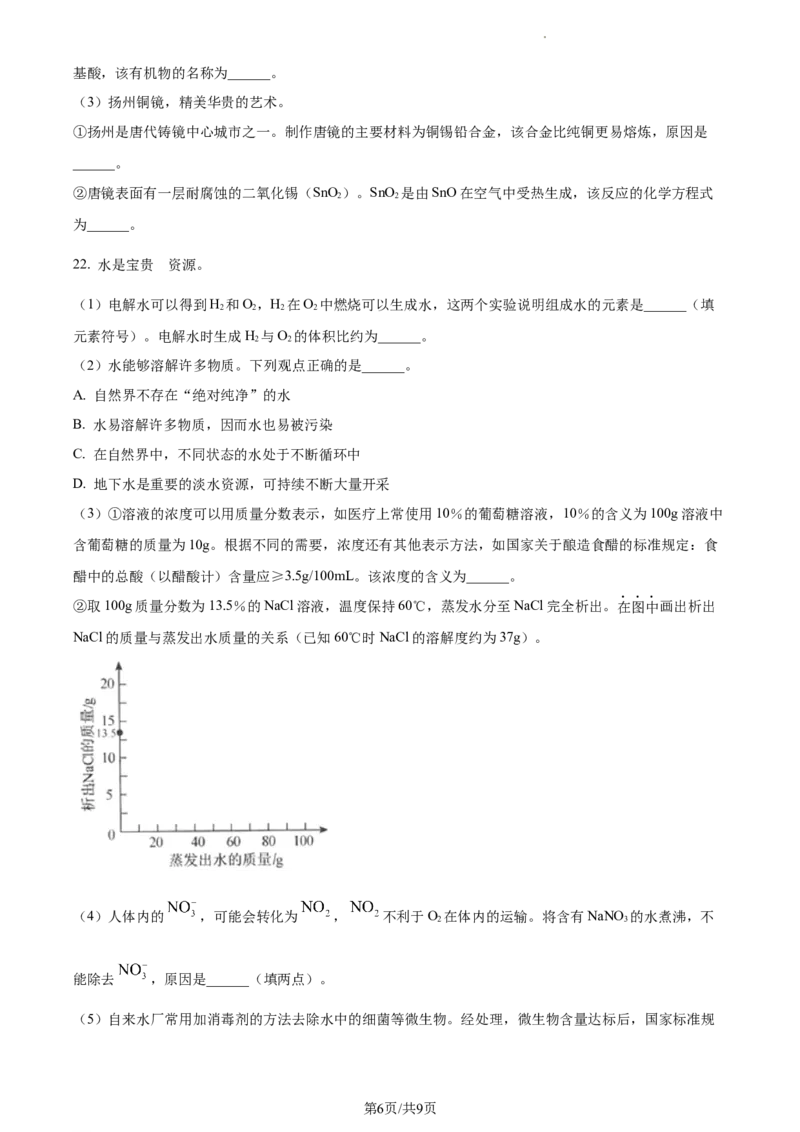
21. 扬州是国家首批历史文化名城,有着深厚的文化积淀。
(1)扬州漆器,隽秀精致的艺术。
①制作漆器使用的生漆中含有C H O。C H O 中C、H、O元素的质量比为______。
21 32 2 21 32 2
②朱漆由生漆和红色硫化汞(HgS)调和而成。Hg和硫磺(S)加热化合可生成HgS,该反应的化学方程
8
式为______。朱漆经调和后,需透过细纱布,以除去其中较大的固体颗粒,该操作的名称为______。
(2)扬州厨刀,心手相应的艺术。
的
①新购 厨刀表面往往涂有一层油膜,目的是______。
②厨刀的材质多为钢,钢属于______(填序号)。
A.金属材料 B.合成材料 C.复合材料
③“文思豆腐”刀工精细、根根分明。豆腐中含有丰富的营养物质,其中含量较多的某有机物可转化为氨
第5页/共9页
学科网(北京)股份有限公司基酸,该有机物的名称为______。
(3)扬州铜镜,精美华贵的艺术。
①扬州是唐代铸镜中心城市之一。制作唐镜的主要材料为铜锡铅合金,该合金比纯铜更易熔炼,原因是
______。
②唐镜表面有一层耐腐蚀的二氧化锡(SnO )。SnO 是由SnO在空气中受热生成,该反应的化学方程式
2 2
为______。
的
22. 水是宝贵 资源。
(1)电解水可以得到H 和O,H 在O 中燃烧可以生成水,这两个实验说明组成水的元素是______(填
2 2 2 2
元素符号)。电解水时生成H 与O 的体积比约为______。
2 2
(2)水能够溶解许多物质。下列观点正确的是______。
A. 自然界不存在“绝对纯净”的水
B. 水易溶解许多物质,因而水也易被污染
C. 在自然界中,不同状态的水处于不断循环中
D. 地下水是重要的淡水资源,可持续不断大量开采
(3)①溶液的浓度可以用质量分数表示,如医疗上常使用10%的葡萄糖溶液,10%的含义为100g溶液中
含葡萄糖的质量为10g。根据不同的需要,浓度还有其他表示方法,如国家关于酿造食醋的标准规定:食
醋中的总酸(以醋酸计)含量应≥3.5g/100mL。该浓度的含义为______。
②取100g质量分数为13.5%的NaCl溶液,温度保持60℃,蒸发水分至NaCl完全析出。在图中画出析出
NaCl的质量与蒸发出水质量的关系(已知60℃时NaCl的溶解度约为37g)。
(4)人体内的 ,可能会转化为 , 不利于O 在体内的运输。将含有NaNO 的水煮沸,不
2 3
能除去 ,原因是______(填两点)。
(5)自来水厂常用加消毒剂的方法去除水中的细菌等微生物。经处理,微生物含量达标后,国家标准规
第6页/共9页
学科网(北京)股份有限公司定自来水出厂时仍需留有一定浓度的消毒剂,原因是______。
(6)联合国将每年的3月22日定为“世界水日”。2023年的主题是“加速变革”,呼吁加快落实保护并
合理利用水资源的措施,以应对全球淡水资源匮乏的挑战。请写出家庭中可采取的一个节水措施:______。
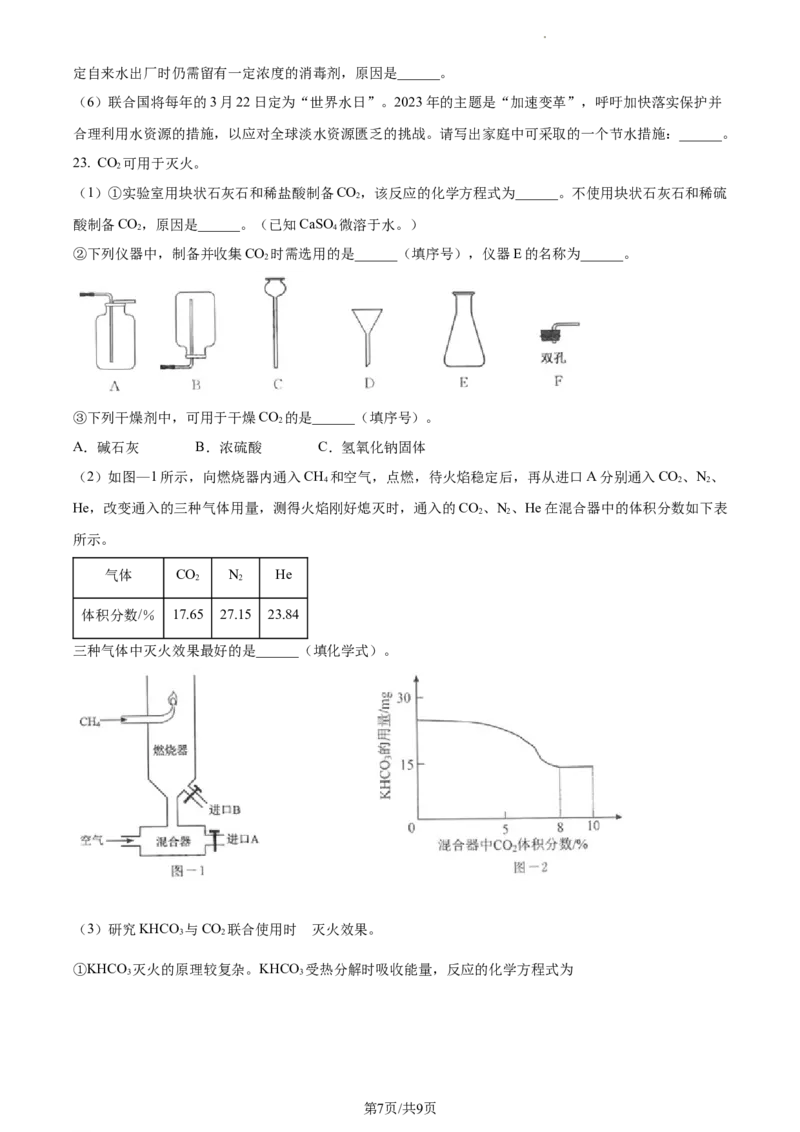
23. CO 可用于灭火。
2
(1)①实验室用块状石灰石和稀盐酸制备CO,该反应的化学方程式为______。不使用块状石灰石和稀硫
2
酸制备CO,原因是______。(已知CaSO 微溶于水。)
2 4
②下列仪器中,制备并收集CO 时需选用的是______(填序号),仪器E的名称为______。
2
③下列干燥剂中,可用于干燥CO 的是______(填序号)。
2
A.碱石灰 B.浓硫酸 C.氢氧化钠固体
(2)如图—1所示,向燃烧器内通入CH 和空气,点燃,待火焰稳定后,再从进口A分别通入CO、N、
4 2 2
He,改变通入的三种气体用量,测得火焰刚好熄灭时,通入的CO、N、He在混合器中的体积分数如下表
2 2
所示。
气体 CO N He
2 2
体积分数/% 17.65 27.15 23.84
三种气体中灭火效果最好的是______(填化学式)。
的
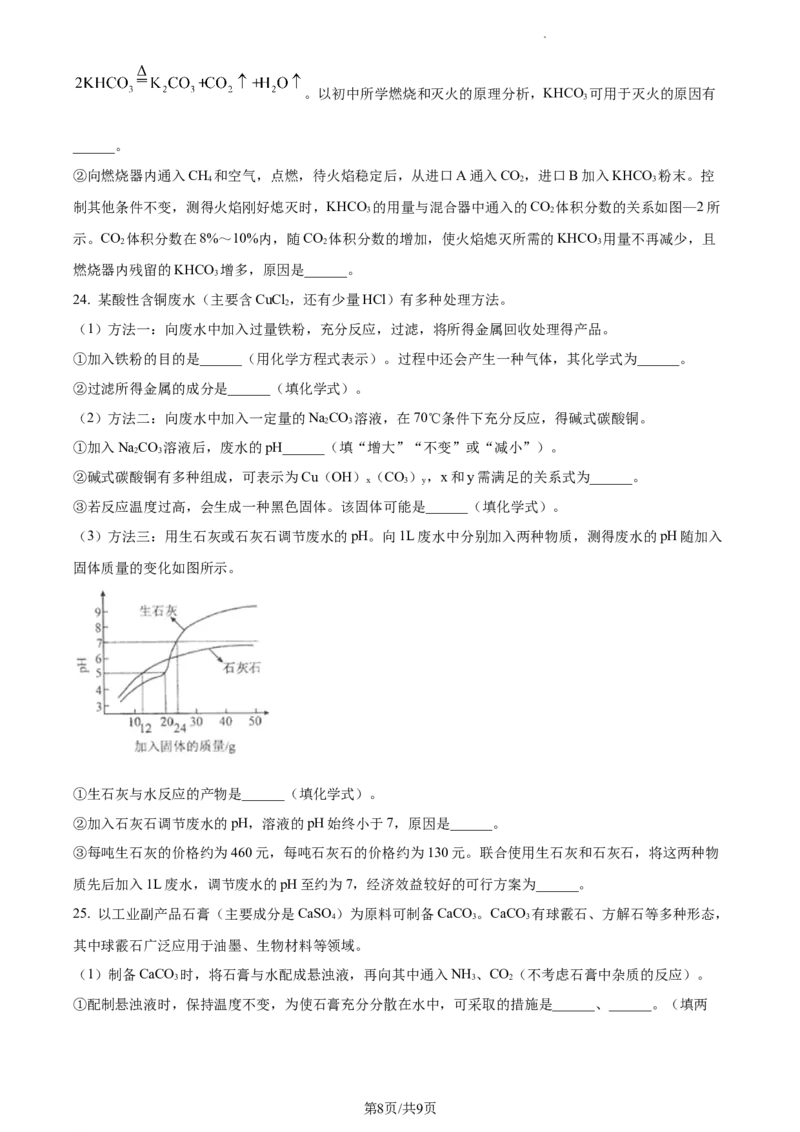
(3)研究KHCO 与CO 联合使用时 灭火效果。
3 2
①KHCO 灭火的原理较复杂。KHCO 受热分解时吸收能量,反应的化学方程式为
3 3
第7页/共9页
学科网(北京)股份有限公司。以初中所学燃烧和灭火的原理分析,KHCO 可用于灭火的原因有
3
______。
②向燃烧器内通入CH 和空气,点燃,待火焰稳定后,从进口A通入CO,进口B加入KHCO 粉末。控
4 2 3
制其他条件不变,测得火焰刚好熄灭时,KHCO 的用量与混合器中通入的CO 体积分数的关系如图—2所
3 2
示。CO 体积分数在8%~10%内,随CO 体积分数的增加,使火焰熄灭所需的KHCO 用量不再减少,且
2 2 3
燃烧器内残留的KHCO 增多,原因是______。
3
24. 某酸性含铜废水(主要含CuCl ,还有少量HCl)有多种处理方法。
2
(1)方法一:向废水中加入过量铁粉,充分反应,过滤,将所得金属回收处理得产品。
①加入铁粉的目的是______(用化学方程式表示)。过程中还会产生一种气体,其化学式为______。
②过滤所得金属的成分是______(填化学式)。
(2)方法二:向废水中加入一定量的NaCO 溶液,在70℃条件下充分反应,得碱式碳酸铜。
2 3
①加入NaCO 溶液后,废水的pH______(填“增大”“不变”或“减小”)。
2 3
②碱式碳酸铜有多种组成,可表示为Cu(OH)(CO),x和y需满足的关系式为______。
x 3 y
③若反应温度过高,会生成一种黑色固体。该固体可能是______(填化学式)。
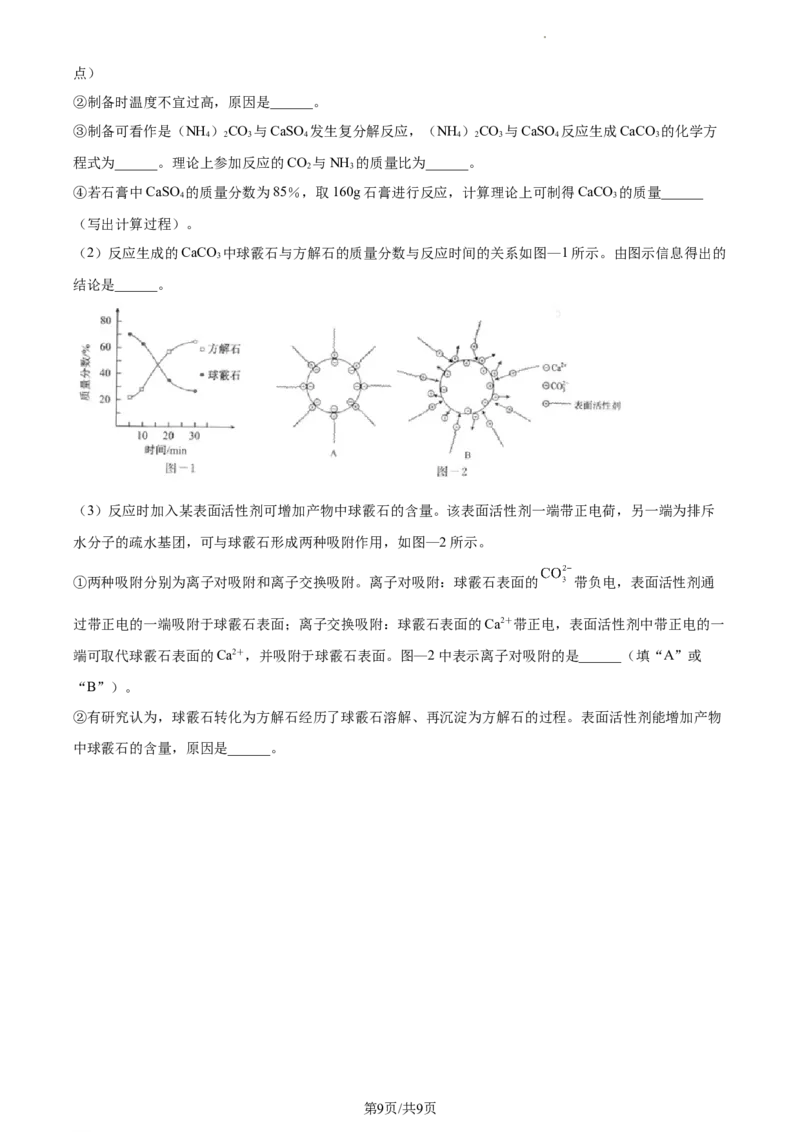
(3)方法三:用生石灰或石灰石调节废水的pH。向1L废水中分别加入两种物质,测得废水的pH随加入
固体质量的变化如图所示。
①生石灰与水反应的产物是______(填化学式)。
②加入石灰石调节废水的pH,溶液的pH始终小于7,原因是______。
③每吨生石灰的价格约为460元,每吨石灰石的价格约为130元。联合使用生石灰和石灰石,将这两种物
质先后加入1L废水,调节废水的pH至约为7,经济效益较好的可行方案为______。
25. 以工业副产品石膏(主要成分是CaSO)为原料可制备CaCO 。CaCO 有球霰石、方解石等多种形态,
4 3 3
其中球霰石广泛应用于油墨、生物材料等领域。
(1)制备CaCO 时,将石膏与水配成悬浊液,再向其中通入NH 、CO(不考虑石膏中杂质的反应)。
3 3 2
①配制悬浊液时,保持温度不变,为使石膏充分分散在水中,可采取的措施是______、______。(填两
第8页/共9页
学科网(北京)股份有限公司点)
②制备时温度不宜过高,原因是______。
③制备可看作是(NH )CO 与CaSO 发生复分解反应,(NH )CO 与CaSO 反应生成CaCO 的化学方
4 2 3 4 4 2 3 4 3
程式为______。理论上参加反应的CO 与NH 的质量比为______。
2 3
④若石膏中CaSO 的质量分数为85%,取160g石膏进行反应,计算理论上可制得CaCO 的质量______
4 3
(写出计算过程)。
(2)反应生成的CaCO 中球霰石与方解石的质量分数与反应时间的关系如图—1所示。由图示信息得出的
3
结论是______。
(3)反应时加入某表面活性剂可增加产物中球霰石的含量。该表面活性剂一端带正电荷,另一端为排斥
水分子的疏水基团,可与球霰石形成两种吸附作用,如图—2所示。
①两种吸附分别为离子对吸附和离子交换吸附。离子对吸附:球霰石表面的 带负电,表面活性剂通
过带正电的一端吸附于球霰石表面;离子交换吸附:球霰石表面的Ca2+带正电,表面活性剂中带正电的一
端可取代球霰石表面的Ca2+,并吸附于球霰石表面。图—2中表示离子对吸附的是______(填“A”或
“B”)。
②有研究认为,球霰石转化为方解石经历了球霰石溶解、再沉淀为方解石的过程。表面活性剂能增加产物
中球霰石的含量,原因是______。
第9页/共9页
学科网(北京)股份有限公司