文档内容
2010年全国统一高考化学试卷(全国卷Ⅱ)
一、选择题
1.(3分)下列反应中,可用离子方程式H++OH﹣=H 2 O表示的是( ) A. B.
A.NH Cl+NaOH NaCl+NH ↑+H O
4 3 2
B.Mg(OH) +2HCl=MgCl +2H O
2 2 2
C.NaOH+NaHCO =Na CO +H O
3 2 3 2
D.NaOH+HNO =NaNO +H O C. D.
3 3 2
2.(3分)下面均是正丁烷与氧气反应的热化学方程式(25°,101kPa):
5.(3分)若(NH ) SO 在强热时分解的产物是SO 、N 、NH 和H O,则该反应中化合价发生
4 2 4 2 2 3 2
①C H (g)+ O (g)=4CO (g)+5H O(l)△H=﹣2878kJ/mol 变化和未发生变化的N原子数之比为( )
4 10 2 2 2
A.1:4 B.1:2 C.2:1 D.4:1
②C H (g)+ O (g)=4CO (g)+5H O(g)△H=﹣2658kJ/mol
4 10 2 2 2 6.(3分)在一定温度、压强下,向100mLCH 和Ar的混合气体中通入400mLO ,点燃使其完
4 2
全燃烧,最后在相同条件下得到干燥气体 460mL,则反应前混合气体中CH 和Ar物质的量之
③C H (g)+ O (g)=4CO(g)+5H O(l)△H=﹣1746kJ/mol 4
4 10 2 2
比是( )
④C 4 H 10 (g)+ O 2 (g)=4CO(g)+5H 2 O(g)△H=﹣1526kJ/mol A.1:4 B.1:3 C.1:2 D.1:1
7.(3分)短周期元素W、X、Y、Z的原子序数依次增大,且 W、X、Y+、Z的最外层电子数与
由此判断,正丁烷的燃烧热是( )
其电子层数的比值依次为2、3、4、2(不考虑零族元素).下列关于这些元素的叙述错误的是
A.﹣2878kJ/mol B.﹣2658kJ/mol C.﹣1746kJ/mol D.﹣1526kJ/mol
( )
3.(3分)在相同条件下,下列说法错误的是( )
A.X和其他三种元素均可形成至少2种二元化合物
A.氯气在饱和食盐水中的溶解度小于在纯水中的溶解度
B.W和X、Z两种元素分别形成的二元化合物中,均有直线形分子
B.碘在碘化钾溶液中的溶解度大于在纯水中的溶解度
C.W、X和Y三种元素可以形成碱性化合物
C.醋酸在醋酸钠溶液中电离的程度大于在纯水中电离的程度
D.Z和其他三种元素形成的二元化合物,其水溶液均呈酸性
D.工业上生产硫酸的过程中使用过量的空气可提高SO 的利用率
2
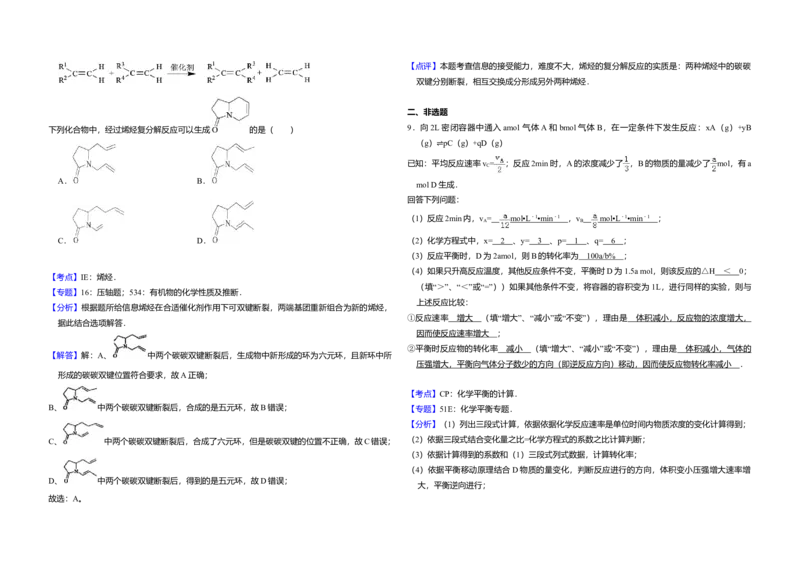
8.(3分)三位科学家因在烯烃复分解反应研究中的杰出贡献而荣获2005年度诺贝尔化学奖,烯
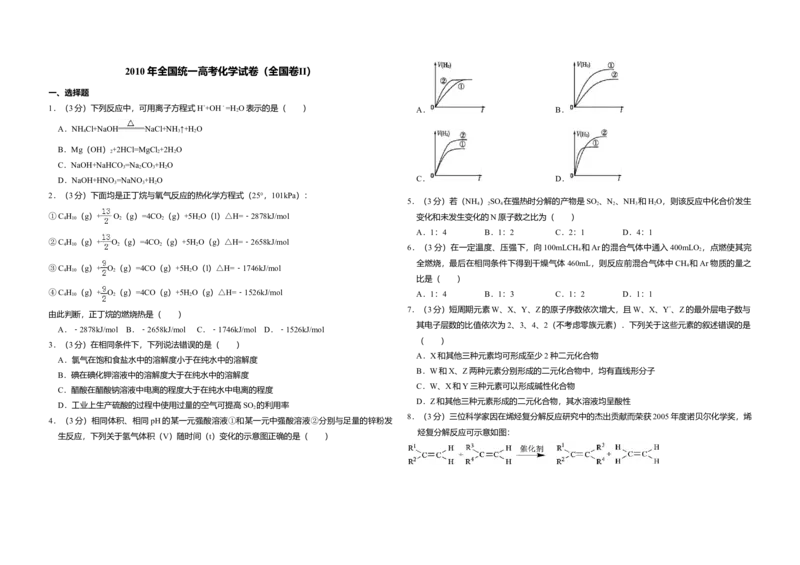
4.(3分)相同体积、相同pH的某一元强酸溶液①和某一元中强酸溶液②分别与足量的锌粉发
烃复分解反应可示意如图:
生反应,下列关于氢气体积(V)随时间(t)变化的示意图正确的是( )能使湿润的石蕊试纸变色;
②A和I相遇产生白色烟雾;
下列化合物中,经过烯烃复分解反应可以生成 的是( ) ③B和E都能使品红溶液褪色;
④将红热的铜丝放入装有B的瓶中,瓶内充满棕黄色的烟;
⑤将点燃的镁条放入装有F的瓶中,镁条剧烈燃烧,生成白色粉末,瓶内壁附着黑色颗粒;
A. B.
⑥C和D相遇生成红棕色气体;
⑦G在D中燃烧可以产生E和H O;
2
⑧将B和H 在瓶中混合后于亮处放置几分钟,瓶内壁出现油状液滴并产生A.
回答下列问题:
C. D. (1)A的化学式是 ,②中烟雾的化学式是 ;
(2)④中发生反应的化学方程式是 ;
(3)⑤中发生反应的化学方程式是 ;
二、非选题
(4)C的化学式是 ,D的化学式是 ;
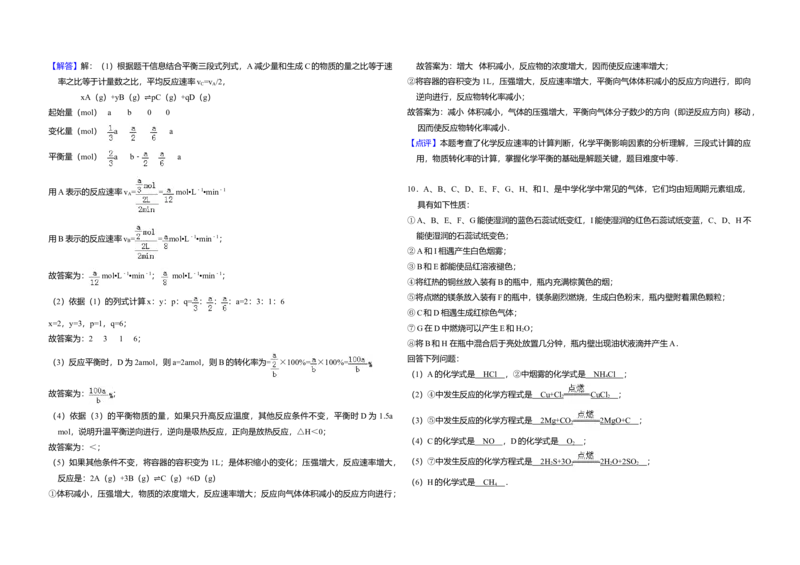
9.向 2L 密闭容器中通入 amol 气体 A 和 bmol 气体 B,在一定条件下发生反应:xA(g)+yB
(5)⑦中发生反应的化学方程式是 ;
(g) pC(g)+qD(g)
(6)H的化学式是 .
⇌
已知:平均反应速率v = ;反应2min 时,A的浓度减少了 ,B的物质的量减少了 mol,有a
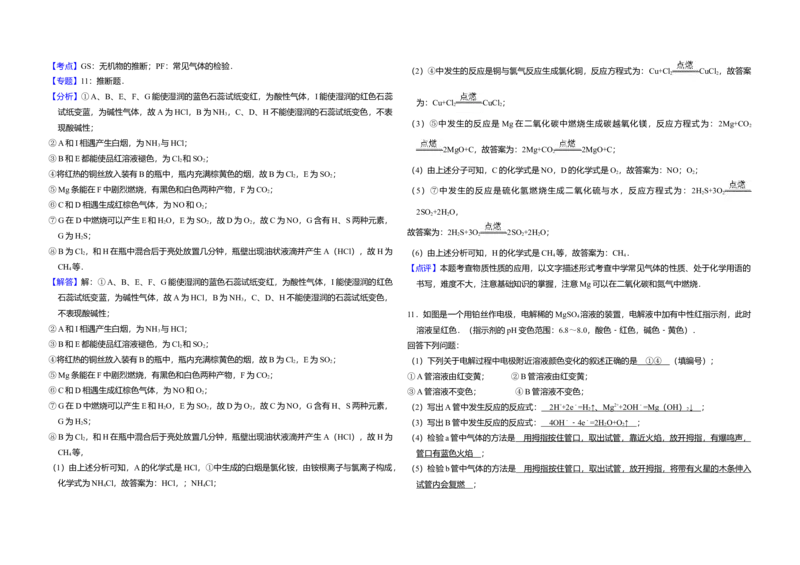
C 11.如图是一个用铂丝作电极,电解稀的MgSO 溶液的装置,电解液中加有中性红指示剂,此时
4
溶液呈红色.(指示剂的pH变色范围:6.8~8.0,酸色﹣红色,碱色﹣黄色).
mol D生成.
回答下列问题:
回答下列问题:
(1)下列关于电解过程中电极附近溶液颜色变化的叙述正确的是 (填编号);
(1)反应2min内,v = ,v ;
A B
(2)化学方程式中,x= 、y= 、p= 、q= ;
①A管溶液由红变黄; ②B管溶液由红变黄;
(3)反应平衡时,D为 2amol,则B的转化率为 ;
③A管溶液不变色; ④B管溶液不变色;
(4)如果只升高反应温度,其他反应条件不变,平衡时 D为 1.5a mol,则该反应的△H 0; (2)写出A管中发生反应的反应式: ;
(填“>”、“<”或“=”))如果其他条件不变,将容器的容积变为 1L,进行同样的实验,则与 (3)写出B管中发生反应的反应式: ;
(4)检验a管中气体的方法是 ;
上述反应比较:
(5)检验b管中气体的方法是 ;
①反应速率 (填“增大”、“减小”或“不变”),理由是 ;
(6)电解一段时间后,切断电源,将电解液倒入烧杯内观察到的现象是 .
②平衡时反应物的转化率 (填“增大”、“减小”或“不变”),理由是 .
10.A、B、C、D、E、F、G、H、和I、是中学化学中常见的气体,它们均由短周期元素组成,
具有如下性质:
①A、B、E、F、G能使湿润的蓝色石蕊试纸变红,I能使湿润的红色石蕊试纸变蓝,C、D、H不12.如图中A~J均为有机化合物,根据图1中的信息,回答下列问题:
(1)环状化合物A的相对分子质量为82,其中含碳87.80%,含氢12.20%.B的一氯代物仅有一
种,B的结构简式为 ;
(2)M是B的一种同分异构体,M能使溴的四氯化碳溶液褪色,分子中所有的碳原子共平面,
则M的结构简式为 ;
(3)由A生成D的反应类型是 ,由D生成E的反应类型是 ;
(4)G的分子式为C H O ,0.146gG需用20mL0.100mol/L NaOH溶液完全中和,J是一种高分子
6 10 4
化合物.则由G转化为J的化学方程式为 ;
(5)分子中含有两个碳碳双键,且两个双键之间有一个碳碳单键的烯烃与单烯烃可发生如图2反
应则由E和A反应生成F的化学方程式为 ;
(6)H中含有的官能团是 ,I中含有的官能团是 .②C H (g)+ O (g)=4CO (g)+5H O(g)△H=﹣2658kJ/mol
4 10 2 2 2
2010 年全国统一高考化学试卷(全国卷Ⅱ)
③C H (g)+ O (g)=4CO(g)+5H O(l)△H=﹣1746kJ/mol
4 10 2 2
参考答案与试题解析
④C H (g)+ O (g)=4CO(g)+5H O(g)△H=﹣1526kJ/mol
4 10 2 2
一、选择题
由此判断,正丁烷的燃烧热是( )
1.(3分)下列反应中,可用离子方程式H++OH﹣=H O表示的是( )
2
A.﹣2878kJ/mol B.﹣2658kJ/mol C.﹣1746kJ/mol D.﹣1526kJ/mol
A.NH Cl+NaOH NaCl+NH ↑+H O
4 3 2
【考点】BC:燃烧热.
B.Mg(OH) +2HCl=MgCl +2H O 菁优网版权所有
2 2 2
【专题】517:化学反应中的能量变化.
C.NaOH+NaHCO =Na CO +H O
3 2 3 2
【分析】根据燃烧热指1mol 可燃物完全燃烧生成稳定的化合物时所放出的热量,如:C→CO
D.NaOH+HNO =NaNO +H O 2
3 3 2
(气),H→H O(液),S→SO (气)等.
2 2
【解答】解:正丁烷的燃烧热是指1mol正丁烷完全燃烧生成气态CO ,液态H O放出的热量,所
【考点】49:离子方程式的书写. 2 2
菁优网版权所有
【专题】516:离子反应专题.
以表示燃烧热的热化学方程式为:C H (g)+ O (g)═4CO (g)+5H O(l)△H=﹣
4 10 2 2 2
【分析】稀的强酸与稀的强碱反应生成可溶性盐和水的离子反应可用 H++OH﹣=H O表示,以此来
2
2878kJ/mol,正丁烷的燃烧热为﹣2878 kJ/mol。故选:A。
解答.
【点评】考查学生对燃烧热理解以及对热化学方程式的理解,难度不大,注意燃烧热概念中的注
【解答】解:A.该反应为固体与固体加热条件下的反应,不属于离子反应,故A不选;
B.Mg(OH) 为不溶性弱碱,不能用H++OH﹣=H O表示,故B不选; 意点.
2 2
C.NaOH+NaHCO =Na CO +H O的离子反应为OH﹣+HCO ﹣=CO 2﹣+H O,故C不选;
3 2 3 2 3 3 2
D.NaOH+HNO =NaNO +H O为稀的强酸与稀的强碱反应生成可溶性盐和水的离子反应,可用 H+ 3.(3分)在相同条件下,下列说法错误的是( )
3 3 2
A.氯气在饱和食盐水中的溶解度小于在纯水中的溶解度
+OH﹣=H O表示,故选D;
2
B.碘在碘化钾溶液中的溶解度大于在纯水中的溶解度
故选:D。
C.醋酸在醋酸钠溶液中电离的程度大于在纯水中电离的程度
【点评】本题考查离子反应方程式的书写,明确发生的化学反应是解答本题的关键,注意电解质
D.工业上生产硫酸的过程中使用过量的空气可提高SO 的利用率
的强弱及离子反应中应保留化学式的物质即可解答,题目难度不大. 2
【考点】CB:化学平衡的影响因素;D5:弱电解质在水溶液中的电离平衡;DH:难溶电解质的
2.(3分)下面均是正丁烷与氧气反应的热化学方程式(25°,101kPa):
溶解平衡及沉淀转化的本质.
①C H (g)+ O (g)=4CO (g)+5H O(l)△H=﹣2878kJ/mol 菁优网版权所有
4 10 2 2 2
【专题】51E:化学平衡专题.
【分析】A、氯气溶于水存在平衡Cl +H O H++Cl﹣+HClO,氯离子浓度增大,平衡向左移动,抑
2 2
⇌制氯气的溶解; 【考点】D5:弱电解质在水溶液中的电离平衡.
菁优网版权所有
B、碘在碘化钾溶液中的存在平衡I +I﹣ I ﹣,碘离子浓度增大,平衡向右移动; 【专题】51G:电离平衡与溶液的pH专题.
2 3
C、醋酸存在电离平衡HAc H++Ac﹣,Ac﹣浓度增大抑制醋酸的电离; 【分析】相同体积、相同pH的一元强酸和一元中强酸溶液,初始时C(H+)相同,一元中强酸溶
⇌
D、增大一种反应物的浓度,平衡向正反应移动,可以提高其它反应物的转化率. 液中存在酸的电离平衡,则一元中强酸的浓度大于一元强酸的浓度,与足量的锌粉反应产生的
⇌
【解答】解:A、氯气溶于水存在平衡Cl +H O H++Cl﹣+HClO,饱和氯化钠溶液含有电离氯离子, 氢气体积大,反应过程中一元中强酸溶液②继续电离,溶液中氢离子浓度大,产生氢气速率快.
2 2
氯离子浓度增大,使平衡向左移动,抑制氯气
⇌
的溶解,故A正确; 【解答】解:因为强酸完全电离,一元中强酸部分电离,因此相同的PH值,即C(H+)相同时,
B、碘在碘化钾溶液中的存在平衡I +I﹣ I ﹣,KI溶液中,含有电离碘离子,碘离子浓度增大,使 一元中强酸的浓度比强酸浓度大,由于体积相等,因此一元中强酸的物质的量大于强酸,因此
2 3
平衡向右移动,碘的溶解度增大,故 ⇌ B正确; 产生的H 2 也比强酸多。反应过程由于H+不断被消耗掉,促使一元中强酸继续电离出 H+,由于
C、醋酸存在电离平衡HAc H++Ac﹣,醋酸钠溶液中有大量的Ac﹣,Ac﹣浓度增大抑制醋酸的电离, 其他条件都相同,反应速率取决于H+浓度,由于开始时H+浓度相等,因此反应速率也相等(在
故C错误; ⇌ 图中反应速率就是斜率),后面强酸的反应速率下降得快,斜率也就更小,曲线更平坦。最终
D、工业生成硫酸存在平衡:2SO 2 +O 2 2SO 3 ,增大氧气的浓度,平衡向正反应移动,可以提高二 生成H 2 的体积也比一元中强酸少,因此曲线在一元中强酸下面,故C符合;
氧化硫的转化率,故D正确; ⇌ 故选:C。
故选:C。 【点评】本题考查了弱电解质溶液的电离平衡移动,题目难度不大,注意一元中强酸属于弱电解
【点评】本题考查影响化学平衡的因素等,难度中等,C选项为易错点,容易利用盐类水解分析,
质,在溶液中存在电离平衡,侧重于考查学生的分析能力.
醋酸钠溶液呈碱性,中和氢离子,促进电离,这是次要因素,醋酸根浓度远远高于氢氧根离子
浓度,醋酸根的影响是主要因素. 5.(3分)若(NH ) SO 在强热时分解的产物是SO 、N 、NH 和H O,则该反应中化合价发生
4 2 4 2 2 3 2
变化和未发生变化的N原子数之比为( )
4.(3分)相同体积、相同pH的某一元强酸溶液①和某一元中强酸溶液②分别与足量的锌粉发 A.1:4 B.1:2 C.2:1 D.4:1
生反应,下列关于氢气体积(V)随时间(t)变化的示意图正确的是( )
【考点】BQ:氧化还原反应的计算.
菁优网版权所有
【专题】515:氧化还原反应专题.
【分析】先根据氧化还原反应中得失电子相等配平方程式,再根据化合价变化的和化合价不变的
A. B.
氮原子判断.
【解答】解:该反应中,NH +→N 氮元素的化合价由﹣3价→0价,生成一个氮气分子需要铵根离
4 2
子失去6个电子,生成一个二氧化硫分子需要硫酸根离子得到2个电子,所以其最小公倍数是
6,然后其它元素根据原子守恒进行配平方程式,所以该方程式为 3(NH ) SO
4 2 4
C. D.
3SO ↑+N ↑+4NH ↑+6H O,该方程式中铵根离子和氨气分子中氮原子的化合价都是﹣3价,化合
2 2 3 2
价不变,所以则该反应中化合价发生变化和未发生变化的N原子数之比为1×2:4×1=1:2,故选:B。 A.X和其他三种元素均可形成至少2种二元化合物
【点评】本题考查了根据方程式进行有关计算,难度不大,注意该方程式中氧化剂和还原剂是同 B.W和X、Z两种元素分别形成的二元化合物中,均有直线形分子
一种物质,但氧化产物和还原产物不同,所以从生成物进行配平较简便. C.W、X和Y三种元素可以形成碱性化合物
D.Z和其他三种元素形成的二元化合物,其水溶液均呈酸性
6.(3分)在一定温度、压强下,向 100mLCH 和Ar的混合气体中通入 400mLO ,点燃使其完
4 2
全燃烧,最后在相同条件下得到干燥气体 460mL,则反应前混合气体中CH 和Ar物质的量之 【考点】8G:原子结构与元素的性质.
4 菁优网版权所有
【专题】16:压轴题;51C:元素周期律与元素周期表专题.
比是( )
A.1:4 B.1:3 C.1:2 D.1:1
【分析】短周期元素W、X、Y、Z原子序数依次增大,且W、X、Y+、Z的最外层电子数与其电
子层数的比值依次为2、3、4、2,若W的电子层数为2,最外层电子数为4,所以W为C,若
【考点】5A:化学方程式的有关计算;IA:甲烷的化学性质;M3:有关混合物反应的计算. W的电子层数为3,最外层电子数为6,所以W为S;X的电子层数为2,最外层电子数为6,
菁优网版权所有
【专题】1A:计算题. 所以 X 为 O,即 W 只能为 C;Y+的电子层数为 2,最外层电子数为 8,所以 Y 的质子数为
【分析】反应的方程式为:CH +2O →CO +2H O,Ar为惰性气体,不参与反应,根据反应前后的 2+8+1=11,所以Y为Na;Z的电子层数为3,最外层电子数为6,所以Z为S,然后结合元素
4 2 2 2
气体体积的变化用差量法计算. 及其化合物的性质来解答.
【解答】解:设原混合气体中含有xmlCH ,反应的方程式为CH +2O →CO +2H O,利用差量法 【解答】解:短周期元素W、X、Y、Z原子序数依次增大,且W、X、Y+、Z的最外层电子数与
4 4 2 2 2
计算: 其电子层数的比值依次为2、3、4、2,若W的电子层数为2,最外层电子数为4,所以W为
CH +2O →CO +2H O△V C,若W的电子层数为3,最外层电子数为6,所以W为S;X的电子层数为2,最外层电子数
4 2 2 2
1 2 1 2 为6,所以X为O,即W只能为C;Y+的电子层数为2,最外层电子数为8,所以Y的质子数
x 2x x 2x 为2+8+1=11,所以Y为Na;Z的电子层数为3,最外层电子数为6,所以Z为S,
则2x=(100ml+400ml)﹣460ml=40ml,
A.O和C形成CO、CO ,O和Na形成Na O、Na O ,O和S形成SO 、SO ,故A正确;
2 2 2 2 2 3
解得x=20ml,
B.W和X、Z两种元素分别形成的CO 、CS ,均为直线型分子,故B正确;
2 2
所以:Ar的体积为V(Ar)=100ml﹣20ml=80ml,
C.W、X和Y三种元素可以形成碳酸钠,碳酸钠溶液呈碱性,故C正确;
气体的体积之比等于物质的量之比, D.S与Na可形成二元化合物Na S,其水溶液呈碱性,故D错误;
2
所以:n(CH
4
):n(Ar)=V(CH
4
):v(Ar)=20ml:80ml=1:4,
故选:D。
故选:A。
【点评】本题考查原子结构和元素周期律,元素的推断是解答本题的关系,注意短周期,不考虑
【点评】本题考查混合气体的计算,题目难度不大,注意利用体积变化,用差量法计算.
稀有气体时电子层为2或3即可解答,题目难度不大.
7.(3分)短周期元素W、X、Y、Z的原子序数依次增大,且 W、X、Y+、Z的最外层电子数与
8.(3分)三位科学家因在烯烃复分解反应研究中的杰出贡献而荣获2005年度诺贝尔化学奖,烯
其电子层数的比值依次为2、3、4、2(不考虑零族元素).下列关于这些元素的叙述错误的是
烃 复 分 解 反 应 可 示 意 如 图 :
( )【点评】本题考查信息的接受能力,难度不大,烯烃的复分解反应的实质是:两种烯烃中的碳碳
双键分别断裂,相互交换成分形成另外两种烯烃.
二、非选题
下列化合物中,经过烯烃复分解反应可以生成 的是( )
9.向 2L 密闭容器中通入 amol 气体 A 和 bmol 气体 B,在一定条件下发生反应:xA(g)+yB
(g) pC(g)+qD(g)
⇌
已知:平均反应速率v = ;反应2min 时,A的浓度减少了 ,B的物质的量减少了 mol,有a
C
A. B.
mol D生成.
回答下列问题:
(1)反应2min内,v = mol•L ﹣1 •min ﹣1 ,v mol•L ﹣1 •min ﹣1 ;
A B
C. D. (2)化学方程式中,x= 2 、y= 3 、p= 1 、q= 6 ;
(3)反应平衡时,D为 2amol,则B的转化率为 100a/b% ;
(4)如果只升高反应温度,其他反应条件不变,平衡时D为 1.5a mol,则该反应的△H < 0;
【考点】IE:烯烃.
菁优网版权所有
(填“>”、“<”或“=”))如果其他条件不变,将容器的容积变为 1L,进行同样的实验,则与
【专题】16:压轴题;534:有机物的化学性质及推断.
上述反应比较:
【分析】根据题所给信息烯烃在合适催化剂作用下可双键断裂,两端基团重新组合为新的烯烃,
①反应速率 增大 (填“增大”、“减小”或“不变”),理由是 体积减小,反应物的浓度增大,
据此结合选项解答.
因而使反应速率增大 ;
②平衡时反应物的转化率 减小 (填“增大”、“减小”或“不变”),理由是 体积减小,气体的
【解答】解:A、 中两个碳碳双键断裂后,生成物中新形成的环为六元环,且新环中所
压强增大,平衡向气体分子数少的方向(即逆反应方向)移动,因而使反应物转化率减小 .
形成的碳碳双键位置符合要求,故A正确;
【考点】CP:化学平衡的计算.
菁优网版权所有
B、 中两个碳碳双键断裂后,合成的是五元环,故B错误; 【专题】51E:化学平衡专题.
【分析】(1)列出三段式计算,依据依据化学反应速率是单位时间内物质浓度的变化计算得到;
C、 中两个碳碳双键断裂后,合成了六元环,但是碳碳双键的位置不正确,故C错误;
(2)依据三段式结合变化量之比=化学方程式的系数之比计算判断;
(3)依据计算得到的系数和(1)三段式列式数据,计算转化率;
(4)依据平衡移动原理结合 D物质的量变化,判断反应进行的方向,体积变小压强增大速率增
D、 中两个碳碳双键断裂后,得到的是五元环,故D错误;
大,平衡逆向进行;
故选:A。【解答】解:(1)根据题干信息结合平衡三段式列式,A减少量和生成C的物质的量之比等于速 故答案为:增大 体积减小,反应物的浓度增大,因而使反应速率增大;
率之比等于计量数之比,平均反应速率v =v /2, ②将容器的容积变为 1L,压强增大,反应速率增大,平衡向气体体积减小的反应方向进行,即向
C A
xA(g)+yB(g) pC(g)+qD(g) 逆向进行,反应物转化率减小;
起始量(mol) a b 0 0 故答案为:减小 体积减小,气体的压强增大,平衡向气体分子数少的方向(即逆反应方向)移动,
⇌
因而使反应物转化率减小.
变化量(mol) a a
【点评】本题考查了化学反应速率的计算判断,化学平衡影响因素的分析理解,三段式计算的应
平衡量(mol) a b﹣ a
用,物质转化率的计算,掌握化学平衡的基础是解题关键,题目难度中等.
10.A、B、C、D、E、F、G、H、和I、是中学化学中常见的气体,它们均由短周期元素组成,
用A表示的反应速率v = = mol•L﹣1•min﹣1
A
具有如下性质:
①A、B、E、F、G能使湿润的蓝色石蕊试纸变红,I能使湿润的红色石蕊试纸变蓝,C、D、H不
能使湿润的石蕊试纸变色;
用B表示的反应速率v = = mol•L﹣1•min﹣1;
B
②A和I相遇产生白色烟雾;
③B和E都能使品红溶液褪色;
故答案为: mol•L﹣1•min﹣1; mol•L﹣1•min﹣1;
④将红热的铜丝放入装有B的瓶中,瓶内充满棕黄色的烟;
⑤将点燃的镁条放入装有F的瓶中,镁条剧烈燃烧,生成白色粉末,瓶内壁附着黑色颗粒;
(2)依据(1)的列式计算x:y:p:q= : : :a=2:3:1:6
⑥C和D相遇生成红棕色气体;
x=2,y=3,p=1,q=6;
⑦G在D中燃烧可以产生E和H O;
2
故答案为:2 3 1 6;
⑧将B和H 在瓶中混合后于亮处放置几分钟,瓶内壁出现油状液滴并产生A.
回答下列问题:
(3)反应平衡时,D为 2amol,则a=2amol,则B的转化率为= ×100%= ×100%=
(1)A的化学式是 HCl ,②中烟雾的化学式是 NH Cl ;
4
故答案为: ; (2)④中发生反应的化学方程式是 Cu + Cl CuCl ;
2 2
(4)依据(3)的平衡物质的量,如果只升高反应温度,其他反应条件不变,平衡时 D为 1.5a
(3)⑤中发生反应的化学方程式是 2Mg + CO 2MgO + C ;
2
mol,说明升温平衡逆向进行,逆向是吸热反应,正向是放热反应,△H<0;
(4)C的化学式是 NO ,D的化学式是 O ;
2
故答案为:<;
(5)如果其他条件不变,将容器的容积变为 1L;是体积缩小的变化;压强增大,反应速率增大, (5)⑦中发生反应的化学方程式是 2H S + 3O 2H O + 2SO ;
2 2 2 2
反应是:2A(g)+3B(g) C(g)+6D(g)
(6)H的化学式是 CH .
4
①体积减小,压强增大,物质的浓度增大,反应速率增大;反应向气体体积减小的反应方向进行;
⇌【考点】GS:无机物的推断;PF:常见气体的检验.
菁优网版权所有 (2)④中发生的反应是铜与氯气反应生成氯化铜,反应方程式为:Cu+Cl CuCl ,故答案
2 2
【专题】11:推断题.
【分析】①A、B、E、F、G能使湿润的蓝色石蕊试纸变红,为酸性气体,I能使湿润的红色石蕊
为:Cu+Cl CuCl ;
2 2
试纸变蓝,为碱性气体,故A为HCl,B为NH ,C、D、H不能使湿润的石蕊试纸变色,不表
3
(3)⑤中发生的反应是 Mg 在二氧化碳中燃烧生成碳越氧化镁,反应方程式为:2Mg+CO
现酸碱性; 2
②A和I相遇产生白烟,为NH 与HCl;
3
2MgO+C,故答案为:2Mg+CO 2MgO+C;
2
③B和E都能使品红溶液褪色,为Cl 和SO ;
2 2
(4)由上述分子可知,C的化学式是NO,D的化学式是O ,故答案为:NO;O ;
④将红热的铜丝放入装有B的瓶中,瓶内充满棕黄色的烟,故B为Cl ,E为SO ; 2 2
2 2
⑤Mg条能在F中剧烈燃烧,有黑色和白色两种产物,F为CO
2
; (5)⑦中发生的反应是硫化氢燃烧生成二氧化硫与水,反应方程式为:2H
2
S+3O
2
⑥C和D相遇生成红棕色气体,为NO和O ;
2
2SO +2H O,
2 2
⑦G在D中燃烧可以产生E和H O,E为SO ,故D为O ,故C为NO,G含有H、S两种元素,
2 2 2
故答案为:2H S+3O 2SO +2H O;
G为H S; 2 2 2 2
2
⑧B为Cl 2 ,和H在瓶中混合后于亮处放置几分钟,瓶壁出现油状液滴并产生 A(HCl),故H为 (6)由上述分析可知,H的化学式是CH 4 等,故答案为:CH 4 .
CH 4 等. 【点评】本题考查物质性质的应用,以文字描述形式考查中学常见气体的性质、处于化学用语的
【解答】解:①A、B、E、F、G能使湿润的蓝色石蕊试纸变红,为酸性气体,I能使湿润的红色
书写,难度不大,注意基础知识的掌握,注意Mg可以在二氧化碳和氮气中燃烧.
石蕊试纸变蓝,为碱性气体,故A为HCl,B为NH
3
,C、D、H不能使湿润的石蕊试纸变色,
不表现酸碱性; 11.如图是一个用铂丝作电极,电解稀的MgSO 溶液的装置,电解液中加有中性红指示剂,此时
4
②A和I相遇产生白烟,为NH
3
与HCl; 溶液呈红色.(指示剂的pH变色范围:6.8~8.0,酸色﹣红色,碱色﹣黄色).
③B和E都能使品红溶液褪色,为Cl 2 和SO 2 ; 回答下列问题:
④将红热的铜丝放入装有B的瓶中,瓶内充满棕黄色的烟,故B为Cl 2 ,E为SO 2 ; (1)下列关于电解过程中电极附近溶液颜色变化的叙述正确的是 ①④ (填编号);
⑤Mg条能在F中剧烈燃烧,有黑色和白色两种产物,F为CO
2
; ①A管溶液由红变黄; ②B管溶液由红变黄;
⑥C和D相遇生成红棕色气体,为NO和O
2
; ③A管溶液不变色; ④B管溶液不变色;
⑦G在D中燃烧可以产生E和H 2 O,E为SO 2 ,故D为O 2 ,故C为NO,G含有H、S两种元素, (2)写出A管中发生反应的反应式: 2H + + 2e ﹣ =H 2 ↑ 、 Mg 2 + + 2OH ﹣ =Mg ( OH ) 2 ↓ ;
G为H 2 S; (3)写出B管中发生反应的反应式: 4OH ﹣ ﹣4e ﹣ =2H 2 O + O 2 ↑ ;
⑧B为Cl ,和H在瓶中混合后于亮处放置几分钟,瓶壁出现油状液滴并产生 A(HCl),故H为 (4)检验a管中气体的方法是 用拇指按住管口,取出试管,靠近火焰,放开拇指,有爆鸣声,
2
CH 4 等, 管口有蓝色火焰 ;
(1)由上述分析可知,A的化学式是HCl,①中生成的白烟是氯化铵,由铵根离子与氯离子构成, (5)检验b管中气体的方法是 用拇指按住管口,取出试管,放开拇指,将带有火星的木条伸入
化学式为NH 4 Cl,故答案为:HCl,;NH 4 Cl; 试管内会复燃 ;(6)电解一段时间后,切断电源,将电解液倒入烧杯内观察到的现象是 溶液呈红色,白色沉淀 ﹣﹣4e﹣=2H O+O ↑;
2 2
溶解 . (4)a管中收集的气体是氢气,氢气具有可燃性,其检验方法为:用拇指按住管口,取出试管,
靠近火焰,放开拇指,有爆鸣声,管口有蓝色火焰,
故答案为:用拇指按住管口,取出试管,靠近火焰,放开拇指,有爆鸣声,管口有蓝色火焰;
(5)b管中收集的气体是氧气,氧气能使带火星的木条复燃,其检验方法为:用拇指按住管口,
取出试管,放开拇指,将带有火星的木条伸入试管内会复燃,
故答案为:用拇指按住管口,取出试管,放开拇指,将带有火星的木条伸入试管内会复燃;
(6)将电解液倒入烧杯中,溶液中含有硫酸,溶液呈酸性,所以溶液为红色,A管生成的氢氧化
镁能溶于稀硫酸,所以看到的现象是:溶液呈红色,白色沉淀溶解(或大部分溶解),
故答案为:溶液呈红色,白色沉淀溶解(或大部分溶解).
【考点】DI:电解原理.
菁优网版权所有
【点评】本题考查了电解原理,根据各个电极上发生的电极反应及溶液的酸碱性来分析解答,注
【专题】16:压轴题;51I:电化学专题.
意A管中不仅有氢气生成,还产生白色沉淀,为易错点.
【分析】(1)电解时,阳极上氢氧根离子放电,同时电极附近有氢离子生成,溶液呈酸性;阴极
上氢离子放电生成氢气,同时电极附近有氢氧根离子生成,溶液呈碱性,根据指示剂和酸碱的
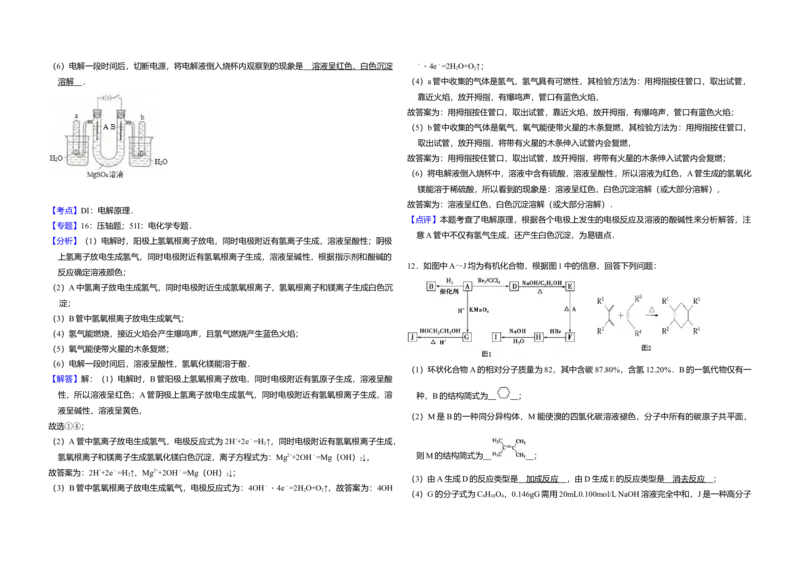
12.如图中A~J均为有机化合物,根据图1中的信息,回答下列问题:
反应确定溶液颜色;
(2)A中氢离子放电生成氢气,同时电极附近生成氢氧根离子,氢氧根离子和镁离子生成白色沉
淀;
(3)B管中氢氧根离子放电生成氧气;
(4)氢气能燃烧,接近火焰会产生爆鸣声,且氢气燃烧产生蓝色火焰;
(5)氧气能使带火星的木条复燃;
(6)电解一段时间后,溶液呈酸性,氢氧化镁能溶于酸.
(1)环状化合物A的相对分子质量为82,其中含碳87.80%,含氢12.20%.B的一氯代物仅有一
【解答】解:(1)电解时,B管阳极上氢氧根离子放电,同时电极附近有氢原子生成,溶液呈酸
性,所以溶液呈红色;A管阴极上氢离子放电生成氢气,同时电极附近有氢氧根离子生成,溶 种,B的结构简式为 ;
液呈碱性,溶液呈黄色,
(2)M是B的一种同分异构体,M能使溴的四氯化碳溶液褪色,分子中所有的碳原子共平面,
故选①④;
(2)A管中氢离子放电生成氢气,电极反应式为2H++2e﹣=H ↑,同时电极附近有氢氧根离子生成,
2
氢氧根离子和镁离子生成氢氧化镁白色沉淀,离子方程式为:Mg2++2OH﹣=Mg(OH) ↓, 则M的结构简式为 ;
2
故答案为:2H++2e﹣=H ↑、Mg2++2OH﹣=Mg(OH) ↓;
2 2
(3)由A生成D的反应类型是 加成反应 ,由D生成E的反应类型是 消去反应 ;
(3)B管中氢氧根离子放电生成氧气,电极反应式为:4OH﹣﹣4e﹣=2H O+O ↑,故答案为:4OH
2 2
(4)G的分子式为C H O ,0.146gG需用20mL0.100mol/L NaOH溶液完全中和,J是一种高分子
6 10 4化 合 物 . 则 由 G 转 化 为 J 的 化 学 方 程 式 为
量= ,20mL0.100mol/L NaOH 的物质的量=0.100mol/L×0.02L=0.002mol,
所以G中含有两个羧基,其结构简式为:HOOCCH CH CH CH COOH,G和乙二醇反应生成
2 2 2 2
;
(5)分子中含有两个碳碳双键,且两个双键之间有一个碳碳单键的烯烃与单烯烃可发生如图2反
J,J是一种高分子化合物,所以J的结构简式为: .
应则由E和A反应生成F的化学方程式为 ; 【解答】解:根据 A 中碳氢含量知 A 是烃,A 中碳原子个数= =6,氢原子个数=
(6)H中含有的官能团是 ﹣ Br ,I中含有的官能团是 ﹣ OH .
,所以A的分子式为C H ,A能和氢气发生加成反应生成B,说明A中含有碳
6 10
【考点】HB:有机物的推断.
菁优网版权所有
【专题】16:压轴题;534:有机物的化学性质及推断.
碳双键,B的一氯代物仅有一种,说明环烷烃B没有支链,所以A的结构简式为 ,B的结
【分析】根据 A 中碳氢含量知 A 是烃,A 中碳原子个数= =6,氢原子个数=
构简式为: ;
,所以A的分子式为C H ,A能和氢气发生加成反应生成B,说明A中含有碳
6 10
A和溴发生加成反应生成D,所以D的结构简式为: ,D和氢氧化钠的醇溶液发生消去
碳双键,B的一氯代物仅有一种,说明环烷烃B没有支链,所以A的结构简式为 ,B的结
反应生成E,E能和A发生反应生成F,结合题给信息知,E的结构简式为: ,F的结构
构简式为: ;
简式为: ,F和HBr发生加成反应生成H,则H的结构简式为: ,H和氢
A和溴发生加成反应生成D,所以D的结构简式为: ,D和氢氧化钠的醇溶液发生消去
氧化钠的水溶液发生取代反应生成I,I的结构简式为: ,A被酸性高锰酸钾氧化
反应生成E,E能和A发生反应生成F,结合题给信息知,E的结构简式为: ,F的结构 生成G,碳碳双键能被酸性高锰酸钾氧化生成羧酸,G的分子式为C H O ,0.146gG的物质的
6 10 4
量= ,20mL0.100mol/L NaOH 的物质的量=0.100mol/L×0.02L=0.002mol,
简式为: ,F和HBr发生加成反应生成H,则H的结构简式为: ,H和氢
所以G中含有两个羧基,其结构简式为:HOOCCH CH CH CH COOH,G和乙二醇反应生成
2 2 2 2
氧化钠的水溶液发生取代反应生成 I,I的结构简式为: ,A被酸性高锰酸钾氧化
生成G,碳碳双键能被酸性高锰酸钾氧化生成羧酸,G的分子式为C H O ,0.146gG的物质的
6 10 4【点评】本题考查有机物的推断和合成,会运用题给信息是解本题关键,注意有机反应中的断键
J,J是一种高分子化合物,所以J的结构简式为: .
和成键方式,为易错点.
(1)通过以上分析知,B的结构简式为: ,故答案为: ;
(2)M是B的一种同分异构体,M能使溴的四氯化碳溶液褪色,说明含有碳碳双键,分子中所
有的碳原子共平面,则M中的碳碳双键位于中间,相当于乙烯中的氢原子被甲基取代,所以则
M的结构简式为 ,
故答案为: ;
(3)A和溴发生加成反应生成D,D和氢氧化钠的醇溶液发生消去反应生成E,故答案为:加成
反应;消去反应;
(4)G和乙二醇反应生成 J,J是一种高分子化合物,则该反应是缩聚反应,反应方程式为:
,
故答案为: ;
(5)A和E发生加聚反应生成F,该反应方程式为: ,
故答案为: ;
(6)H的结构简式为: ,所以H中含有的官能团是溴原子(﹣Br),I的结构简式为:
,I中含有的官能团是羟基(﹣OH),
故答案为:﹣Br;﹣OH.