文档内容
2017 年北京市高考化学试卷
一、本部分共 7小题,每小题 6分,共 42分.在每小题列出的四个选项中,
选出最符合题目要求的一项.
1.(6分)古丝绸之路贸易中的下列商品,主要成分属于无机物的是( )
A. 瓷器 B. 丝绸
C. 茶叶 D. 中草药
2.(6分)2016年 IUPAC 命名 117号元素为 Ts(中文名“ ”,tián),Ts
的原子核外最外层电子数是 7,下列说法不正确的是( )
A.Ts是第七周期第ⅦA 族元素
B.Ts 的同位素原子具有相同的电子数
C.Ts 在同族元素中非金属性最弱
D.中子数为176的Ts核素符号是 Ts
3.(6分)下列变化中,气体被还原的是( )
A.二氧化碳使Na O 固体变白
2 2
B.氯气使 KBr 溶液变黄
C.乙烯使 Br 的四氯化碳溶液褪色
2
D.氨气使AlCl 溶液产生白色沉淀
3
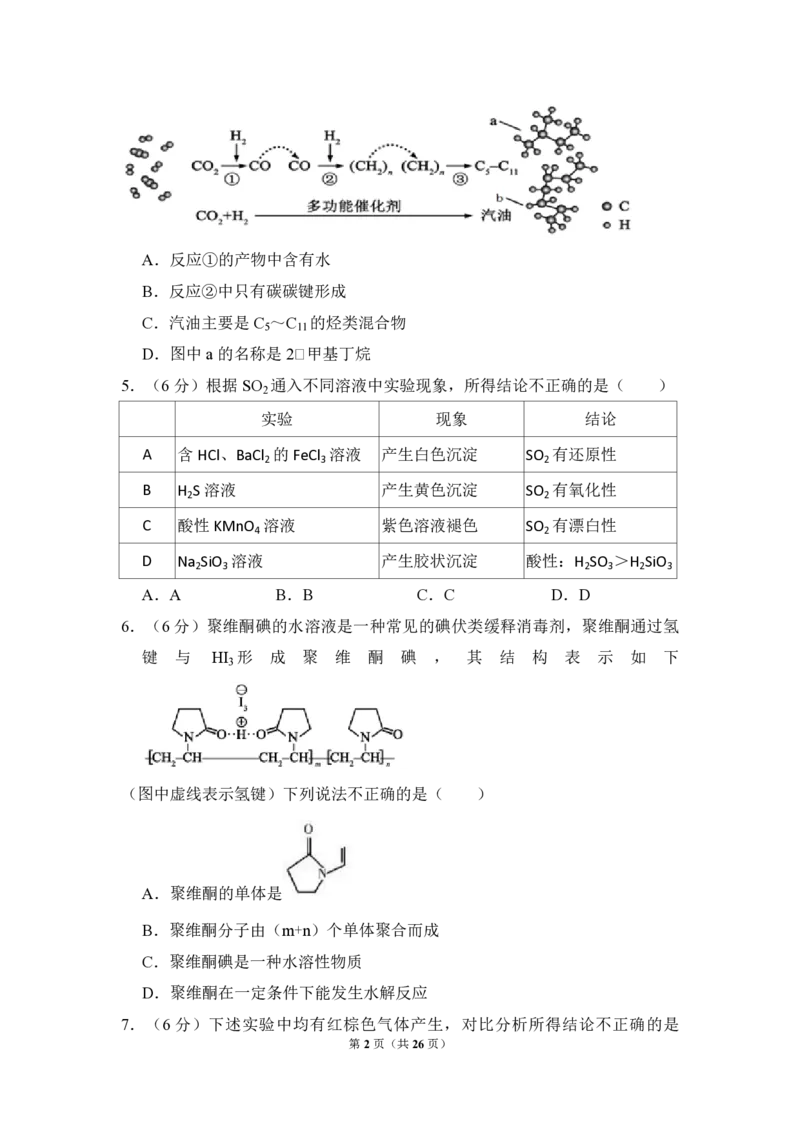
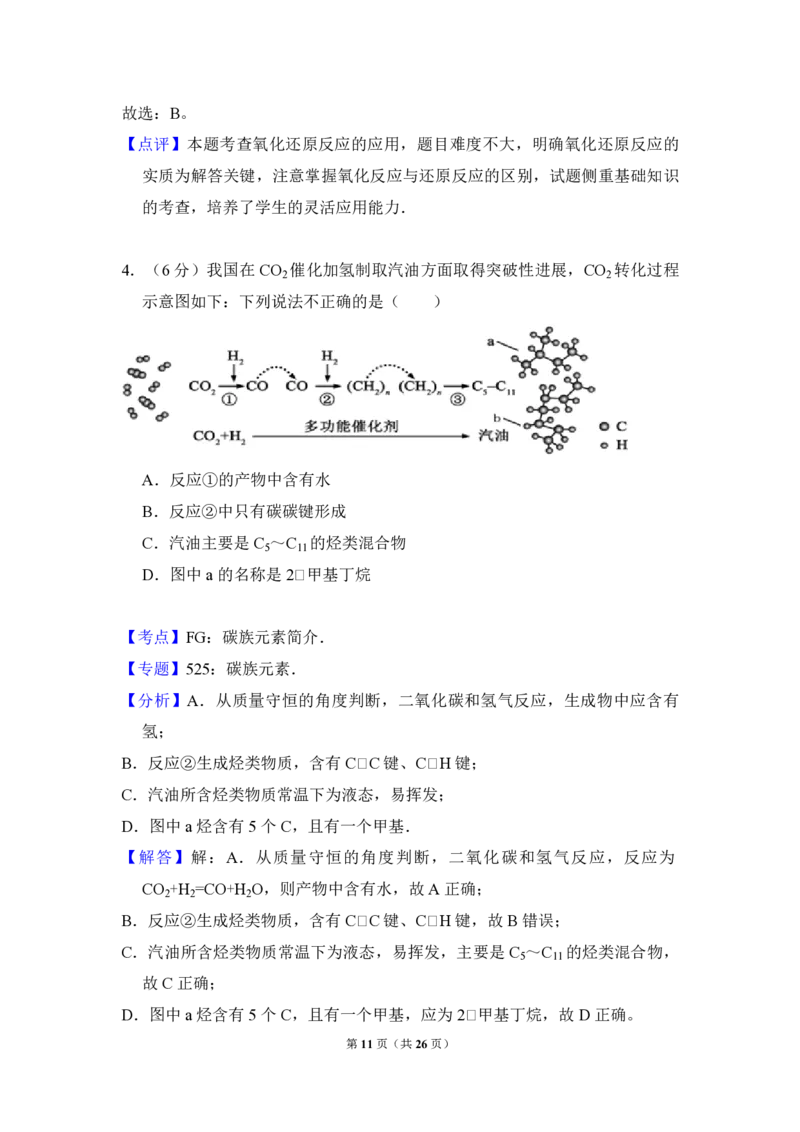
4.(6 分)我国在 CO 催化加氢制取汽油方面取得突破性进展,CO 转化过程
2 2
示意图如下:下列说法不正确的是( )
第1页(共26页)A.反应①的产物中含有水
B.反应②中只有碳碳键形成
C.汽油主要是C ~C 的烃类混合物
5 11
D.图中a的名称是2﹣甲基丁烷
5.(6分)根据SO 通入不同溶液中实验现象,所得结论不正确的是( )
2
实验 现象 结论
A 含HCl、BaCl 的FeCl 溶液 产生白色沉淀 SO 有还原性
2 3 2
B H S 溶液 产生黄色沉淀 SO 有氧化性
2 2
C 酸性KMnO 溶液 紫色溶液褪色 SO 有漂白性
4 2
D Na SiO 溶液 产生胶状沉淀 酸性:H SO >H SiO
2 3 2 3 2 3
A.A B.B C.C D.D
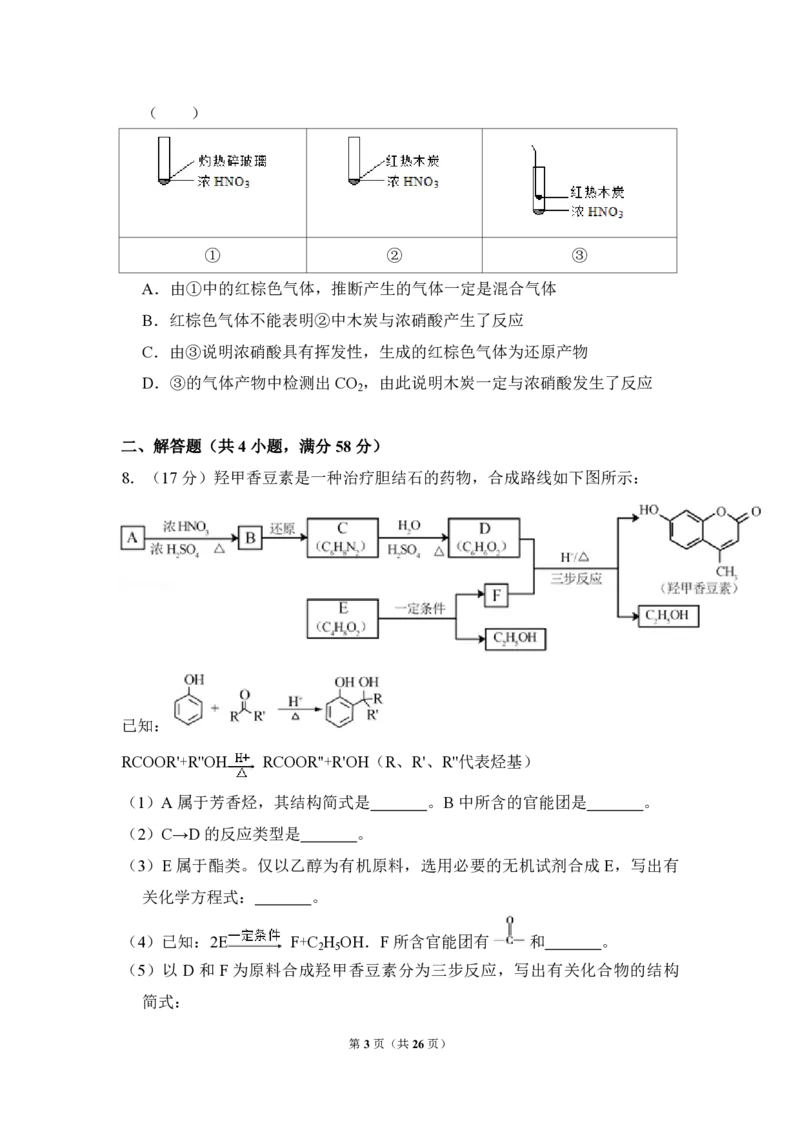
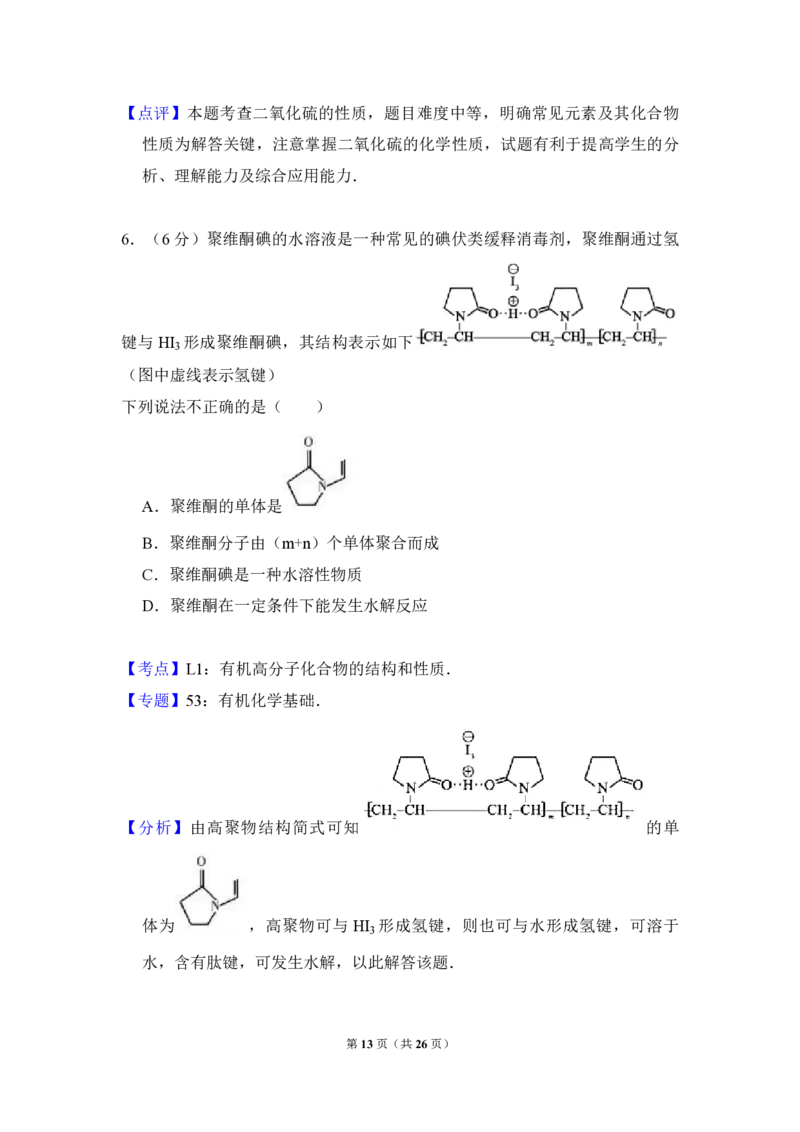
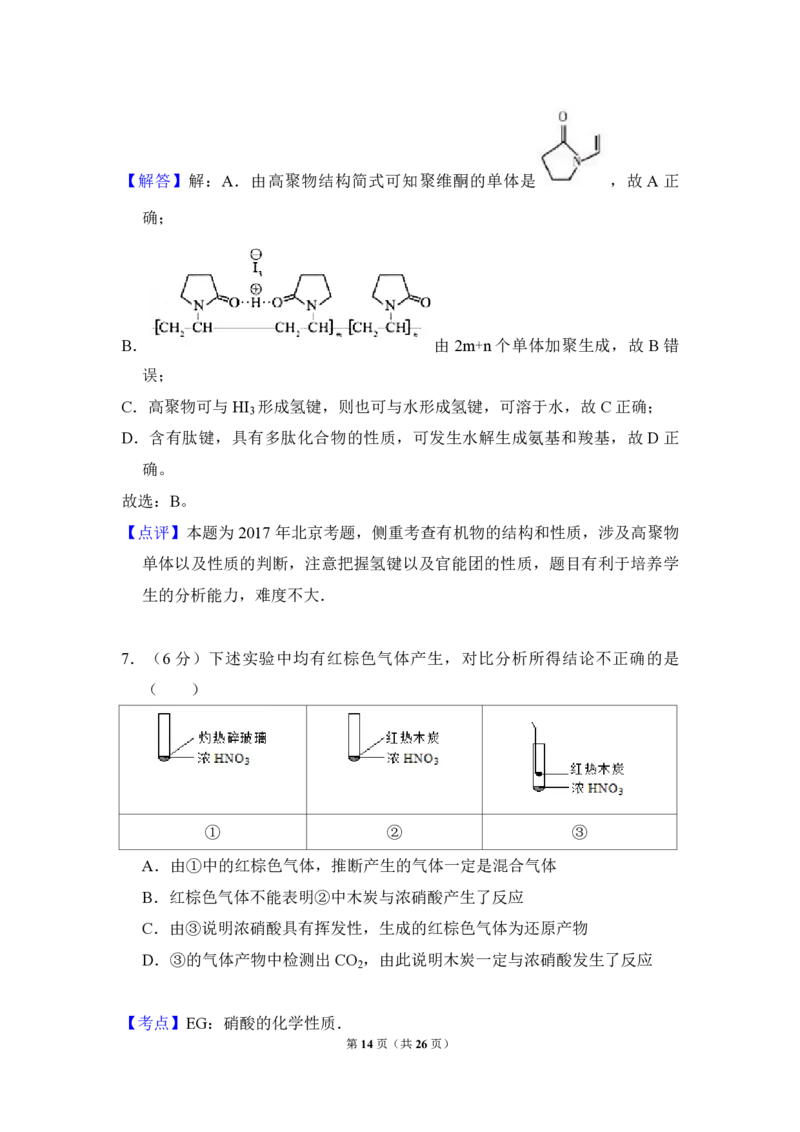
6.(6 分)聚维酮碘的水溶液是一种常见的碘伏类缓释消毒剂,聚维酮通过氢
键 与 HI 形 成 聚 维 酮 碘 , 其 结 构 表 示 如 下
3
(图中虚线表示氢键)下列说法不正确的是( )
A.聚维酮的单体是
B.聚维酮分子由(m+n)个单体聚合而成
C.聚维酮碘是一种水溶性物质
D.聚维酮在一定条件下能发生水解反应
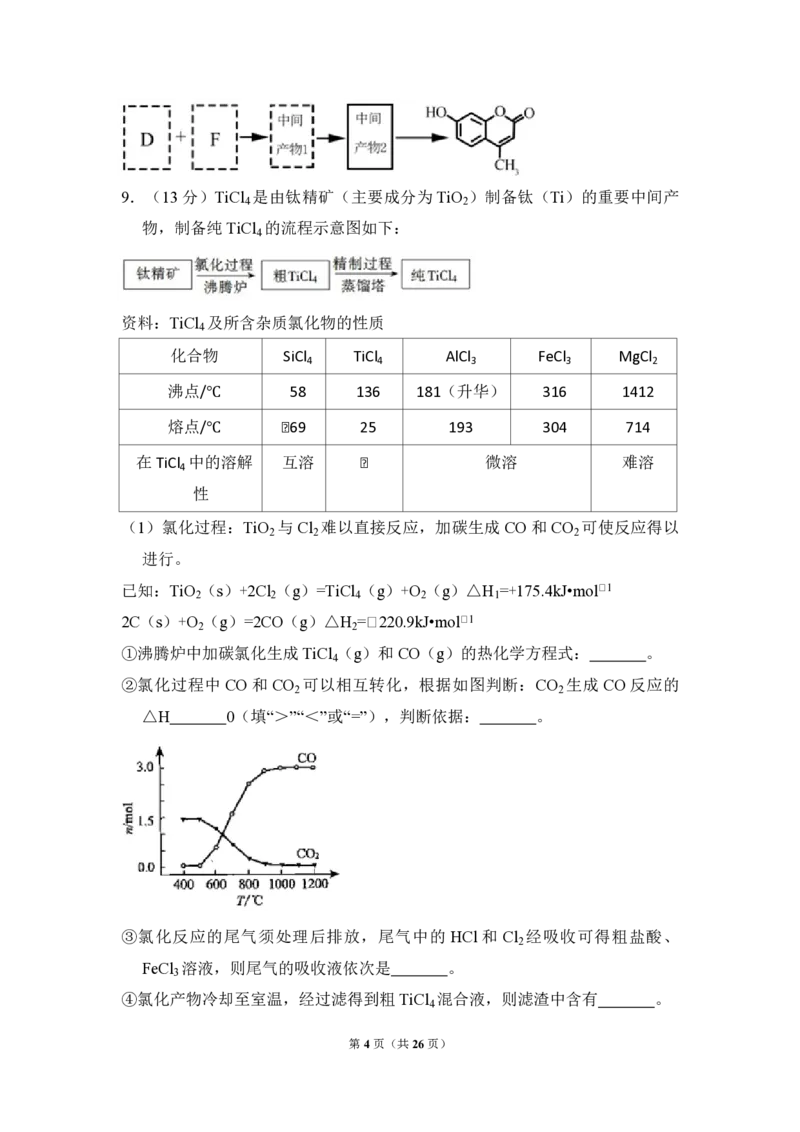
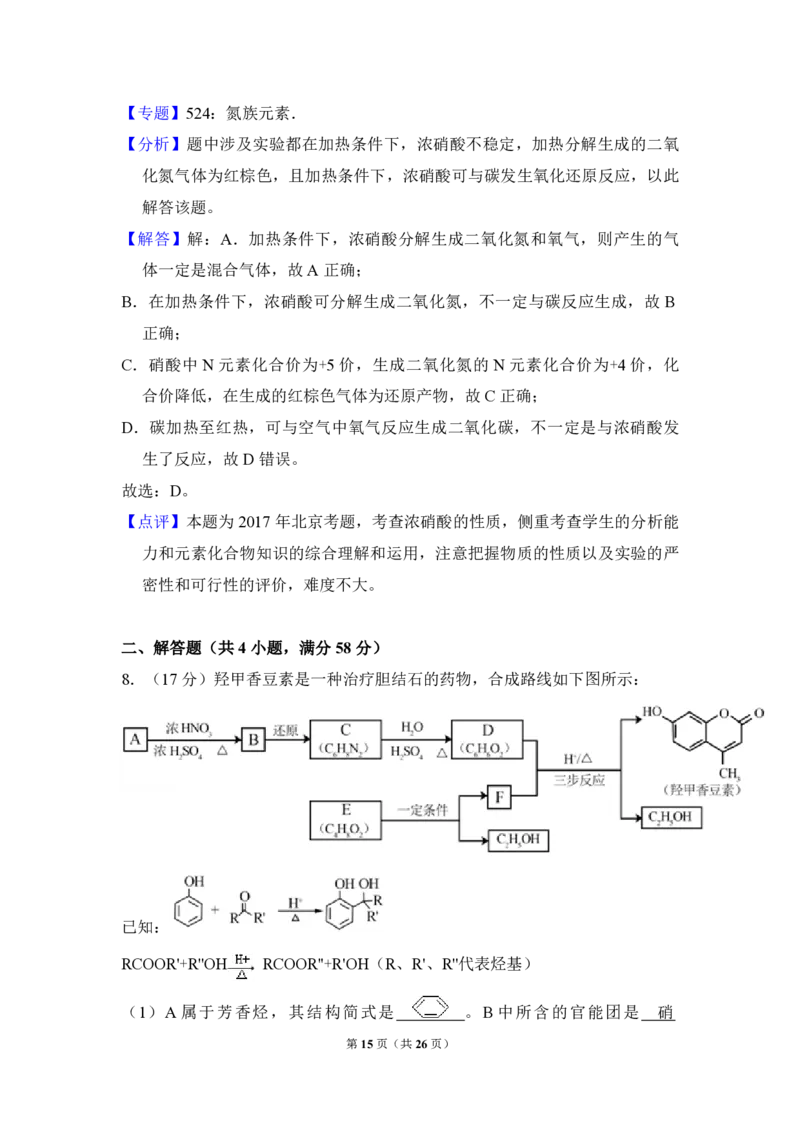
7.(6分)下述实验中均有红棕色气体产生,对比分析所得结论不正确的是
第2页(共26页)( )
① ② ③
A.由①中的红棕色气体,推断产生的气体一定是混合气体
B.红棕色气体不能表明②中木炭与浓硝酸产生了反应
C.由③说明浓硝酸具有挥发性,生成的红棕色气体为还原产物
D.③的气体产物中检测出CO ,由此说明木炭一定与浓硝酸发生了反应
2
二、解答题(共 4小题,满分 58分)
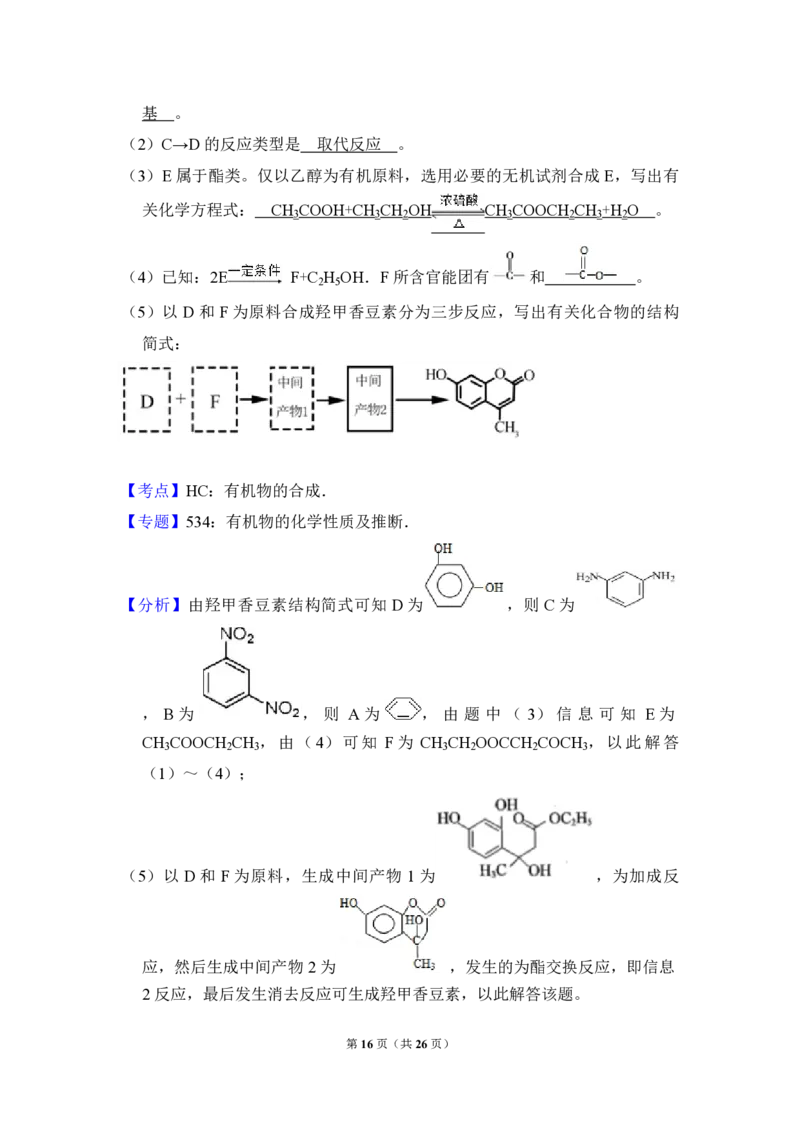
8.(17分)羟甲香豆素是一种治疗胆结石的药物,合成路线如下图所示:
已知:
RCOOR'+R''OH RCOOR''+R'OH(R、R'、R''代表烃基)
(1)A 属于芳香烃,其结构简式是 。B中所含的官能团是 。
(2)C→D 的反应类型是 。
(3)E属于酯类。仅以乙醇为有机原料,选用必要的无机试剂合成 E,写出有
关化学方程式: 。
(4)已知:2E F+C H OH.F 所含官能团有 和 。
2 5
(5)以 D 和 F 为原料合成羟甲香豆素分为三步反应,写出有关化合物的结构
简式:
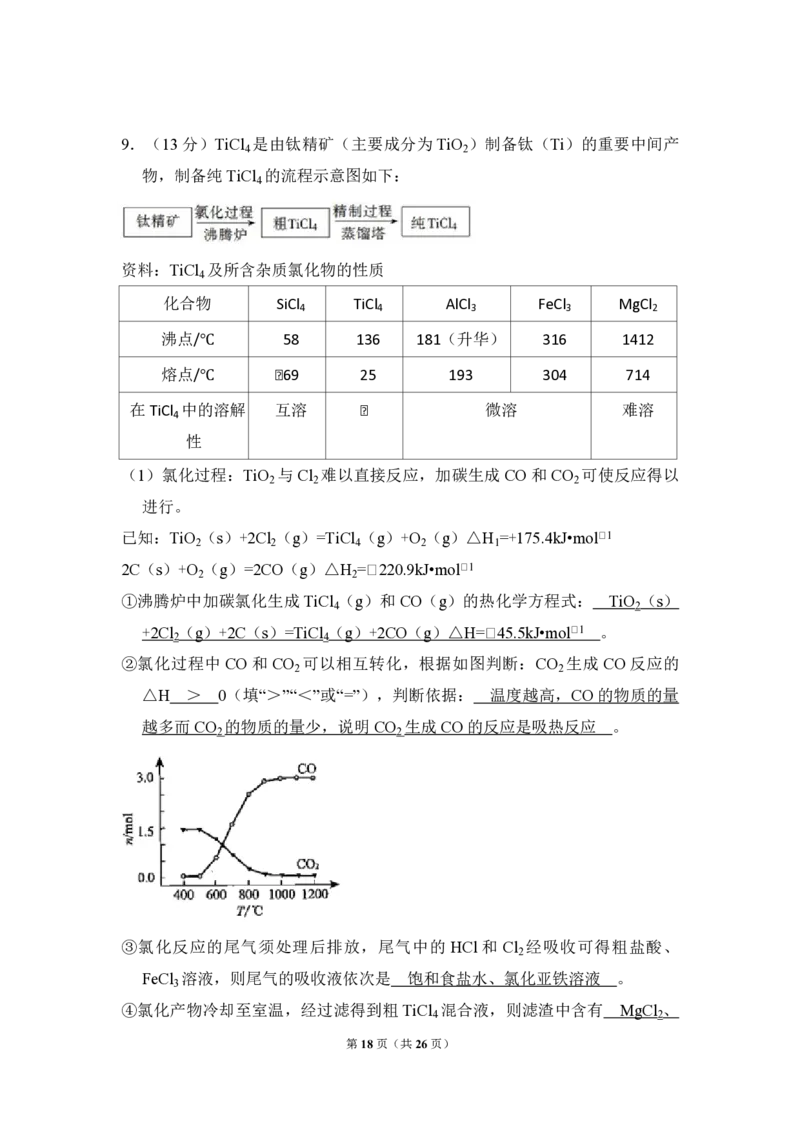
第3页(共26页)9.(13分)TiCl 是由钛精矿(主要成分为 TiO )制备钛(Ti)的重要中间产
4 2
物,制备纯TiCl 的流程示意图如下:
4
资料:TiCl 及所含杂质氯化物的性质
4
化合物 SiCl TiCl AlCl FeCl MgCl
4 4 3 3 2
沸点/℃ 58 136 181(升华) 316 1412
熔点/℃ ﹣69 25 193 304 714
在TiCl 中的溶解 互溶 ﹣ 微溶 难溶
4
性
(1)氯化过程:TiO 与 Cl 难以直接反应,加碳生成 CO 和 CO 可使反应得以
2 2 2
进行。
已知:TiO (s)+2Cl (g)=TiCl (g)+O (g)△H =+175.4kJ•mol﹣1
2 2 4 2 1
2C(s)+O (g)=2CO(g)△H =﹣220.9kJ•mol﹣1
2 2
①沸腾炉中加碳氯化生成TiCl (g)和CO(g)的热化学方程式: 。
4
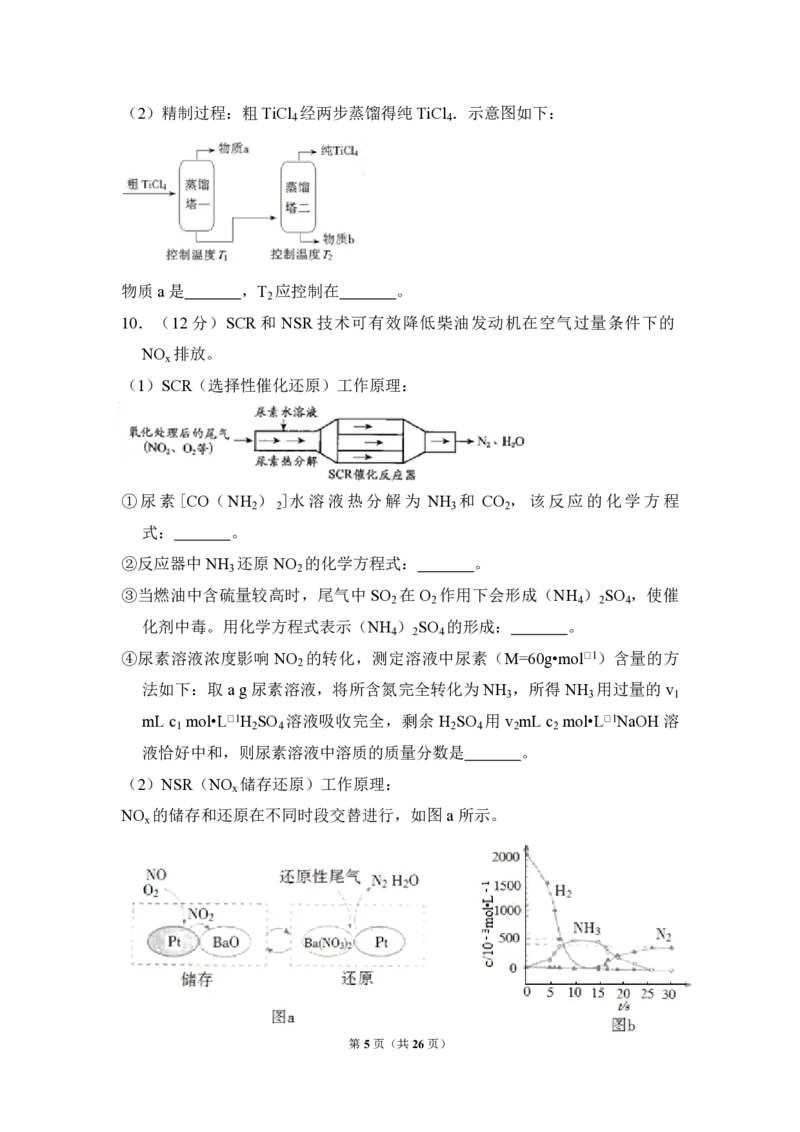
②氯化过程中 CO 和 CO 可以相互转化,根据如图判断:CO 生成 CO 反应的
2 2
△H 0(填“>”“<”或“=”),判断依据: 。
③氯化反应的尾气须处理后排放,尾气中的 HCl和 Cl 经吸收可得粗盐酸、
2
FeCl 溶液,则尾气的吸收液依次是 。
3
④氯化产物冷却至室温,经过滤得到粗TiCl 混合液,则滤渣中含有 。
4
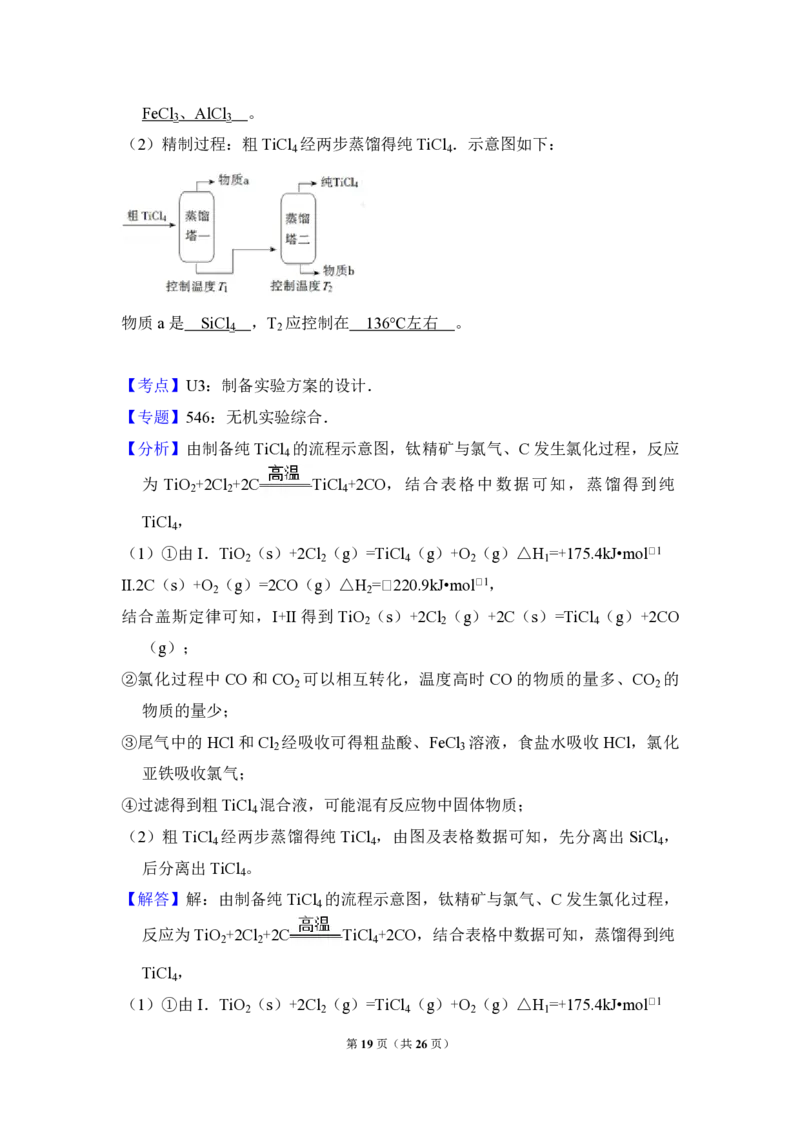
第4页(共26页)(2)精制过程:粗TiCl 经两步蒸馏得纯TiCl .示意图如下:
4 4
物质a是 ,T 应控制在 。
2
10.(12分)SCR 和 NSR 技术可有效降低柴油发动机在空气过量条件下的
NO 排放。
x
(1)SCR(选择性催化还原)工作原理:
①尿素[CO(NH ) ]水溶液热分解为 NH 和 CO ,该反应的化学方程
2 2 3 2
式: 。
②反应器中NH 还原NO 的化学方程式: 。
3 2
③当燃油中含硫量较高时,尾气中 SO 在 O 作用下会形成(NH ) SO ,使催
2 2 4 2 4
化剂中毒。用化学方程式表示(NH ) SO 的形成: 。
4 2 4
④尿素溶液浓度影响 NO 的转化,测定溶液中尿素(M=60g•mol﹣1)含量的方
2
法如下:取 a g尿素溶液,将所含氮完全转化为 NH ,所得 NH 用过量的 v
3 3 1
mL c mol•L﹣1H SO 溶液吸收完全,剩余 H SO 用 v mL c mol•L﹣1NaOH 溶
1 2 4 2 4 2 2
液恰好中和,则尿素溶液中溶质的质量分数是 。
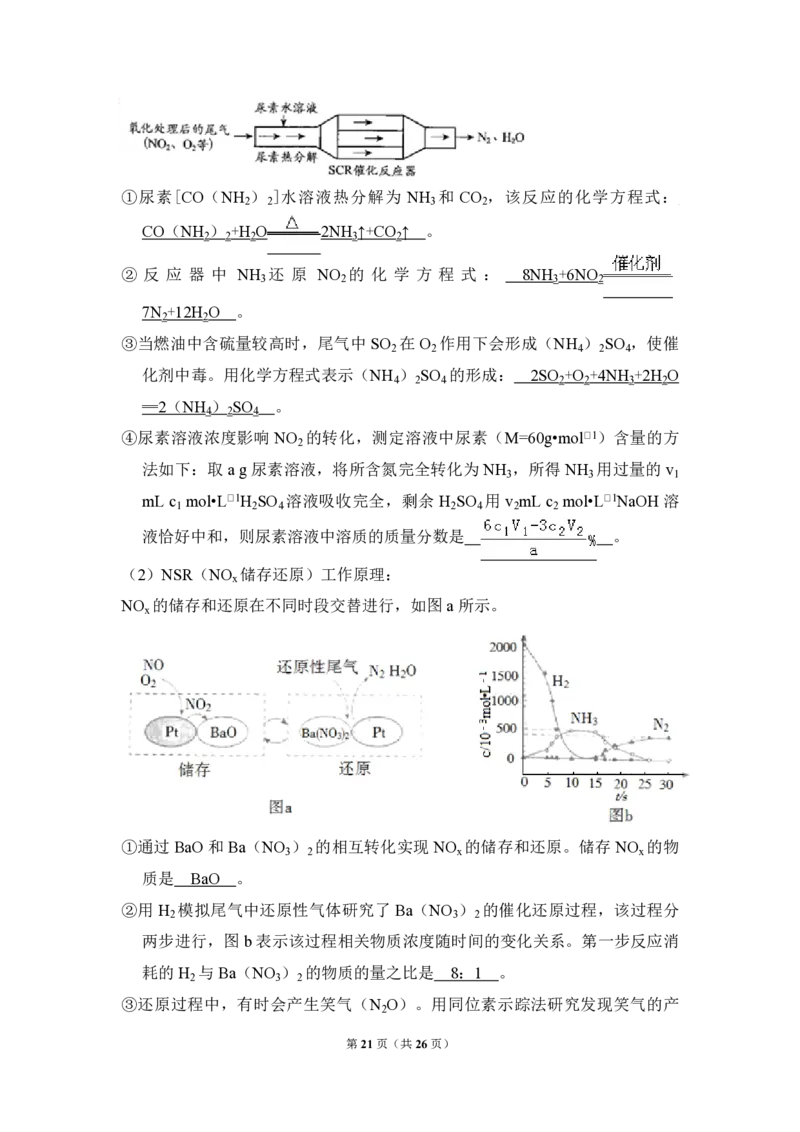
(2)NSR(NO 储存还原)工作原理:
x
NO 的储存和还原在不同时段交替进行,如图a所示。
x
第5页(共26页)①通过 BaO 和 Ba(NO ) 的相互转化实现 NO 的储存和还原。储存 NO 的物
3 2 x x
质是 。
②用 H 模拟尾气中还原性气体研究了 Ba(NO ) 的催化还原过程,该过程分
2 3 2
两步进行,图 b表示该过程相关物质浓度随时间的变化关系。第一步反应消
耗的H 与Ba(NO ) 的物质的量之比是 。
2 3 2
③还原过程中,有时会产生笑气(N O)。用同位素示踪法研究发现笑气的产
2
生与 NO 有关。在有氧条件下,15NO 与 NH 以一定比例反应时,得到的笑
3
气几乎都是15NNO.将该反应的化学方程式补充完整:
15NNO+ H O。
2
11.(16分)某小组在验证反应“Fe+2Ag+=Fe2++2Ag”的实验中检测到 Fe3+,发
现和探究过程如下。
向硝酸酸化的 0.05mol•L﹣1硝酸银溶液(pH≈2)中加入过量铁粉,搅拌后静
置,烧杯底部有黑色固体,溶液呈黄色。
(1)检验产物
①取少量黑色固体,洗涤后, (填操作和现象),证明黑色固体中含有
Ag。
②取上层清液,滴加 K [Fe(CN) ]溶液,产生蓝色沉淀,说明溶液中含
3 6
有 。
(2)针对“溶液呈黄色”,甲认为溶液中有 Fe3+,乙认为铁粉过量时不可能有
Fe3+,乙依据的原理是 (用离子方程式表示)。针对两种观点继续实
验:
①取上层清液,滴加 KSCN 溶液,溶液变红,证实了甲的猜测。同时发现有白
色沉淀产生,且溶液颜色变浅、沉淀量多少与取样时间有关,对比实验记录
如下:
序号 取样时间/min 现象
ⅰ 3 产生大量白色沉淀;溶液呈红色
ⅱ 30 产生白色沉淀;较 3min 时量少;溶液红色较 3min 时加
深
第6页(共26页)ⅲ 120 产生白色沉淀;较 30min 时量少;溶液红色较 3 0min 时
变浅
(资料:Ag+与SCN﹣生成白色沉淀AgSCN)
②对Fe3+产生的原因作出如下假设:
假设a:可能是铁粉表面有氧化层,能产生 Fe3+;
假设b:空气中存在O ,由于 (用离子方程式表示),可产生Fe3+;
2
假设c:酸性溶液中NO ﹣具有氧化性,可产生Fe3+;
3
假设d:根据 现象,判断溶液中存在Ag+,可产生Fe3+。
③下列实验Ⅰ可证实假设 a、b、c不是产生 Fe3+的主要原因。实验Ⅱ可证实假设
d成立。
实验Ⅰ:向硝酸酸化的 溶液(pH≈2)中加入过量铁粉,搅拌后静置,不
同时间取上层清液滴加 KSCN 溶液,3min时溶液呈浅红色,30min后溶液几
乎无色。
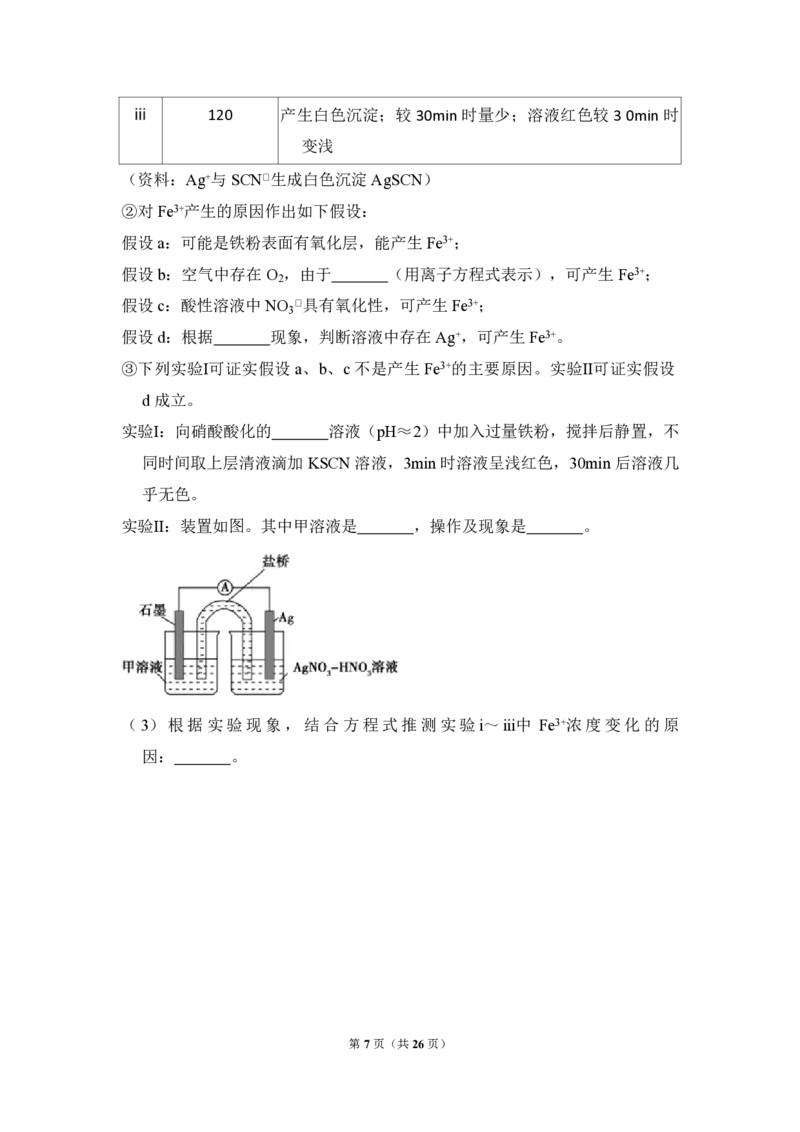
实验Ⅱ:装置如图。其中甲溶液是 ,操作及现象是 。
(3)根据实验现象,结合方程式推测实验ⅰ~ⅲ中 Fe3+浓度变化的原
因: 。
第7页(共26页)2017 年北京市高考化学试卷
参考答案与试题解析
一、本部分共 7小题,每小题 6分,共 42分.在每小题列出的四个选项中,
选出最符合题目要求的一项.
1.(6分)古丝绸之路贸易中的下列商品,主要成分属于无机物的是( )
A. 瓷器 B. 丝绸
C. 茶叶 D. 中草药
【考点】3B:无机化合物与有机化合物的概念.
菁优网版权所有
【专题】512:物质的分类专题.
【分析】含有碳元素的化合物为有机物,有机物大多数能够燃烧,且多数难溶
于水;无机物指的是不含碳元素的化合物,无机物多数不能燃烧,据此分
析.
【解答】解:A、瓷器是硅酸盐产品,不含碳元素,不是有机物,是无机物,
故A 正确;
B、丝绸的主要成分是蛋白质,是有机物,故B错误;
C、茶叶的主要成分是纤维素,是有机物,故C错误;
D、中草药的主要成分是纤维素,是有机物,故D 错误。
故选:A。
【点评】本题依托有机物和无机物的概念考查了化学知识与生活中物质的联
系,难度不大,应注意有机物中一定含碳元素,但含碳元素的却不一定是有
第8页(共26页)机物.
2.(6分)2016年 IUPAC 命名 117号元素为 Ts(中文名“ ”,tián),Ts
的原子核外最外层电子数是 7,下列说法不正确的是( )
A.Ts是第七周期第ⅦA 族元素
B.Ts 的同位素原子具有相同的电子数
C.Ts 在同族元素中非金属性最弱
D.中子数为176的Ts核素符号是 Ts
【考点】8G:原子结构与元素的性质.
菁优网版权所有
【专题】51C:元素周期律与元素周期表专题.
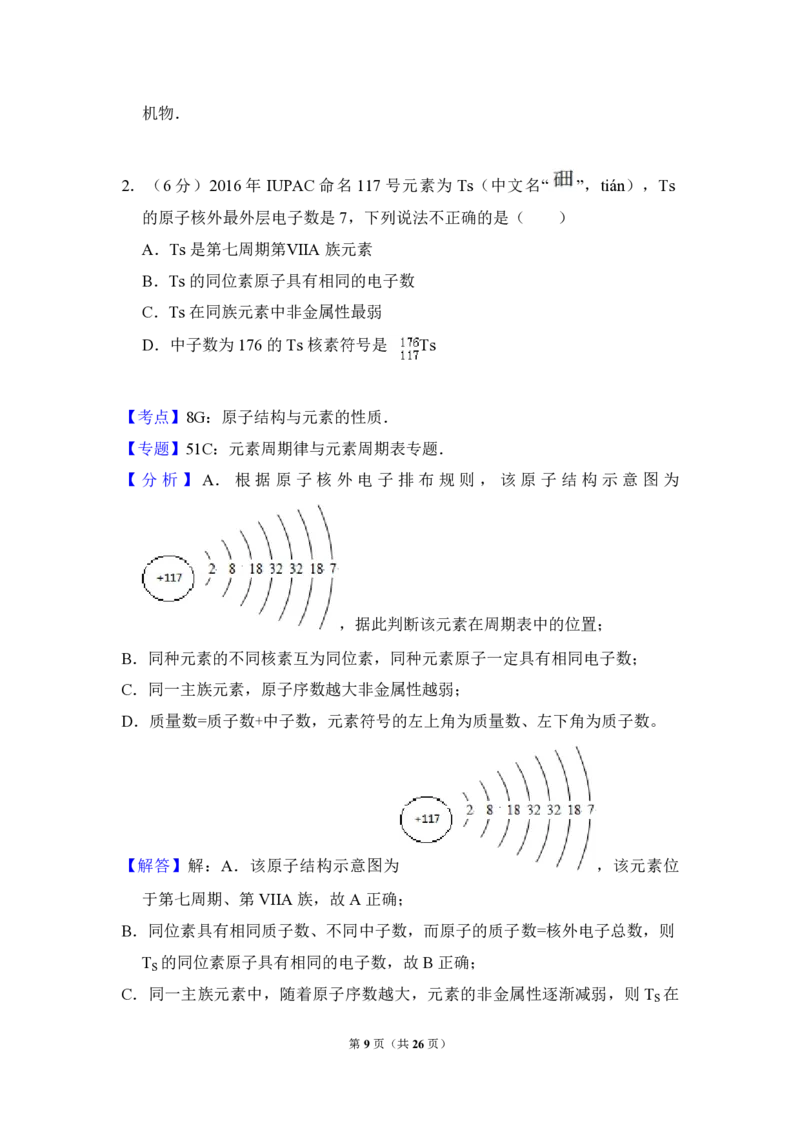
【 分 析 】 A. 根 据 原 子 核 外 电 子 排 布 规 则 , 该 原 子 结 构 示 意 图 为
,据此判断该元素在周期表中的位置;
B.同种元素的不同核素互为同位素,同种元素原子一定具有相同电子数;
C.同一主族元素,原子序数越大非金属性越弱;
D.质量数=质子数+中子数,元素符号的左上角为质量数、左下角为质子数。
【解答】解:A.该原子结构示意图为 ,该元素位
于第七周期、第VIIA 族,故 A 正确;
B.同位素具有相同质子数、不同中子数,而原子的质子数=核外电子总数,则
T 的同位素原子具有相同的电子数,故 B正确;
S
C.同一主族元素中,随着原子序数越大,元素的非金属性逐渐减弱,则 T 在
S
第9页(共26页)同族元素中非金属性最弱,故C正确;
D.该元素的质量数=质子数+中子数=176+117=293,该原子正确的表示方法
为: 293Ts,故D 错误;
117
故选:D。
【点评】本题考查原子结构与元素性质,题目难度不大,明确原子结构与元素
周期律的关系为解答关键,注意掌握原子构成及表示方法,试题培养了学生
的分析能力及灵活应用能力。
3.(6分)下列变化中,气体被还原的是( )
A.二氧化碳使Na O 固体变白
2 2
B.氯气使 KBr 溶液变黄
C.乙烯使 Br 的四氯化碳溶液褪色
2
D.氨气使AlCl 溶液产生白色沉淀
3
【考点】B1:氧化还原反应.
菁优网版权所有
【专题】515:氧化还原反应专题.
【分析】A.过氧化钠与二氧化碳的反应中,二氧化碳既不是氧化剂又不是还
原剂;
B.氯气将溴离子氧化成溴单质;
C.溴的化合价从0变为﹣1,做氧化剂,则乙烯被氧化;
D.氨气与氯化铝溶液反应生成氢氧化铝沉淀和氯化铵,该反应不属于氧化还
原反应.
【解答】解:A.二氧化碳与淡黄色的 Na O 反应生成白色的碳酸钠,该反应
2 2
中 Na O 既是氧化剂又是还原剂,二氧化碳不是氧化剂和还原剂,故 A 错
2 2
误;
B.氯气使 KBr 溶液变黄,该反应中氯气做氧化剂,反应中被还原,故 B正
确;
C.乙烯与溴的反应中,溴做氧化剂,乙烯被氧化,故C错误;
D.氨气与AlCl 溶液的反应不是氧化还原反应,故D 错误;
3
第10页(共26页)故选:B。
【点评】本题考查氧化还原反应的应用,题目难度不大,明确氧化还原反应的
实质为解答关键,注意掌握氧化反应与还原反应的区别,试题侧重基础知识
的考查,培养了学生的灵活应用能力.
4.(6 分)我国在 CO 催化加氢制取汽油方面取得突破性进展,CO 转化过程
2 2
示意图如下:下列说法不正确的是( )
A.反应①的产物中含有水
B.反应②中只有碳碳键形成
C.汽油主要是C ~C 的烃类混合物
5 11
D.图中a的名称是2﹣甲基丁烷
【考点】FG:碳族元素简介.
菁优网版权所有
【专题】525:碳族元素.
【分析】A.从质量守恒的角度判断,二氧化碳和氢气反应,生成物中应含有
氢;
B.反应②生成烃类物质,含有C﹣C键、C﹣H 键;
C.汽油所含烃类物质常温下为液态,易挥发;
D.图中a烃含有5个C,且有一个甲基.
【解答】解:A.从质量守恒的角度判断,二氧化碳和氢气反应,反应为
CO +H =CO+H O,则产物中含有水,故 A 正确;
2 2 2
B.反应②生成烃类物质,含有C﹣C键、C﹣H 键,故B错误;
C.汽油所含烃类物质常温下为液态,易挥发,主要是 C ~C 的烃类混合物,
5 11
故C正确;
D.图中a烃含有5个C,且有一个甲基,应为2﹣甲基丁烷,故D 正确。
第11页(共26页)故选:B。
【点评】本题综合考查碳循环知识,为高频考点,侧重考查学生的分析能力,
本题注意把握化学反应的特点,把握物质的组成以及有机物的结构和命名,
难度不大.
5.(6分)根据SO 通入不同溶液中实验现象,所得结论不正确的是( )
2
实验 现象 结论
A 含HCl、BaCl 的FeCl 溶液 产生白色沉淀 SO 有还原性
2 3 2
B H S 溶液 产生黄色沉淀 SO 有氧化性
2 2
C 酸性KMnO 溶液 紫色溶液褪色 SO 有漂白性
4 2
D Na SiO 溶液 产生胶状沉淀 酸性:H SO >H SiO
2 3 2 3 2 3
A.A B.B C.C D.D
【考点】F5:二氧化硫的化学性质;FH:硅和二氧化硅.
菁优网版权所有
【专题】523:氧族元素.
【分析】A.铁离子能够将二氧化硫氧化成硫酸,生成的白色沉淀为硫酸钡,
二氧化硫被氧化;
B.黄色沉淀为S 单质,结合化合价变化分析;
C.酸性高锰酸钾溶液具有强氧化性,能够氧化二氧化硫;
D.生成的胶状沉淀为H SiO ,根据强酸制取弱酸原理分析.
2 3
【解答】解:A.FeCl 将 SO 氧化成硫酸根离子,硫酸根离子与 BaCl 反应生
3 2 2
成硫酸钡沉淀,该反应中二氧化硫被氧化,表现了还原性,故 A 正确;
B.SO 与 H S 反应生成 S 单质,该反应中 SO 中+4价 S 元素被还原生成 0价
2 2 2
的单质S,二氧化硫被还原,做氧化剂,故B正确;
C.酸性 KMnO 溶液能够氧化 SO ,导致溶液褪色,SO 表现了还原性,故 C
4 2 2
错误;
D.Na SiO 溶液中通入二氧化硫生成 H SiO ,说明亚硫酸的酸性较强,即酸
2 3 2 3
性:H SO >H SiO ,故D 正确;
2 3 2 3
故选:C。
第12页(共26页)【点评】本题考查二氧化硫的性质,题目难度中等,明确常见元素及其化合物
性质为解答关键,注意掌握二氧化硫的化学性质,试题有利于提高学生的分
析、理解能力及综合应用能力.
6.(6 分)聚维酮碘的水溶液是一种常见的碘伏类缓释消毒剂,聚维酮通过氢
键与 HI 形成聚维酮碘,其结构表示如下
3
(图中虚线表示氢键)
下列说法不正确的是( )
A.聚维酮的单体是
B.聚维酮分子由(m+n)个单体聚合而成
C.聚维酮碘是一种水溶性物质
D.聚维酮在一定条件下能发生水解反应
【考点】L1:有机高分子化合物的结构和性质.
菁优网版权所有
【专题】53:有机化学基础.
【分析】由高聚物结构简式可知 的单
体为 ,高聚物可与 HI 形成氢键,则也可与水形成氢键,可溶于
3
水,含有肽键,可发生水解,以此解答该题.
第13页(共26页)【解答】解:A.由高聚物结构简式可知聚维酮的单体是 ,故 A 正
确;
B. 由 2m+n个单体加聚生成,故 B错
误;
C.高聚物可与HI 形成氢键,则也可与水形成氢键,可溶于水,故C 正确;
3
D.含有肽键,具有多肽化合物的性质,可发生水解生成氨基和羧基,故 D 正
确。
故选:B。
【点评】本题为 2017年北京考题,侧重考查有机物的结构和性质,涉及高聚物
单体以及性质的判断,注意把握氢键以及官能团的性质,题目有利于培养学
生的分析能力,难度不大.
7.(6分)下述实验中均有红棕色气体产生,对比分析所得结论不正确的是
( )
① ② ③
A.由①中的红棕色气体,推断产生的气体一定是混合气体
B.红棕色气体不能表明②中木炭与浓硝酸产生了反应
C.由③说明浓硝酸具有挥发性,生成的红棕色气体为还原产物
D.③的气体产物中检测出CO ,由此说明木炭一定与浓硝酸发生了反应
2
【考点】EG:硝酸的化学性质.
菁优网版权所有
第14页(共26页)【专题】524:氮族元素.
【分析】题中涉及实验都在加热条件下,浓硝酸不稳定,加热分解生成的二氧
化氮气体为红棕色,且加热条件下,浓硝酸可与碳发生氧化还原反应,以此
解答该题。
【解答】解:A.加热条件下,浓硝酸分解生成二氧化氮和氧气,则产生的气
体一定是混合气体,故 A 正确;
B.在加热条件下,浓硝酸可分解生成二氧化氮,不一定与碳反应生成,故 B
正确;
C.硝酸中 N 元素化合价为+5价,生成二氧化氮的 N 元素化合价为+4价,化
合价降低,在生成的红棕色气体为还原产物,故 C正确;
D.碳加热至红热,可与空气中氧气反应生成二氧化碳,不一定是与浓硝酸发
生了反应,故D 错误。
故选:D。
【点评】本题为 2017年北京考题,考查浓硝酸的性质,侧重考查学生的分析能
力和元素化合物知识的综合理解和运用,注意把握物质的性质以及实验的严
密性和可行性的评价,难度不大。
二、解答题(共 4小题,满分 58分)
8.(17分)羟甲香豆素是一种治疗胆结石的药物,合成路线如下图所示:
已知:
RCOOR'+R''OH RCOOR''+R'OH(R、R'、R''代表烃基)
(1)A 属于芳香烃,其结构简式是 。B中所含的官能团是 硝
第15页(共26页)基 。
(2)C→D 的反应类型是 取代反应 。
(3)E属于酯类。仅以乙醇为有机原料,选用必要的无机试剂合成 E,写出有
关化学方程式: CH COOH+CH CH OH CH COOCH CH +H O 。
3 3 2 3 2 3 2
(4)已知:2E F+C H OH.F 所含官能团有 和 。
2 5
(5)以 D 和 F 为原料合成羟甲香豆素分为三步反应,写出有关化合物的结构
简式:
【考点】HC:有机物的合成.
菁优网版权所有
【专题】534:有机物的化学性质及推断.
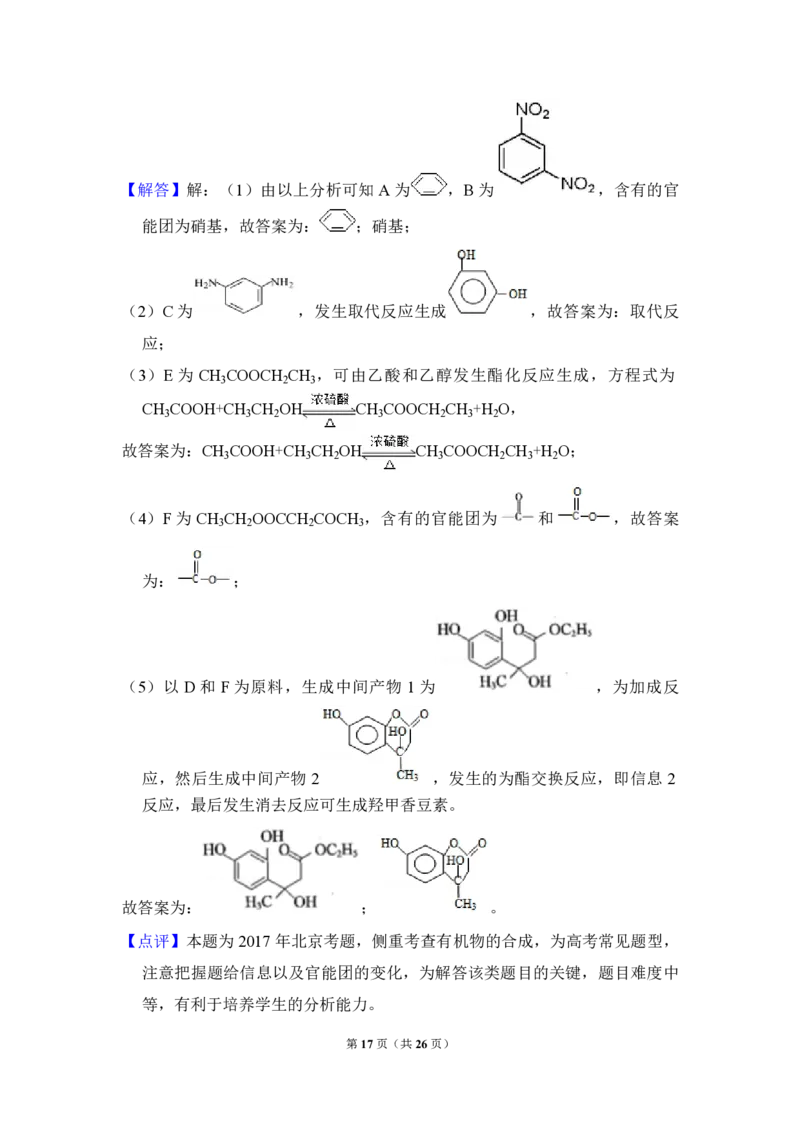
【分析】由羟甲香豆素结构简式可知 D 为 ,则 C为
, B 为 , 则 A 为 , 由 题 中 ( 3) 信 息 可 知 E为
CH COOCH CH ,由(4)可知 F 为 CH CH OOCCH COCH ,以此解答
3 2 3 3 2 2 3
(1)~(4);
(5)以 D 和 F 为原料,生成中间产物 1为 ,为加成反
应,然后生成中间产物 2为 ,发生的为酯交换反应,即信息
2反应,最后发生消去反应可生成羟甲香豆素,以此解答该题。
第16页(共26页)【解答】解:(1)由以上分析可知 A 为 ,B为 ,含有的官
能团为硝基,故答案为: ;硝基;
(2)C为 ,发生取代反应生成 ,故答案为:取代反
应;
(3)E为 CH COOCH CH ,可由乙酸和乙醇发生酯化反应生成,方程式为
3 2 3
CH COOH+CH CH OH CH COOCH CH +H O,
3 3 2 3 2 3 2
故答案为:CH COOH+CH CH OH CH COOCH CH +H O;
3 3 2 3 2 3 2
(4)F 为 CH CH OOCCH COCH ,含有的官能团为 和 ,故答案
3 2 2 3
为: ;
(5)以 D 和 F 为原料,生成中间产物 1为 ,为加成反
应,然后生成中间产物 2 ,发生的为酯交换反应,即信息 2
反应,最后发生消去反应可生成羟甲香豆素。
故答案为: ; 。
【点评】本题为 2017年北京考题,侧重考查有机物的合成,为高考常见题型,
注意把握题给信息以及官能团的变化,为解答该类题目的关键,题目难度中
等,有利于培养学生的分析能力。
第17页(共26页)9.(13分)TiCl 是由钛精矿(主要成分为 TiO )制备钛(Ti)的重要中间产
4 2
物,制备纯TiCl 的流程示意图如下:
4
资料:TiCl 及所含杂质氯化物的性质
4
化合物 SiCl TiCl AlCl FeCl MgCl
4 4 3 3 2
沸点/℃ 58 136 181(升华) 316 1412
熔点/℃ ﹣69 25 193 304 714
在 TiCl 中的溶解 互溶 ﹣ 微溶 难溶
4
性
(1)氯化过程:TiO 与 Cl 难以直接反应,加碳生成 CO 和 CO 可使反应得以
2 2 2
进行。
已知:TiO (s)+2Cl (g)=TiCl (g)+O (g)△H =+175.4kJ•mol﹣1
2 2 4 2 1
2C(s)+O (g)=2CO(g)△H =﹣220.9kJ•mol﹣1
2 2
①沸腾炉中加碳氯化生成 TiCl (g)和 CO(g)的热化学方程式: TiO (s)
4 2
+2Cl (g)+2C(s)=TiCl (g)+2CO(g)△H=﹣45.5kJ•mol﹣1 。
2 4
②氯化过程中 CO 和 CO 可以相互转化,根据如图判断:CO 生成 CO 反应的
2 2
△H > 0(填“>”“<”或“=”),判断依据: 温度越高,CO 的物质的量
越多而CO 的物质的量少,说明 CO 生成CO 的反应是吸热反应 。
2 2
③氯化反应的尾气须处理后排放,尾气中的 HCl和 Cl 经吸收可得粗盐酸、
2
FeCl 溶液,则尾气的吸收液依次是 饱和食盐水、氯化亚铁溶液 。
3
④氯化产物冷却至室温,经过滤得到粗 TiCl 混合液,则滤渣中含有 MgCl 、
4 2
第18页(共26页)FeCl 、AlCl 。
3 3
(2)精制过程:粗TiCl 经两步蒸馏得纯TiCl .示意图如下:
4 4
物质a是 SiCl ,T 应控制在 136℃左右 。
4 2
【考点】U3:制备实验方案的设计.
菁优网版权所有
【专题】546:无机实验综合.
【分析】由制备纯 TiCl 的流程示意图,钛精矿与氯气、C发生氯化过程,反应
4
为 TiO +2Cl +2C TiCl +2CO,结合表格中数据可知,蒸馏得到纯
2 2 4
TiCl ,
4
(1)①由I.TiO (s)+2Cl (g)=TiCl (g)+O (g)△H =+175.4kJ•mol﹣1
2 2 4 2 1
II.2C(s)+O (g)=2CO(g)△H =﹣220.9kJ•mol﹣1,
2 2
结合盖斯定律可知,I+II得到 TiO (s)+2Cl (g)+2C(s)=TiCl (g)+2CO
2 2 4
(g);
②氯化过程中 CO 和 CO 可以相互转化,温度高时 CO 的物质的量多、CO 的
2 2
物质的量少;
③尾气中的 HCl 和 Cl 经吸收可得粗盐酸、FeCl 溶液,食盐水吸收 HCl,氯化
2 3
亚铁吸收氯气;
④过滤得到粗TiCl 混合液,可能混有反应物中固体物质;
4
(2)粗 TiCl 经两步蒸馏得纯 TiCl ,由图及表格数据可知,先分离出 SiCl ,
4 4 4
后分离出TiCl 。
4
【解答】解:由制备纯 TiCl 的流程示意图,钛精矿与氯气、C发生氯化过程,
4
反应为 TiO +2Cl +2C TiCl +2CO,结合表格中数据可知,蒸馏得到纯
2 2 4
TiCl ,
4
(1)①由I.TiO (s)+2Cl (g)=TiCl (g)+O (g)△H =+175.4kJ•mol﹣1
2 2 4 2 1
第19页(共26页)II.2C(s)+O (g)=2CO(g)△H =﹣220.9kJ•mol﹣1,
2 2
结合盖斯定律可知,I+II得到 TiO (s)+2Cl (g)+2C(s)=TiCl (g)+2CO
2 2 4
(g),△H=(+175.4kJ•mol﹣1)+(﹣220.9kJ•mol﹣1)=﹣45.5kJ•mol﹣1,
即热化学方程式为 TiO (s)+2Cl (g)+2C(s)=TiCl (g)+2CO(g)△
2 2 4
H=﹣45.5kJ•mol﹣1,
故 答 案 为 : TiO ( s) +2Cl ( g) +2C( s) =TiCl ( g) +2CO( g) △
2 2 4
H=﹣45.5kJ•mol﹣1;
②因温度越高,CO 的物质的量越多而 CO 的物质的量少,说明 CO 生成 CO
2 2
的反应是吸热反应,所以△H>0,
故答案为:>;温度越高,CO 的物质的量越多而 CO 的物质的量少,说明
2
CO 生成CO 的反应是吸热反应;
2
③尾气中的 HCl 和 Cl 经吸收可得粗盐酸、FeCl 溶液,食盐水吸收 HCl,氯化
2 3
亚铁吸收氯气生成氯化铁,则尾气的吸收液依次是饱和食盐水、氯化亚铁溶
液,
故答案为:饱和食盐水、氯化亚铁溶液;
④由反应可知,氯化产物冷却至室温,经过滤得到粗 TiCl 混合液,结合表格中
4
氯化物的性质可知滤渣中含有 MgCl 、FeCl 、AlCl ,
2 3 3
故答案为:MgCl 、AlCl 、FeCl ;
2 3 3
(2)粗 TiCl 经两步蒸馏得纯 TiCl ,由图及表格数据可知,先分离出 SiCl ,
4 4 4
后分离出 TiCl ,则先控制温度 T 为 58℃左右时分离出物质 a为 SiCl ,控
4 1 4
制温度T 为136℃左右时分离出纯 TiCl ,故答案为:SiCl ;136℃左右。
2 4 4
【点评】本题考查物质的制备实验,为高频考点,把握流程中发生的反应、混
合物分离提纯、发生的反应为解答的关键,侧重分析与实验能力的考查,注
意反应原理与实验的结合,题目难度不大。
10.(12分)SCR 和 NSR 技术可有效降低柴油发动机在空气过量条件下的
NO 排放。
x
(1)SCR(选择性催化还原)工作原理:
第20页(共26页)①尿素[CO(NH ) ]水溶液热分解为 NH 和 CO ,该反应的化学方程式:
2 2 3 2
CO(NH ) +H O 2NH ↑+CO ↑ 。
2 2 2 3 2
② 反 应 器 中 NH 还 原 NO 的 化 学 方 程 式 : 8NH +6NO
3 2 3 2
7N +12H O 。
2 2
③当燃油中含硫量较高时,尾气中 SO 在 O 作用下会形成(NH ) SO ,使催
2 2 4 2 4
化剂中毒。用化学方程式表示(NH ) SO 的形成: 2SO +O +4NH +2H O
4 2 4 2 2 3 2
═2(NH ) SO 。
4 2 4
④尿素溶液浓度影响 NO 的转化,测定溶液中尿素(M=60g•mol﹣1)含量的方
2
法如下:取 a g尿素溶液,将所含氮完全转化为 NH ,所得 NH 用过量的 v
3 3 1
mL c mol•L﹣1H SO 溶液吸收完全,剩余 H SO 用 v mL c mol•L﹣1NaOH 溶
1 2 4 2 4 2 2
液恰好中和,则尿素溶液中溶质的质量分数是 。
(2)NSR(NO 储存还原)工作原理:
x
NO 的储存和还原在不同时段交替进行,如图a所示。
x
①通过 BaO 和 Ba(NO ) 的相互转化实现 NO 的储存和还原。储存 NO 的物
3 2 x x
质是 BaO 。
②用 H 模拟尾气中还原性气体研究了 Ba(NO ) 的催化还原过程,该过程分
2 3 2
两步进行,图 b表示该过程相关物质浓度随时间的变化关系。第一步反应消
耗的H 与Ba(NO ) 的物质的量之比是 8:1 。
2 3 2
③还原过程中,有时会产生笑气(N O)。用同位素示踪法研究发现笑气的产
2
第21页(共26页)生与 NO 有关。在有氧条件下,15NO 与 NH 以一定比例反应时,得到的笑
3
气几乎都是 15NNO.将该反应的化学方程式补充完整: 415NO+4NH +3O
3 2
4 15NNO+ 6 H O。
2
【考点】5A:化学方程式的有关计算;EK:氮的氧化物的性质及其对环境的影
响;FE:"三废"处理与环境保护.
菁优网版权所有
【专题】52:元素及其化合物;559:利用化学方程式的计算.
【分析】(1)①尿素[CO(NH ) ]水溶液热分解为 NH 和 CO ,结合原子守
2 2 3 2
恒配平书写化学方程式;
②反应器中 NH 还原 NO 生成氮气和水,根据电子守恒和原子守恒可得此反应
3 2
的化学方程式;
③SO 在 O 作用下与 NH 、H O 反应形成(NH ) SO ,此反应中 SO 是还原
2 2 3 2 4 2 4 2
剂,氧气是氧化剂,结合电子守恒和原子守恒可得此反应的化学方程式;
④涉及反应为 2NH +H SO =n(NH ) SO ,2NaOH+H SO =Na SO +H O,由
3 2 4 4 2 4 2 4 2 4 2
方程式可知n(NaOH)+n(NH )=2n(H SO ),以此计算;
3 2 4
(2)①由图a可知储存 NO 的物质是BaO;
x
②第一步反应中 H 被氧化生成水,化合价由 0价升高到+1价,Ba(NO ) 的
2 3 2
N 元素化合价由+5价降低到﹣3价,生成氨气,结合得失电子数目相等计
算;
③在有氧条件下 15NO 与 NH 以一定比例反应时,得到的笑气几乎都是
3
15NNO,由 N 元素守恒可知 15NO 与 NH 应为 1:1,结合电子得失相等配
3
平.
【解答】解:(1)①尿素[CO(NH ) ]水溶液热分解为 NH 和 CO ,反应物
2 2 3 2
为尿素和水,反应生成物为氨气和水,原子守恒书写化学方程式为:CO
(NH ) +H O 2NH ↑+CO ↑,
2 2 2 3 2
故答案为:CO(NH ) +H O 2NH ↑+CO ↑;
2 2 2 3 2
②NH 在催化剂作用下还原 NO 生成氮气和水,反应的化学方程式为
3 2
8NH +6NO 7N +12H O,
3 2 2 2
第22页(共26页)故答案为:8NH +6NO 7N +12H O;
3 2 2 2
③SO 在 O 作用下与 NH 、H O 反应形成(NH ) SO ,此反应中 SO 是还原
2 2 3 2 4 2 4 2
剂,氧气是氧化剂,反应的化学方程式为 2SO +O +4NH +2H O═2(NH )
2 2 3 2 4
SO ,
2 4
故答案为:2SO +O +4NH +2H O═2(NH ) SO ;
2 2 3 2 4 2 4
④涉及反应为 2NH +H SO =n(NH ) SO ,2NaOH+H SO =Na SO +H O,反
3 2 4 4 2 4 2 4 2 4 2
应中n(H SO )=v ×c ×10﹣3mol,n(NaOH)=v ×c ×10﹣3mol,
2 4 1 1 2 2
由方程式可知n(NaOH)+n(NH )=2n(H SO ),
3 2 4
则n(NH )=(2v ×c ×10﹣3﹣v ×c ×10﹣3)mol,
3 1 1 2 2
则 m(CO(NH ) )= ×(2v ×c ×10﹣3﹣v ×c ×10﹣3)mol×60g/mol=
2 2 1 1 2 2
(0.06v c ﹣0.03v c )g,
1 1 2 2
尿素溶液中溶质的质量分数是 = ,
故答案为: ;
(2)①由图示可知 BaO 和 NO 反应生成 Ba(NO ) ,Ba(NO ) 再还原为
x 3 2 3 2
N ,则储存NO 的物质为 BaO,故答案为:BaO;
2 x
②第一步反应中 H 被氧化生成水,化合价由 0价升高到+1价,Ba(NO ) 的
2 3 2
N 元素化合价由+5价降低到﹣3价,生成氨气,则 1molBa(NO ) 生成氨
3 2
气转移 16mol电子,参加反应的氢气的物质的量为 =8mol,则消耗的 H
2
与Ba(NO ) 的物质的量之比是 8:1,
3 2
故答案为:8:1;
③在有氧条件下 15NO 与 NH 以一定比例反应时,得到的笑气几乎都是
3
15NNO,由 N 元素守恒可知 15NO 与 NH 应为 1:1,可知反应的化学方程式
3
为415NO+4NH +3O 415NNO+6H O,
3 2 2
故答案为:415NO+4NH +3O ;4;6.
3 2
【点评】本题为 2017北京考题,题目以氮氧化物为载体考查元素化合物知识以
及化学方程式的相关计算,侧重于学生的分析能力和计算能力的考查,题目
难度中等,注意把握题给信息,结合质量守恒计算该题.
第23页(共26页)11.(16分)某小组在验证反应“Fe+2Ag+=Fe2++2Ag”的实验中检测到 Fe3+,发
现和探究过程如下。
向硝酸酸化的 0.05mol•L﹣1硝酸银溶液(pH≈2)中加入过量铁粉,搅拌后静
置,烧杯底部有黑色固体,溶液呈黄色。
(1)检验产物
①取少量黑色固体,洗涤后, 加入足量稀盐酸(或稀硫酸)酸化,固体未完
全溶解 (填操作和现象),证明黑色固体中含有 Ag。
②取上层清液,滴加 K [Fe(CN) ]溶液,产生蓝色沉淀,说明溶液中含有
3 6
Fe2+ 。
(2)针对“溶液呈黄色”,甲认为溶液中有 Fe3+,乙认为铁粉过量时不可能有
Fe3+,乙依据的原理是 Fe+2Fe3+=3Fe2+ (用离子方程式表示)。针对两种
观点继续实验:
①取上层清液,滴加 KSCN 溶液,溶液变红,证实了甲的猜测。同时发现有白
色沉淀产生,且溶液颜色变浅、沉淀量多少与取样时间有关,对比实验记录
如下:
序号 取样时间/min 现象
ⅰ 3 产生大量白色沉淀;溶液呈红色
ⅱ 30 产生白色沉淀;较 3min 时量少;溶液红色较 3min
时加深
ⅲ 120 产生白色沉淀;较 30min 时量少;溶液红色较 3
0min 时变浅
(资料:Ag+与SCN﹣生成白色沉淀AgSCN)
②对Fe3+产生的原因作出如下假设:
假设a:可能是铁粉表面有氧化层,能产生 Fe3+;
假设 b:空气中存在 O ,由于 4Fe2++O +4H+=4Fe3++2H O (用离子方程式表
2 2 2
示),可产生Fe3+;
假设c:酸性溶液中NO ﹣具有氧化性,可产生Fe3+;
3
假设d:根据 白色沉淀 现象,判断溶液中存在Ag+,可产生Fe3+。
③下列实验Ⅰ可证实假设 a、b、c不是产生 Fe3+的主要原因。实验Ⅱ可证实假设
第24页(共26页)d成立。
实验Ⅰ:向硝酸酸化的 0.05mol•L﹣1NaNO 溶液(pH≈2)中加入过量铁粉,
3
搅拌后静置,不同时间取上层清液滴加 KSCN 溶液,3min时溶液呈浅红
色,30min后溶液几乎无色。
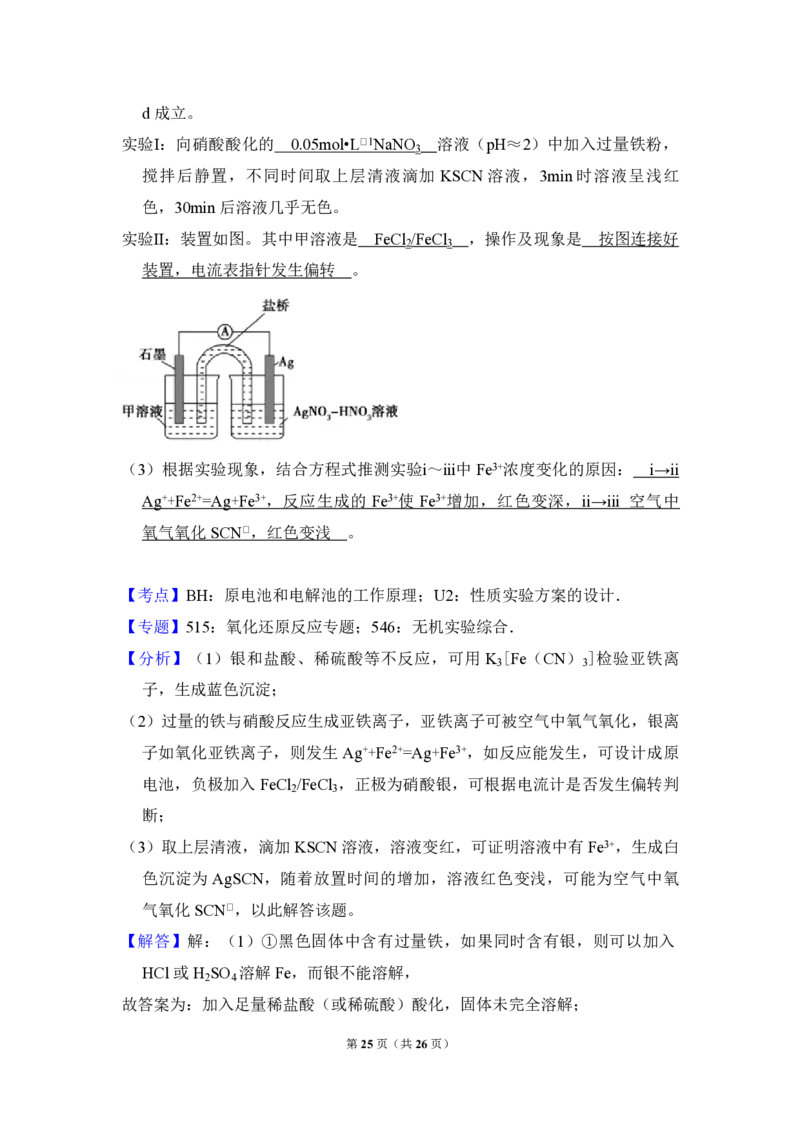
实验Ⅱ:装置如图。其中甲溶液是 FeCl /FeCl ,操作及现象是 按图连接好
2 3
装置,电流表指针发生偏转 。
(3)根据实验现象,结合方程式推测实验ⅰ~ⅲ中 Fe3+浓度变化的原因: i→ii
Ag++Fe2+=Ag+Fe3+,反应生成的 Fe3+使 Fe3+增加,红色变深,ii→iii 空气中
氧气氧化SCN﹣,红色变浅 。
【考点】BH:原电池和电解池的工作原理;U2:性质实验方案的设计.
菁优网版权所有
【专题】515:氧化还原反应专题;546:无机实验综合.
【分析】(1)银和盐酸、稀硫酸等不反应,可用 K [Fe(CN) ]检验亚铁离
3 3
子,生成蓝色沉淀;
(2)过量的铁与硝酸反应生成亚铁离子,亚铁离子可被空气中氧气氧化,银离
子如氧化亚铁离子,则发生 Ag++Fe2+=Ag+Fe3+,如反应能发生,可设计成原
电池,负极加入 FeCl /FeCl ,正极为硝酸银,可根据电流计是否发生偏转判
2 3
断;
(3)取上层清液,滴加 KSCN 溶液,溶液变红,可证明溶液中有 Fe3+,生成白
色沉淀为 AgSCN,随着放置时间的增加,溶液红色变浅,可能为空气中氧
气氧化SCN﹣,以此解答该题。
【解答】解:(1)①黑色固体中含有过量铁,如果同时含有银,则可以加入
HCl或 H SO 溶解Fe,而银不能溶解,
2 4
故答案为:加入足量稀盐酸(或稀硫酸)酸化,固体未完全溶解;
第25页(共26页)②K [Fe(CN) ]是检验Fe2+的试剂,所以产生蓝色沉淀说明含有Fe2+,
3 3
故答案为:Fe2+;
(2)过量铁粉与Fe3+反应生成Fe2+,即Fe+2Fe3+=3Fe2+,
故答案为:Fe+2Fe3+=3Fe2+;
②O 氧化 Fe2+反应为 4Fe2++O +4H+=4Fe3++2H O,白色沉淀是 AgSCN,所以实
2 2 2
验可以说明含有Ag+,Ag+可能氧化Fe2+生成Fe3+,
故答案为:4Fe2++O +4H+=4Fe3++2H O;白色沉淀;
2 2
③证明假设 abc错误,就是排除 Ag+时实验比较,相当于没有 Ag+存在的空白实
验,考虑其他条件不要变化,可以选用 0.05mol•L﹣1NaNO ,原电池实验需
3
要证明的是假设 d的反应 Ag++Fe2+=Ag+Fe3+能够实现,所以甲池应当注入
FeCl 、FeCl 混合溶液,按图连接好装置,如电流表指针发生偏转,可说明
2 3
d正确,
故答案为:0.05mol•L﹣1NaNO ;FeCl /FeCl ;按图连接好装置,电流表指针发
3 2 3
生偏转;
(3)i→iii 中 Fe3+变化的原因:i→ii Ag++Fe2+=Ag+Fe3+,反应生成的 Fe3+使 Fe3+
浓度增加,ii→iii 溶液红色较 3 0min时变浅,说明空气中氧气氧化 SCN﹣,
使平衡向生成 Fe3+的方向移动,Fe(SCN) 浓度减小,则溶液的颜色变
3
浅,
故答案为:i→ii Ag++Fe2+=Ag+Fe3+,反应生成的 Fe3+使 Fe3+增加,红色变深,
ii→iii 空气中氧气氧化 SCN﹣,红色变浅。
【点评】本题为 2017年北京考题,涉及物质的性质的探究,侧重于学生的分析
能力和实验能力的考查,注意把握物质的性质以及实验的严密性和可行性的
评价,难度中等。
第26页(共26页)