文档内容
2019 年普通高等学校招生全国统一考试·全国Ⅰ卷
理科综合(化学部分)
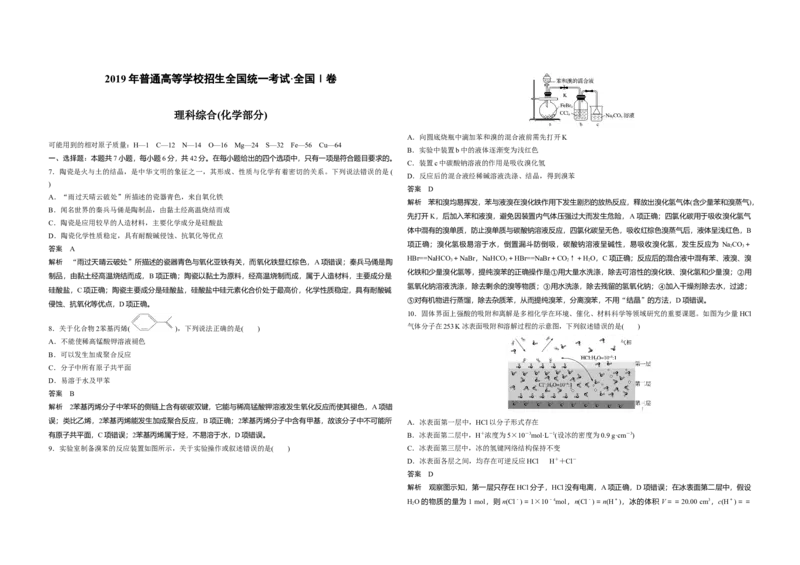
A.向圆底烧瓶中滴加苯和溴的混合液前需先打开K
可能用到的相对原子质量:H—1 C—12 N—14 O—16 Mg—24 S—32 Fe—56 Cu—64
B.实验中装置b中的液体逐渐变为浅红色
一、选择题:本题共7小题,每小题6分,共42分。在每小题给出的四个选项中,只有一项是符合题目要求的。
C.装置c中碳酸钠溶液的作用是吸收溴化氢
7.陶瓷是火与土的结晶,是中华文明的象征之一,其形成、性质与化学有着密切的关系。下列说法错误的是(
D.反应后的混合液经稀碱溶液洗涤、结晶,得到溴苯
)
答案 D
A.“雨过天晴云破处”所描述的瓷器青色,来自氧化铁
解析 苯和溴均易挥发,苯与液溴在溴化铁作用下发生剧烈的放热反应,释放出溴化氢气体(含少量苯和溴蒸气),
B.闻名世界的秦兵马俑是陶制品,由黏土经高温烧结而成
先打开K,后加入苯和液溴,避免因装置内气体压强过大而发生危险,A项正确;四氯化碳用于吸收溴化氢气
C.陶瓷是应用较早的人造材料,主要化学成分是硅酸盐
体中混有的溴单质,防止溴单质与碳酸钠溶液反应,四氯化碳呈无色,吸收红棕色溴蒸气后,液体呈浅红色,B
D.陶瓷化学性质稳定,具有耐酸碱侵蚀、抗氧化等优点
项正确;溴化氢极易溶于水,倒置漏斗防倒吸,碳酸钠溶液呈碱性,易吸收溴化氢,发生反应为 NaCO +
答案 A 2 3
HBr==NaHCO +NaBr,NaHCO +HBr==NaBr+CO↑+HO,C项正确;反应后的混合液中混有苯、液溴、溴
解析 “雨过天晴云破处”所描述的瓷器青色与氧化亚铁有关,而氧化铁显红棕色,A项错误;秦兵马俑是陶 3 3 2 2
化铁和少量溴化氢等,提纯溴苯的正确操作是①用大量水洗涤,除去可溶性的溴化铁、溴化氢和少量溴;②用
制品,由黏土经高温烧结而成,B项正确;陶瓷以黏土为原料,经高温烧制而成,属于人造材料,主要成分是
氢氧化钠溶液洗涤,除去剩余的溴等物质;③用水洗涤,除去残留的氢氧化钠;④加入干燥剂除去水,过滤;
硅酸盐,C项正确;陶瓷主要成分是硅酸盐,硅酸盐中硅元素化合价处于最高价,化学性质稳定,具有耐酸碱
⑤对有机物进行蒸馏,除去杂质苯,从而提纯溴苯,分离溴苯,不用“结晶”的方法,D项错误。
侵蚀、抗氧化等优点,D项正确。
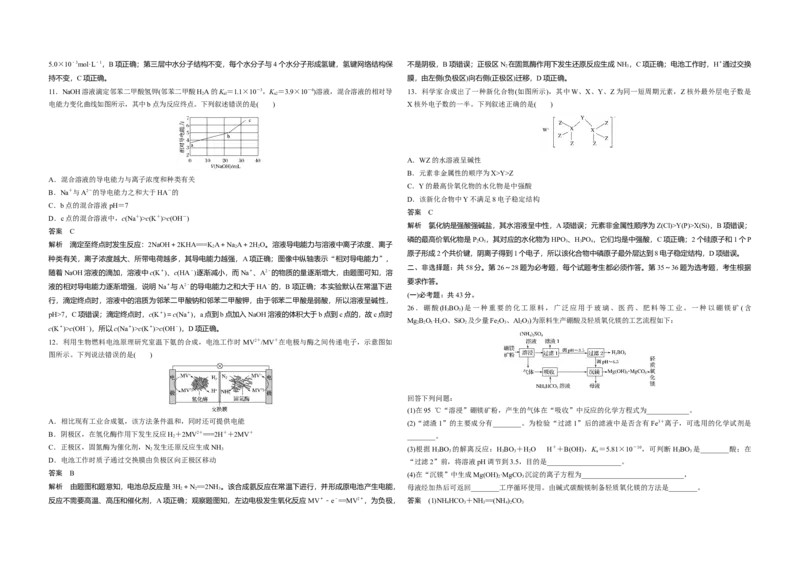
10.固体界面上强酸的吸附和离解是多相化学在环境、催化、材料科学等领域研究的重要课题。如图为少量HCl
8.关于化合物2苯基丙烯( ),下列说法正确的是( ) 气体分子在253 K冰表面吸附和溶解过程的示意图,下列叙述错误的是( )
A.不能使稀高锰酸钾溶液褪色
B.可以发生加成聚合反应
C.分子中所有原子共平面
D.易溶于水及甲苯
答案 B
解析 2苯基丙烯分子中苯环的侧链上含有碳碳双键,它能与稀高锰酸钾溶液发生氧化反应而使其褪色,A项错
误;类比乙烯,2苯基丙烯能发生加成聚合反应,B项正确;2苯基丙烯分子中含有甲基,故该分子中不可能所 A.冰表面第一层中,HCl以分子形式存在
有原子共平面,C项错误;2苯基丙烯属于烃,不易溶于水,D项错误。 B.冰表面第二层中,H+浓度为5×10-3mol·L-1(设冰的密度为0.9 g·cm-3)
9.实验室制备溴苯的反应装置如图所示,关于实验操作或叙述错误的是( ) C.冰表面第三层中,冰的氢键网络结构保持不变
D.冰表面各层之间,均存在可逆反应HClH++Cl-
答案 D
解析 观察图示知,第一层只存在HCl分子,HCl没有电离,A项正确,D项错误;在冰表面第二层中,假设
HO的物质的量为1 mol,则n(Cl-)=1×10-4mol,n(Cl-)=n(H+),冰的体积V==20.00 cm3,c(H+)==
25.0×10-3mol·L-1,B项正确;第三层中水分子结构不变,每个水分子与4个水分子形成氢键,氢键网络结构保 不是阴极,B项错误;正极区N 在固氮酶作用下发生还原反应生成NH ,C项正确;电池工作时,H+通过交换
2 3
持不变,C项正确。 膜,由左侧(负极区)向右侧(正极区)迁移,D项正确。
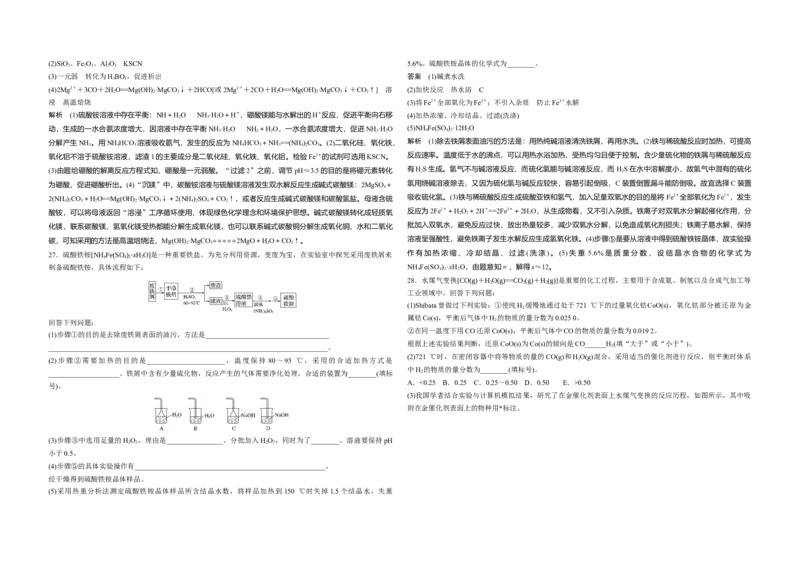
11.NaOH溶液滴定邻苯二甲酸氢钾(邻苯二甲酸HA的K =1.1×10-3,K =3.9×10-6)溶液,混合溶液的相对导 13.科学家合成出了一种新化合物(如图所示),其中W、X、Y、Z为同一短周期元素,Z核外最外层电子数是
2 al a2
电能力变化曲线如图所示,其中b点为反应终点。下列叙述错误的是( ) X核外电子数的一半。下列叙述正确的是( )
A.WZ的水溶液呈碱性
B.元素非金属性的顺序为X>Y>Z
A.混合溶液的导电能力与离子浓度和种类有关
C.Y的最高价氧化物的水化物是中强酸
B.Na+与A2-的导电能力之和大于HA-的
D.该新化合物中Y不满足8电子稳定结构
C.b点的混合溶液pH=7
答案 C
D.c点的混合溶液中,c(Na+)>c(K+)>c(OH-)
解析 氯化钠是强酸强碱盐,其水溶液呈中性,A项错误;元素非金属性顺序为Z(Cl)>Y(P)>X(Si),B项错误;
答案 C
磷的最高价氧化物是PO ,其对应的水化物为HPO 、HPO ,它们均是中强酸,C项正确;2个硅原子和1个P
解析 滴定至终点时发生反应:2NaOH+2KHA===KA+NaA+2HO。溶液导电能力与溶液中离子浓度、离子 2 5 3 3 4
2 2 2
原子形成2个共价键,阴离子得到1个电子,所以该化合物中磷原子最外层达到8电子稳定结构,D项错误。
种类有关,离子浓度越大、所带电荷越多,其导电能力越强,A项正确;图像中纵轴表示“相对导电能力”,
二、非选择题:共58分。第26~28题为必考题,每个试题考生都必须作答。第35~36题为选考题,考生根据
随着NaOH溶液的滴加,溶液中c(K+)、c(HA-)逐渐减小,而Na+、A2-的物质的量逐渐增大,由题图可知,溶
要求作答。
液的相对导电能力逐渐增强,说明Na+与A2-的导电能力之和大于HA-的,B项正确;本实验默认在常温下进
(一)必考题:共43分。
行,滴定终点时,溶液中的溶质为邻苯二甲酸钠和邻苯二甲酸钾,由于邻苯二甲酸是弱酸,所以溶液呈碱性,
26.硼酸(H BO)是一种重要的化工原料,广泛应用于玻璃、医药、肥料等工业。一种以硼镁矿(含
3 3
pH>7,C项错误;滴定终点时,c(K+)=c(Na+),a点到b点加入NaOH溶液的体积大于b点到c点的,故c点时
MgB O·H O、SiO 及少量Fe O、Al O)为原料生产硼酸及轻质氧化镁的工艺流程如下:
2 2 5 2 2 2 3 2 3
c(K+)>c(OH-),所以c(Na+)>c(K+)>c(OH-),D项正确。
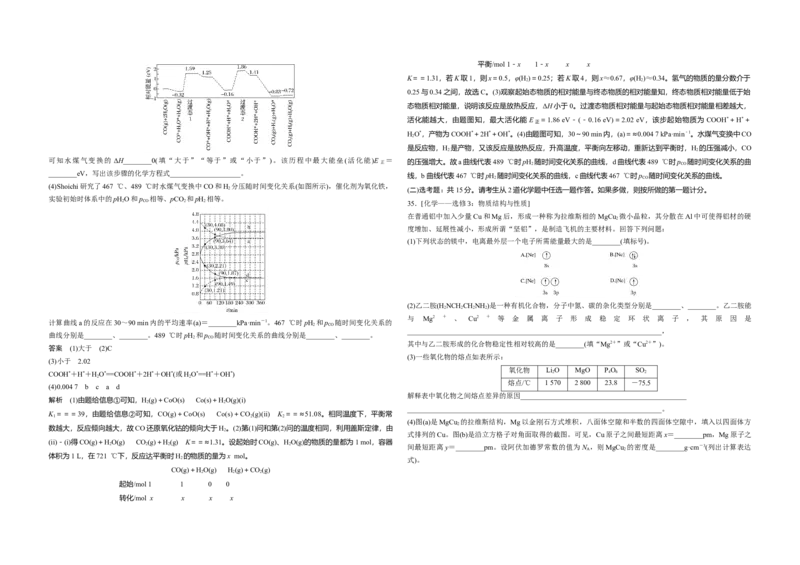
12.利用生物燃料电池原理研究室温下氨的合成,电池工作时 MV2+/MV+在电极与酶之间传递电子,示意图如
图所示。下列说法错误的是( )
回答下列问题:
(1)在95 ℃“溶浸”硼镁矿粉,产生的气体在“吸收”中反应的化学方程式为____________。
A.相比现有工业合成氨,该方法条件温和,同时还可提供电能 (2)“滤渣1”的主要成分有________。为检验“过滤1”后的滤液中是否含有Fe3+离子,可选用的化学试剂是
B.阴极区,在氢化酶作用下发生反应H 2 +2MV2+===2H++2MV+ ________。
C.正极区,固氮酶为催化剂,N 2 发生还原反应生成NH 3 (3)根据H 3 BO 3 的解离反应:H 3 BO 3 +H 2 OH++B(OH),K a =5.81×10-10,可判断H 3 BO 3 是________酸;在
D.电池工作时质子通过交换膜由负极区向正极区移动 “过滤2”前,将溶液pH调节到3.5,目的是_____________________。
答案 B (4)在“沉镁”中生成Mg(OH) ·MgCO 沉淀的离子方程为_____________________________,
2 3
解析 由题图和题意知,电池总反应是3H
2
+N
2
==2NH
3
。该合成氨反应在常温下进行,并形成原电池产生电能, 母液经加热后可返回________工序循环使用。由碱式碳酸镁制备轻质氧化镁的方法是________。
反应不需要高温、高压和催化剂,A项正确;观察题图知,左边电极发生氧化反应MV+-e-==MV2+,为负极, 答案 (1)NH HCO +NH ==(NH )CO
4 3 3 4 2 3(2)SiO、Fe O、Al O KSCN 5.6%。硫酸铁铵晶体的化学式为________。
2 2 3 2 3
(3)一元弱 转化为HBO,促进析出 答案 (1)碱煮水洗
3 3
(4)2Mg2++3CO+2HO==Mg(OH) ·MgCO ↓+2HCO[或2Mg2++2CO+HO==Mg(OH) ·MgCO ↓+CO↑] 溶 (2)加快反应 热水浴 C
2 2 3 2 2 3 2
浸 高温焙烧 (3)将Fe2+全部氧化为Fe3+;不引入杂质 防止Fe3+水解
解析 (1)硫酸铵溶液中存在平衡:NH+HONH ·H O+H+,硼酸镁能与水解出的H+反应,促进平衡向右移 (4)加热浓缩、冷却结晶、过滤(洗涤)
2 3 2
动,生成的一水合氨浓度增大,因溶液中存在平衡NH
3
·H
2
ONH
3
+H
2
O,一水合氨浓度增大,促进NH
3
·H
2
O (5)NH
4
Fe(SO
4
)
2
·12H
2
O
分解产生NH 。用NH HCO 溶液吸收氨气,发生的反应为NH HCO +NH ==(NH )CO 。(2)二氧化硅、氧化铁、 解析 (1)除去铁屑表面油污的方法是:用热纯碱溶液清洗铁屑,再用水洗。(2)铁与稀硫酸反应时加热,可提高
3 4 3 4 3 3 4 2 3
氧化铝不溶于硫酸铵溶液,滤渣1的主要成分是二氧化硅、氧化铁、氧化铝。检验Fe3+的试剂可选用KSCN。 反应速率。温度低于水的沸点,可以用热水浴加热,受热均匀且便于控制。含少量硫化物的铁屑与稀硫酸反应
(3)由题给硼酸的解离反应方程式知,硼酸是一元弱酸。“过滤2”之前,调节pH≈3.5的目的是将硼元素转化 有H 2 S生成。氢气不与碱溶液反应,而硫化氢能与碱溶液反应,而 H 2 S在水中溶解度小,故氢气中混有的硫化
为硼酸,促进硼酸析出。(4)“沉镁”中,碳酸铵溶液与硫酸镁溶液发生双水解反应生成碱式碳酸镁:2MgSO + 氢用烧碱溶液除去,又因为硫化氢与碱反应较快,容易引起倒吸,C装置倒置漏斗能防倒吸。故宜选择C装置
4
2(NH )CO +HO==Mg(OH) ·MgCO ↓+2(NH )SO +CO↑,或者反应生成碱式碳酸镁和碳酸氢盐。母液含硫 吸收硫化氢。(3)铁与稀硫酸反应生成硫酸亚铁和氢气,加入足量双氧水的目的是将 Fe2+全部氧化为Fe3+,发生
4 2 3 2 2 3 4 2 4 2
酸铵,可以将母液返回“溶浸”工序循环使用,体现绿色化学理念和环境保护思想。碱式碳酸镁转化成轻质氧 反应为2Fe2++H 2 O 2 +2H+==2Fe3++2H 2 O,从生成物看,又不引入杂质。铁离子对双氧水分解起催化作用,分
化镁,联系碳酸镁、氢氧化镁受热都能分解生成氧化镁,也可以联系碱式碳酸铜分解生成氧化铜、水和二氧化 批加入双氧水,避免反应过快、放出热量较多,减少双氧水分解,以免造成氧化剂损失;铁离子易水解,保持
碳,可知采用的方法是高温焙烧法,Mg(OH) ·MgCO =====2MgO+HO+CO↑。 溶液呈强酸性,避免铁离子发生水解反应生成氢氧化铁。(4)步骤⑤是要从溶液中得到硫酸铁铵晶体,故实验操
2 3 2 2
27.硫酸铁铵[NH Fe(SO )·xHO]是一种重要铁盐。为充分利用资源,变废为宝,在实验室中探究采用废铁屑来 作有加热浓缩、冷却结晶、过滤(洗涤)。(5)失重 5.6%是质量分数,设结晶水合物的化学式为
4 4 2 2
制备硫酸铁铵,具体流程如下: NH Fe(SO ) ·xH O,由题意知=,解得x≈12。
4 4 2 2
28.水煤气变换[CO(g)+HO(g)==CO(g)+H(g)]是重要的化工过程,主要用于合成氨、制氢以及合成气加工等
2 2 2
工业领域中。回答下列问题:
(1)Shibata曾做过下列实验:①使纯H 缓慢地通过处于721 ℃下的过量氧化钴CoO(s),氧化钴部分被还原为金
2
属钴Co(s),平衡后气体中H 的物质的量分数为0.025 0。
回答下列问题: 2
②在同一温度下用CO还原CoO(s),平衡后气体中CO的物质的量分数为0.019 2。
(1)步骤①的目的是去除废铁屑表面的油污,方法是___________________________________
根据上述实验结果判断,还原CoO(s)为Co(s)的倾向是CO______H (填“大于”或“小于”)。
_______________________________________________________________________________。 2
(2)721 ℃时,在密闭容器中将等物质的量的CO(g)和HO(g)混合,采用适当的催化剂进行反应,则平衡时体系
(2)步骤②需要加热的目的是______________________,温度保持 80~95 ℃,采用的合适加热方式是 2
中H 的物质的量分数为________(填标号)。
____________________。铁屑中含有少量硫化物,反应产生的气体需要净化处理,合适的装置为________(填标 2
A.<0.25 B.0.25 C.0.25~0.50 D.0.50 E.>0.50
号)。
(3)我国学者结合实验与计算机模拟结果,研究了在金催化剂表面上水煤气变换的反应历程,如图所示,其中吸
附在金催化剂表面上的物种用*标注。
(3)步骤③中选用足量的HO ,理由是________________。分批加入HO ,同时为了________,溶液要保持pH
2 2 2 2
小于0.5。
(4)步骤⑤的具体实验操作有______________________________________________________,
经干燥得到硫酸铁铵晶体样品。
(5)采用热重分析法测定硫酸铁铵晶体样品所含结晶水数,将样品加热到150 ℃时失掉1.5个结晶水,失重平衡/mol 1-x 1-x x x
K==1.31,若K取1,则x=0.5,φ(H )=0.25;若K取4,则x≈0.67,φ(H )≈0.34。氢气的物质的量分数介于
2 2
0.25与0.34之间,故选C。(3)观察起始态物质的相对能量与终态物质的相对能量知,终态物质相对能量低于始
态物质相对能量,说明该反应是放热反应,ΔH小于0。过渡态物质相对能量与起始态物质相对能量相差越大,
活化能越大,由题图知,最大活化能 E =1.86 eV-(-0.16 eV)=2.02 eV,该步起始物质为 COOH*+H*+
正
HO*,产物为COOH*+2H*+OH*。(4)由题图可知,30~90 min内,(a)=≈0.004 7 kPa·min-1。水煤气变换中CO
2
是反应物,H 是产物,又该反应是放热反应,升高温度,平衡向左移动,重新达到平衡时,H 的压强减小,CO
2 2
可知水煤气变换的 ΔH________0(填“大于”“等于”或“小于”)。该历程中最大能垒(活化能)E 正 = 的压强增大。故a曲线代表489 ℃时pH 2 随时间变化关系的曲线,d曲线代表489 ℃时p CO 随时间变化关系的曲
________eV,写出该步骤的化学方程式____________________。
线,b曲线代表467 ℃时pH 随时间变化关系的曲线,c曲线代表467 ℃时p 随时间变化关系的曲线。
2 CO
(4)Shoichi研究了467 ℃、489 ℃时水煤气变换中CO和H 分压随时间变化关系(如图所示),催化剂为氧化铁,
2 (二)选考题:共15分。请考生从2道化学题中任选一题作答。如果多做,则按所做的第一题计分。
实验初始时体系中的pHO和p 相等、pCO 和pH 相等。
2 CO 2 2 35.[化学——选修3:物质结构与性质]
在普通铝中加入少量Cu和Mg后,形成一种称为拉维斯相的MgCu 微小晶粒,其分散在Al中可使得铝材的硬
2
度增加、延展性减小,形成所谓“坚铝”,是制造飞机的主要材料。回答下列问题:
(1)下列状态的镁中,电离最外层一个电子所需能量最大的是________(填标号)。
(2)乙二胺(H NCH CHNH )是一种有机化合物,分子中氮、碳的杂化类型分别是________、________。乙二胺能
2 2 2 2
与 Mg2 + 、 Cu2 + 等 金 属 离 子 形 成 稳 定 环 状 离 子 , 其 原 因 是
计算曲线a的反应在30~90 min内的平均速率(a)=________kPa·min-1。467 ℃时pH 和p 随时间变化关系的
2 CO
________________________________________________________________________,
曲线分别是________、________。489 ℃时pH 和p 随时间变化关系的曲线分别是________、________。
2 CO
其中与乙二胺形成的化合物稳定性相对较高的是________(填“Mg2+”或“Cu2+”)。
答案 (1)大于 (2)C
(3)一些氧化物的熔点如表所示:
(3)小于 2.02
氧化物 LiO MgO PO SO
COOH*+H*+HO*==COOH*+2H*+OH*(或HO*==H*+OH*) 2 4 6 2
2 2
熔点/℃ 1 570 2 800 23.8 -75.5
(4)0.004 7 b c a d
解释表中氧化物之间熔点差异的原因_______________________________________________
解析 (1)由题给信息①可知,H(g)+CoO(s)Co(s)+HO(g)(i)
2 2
________________________________________________________________________。
K ===39,由题给信息②可知,CO(g)+CoO(s)Co(s)+CO (g)(ii) K ==≈51.08。相同温度下,平衡常
1 2 2
(4)图(a)是MgCu 的拉维斯结构,Mg以金刚石方式堆积,八面体空隙和半数的四面体空隙中,填入以四面体方
2
数越大,反应倾向越大,故CO还原氧化钴的倾向大于H 。(2)第(1)问和第(2)问的温度相同,利用盖斯定律,由
2
式排列的Cu。图(b)是沿立方格子对角面取得的截图。可见,Cu原子之间最短距离x=________pm,Mg原子之
(ii)-(i)得CO(g)+HO(g)CO(g)+H(g) K==≈1.31。设起始时CO(g)、HO(g)的物质的量都为1 mol,容器
2 2 2 2 间最短距离y=________pm。设阿伏加德罗常数的值为N ,则MgCu 的密度是________g·cm-3(列出计算表达
A 2
体积为1 L,在721 ℃下,反应达平衡时H 的物质的量为x mol。
2 式)。
CO(g)+HO(g)H(g)+CO(g)
2 2 2
起始/mol 1 1 0 0
转化/mol x x x x回答下列问题:
(1)A中的官能团名称是________。
(2)碳原子上连有4个不同的原子或基团时,该碳称为手性碳。写出B的结构简式,用星号(*)标出B中的手性碳
________。
答案 (1)A (2)sp3 sp3 乙二胺的两个N提供孤对电子与金属离子形成配位键 Cu2+ (3)写出具有六元环结构、并能发生银镜反应的B的同分异构体的结构简式________。(不考虑立体异构,只需写
(3)Li O、MgO为离子晶体,PO、SO 为分子晶体。晶格能:MgO>Li O。分子间作用力(分子量):PO>SO 出3个)
2 4 6 2 2 4 6 2
(4)a a (4)反应④所需的试剂和条件是___________________________________________________。
解析 (1)由题给信息知,A项和D项代表Mg+,B项和C项代表Mg。A项,Mg+再失去一个电子较难,即第 (5)⑤的反应类型是________。
二电离能大于第一电离能,所以电离最外层一个电子所需能量 A大于B;3p能级的能量高于3s,3p能级上电子 (6)写出F到G的反应方程式_______________________________________________________
________________________________________________________________________。
较3s上易失去,故电离最外层一个电子所需能量:A>C、A>D,选A。(2)乙二胺分子中,1个N原子形成3个
(7)设计由甲苯和乙酰乙酸乙酯(CHCOCH COOC H)制备OOOHC H 的合成路线________(无机试剂任选)。
单键,还有一个孤电子对,故N原子价层电子对数为4,N原子采取sp3杂化;1个C原子形成4个单键,没有 3 2 2 5 6 5
孤电子对,价层电子对数为4,采取sp3杂化。乙二胺中2个N原子提供孤电子对与金属镁离子或铜离子形成稳
定的配位键,故能形成稳定环状离子。由于铜离子半径大于镁离子,形成配位键时头碰头重叠程度较大,其与
答案 (1)羟基 (2)
乙二胺形成的化合物较稳定。(3)氧化锂、氧化镁是离子晶体,六氧化四磷和二氧化硫是分子晶体,离子键比分
子间作用力强。(4)观察图(a)和图(b)知,4个铜原子相切并与面对角线平行,有(4x)2=2a2,x=a。镁原子堆积方
式类似金刚石,有y=a。已知1 cm=1010 pm,晶胞体积为(a×10-10)3 cm3,代入密度公式计算即可。
36.[化学——选修5:有机化学基础]
(3) (任意写出其中3个即可)
化合物G是一种药物合成中间体,其合成路线如下:
(4)C HOH/浓HSO 、加热 (5)取代反应
2 5 2 4
――-----→ ――→ ――------→
(7)C HCH――→C HCHBr,CHCOCH COOC H―——————————―→
6 5 3 6 5 2 3 2 2 5
① ② ③
――--------→
解析 (1)A中的官能团为羟基。(2)根据手性碳原子的定义,B中CH 上没有手性碳, 上没有手性碳,
2
④ ⑤ ⑥
故B分子中只有2个手性碳原子。(3)B的同分异构体能发生银镜反应,说明含有醛基,所以可以看成环己烷分
子中2个氢原子分别被甲基、醛基取代,或一个氢原子被CHCHO取代。(4)反应④所需的试剂和条件是乙醇/浓
2
硫酸、加热。(5)反应⑤中,CHCHCHBr与E发生取代反应。(6)F在碱溶液中水解生成羧酸盐,再酸化得到
3 2 2
G。