文档内容
2022 年 1 月浙江省选考化学试题
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Na-23 Mg-24 Al-27
Si-28 S-32 Cl-35.5 K-39 Ca-40 Mn-55 Fe-56 Cu-64 Zn-65
Ba-137
一、选择题(本大题共25小题,每小题2分,共50分。每小题列出的四个备选项中只有一个
是符合题目要求的,不选、多选、错选均不得分)
1. 水溶液呈酸性的盐是
A. NH Cl B. BaCl C. HSO D. Ca(OH)
4 2 2 4 2
2. 下列物质属于非电解质的是
A. CH B. KI C. NaOH D. CH COOH
4 3
3. 名称为“干燥管”的仪器是
A. B. C. D.
4. 下列物质对应的化学式不正确的是
A. 氯仿:CHCl B. 黄铜矿的主要成分:Cu S
3 2
C. 芒硝:NaSO ·10H O D. 铝土矿的主要成分:Al O
2 4 2 2 3
5. 下列表示不正确的是
A. 乙炔的结构简式HC≡CH B. KOH的电子式
C. 乙烷的球棍模型: D. 氯离子的结构示意图:
6. 下列说法不正确的是
A. 液化石油气是纯净物 B. 工业酒精中往往含有甲醇
C. 福尔马林是甲醛的水溶液 D. 许多水果和花卉有芳香气味是因为含有酯
7. 下列说法不正确的是
A. 32S和34S互为同位素 B. C 和纳米碳管互为同素异形体
70
C. CHClCH Cl和CHCHCl 互为同分异构体 D. C H 和C H 一定互为同系物
2 2 3 2 3 6 4 88. 下列说法不正确的是
A. 镁合金密度较小、强度较大,可用于制造飞机部件
B. 还原铁粉可用作食品干燥剂
C. 氯气、臭氧、二氧化氯都可用于饮用水的消毒
D. 油脂是热值最高的营养物质
9. 下列说法正确的是
A. 铁与碘反应易生成碘化铁
B. 电解ZnSO 溶液可以得到Zn
4
C. 用石灰沉淀富镁海水中的Mg2+,生成碳酸镁
D. SO 通入BaCl 溶液中生成BaSO 沉淀
2 2 3
10. 关于反应4CO+SiH 4CO+2HO+SiO,下列说法正确的是
2 4 2 2
A. CO是氧化产物 B. SiH 发生还原反应
4
C. 氧化剂与还原剂的物质的量之比为1∶4 D. 生成1molSiO 时,转移8mol电子
2
11. 下列说法不正确的是
A. 灼烧法做“海带中碘元素的分离及检验”实验时,须将海带进行灰化
B. 用纸层析法分离铁离子和铜离子时,不能将滤纸条上的试样点浸入展开剂中
C. 将盛有苯酚与水形成的浊液的试管浸泡在80℃热水中一段时间,浊液变澄清
D. 不能将实验室用剩的金属钠块放回原试剂瓶
12. 设N 为阿伏加德罗常数的值,下列说法正确的是
A
A. 在25℃时,1LpH为12的Ba(OH) 溶液中含有OH-数目为0.01N
2 A
B. 1.8g重水(D O)中所含质子数为N
2 A
C. 足量的浓盐酸与8.7gMnO 反应,转移电子的数目为0.4N
2 A
D. 32g甲醇的分子中含有C—H键的数目为4N
A
13. 下列实验对应的离子方程式不正确的是
A. 将碳酸氢钙溶液与过量的澄清石灰水混合: +Ca2++OH-=CaCO ↓+H O
3 2
B. 将少量NO 通入NaOH溶液:2NO +2OH-= + +H O
2 2 2
C. 将少量SO 通入NaClO溶液:SO +H O+2ClO-= +2HClO
2 2 2
D. 向氨水中滴入少量硝酸银溶液:Ag++2NH·H O= +2H O
3 2 214. 下列说法正确的是
A. 苯酚、乙醇、硫酸铜、氢氧化钠和硫酸铵均能使蛋白质变性
B. 通过石油的常压分馏可获得石蜡等馏分,常压分馏过程为物理变化
C. 在分子筛固体酸催化下,苯与乙烯发生取代反应获得苯乙烷
D. 含氮量高的硝化纤维可作烈性炸药
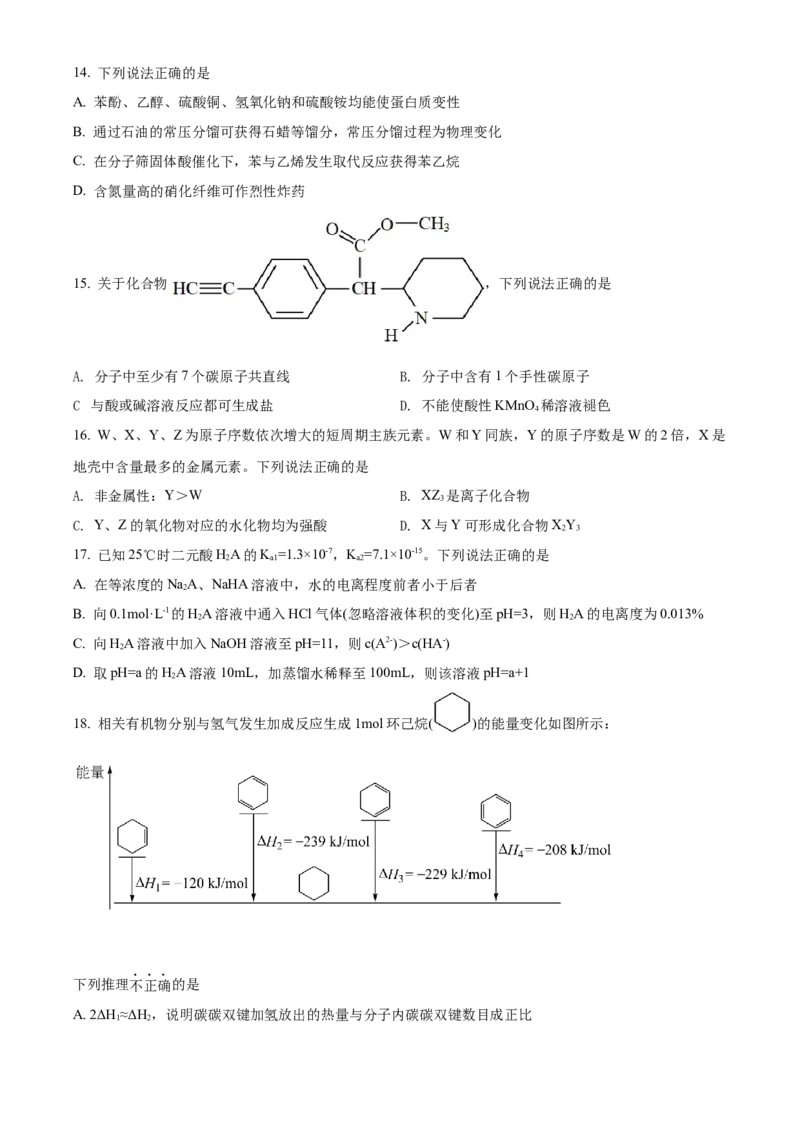
15. 关于化合物 ,下列说法正确的是
A. 分子中至少有7个碳原子共直线 B. 分子中含有1个手性碳原子
.
C 与酸或碱溶液反应都可生成盐 D. 不能使酸性KMnO 稀溶液褪色
4
16. W、X、Y、Z为原子序数依次增大的短周期主族元素。W和Y同族,Y的原子序数是W的2倍,X是
地壳中含量最多的金属元素。下列说法正确的是
A. 非金属性:Y>W B. XZ 是离子化合物
3
C. Y、Z的氧化物对应的水化物均为强酸 D. X与Y可形成化合物XY
2 3
17. 已知25℃时二元酸HA的K =1.3×10-7,K =7.1×10-15。下列说法正确的是
2 a1 a2
A. 在等浓度的NaA、NaHA溶液中,水的电离程度前者小于后者
2
B. 向0.1mol·L-1的HA溶液中通入HCl气体(忽略溶液体积的变化)至pH=3,则HA的电离度为0.013%
2 2
C. 向HA溶液中加入NaOH溶液至pH=11,则c(A2-)>c(HA-)
2
D. 取pH=a的HA溶液10mL,加蒸馏水稀释至100mL,则该溶液pH=a+1
2
18. 相关有机物分别与氢气发生加成反应生成1mol环己烷( )的能量变化如图所示:
下列推理不正确的是
A. 2ΔH ≈ΔH,说明碳碳双键加氢放出的热量与分子内碳碳双键数目成正比
1 2B. ΔH<ΔH,说明单双键交替的两个碳碳双键间存在相互作用,有利于物质稳定
2 3
C. 3ΔH<ΔH,说明苯分子中不存在三个完全独立的碳碳双键
1 4
D. ΔH -ΔH <0,ΔH-ΔH >0,说明苯分子具有特殊稳定性
3 1 4 3
19. 在恒温恒容条件下,发生反应A(s)+2B(g) 3X(g),c(B)随时间的变化如图中曲线甲所示。下列说
法不正确的是
A. 从a、c两点坐标可求得从a到c时间间隔内该化学反应的平均速率
B. 从b点切线的斜率可求得该化学反应在反应开始时的瞬时速率
C. 在不同时刻都存在关系:2v(B)=3v(X)
D. 维持温度、容积、反应物起始的量不变,向反应体系中加入催化剂,c(B)随时间变化关系如图中曲线乙
所示
20. AB型强电解质在水中的溶解(可视作特殊的化学反应)表示为AB(s)=An+(aq)+Bn-(aq),其焓变和熵变分
别为ΔH和ΔS。对于不同组成的AB型强电解质,下列说法正确的是
A. ΔH和ΔS均大于零
B. ΔH和ΔS均小于零
C. ΔH可能大于零或小于零,ΔS大于零
D. ΔH和ΔS均可能大于零或小于零
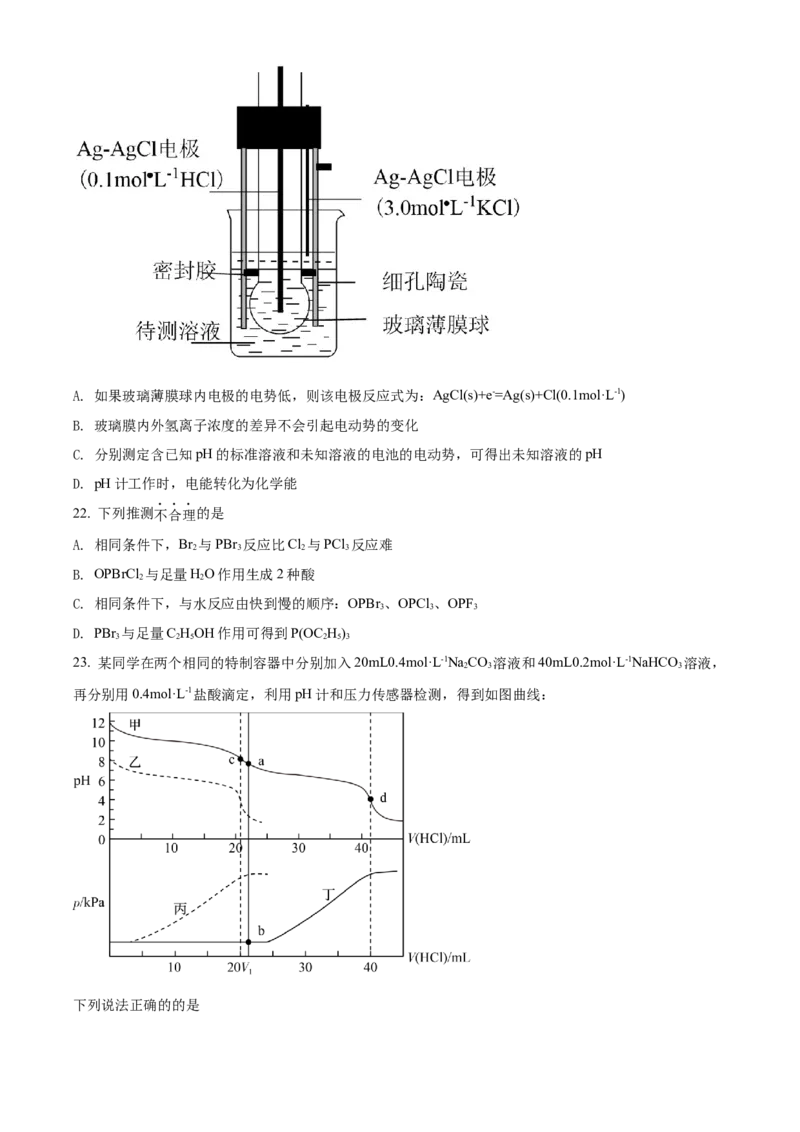
21. pH计是一种采用原电池原理测量溶液pH的仪器。如图所示,以玻璃电极(在特制玻璃薄膜球内放置已
知浓度的HCl溶液,并插入Ag—AgCl电极)和另一Ag—AgCl电极插入待测溶液中组成电池,pH与电池的
电动势E存在关系:pH=(E-常数)/0.059。下列说法正确的是A. 如果玻璃薄膜球内电极的电势低,则该电极反应式为:AgCl(s)+e-=Ag(s)+Cl(0.1mol·L-1)
B. 玻璃膜内外氢离子浓度的差异不会引起电动势的变化
C. 分别测定含已知pH的标准溶液和未知溶液的电池的电动势,可得出未知溶液的pH
D. pH计工作时,电能转化为化学能
22. 下列推测不合理的是
A. 相同条件下,Br 与PBr 反应比Cl 与PCl 反应难
2 3 2 3
B. OPBrCl 与足量HO作用生成2种酸
2 2
C. 相同条件下,与水反应由快到慢的顺序:OPBr 、OPCl 、OPF
3 3 3
D. PBr 与足量C HOH作用可得到P(OC H)
3 2 5 2 5 3
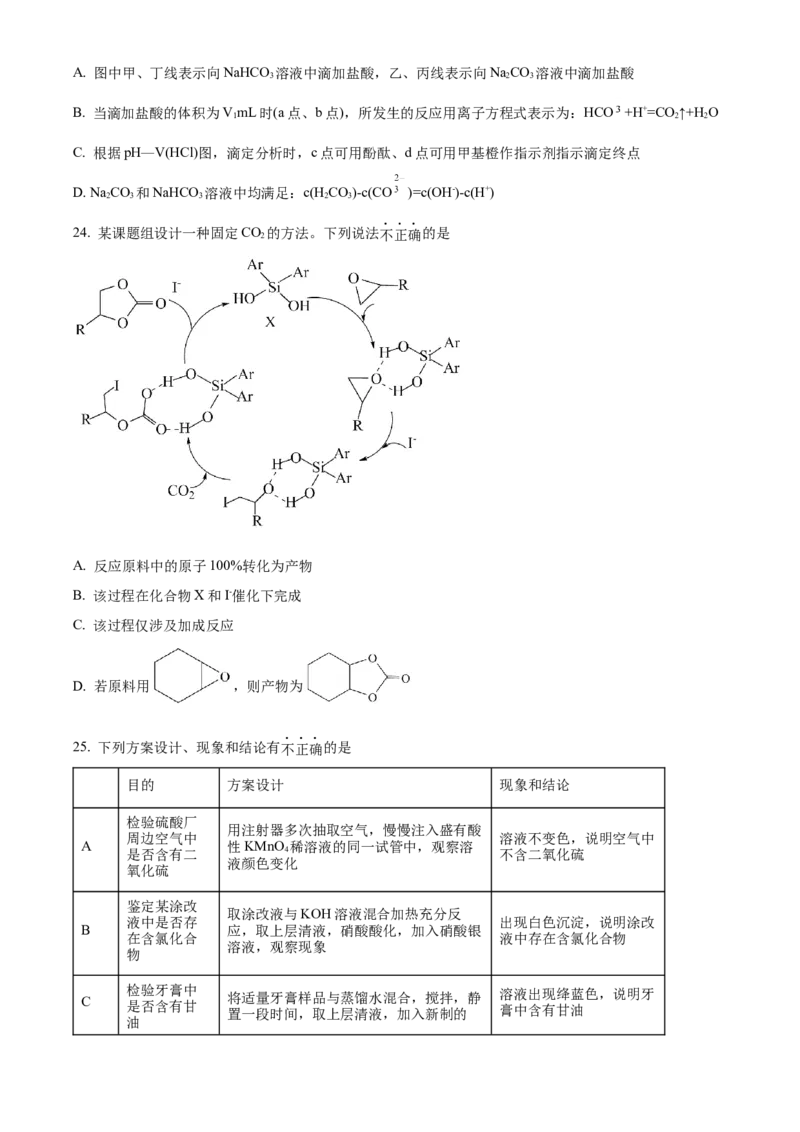
23. 某同学在两个相同的特制容器中分别加入20mL0.4mol·L-1NaCO 溶液和40mL0.2mol·L-1NaHCO 溶液,
2 3 3
再分别用0.4mol·L-1盐酸滴定,利用pH计和压力传感器检测,得到如图曲线:
下列说法正确的的是A. 图中甲、丁线表示向NaHCO 溶液中滴加盐酸,乙、丙线表示向NaCO 溶液中滴加盐酸
3 2 3
B. 当滴加盐酸的体积为VmL时(a点、b点),所发生的反应用离子方程式表示为:HCO +H+=CO ↑+H O
1 2 2
C. 根据pH—V(HCl)图,滴定分析时,c点可用酚酞、d点可用甲基橙作指示剂指示滴定终点
D. Na CO 和NaHCO 溶液中均满足:c(HCO)-c(CO )=c(OH-)-c(H+)
2 3 3 2 3
24. 某课题组设计一种固定CO 的方法。下列说法不正确的是
2
A. 反应原料中的原子100%转化为产物
B. 该过程在化合物X和I-催化下完成
C. 该过程仅涉及加成反应
D. 若原料用 ,则产物为
25. 下列方案设计、现象和结论有不正确的是
目的 方案设计 现象和结论
检验硫酸厂
用注射器多次抽取空气,慢慢注入盛有酸
周边空气中 溶液不变色,说明空气中
A 性KMnO 稀溶液的同一试管中,观察溶
是否含有二 4 不含二氧化硫
液颜色变化
氧化硫
鉴定某涂改
取涂改液与KOH溶液混合加热充分反
液中是否存 出现白色沉淀,说明涂改
B 应,取上层清液,硝酸酸化,加入硝酸银
在含氯化合 液中存在含氯化合物
溶液,观察现象
物
C 检验牙膏中 将适量牙膏样品与蒸馏水混合,搅拌,静 溶液出现绛蓝色,说明牙
是否含有甘 置一段时间,取上层清液,加入新制的 膏中含有甘油
油Cu(OH) ,振荡,观察现象
2
鉴别食盐与 各取少量固体加水溶解,分别滴加含淀粉 溶液变蓝色的为亚硝酸
D
亚硝酸钠 的KI溶液,振荡,观察溶液颜色变化 钠;溶液不变蓝的为食盐
A. A B. B C. C D. D
二、非选择题(本大题共6小题,共50分)
26. 回答下列问题:
(1)两种有机物的相关数据如表:
物质 HCON(CH ) HCONH
3 2 2
相对分子质量 73 45
沸点/℃ 153 220
HCON(CH ) 的相对分子质量比HCONH 的大,但其沸点反而比HCONH 的低,主要原因是______。
3 2 2 2
(2)四种晶体的熔点数据如表:
物质 CF SiF BF AlF
4 4 3 3
熔点/℃ -183 -90 -127 >1000
CF 和SiF 熔点相差较小,BF 和AlF 熔点相差较大,原因是______。
4 4 3 3
27. 某同学设计实验确定Al(NO )·xH O的结晶水数目。称取样品7.50g,经热分解测得气体产物中有
3 3 2
NO 、O、HNO、HO,其中HO的质量为3.06g;残留的固体产物是Al O,质量为1.02g。计算:
2 2 3 2 2 2 3
(1)x=_______(写出计算过程)。
(2)气体产物中n(O )_______mol。
2
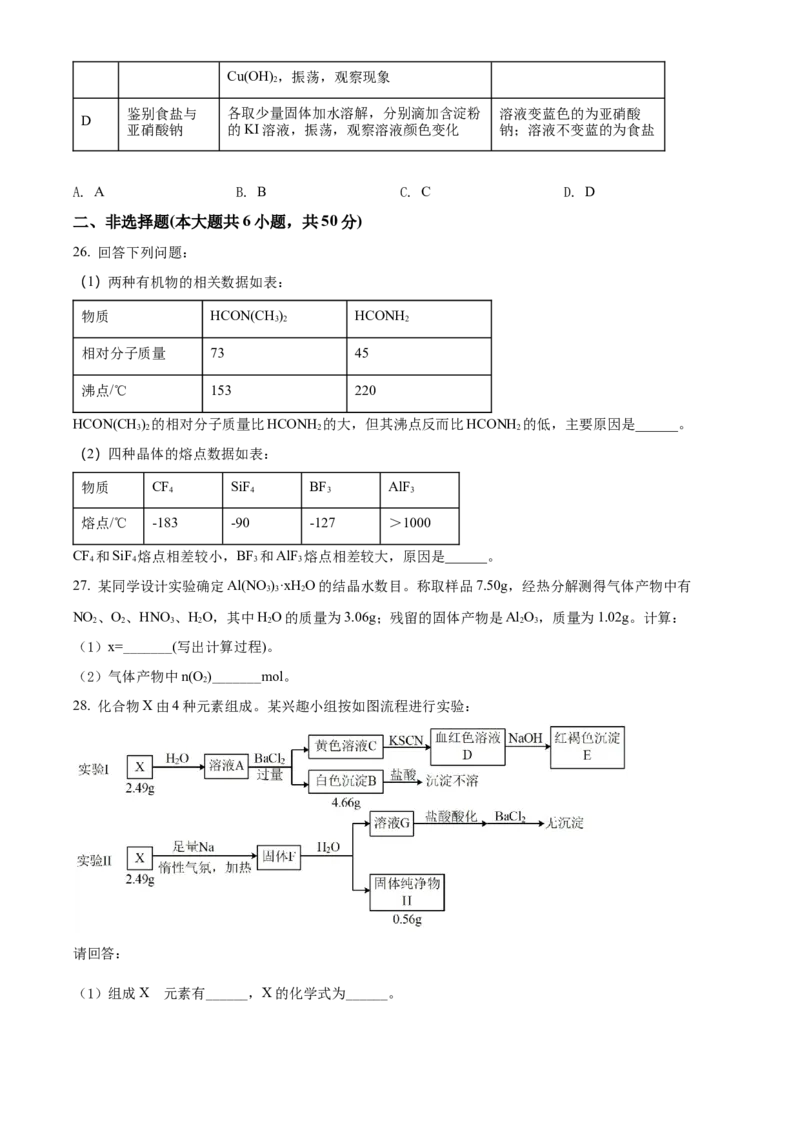
28. 化合物X由4种元素组成。某兴趣小组按如图流程进行实验:
请回答:
的
(1)组成X 元素有______,X的化学式为______。(2)溶液C中溶质的成分是______(用化学式表示);根据C→D→E的现象,给出相应微粒与阳离子结合
由弱到强的排序______。
(3)X与足量Na反应生成固体F的化学方程式是______。
(4)设计实验确定溶液G中阴离子______。
29. 工业上,以煤炭为原料,通入一定比例的空气和水蒸气,经过系列反应可以得到满足不同需求的原料
气。请回答:
(1)在C和O 的反应体系中:
2
反应1:C(s)+O(g)=CO (g) ΔH =-394kJ·mol-1
2 2 1
反应2:2CO(g)+O(g)=2CO (g) ΔH =-566kJ·mol-1
2 2 2
反应3:2C(s)+O(g)=2CO(g) ΔH 。
2 3
① 设y=ΔH-TΔS,反应1、2和3的y随温度的变化关系如图1所示。图中对应于反应3的线条是
______。
②一定压强下,随着温度的升高,气体中CO与CO 的物质的量之比______。
2
A.不变 B.增大 C.减小 D.无法判断
(2)水煤气反应:C(s)+HO(g)=CO(g)+H (g) ΔH=131kJ·mol-1。工业生产水煤气时,通常交替通入合适量
2 2
的空气和水蒸气与煤炭反应,其理由是________。
(3)一氧化碳变换反应:CO(g)+HO(g)=CO(g)+H(g) ΔH=-41kJ·mol-1。
2 2 2
①一定温度下,反应后测得各组分的平衡压强(即组分的物质的量分数×总压):p(CO)=0.25MPa、
p(H O)=0.25MPa、p(CO)=0.75MPa和p(H )=0.75MPa,则反应的平衡常数K的数值为________。
2 2 2
②维持与题①相同的温度和总压,提高水蒸气的比例,使CO的平衡转化率提高到90%,则原料气中水蒸
气和CO的物质的量之比为________。
③生产过程中,为了提高变换反应的速率,下列措施中合适的是________。
A.反应温度愈高愈好 B.适当提高反应物压强
C.选择合适的催化剂 D.通入一定量的氮气④以固体催化剂M催化变换反应,若水蒸气分子首先被催化剂的活性表面吸附而解离,能量-反应过程如
图2所示。
用两个化学方程式表示该催化反应历程(反应机理):步骤Ⅰ:________;步骤Ⅱ:________。
30. 某兴趣小组用四水醋酸锰[(CH COO) Mn·4H O]和乙酰氯(CHCOCl)为原料制备无水二氯化锰,按如图
3 2 2 3
流程开展了实验(夹持仪器已省略):
已知:①无水二氯化锰极易吸水潮解,易溶于水、乙醇和醋酸,不溶于苯。
②制备无水二氯化锰的主要反应:(CHCOO) Mn+CHCOCl MnCl ↓+2(CH COO) O。
3 2 3 2 3 2
③乙酰氯遇水发生反应:CHCOCl+H O→CH COOH+HCl。
3 2 3
请回答:
(1)步骤Ⅰ:所获固体主要成分是_________(用化学式表示)。
(2)步骤Ⅰ在室温下反应,步骤Ⅱ在加热回流下反应,目的分别是________。
(3)步骤Ⅲ:下列操作中正确的是_________。
A. 用蒸馏水润湿滤纸,微开水龙头,抽气使滤纸紧贴在漏斗瓷板上
B. 用倾析法转移溶液,开大水龙头,待溶液快流尽时再转移沉淀
C. 用乙醇作为洗涤剂,在洗涤沉淀时,应开大水龙头,使洗涤剂快速通过沉淀物.
D 洗涤结束后,将固体迅速转移至圆底烧瓶进行后续操作
(4)步骤Ⅳ:①奖装有粗产品的圆底烧瓶接到纯化装置(图2)上,打开安全瓶上旋塞,打开抽气泵,关闭
安全瓶上旋塞,开启加热器,进行纯化。请给出纯化完成后的操作排序:________。
纯化完成→(_____)→(_____)→(_____)→(_____)→将产品转至干燥器中保存
的
a.拔出圆底烧瓶 瓶塞
b.关闭抽气泵
c.关闭加热器,待烧瓶冷却至室温
d.打开安全瓶上旋塞
②图2装置中U形管内NaOH固体的作用是________。
(5)用滴定分析法确定产品纯度。甲同学通过测定产品中锰元素的含量确定纯度;乙同学通过测定产品
中氯元素的含量确定纯度。合理的是_________(填“甲”或“乙”)同学的方法。
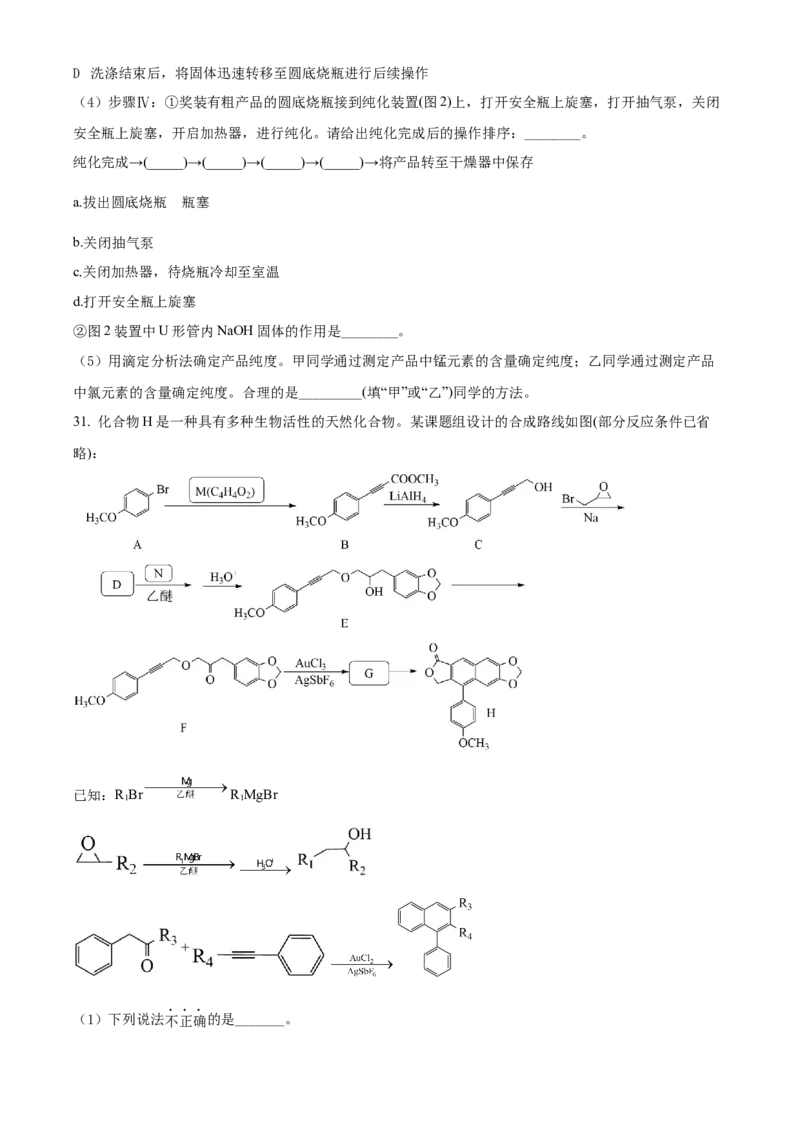
31. 化合物H是一种具有多种生物活性的天然化合物。某课题组设计的合成路线如图(部分反应条件已省
略):
已知:R Br R MgBr
1 1
+
(1)下列说法不正确的是_______。A. 化合物A不易与NaOH溶液反应 B. 化合物E和F可通过红外光谱区别
的
C. 化合物F属于酯类物质 D. 化合物H 分子式是C H O
20 12 5
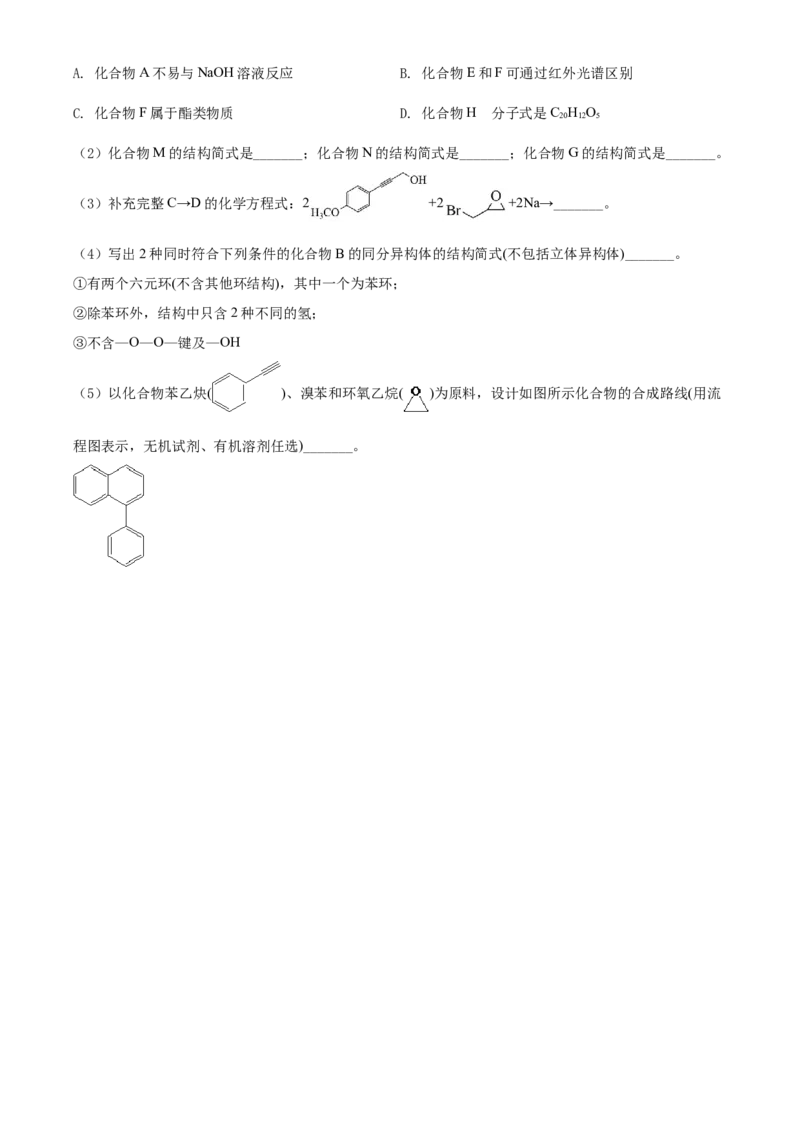
(2)化合物M的结构简式是_______;化合物N的结构简式是_______;化合物G的结构简式是_______。
(3)补充完整C→D的化学方程式:2 +2 +2Na→_______。
(4)写出2种同时符合下列条件的化合物B的同分异构体的结构简式(不包括立体异构体)_______。
①有两个六元环(不含其他环结构),其中一个为苯环;
②除苯环外,结构中只含2种不同的氢;
③不含—O—O—键及—OH
(5)以化合物苯乙炔( )、溴苯和环氧乙烷( )为原料,设计如图所示化合物的合成路线(用流
程图表示,无机试剂、有机溶剂任选)_______。