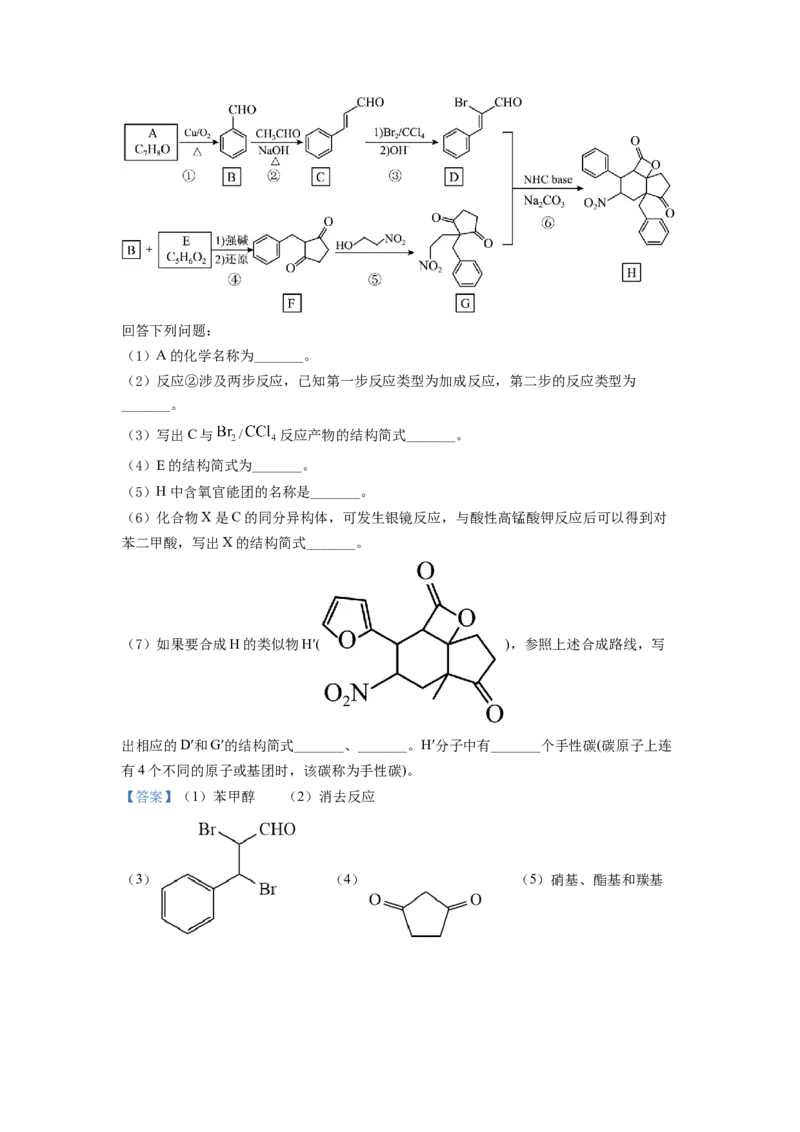
文档内容
2022年全国统一高考化学试卷(全国甲卷)
一、选择题
1. 化学与生活密切相关。下列叙述正确的是
A. 漂白粉与盐酸可混合使用以提高消毒效果 B. 温室气体是形成酸雨的主要物质
C. 棉花、麻和蚕丝均为碳水化合物 D. 干冰可用在舞台上制造“云雾”
【答案】D
【解析】
【详解】A.漂白粉的有效成分次氯酸钙与盐酸混合,会发生氧化还原反应生成有毒的氯
气,两者不能混合使用,A错误;
B.温室气体主要是指二氧化碳,二氧化碳不是形成酸雨的主要物质,形成酸雨的主要物
质是硫氧化物、氮氧化物等,B错误;
C.棉花、麻来源于植物,主要成分均是纤维素,为碳水化合物,但蚕丝来源于动物,主
要成分是蛋白质,蛋白质不是碳水化合物,C错误;
D.干冰是固态的二氧化碳,干冰升华时,吸收大量的热,使周围温度降低,大量的水蒸
气凝结成了小液滴,形成 “云雾”效果,D正确;
答案选D。
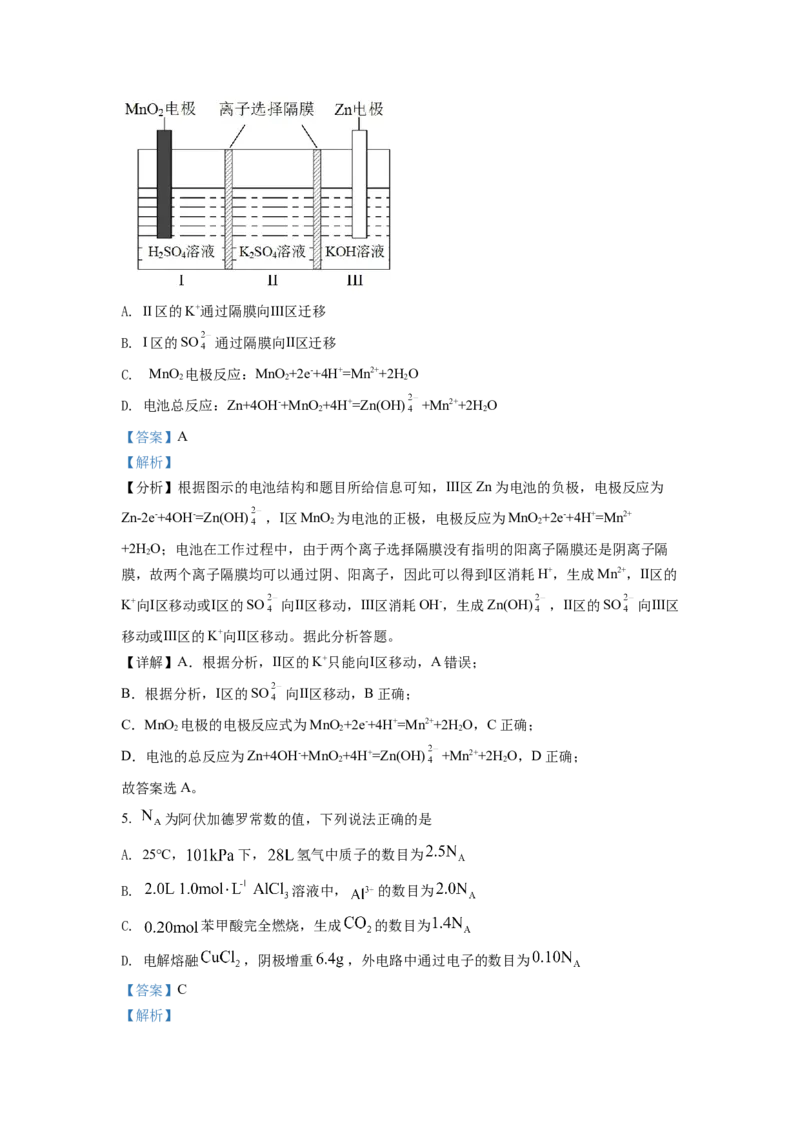
2. 辅酶 具有预防动脉硬化的功效,其结构简式如下。下列有关辅酶 的说法正确的
是
A. 分子式为 B. 分子中含有14个甲基
C. 分子中的四个氧原子不在同一平面 D. 可发生加成反应,不能发生取代
反应
【答案】B
【解析】
【详解】A.由该物质的结构简式可知,其分子式为C H O,A错误;
59 90 4
B.由该物质的结构简式可知,键线式端点代表甲基,10个重复基团的最后一个连接H原
子的碳是甲基,故分子中含有1+1+1+10+1=14个甲基,B正确;
C.双键碳以及与其相连的四个原子共面,羰基碳采取sp2杂化,羰基碳原子和与其相连的
氧原子及另外两个原子共面,因此分子中的四个氧原子在同一平面上,C错误;
D.分子中有碳碳双键,能发生加成反应,分子中含有甲基,能发生取代反应,D错误;答案选B。
3. 能正确表示下列反应的离子方程式为
A. 硫化钠溶液和硝酸混合:S2-+2H+=H S↑
2
B. 明矾溶液与过量氨水湿合:Al3++4NH+2H O=AlO +4NH
3 2
C. 硅酸钠溶液中通入二氧化碳:SiO +CO +H O=HSiO +HCO
2 2
D. 将等物质的量浓度的Ba(OH) 和NH HSO 溶液以体积比1∶2混合:Ba2++2OH-+2H++SO
2 4 4
=BaSO ↓+2H O
4 2
【答案】D
【解析】
【详解】A.硝酸具有强氧化性,可以将S2-氧化为S单质,自身根据其浓度大小还原为NO
或NO ,反应的离子方程式为4H++2NO +S2-=S↓+2NO↑+2H O(浓)或8H++2NO +3S2-
2 2 2
=3S↓+2NO+4H O(稀),A错误;
2
B.明矾在水中可以电离出Al3+,可以与氨水中电离出的OH-发生反应生成Al(OH) ,但由
3
于氨水的碱性较弱,生成的Al(OH) 不能继续与弱碱发生反应,故反应的离子方程式为Al3+
3
+3NH·H O=Al(OH) ↓+3NH ,B错误;
3 2 3
C.硅酸的酸性小于碳酸,向硅酸钠溶液中通入二氧化碳时,生成硅酸沉淀,二氧化碳则
根据其通入的量的多少反应为碳酸根或碳酸氢根,反应的离子方程式为SiO
+H O+CO=H SiO↓+CO (CO 少量)或SiO +2H O+2CO=H SiO↓+2HCO (CO 过量),C
2 2 2 3 2 2 2 2 3 2
错误;
D.将等物质的量浓度的Ba(OH) 与NH HSO 溶液以体积比1:2混合,Ba(OH) 电离出的
2 4 4 2
OH-与NH HSO 电离出的H+反应生成水,Ba(OH) 电离出的Ba2+与NH HSO 电离出的SO
4 4 2 4 4
反应生成BaSO 沉淀,反应的离子方程为为Ba2++2OH-+2H++SO =BaSO ↓+2H O,D正
4 4 2
确;
故答案选D。
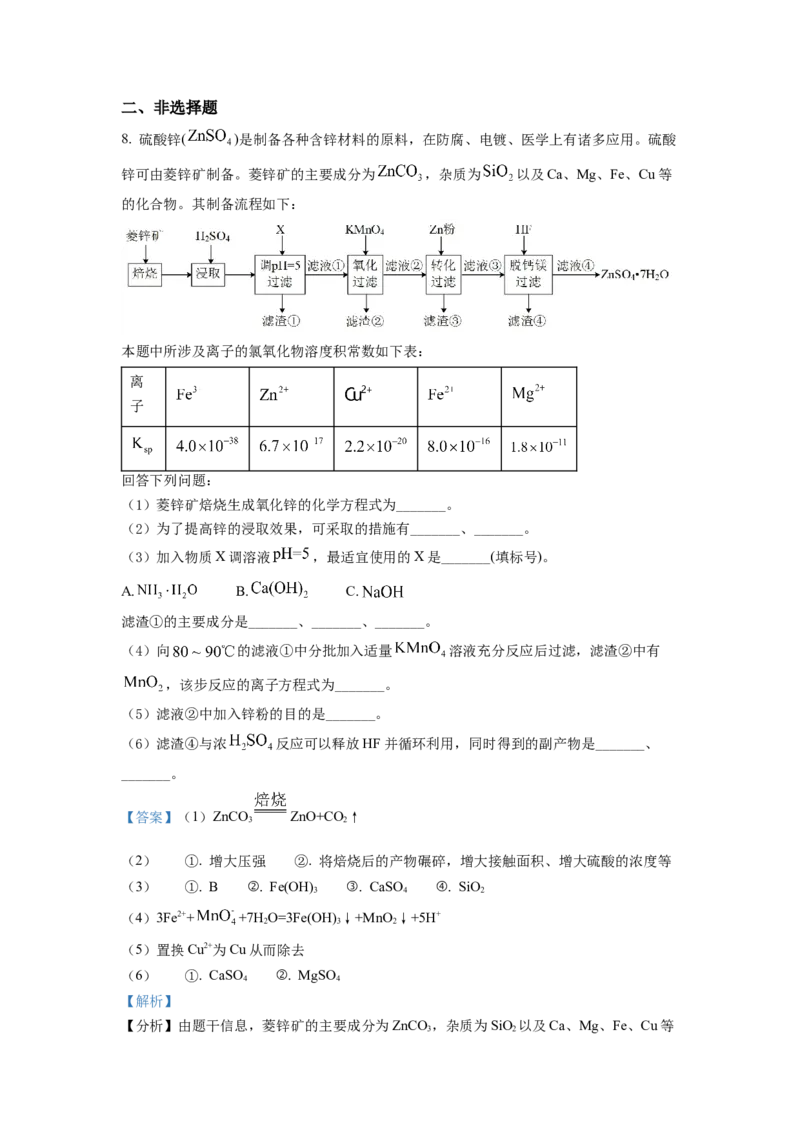
4. 一种水性电解液Zn-MnO 离子选泽双隔膜电池如图所示(KOH溶液中,Zn2+以Zn(OH)
2
存在)。电池放电时,下列叙述错误的是A. Ⅱ区的K+通过隔膜向Ⅲ区迁移
B. Ⅰ区的SO 通过隔膜向Ⅱ区迁移
C. MnO 电极反应:MnO +2e-+4H+=Mn2++2H O
2 2 2
D. 电池总反应:Zn+4OH-+MnO+4H+=Zn(OH) +Mn2++2H O
2 2
【答案】A
【解析】
【分析】根据图示的电池结构和题目所给信息可知,Ⅲ区Zn为电池的负极,电极反应为
Zn-2e-+4OH-=Zn(OH) ,Ⅰ区MnO 为电池的正极,电极反应为MnO +2e-+4H+=Mn2+
2 2
+2H O;电池在工作过程中,由于两个离子选择隔膜没有指明的阳离子隔膜还是阴离子隔
2
膜,故两个离子隔膜均可以通过阴、阳离子,因此可以得到Ⅰ区消耗H+,生成Mn2+,Ⅱ区的
K+向Ⅰ区移动或Ⅰ区的SO 向Ⅱ区移动,Ⅲ区消耗OH-,生成Zn(OH) ,Ⅱ区的SO 向Ⅲ区
移动或Ⅲ区的K+向Ⅱ区移动。据此分析答题。
【详解】A.根据分析,Ⅱ区的K+只能向Ⅰ区移动,A错误;
B.根据分析,Ⅰ区的SO 向Ⅱ区移动,B正确;
C.MnO 电极的电极反应式为MnO +2e-+4H+=Mn2++2H O,C正确;
2 2 2
D.电池的总反应为Zn+4OH-+MnO+4H+=Zn(OH) +Mn2++2H O,D正确;
2 2
故答案选A。
5. 为阿伏加德罗常数的值,下列说法正确的是
A. 25℃, 下, 氢气中质子的数目为
B. 溶液中, 的数目为
C. 苯甲酸完全燃烧,生成 的数目为
D. 电解熔融 ,阴极增重 ,外电路中通过电子的数目为
【答案】C
【解析】【详解】A.25℃、101kPa不是标准状况,不能用标况下的气体摩尔体积计算氢气的物质
的量,故A错误;
B.Al3+在溶液中会发生水解生成Al(OH) ,因此2.0L 1.0 mol/L的AlCl 溶液中Al3+数目小
3 3
于2.0N ,故B错误;
A
C.苯甲酸燃烧的化学方程式为 ,1mol苯甲酸燃
烧生成7molCO ,则0.2mol苯甲酸完全燃烧生成1.4molCO,数目为1.4N ,故C正确;
2 2 A
D.电解熔融CuCl 时,阳极反应为 ,阴极反应为 ,阴极增
2
加的重量为Cu的质量,6.4gCu的物质的量为0.1mol,根据阴极反应可知,外电路中通过
电子的物质的量为0.2mol,数目为0.2N ,故D错误;
A
答案选C。
6. Q、X、Y、Z是原子序数依次增大的短周期主族元素,其最外层电子数之和为19。Q与
X、Y、Z位于不同周期,X、Y相邻,Y原子最外层电子数是Q原子内层电子数的2倍。
下列说法正确的是
A. 非金属性: B. 单质的熔点:
C. 简单氢化物的佛点: D. 最高价含氧酸的酸性:
【答案】D
【解析】
【分析】Q、X、Y、Z为原子序数依次增大的短周期主族元素,Q与X、Y、Z不在同一周
期,Y原子最外层电子数为Q元原子内层电子数的2倍,则Q应为第二周期元素,X、Y、
Z位于第三周期,Y的最外层电子数为4,则Y为Si元素,X、Y相邻,且X的原子序数小
于Y,则X为Al元素,Q、X、Y、Z的最外层电子数之和为19,则Q、Z的最外层电子数
之和为19-3-4=12,主族元素的最外层电子数最多为7,若Q的最外层电子数为7,为F元
素,Z的最外层电子数为5,为P元素,若Q的最外层电子数为6,为O元素,则Z的最外
层电子数为6,为S元素,若Q的最外层电子数为5,为N元素,Z的最外层电子数为7,
为Cl元素;综上所述,Q为N或O或F,X为Al,Y为Si,Z为Cl或S或P,据此分析解
题。
【详解】A.X为Al,Q为N或O或F,同一周期从左往右元素非金属性依次增强,同一
主族从上往下依次减弱,故非金属性:Q>X,A错误;
B.由分析可知,X为Al属于金属晶体,Y为Si属于原子晶体或共价晶体,故单质熔点
Si>Al,即Y>X,B错误;
C.含有氢键的物质沸点升高,由分析可知Q为N或O或F,其简单氢化物为HO或NH
2 3
或HF,Z为Cl或S或P,其简单氢化物为HCl或HS或PH ,由于前者物质中存在分子间
2 3
氢键,而后者物质中不存在,故沸点Q>Z,C错误;
D.元素的非金属性越强,其最高价含氧酸的酸性越强,P、S、Cl的非金属性均强于Si,因此最高价含氧酸酸性:Z>Y,D正确;
故答案为:D。
7. 根据实验目的,下列实验及现象、结论都正确的是
选
实验目的 实验及现象 结论
项
分别测浓度均为
的
比较
A 和
和 的水解
常数 溶液的 ,后
者大于前者
将铁锈落于浓盐酸,滴入
检验铁锈中是否
B 铁绣中含有二价铁
含有二价铁 溶液,紫色褪去
探究氢离子浓度
对 、 增大氢离子浓度,转化平衡向生
向 溶液中缓慢滴
C
成 的方向移动
相互转化 加硫酸,黄色变为橙红色
的影响
检验乙醇中是否 向乙醇中加入一小粒金属
D 乙醇中含有水
含有水 钠,产生无色气体
A. A B. B C. C D. D
【答案】C
【解析】
【详解】A.CHCOONH 中 水解, ,会消耗
3 4
CHCOO-水解生成的OH-,测定相同浓度的CHCOONH 和NaHCO 溶液的pH,后者大于
3 3 4 3
前者,不能说明K(CHCOO-)<K( ),A错误;
h 3 h
B.铁锈中含有Fe单质,单质Fe与浓盐酸可反应生成Fe2+,滴入KMnO 溶液,紫色褪去,
4
不能说明铁锈中一定含有二价铁,B错误;
C.KCrO 中存在平衡2 (黄色)+2H+ (橙红色)+H O,缓慢滴加硫酸,
2 4 2
H+浓度增大,平衡正向移动,故溶液黄色变成橙红色,C正确;
D.乙醇和水均会与金属钠发生反应生成氢气,故不能说明乙醇中含有水,D错误;
答案选C。二、非选择题
8. 硫酸锌( )是制备各种含锌材料的原料,在防腐、电镀、医学上有诸多应用。硫酸
锌可由菱锌矿制备。菱锌矿的主要成分为 ,杂质为 以及Ca、Mg、Fe、Cu等
的化合物。其制备流程如下:
本题中所涉及离子的氯氧化物溶度积常数如下表:
离
子
回答下列问题:
(1)菱锌矿焙烧生成氧化锌的化学方程式为_______。
(2)为了提高锌的浸取效果,可采取的措施有_______、_______。
(3)加入物质X调溶液 ,最适宜使用的X是_______(填标号)。
A. B. C.
滤渣①的主要成分是_______、_______、_______。
(4)向 的滤液①中分批加入适量 溶液充分反应后过滤,滤渣②中有
,该步反应的离子方程式为_______。
(5)滤液②中加入锌粉的目的是_______。
(6)滤渣④与浓 反应可以释放HF并循环利用,同时得到的副产物是_______、
_______。
【答案】(1)ZnCO ZnO+CO ↑
3 2
(2) ①. 增大压强 ②. 将焙烧后的产物碾碎,增大接触面积、增大硫酸的浓度等
(3) ①. B ②. Fe(OH) ③. CaSO ④. SiO
3 4 2
(4)3Fe2++ +7H O=3Fe(OH) ↓+MnO↓+5H+
2 3 2
(5)置换Cu2+为Cu从而除去
(6) ①. CaSO ②. MgSO
4 4
【解析】
【分析】由题干信息,菱锌矿的主要成分为ZnCO ,杂质为SiO 以及Ca、Mg、Fe、Cu等
3 2的化合物,结合流程图分析,菱锌矿焙烧,主要发生反应ZnCO ZnO+CO ↑,再加
3 2
入HSO 酸浸,得到含Zn2+、Ca2+、Ma2+、Fe2+、Fe3+、Cu2+的溶液,加入物质X调节
2 4
pH=5,结合表格数据,过滤得到Fe(OH) 、CaSO、SiO 的滤渣①,滤液①中主要含有
3 4 2
Zn2+、Cu2+、Mg2+、Ca2+、Fe2+,再向滤液①中加入KMnO 溶液氧化Fe2+,过滤得到
4
Fe(OH) 和MnO 的滤渣②,滤液②中加入锌粉,发生反应Zn+Cu2+=Zn2+=Cu,过滤后得到
3 2
滤渣③为Cu,再向滤液③中加入HF脱钙镁,过滤得到滤渣④为CaF 、MgF ,滤液④为
2 2
ZnSO 溶液,经一系列处理得到ZnSO·7HO,据此分析解答。
4 4 2
【小问1详解】
由分析,焙烧时,生成ZnO的反应为:ZnCO ZnO+CO ↑;
3 2
【小问2详解】
可采用增大压强、将焙烧后的产物碾碎,增大接触面积、增大硫酸的浓度等方式提高锌的
浸取率;
【小问3详解】
A.NH ·HO易分解产生NH 污染空气,且经济成本较高,故A不适宜;
3 2 3
B.Ca(OH) 不会引入新的杂质,且成本较低,故B适宜;
2
C.NaOH会引入杂质Na+,且成本较高,C不适宜;
故答案选B;
当沉淀完全时(离子浓度小于10-5mol/L),结合表格Ksp计算各离子完全沉淀时pH<5的只
有Fe3+,故滤渣①中有Fe(OH) ,又CaSO 是微溶物,SiO 不溶于酸,故滤渣①的主要成分
3 4 2
是Fe(OH) 、CaSO、SiO;
3 4 2
【小问4详解】
向80~90℃滤液①中加入KMnO 溶液,可氧化Fe2+,得到Fe(OH) 和MnO 的滤渣②,反应
4 3 2
的离子方程式为3Fe2++ +7H O=3Fe(OH) ↓+MnO↓+5H+;
2 3 2
【小问5详解】
滤液②中加入锌粉,发生反应Zn+Cu2+=Zn2+=Cu,故加入锌粉的目的为置换Cu2+为Cu从而
除去;
【小问6详解】
由分析,滤渣④为CaF 、MgF ,与浓硫酸反应可得到HF,同时得到的副产物为CaSO、
2 2 4
MgSO 。
4
9. 硫化钠可广泛用于染料、医药行业。工业生产的硫化钠粗品中常含有一定量的煤灰及重
金属硫化物等杂质。硫化钠易溶于热乙醇,重金属硫化物难溶于乙醇。实验室中常用95%
乙醇重结晶纯化硫化钠粗品。回答下列问题:
(1)工业上常用芒硝( )和煤粉在高温下生产硫化钠,同时生成CO,该反应的化学方程式为_______。
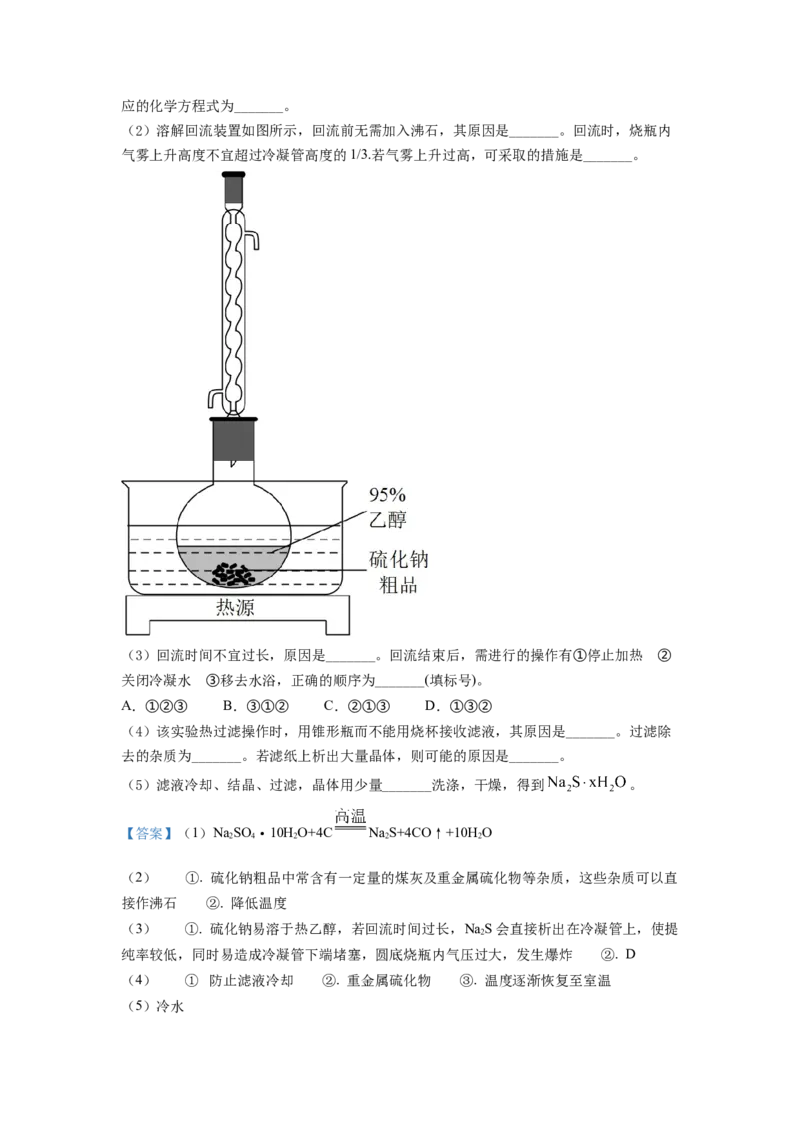
(2)溶解回流装置如图所示,回流前无需加入沸石,其原因是_______。回流时,烧瓶内
气雾上升高度不宜超过冷凝管高度的1/3.若气雾上升过高,可采取的措施是_______。
(3)回流时间不宜过长,原因是_______。回流结束后,需进行的操作有①停止加热 ②
关闭冷凝水 ③移去水浴,正确的顺序为_______(填标号)。
A.①②③ B.③①② C.②①③ D.①③②
(4)该实验热过滤操作时,用锥形瓶而不能用烧杯接收滤液,其原因是_______。过滤除
去的杂质为_______。若滤纸上析出大量晶体,则可能的原因是_______。
(5)滤液冷却、结晶、过滤,晶体用少量_______洗涤,干燥,得到 。
【答案】(1)NaSO ·10HO+4C NaS+4CO↑+10H O
2 4 2 2 2
(2) ①. 硫化钠粗品中常含有一定量的煤灰及重金属硫化物等杂质,这些杂质可以直
接作沸石 ②. 降低温度
(3) ①. 硫化钠易溶于热乙醇,若回流时间过长,NaS会直接析出在冷凝管上,使提
2
纯率较低,同时易造成冷凝管下端堵塞,圆底烧瓶内气压过大,发生爆炸 ②. D
.
(4) ① 防止滤液冷却 ②. 重金属硫化物 ③. 温度逐渐恢复至室温
(5)冷水【解析】
【分析】本实验的实验目的为制备硫化钠并用95%乙醇重结晶纯化硫化钠粗品,工业上常
用芒硝( )和煤粉在高温下生产硫化钠,反应原理为:NaSO ·10HO+4C
2 4 2
NaS+4CO↑+10H O,结合硫化钠的性质解答问题。
2 2
【小问1详解】
工业上常用芒硝( )和煤粉在高温下生产硫化钠,同时生产CO,根据得失
电子守恒,反应的化学方程式为:NaSO ·10HO+4C NaS+4CO↑+10H O;
2 4 2 2 2
【小问2详解】
由题干信息,生产的硫化钠粗品中常含有一定量的煤灰及重金属硫化物等杂质,这些杂质
可以直接作沸石,因此回流前无需加入沸石,若气流上升过高,可直接降低降低温度,使
气压降低;
【小问3详解】
硫化钠易溶于热乙醇,若回流时间过长,NaS会直接析出在冷凝管上,使提纯率较低,同
2
时易造成冷凝管下端堵塞,圆底烧瓶内气压过大,发生爆炸;回流结束后,先停止加热,
再移去水浴后再关闭冷凝水,故正确的顺序为①③②,答案选D。
【小问4详解】
硫化钠易溶于热乙醇,使用锥形瓶可有效防止滤液冷却,重金属硫化物难溶于乙醇,故过
滤除去的杂质为重金属硫化物,由于硫化钠易溶于热乙醇,过滤后温度逐渐恢复至室温,
滤纸上便会析出大量晶体;
【小问5详解】
乙醇与水互溶,硫化钠易溶于热乙醇,因此将滤液冷却、结晶、过滤后,晶体可用少量冷
水洗涤,再干燥,即可得到 。
10. 金属钛(Ti)在航空航天、医疗器械等工业领域有着重要用途,目前生产钛的方法之一是
将金红石 转化为 ,再进一步还原得到钛。回答下列问题:
(1) 转化为 有直接氯化法和碳氯化法。在 时反应的热化学方程式及其
平衡常数如下:
(ⅰ)直接氯化:
(ⅱ)碳氯化:
①反应 的为_______ , _______Pa。
②碳氯化的反应趋势远大于直接氯化,其原因是_______。③对于碳氯化反应:增大压强,平衡_______移动(填“向左”“向右”或“不”);温度升高,平
衡转化率_______(填“变大”“变小”或“不变”)。
(2)在 ,将 、C、 以物质的量比1∶2.2∶2进行反应。体系中气体平衡
组成比例(物质的量分数)随温度变化的理论计算结果如图所示。
①反应 的平衡常数 _______ 。
②图中显示,在 平衡时 几乎完全转化为 ,但实际生产中反应温度却远高
于此温度,其原因是_______。
(3) 碳氯化是一个“气—固—固”反应,有利于 “固—固”接触的措施是
_______。
【答案】(1) ①. -223 ②. 1.2×1014 ③. 碳氯化反应气体分子数增加,∆H小
于0,是熵增、放热过程,熵判据与焓判据均是自发过程,而直接氯化的体系气体分子数
不变、且是吸热过程 ④. 向左 ⑤. 变小
(2) ①. 7.2×105 ②. 为了提高反应速率,在相同时间内得到更多的TiCl 产品,
4
提高效益
(3)将两固体粉碎后混合,同时鼓入Cl,使固体粉末“沸腾”
2
【解析】
【小问1详解】
①根据盖斯定律,将“反应ⅱ-反应ⅰ”得到反应2C(s)+O(g)=2CO(g),则∆H=-51kJ/
2
mol-172kJ/mol=-223kJ/mol;则Kp= = =1.2×1014Pa;
②碳氯化的反应趋势远大于直接氯化,因为碳氯化反应气体分子数增加,∆H小于0,是熵增、放热过程,熵判据与焓判据均是自发过程,而直接氯化的体系气体分子数不变、且是
吸热过程;
③对应碳氯化反应,气体分子数增大,依据勒夏特列原理,增大压强,平衡往气体分子数
减少的方向移动,即平衡向左移动;该反应是放热反应,温度升高,平衡往吸热方向移动,
即向左移动,则平衡转化率变小。
【小问2详解】
①从图中可知,1400℃,体系中气体平衡组成比例CO 是0.05,TiCl 是0.35,CO是0.6,
2 4
反应C(s)+CO(g)=2CO(g)的平衡常数Kp(1400℃)= =
2
Pa=7.2×105Pa;
②实际生产中需要综合考虑反应的速率、产率等,以达到最佳效益,实际反应温度远高于
200℃,就是为了提高反应速率,在相同时间内得到更多的TiCl 产品。
4
【小问3详解】
固体颗粒越小,比表面积越大,反应接触面积越大。有利于TiO – C“固-固”接触,可将两
2
者粉碎后混合,同时鼓入Cl,使固体粉末“沸腾”,增大接触面积。
2
【化学—选修3:物质结构与性质】
11. 2008年北京奥运会的“水立方”,在2022年冬奥会上华丽转身为“冰立方”,实现了奥运
场馆的再利用,其美丽的透光气囊材料由乙烯(CH=CH )与四氟乙烯(CF=CF )的共聚物
2 2 2 2
(ETFE)制成。回答下列问题:
(1)基态F原子的价电子排布图(轨道表示式)为_______。
(2)图a、b、c分别表示C、N、O和F的逐级电离能Ⅰ变化趋势(纵坐标的标度不同)。第
一电离能的变化图是_______(填标号),判断的根据是_______;第三电离能的变化图是
_______(填标号)。
(3)固态氟化氢中存在(HF) 形式,画出(HF) 的链状结构_______。
n 3
(4) CF=CF 和ETFE分子中C的杂化轨道类型分别为_______和_______;聚四氟乙烯的
2 2
化学稳定性高于聚乙烯,从化学键的角度解释原因_______。
(5)萤石(CaF )是自然界中常见的含氟矿物,其晶胞结构如图所示,X代表的离子是
2
_______;若该立方晶胞参数为a pm,正负离子的核间距最小为_______pm。【答案】(1) (2) ①. 图a ②. 同一周期第一电离
能的总体趋势是依次升高的,但由于N元素的2p能级为半充满状态,因此N元素的第一
电离能较C、O两种元素高 ③. 图b
(3) (4) ①. sp2 ②. sp3 ③. C-F键的键
能大于聚乙烯中C-H的键能,键能越大,化学性质越稳定
(5) ①. Ca2+ ②. a pm
【解析】
【分析】根据基态原子的电子表示式书写价电子排布式;根据电离能的排布规律分析电离
能趋势和原因;根据氢键的表示方法书写(HF) 的结构;根据键能影响物质稳定性的规律分
3
析两种物质的稳定性差异;根据均摊法计算晶胞中各粒子的个数,判断粒子种类。
【小问1详解】
F为第9号元素其电子排布为1s22s22p5,则其价电子排布图为 ,
故答案为 。
【小问2详解】
C、N、O、F四种元素在同一周期,同一周期第一电离能的总体趋势是依次升高的,但由
于N元素的2p能级为半充满状态,因此N元素的第一电离能较C、O两种元素高,因此
C、N、O、F四种元素的第一电离能从小到大的顺序为C