文档内容
2022年全国统一高考化学试卷(全国甲卷)
一、选择题
1. 化学与生活密切相关。下列叙述正确的是
A. 漂白粉与盐酸可混合使用以提高消毒效果 B. 温室气体是形成酸雨的主要物质
C. 棉花、麻和蚕丝均为碳水化合物 D. 干冰可用在舞台上制造“云雾”
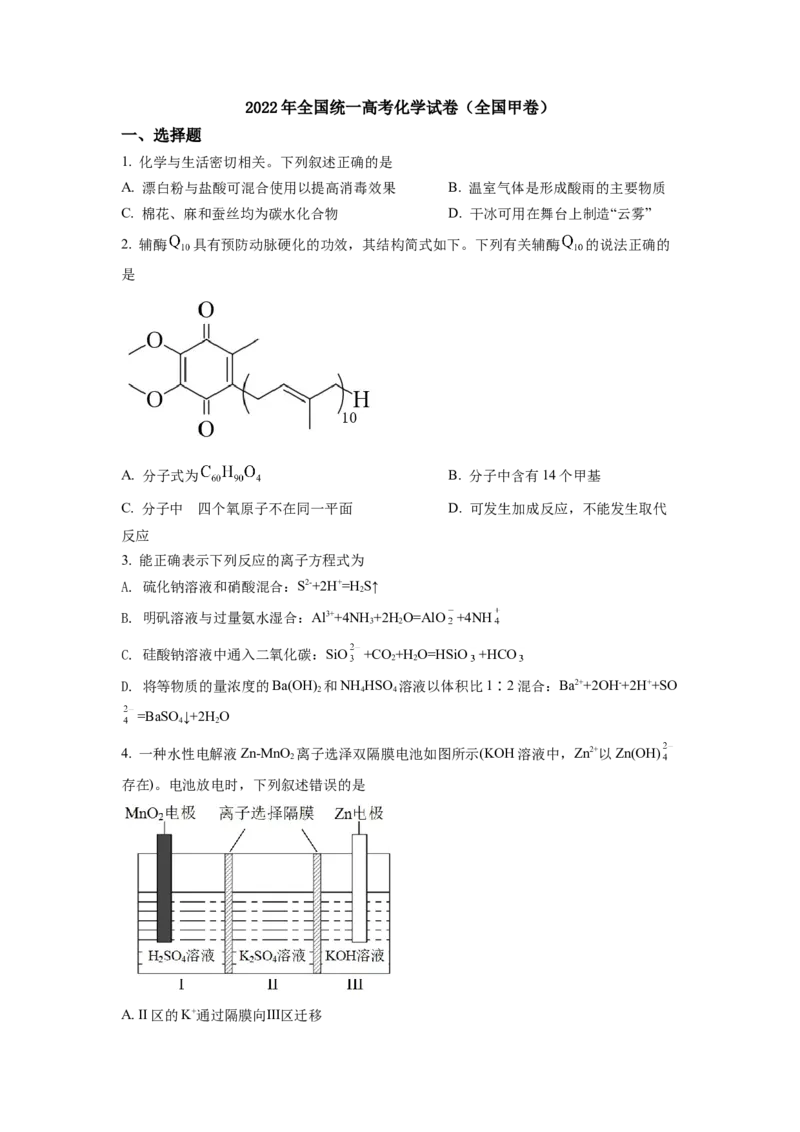
2. 辅酶 具有预防动脉硬化的功效,其结构简式如下。下列有关辅酶 的说法正确的
是
A. 分子式为 B. 分子中含有14个甲基
C. 分子中 四的个氧原子不在同一平面 D. 可发生加成反应,不能发生取代
反应
3. 能正确表示下列反应的离子方程式为
A. 硫化钠溶液和硝酸混合:S2-+2H+=H S↑
2
B. 明矾溶液与过量氨水湿合:Al3++4NH+2H O=AlO +4NH
3 2
C. 硅酸钠溶液中通入二氧化碳:SiO +CO +H O=HSiO +HCO
2 2
D. 将等物质的量浓度的Ba(OH) 和NH HSO 溶液以体积比1∶2混合:Ba2++2OH-+2H++SO
2 4 4
=BaSO ↓+2H O
4 2
4. 一种水性电解液Zn-MnO 离子选泽双隔膜电池如图所示(KOH溶液中,Zn2+以Zn(OH)
2
存在)。电池放电时,下列叙述错误的是
A. Ⅱ区的K+通过隔膜向Ⅲ区迁移B. Ⅰ区的SO 通过隔膜向Ⅱ区迁移
C. MnO 电极反应:MnO +2e-+4H+=Mn2++2H O
2 2 2
D. 电池总反应:Zn+4OH-+MnO+4H+=Zn(OH) +Mn2++2H O
2 2
5. 为阿伏加德罗常数的值,下列说法正确的是
A. 25℃, 下, 氢气中质子的数目为
B. 溶液中, 的数目为
C. 苯甲酸完全燃烧,生成 的数目为
D. 电解熔融 ,阴极增重 ,外电路中通过电子的数目为
6. Q、X、Y、Z是原子序数依次增大的短周期主族元素,其最外层电子数之和为19。Q与
X、Y、Z位于不同周期,X、Y相邻,Y原子最外层电子数是Q原子内层电子数的2倍。
下列说法正确的是
A. 非金属性: B. 单质的熔点:
C. 简单氢化物 佛的点: D. 最高价含氧酸的酸性:
7. 根据实验目的,下列实验及现象、结论都正确的是
选
实验目的 实验及现象 结论
项
分别测浓度均为
的
比较
A 和
和 的水解
常数 溶液的 ,后
者大于前者
将铁锈落于浓盐酸,滴入
检验铁锈中是否
B 铁绣中含有二价铁
含有二价铁 溶液,紫色褪去
探究氢离子浓度
对 、 增大氢离子浓度,转化平衡向生
向 溶液中缓慢滴
C
成 的方向移动
相互转化 加硫酸,黄色变为橙红色
的影响
检验乙醇中是否 向乙醇中加入一小粒金属
D 乙醇中含有水
含有水 钠,产生无色气体A. A B. B C. C D. D
二、非选择题
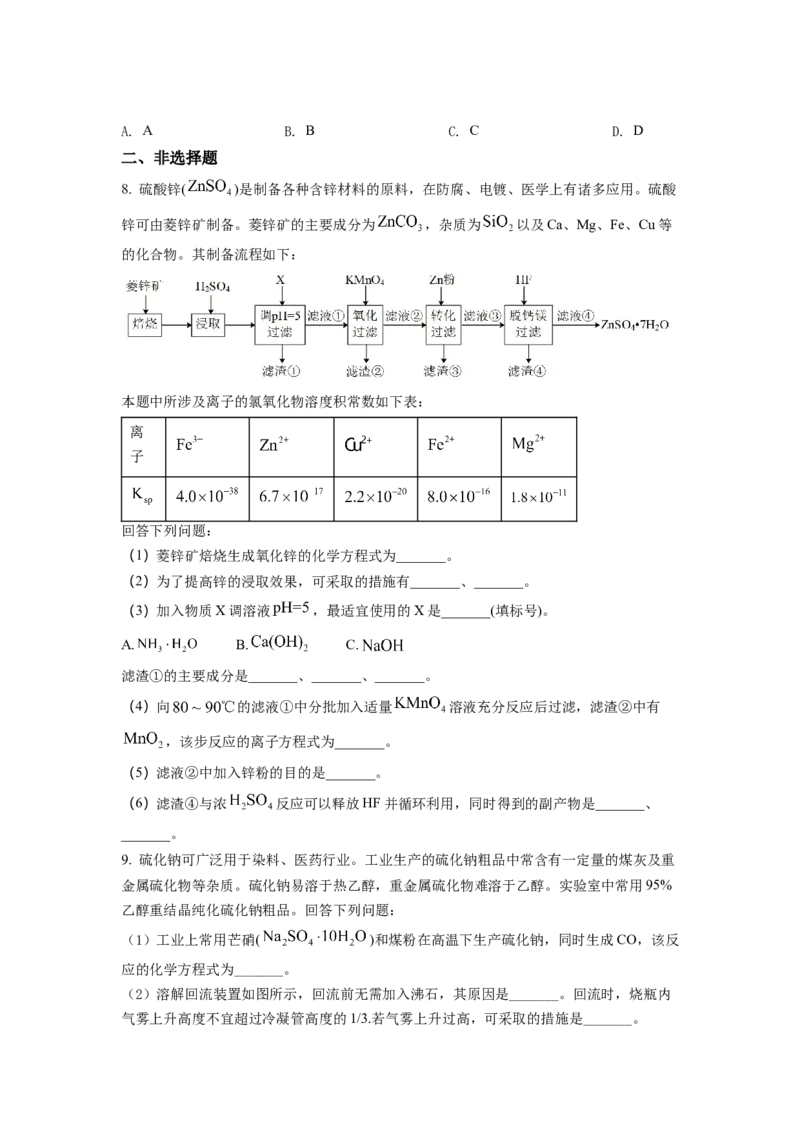
8. 硫酸锌( )是制备各种含锌材料的原料,在防腐、电镀、医学上有诸多应用。硫酸
锌可由菱锌矿制备。菱锌矿的主要成分为 ,杂质为 以及Ca、Mg、Fe、Cu等
的化合物。其制备流程如下:
本题中所涉及离子的氯氧化物溶度积常数如下表:
离
子
回答下列问题:
(1)菱锌矿焙烧生成氧化锌的化学方程式为_______。
(2)为了提高锌的浸取效果,可采取的措施有_______、_______。
(3)加入物质X调溶液 ,最适宜使用的X是_______(填标号)。
A. B. C.
滤渣①的主要成分是_______、_______、_______。
(4)向 的滤液①中分批加入适量 溶液充分反应后过滤,滤渣②中有
,该步反应的离子方程式为_______。
(5)滤液②中加入锌粉的目的是_______。
(6)滤渣④与浓 反应可以释放HF并循环利用,同时得到的副产物是_______、
_______。
9. 硫化钠可广泛用于染料、医药行业。工业生产的硫化钠粗品中常含有一定量的煤灰及重
金属硫化物等杂质。硫化钠易溶于热乙醇,重金属硫化物难溶于乙醇。实验室中常用95%
乙醇重结晶纯化硫化钠粗品。回答下列问题:
(1)工业上常用芒硝( )和煤粉在高温下生产硫化钠,同时生成CO,该反
应的化学方程式为_______。
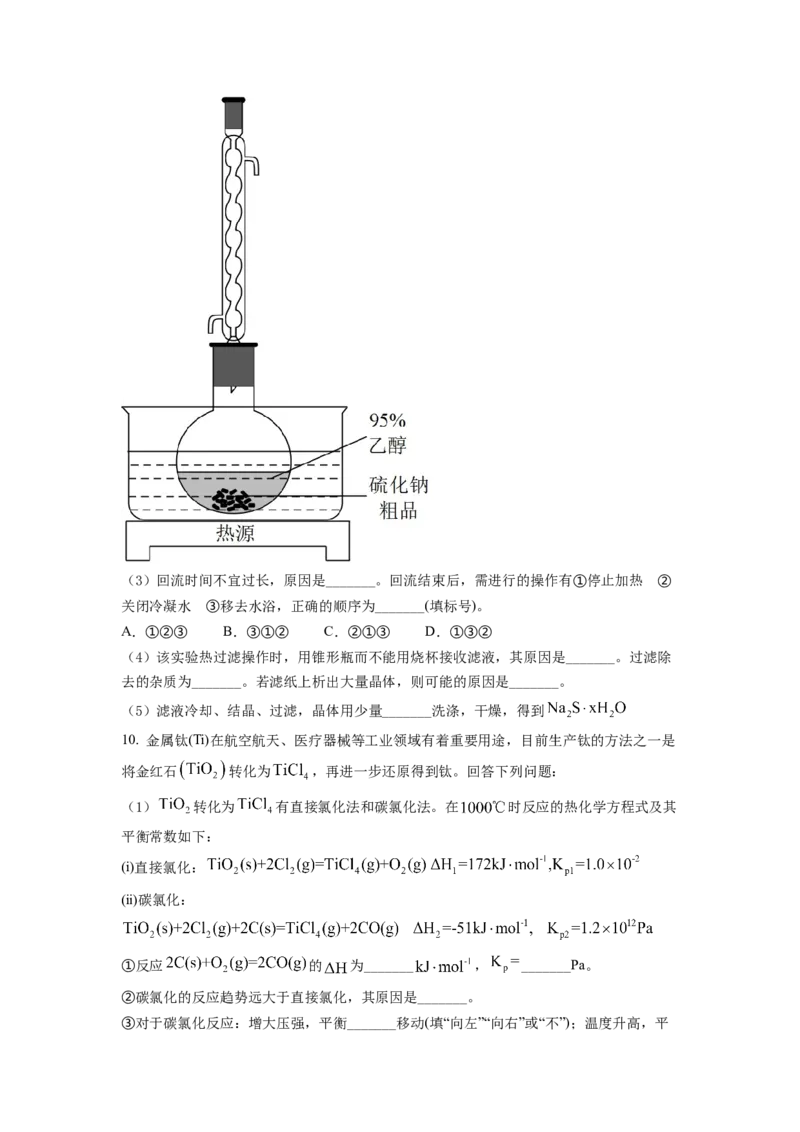
(2)溶解回流装置如图所示,回流前无需加入沸石,其原因是_______。回流时,烧瓶内
气雾上升高度不宜超过冷凝管高度的1/3.若气雾上升过高,可采取的措施是_______。(3)回流时间不宜过长,原因是_______。回流结束后,需进行的操作有①停止加热 ②
关闭冷凝水 ③移去水浴,正确的顺序为_______(填标号)。
A.①②③ B.③①② C.②①③ D.①③②
(4)该实验热过滤操作时,用锥形瓶而不能用烧杯接收滤液,其原因是_______。过滤除
去的杂质为_______。若滤纸上析出大量晶体,则可能的原因是_______。
(5)滤液冷却、结晶、过滤,晶体用少量_______洗涤,干燥,得到 。
10. 金属钛(Ti)在航空航天、医疗器械等工业领域有着重要用途,目前生产钛的方法之一是
将金红石 转化为 ,再进一步还原得到钛。回答下列问题:
(1) 转化为 有直接氯化法和碳氯化法。在 时反应的热化学方程式及其
平衡常数如下:
(ⅰ)直接氯化:
(ⅱ)碳氯化:
①反应 的 为_______ , _______Pa。
②碳氯化的反应趋势远大于直接氯化,其原因是_______。
③对于碳氯化反应:增大压强,平衡_______移动(填“向左”“向右”或“不”);温度升高,平衡转化率_______(填“变大”“变小”或“不变”) 。
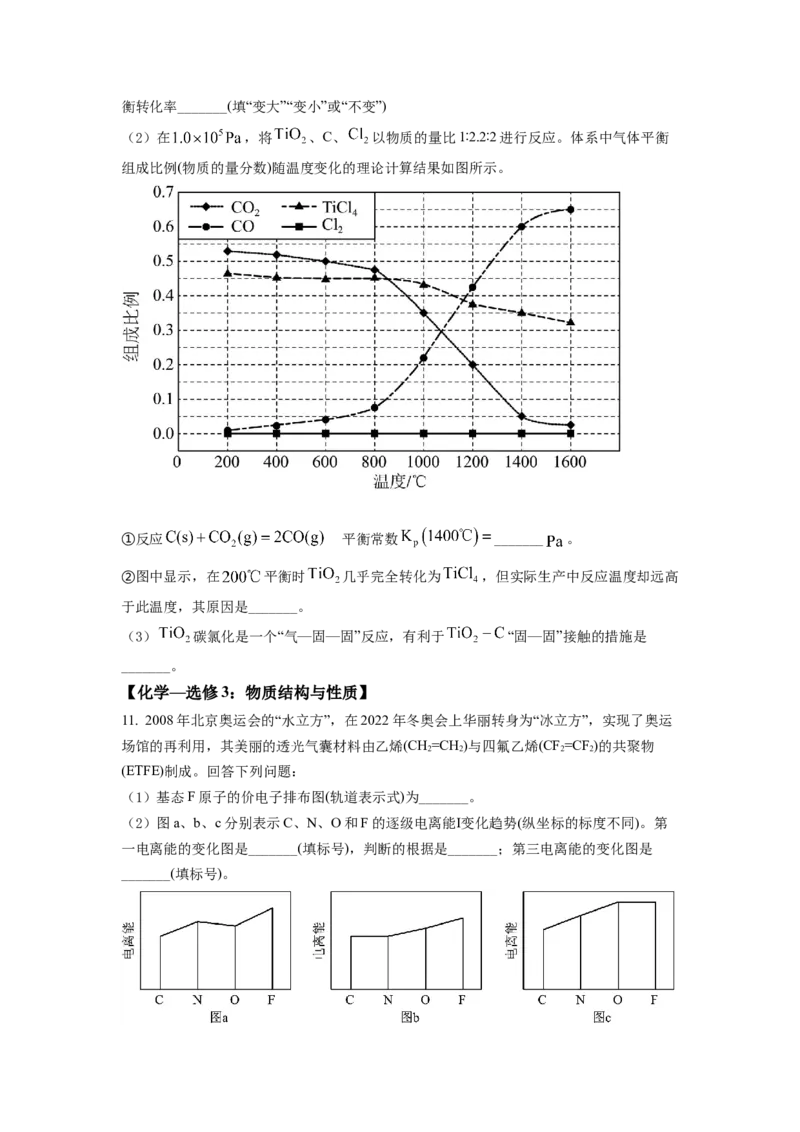
(2)在 ,将 、C、 以物质的量比1∶2.2∶2进行反应。体系中气体平衡
组成比例(物质的量分数)随温度变化的理论计算结果如图所示。
①反应 平的衡常数 _______ 。
②图中显示,在 平衡时 几乎完全转化为 ,但实际生产中反应温度却远高
于此温度,其原因是_______。
(3) 碳氯化是一个“气—固—固”反应,有利于 “固—固”接触的措施是
_______。
【化学—选修3:物质结构与性质】
11. 2008年北京奥运会的“水立方”,在2022年冬奥会上华丽转身为“冰立方”,实现了奥运
场馆的再利用,其美丽的透光气囊材料由乙烯(CH=CH )与四氟乙烯(CF=CF )的共聚物
2 2 2 2
(ETFE)制成。回答下列问题:
(1)基态F原子的价电子排布图(轨道表示式)为_______。
(2)图a、b、c分别表示C、N、O和F的逐级电离能Ⅰ变化趋势(纵坐标的标度不同)。第
一电离能的变化图是_______(填标号),判断的根据是_______;第三电离能的变化图是
_______(填标号)。(3)固态氟化氢中存在(HF) 形式,画出(HF) 的链状结构_______。
n 3
(4) CF=CF 和ETFE分子中C的杂化轨道类型分别为_______和_______;聚四氟乙烯的
2 2
化学稳定性高于聚乙烯,从化学键的角度解释原因_______。
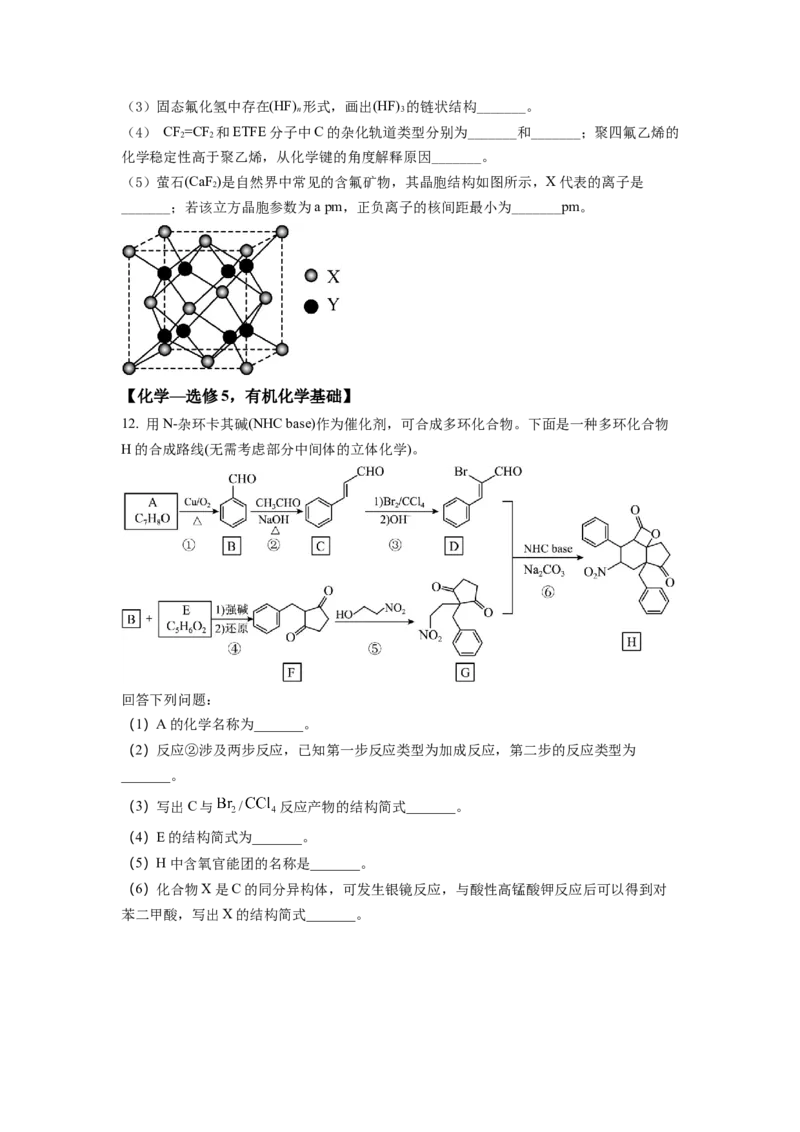
(5)萤石(CaF )是自然界中常见的含氟矿物,其晶胞结构如图所示,X代表的离子是
2
_______;若该立方晶胞参数为a pm,正负离子的核间距最小为_______pm。
【化学—选修5,有机化学基础】
12. 用N-杂环卡其碱(NHC base)作为催化剂,可合成多环化合物。下面是一种多环化合物
H的合成路线(无需考虑部分中间体的立体化学)。
回答下列问题:
(1)A的化学名称为_______。
(2)反应②涉及两步反应,已知第一步反应类型为加成反应,第二步的反应类型为
_______。
(3)写出C与 / 反应产物的结构简式_______。
(4)E的结构简式为_______。
(5)H中含氧官能团的名称是_______。
(6)化合物X是C的同分异构体,可发生银镜反应,与酸性高锰酸钾反应后可以得到对
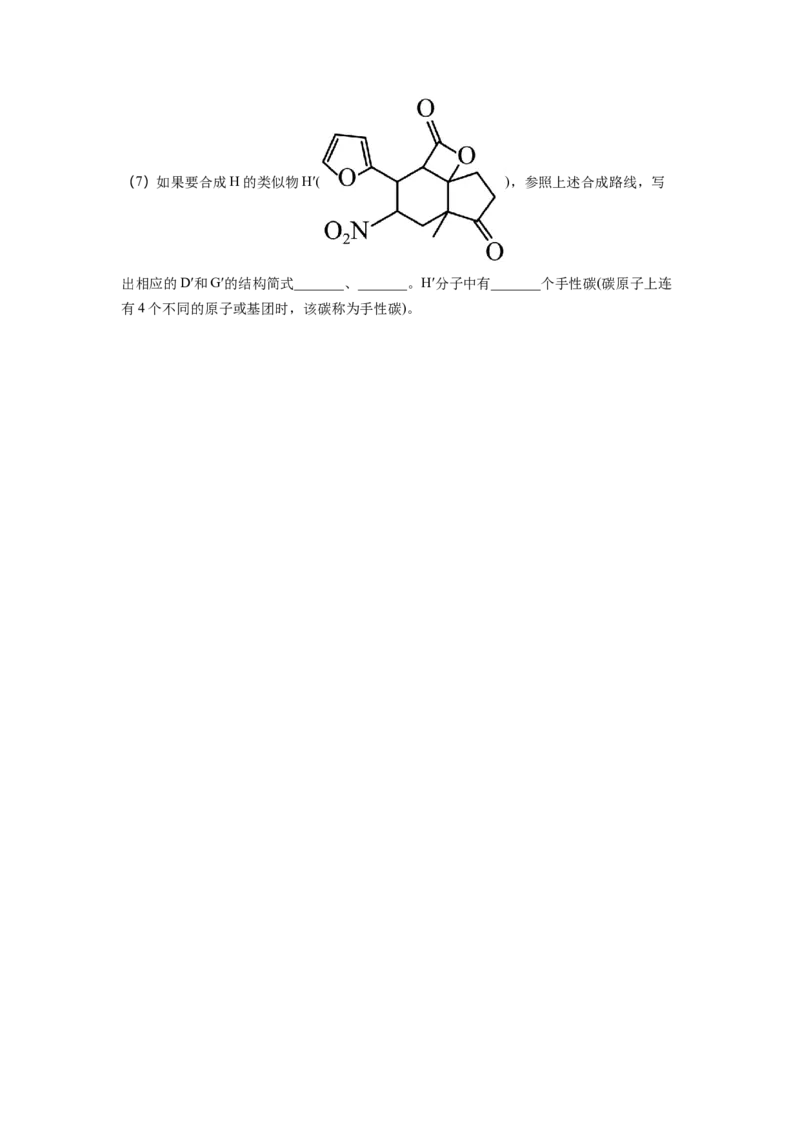
苯二甲酸,写出X的结构简式_______。(7)如果要合成H的类似物H′( ),参照上述合成路线,写
出相应的D′和G′的结构简式_______、_______。H′分子中有_______个手性碳(碳原子上连
有4个不同的原子或基团时,该碳称为手性碳)。