文档内容
关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
专题 17 物质的分离和提纯
知识点一、物质分离和提纯的原则
1.不能与主试剂反应
指所选试剂只与杂质反应,而不能与被提纯的物质反应。如NaOH中混有杂质NaCO,就不能用稀盐
2 3
酸,因稀盐酸和NaCO、NaOH都可以反应,而用Ca(OH) 溶液,就能达到只除去NaCO,保留NaOH
2 3 2 2 3
的目的。
2.不能引入新杂质
指在操作过程中,不能除掉杂质,又引入新杂质。如 NaOH 中混有杂质 NaCO,不能用 BaCl ,因
2 3 2
BaCl +Na CO BaCO ↓+2NaCl,会引入新杂质 NaCl。故要用Ba(OH) 溶液:Ba(OH) +Na CO
2 2 3 3 2 2 2 3
BaCO ↓+2NaOH。
3
3.易分离
指操作结束之后,杂质能与主试剂分开。如CO 中混有杂质CO,就不能用点燃的方法,引入O 虽与
2 2
CO反应生成CO,但O 无法与CO 分离;且CO2量多而CO量少时,也无法点燃。
2 2 2
1关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
知识点二、物质分离和提纯的方法
1.物理方法
方法 适用范围 举例
过滤 不溶固体和液体或可溶固体和不溶固体之间 粗盐提纯、分离NaCl和CaCO 的混合物
3
法 的分离或提纯
结 蒸发结晶:溶解度受温度影响 的物质 从含有少量KNO 的NaCl中提纯NaCl
3
晶 降温结晶(冷却热饱和溶液),适用于溶解度随 从含有少量NaCl的KNO 中提纯KNO
3 3
温度降低而明显 的物质
法
升温结晶,适用于溶解度随温度升高而 的 从石灰水中分离出氢氧化钙
物质
蒸馏 液液混合物中各成分的沸点不同 分离酒精和水的混合物
法
吸附 利用某些物质具有吸附性 活性炭可以除去水中的色素和异味
法
2.化学方法
(1)化气法:向混合物中加入适量的某种试剂,使其中的杂质转变为气体逸出而除去。如
KCl(KCO),可加入适量的 ,将KCO 转化为CO 而除去(K CO+2HCl 2KCl+H O+CO↑)。
2 3 2 3 2 2 3 2 2
CO 中含有杂质CO,可通过灼热的CuO除去CO。
2
(2)化水法:向混合物中加入适量的某种试剂,使其中的杂质转变为水而除去(在通常情况下,水不算
杂质)。如NaCl(NaOH),可加入适量的 ,将NaOH转化为NaCl(NaOH+HCl NaCl+H O)。
2
(3)沉淀法:向混合物的溶液中加入适量的某种试剂,使杂质与该试剂反应转化为沉淀,再过滤除掉
沉淀。如NaNO (NaCl),可加入适量的 溶液,再过滤掉沉淀(NaCl+AgNO AgCl↓+NaNO )。
3 3 3
(4)加热(高温)法:加热(高温)混合物使杂质分解(或变成气体)而除去。如CaO(CaCO),CaCO
3 3
CaO+CO ↑。
2
(5)溶解法:向混合物中加入某种试剂,使杂质与试剂反应而被溶解掉,以除去杂质。
如Cu(CuO),CuO+H SO CuSO +H O。
2 4 4 2
(6)置换法:向混合物中加入一种试剂,利用该试剂与杂质发生置换反应,而将杂质除去。
如FeSO (CuSO ),CuSO+Fe FeSO +Cu。
4 4 4 4
(7)吸收法:将气体混合物通过洗气装置,杂质气体被装置内所盛试剂吸收而除去。如:
① 水蒸气,可用浓硫酸来吸收。
② 酸性气体(CO、SO 、HCl等),可用碱溶液(NaOH溶液)吸收。
2 2
③ 碱性气体(NH 等),可用酸溶液(H SO 溶液)吸收。
3 2 4
2关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
考点一.混合物的分离方法
1.(2023•南平模拟)《本草纲目》中“黄连”条目下记载:“吐血不止,取黄连一两,捣碎,加
鼓二十粒,水煎去渣,温服。”该过程中没有涉及的操作是( )
A.加热 B.称量 C.过滤 D.蒸发结晶
2.(2023•威海模拟)海水淡化常用太阳能蒸馏和膜分离等方法,根据图示回答问题。
(1)太阳能蒸馏的原理如上图图1所示。太阳能蒸馏属于 (物理/化学)变化。太阳能
蒸馏淡化的优点是 。
(2)膜分离的原理上图如图2所示。将海水加压,水分子能透过分离膜,Na+和Cl﹣却不能透过,
一段时间后,右侧海水中氯化钠的质量分数 (变大/变小/不变)。膜分离的原理与化
学实验中物质分离的 (操作方法)相似。
考点二.过滤的原理、方法及其应用(共5小题)
3.(2023•达州)化学是一门以实验为基础的学科,规范的实验操作是实验成功的保障。下列实验
操作正确的是( )
A. 闻药品气味 B. 加热固体
C. 过滤泥水 D. 熄灭酒精灯
3关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
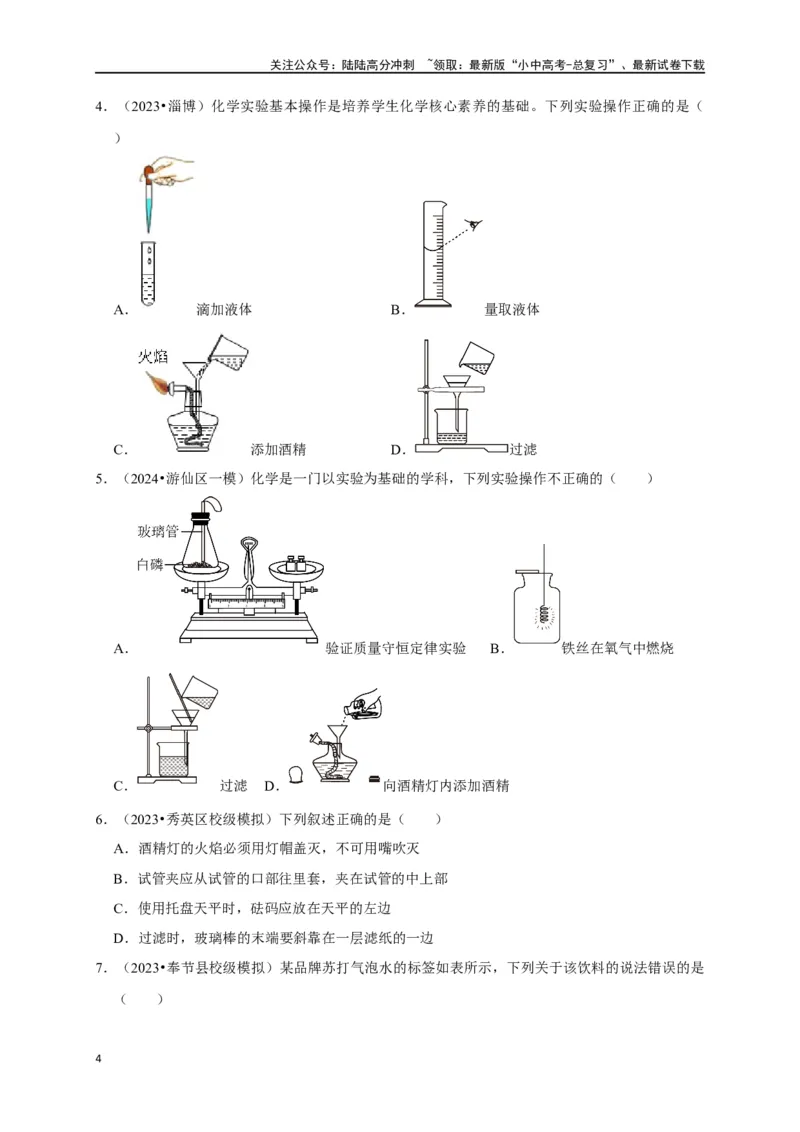
4.(2023•淄博)化学实验基本操作是培养学生化学核心素养的基础。下列实验操作正确的是(
)
A. 滴加液体 B. 量取液体
C. 添加酒精 D. 过滤
5.(2024•游仙区一模)化学是一门以实验为基础的学科,下列实验操作不正确的( )
A. 验证质量守恒定律实验 B. 铁丝在氧气中燃烧
C. 过滤 D. 向酒精灯内添加酒精
6.(2023•秀英区校级模拟)下列叙述正确的是( )
A.酒精灯的火焰必须用灯帽盖灭,不可用嘴吹灭
B.试管夹应从试管的口部往里套,夹在试管的中上部
C.使用托盘天平时,砝码应放在天平的左边
D.过滤时,玻璃棒的末端要斜靠在一层滤纸的一边
7.(2023•奉节县校级模拟)某品牌苏打气泡水的标签如表所示,下列关于该饮料的说法错误的是
( )
4关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
类别:弱酸性饮料,pH≈6.5
配料:水、食用盐、二氧化碳、柠檬酸、碳
酸氢钠等
A.用pH试纸精确测定该饮料的pH
B.整瓶口感一致说明溶液具有均一性
C.过滤不能分离水和碳酸氢钠
D.能补充运动后流失的水和无机盐
考点三.结晶的原理、方法及其应用
8.(2023•秀英区校级模拟)若要从饱和的氯化钠溶液中获得较多的晶体,下列方法中,你认为最
合理的是( )
A.升高溶液的温度
B.蒸发溶剂
C.降低溶液的温度
D.从溶液中倒掉一部分水
9.(2023•瑶海区校级模拟)海洋中蕴藏着丰富的化学资源,按目前测定,海水中含有的化学元素
有 80 多种。氯化钠是海水中的主要成分,氯化钠的溶解度如下表,下列说法不正确的是
( )
温度/℃ 0 10 20 30 40 50
溶解度/g 35.7 35.8 36.0 36.3 36.6 37.0
A.氯化钠易溶于水
B.从氯化钠溶液中得到氯化钠固体,一般采用的方法是蒸发结晶
C.20℃时,将20g氯化钠放入50g水中,搅拌溶解,所得溶液是饱和溶液
D.50℃时,将氯化钠饱和溶液降温至10℃,共析出1.2g氯化钠固体
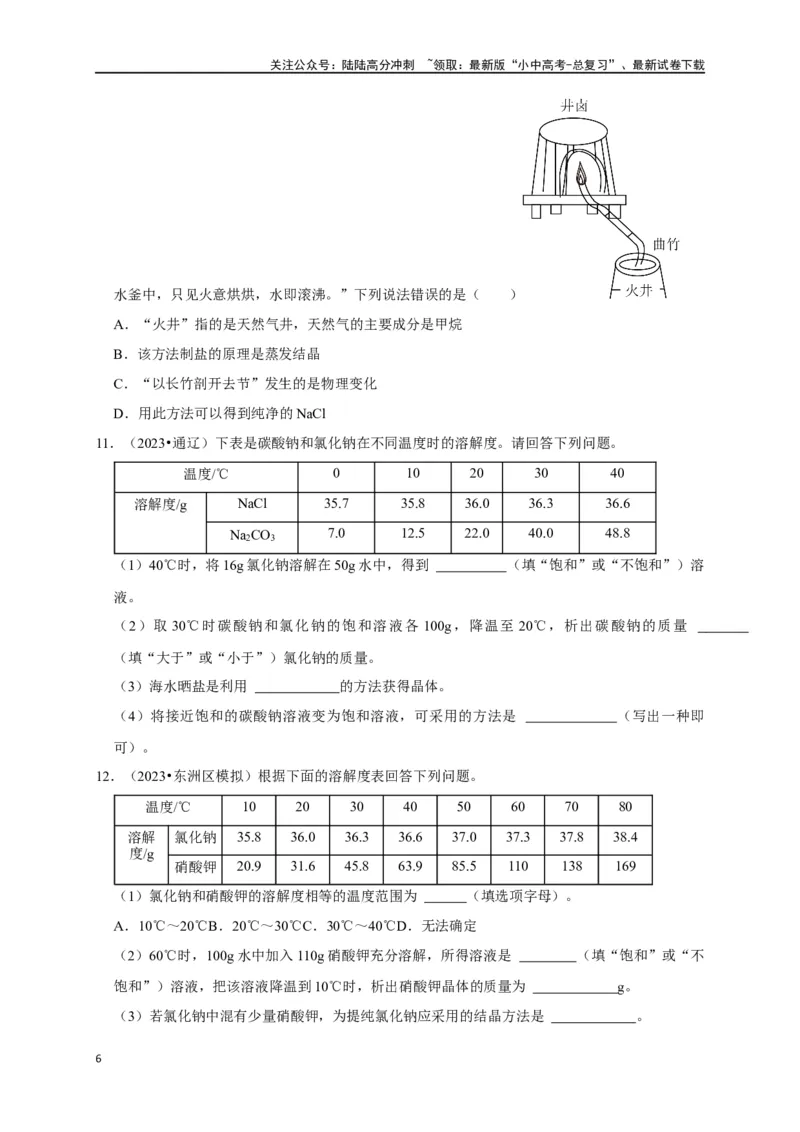
10.(2023•五华区校级模拟)《天工开物》是我国古代的科学技术著作,记载了制盐的场景:
“西川有火井…以长竹剖开去节,合缝漆布,一头插入井底,其上曲接,以口紧对釜脐,注卤
5关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
水釜中,只见火意烘烘,水即滚沸。”下列说法错误的是( )
A.“火井”指的是天然气井,天然气的主要成分是甲烷
B.该方法制盐的原理是蒸发结晶
C.“以长竹剖开去节”发生的是物理变化
D.用此方法可以得到纯净的NaCl
11.(2023•通辽)下表是碳酸钠和氯化钠在不同温度时的溶解度。请回答下列问题。
温度/℃ 0 10 20 30 40
溶解度/g NaCl 35.7 35.8 36.0 36.3 36.6
Na CO 7.0 12.5 22.0 40.0 48.8
2 3
(1)40℃时,将16g氯化钠溶解在50g水中,得到 (填“饱和”或“不饱和”)溶
液。
(2)取 30℃时碳酸钠和氯化钠的饱和溶液各 100g,降温至 20℃,析出碳酸钠的质量
(填“大于”或“小于”)氯化钠的质量。
(3)海水晒盐是利用 的方法获得晶体。
(4)将接近饱和的碳酸钠溶液变为饱和溶液,可采用的方法是 (写出一种即
可)。
12.(2023•东洲区模拟)根据下面的溶解度表回答下列问题。
温度/℃ 10 20 30 40 50 60 70 80
溶解 氯化钠 35.8 36.0 36.3 36.6 37.0 37.3 37.8 38.4
度/g
硝酸钾 20.9 31.6 45.8 63.9 85.5 110 138 169
(1)氯化钠和硝酸钾的溶解度相等的温度范围为 (填选项字母)。
A.10℃~20℃B.20℃~30℃C.30℃~40℃D.无法确定
(2)60℃时,100g水中加入110g硝酸钾充分溶解,所得溶液是 (填“饱和”或“不
饱和”)溶液,把该溶液降温到10℃时,析出硝酸钾晶体的质量为 g。
(3)若氯化钠中混有少量硝酸钾,为提纯氯化钠应采用的结晶方法是 。
6关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
13.(2023•丹东二模)明末科学家宋应星编写的《天工开物》是一部百科全书式的科学巨著。书
中全面、系统地记录了我国古代农业和手工业的生产技术,在科学史上具有很高的价值。
(1)书中记载明矾可用于净水。明矾中含有钾离子,钾离子的符号是 。
(2)“每红铜六斤,入倭铅四斤,先后入罐熔化,冷定取出,即成黄铜”,其中红铜是纯铜,
倭铅是金属锌。得到黄铜的过程是变化 (填“物理”或“化学”)。
(3)造纸:古法造纸的步骤是斩竹漂塘、煮楻足火、荡料入帘、覆帘压纸、透火焙干。“透火
焙干”是将纸张加热焙干,加热时需要将木炭架空燃烧,火才更旺,原因是
。
(4)制盐:“汲水而上,于釜中煎炼,顷刻结盐,色成至白。”该制盐方法中,提纯盐的方法
是 。
14.(2023•碑林区校级模拟)根据不同温度下氯化钠和硝酸钾的溶解度,回答问题:
温度/℃ 0 10 20 30 40 50
溶解度/g NaCl 35.7 35.8 36.0 36.3 36.6 37.0
KNO 13.3 20.9 31.6 45.8 63.9 85.5
3
(1)40℃时,硝酸钾的溶解度为 。
(2)硝酸钾中混有少量氯化钠时,提纯硝酸钾的方法是 (填“降温”或“蒸发”)
结晶。
(3)T℃时NaCl和KNO 具有相同的溶解度mg,则T和m的取值范围是 (填序号)。
3
A.10<T<20,20.9<m<31.6
B.20<T<30,31.6<m<45.8
C.10<T<20,35.8<m<36.0
D.20<T<30,36.0<m<36.3
(4)烧杯①和④中分别盛有50℃时50g的热水,按下列图示操作:
则最终烧杯⑤中析出的固体质量为 g。
15.(2023•本溪模拟)下列表格是氯化钠和硝酸钾在水中的部分溶解度数据,回答下列问题。
℃温度 0 20 40 60 80
7关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
溶解度/g 氯化钠 35.7 36.0 36.6 37.3 38.4
硝酸钾 13.3 31.6 63.9 x 169.0
(1)20℃时,将30gKNO 固体加入到50g水中不断搅拌,得到的溶液是 (填“饱和”
3
或“不饱和”)溶液,若升温到40℃所得溶液的溶质质量分数为 。
(2)若KNO 固体中混有少量的NaCl,可采用 的方法提纯
3
KNO 。
3
(3)为测定x的值,取4份60℃的水各50g,分别加入一定质量的KNO 进行实验,并记录数
3
据如下表:
实验编号 甲 乙 丙 丁
KNO 质量/g 40 50 60 70
3
溶液质量/g 90 100 105 105
由实验可知x的值为 。
考点四.蒸发与蒸馏操作
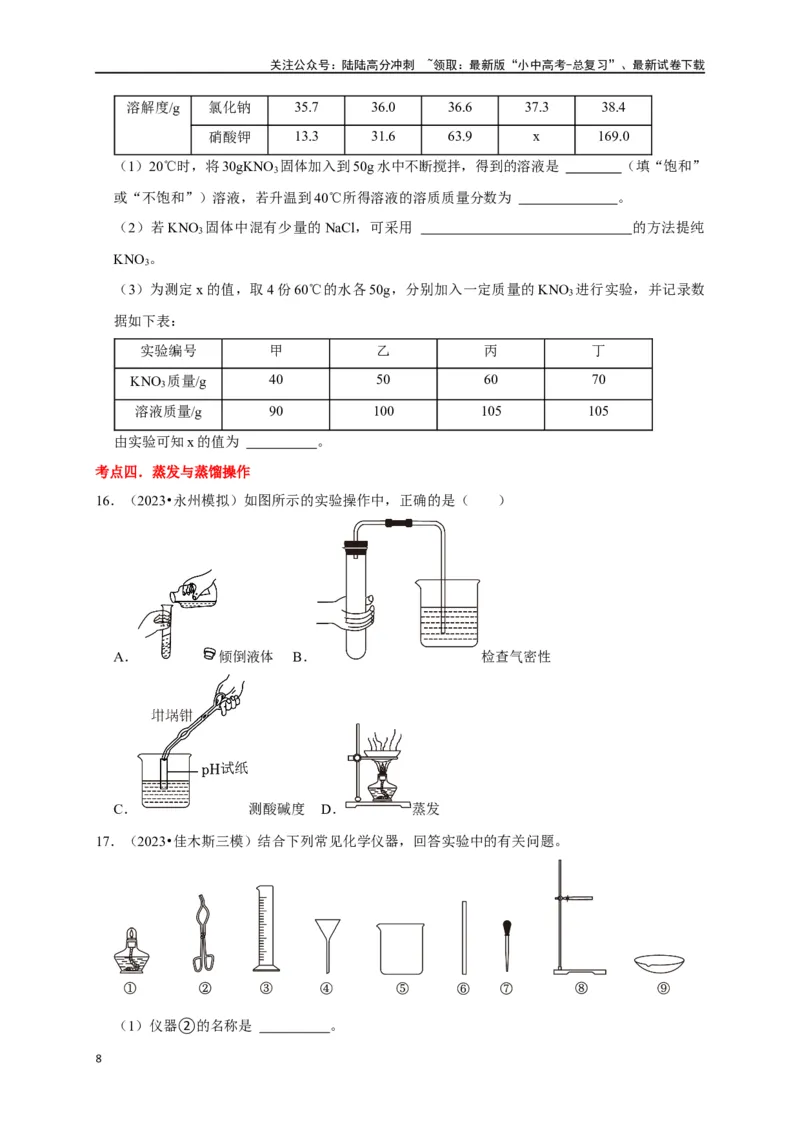
16.(2023•永州模拟)如图所示的实验操作中,正确的是( )
A. 倾倒液体 B. 检查气密性
C. 测酸碱度 D. 蒸发
17.(2023•佳木斯三模)结合下列常见化学仪器,回答实验中的有关问题。
(1)仪器②的名称是 。
8关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(2)在过滤粗盐水时,除用到③⑤⑥⑦⑧,还需要用到图中的一种玻璃仪器是
(填名称)。
(3)做稀盐酸和氢氧化钠溶液中和反应的实验可用到图中的仪器有 (填序号)。
(4)下列有关蒸发结晶操作描述正确的是 。(填字母)
A.当加热至有晶体析出时,停止加热
B.当蒸发皿中出现较多固体时,停止加热
C.当水分完全蒸干时,停止加热
D.蒸发皿应放在陶土网上加热,防止受热不均而炸裂
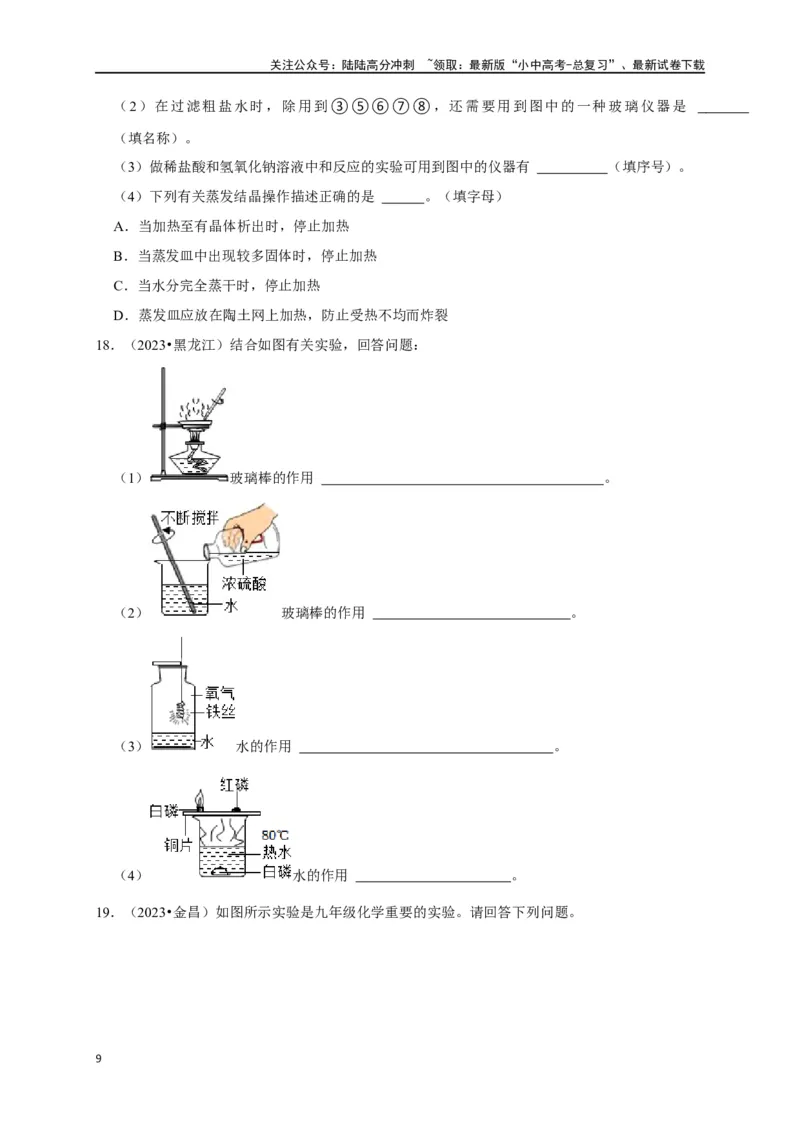
18.(2023•黑龙江)结合如图有关实验,回答问题:
(1) 玻璃棒的作用 。
(2) 玻璃棒的作用 。
(3) 水的作用 。
(4) 水的作用 。
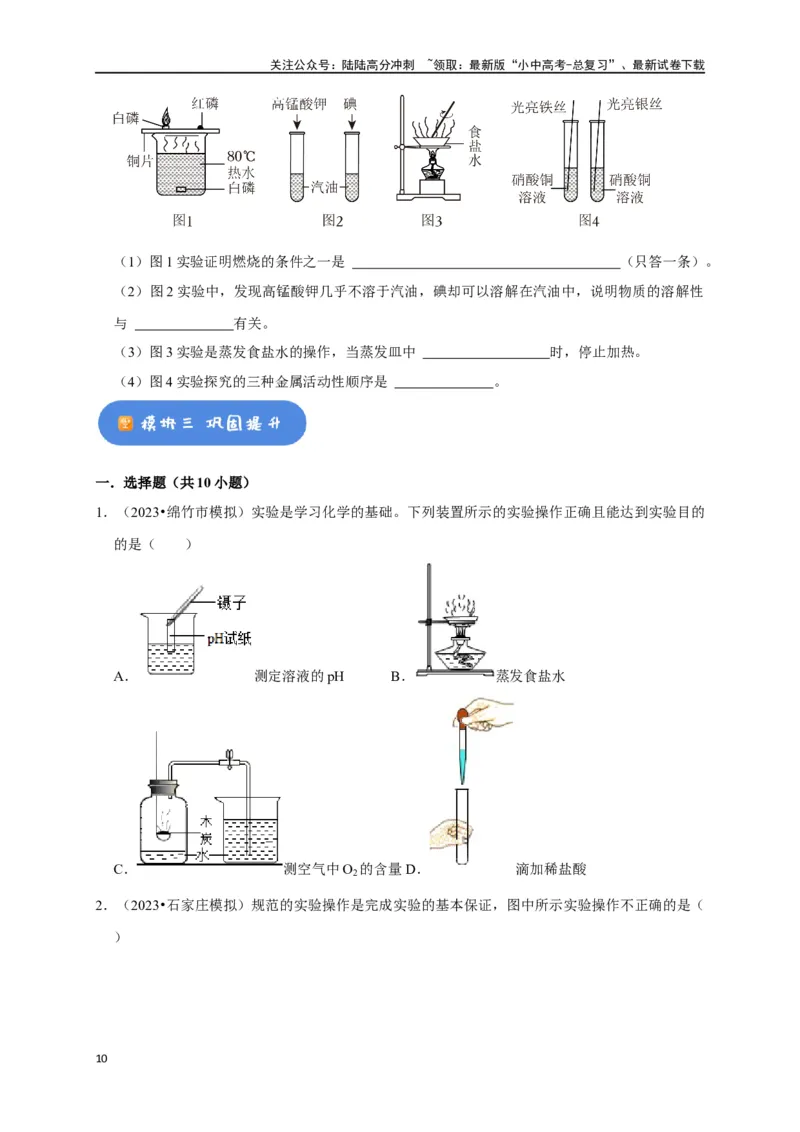
19.(2023•金昌)如图所示实验是九年级化学重要的实验。请回答下列问题。
9关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(1)图1实验证明燃烧的条件之一是 (只答一条)。
(2)图2实验中,发现高锰酸钾几乎不溶于汽油,碘却可以溶解在汽油中,说明物质的溶解性
与 有关。
(3)图3实验是蒸发食盐水的操作,当蒸发皿中 时,停止加热。
(4)图4实验探究的三种金属活动性顺序是 。
一.选择题(共10小题)
1.(2023•绵竹市模拟)实验是学习化学的基础。下列装置所示的实验操作正确且能达到实验目的
的是( )
A. 测定溶液的pH B. 蒸发食盐水
C. 测空气中O 的含量 D. 滴加稀盐酸
2
2.(2023•石家庄模拟)规范的实验操作是完成实验的基本保证,图中所示实验操作不正确的是(
)
10关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
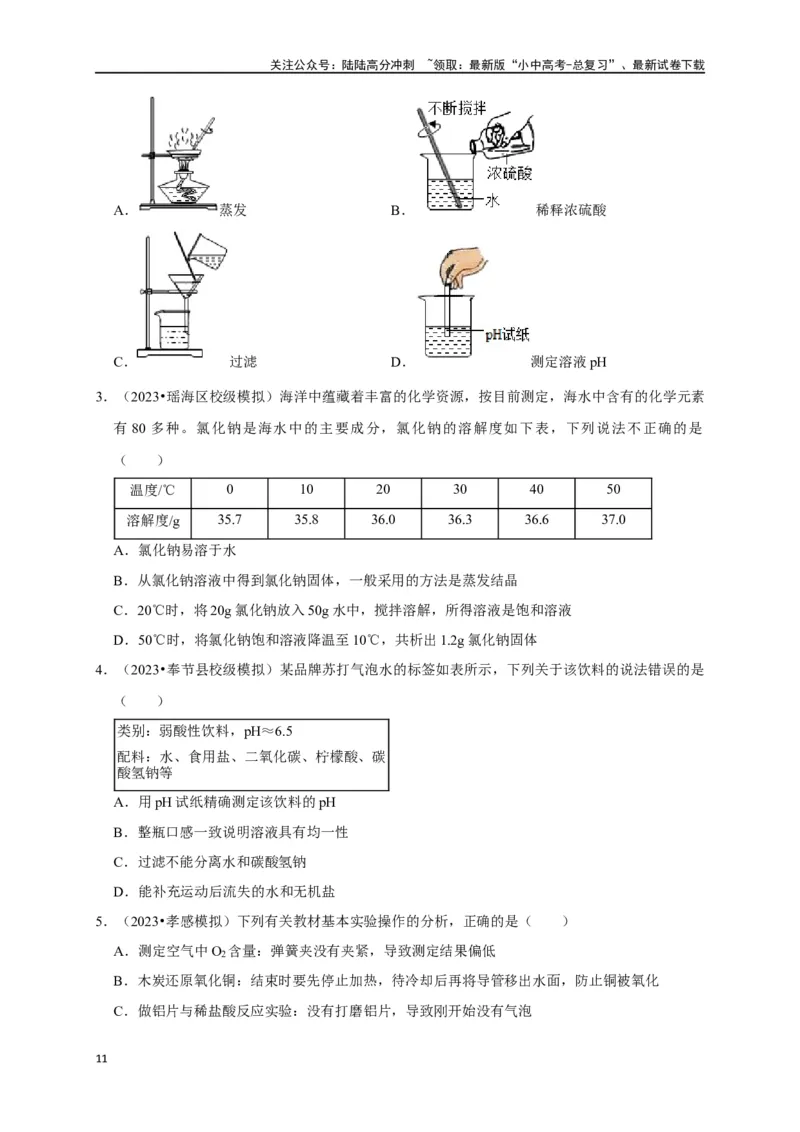
A. 蒸发 B. 稀释浓硫酸
C. 过滤 D. 测定溶液pH
3.(2023•瑶海区校级模拟)海洋中蕴藏着丰富的化学资源,按目前测定,海水中含有的化学元素
有 80 多种。氯化钠是海水中的主要成分,氯化钠的溶解度如下表,下列说法不正确的是
( )
温度/℃ 0 10 20 30 40 50
溶解度/g 35.7 35.8 36.0 36.3 36.6 37.0
A.氯化钠易溶于水
B.从氯化钠溶液中得到氯化钠固体,一般采用的方法是蒸发结晶
C.20℃时,将20g氯化钠放入50g水中,搅拌溶解,所得溶液是饱和溶液
D.50℃时,将氯化钠饱和溶液降温至10℃,共析出1.2g氯化钠固体
4.(2023•奉节县校级模拟)某品牌苏打气泡水的标签如表所示,下列关于该饮料的说法错误的是
( )
类别:弱酸性饮料,pH≈6.5
配料:水、食用盐、二氧化碳、柠檬酸、碳
酸氢钠等
A.用pH试纸精确测定该饮料的pH
B.整瓶口感一致说明溶液具有均一性
C.过滤不能分离水和碳酸氢钠
D.能补充运动后流失的水和无机盐
5.(2023•孝感模拟)下列有关教材基本实验操作的分析,正确的是( )
A.测定空气中O 含量:弹簧夹没有夹紧,导致测定结果偏低
2
B.木炭还原氧化铜:结束时要先停止加热,待冷却后再将导管移出水面,防止铜被氧化
C.做铝片与稀盐酸反应实验:没有打磨铝片,导致刚开始没有气泡
11关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
D.蒸发氯化钠溶液:没有用玻璃棒搅拌,导致蒸发皿炸裂
6.(2023•纳溪区模拟)《本草衍义》中对精制砒霜过程有如下叙述:“取砒之法,将生砒就置火
上,以器覆之,令砒烟上飞着覆器,遂凝结累然下垂如乳,尖长者为胜,平短者次之。”文中
涉及的操作方法是( )
A.蒸馏 B.升华 C.蒸发 D.过滤
7.(2023•桂林二模)下列对有关实验的操作或分析正确的是( )
A.稀释浓硫酸时,将水迅速倒入浓硫酸中,并用玻璃棒搅拌
B.除去粗盐中难溶性杂质的实验中,等蒸发皿中的水全部蒸干才停止加热
C.配制6%的氯化钠溶液,量水时俯视读数,会导致溶液溶质质量分数偏大
D.测定溶液的pH时,若用蒸馏水润湿的pH试纸测量,测得酸性溶液的pH会偏小
8.(2023•高新区校级二模)过滤操作完毕后展开滤纸,若黑色代表滤渣,则看到的情况最接近图
中的( )
A.① B.② C.③ D.④
9.(2023•五华区一模)《天工开物》记载了我国古代废纸回收再造的方法:“废纸洗去朱墨污秽,
浸烂入槽再造……压水去湿,日晒成干而已”。其过程中涉及过滤操作的是( )
A.洗去污秽——用水冲洗表面的墨
B.浸烂入槽——将纸放入水中浸泡,使其腐烂
C.压水去湿——将做好的纸放在竹帘中,滤去水分
D.日晒成干——经过阳光照射蒸发水分
10.(2023•鲤城区校级模拟)规范的操作是实验安全的保证。下列有关实验基本操作中,正确的
是( )
A. 在玻璃管上套上胶皮管B. 收集CO
2
12关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
C. 胶头滴管使用后,用水洗涤,放回原滴瓶
D. 移走蒸发皿
二.填空题(共6小题)
11.(2023•黑龙江二模)化学是一门以实验为基础的科学,化学的许多重大发现和研究成果都是
通过实验得到的,正确规范的操作是实验成功的关键。请回答下列问题。
( 1 ) 倾 倒 液 体 时 , 试 剂 瓶 标 签 要 朝 向 手 心 处 的 原 因 :
。
( 2 ) 给 试 管 中 的 液 体 加 热 时 , 试 管 倾 斜 , 与 桌 面 呈 45° 角 的 理 由 :
。
( 3 ) 熄 灭 酒 精 灯 时 , 通 常 要 用 灯 帽 盖 灭 后 , 提 起 灯 帽 再 盖 一 次 是 为 了 :
。
( 4 ) 过 滤 操 作 时 , 一 定 要 把 引 流 的 玻 璃 棒 轻 靠 在 三 层 滤 纸 一 侧 是 防 止 :
。
12.(2023•常州模拟)水是生命之源,可由多种途径获得水。
Ⅰ.空气制水机能充分利用大气中的水分制出饮用水,其工作原理如下:
(1)①中可阻挡直径 (填“大于”或“小于”)滤孔直径的物质。
(2)③中需吸附色素和异味,常用的物质是 。
Ⅱ.蒸馏法和膜分离法(如图)是两种常用的海水淡化方法。
13关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(3)海水蒸发冷凝得到淡水的过程中,分子的 (选填“空隙”或“种类”)发生了
变化。
(4)图中,加压后钠离子、镁离子等不能通过反渗透膜。
①图中微粒属于原子团的是 。
②一段时间后装置左侧海水中溶质的质量分数会 (填“增大”、“减小”或“不变”)
13.(2023•梁溪区一模)淡化水
(1)冷凝法:海水蒸发冷凝获得淡水,冷凝过程中未发生变化的是 (填字母)。
a.分子的质量
b.分子的种类
c.分子的间隔
(2)膜分离法:海水加压后,水分子能通过反渗透膜,钠离子、镁离子等不能通过,该分离原
理与化学实验中的 操作相似。加压后,海水中钠离子的浓度 。
14.(2022•天宁区校级二模)请从以下选项中选择符合题意的化学术语,并用其序号填空。
A.溶解B.乳化C.催化D.吸附E.结晶
(1)在双氧水中加入少量猪肝以快速获得氧气: ;
(2)刷洗碗筷时,加入洗洁精使碗筷清洗得更洁净: ;
(3)在新车内放置“炭包”,除去可能散发的有害气体: ;
(4)冬天,超市出售的蜂蜜瓶底出现较多的“沉淀”: 。
15.(2022•陇县三模)KNO 和NaCl在不同温度下的溶解度如表所示:
3
14关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
温度/℃ 10 20 30 40 50 60
溶解度 NaCl 35.8 36.0 36.3 36.6 37.0 37.3
KNO 20.9 31.6 45.8 63.9 85.5 110.0
3
(1)20℃时,将NaCl和KNO 各取35.0g,分别加入100g水中,充分溶解,形成不饱和溶液的
3
物质是 。将该不饱和溶液升温至50℃时,溶质和溶剂的质量比为 (填
最简整数比)。
(2)40℃时,将一定质量的KNO 饱和溶液降温至10℃,析出43.0g晶体,则10℃时溶液的质
3
量为 g。
(3)NaCl中混有少量KNO 时,欲得到较纯的NaCl,宜采取的方法是 (填“蒸
3
发结晶”或“降温结晶”)。
16.(2022•长春模拟)根据NaCl和KNO 的溶解度数据表,回答下列问题:
3
温度/℃ 0 10 20 30 40 50 60 70
溶 解 NaCl 35.7 35.8 36.0 36.3 36.6 37.0 37.3 37.8
度/g
KNO 13.3 20.9 31.6 45.8 63.9 85.5 110 138
3
(1)10℃时,NaCl的溶解度是 g;
(2)30℃时,溶解度较大的是 (选填“NaCl”或“KNO
3
”);
(3)20℃时,将10gKNO 溶解在50g水中,若变成20℃的饱和溶液,至少需要再加入KNO
3 3
g;
(4)根据NaCl的溶解度表可知,从海水中提取氯化钠,通常采用的方法是 (选
填“降温结晶”或“蒸发结晶”)。
15