文档内容
天津市南开中学 2024-2025 学年度第一学期
高三年级 化学学科 第一次月考
I卷 (共计 36分)
可能用到的相对原子质量:
一、选择题(每小题只有一个最佳选项,共12小题)
1. 景德镇青花瓷素有“国瓷”的美誉。是以黏土为原料,用含钴、铁的颜料着色,上釉后一次性高温烧制而
成的青蓝色彩瓷。下列关于青花瓷说法正确的是
的
A. 青蓝色是由于生成了单质钴 B. 表面 釉属于有机高分子膜
C. 主要成分为铝硅酸盐 D. 铁元素的存在形式只有Fe O
2 3
2. 下列对所涉及化学知识的叙述错误的是
A. “天宫”空间站新补充了一批氙推进剂,氙 是非金属
B. “天舟六号”壳体使用了铝合金,合金是金属材料
C. “长征七号”采用了液氧煤油发动机,煤油是混合物
D. “嫦娥五号”取回的月壤样品中含有天然玻璃,玻璃是无机非金属材料
3. 下列常见物质及用途,错误的是
A. 氢氧化铝可用于治疗胃酸过多
B. 液氨可用作制冷剂
C. FeO是铁红,可以用作染料
.
D NaO 能与CO 反应, 可作供氧剂
2 2 2
4. 下列各组物质的鉴别方法中,不可行的是
A. 过氧化钠和硫黄:加水,振荡
B. 硫化亚铁和硫化铜:加硫酸,振荡
C. 氯化铁溶液和碘水:加 或淀粉
D. 氢氧化镁和氢氧化铝:加氨水,振荡
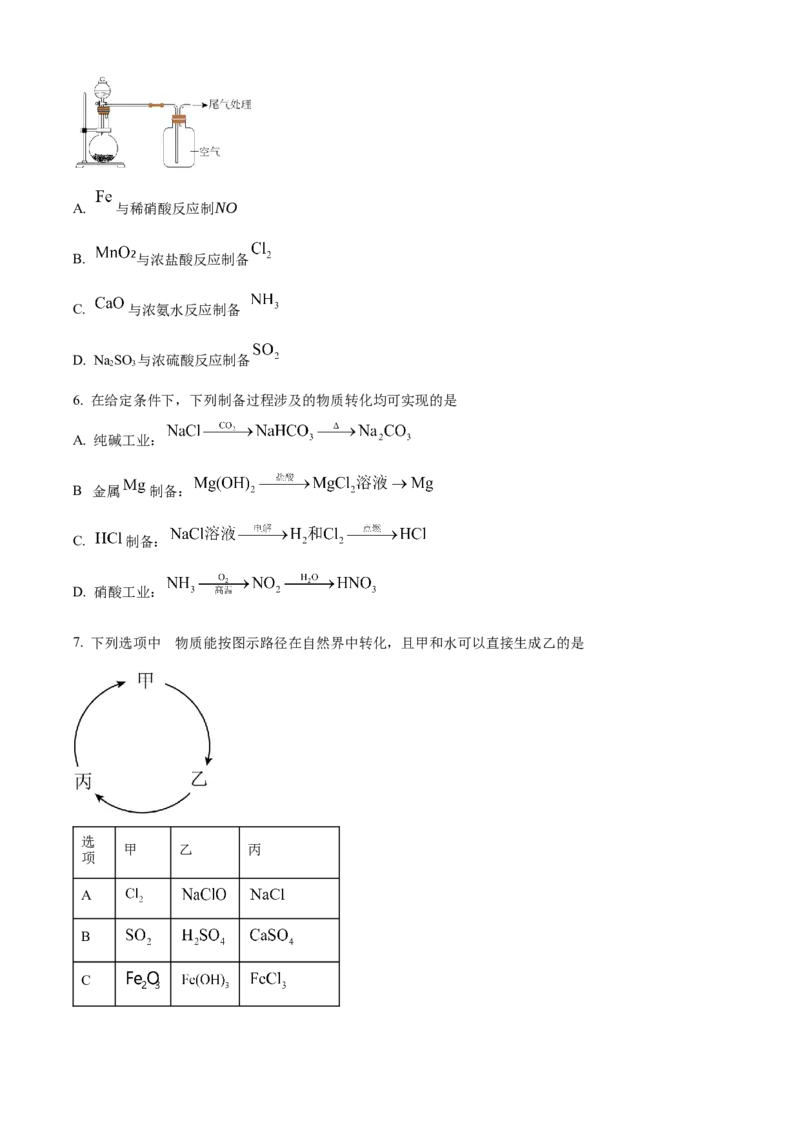
5. 实验室制备和收集相应气体可使用下图装置的是A. 与稀硝酸反应制NO
B. 与浓盐酸反应制备
C. 与浓氨水反应制备
D. NaSO 与浓硫酸反应制备
2 3
6. 在给定条件下,下列制备过程涉及的物质转化均可实现的是
A. 纯碱工业:
.
B 金属 制备:
C. 制备:
D. 硝酸工业:
的
7. 下列选项中 物质能按图示路径在自然界中转化,且甲和水可以直接生成乙的是
选
甲 乙 丙
项
A
B
CD
A. A B. B C. C D. D
8. 下列叙述正确的是
A. SO 具有还原性,因此不能用浓硫酸干燥
2
B. SO 有毒,不可用于食品添加剂
2
C. SO 与氧气混合, 可制得SO
2 3
D. SO 通入过量碳酸钠溶液中,生成碳酸氢钠和亚硫酸钠
2
9. 兴趣小组设计了从 中提取 的实验方案,下列说法正确的是
A. 溶液①中的金属离子是 Fe2+
B. 反应①的离子方程式是
C. 前2步反应均利用了平衡移动原理
D. 按上述方案消耗 可回收
10. 过量 与以下 的溶液反应,下列总反应方程式错误的是
溶液 现象 化学方程式
A 产生淡黄色沉淀
B 溶液由棕黄色变浅绿色
溶液褪色,产生白色沉
C
淀
D (含酚酞) 溶液由红色变无色
A. A B. B C. C D. D
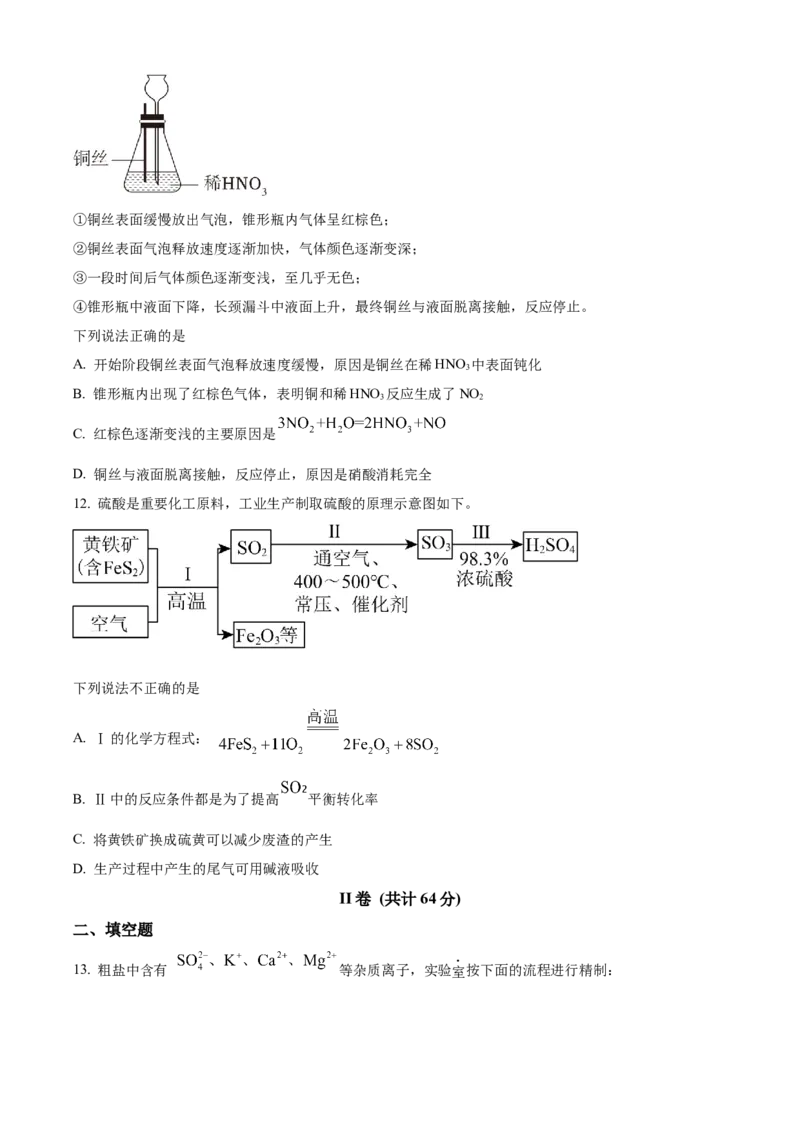
11. 某学生按图示方法进行实验,观察到以下实验现象:①铜丝表面缓慢放出气泡,锥形瓶内气体呈红棕色;
②铜丝表面气泡释放速度逐渐加快,气体颜色逐渐变深;
③一段时间后气体颜色逐渐变浅,至几乎无色;
④锥形瓶中液面下降,长颈漏斗中液面上升,最终铜丝与液面脱离接触,反应停止。
下列说法正确的是
A. 开始阶段铜丝表面气泡释放速度缓慢,原因是铜丝在稀HNO 中表面钝化
3
B. 锥形瓶内出现了红棕色气体,表明铜和稀HNO 反应生成了NO
3 2
C. 红棕色逐渐变浅的主要原因是
D. 铜丝与液面脱离接触,反应停止,原因是硝酸消耗完全
12. 硫酸是重要化工原料,工业生产制取硫酸的原理示意图如下。
下列说法不正确的是
A. Ⅰ的化学方程式:
B. Ⅱ中的反应条件都是为了提高 平衡转化率
C. 将黄铁矿换成硫黄可以减少废渣的产生
D. 生产过程中产生的尾气可用碱液吸收
II卷 (共计64分)
二、填空题
13. 粗盐中含有 等杂质离子,实验室按下面的流程进行精制:已知: 的溶解度如图所示:
(1)证明该粗盐中含有 的方法为_______。
(2)步骤①中 要稍过量。请描述检验) 已过量的方法:_______。
(3)若加 后不先过滤就加氢氧化钠和碳酸钠,会导致_______。
A. 不能完全去除 B. 消耗更多
C. 不能完全去除 D. 消耗更多
(4)“一系列操作”是指_______。
A. 蒸发至晶膜形成后,趁热过滤 B. 蒸发至晶膜形成后,冷却结晶
C. 蒸发至大量晶体析出后,趁热过滤 D. 蒸发至大量晶体析出后,冷却结晶
(5)用离子方程式表示加入盐酸后发生的反应_______。
另有两种方案进行粗盐提纯:
方案2:向粗盐水中加入石灰乳[主要成分为 除去 再通入含 的工业废气除
去
方案3:向粗盐水中加入石灰乳除去 再加入碳酸钠溶液除去
(6)相比于方案3,方案2的优点是_______。(7)已知粗盐水中 含量为 含量为 现用方案3提纯10L该粗盐水,求
需要加入碳酸钠的物质的量_______。
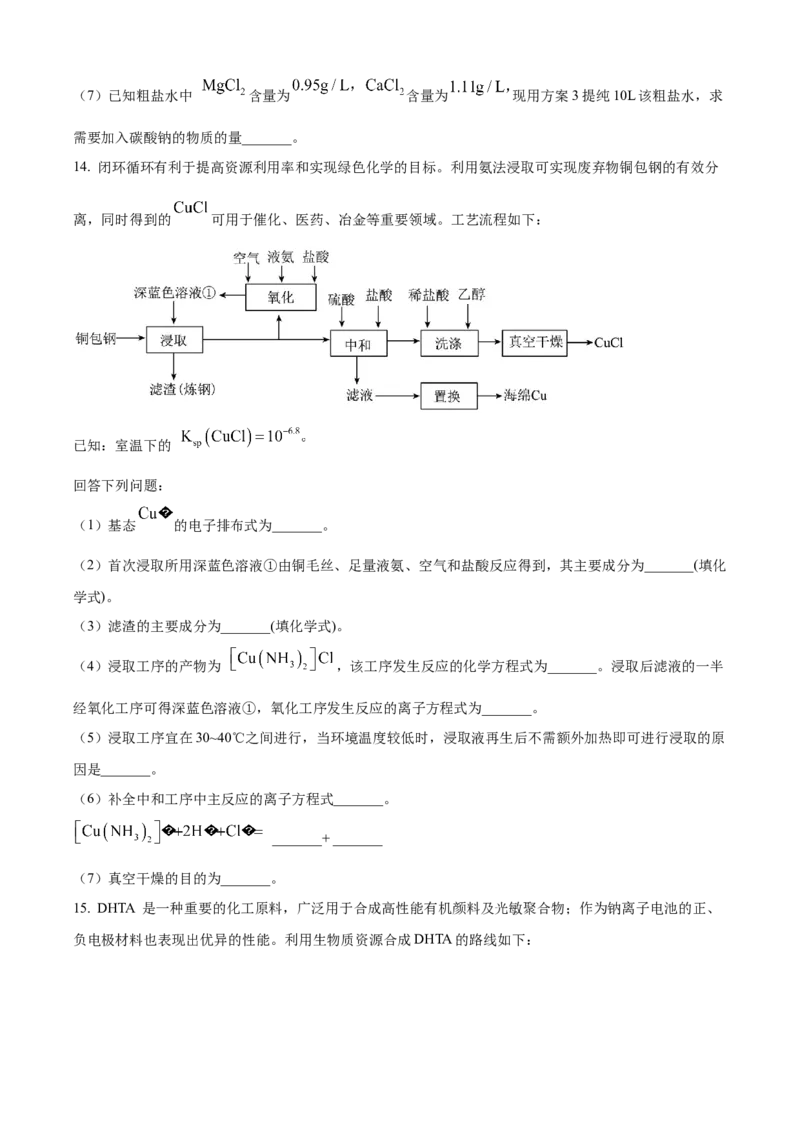
14. 闭环循环有利于提高资源利用率和实现绿色化学的目标。利用氨法浸取可实现废弃物铜包钢的有效分
离,同时得到的 可用于催化、医药、冶金等重要领域。工艺流程如下:
已知:室温下的
回答下列问题:
(1)基态 的电子排布式为_______。
(2)首次浸取所用深蓝色溶液①由铜毛丝、足量液氨、空气和盐酸反应得到,其主要成分为_______(填化
学式)。
(3)滤渣的主要成分为_______(填化学式)。
(4)浸取工序的产物为 ,该工序发生反应的化学方程式为_______。浸取后滤液的一半
经氧化工序可得深蓝色溶液①,氧化工序发生反应的离子方程式为_______。
(5)浸取工序宜在30~40℃之间进行,当环境温度较低时,浸取液再生后不需额外加热即可进行浸取的原
因是_______。
(6)补全中和工序中主反应的离子方程式_______。
_______+ _______
(7)真空干燥的目的为_______。
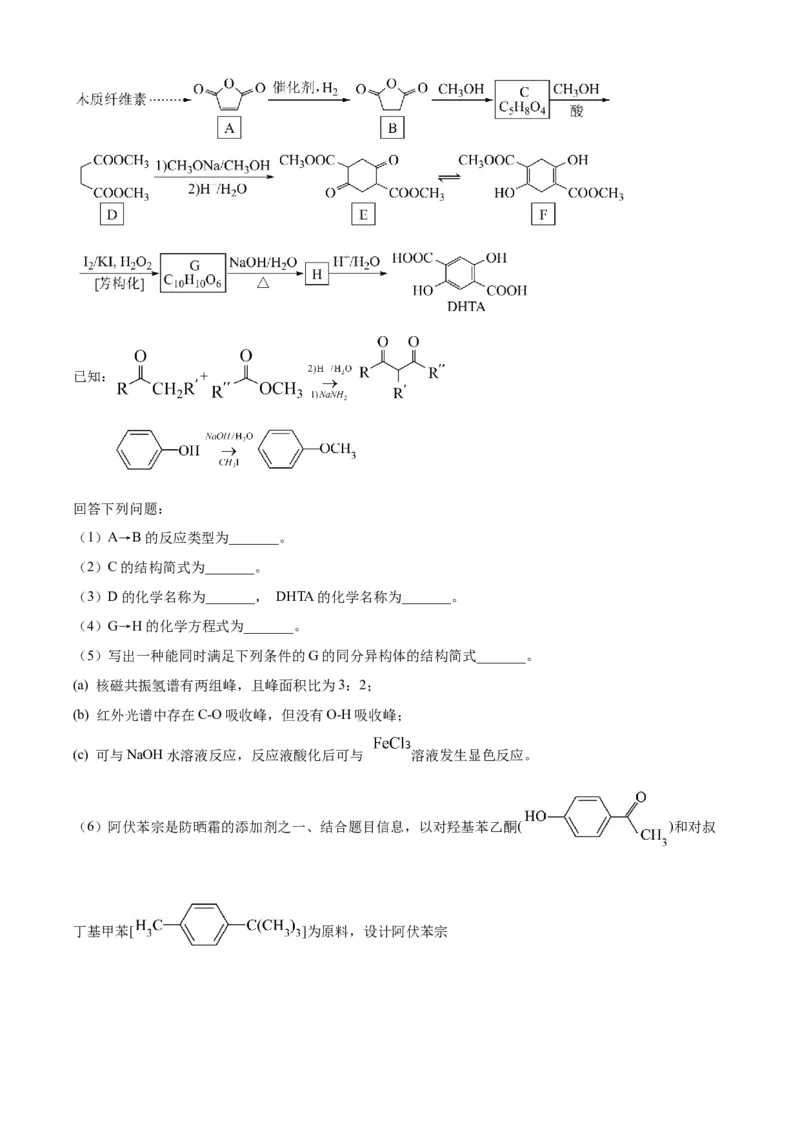
15. DHTA 是一种重要的化工原料,广泛用于合成高性能有机颜料及光敏聚合物;作为钠离子电池的正、
负电极材料也表现出优异的性能。利用生物质资源合成DHTA的路线如下:已知: +
回答下列问题:
(1)A→B的反应类型为_______。
(2)C的结构简式为_______。
(3)D的化学名称为_______, DHTA的化学名称为_______。
(4)G→H的化学方程式为_______。
(5)写出一种能同时满足下列条件的G的同分异构体的结构简式_______。
(a) 核磁共振氢谱有两组峰,且峰面积比为3:2;
(b) 红外光谱中存在C-O吸收峰,但没有O-H吸收峰;
(c) 可与NaOH水溶液反应,反应液酸化后可与 溶液发生显色反应。
(6)阿伏苯宗是防晒霜的添加剂之一、结合题目信息,以对羟基苯乙酮( )和对叔
丁基甲苯[ ]为原料,设计阿伏苯宗的合成路线_______。 (无机试剂和三个碳以下的有机试
剂任选)
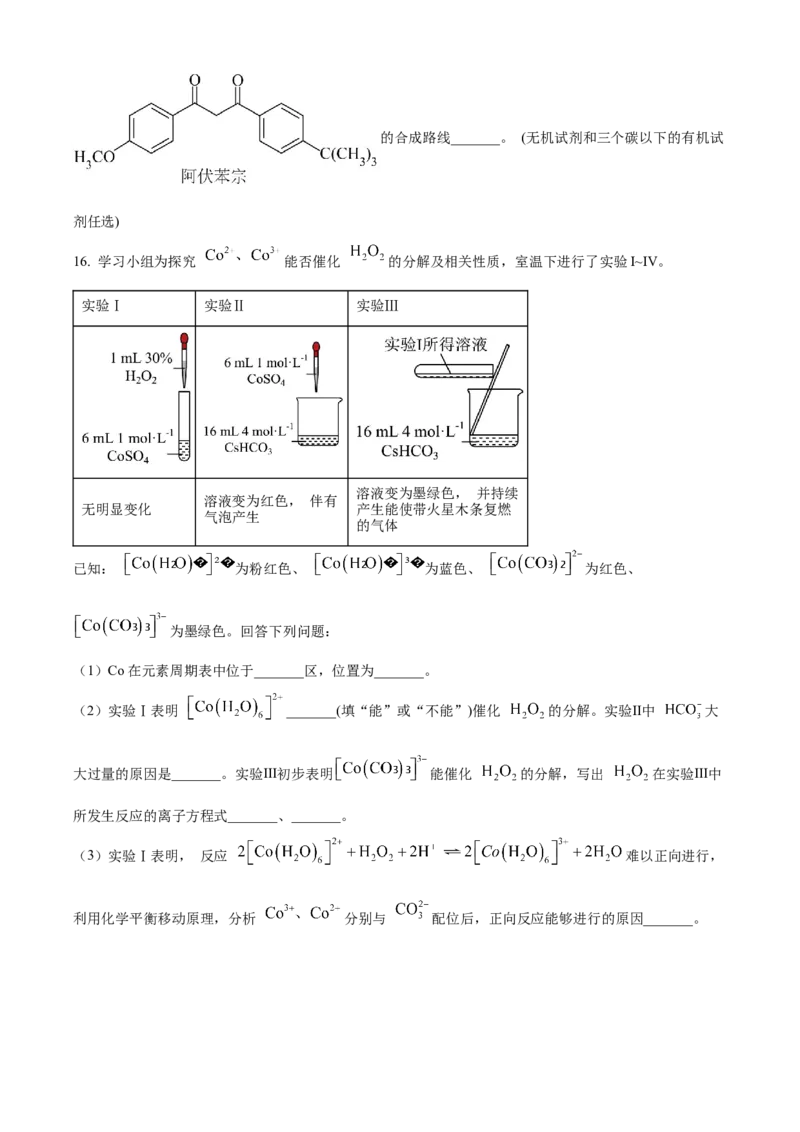
16. 学习小组为探究 能否催化 的分解及相关性质,室温下进行了实验I~Ⅳ。
实验Ⅰ 实验Ⅱ 实验Ⅲ
溶液变为墨绿色, 并持续
溶液变为红色, 伴有
无明显变化 产生能使带火星木条复燃
气泡产生
的气体
已知: 为粉红色、 为蓝色、 为红色、
为墨绿色。回答下列问题:
(1)Co在元素周期表中位于_______区,位置为_______。
(2)实验Ⅰ表明 _______(填“能”或“不能”)催化 的分解。实验Ⅱ中 大
大过量的原因是_______。实验Ⅲ初步表明 能催化 的分解,写出 在实验Ⅲ中
所发生反应的离子方程式_______、_______。
(3)实验Ⅰ表明, 反应 难以正向进行,
利用化学平衡移动原理,分析 分别与 配位后,正向反应能够进行的原因_______。实验Ⅳ:
(4)实验Ⅳ中,A到B 溶液变为蓝色,并产生气体; B到C溶液变为粉红色,并产生气体。从A到C
所产生的气体的分子式分别为_______、_______。