文档内容
微信:cs5311742016 主营各地名校期中期末真题卷及小初高全套教材教案讲义知识点总结
北京二中教育集团 2023-2024 学年初三下学期阶段检测(三)
化学试题
可能用到的相对原子质量:H1 C12 O16 Na23 C135.5
第一部分
本部分共25题,每题1分,共25分。在每题列出的四个选项中,选出最符合题目要求的一
项。
化学与生活、生产息息相关。回答1~8题。
1. 下列不属于化石燃料的是( )
A. 天然气 B. 石油 C. 煤 D. 乙醇
2. 化学元素与人体健康密切相关。为了防止骨质疏松应适当摄入的元素是
A. 钙 B. 铁 C. 锌 D. 硒
3. 下列物质的主要成分属于氧化物的是( )
A. 钻石(C)B. 水晶(SiO) C. 食
2
盐(NaCl) D. 钟乳石(CaCO )
3
4. “垃圾是放错位置的资源”,垃圾分类人人有责。矿泉水瓶、易拉罐属于
A. B. C. D.
5. 下列不是NaOH俗称的是
A. 烧碱 B. 火碱 C. 纯碱 D. 苛性钠
6. 下列净水方法中,净化程度最高的是
A. 蒸馏 B. 消毒 C. 吸附 D. 沉淀
7. 切洋葱时可闻到刺激性气味,这说明
A. 分子在不断运动 B. 分子的质量很小
C. 分子之间有间隔 D. 分子的体积很小
微信:cs5311742016 主营各地名校期中期末真题卷及小初高全套教材教案讲义知识点总结微信:cs5311742016 主营各地名校期中期末真题卷及小初高全套教材教案讲义知识点总结
8. 下列物质的用途不正确的是
A. 用CO 作气体肥料 B. 用碳酸钙作补钙剂
2
C. 用浓硫酸作食品干燥剂 D. 用稀有气体作电光源
氧气是人类生命活动的重要物质。回答9~11题。
9. 空气成分中,体积分数最大的是( )
A. 氮气 B. 二氧化碳 C. 氧气 D. 稀有气体
10. 下列氧气的性质中,属于化学性质的是
A. 无色无味 B. 密度大于空气 C. 能支持燃烧 D. 沸点低
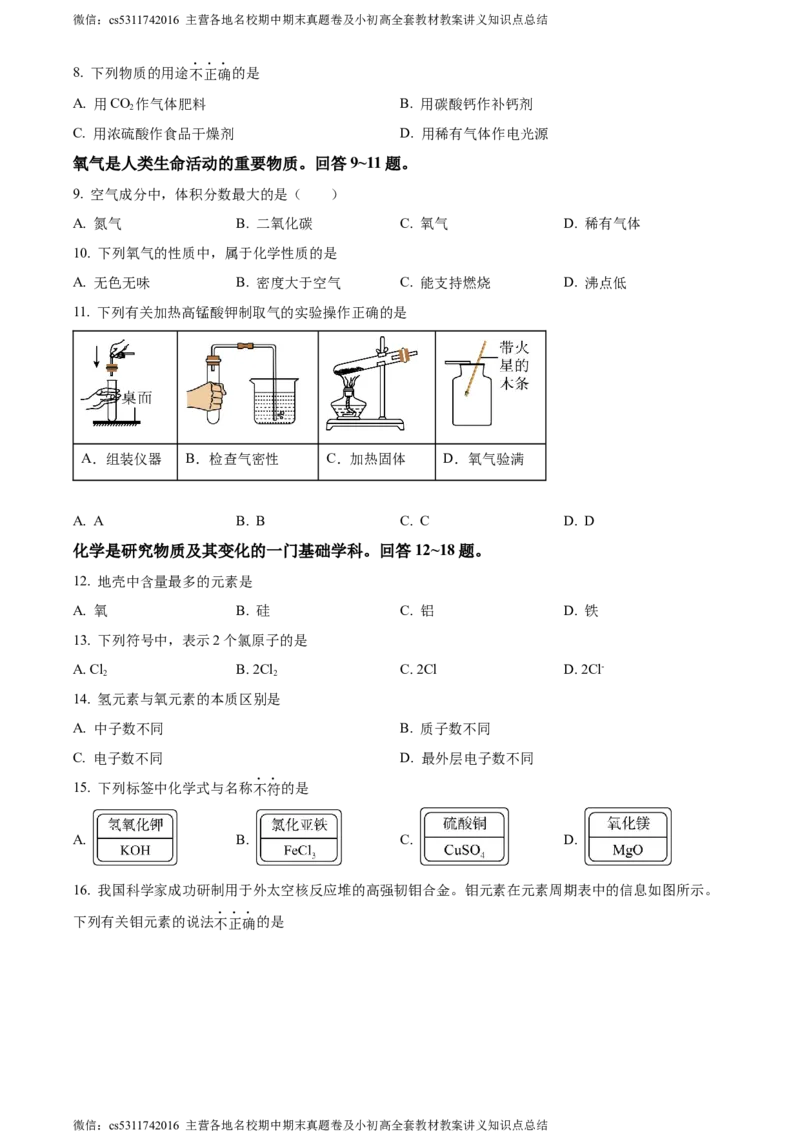
11. 下列有关加热高锰酸钾制取气的实验操作正确的是
A.组装仪器 B.检查气密性 C.加热固体 D.氧气验满
A. A B. B C. C D. D
化学是研究物质及其变化的一门基础学科。回答12~18题。
12. 地壳中含量最多的元素是
A. 氧 B. 硅 C. 铝 D. 铁
13. 下列符号中,表示2个氯原子的是
A. Cl B. 2Cl C. 2Cl D. 2Cl-
2 2
14. 氢元素与氧元素的本质区别是
A. 中子数不同 B. 质子数不同
C. 电子数不同 D. 最外层电子数不同
15. 下列标签中化学式与名称不符的是
A. B. C. D.
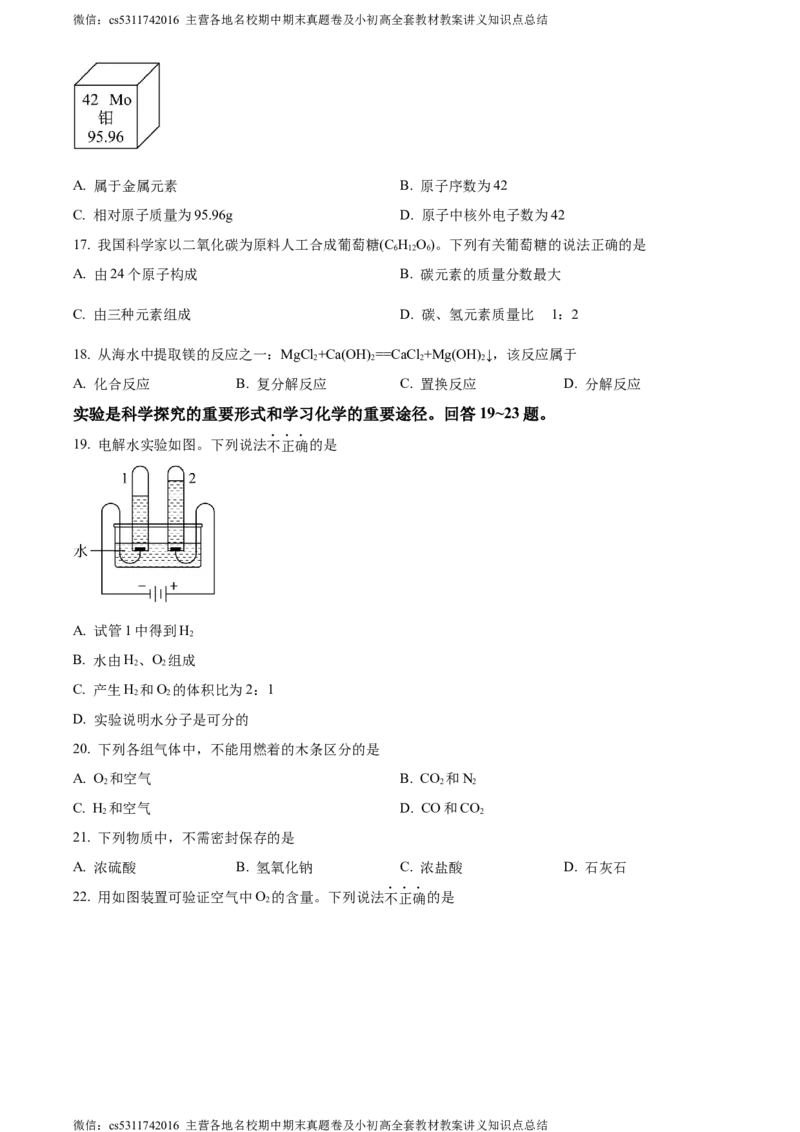
16. 我国科学家成功研制用于外太空核反应堆的高强韧钼合金。钼元素在元素周期表中的信息如图所示。
下列有关钼元素的说法不正确的是
微信:cs5311742016 主营各地名校期中期末真题卷及小初高全套教材教案讲义知识点总结微信:cs5311742016 主营各地名校期中期末真题卷及小初高全套教材教案讲义知识点总结
A. 属于金属元素 B. 原子序数为42
C. 相对原子质量为95.96g D. 原子中核外电子数为42
17. 我国科学家以二氧化碳为原料人工合成葡萄糖(C H O)。下列有关葡萄糖的说法正确的是
6 12 6
A. 由24个原子构成 B. 碳元素的质量分数最大
为
C. 由三种元素组成 D. 碳、氢元素质量比 1:2
18. 从海水中提取镁的反应之一:MgCl +Ca(OH) ==CaCl +Mg(OH) ↓,该反应属于
2 2 2 2
A. 化合反应 B. 复分解反应 C. 置换反应 D. 分解反应
实验是科学探究的重要形式和学习化学的重要途径。回答19~23题。
19. 电解水实验如图。下列说法不正确的是
A. 试管1中得到H
2
B. 水由H、O 组成
2 2
C. 产生H 和O 的体积比为2:1
2 2
D. 实验说明水分子是可分的
20. 下列各组气体中,不能用燃着的木条区分的是
A. O 和空气 B. CO 和N
2 2 2
C. H 和空气 D. CO和CO
2 2
21. 下列物质中,不需密封保存的是
A. 浓硫酸 B. 氢氧化钠 C. 浓盐酸 D. 石灰石
22. 用如图装置可验证空气中O 的含量。下列说法不正确的是
2
微信:cs5311742016 主营各地名校期中期末真题卷及小初高全套教材教案讲义知识点总结微信:cs5311742016 主营各地名校期中期末真题卷及小初高全套教材教案讲义知识点总结
A. 实验前需检查装置气密性
B. 红磷燃烧产生大量白烟
C. 红磷熄灭后应立即打开止水夹
D. 集气瓶中水面最终上升至2处
23. 下列关于“粗盐中难溶性杂质的去除”实验的叙述不正确的是
A. 该实验利用了NaCl溶于水的性质
B. 溶解时,用玻璃棒搅拌的目的是加速溶解
C. 过滤时,使用的玻璃仪器有烧杯、漏斗、玻璃棒
D. 蒸发时,必须蒸干蒸发皿中的水分才能停止加热
24. 如图是硼酸的溶解度曲线,下列说法正确的是
A. a点的硼酸溶液中溶质的质量分数为10%
B. 将a点的硼酸溶液升温至t℃时,仍是饱和溶液
2
C. 将b点的硼酸溶液降温至t℃时,有晶体析出
1
D. t℃时,向50g水中加入20g硼酸后充分搅拌,可得70g溶液
2
25. 中国芯片蚀刻技术国际领先。NF 进行硅芯片蚀刻时反应的微观示意图如下:
3
下列说法正确的是
A. 从微观构成看:四种物质均由分子构成
B. 从守恒关系看:反应前后原子的种类、数目不变
C. 从价态变化看:反应前后各元素的化合价不变
微信:cs5311742016 主营各地名校期中期末真题卷及小初高全套教材教案讲义知识点总结微信:cs5311742016 主营各地名校期中期末真题卷及小初高全套教材教案讲义知识点总结
D. 从表示方法看:反应的化学方程式为NF +Si SiF+N
3 4 2
第二部分
本部分共14题,共45分。
〖生活现象解释〗
26. 厨房中蕴含着许多化学知识。
(1)小苏打常用于焙制糕点,其化学式为_____。
(2)天然气的主要成分为CH,CH 充分燃烧的化学方程式为_____。
4 4
27. 通常,金属活动性越强,冶炼难度越大,人类使用该金属的时间越晚。
(1)下图为四种金属的最早冶炼历史年代。甲代表的金属是_____。
A. 铁 B. 铜 C. 钠 D. 锌
(2)将鱼用铝箔包好进行烤制,鱼很快被烤熟,在烤制过程中体现了铝箔具有良好的_____性;使用后的
铝箔依然光亮如新,说明铝具有很好的抗腐蚀性,用化学方程式解释其原因_____。
28. 洁厕灵(主要成分稀盐酸)和管道疏通剂(主要成分NaOH)是生活中常用的清洁剂。
(1)洁厕灵与铁锈接触时发生反应的化学方程式为_____。
(2)管道疏通剂使用时不能与皮肤接触的原因是_____。
【科普阅读理解】
29. 阅读下面科普短文。
谈到二氧化硫,人们可能会想到它对人体健康和环境的危害。其实在食品行业,SO 是一种国内外允许使
2
用的食品添加剂,通常以焦亚硫酸钠、亚硫酸钠等形式添加在食品中,起到护色、漂白、防腐和抗氧化的
作用。
的
SO 常用于葡萄酒 生产加工。SO 作为保鲜剂,在低温环境下可有效减缓酿酒葡萄的腐烂。研究人员在
2 2
4℃时,采用不同浓度的SO 对酿酒葡萄进行预处理,经过四周的储藏,测得酿酒葡萄的腐烂率如右图所示。
2
葡萄酒的生产过程包括葡萄除梗、榨汁和葡萄汁发酵等步骤。葡萄汁的发酵过程是在酵母的作用下将多糖
转化为酒精(C HOH),此过程需添加SO 抑制杂菌的滋生。
2 5 2
为保证SO 安全使用,我国《食品添加剂使用标准(GB2760-2014)》明确了各种食品中SO 最大残留量:
2 2
食品 蜜饯 葡萄酒 食糖 水果干 巧克力 果蔬汁
最大残留量 0.35g/kg 0.25g/L 0.1g/kg 0.1g/kg 0.1g/kg 0.05g/kg
微信:cs5311742016 主营各地名校期中期末真题卷及小初高全套教材教案讲义知识点总结微信:cs5311742016 主营各地名校期中期末真题卷及小初高全套教材教案讲义知识点总结
世界卫生组织也规定,每人每天摄入的SO (比体重)应控制在0.7mg/kg以内,否则人体会产生中毒现象。
2
依据文章内容回答下列问题。
(1)酒精属于_____(填“无机化合物”或“有机化合物”)。
(2)葡萄汁发酵过程中添加SO 的作用是_____。
2
(3)由图可知,酿酒葡萄在4℃时储存一周,腐烂率最高的是_____。
A. 未添加SO B. 低浓度SO C. 高浓度SO
2 2 2
(4)一个体重为60kg的成年人,每天SO 安全摄入量是_____mg以内。
2
(5)判断下列说法是否正确(填“对”或“错”)。
①按照国家标准,巧克力中的SO 最大残留量为0.1g/kg。_____
2
②生产葡萄酒的步骤中,所涉及的变化均属于化学变化。_____
【生产实际分析】
30. 某化工厂用石灰乳对工业烟气进行脱硫,同时生产石膏(CaSO)的工艺流程如下:
4
(1)步骤①中常将NaOH溶液喷成雾状,其目的是_____。
(2)NaSO 中S元素的化合价为_____。
2 3
(3)步骤③中发生化合反应的化学方程式为_____。
的
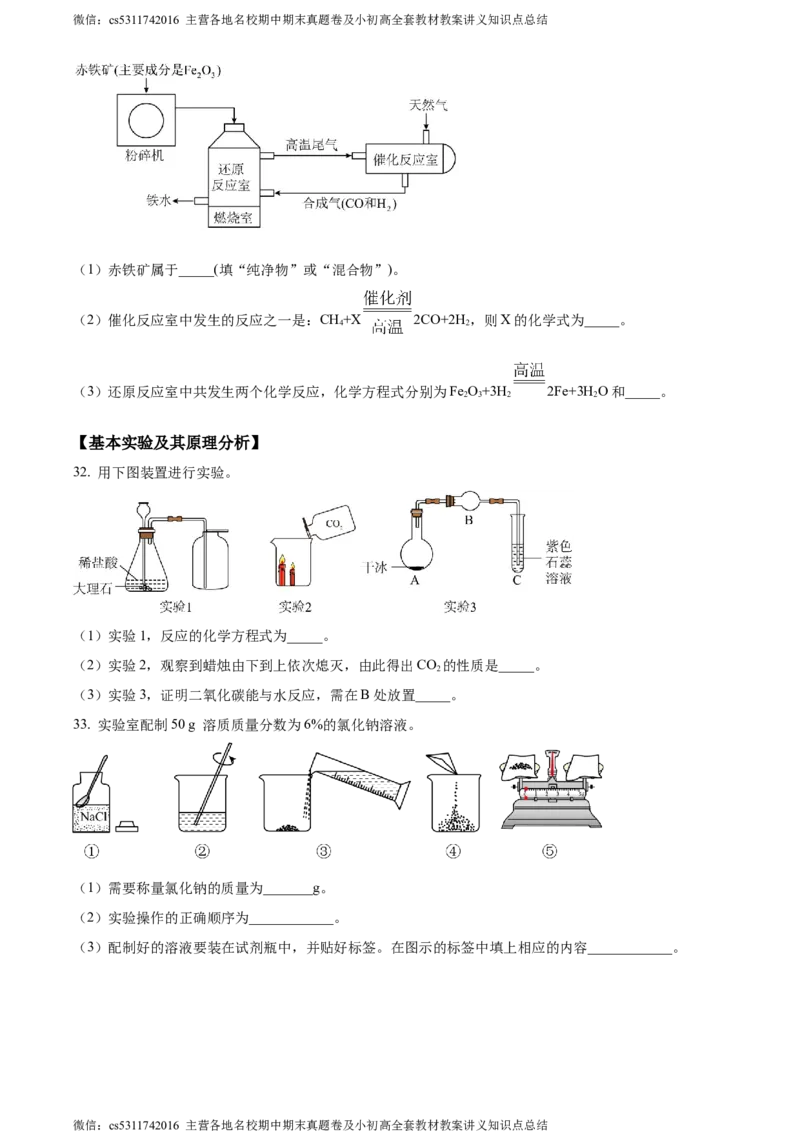
31. 高炉炼铁 工艺流程如下:
微信:cs5311742016 主营各地名校期中期末真题卷及小初高全套教材教案讲义知识点总结微信:cs5311742016 主营各地名校期中期末真题卷及小初高全套教材教案讲义知识点总结
(1)赤铁矿属于_____(填“纯净物”或“混合物”)。
(2)催化反应室中发生的反应之一是:CH+X 2CO+2H,则X的化学式为_____。
4 2
(3)还原反应室中共发生两个化学反应,化学方程式分别为Fe O+3H 2Fe+3H O和_____。
2 3 2 2
【基本实验及其原理分析】
32. 用下图装置进行实验。
(1)实验1,反应的化学方程式为_____。
(2)实验2,观察到蜡烛由下到上依次熄灭,由此得出CO 的性质是_____。
2
(3)实验3,证明二氧化碳能与水反应,需在B处放置_____。
33. 实验室配制50 g 溶质质量分数为6%的氯化钠溶液。
(1)需要称量氯化钠的质量为_______g。
(2)实验操作的正确顺序为____________。
(3)配制好的溶液要装在试剂瓶中,并贴好标签。在图示的标签中填上相应的内容____________。
微信:cs5311742016 主营各地名校期中期末真题卷及小初高全套教材教案讲义知识点总结微信:cs5311742016 主营各地名校期中期末真题卷及小初高全套教材教案讲义知识点总结
34. 取一定量碳酸钠溶液于三支试管中,进行如图所示实验。
(1)①实验的目的是_____。
(2)②中发生反应的化学方程式为_____。
(3)③中观察到的现象是_____,向所得溶液中滴入2滴紫色石蕊溶液,观察到溶液变为红色,则溶液中
含有的溶质是_____。
35. 根据下图所示实验回答问题。
的
已知:白磷、红磷 着火点分别为40℃、240℃。
(1)实验1,影响物质溶解性的因素是___________。
(2)实验2,观察到①中白磷燃烧,②中红磷不燃烧,可得出可燃物燃烧的条件之一是___________。写
出涉及的化学方程式___________。
36. 用如图装置验证Al、Cu、Ag三种金属的活动性顺序。
微信:cs5311742016 主营各地名校期中期末真题卷及小初高全套教材教案讲义知识点总结微信:cs5311742016 主营各地名校期中期末真题卷及小初高全套教材教案讲义知识点总结
(1)实验A可得出Cu的金属活动性比Ag强,反应的化学方程式为_______________。
(2)能证明Al的金属活动性比Cu强的实验现象是_______ 。
37. 用下图实验证明无明显现象反应发生。
能证明NaOH与CO 发生反应的现象是___________,NaOH与CO 反应的化学方程式为___________。
2 2
〖科学探究〗
38. 实验小组的同学探究不同配制方法对紫色石蕊溶液显色的影响。
【查阅资料】石蕊能溶于水或乙醇中。
【进行实验1】分别用某品牌的石蕊1g进行4种方法的石蕊溶液配制。
方 蒸馏水体 溶液颜
操作 石蕊溶液
法 积/mL 色
搅拌,静置1h,
① 100 滤液 紫色
过滤
② 100 煮沸后过滤 滤液 紫色
搅拌,静置24h,
③ 100 滤液 紫色
过滤
搅拌,静置24h, 滤液加30mL乙醇,再加蒸馏水稀
④ 50 紫色
过滤 释至100mL
【解释与结论】
(1)方法①配制的石蕊溶液中,溶质是___________。
(2)方法④中,加蒸馏水稀释至100mL时,加入的蒸馏水体积大于20mL。说明分子具有的性质是
___________。
【进行实验2】用4种方法配制的石蕊溶液进行显色实验:向被试溶液中滴加石蕊溶液。
被试溶液 方法 方法 方法 方法
微信:cs5311742016 主营各地名校期中期末真题卷及小初高全套教材教案讲义知识点总结微信:cs5311742016 主营各地名校期中期末真题卷及小初高全套教材教案讲义知识点总结
① ② ③ ④
10%盐酸 红 红 红 浅红
饱和二氧化碳溶 不明
浅红 浅红 浅红
液 显
饱和碳酸钠溶液 蓝 蓝 蓝 浅蓝
澄清石灰水 蓝 蓝 蓝 浅蓝
【解释与结论】
(3)通过实验可得出饱和碳酸钠溶液呈___________(填“酸性”或“碱性”)。
(4)向饱和二氧化碳溶液中滴加石蕊溶液呈浅红色,用化学方程式解释原因:___________。
(5)进行实验2需要控制的相同条件是:取用被试溶液的体积相同、___________。
【反思与评价】
的
(6)用方法④配制 石蕊溶液进行显色实验现象不明显,原因可能是___________。
【实际应用定量计算】
39. 氧烛是一种供氧发生器,通过催化分解氯酸钠来产生氧气。主要反应原理是:2NaClO
3
2NaCl+3O ↑。计算106.5g氯酸钠分解生成氧气的质量。
2
微信:cs5311742016 主营各地名校期中期末真题卷及小初高全套教材教案讲义知识点总结