文档内容
查补易混易错 18 物质结构与性质
物质结构与性质的常见题型为综合题,常以元素推断或某一主题两种方式引入,考查学生的归纳推理能力、
信息迁移能力以及综合应用能力。物质结构包括原子结构(原子核外电子排布、原子的杂化方式、元素电负
性大小比较、元素金属性、非金属性的强弱)、分子结构(化学键、分子的电子式、结构式、结构简式的书
写、化学式的种类、官能团等)、晶体结构(晶体类型的判断、物质熔沸点的高低、影响因素、晶体的密度、
均摊方法的应用等)。
易错01原子结构与性质
原子结构与性质在高考中常见的命题角度有原子核外电子的排布规律及其表示方法、原子结构与元素电离
能和电负性的关系及其应用。在高考试题中,各考查点相对独立,难度不大。试题侧重原子核外电子排布
式或轨道表示式,未成对电子数判断,电负性、电离能、原子半径和元素金属性与非金属性比较的考查。
高考中考查点主要集中在电子排布的书写及电离能、电负性大小比较上,所以在书写基态原子电子排布时,
应避免违反能量最低原理、泡利原理、洪特规则及特例;还需注意同能级的轨道半充满、全充满或全空状
态的原子结构稳定如Cr:3d54s1、Mn:3d54s2、Cu:3d104s1、Zn:3d104s2;另外需理解电离能与金属性及金
属元素价态的关系,电负性与非金属性及组成化合物所形成的化学键的关系。
易错02分子结构与性质
分子结构与性质在高考中的常见命题角度有围绕某物质判断共价键的类型和数目,分子的极性、中心原子
的杂化方式,微粒的立体构型,氢键的形成及对物质的性质影响等,考查角度较多,但各个角度独立性大,
难度不大。试题侧重微粒构型、杂化方式、中心原子的价层电子对数、配位原子判断与配位数、化学键类
型、分子间作用力与氢键、分子极性的考查。常考点有对σ键和π键判断,要掌握好方法;杂化轨道的判
断,要理解常见物质的杂化方式;通过三种作用力对性质的影响解释相关现象及结论。注意以下三个误区:
不要误认为分子的稳定性与分子间作用力和氢键有关,其实分子的稳定性与共价键的强弱有关;不要误认
为组成相似的分子,中心原子的杂化类型相同,关键是要看其 σ键和孤电子对数是否相同。如BCl 中B原
3
子为sp2杂化,NCl 中N原子为sp3杂化;不要误认为只要含有氢键物质的熔、沸点就高,其实不一定,分
3
子间的氢键会使物质的熔、沸点升高,而分子内氢键一般会使物质的熔、沸点降低。易错03晶体结构与性质
晶体结构与性质在高考中常见的命题角度有晶体的类型、结构与性质的关系,晶体熔沸点高低的比较,配
位数、晶胞模型分析及有关计算等是物质结构选考模块的必考点。试题侧重晶体类型判断、物质熔沸点的
比较与原因、晶胞中微粒数的判断、配位数、晶胞密度计算、晶胞参数、空间利用率计算的考查。物质结
构与性质的难点就是涉及到晶胞特点的计算类题目,涉及有关晶胞的计算时,注意单位的换算。如面心立
方晶胞与体心立方晶胞的配位数不同;晶胞参数给定单位是nm或pm时,忽略换算成cm。
1.(2023·浙江·高考真题)硅材料在生活中占有重要地位。请回答:
(1) 分子的空间结构(以 为中心)名称为________,分子中氮原子的杂化轨道类型是_______。
受热分解生成 和 ,其受热不稳定的原因是________。
(2)由硅原子核形成的三种微粒,电子排布式分别为:① 、② 、③ ,有关
这些微粒的叙述,正确的是___________。
A.微粒半径:③>①>②
B.电子排布属于基态原子(或离子)的是:①②
C.电离一个电子所需最低能量:①>②>③
D.得电子能力:①>②
(3)Si与P形成的某化合物晶体的晶胞如图。该晶体类型是___________,该化合物的化学式为___________。
2.(2022·北京·高考真题)工业中可利用生产钛白的副产物 和硫铁矿 联合制备铁精粉
和硫酸,实现能源及资源的有效利用。(1) 结构示意图如图1。
① 的价层电子排布式为___________。
② 中O和 中S均为 杂化,比较 中 键角和 中 键角的大小并解释原
因___________
。
③ 中 与 与 的作用力类型分别是___________。
(2) 晶体的晶胞形状为立方体,边长为 ,结构如图2。
①距离 最近的阴离子有___________个。
② 的摩尔质量为 ,阿伏加德罗常数为 。
该晶体的密度为___________ 。
(3) 加热脱水后生成 ,再与 在氧气中掺烧可联合制备铁精粉和硫酸。
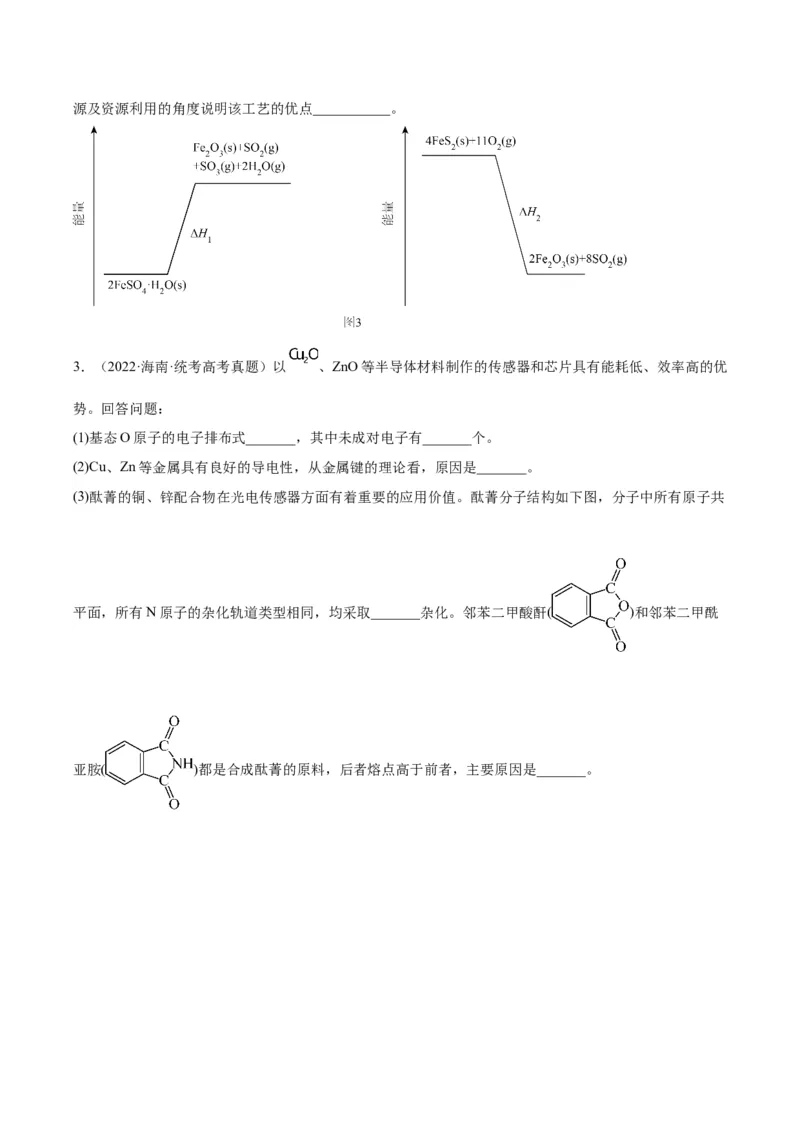
分解和 在氧气中燃烧的能量示意图如图3。利用 作为 分解的燃料,从能源及资源利用的角度说明该工艺的优点___________。
3.(2022·海南·统考高考真题)以 、ZnO等半导体材料制作的传感器和芯片具有能耗低、效率高的优
势。回答问题:
(1)基态O原子的电子排布式_______,其中未成对电子有_______个。
(2)Cu、Zn等金属具有良好的导电性,从金属键的理论看,原因是_______。
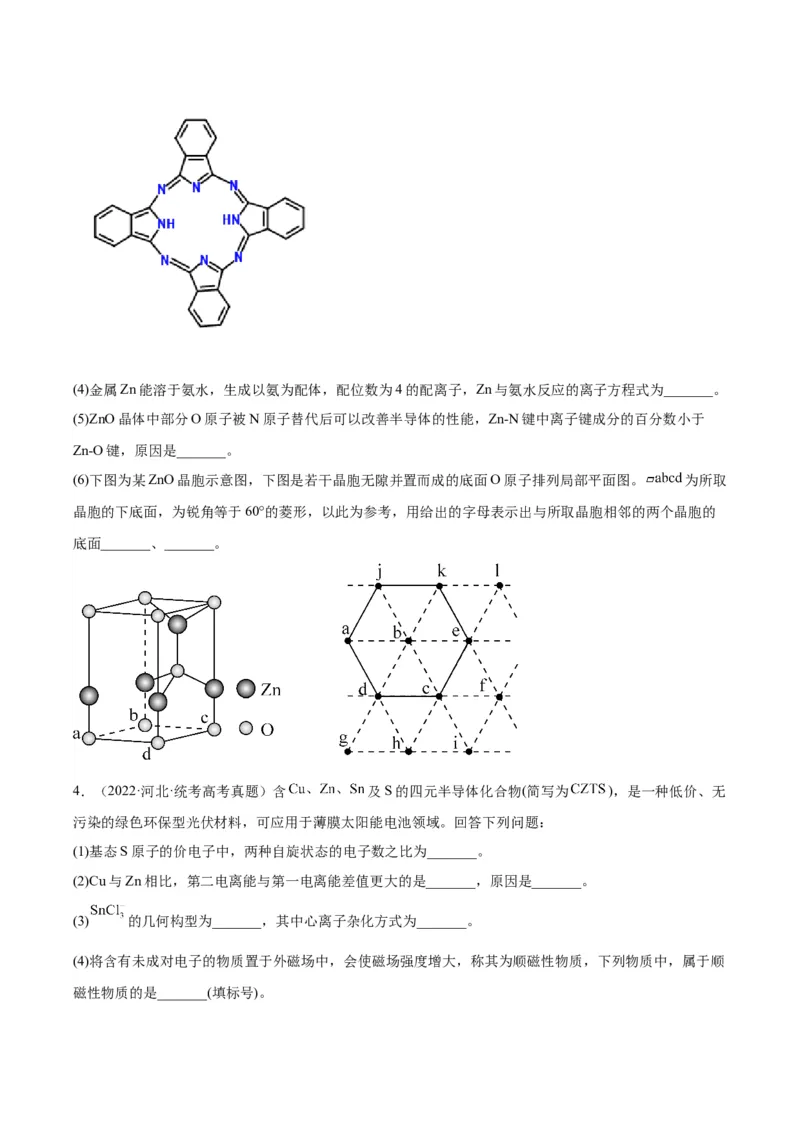
(3)酞菁的铜、锌配合物在光电传感器方面有着重要的应用价值。酞菁分子结构如下图,分子中所有原子共
平面,所有N原子的杂化轨道类型相同,均采取_______杂化。邻苯二甲酸酐( )和邻苯二甲酰
亚胺( )都是合成酞菁的原料,后者熔点高于前者,主要原因是_______。(4)金属Zn能溶于氨水,生成以氨为配体,配位数为4的配离子,Zn与氨水反应的离子方程式为_______。
(5)ZnO晶体中部分O原子被N原子替代后可以改善半导体的性能,Zn-N键中离子键成分的百分数小于
Zn-O键,原因是_______。
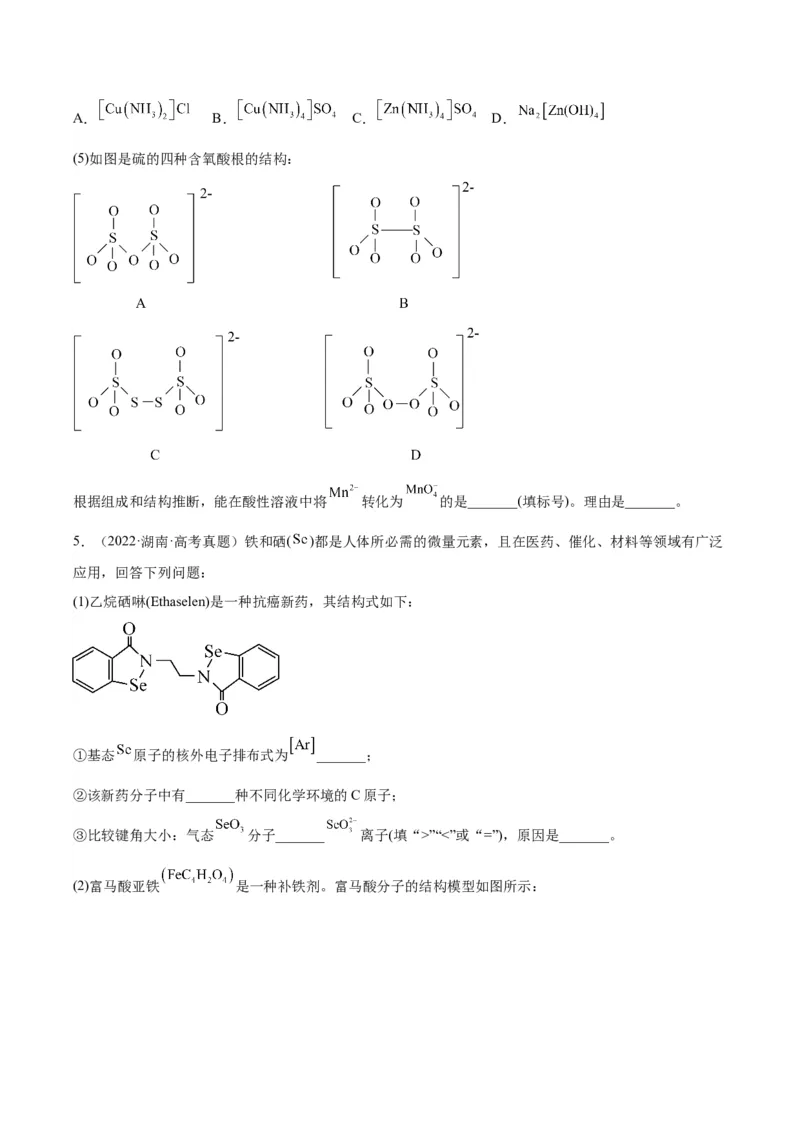
(6)下图为某ZnO晶胞示意图,下图是若干晶胞无隙并置而成的底面O原子排列局部平面图。 为所取
晶胞的下底面,为锐角等于60°的菱形,以此为参考,用给出的字母表示出与所取晶胞相邻的两个晶胞的
底面_______、_______。
4.(2022·河北·统考高考真题)含 及S的四元半导体化合物(简写为 ),是一种低价、无
污染的绿色环保型光伏材料,可应用于薄膜太阳能电池领域。回答下列问题:
(1)基态S原子的价电子中,两种自旋状态的电子数之比为_______。
(2)Cu与Zn相比,第二电离能与第一电离能差值更大的是_______,原因是_______。
(3) 的几何构型为_______,其中心离子杂化方式为_______。
(4)将含有未成对电子的物质置于外磁场中,会使磁场强度增大,称其为顺磁性物质,下列物质中,属于顺
磁性物质的是_______(填标号)。A. B. C. D.
(5)如图是硫的四种含氧酸根的结构:
根据组成和结构推断,能在酸性溶液中将 转化为 的是_______(填标号)。理由是_______。
5.(2022·湖南·高考真题)铁和硒( )都是人体所必需的微量元素,且在医药、催化、材料等领域有广泛
应用,回答下列问题:
(1)乙烷硒啉(Ethaselen)是一种抗癌新药,其结构式如下:
①基态 原子的核外电子排布式为 _______;
②该新药分子中有_______种不同化学环境的C原子;
③比较键角大小:气态 分子_______ 离子(填“>”“<”或“=”),原因是_______。
(2)富马酸亚铁 是一种补铁剂。富马酸分子的结构模型如图所示:①富马酸分子中 键与 键的数目比为_______;
②富马酸亚铁中各元素的电负性由大到小的顺序为_______。
(3)科学家近期合成了一种固氮酶模型配合物,该物质可以在温和条件下直接活化 ,将 转化为 ,
反应过程如图所示:
①产物中N原子的杂化轨道类型为_______;
②与 互为等电子体的一种分子为_______(填化学式)。
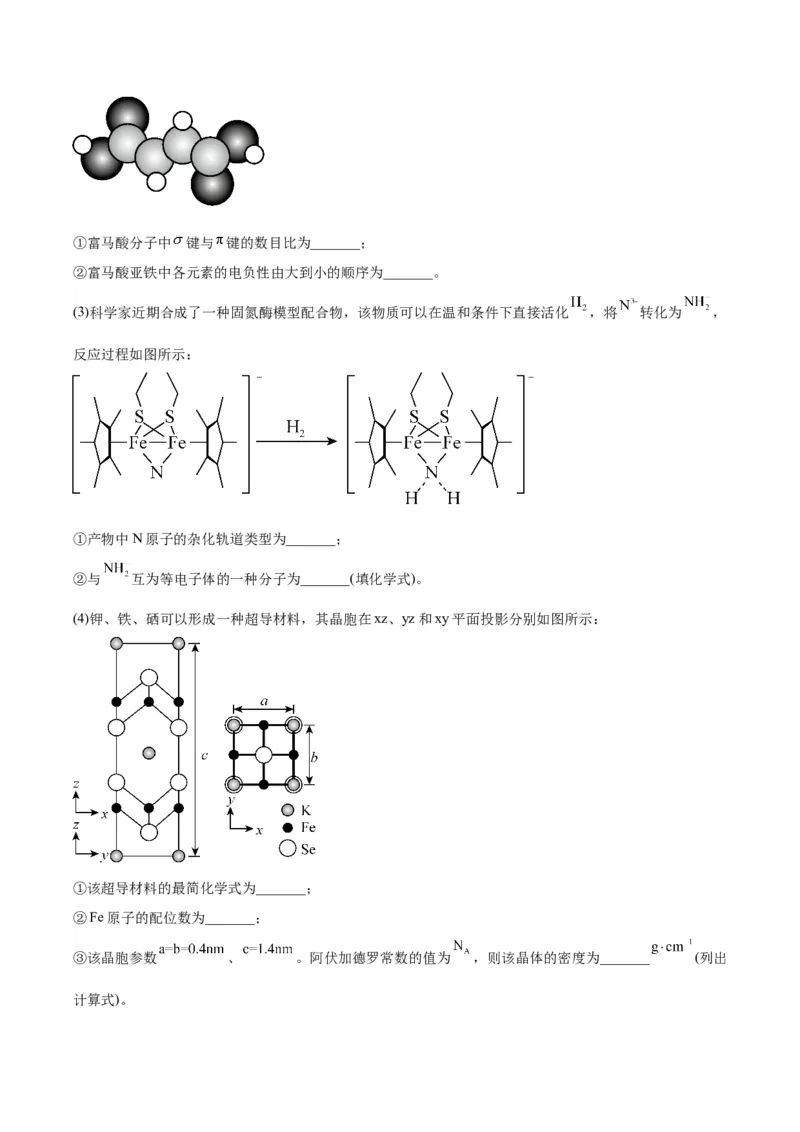
(4)钾、铁、硒可以形成一种超导材料,其晶胞在xz、yz和xy平面投影分别如图所示:
①该超导材料的最简化学式为_______;
②Fe原子的配位数为_______;
③该晶胞参数 、 。阿伏加德罗常数的值为 ,则该晶体的密度为_______ (列出
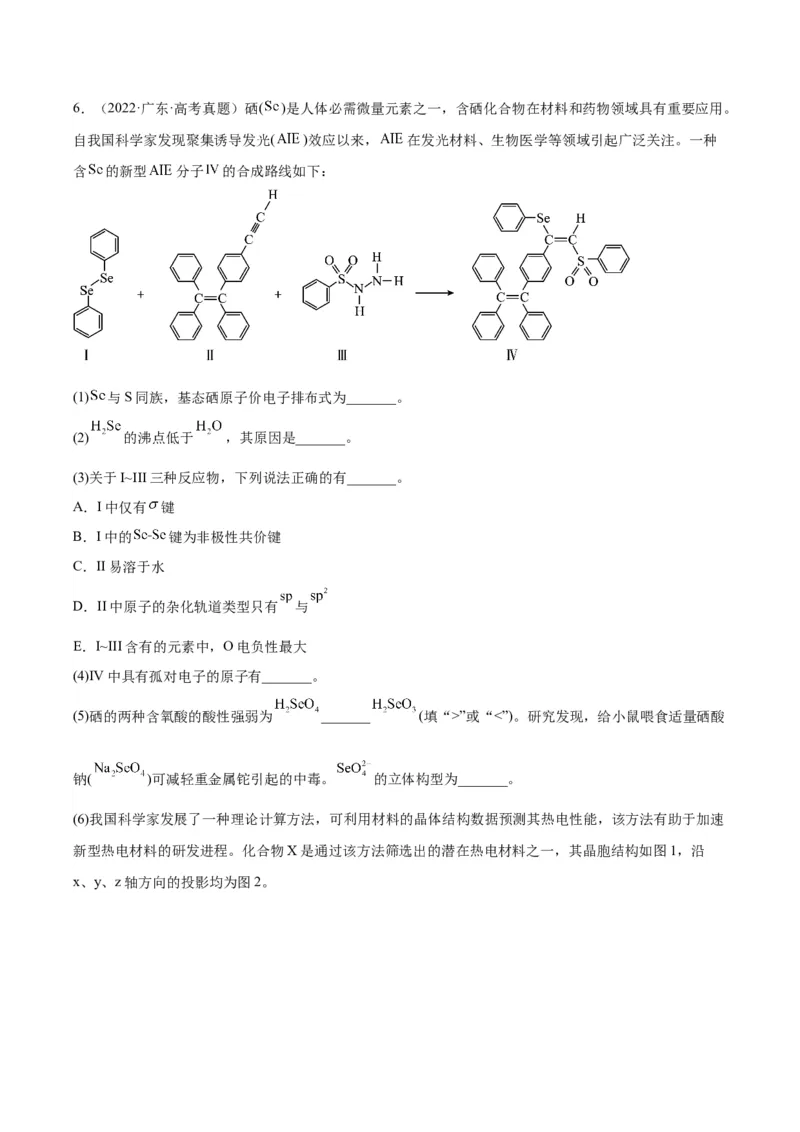
计算式)。6.(2022·广东·高考真题)硒( )是人体必需微量元素之一,含硒化合物在材料和药物领域具有重要应用。
自我国科学家发现聚集诱导发光( )效应以来, 在发光材料、生物医学等领域引起广泛关注。一种
含 的新型 分子 的合成路线如下:
(1) 与S同族,基态硒原子价电子排布式为_______。
(2) 的沸点低于 ,其原因是_______。
(3)关于I~III三种反应物,下列说法正确的有_______。
A.I中仅有 键
B.I中的 键为非极性共价键
C.II易溶于水
D.II中原子的杂化轨道类型只有 与
E.I~III含有的元素中,O电负性最大
(4)IV中具有孤对电子的原子有_______。
(5)硒的两种含氧酸的酸性强弱为 _______ (填“>”或“<”)。研究发现,给小鼠喂食适量硒酸
钠( )可减轻重金属铊引起的中毒。 的立体构型为_______。
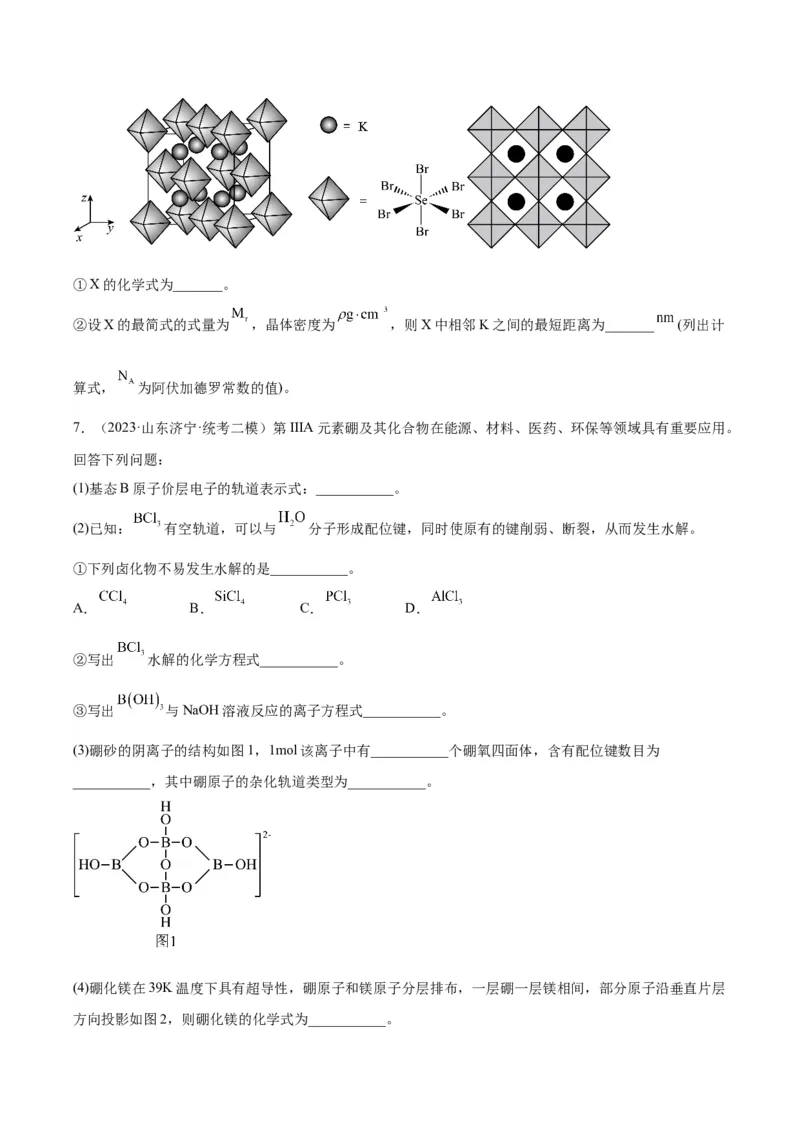
(6)我国科学家发展了一种理论计算方法,可利用材料的晶体结构数据预测其热电性能,该方法有助于加速
新型热电材料的研发进程。化合物X是通过该方法筛选出的潜在热电材料之一,其晶胞结构如图1,沿
x、y、z轴方向的投影均为图2。①X的化学式为_______。
②设X的最简式的式量为 ,晶体密度为 ,则X中相邻K之间的最短距离为_______ (列出计
算式, 为阿伏加德罗常数的值)。
7.(2023·山东济宁·统考二模)第IIIA元素硼及其化合物在能源、材料、医药、环保等领域具有重要应用。
回答下列问题:
(1)基态B原子价层电子的轨道表示式:___________。
(2)已知: 有空轨道,可以与 分子形成配位键,同时使原有的键削弱、断裂,从而发生水解。
①下列卤化物不易发生水解的是___________。
A. B. C. D.
②写出 水解的化学方程式___________。
③写出 与NaOH溶液反应的离子方程式___________。
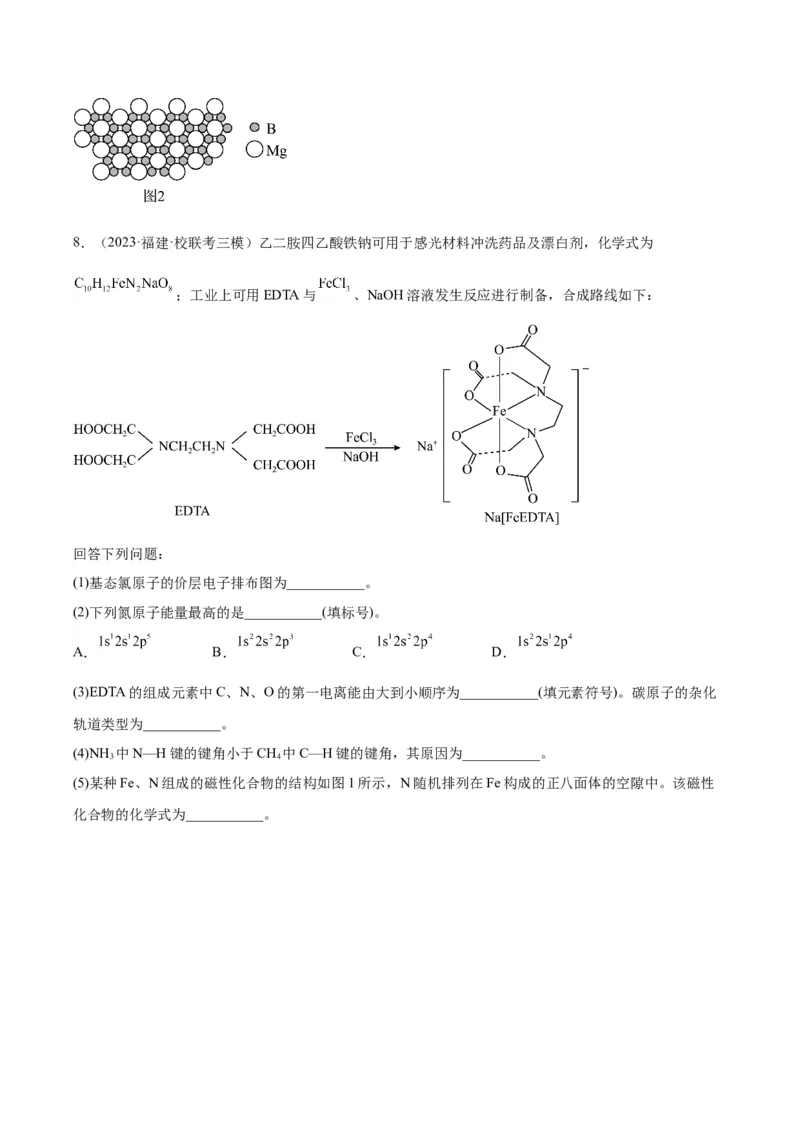
(3)硼砂的阴离子的结构如图1,1mol该离子中有___________个硼氧四面体,含有配位键数目为
___________,其中硼原子的杂化轨道类型为___________。
(4)硼化镁在39K温度下具有超导性,硼原子和镁原子分层排布,一层硼一层镁相间,部分原子沿垂直片层
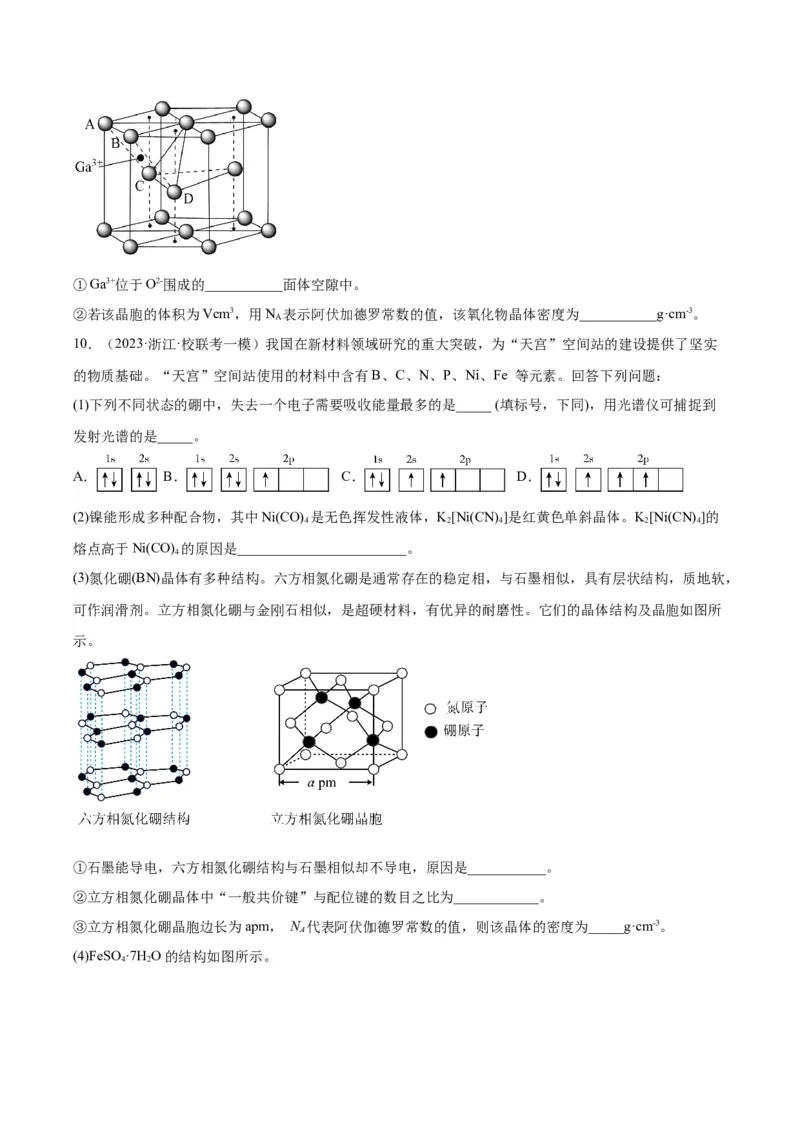
方向投影如图2,则硼化镁的化学式为___________。8.(2023·福建·校联考三模)乙二胺四乙酸铁钠可用于感光材料冲洗药品及漂白剂,化学式为
;工业上可用EDTA与 、NaOH溶液发生反应进行制备,合成路线如下:
回答下列问题:
(1)基态氯原子的价层电子排布图为___________。
(2)下列氮原子能量最高的是___________(填标号)。
A. B. C. D.
(3)EDTA的组成元素中C、N、O的第一电离能由大到小顺序为___________(填元素符号)。碳原子的杂化
轨道类型为___________。
(4)NH 中N—H键的键角小于CH 中C—H键的键角,其原因为___________。
3 4
(5)某种Fe、N组成的磁性化合物的结构如图1所示,N随机排列在Fe构成的正八面体的空隙中。该磁性
化合物的化学式为___________。(6)在元素周期表中,铁元素位于___________区(填“s”“p”“d”或“ds”)。铁的某种晶胞沿面对角线的位置切
下之后可以得到如图2所示的截面。假设铁的原子半径为a nm,则该铁晶体的密度为___________
(列出计算式,设 为阿伏加德罗常数的值)。
9.(2023·内蒙古赤峰·统考模拟预测)离子液体是指室温或接近室温时呈液态,而本身由阴、阳离子构成
的化合物。GaCl 和氯化- 1-乙基- 3-甲基咪唑( ,简称EMIC)混合形成的离子液体被认为是21
3
世纪理想的绿色溶剂。请回答下列问题:
(1)请写出基态Ga原子的核外电子排布式___________, 同周期主族元素中基态原子未成对电子数与Ga相
同的___________ ( 填元素符号)。
(2)EMIC阳离子中的几种元素电负性由大到小顺序为___________。
(3)EMIC中碳原子的杂化类型为___________。
(4)已知分子中的大 键可用符号 表示,其中m代表参与形成大 键的原子数,n代表大II键中的电子
数,则EMIC中大 键可表示为___________。
(5)GaCl 熔点为77.8°C, GaF 熔点高于1000°C,其原因是___________。
3 3
(6)某种Ga的氧化物晶胞结构如图所示。O2-以六方密堆积形成晶胞, Ga3+位于由A、B、C、D四个O2-围
成的四边形的中心,但晶胞中只,有 的四边形中心位置占据了Ga3+,另外 的位置空置。①Ga3+位于O2-围成的___________面体空隙中。
②若该晶胞的体积为Vcm3,用N 表示阿伏加德罗常数的值,该氧化物晶体密度为___________g·cm-3。
A
10.(2023·浙江·校联考一模)我国在新材料领域研究的重大突破,为“天宫”空间站的建设提供了坚实
的物质基础。“天宫”空间站使用的材料中含有B、C、N、P、Ni、Fe 等元素。回答下列问题:
(1)下列不同状态的硼中,失去一个电子需要吸收能量最多的是_____ (填标号,下同),用光谱仪可捕捉到
发射光谱的是_____。
A. B. C. D.
(2)镍能形成多种配合物,其中Ni(CO) 是无色挥发性液体,K[Ni(CN) ]是红黄色单斜晶体。K[Ni(CN) ]的
4 2 4 2 4
熔点高于Ni(CO) 的原因是________________________。
4
(3)氮化硼(BN)晶体有多种结构。六方相氮化硼是通常存在的稳定相,与石墨相似,具有层状结构,质地软,
可作润滑剂。立方相氮化硼与金刚石相似,是超硬材料,有优异的耐磨性。它们的晶体结构及晶胞如图所
示。
①石墨能导电,六方相氮化硼结构与石墨相似却不导电,原因是___________。
②立方相氮化硼晶体中“一般共价键”与配位键的数目之比为____________。
③立方相氮化硼晶胞边长为apm, N 代表阿伏伽德罗常数的值,则该晶体的密度为_____g·cm-3。
A
(4)FeSO ·7H O的结构如图所示。
4 2FeSO ·7H O中∠1、∠2、∠3由大到小的顺序是_________。
4 2
参考答案
1.(1)四面体 周围的 基团体积较大,受热时斥力较强 中 键能相对较
小];产物中气态分子数显著增多(熵增)
(2)AB
(3)共价晶体
【详解】(1) 分子可视为SiH 分子中的4个氢原子被—NH (氨基)取代形成的,所以
4 2
分子中Si原子轨道的杂化类型是sp3,分子的空间结构(以 为中心)名称为四面体;
氨基(-NH )氮原子形成3个σ键,含有1对孤对电子,N原子杂化轨道数目为4,N原子轨道的杂化类型是
2
sp3;
周围的 基团体积较大,受热时斥力较强 中 键能相对较小];产物中气态分子数显著
增多(熵增),故 受热不稳定,容易分解生成 和 ;
(2)电子排布式分别为:① 、② 、③ ,可推知分别为基态Si原子、
Si+离子、激发态Si原子;
A.激发态Si原子有四层电子,Si+离子失去了一个电子,根据微粒电子层数及各层电子数多少可推知,微
粒半径:③>①>②,选项A正确;
B.根据上述分析可知,电子排布属于基态原子(或离子)的是:①②,选项B正确;
C.激发态Si原子不稳定,容易失去电子;基态Si原子失去一个电子是硅的第一电离能,Si+离子失去一个
电子是硅的第二电离能,由于I>I ,可以得出电离一个电子所需最低能量:②>①>③,选项C错误;
2 1
D.由C可知②比①更难失电子,则②比①更容易得电子,即得电子能力:②>①,选项D错误;
答案选AB;
(3)Si与P形成的某化合物晶体的晶胞如图可知,原子间通过共价键形成的空间网状结构,形成共价晶体;根据均摊法可知,一个晶胞中含有 个Si,8个P,故该化合物的化学式为 。
2.(1) 孤电子对有较大斥力,使 键角小于 键角 配位键、氢键
(2) 6
(3) 燃烧放热为 分解提供能量;反应产物是制备铁精粉和硫酸的原料
【详解】(1)①Fe的价层电子排布为3d64s2,形成Fe2+时失去4s上的2个电子,于是Fe2+的价层电子排布
为3d6。
②HO中O 和 中S都是sp3杂化,HO中O杂化形成的4个杂化轨道中2个被孤电子对占据,2个被
2 2
键合电子对占据,而 中S杂化形成的4个杂化轨道均被键合电子对占据。孤电子对与键合电子对间的
斥力大于键合电子对与键合电子对间的斥力,使得 键角与 键角相比被压缩减小。
③HO中O有孤电子对,Fe2+有空轨道,二者可以形成配位键。 中有电负性较大的O元素可以与HO
2 2
中H元素形成氢键。
答案为:3d6;孤电子对有较大斥力,使 键角小于 键角;配位键、氢键。
(2)①以位于面心Fe2+为例,与其距离最近的阴离子所处位置如图所示(圆中):
。
4个阴离子位于楞上,2个位于体心位置上,共6个。
②依据分摊法可知晶胞中Fe2+离子个数为 , 个数为 。一个晶胞中相当于含
有4个FeS,因此一个晶胞的质量 。所以晶体密度
2。
答案为:6;
(3) 燃烧为放热反应, 分解为吸热反应, 燃烧放出的热量恰好为 分解
提供能量。另外, 燃烧和 分解的产物如Fe O、SO 、SO 可以作为制备铁精粉或硫酸的原
2 3 2 3
料。
答案为: 燃烧放热为 分解提供能量;反应产物是制备铁精粉和硫酸的原料。
3.(1) 1s22s22p4或[He]2s22p4 2
(2)自由电子在外加电场中作定向移动
(3) sp2 两者均为分子晶体,后者能形成分子间氢键,使分子间作用力增大,熔点更高
(4)Zn+4NH+2H O=[Zn(NH )]2++2OH-+H ↑
3 2 3 4 2
(5)电负性O>N,O对电子的吸引能力更强,Zn和O更易形成离子键
(6) cdhi bcfe
【详解】▱(1)O为8▱号元素,其基态O原子核外有8个电子,因此基态O原子的电子排布式为1s22s22p4或
[He]2s22p4,其2p轨道有2个未成对电子,即O原子有2个未成对电子;
(2)由于金属的自由电子可在外加电场中作定向移动,因此Cu、Zn等金属具有良好的导电性;
(3)根据结构式可知,N原子以双键或以NH三键的形式存在,故N原子的杂化方式均为sp2,由于邻苯
二甲酸酐和邻苯二甲酰亚胺均为分子晶体,而后者能形成分子间氢键,使分子间作用力增大,因此熔点更
高;
(4)金属Zn与氨水反应可生成[Zn(NH )](OH) 和H,反应的离子方程式为Zn+4NH +2H O=[Zn(NH )]2+
3 4 2 2 3 2 3 4
+2OH-+H ↑;
2
(5)由于电负性O>N,O对电子的吸引能力更强,Zn和O更易形成离子键,因此Zn—N键中离子键成
分的百分数小于Zn—O键;
(6)根据晶胞示意图,一个晶胞中8个O原子位于晶胞的顶点,1个O原子位于晶胞体内,4个Zn原子
位于晶胞的棱上,1个Zn原子位于晶胞体内,棱上的3个Zn原子和体内的Zn原子、O原子形成四面体结
构,从底面O原子排列图看,能平移且与abcd共边的只有二个四边形,为cdhi和bcfe。4.(1)1:2/2:1
(2) Cu Cu的第二电离能失去的是3d10的电子,第一电离能失去的是4s1电子,Zn的第二电离能失
去的是4s1的电子,第一电离能失去的是4s2电子,3d10电子处于全充满状态,其与4s1电子能量差值更大
(3)三角锥形 sp3杂化
(4)B
(5) D D中含有-1价的O,易被还原,具有强氧化性,能将Mn2+转化为MnO
【详解】(1)基态S的价电子排布是3s23p4,根据基态原子电子排布规则,两种自旋状态的电子数之比为:
1:2或2:1;
(2)Cu的第二电离能失去的是3d10的电子,第一电离能失去的是4s1电子,Zn的第二电离能失去的是4s1
的电子,第一电离能失去的是4s2电子,3d10电子处于全充满状态,其与4s1电子能量差值更大;
(3)Sn是ⅣA族元素,SnCl 的中心离子Sn2+价层电子对数为3+ ,有1对孤电子对,中心离
子是sp3杂化,SnCl 的几何构型是三角锥形;
(4)根据题意,具有顺磁性物质含有未成对电子。A.[Cu(NH )]Cl各原子核外电子均已成对,不符合题意;
3 2
B.[Cu(NH)]SO 中的Cu2+外围电子排布是3d9,有未成对电子,符合题意;C.[Zn(NH )]SO 各原子核外电
3 4 4 3 4 4
子均已成对,不符合题意;D.Na [Zn(OH)] 各原子核外电子均已成对,不符合题意;故答案选B。
2
(5)Mn2+转化为MnO 需要氧化剂,且氧化性比MnO 的强,由SO 使KMnO 溶液褪色可知HSO 的氧
2 4 2 4
化性弱于MnO ,故A不符合;B、C中的S化合价比HSO 低,氧化性更弱,故B、C均不符合;D中含
2 4
有-1价的O,易被还原,具有强氧化性,能将Mn2+转化为MnO ,故D符合。
5.(1) [Ar] 3d104s24p4 8
> SeO 的空间构型为平面三角形,SeO 的空间构型为三角锥形
3
(2) 11:3 O>C>H>Fe
(3) sp3杂化 HO
2
(4) KFe Se 4
2 2
【详解】(1)①硒元素的原子序数为34,基态原子的电子排布式为[Ar] 3d104s24p4,故答案为:[Ar]3d104s24p4;
②由结构简式可知,乙烷硒啉的分子结构对称,分子中含有8种化学环境不同的碳原子,故答案为:8;
③三氧化硒分子中硒原子的价层电子对数为3,孤对电子对数为0,分子的空间构型为平面三角形,键角为
120°,亚硒酸根离子中硒原子的价层电子对数为4,孤对电子对数为1,离子的空间构型为三角锥形,键角
小于120°,故答案为:>;SeO 的空间构型为平面三角形,SeO 的空间构型为三角锥形;
3
(2)①由球棍模型可知,富马酸的结构式为HOOCCH=CHCOOH,分子中的单键为σ键,双键中含有1
个σ键和1个π键,则分子中σ键和π键的数目比为11:3,故答案为:11:3;
②金属元素的电负性小于非金属元素,则铁元素的电负性最小,非金属元素的非金属性越强,电负性越大,
氢碳氧的非金属性依次增强,则电负性依次增大,所以富马酸亚铁中四种元素的电负性由大到小的顺序为
O>C>H>Fe,故答案为:O>C>H>Fe;
(3)①由结构简式可知,产物中氮原子的价层电子对数为4,原子的杂化方式为sp3杂化,故答案为:sp3
杂化;
②水分子和氨基阴离子的原子个数都为3、价电子数都为8,互为等电子体,故答案为:HO;
2
(4)①由平面投影图可知,晶胞中位于顶点和体心的钾原子个数为8× +1=2,铁原子位于面心,原子个
数为8× =4,位于棱上和体心的硒原子的个数为8× +2=4,则超导材料最简化学式为KFe Se ,故答案为:
2 2
KFe Se ;
2 2
②由平面投影图可知,位于棱上的铁原子与位于面上的硒原子的距离最近,所以铁原子的配位数为4,故
答案为:4;
③设晶体的密度为dg/cm3,由晶胞的质量公式可得: =abc×10—21×d,解得d=
,故答案为: 。
6.(1)4s24p4
(2)两者都是分子晶体,由于水存在分子间氢键,沸点高
(3)BDE
(4)O、Se
(5)> 正四面体形(6) K SeBr
2 6
【详解】(1)基态硫原子价电子排布式为3s23p4, 与S同族,Se为第四周期元素,因此基态硒原子价
电子排布式为4s24p4;故答案为:4s24p4。
(2) 的沸点低于 ,其原因是两者都是分子晶体,由于水存在分子间氢键,沸点高;故答案为:
两者都是分子晶体,由于水存在分子间氢键,沸点高。
(3)A.I中有 键,还有大π键,故A错误;B.Se−Se是同种元素,因此I中的 键为非极性共价
键,故B正确;C.烃都是难溶于水,因此II难溶于水,故C错误;D.II中苯环上的碳原子和碳碳双键
上的碳原子杂化类型为sp2,碳碳三键上的碳原子杂化类型为sp,故D正确;E.根据同周期从左到右电负
性逐渐增大,同主族从上到下电负性逐渐减小,因此I~III含有的元素中,O电负性最大,故E正确;综上
所述,答案为:BDE。
(4)根据题中信息IV中O、Se都有孤对电子,碳、氢、硫都没有孤对电子;故答案为:O、Se。
(5)根据非羟基氧越多,酸性越强,因此硒的两种含氧酸的酸性强弱为 > 。 中Se
价层电子对数为 ,其立体构型为正四面体形;故答案为:>;正四面体形。
(6)①根据晶胞结构得到K有8个, 有 ,则X的化学式为KSeBr ;故答案为:
2 6
KSeBr 。
2 6
②设X的最简式的式量为 ,晶体密度为 ,设晶胞参数为anm,得到
,解得 ,X中相邻K之间的最短距离为晶胞参数的一半
即 ;故答案为: 。7.(1)
(2) A
(3)
(4)
【详解】(1)基态B原子价层电子的轨道表示式为: ;
(2)① 中C原子没有空轨道,不能与 分子形成配位键,不能使原有的键削弱、断裂,所以不易
发生水解, 、 、 都已发生水解,故选A;
② 水解的化学方程式: ;
③ 与NaOH溶液反应的离子方程式为:
(3)由图1可知,1mol该离子中有 个硼氧四面体,含有配位键数目为 ,其中硼原子的杂化轨道
类型为: 杂化;
(4)根据投影可知,1个B原子为3个Mg原子共用,故属于1个Mg原子的B原子为 ;1个Mg原子为
6个B原子共用,故属于1个B原子的Mg原子为 ,由此可知,Mg和B原子个数比为: ,所
以硼化镁的化学式为: 。
8.(1)
(2)A
(3) N>O>C sp2、sp3(4)CH 中的C和NH 中的N均为sp3杂化,但NH 中的N有一孤电子对,孤电子对和成键电子对的斥力大
4 3 3
于成键电子对之间的斥力
(5)Fe N
4
(6) d
【详解】(1)已知Cl是17号元素,故基态氯原子的核外电子排布式为:[Ne]3s23p5,故其价层电子排布
图为 ,故答案为: ;
(2)A项 即基态氮原子上1个1s电子跃迁到2p上,1个2s电子跃迁到2p上,B项 为
基态原子,C项 即1个1s电子跃迁到2p上,D项 即1个2s电子跃迁到2p上,故A所
示氮原子的能量最高,故答案为:A;
(3)根据同一周期从左往右元素第一电离能呈增大趋势,ⅤA与ⅥA反常,故EDTA的组成元素中C、
N、O的第一电离能由大到小顺序为N>O>C,由题干EDTA的结构简式可知,除羧基上的碳原子周围价
层电子对数为3,其他碳原子周围价层电子数为4,故碳原子的杂化轨道类型为sp2、sp3,故答案为:N>O
>C;sp2、sp3;
(4)CH 中的C和NH 中的N均为sp3杂化,但NH 中的N有一孤电子对,孤电子对和成键电子对的斥力
4 3 3
大于成键电子对之间的斥力,所以NH 的键角小于CH 的键角,故答案为:CH 中的C和NH 中的N均为
3 4 4 3
sp3杂化,但NH 中的N有一孤电子对,孤电子对和成键电子对的斥力大于成键电子对之间的斥力;
3
(5)由题干图1所示某种Fe、N组成的磁性化合物的结构,N随机排列在Fe构成的正八面体的空隙中,1
个晶胞中含有+3价铁个数为: =4,含+2价铁个数为: =12,含有N为4个,故该
磁性化合物的化学式为Fe N,故答案为:Fe N;
4 4
(6)已知Fe是26号元素,在元素周期表中第4周期第Ⅷ族,则铁元素位于d区,铁的某种晶胞沿面对角
线的位置切下之后可以得到如图2所示的截面可知,该铁晶体为体心立方,在铁晶胞中,与一个铁原子最
近的铁原子距离为立方体边长的 ,这样的原子有八个,因为铁原子的半径是anm,根据铁晶胞的结构可知,晶胞的边长为 nm,在每个晶胞中含有铁原子的数目为1+8× =2个,晶胞密度ρ═ = =
= g•cm-3,故答案为:d; 。
9.(1) [Ar]3dl04s24p1 (或1s22s22p63s23p63d104s24p1) K、Br
(2)N>C>H (或者N、C、H)
(3)sp2 sp3
(4)
(5)GaCl 属于分子晶体,而GaF 属于离子晶体,熔化时前者克服分子间作用力,后者克服离子键,而离子
3 2
键比分子间作用力更强,离子晶体熔点高于分子晶体
(6)正八
【详解】(1)Ga是31号元素,处于第四周期第IIIA族,原子核外电子排布式为[Ar]3dl04s24p1或
1s22s22p63s23p63d104s24p1;Ga原子未成对电子数为1,同周期主族元素中基态原子未成对电子数与Ga相同
的元素原子价电子排布式为4s1、4s24p5,分别为K元素、Br元素;
(2)EMIC阳离子含有C、N、H三种元素,同周期自左而右电负性增大,故电负性N>C,而C、N的氢
化物中它们均表现负化合价,电负性均大于氢元素的,即电负性N>C>H;
(3)EMIC中饱和碳原子是sp3杂化,五元环上的碳原子杂化类型为sp2杂化;
(4)五元环上原子形成大π键,环上C、N原子都采取sp2杂化,每个C原子有1个未杂化的电子,每个
N原子有2个未杂化的电子,该离子失去1个电子,大π键中的电子数为6,则EMIC中大π键可表示为
;
(5)GaCl 属于分子晶体,而GaF 属于离子晶体,融化时前者克服分子间作用力,后者克服离子键,而离
3 3
子键比分子间作用力更强,离子晶体熔点高于分子晶体的;
(6)①A、B、C、D位置氧离子与上底面面心的氧离子是氧离子构成的正八面体的一半,Ga3+位于O2-围
成的正八面体空隙中;②晶胞中O2-数目=3+12× +2× =6,则Ga3+的数目=6× =4,晶胞质量= g,故晶体密度=
。
10.(1) A CD
(2)K [Ni(CN) ]为离子晶体,熔化破坏离子键,离子键键能大,故熔沸点高,Ni(CO) 为分子晶体,熔化破坏
2 4 4
分子间作用力,分子间作用力小,故熔沸点小
(3)六方相氮化硼中没有自由移动电子,不可以导电 3:1
(4)∠3>∠2>∠1
【详解】(1)A中各轨道都处于全满状态比较稳定,较难失去电子,因此失去一个电子需要的能量最高;
发射光谱是指电子从高能量轨道跃迁到低能量轨道时释放能量的现象,即原子从激发态到稳态过程发出电
离辐射的过程,选项中处于激发态的原子为C、D。
(2)K[Ni(CN) ]为离子晶体,熔化破坏离子键,离子键键能大,故熔沸点高,Ni(CO) 为分子晶体,熔化破
2 4 4
坏分子间作用力,分子间作用力小,故熔沸点小。
(3)①石墨能导电,六方相氮化硼结构与石墨相似却不导电,原因是:六方相氮化硼与石墨一样都具有
层状结构,但石墨中每个碳原子最外层4个电子,形成3条共价键后,还有1个电子自由移动,而六方相
氮化硼中没有自由移动电子,不可以导电;
②立方相氮化硼晶体中B-N原子之间存在“一般共价键”,N原子含有孤电子对,B原子含有空轨道,可
以形成配位键,由立方相氮化硼晶体结构可知“一般共价键”与配位键的数目之比为:3:1;
③由晶胞结构可知,晶胞中含有4个N、8× +6× =4个B,即4个BN,故晶胞的摩尔质量为
[4×(11+14) ]g/mol,N = 。
A
(4)HO中O原子是sp3杂化,有2个孤电子对,空间构型为V形,两个H-O之间的夹角∠2为105°,
2
∠3为 中两个氧硫键之间的夹角, 中S原子是sp3杂化,且没有孤电子对,空间构型为正四面体形,
键角为109°28′,∠3为109°28′,形成∠1的水分子中的O原子和Fe原子形成了配位键,仍然是sp3杂化,但只有1个孤电子对,空间构型为三角锥形,∠1为107°,FeSO ·7H O中∠1、∠2、∠3由大到小的顺序
4 2
是∠3>∠2>∠1。