文档内容
【基础知识】电解池及金属的电化学腐蚀与防护
考点三 陌生电解池电极反应式书写
电解池电极反应式书写注意事项
(1)阳极材料不同,电极产物、电极反应式可能不同。
(2)电解质溶液中未参与放电的离子是否与放电后生成的离子发生反应(离子共存)。
(3)注意离子导体(电解质)是水溶液还是非水状态。
【课堂练习】
1. 按要求书写电极反应式和总反应方程式:
(1)用惰性电极电解MgCl 溶液
2
阳极反应式:_______________________________________________________________;
阴极反应式:_______________________________________________________________;
总反应离子方程式:_________________________________________________________;
(2)用Al作电极电解NaOH溶液
阳极反应式:_______________________________________________________________;
阴极反应式:_______________________________________________________________;
总反应离子方程式:_________________________________________________________;
(3)用铁作电极电解NaCl溶液
阳极反应式:_______________________________________________________________;
阴极反应式:_______________________________________________________________;
总反应方程式:_____________________________________________________________;
(4)离子液体是一种室温熔融盐,为非水体系。由有机阳离子、Al Cl和AlCl组成的离子液体作电解液时,
2
可在钢制品上电镀铝。钢制品应接电源的________极,已知电镀过程中不产生其他离子且有机阳离子不参
与电极反应,阴极反应式为____________________________________________________。
若改用AlCl 水溶液作电解液,则阴极产物为________________。
3
【答案】 (1)2Cl--2e-===Cl ↑ Mg2++2HO+2e-===H↑+Mg(OH) ↓
2 2 2 2
Mg2++2Cl-+2HO=====Mg(OH) ↓+Cl ↑+H↑
2 2 2 2
(2)2Al-6e-+8OH-===2AlO+4HO 6HO+6e-===3H↑+6OH-
2 2 2
2Al+2HO+2OH-=====2AlO+3H↑
2 2
(3)Fe-2e-===Fe2+ 2HO+2e-===H↑+2OH- Fe+2HO=====Fe(OH) ↓+H↑
2 2 2 2 2
(4)负 4Al Cl+3e-===Al+7AlCl H
2 2
2.按要求书写电极反应式和总反应方程式:(1)以铝材为阳极,电解HSO 溶液,铝材表面形成氧化膜
2 4
阳极反应式:_________________________________________________________________;
阴极反应式:_________________________________________________________________;
总反应方程式:_______________________________________________________________。
(2)电解MnSO 溶液可制备MnO ,其阳极的电极反应式为___________________________。
4 2
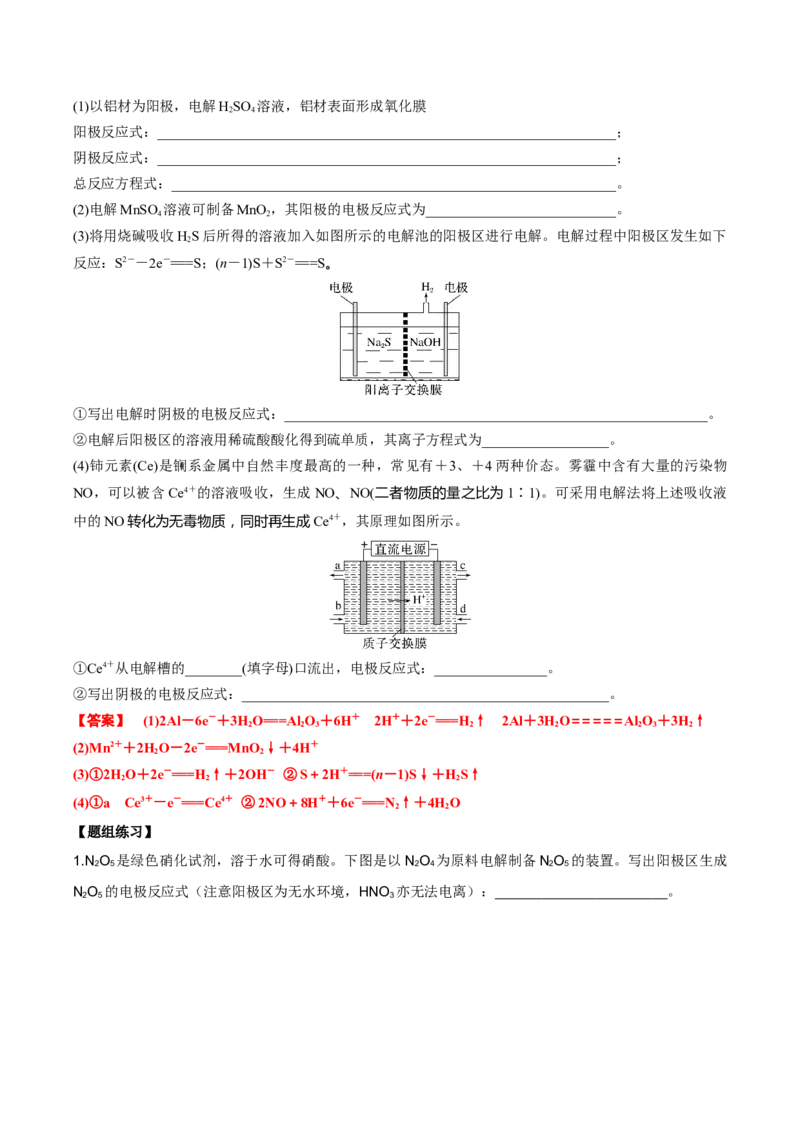
(3)将用烧碱吸收HS后所得的溶液加入如图所示的电解池的阳极区进行电解。电解过程中阳极区发生如下
2
反应:S2--2e-===S;(n-1)S+S2-===S。
①写出电解时阴极的电极反应式:____________________________________________________________。
②电解后阳极区的溶液用稀硫酸酸化得到硫单质,其离子方程式为__________________。
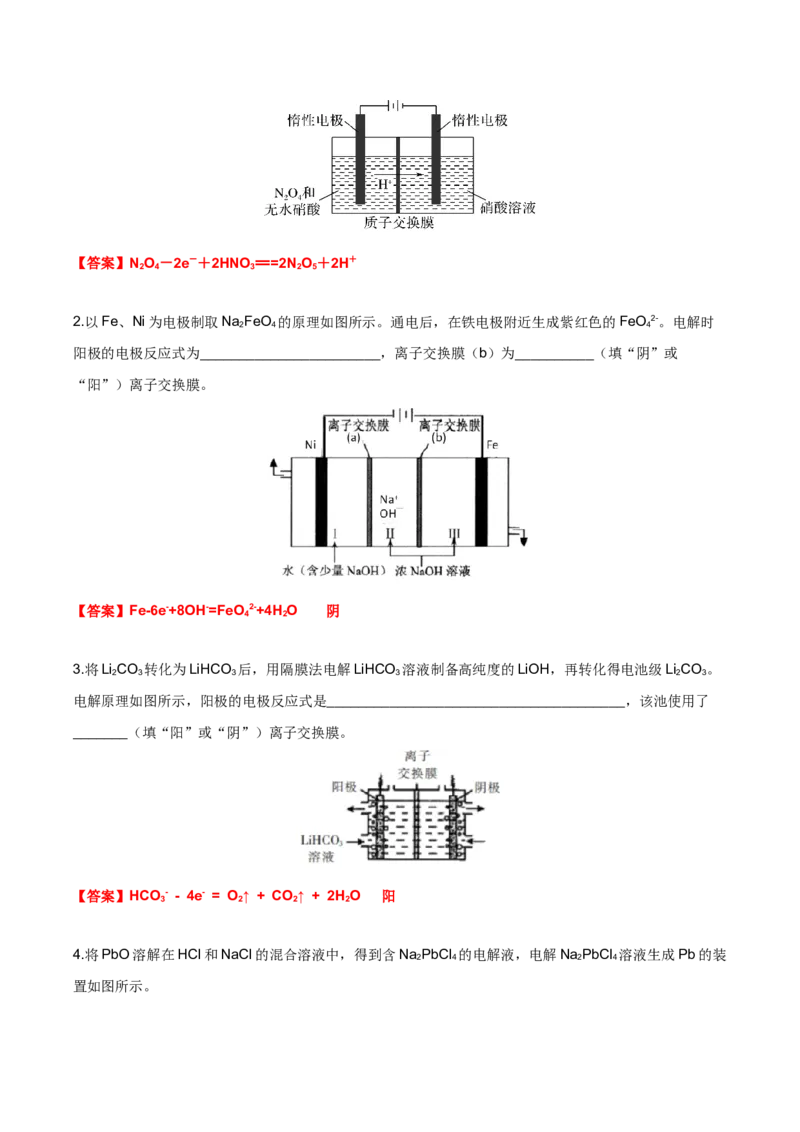
(4)铈元素(Ce)是镧系金属中自然丰度最高的一种,常见有+3、+4两种价态。雾霾中含有大量的污染物
NO,可以被含Ce4+的溶液吸收,生成NO、NO(二者物质的量之比为1∶1)。可采用电解法将上述吸收液
中的NO转化为无毒物质,同时再生成Ce4+,其原理如图所示。
①Ce4+从电解槽的________(填字母)口流出,电极反应式:________________。
②写出阴极的电极反应式:____________________________________________________。
【答案】 (1)2Al-6e-+3HO===Al O+6H+ 2H++2e-===H↑ 2Al+3HO=====Al O+3H↑
2 2 3 2 2 2 3 2
(2)Mn2++2HO-2e-===MnO ↓+4H+
2 2
(3)①2HO+2e-===H↑+2OH- ②S+2H+===(n-1)S↓+HS↑
2 2 2
(4)①a Ce3+-e-===Ce4+ ②2NO+8H++6e-===N↑+4HO
2 2
【题组练习】
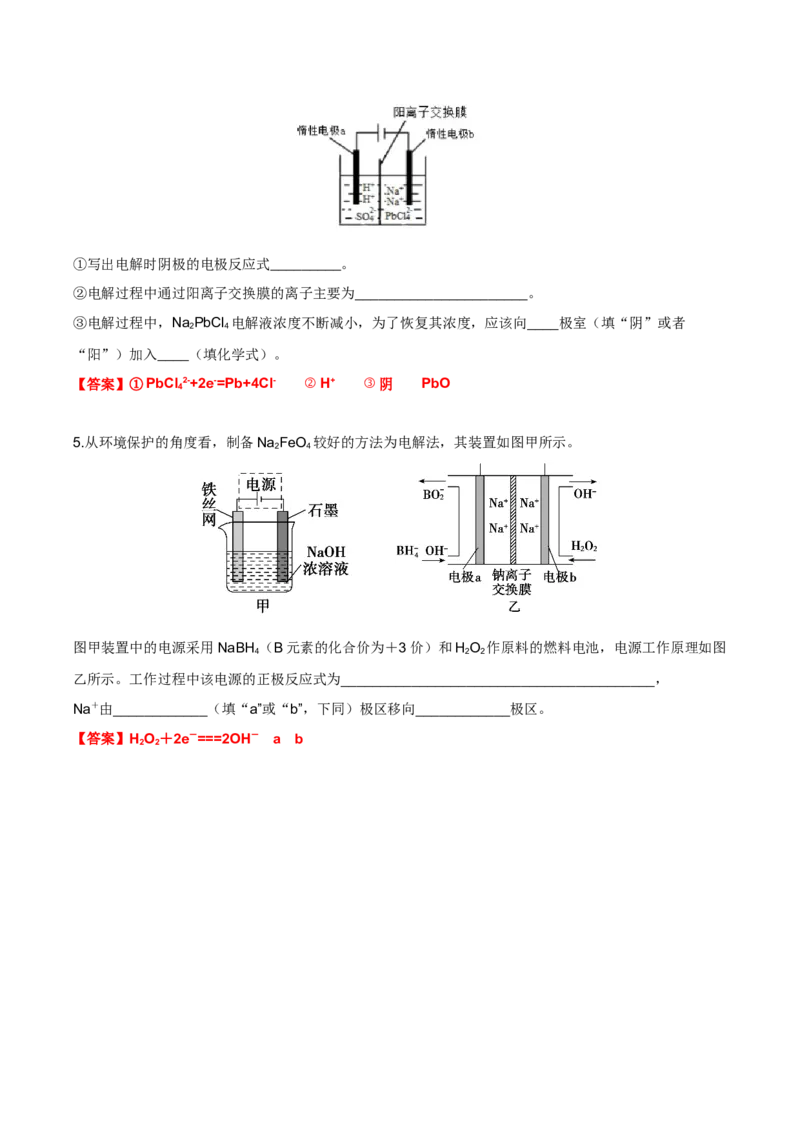
1.N O 是绿色硝化试剂,溶于水可得硝酸。下图是以N O 为原料电解制备N O 的装置。写出阳极区生成
2 5 2 4 2 5
N O 的电极反应式(注意阳极区为无水环境,HNO 亦无法电离):______________________。
2 5 3【答案】N O -2e-+2HNO ===2N O +2H+
2 4 3 2 5
2.以Fe、Ni为电极制取Na FeO 的原理如图所示。通电后,在铁电极附近生成紫红色的FeO 2-。电解时
2 4 4
阳极的电极反应式为_______________________,离子交换膜(b)为__________(填“阴”或
“阳”)离子交换膜。
【答案】Fe-6e-+8OH-=FeO 2-+4H O 阴
4 2
3.将Li CO 转化为LiHCO 后,用隔膜法电解LiHCO 溶液制备高纯度的LiOH,再转化得电池级Li CO 。
2 3 3 3 2 3
电解原理如图所示,阳极的电极反应式是______________________________________,该池使用了
_______(填“阳”或“阴”)离子交换膜。
【答案】HCO - - 4e- = O ↑ + CO ↑ + 2H O 阳
3 2 2 2
4.将PbO溶解在HCl和NaCl的混合溶液中,得到含Na PbCl 的电解液,电解Na PbCl 溶液生成Pb的装
2 4 2 4
置如图所示。①写出电解时阴极的电极反应式_________。
②电解过程中通过阳离子交换膜的离子主要为______________________。
③电解过程中,Na PbCl 电解液浓度不断减小,为了恢复其浓度,应该向____极室(填“阴”或者
2 4
“阳”)加入____(填化学式)。
【答案】①PbCl 2-+2e-=Pb+4Cl- ② H+ ③阴 PbO
4
5.从环境保护的角度看,制备Na FeO 较好的方法为电解法,其装置如图甲所示。
2 4
图甲装置中的电源采用NaBH (B元素的化合价为+3价)和H O 作原料的燃料电池,电源工作原理如图
4 2 2
乙所示。工作过程中该电源的正极反应式为________________________________________,
Na+由____________(填“a”或“b”,下同)极区移向____________极区。
【答案】H O +2e-===2OH- a b
2 2