文档内容
2022 届高三化学二轮复习原子结构与性质专题练习
一、选择题(共17题)
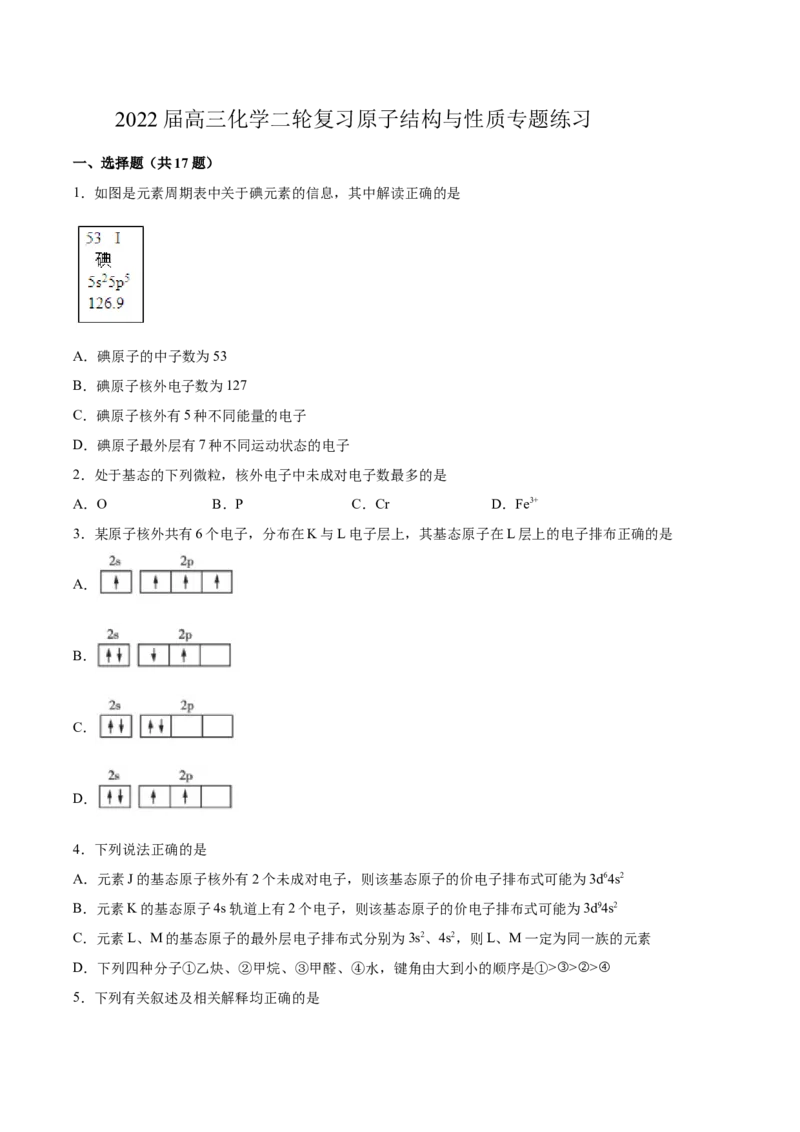
1.如图是元素周期表中关于碘元素的信息,其中解读正确的是
A.碘原子的中子数为53
B.碘原子核外电子数为127
C.碘原子核外有5种不同能量的电子
D.碘原子最外层有7种不同运动状态的电子
2.处于基态的下列微粒,核外电子中未成对电子数最多的是
A.O B.P C.Cr D.Fe3+
3.某原子核外共有6个电子,分布在K与L电子层上,其基态原子在L层上的电子排布正确的是
A.
B.
C.
D.
4.下列说法正确的是
A.元素J的基态原子核外有2个未成对电子,则该基态原子的价电子排布式可能为3d64s2
B.元素K的基态原子4s轨道上有2个电子,则该基态原子的价电子排布式可能为3d94s2
C.元素L、M的基态原子的最外层电子排布式分别为3s2、4s2,则L、M一定为同一族的元素
D.下列四种分子①乙炔、②甲烷、③甲醛、④水,键角由大到小的顺序是①>③>②>④
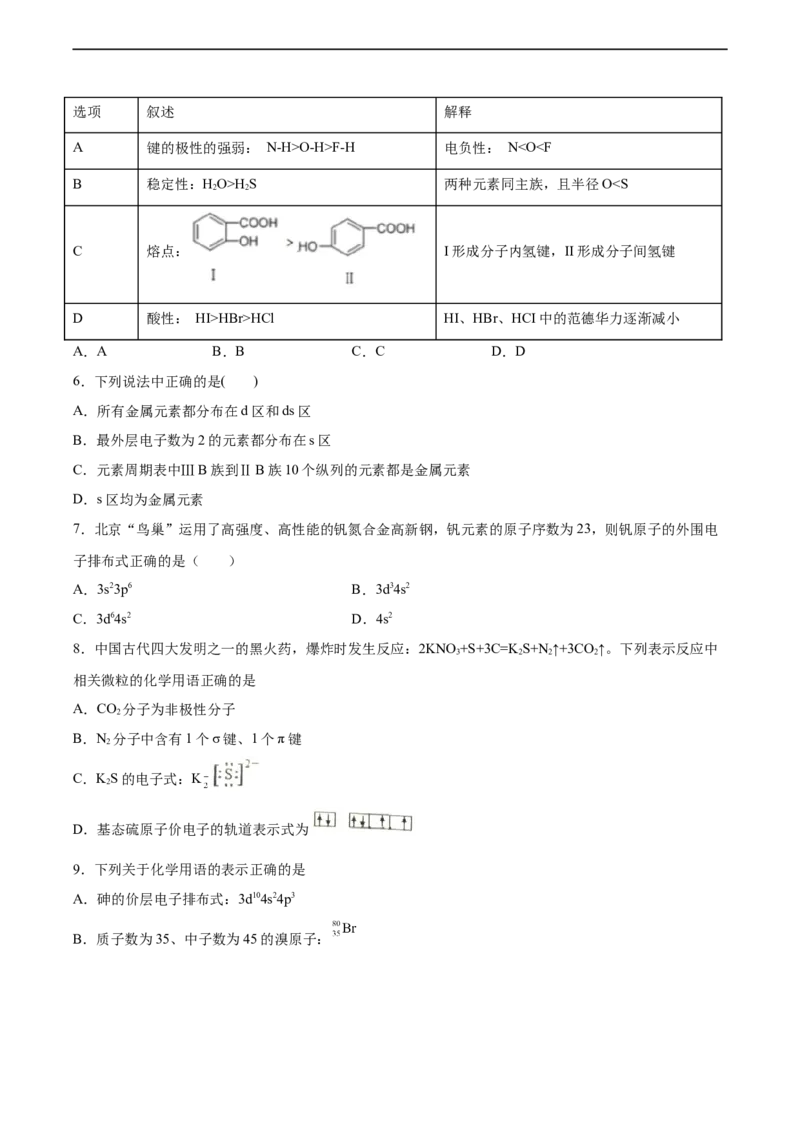
5.下列有关叙述及相关解释均正确的是选项 叙述 解释
A 键的极性的强弱: N-H>O-H>F-H 电负性: NHS 两种元素同主族,且半径OHBr>HCl HI、HBr、HCI中的范德华力逐渐减小
A.A B.B C.C D.D
6.下列说法中正确的是( )
A.所有金属元素都分布在d区和ds区
B.最外层电子数为2的元素都分布在s区
C.元素周期表中ⅢB族到ⅡB族10个纵列的元素都是金属元素
D.s区均为金属元素
7.北京“鸟巢”运用了高强度、高性能的钒氮合金高新钢,钒元素的原子序数为23,则钒原子的外围电
子排布式正确的是( )
A.3s23p6 B.3d34s2
C.3d64s2 D.4s2
8.中国古代四大发明之一的黑火药,爆炸时发生反应:2KNO+S+3C=KS+N↑+3CO ↑。下列表示反应中
3 2 2 2
相关微粒的化学用语正确的是
A.CO 分子为非极性分子
2
B.N 分子中含有1个σ键、1个π键
2
C.KS的电子式:K
2
D.基态硫原子价电子的轨道表示式为
9.下列关于化学用语的表示正确的是
A.砷的价层电子排布式:3d104s24p3
B.质子数为35、中子数为45的溴原子:C.硫离子的结构示意图:
D.过氧化钠的电子式:
10.硒( Se)是人体必需的微量元素,它能有效提高人体免疫机能,抑制癌症和心脑血管等疾病的发病率。
34
下列有关说法错误的是
A.硒元素位于元素周期表中第15列
B.硒元素原子的价电子排布式为4s24p4
C.硒的最高价氧化物对应的水化物的化学式为HSeO
2 4
D.O和Se均为p区非金属元素
11.下列说法正确的是
A.电中性基态原子失去一个电子转化为气态基态正离子所需的最低能量叫第一电离能
B.电负性大于1.8的元素一定是非金属元素
C.s能级电子云轮廓呈球形,s电子在球形内绕核运动
D.节日燃放的焰火与电子跃迁有关
12.短周期主族元素X、Y、Z、W的原子序数依次增大,X和Y的基态原子的2p能级上各有两个未成对
电子,Z元素基态原子的最高s能级电子数是其基态原子最低能级电子数的一半,W的原子半径在同周期
中最小.下列说法正确的是
A.X、Y、Z、W四种元素组成的常见单质熔沸点依次升高
B.X、Y、Z、W四种元素中的某些元素既可组成含有非极性共价键的离子晶体,也能组成含有极性共价
键的离子晶体
C.Z、W元素组成的物质其晶胞结构中Z的配位数为8
D.X元素的单质存在多种同素异形体,且熔点都很高
13.下列说法错误的是
A.晶格能:NaF>NaCl>NaBr
B.某原子的质量数是52,中子数是28,则其基态原子中,未成对电子数为6
C.已知金属铜的晶胞为面心立方最密堆积,则铜原子的配位数为12
D.某元素基态原子4s轨道上有2个电子,则该基态原子价电子排布可能是3d94s2
14.元素周期表中铋元素的数据见图,下列说法不正确的是A.Bi原子s轨道的形状是球形的,p轨道的形状是哑铃形
B.Bi元素的相对原子质量是209.0
C.Bi原子6p能级中6p、6p、 6p 轨道上各有一个电子
x y z
D.Bi元素与Ga元素属于同一主族
15.下列有关微粒性质的排列顺序正确的是
A.离子半径:O2- >Na +> S2-
B.最高化合价:O>N>C
C.电负性:F>P>O
D.基态原子中未成对电子数:Mn>Si>Cl
16.FeO晶胞结构如图所示,其摩尔质量为Mg/mol,阿伏加德罗常数为N ,晶体的密度为dg/cm3,下列
A
说法错误的是
A.Fe位于第四周期第ⅧB族,属于d区
B.Fe2+的电子排布简式为[Ar]3d6
C.该晶体中,距Fe2+最近的O2-形成正八面体
D.该晶体中两个距离最近的同种离子的核间距为 cm
17.已知X、Y是主族元素,I为电离能,单位是KJ/mol。根据下表所列数据判断错误的是
元素 I I I I
1 2 3 4
X 500 4600 6900 9500
Y 580 1800 2700 11600A.元素X的常见化合价是+1价 B.元素X与氯形成化合物时,化学式可能是XCl
2
C.元素Y是ⅢA族的元素 D.若元素Y处于第3周期,它不能与冷水剧烈反应
二、综合题(共6题)
18.苯甲酸是一种重要原料。实验室可以用高锰酸钾在中性条件下氧化甲苯(副产品为MnO )制得,有关数
2
据如下:
熔点/℃ 沸点/℃ 水中溶解度/g(25℃) 相对分子质量 密度/(g·cm-3)
甲苯 -94.9 110.6 难溶 92 0.85
苯甲酸 122.13 249 0.344 122 1.27
合成步骤:
①在装有电动搅拌,温度计和球形冷凝管的三颈烧瓶中加入2.7mL甲苯和100mL蒸馏水,分批加入8.5g
高锰酸钾固体,回流4小时。
②反应结束后,趁热过滤,热水洗涤后,冰水冷却,盐酸酸化,抽滤,洗涤,沸水浴干燥得苯甲酸粗品。
回答下列问题;
(1)基态Mn原子的电子排布式:_______。
(2)请写出甲苯被高锰酸钾氧化的化学反应方程式:_______。
(3)球形冷凝管的作用是_______,步骤①中反应完全的现象是_______。
(4)实验过程中,发现滤液呈紫色,盐酸酸化时产生了黄绿色气体,酸化操作前加入最理想的_______溶液
消除过量的高锰酸钾。
A.NaHSO B.HO C.Na D.FeCl
3 2 2 3
(5)重结晶时,苯甲酸粗品完全溶解后,须补加少量蒸馏水,目的是_______。
(6)副产品MnO 是碱式锌锰电池的正极材料,放电时产生MnO(OH),正极的反应式为_______。
2
19.W、X、Y、Z为原子序数依次增大的前四周期元素,元素W是宇宙中最丰富的元素,元素X的原子
最外层电子数是其内层的3倍,元素Z的基态原子核外电子有24种运动状态,Y、X、Z不在同一周期,
且Y原子核外p电子比s电子多5个。
(1)Z基态原子的核外电子排布式为____________。
(2)Z的氧化物是石油化工中重要的催化剂之一,如催化异丙苯( )裂化生成苯和丙烯。
①1 mol丙烯分子中含有σ键与π键的数目之比为________。
②苯分子中碳原子轨道的杂化类型为________。
③Z的一种氧化物ZO 中,Z的化合价为+6,则其中过氧键的数目为________个。
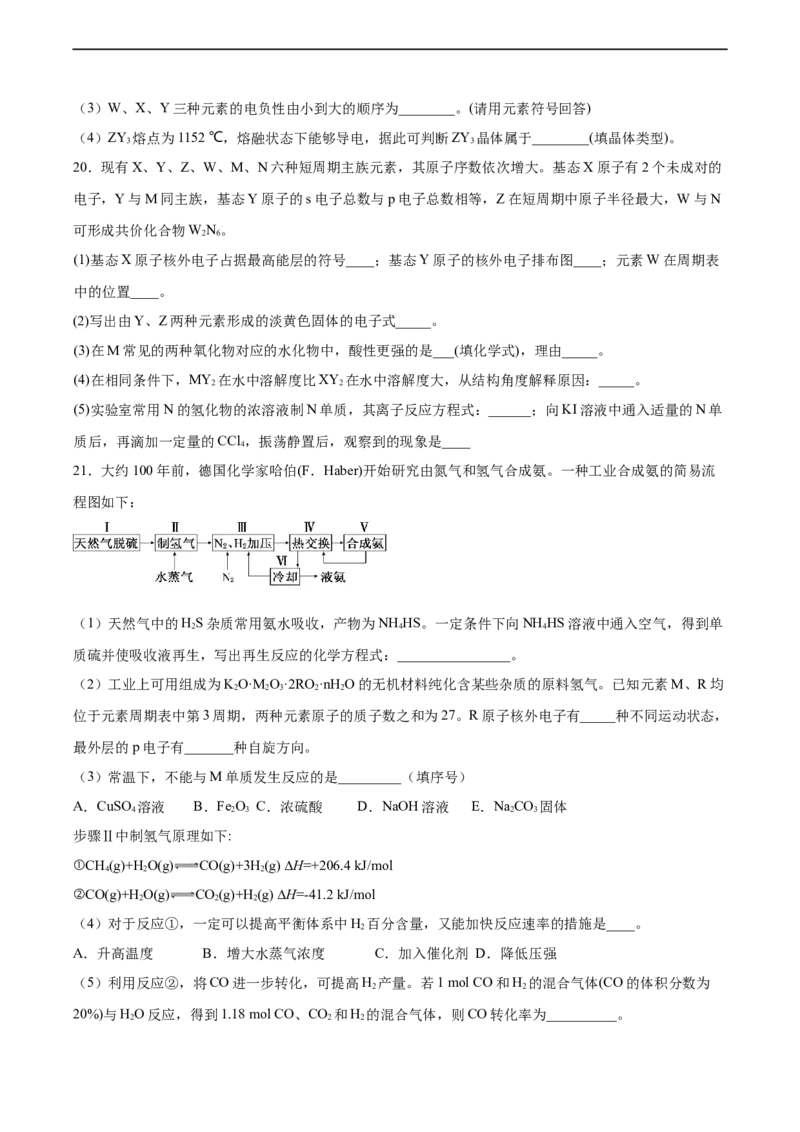
5(3)W、X、Y三种元素的电负性由小到大的顺序为________。(请用元素符号回答)
(4)ZY 熔点为1152 ℃,熔融状态下能够导电,据此可判断ZY 晶体属于________(填晶体类型)。
3 3
20.现有X、Y、Z、W、M、N六种短周期主族元素,其原子序数依次增大。基态X原子有2个未成对的
电子,Y与M同主族,基态Y原子的s电子总数与p电子总数相等,Z在短周期中原子半径最大,W 与N
可形成共价化合物WN。
2 6
(1)基态X原子核外电子占据最高能层的符号____;基态Y原子的核外电子排布图____;元素W在周期表
中的位置____。
(2)写出由Y、Z两种元素形成的淡黄色固体的电子式_____。
(3)在M常见的两种氧化物对应的水化物中,酸性更强的是___(填化学式),理由_____。
(4)在相同条件下,MY 在水中溶解度比XY 在水中溶解度大,从结构角度解释原因:_____。
2 2
(5)实验室常用N的氢化物的浓溶液制N单质,其离子反应方程式:______;向KI溶液中通入适量的N单
质后,再滴加一定量的CCl ,振荡静置后,观察到的现象是____
4
21.大约100年前,德国化学家哈伯(F.Haber)开始研究由氮气和氢气合成氨。一种工业合成氨的简易流
程图如下:
(1)天然气中的HS杂质常用氨水吸收,产物为NH HS。一定条件下向NH HS溶液中通入空气,得到单
2 4 4
质硫并使吸收液再生,写出再生反应的化学方程式:________________。
(2)工业上可用组成为KO·M O·2RO·nH O的无机材料纯化含某些杂质的原料氢气。已知元素M、R均
2 2 3 2 2
位于元素周期表中第3周期,两种元素原子的质子数之和为27。R原子核外电子有_____种不同运动状态,
最外层的p电子有_______种自旋方向。
(3)常温下,不能与M单质发生反应的是_________(填序号)
A.CuSO 溶液 B.Fe O C.浓硫酸 D.NaOH溶液 E.NaCO 固体
4 2 3 2 3
步骤Ⅱ中制氢气原理如下:
①CH(g)+HO(g) CO(g)+3H(g) ∆H=+206.4 kJ/mol
4 2 2
②CO(g)+H O(g) CO(g)+H(g) ∆H=-41.2 kJ/mol
2 2 2
(4)对于反应①,一定可以提高平衡体系中H 百分含量,又能加快反应速率的措施是____。
2
A.升高温度 B.增大水蒸气浓度 C.加入催化剂 D.降低压强
(5)利用反应②,将CO进一步转化,可提高H 产量。若1 mol CO和H 的混合气体(CO的体积分数为
2 2
20%)与HO反应,得到1.18 mol CO、CO 和H 的混合气体,则CO转化率为__________。
2 2 2(6)依据温度对合成氨反应的影响,在下图坐标系中,画出一定条件下的密闭容器内,从通入原料气开
始,随温度不断升高,NH 物质的量变化的曲线示意图。______________
3
22.中国炼丹家约在唐代或五代时期掌握了以炉甘石点化鑰石(即石金)的技艺:将炉甘石(ZnCO)、赤铜矿
3
(主要成分Cu O和木炭粉混合加热至800℃左右可制得与黄金相似的输石金。回答下列问题:
2
(1)锌元素基态原子的价电子排布式为___________,铜元素基态原子中的未成对电子数为___________。
(2)硫酸锌溶于过量氨水形成[Zn(NH )]SO 溶液。
3 4
①[Zn(NH )]SO 中,阴离子的立体构型是___________,[Zn(NH )]2+中含有的化学键有_______。
3 4 4 3 4
②NH 分子中,中心原子的轨道杂化类型为___________,NH 在HO中的溶解度___________(填“大”或
3 3 2
“小”),原因是_________________________________。
(3)铜的第一电离能为I =745.5 kJ·mol-1,第二电离能为l =1957.9 kJ·mol-1,锌的第一电离能为
1(Cu) 2(Cu)
I =906.4 kJ·mol-1,第二电离能为I =1733.3kJ·mol-1,I >I 的原因是_______________
1(Zn) 2(Zn) 2(Cu) 2(Zn)
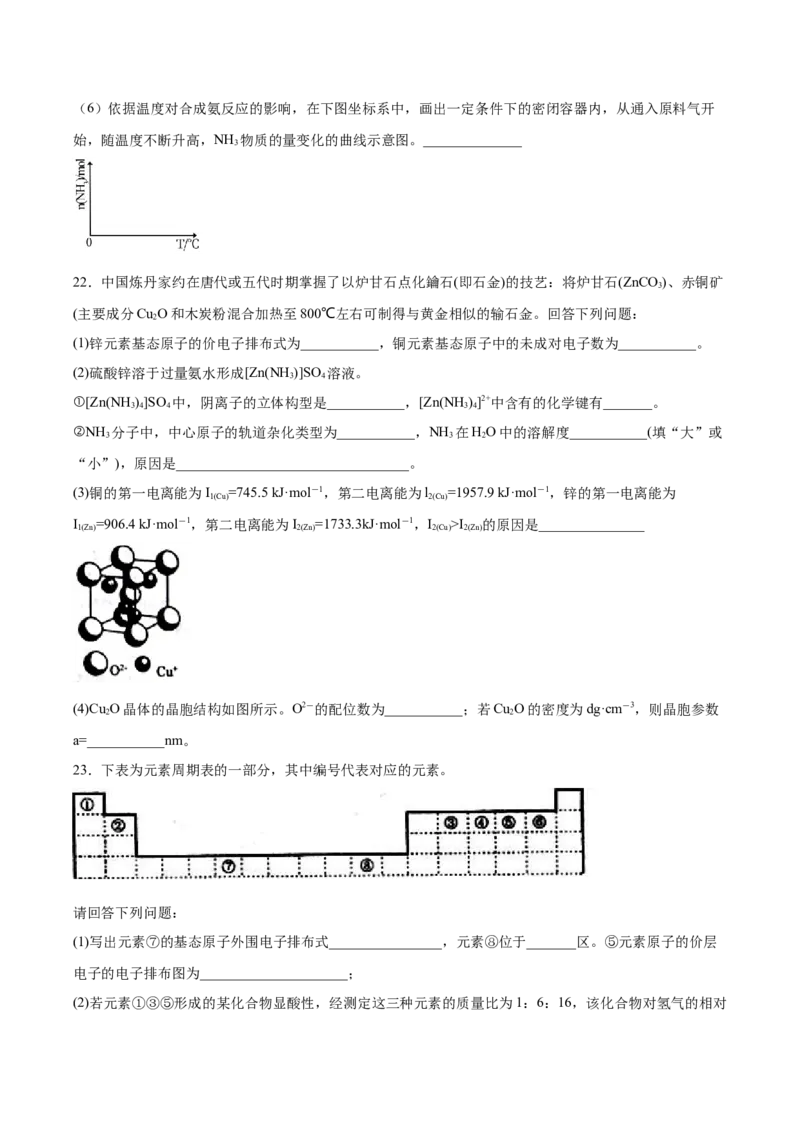
(4)Cu O晶体的晶胞结构如图所示。O2-的配位数为___________;若Cu O的密度为dg·cm-3,则晶胞参数
2 2
a=___________nm。
23.下表为元素周期表的一部分,其中编号代表对应的元素。
请回答下列问题:
(1)写出元素⑦的基态原子外围电子排布式________________,元素⑧位于_______区。⑤元素原子的价层
电子的电子排布图为_____________________;
(2)若元素①③⑤形成的某化合物显酸性,经测定这三种元素的质量比为1:6:16,该化合物对氢气的相对密度为23,则其中所有杂化原子的杂化方式分别为___________和________________。
(3)元素③④⑤⑥的第一电离能由大到小的顺序是_________(用元素符号表示)。请写出由④和⑤两种元
素形成的与Nˉ互为等电子体的分子的化学式________________,(写出一种即可)其VSEPR构型为
3
___________。
(4)ZnS的晶胞结构如图1所示,在ZnS晶胞中,S2-的配位数为 ___________。
(5)铜能与类卤素(SCN) 分子(与氯气分子性质相似)反应生成Cu(SCN) ,1mol(SCN) 分子中含有共价键
2 2 2
的数目为______________。铜与金形成的金属互化物结构如图2,其晶胞边长为a nm,该金属互化物的密
度为__________(用含“a、N 的代数式表示)g/cm3)。
A参考答案
1.D
【详解】
A.由图可知,碘元素的原子序数为53,原子序数=质子数=53,故A错误;
B.碘元素的相对原子质量为126.9,原子序数=原子核外电子数=53,故B错误;
C.外围电子排布为5s25p5,处于第五周期ⅦA族,有1s、2s、2p、3s、3p、3d、4s、4p、
4d、5s、5p共11种不同能量的电子,故C错误;
D.最外层电子排布为5s25p5,最外层有7种不同运动状态的电子,故D正确;
答案选D。
2.C
【详解】
O价电子为2s22p4,未成对电子数为2个;P价电子为3s23p3,未成对电子数为3个;Cr价
电子为3d54s1,未成对电子数为6个;Fe3+价电子为3d5,未成对电子数为5个;因此核外电
子中未成对电子数最多的是Cr,故C符合题意。
综上所述,答案为C。
3.D
【详解】
根据构造原理,6个电子的基态原子的电子排布式为:1s22s22p2,其中L能层的2p能级的2
个电子排布需遵守洪特规则,单独占据一个轨道,而且自旋方向相同,所以,该基态原子
在L层上的电子排布为: ,D选项正确;
答案选D。
4.D
【详解】
A.若基态原子的价电子排布式为3d64s2,则其3d能级有4个未成对电子,故A错误;
B.能级全空、半满、全满能量更低,所以基态原子的价电子排布式不可能为3d94s2,此时
应为3d104s1,故B错误;
C.L的最外层电子排布式为3s2,则为镁元素,M的最外层电子排布式为4s2,其可能为钙
元素,但也可能为过渡元素,如Fe(3d64s2),不一定为同族元素,故C错误;
D.乙炔分子为直线形,键角为180°;甲烷分子为正四面体,键角为109°28′;甲醛分子为
平面三角形,键角略小于120°;水分子为V形,键角为104.5°,所以键角由大到小的顺序
是①>③>②>④,故D正确;
故答案为D。
5.B
【详解】A. 电负性:NHBr>HCl,HI、HBr、HCI中共价键越来越强,在水中电离能力变弱,故D
项错误;
综上所述,本题正确答案为B。
6.C
【详解】
A、所有金属元素都分布在s区、d区和ds区,A错误;B、第ⅡB族最外层电子数为2,
在ds区,B错误;C、元素周期表中ⅢB族到ⅡB族10个纵行的元素,称为过渡元素全部
为金属,C正确;D、s区均的氢为非金属元素,D错误;答案选C。
7.B
【详解】
钒元素的原子序数为23,钒原子核外电子数为23,根据电子排布规律,钒原子电子排布式
为1s22s22p63s23p63d34s2,钒元素为副族元素,其外围电子排布式为3d34s2;
综上所述,答案为B。
8.A
【分析】
【详解】
A.CO 是直线形,为非极性分子,故A正确;
2
B.N 分子中存在氮氮三键,含有1个σ键、2个π键,故B错误;
2
C.KS的电子式为:K K ,故C错误;
2
D.基态硫原子价电子的轨道表示式为基态硫原子价电子的轨道表示式为 ,
故D错误;
故选A。
9.B
【详解】
A.砷的价层电子排布式为4s24p3,A用语错误;
B.质子数为35、中子数为45的溴原子的质量数为80,B用语正确:
C.硫离子为硫原子得到2个电子形成,最外层达到8电子的稳定结构,结构示意图中,最
外层应有8个电子,C用语错误;D.过氧化钠是由钠离子和过氧根离子构成的,电子式为 ,D用语错误;
答案为B。
10.A
【详解】
A.O、S、Se位于同一主族,因此硒元素位于元素周期表中第16列,故A错误;
B.硒( Se)元素原子的电子排布式为[Ne]4s24p4,价电子排布式为4s24p4,故B正确;
34
C.硒是第VIA族元素,Se的最高价氧化物对应的水化物的化学式为HSeO,故C正确;
2 4
D.O和Se价电子排布式为ns2np4,都为p区非金属元素,故D正确。
综上所述,答案为A。
11.D
【详解】
A.气态电中性基态原子失去一个电子转化为气态基态正离子所需要的最低能量叫第一电
离能,故A错误;
B.电负性大于1.8的元素不一定是非金属元素,如Bi等,故B错误;
C.s能级的原子轨道呈球形,处在该轨道上的电子不只在球壳内运动,还在球壳外运动,
只是在球壳外运动概率较小,故C错误;
D.焰色反应时原子中的电子吸收了能量,从能量较低的基态跃迁到能量较高的激发态,
但处于能量较高激发态的电子是不稳定的,很快跃迁回能量较低的基态,将多余的能量以
光的形式放出,因而能使火焰呈现颜色,与电子跃迁有关,故D正确;
故选D。
12.B
【分析】
X和Y的基态原子的2p能级上各有两个未成对电子,Y的原子序数较大,则X为C元素,
Y为O元素;Z元素基态原子的最高s能级电子数是其基态原子最低能级电子数的一半,
则Z的最高s能级有1个电子,即最外层有1个电子,其原子序数大于O,则Z为Na元素;
W的原子半径在同周期中最小,W的原子序数大于Na,应为第三周期元素,则W为Cl元
素;综上所述X为C、Y为O、Z为Na、W为Cl。
【详解】
A.X、Y、Z、W四种元素组成的常见单质为C(金刚石、石墨等)、O、Na、Cl,常见的
2 2
碳单质(金刚石、石墨等)为共价晶体,熔点最高,O、Cl 均为分子晶体,且结构相似,氯
2 2
气的相对原子质量较大,熔点较高,Na为金属晶体,熔点高于O、Cl,所以四种元素组
2 2
成的常见单质熔沸点为X>Z>W>Y,A错误;
B.O和Na可以形成化合物NaO,为含有非极性键的离子晶体,C、O、Na可以形成
2 2
NaCO,为含有极性共价键的离子晶体,B正确;
2 3C.Z、W元素组成的物质为NaCl,其晶胞结构如图 ,Na+的配位数为6,C
错误;
D.碳元素的同素异形体中也有分子晶体,如C ,其熔点不是很高,D错误;
60
综上所述答案为B。
13.D
【详解】
A.离子半径:Br->Cl->F-,离子半径越小,晶格能越大,因此晶格能:NaF>NaCl>
NaBr,故A正确;
B.某原子的质量数是52,中子数是28,则质子数=52-28=24,该元素为Cr,基态Cr原子
的价电子排布式为3d54s1,轨道表达式为 ,未成对电子数
为6,故B正确;
C.面心立方堆积,这样看,先取一个面,与之相邻且等距的有8个面,每个面的面心到
取的标准面的面心的距离是 (把棱长看成1),同时,面心这一点倒顶点最近且等距的有
4个,距离也是 ,所以配位数是12,故C正确;
D.3d94s2不满足洪特规则特例,正确排布式为3d104s1,故D错误;
综上所述,说法错误的是D项,故答案为D。
14.D
【详解】
A.s轨道的形状是球形的,p轨道的形状是哑铃形,选项A正确;
B.由图可知,Bi元素的相对原子质量是209.0,选项B正确;
C.根据洪特规则可知,电子排布在同一能级的不同轨道时,总是首先单独占一个轨道,
而且自旋方向相同,故Bi原子6p能级中6p、6p、6p 轨道上各有一个电子,选项C正确;
x y z
D.Bi元素是第六周期V A族元素,Ga元素为第四周期ⅢA族元素,两者不属于同一主族,
选项D不正确。
答案选D。
15.D
【详解】
A. 同主族时电子层越多,离子半径越大;具有相同电子排布的离子,原子序数大的离子半
径小,因此离子半径大小顺序是:S2->O2->Na+,故A错误;B. 同周期从左向右第一电离能呈增大趋势 ,但IIA>IIIA,VA>VIA,因此第一电离能大小
顺序是N>O>C,故B错误;
C. 同周期从左向右电负性增大,同主族从上到下电负性减小,F的电负性大于O,N的电
负性大于P,O的电负性大于N,因此电负性大小顺序是F>O>P,故C错误;
D. Mn的价电子排布式为3d54s2,未成对电子数为5,Si的价电子排布式为3s23p2,未成对
电子数为2,Cl的价电子排布式为3s23p5,未成对电子数为1,因此顺序是Mn>Si>Cl,故
D正确;
答案选D。
16.A
【详解】
A.Fe位于第四周期第Ⅷ族,铁不是副族元素,故A错误;
B.Fe是26号元素,Fe失去最外层2个电子生成Fe2+,Fe2+的电子排布简式为[Ar]3d6,故
B正确;
C.该晶体中,距Fe2+最近的O2-有6个,形成正八面体,故C正确;
D.设晶胞边长为a,根据均摊原则,每个晶胞含有4个FeO,则 ,a= ,
该晶体中两个距离最近的同种离子的核间距为面对角线的一半,所以距离为
cm,故D正确;
选A。
17.B
【详解】
分析表格中逐级电离能数据可知,元素X的第二电离能I 是其第一电离能I 的9.2倍,第
2 1
二级电离能发生突变;元素Y的第四电离能I 是其第三电离能I 的4.3倍,第四级电离能
4 3
发生突变,说明X元素原子最外层只有1个电子,Y元素原子最外层有3个电子。
A.主族元素的最高正价等于最外层电子数,所以元素X的常见化合价是+1价,A项正确;
B.元素X的常见化合价为+1价,X与氯形成化合物时化学式应该是XCl。B项错误;
C.元素Y最外层有3个电子且是主族元素,所以元素Y是IIIA族元素,C项正确;
D. 若元素Y处于第3周期,结合C项分析可知元素Y是铝元素,铝不能与冷水剧烈反应,
D项正确;答案选B。
18.[Ar]3d54s2 +2KMnO +2MnO+2H O 冷凝回
4 2 2
流,使反应充分进行 三颈烧瓶内的液体不再分层 B 使杂质及苯甲酸充分溶解,
便于重结晶得到纯净的苯甲酸 MnO +e-+H O= MnO(OH)+OH-
2 2
【详解】(1) Mn原子序数为25,故基态Mn原子的电子排布式为[Ar]3d54s2,故答案为:[Ar]
3d54s2;
(2)根据题中已知,甲苯被高锰酸钾氧化为苯甲酸钾,苯甲酸钾经酸化得苯甲酸,甲苯被高
锰酸钾氧化的化学反应方程式为 +2KMnO
4
+2MnO+2H O,故答案为: +2KMnO +2MnO+2H O;
2 2 4 2 2
(3) 球形冷凝管的作用是冷凝回流,使反应充分进行;三颈烧瓶内的液体不再分层即步骤
①中反应完全,故答案为:冷凝回流,使反应充分进行;三颈烧瓶内的液体不再分层;
(4) 为防止引入新的杂质,最理想的试剂为HO,故答案为:B;
2 2
(5) 补加少量蒸馏水是确保所有物质完全溶解,提高重结晶后苯甲酸的纯度,使杂质及苯
甲酸充分溶解,便于重结晶得到纯净的苯甲酸,故答案为:使杂质及苯甲酸充分溶解,便
于重结晶得到纯净的苯甲酸;
(6) 正极反应式MnO 得电子生成MnO(OH),Mn元素降1价,由元素守恒、电荷守恒得正
2
极反应式为:MnO +e-+H O= MnO(OH)+OH-,故答案为:MnO +e-+H O= MnO(OH)+OH-。
2 2 2 2
19.1s22s22p63s23p63d54s1(或[Ar]3d54s1) 8∶1 sp2 2 H