文档内容
16 新型电源及电极反应式的书写
1.电极反应式书写的一般步骤(类似氧化还原反应方程式的书写)
2.新型燃料电池
(1)燃料电池常用的燃料
H、CO、烃(如CH、C H)、醇(如CHOH)、肼(N H)等。
2 4 2 6 3 2 4
(2)燃料电池常用的电解质
①酸性电解质溶液,如HSO 溶液;②碱性电解质溶液,如NaOH溶液;③熔融氧化物;④
2 4
熔融碳酸盐,如KCO;⑤质子交换膜等。
2 3
(3)燃料电池电极反应式书写的常用方法
第一步,写出电池总反应式。
燃料电池的总反应与燃料燃烧的反应一致,若产物能和电解质反应,则总反应为加合后的反
应。
如甲烷燃料电池(电解质溶液为NaOH溶液)的反应如下:
CH+2O===CO+2HO ①
4 2 2 2
CO+2NaOH===NaCO+HO ②
2 2 3 2
①+②可得甲烷燃料电池的总反应式:CH+2O+2NaOH===NaCO+3HO。
4 2 2 3 2
第二步,写出电池的正极反应式。
根据燃料电池的特点,一般在正极上发生还原反应的物质都是 O ,因电解质溶液不同,故
2
其电极反应也会有所不同:
①酸性电解质:O+4H++4e-===2HO。
2 2
②碱性电解质:O+2HO+4e-===4OH-。
2 2
③固体电解质(高温下能传导O2-):O+4e-===2O2-。
2
④熔融碳酸盐(如熔融KCO):O+2CO+4e-===2CO。
2 3 2 2
第三步,电池的总反应式-电池的正极反应式=电池的负极反应式。
3.新型可逆电池
(1)铁镍电池(负极—Fe,正极—NiO,电解液—KOH溶液)
2
已知:Fe+NiO+2HOFe(OH) +Ni(OH) ,则
2 2 2 2放电:
负极:Fe-2e-+2OH-===Fe(OH) ;
2
正极:NiO+2HO+2e-===Ni(OH) +2OH-。
2 2 2
充电:
阴极:Fe(OH) +2e-===Fe+2OH-;
2
阳极:Ni(OH) -2e-+2OH-===NiO+2HO。
2 2 2
(2)LiFePO 电池(正极—LiFePO ,负极—Li,含Li+导电固体为电解质)
4 4
已知:FePO +LiLiFePO ,则
4 4
放电:
负极:Li-e-===Li+;
正极:FePO +Li++e-===LiFePO 。
4 4
充电:
阴极:Li++e-===Li;
阳极:LiFePO -e-===FePO +Li+。
4 4
(3)高铁电池(负极—Zn,正极—石墨,电解质为浸湿的固态碱性物质)
已知:3Zn+2KFeO+8HO3Zn(OH) +2Fe(OH) +4KOH,则
2 4 2 2 3
放电:
负极:3Zn-6e-+6OH-===3Zn(OH) ;
2
正极:2FeO+6e-+8HO===2Fe(OH) +10OH-。
2 3
充电:
阴极:3Zn(OH) +6e-===3Zn+6OH-;
2
阳极:2Fe(OH) -6e-+10OH-===2FeO+8HO。
3 2
题组一 新型燃料电池
1.以甲烷燃料电池为例,分析不同的环境下电极反应式的书写。
(1)酸性介质(如HSO )
2 4
总反应式:_______________________。
负极:___________________________。
正极:___________________________。
答案 CH+2O===CO+2HO
4 2 2 2
CH-8e-+2HO===CO+8H+
4 2 2
2O+8e-+8H+===4HO
2 2
(2)碱性介质(如KOH)
总反应式:__________________________________。
负极:______________________________________。
正极:______________________________________。答案 CH+2O+2OH-===CO+3HO
4 2 2
CH-8e-+10OH-===CO+7HO
4 2
2O+8e-+4HO===8OH-
2 2
(3)固体电解质(高温下能传导O2-)
总反应式:____________________________________。
负极:________________________________________。
正极:________________________________________。
答案 CH+2O===CO+2HO
4 2 2 2
CH-8e-+4O2-===CO+2HO
4 2 2
2O+8e-===4O2-
2
2.(1)肼分子(H N—NH)可以在氧气中燃烧生成氮气和水,利用肼、氧气与KOH溶液组成
2 2
碱性燃料电池,请写出该电池的负极、正极反应式:________________________________、
________________________________________________________________________。
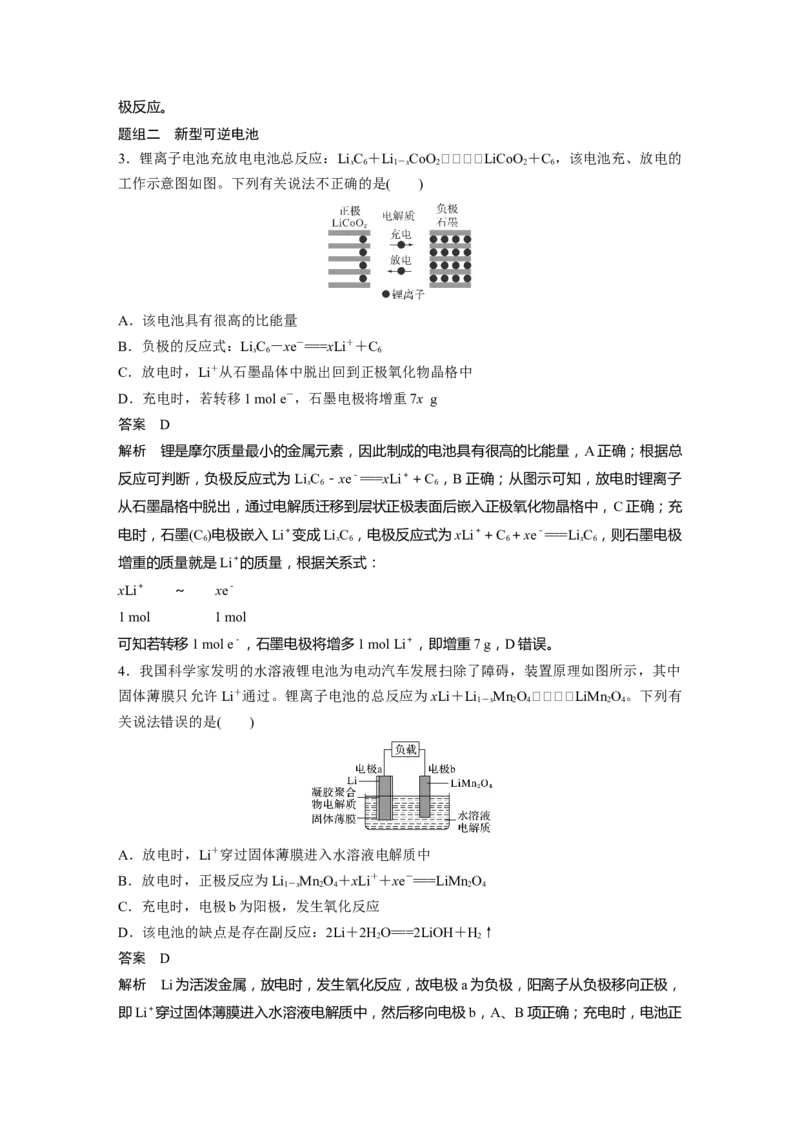
(2)化学家正在研究尿素动力燃料电池,用这种电池直接去除城市废水中的尿素,既能产生
净化的水,又能发电。尿素燃料电池结构如图所示,写出该电池的负极反应式:
______________
_______________________________________________________________________________
。
答案 (1)N H-4e-+4OH-===4HO+N O+4e-+2HO===4OH-
2 4 2 2 2 2
(2)CO(NH)+HO-6e-===CO+N+6H+
2 2 2 2 2
(1)新型燃料电池的分析模板
(2)解答燃料电池题目的几个关键点
①通入负极的物质为燃料,通入正极的物质为氧气。
②注意介质的成分,是电解质溶液还是熔融盐或氧化物。
③通过介质中离子的移动方向,可以判断电池的正负极,同时考虑该离子参与靠近一极的电极反应。
题组二 新型可逆电池
3.锂离子电池充放电电池总反应:LiC +Li CoOLiCoO +C ,该电池充、放电的
x 6 1-x 2 2 6
工作示意图如图。下列有关说法不正确的是( )
A.该电池具有很高的比能量
B.负极的反应式:LiC -xe-===xLi++C
x 6 6
C.放电时,Li+从石墨晶体中脱出回到正极氧化物晶格中
D.充电时,若转移1 mol e-,石墨电极将增重7x g
答案 D
解析 锂是摩尔质量最小的金属元素,因此制成的电池具有很高的比能量,A正确;根据总
反应可判断,负极反应式为LiC -xe-===xLi++C ,B正确;从图示可知,放电时锂离子
x 6 6
从石墨晶格中脱出,通过电解质迁移到层状正极表面后嵌入正极氧化物晶格中,C正确;充
电时,石墨(C )电极嵌入Li+变成LiC ,电极反应式为xLi++C +xe-===LiC ,则石墨电极
6 x 6 6 x 6
增重的质量就是Li+的质量,根据关系式:
xLi+ ~ xe-
1 mol 1 mol
可知若转移1 mol e-,石墨电极将增多1 mol Li+,即增重7 g,D错误。
4.我国科学家发明的水溶液锂电池为电动汽车发展扫除了障碍,装置原理如图所示,其中
固体薄膜只允许Li+通过。锂离子电池的总反应为xLi+Li MnOLiMn O 。下列有
1-x 2 4 2 4
关说法错误的是( )
A.放电时,Li+穿过固体薄膜进入水溶液电解质中
B.放电时,正极反应为Li MnO+xLi++xe-===LiMn O
1-x 2 4 2 4
C.充电时,电极b为阳极,发生氧化反应
D.该电池的缺点是存在副反应:2Li+2HO===2LiOH+H↑
2 2
答案 D
解析 Li为活泼金属,放电时,发生氧化反应,故电极a为负极,阳离子从负极移向正极,
即Li+穿过固体薄膜进入水溶液电解质中,然后移向电极b,A、B项正确;充电时,电池正极接电源正极,发生氧化反应,是阳极,C项正确;由于固体薄膜只允许Li+通过,水不能
与Li接触,故不存在Li与水的反应,D项错误。
锂离子电池充放电分析
常见的锂离子电极材料
正极材料:LiMO (M:Co、Ni、Mn等)
2
LiM O(M:Co、Ni、Mn等)
2 4
LiMPO(M:Fe等)
4
负极材料:石墨(能吸附锂原子)
负极反应:LiC -xe-===xLi++C ,
x n n
正极反应:Li MO +xLi++xe-===LiMO ,
1-x 2 2
总反应:Li MO +LiC C +LiMO
1-x 2 x n n 2
5.(2018·全国卷Ⅱ,12)我国科学家研发了一种室温下“可呼吸”的Na—CO 二次电池。将
2
NaClO 溶于有机溶剂作为电解液,钠和负载碳纳米管的镍网分别作为电极材料,电池的总
4
反应为3CO+4Na2NaCO+C。下列说法错误的是( )
2 2 3
A.放电时,ClO向负极移动
B.充电时释放CO,放电时吸收CO
2 2
C.放电时,正极反应为3CO+4e-===2CO+C
2
D.充电时,正极反应为Na++e-===Na
答案 D
解析 根据电池的总反应知,放电时,负极反应:
4Na-4e-===4Na+
正极反应:3CO+4e-===2CO+C
2
充电时,阴极反应:4Na++4e-===4Na
阳极反应:2CO+C-4e-===3CO
2
放电时,ClO向负极移动。根据充电和放电时的电极反应式知,充电时释放 CO ,放电时吸
2
收CO。
2
题组三 复杂电极反应式的书写方法
6.铁炭混合物(铁屑和活性炭的混合物)在水溶液中可形成许多微电池。将含有Cr O的酸性
2
废水通过铁炭混合物,在微电池正极上Cr O转化为Cr3+,其电极反应式为___________。
2答案 Cr O+14H++6e-===2Cr3++7HO
2 2
7.用零价铁(Fe)去除水体中的硝酸盐(NO)已成为环境修复研究的热点之一。
Fe还原水体中NO的反应原理如图所示。
(1)作负极的物质是________。
(2)正极的电极反应式是_______________________________________。
答案 (1)铁 (2)NO+8e-+10H+===NH+3HO
2
8.如图为钠高能电池的结构示意图,该电池的工作温度为320 ℃左右,电池的反应式为2Na
+xS===NaS ,正极的电极反应式为____________________________________________。
2 x
M(由NaO和Al O 制得)的两个作用是____________________________。
2 2 3
答案 xS+2e-===S(或2Na++xS+2e-===NaS) 导电和隔离钠与硫
2 x
根据题干信息找出放电粒子→正确判断产物→根据电子守恒配电子→根据电荷守恒配电荷
(注意电解质的环境,酸性溶液还是碱性溶液,还是非水体系)→根据质量守恒配原子。