文档内容
热点强化 3 信息型方程式的书写
突破信息型方程式的书写,只要抓住反应本质“得失电子守恒”,利用氧化还原反应配平的
方法和技巧,书写就会得心应手。
一般书写步骤:(1)根据题干信息或流程图,结合氧化还原反应中元素价态变化确定氧化剂、
还原剂及氧化产物、还原产物。(2)结合溶液的酸碱性,配平化学方程式或离子方程式。
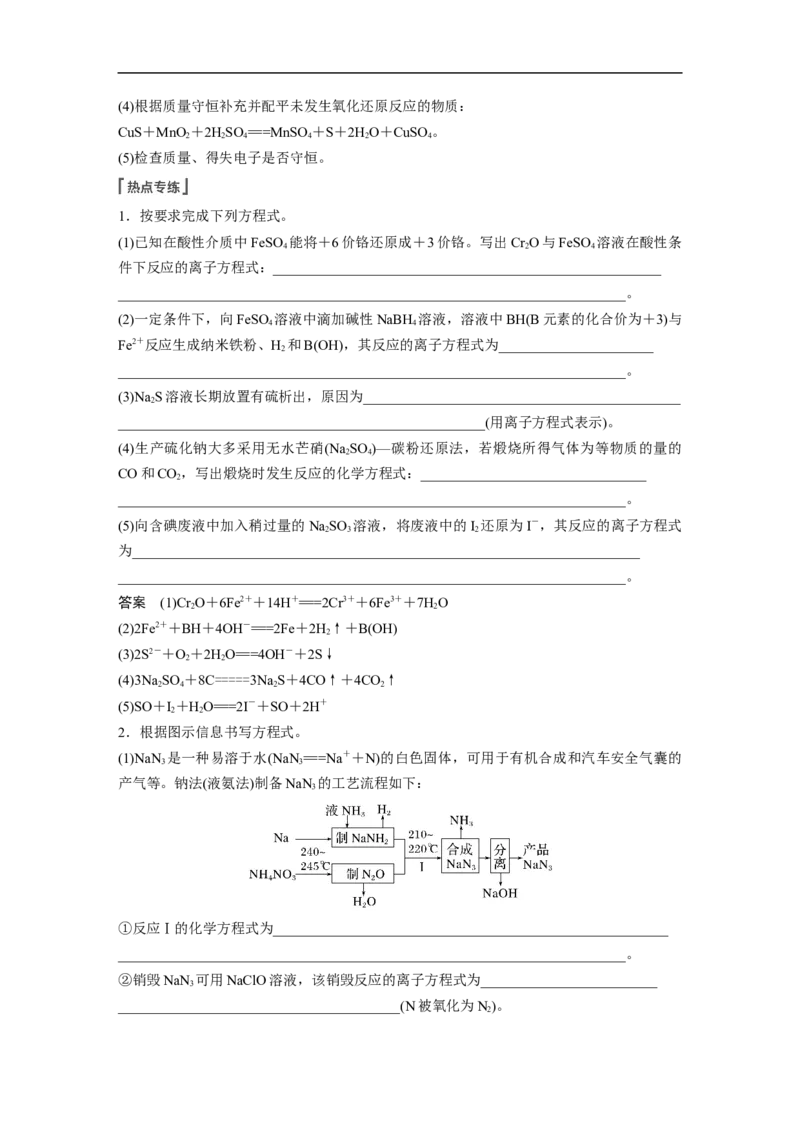
例1 [2020·全国卷Ⅲ,27(5)]硫酸镍在强碱溶液中用NaClO氧化,可沉淀出能用作镍镉电
池正极材料的NiOOH。写出该反应的离子方程式:
________________________________________________________________________。
分析 书写步骤:
例2 以低品位铜矿砂(主要成分为CuS)为原料制备氯化亚铜的路线如下:
写出酸溶1发生反应的化学方程式:____________________________________________
________________________________________________________________________。
分析 书写步骤:
(1)“瞻前”确定反应物
根据进料确定反应物:CuS+MnO +HSO 。
2 2 4
(2)“顾后”确定生成物
根据出料中含有S,后续除锰生成MnCO ,说明酸溶1生成的是S和MnSO 。
3 4
(3)根据得失电子守恒配平发生氧化还原反应的物质:
CuS+MnO +HSO ―→MnSO +S。
2 2 4 4(4)根据质量守恒补充并配平未发生氧化还原反应的物质:
CuS+MnO +2HSO ===MnSO +S+2HO+CuSO 。
2 2 4 4 2 4
(5)检查质量、得失电子是否守恒。
1.按要求完成下列方程式。
(1)已知在酸性介质中FeSO 能将+6价铬还原成+3价铬。写出Cr O与FeSO 溶液在酸性条
4 2 4
件下反应的离子方程式:_______________________________________________________
________________________________________________________________________。
(2)一定条件下,向FeSO 溶液中滴加碱性NaBH 溶液,溶液中BH(B元素的化合价为+3)与
4 4
Fe2+反应生成纳米铁粉、H 和B(OH),其反应的离子方程式为______________________
2
________________________________________________________________________。
(3)Na S溶液长期放置有硫析出,原因为_____________________________________________
2
____________________________________________________(用离子方程式表示)。
(4)生产硫化钠大多采用无水芒硝(Na SO )—碳粉还原法,若煅烧所得气体为等物质的量的
2 4
CO和CO,写出煅烧时发生反应的化学方程式:________________________________
2
________________________________________________________________________。
(5)向含碘废液中加入稍过量的NaSO 溶液,将废液中的I 还原为I-,其反应的离子方程式
2 3 2
为________________________________________________________________________
________________________________________________________________________。
答案 (1)Cr O+6Fe2++14H+===2Cr3++6Fe3++7HO
2 2
(2)2Fe2++BH+4OH-===2Fe+2H↑+B(OH)
2
(3)2S2-+O+2HO===4OH-+2S↓
2 2
(4)3Na SO +8C=====3NaS+4CO↑+4CO↑
2 4 2 2
(5)SO+I+HO===2I-+SO+2H+
2 2
2.根据图示信息书写方程式。
(1)NaN 是一种易溶于水(NaN ===Na++N)的白色固体,可用于有机合成和汽车安全气囊的
3 3
产气等。钠法(液氨法)制备NaN 的工艺流程如下:
3
①反应Ⅰ的化学方程式为________________________________________________________
________________________________________________________________________。
②销毁NaN 可用NaClO溶液,该销毁反应的离子方程式为_________________________
3
________________________________________(N被氧化为N)。
2(2)利用钴渣[含Co(OH) 、Fe(OH) 等]制备钴氧化物的工艺流程如下:
3 3
Co(OH) 溶解还原反应的离子方程式为_________________________________________
3
________________________________________________________________________。
答案 (1)①2NaNH +NO========NaN +NH +NaOH
2 2 3 3
②ClO-+2N+HO===Cl-+2OH-+3N↑
2 2
(2)2Co(OH) +SO+4H+===2Co2++SO+5HO
3 2
3.[2020·全国卷Ⅰ,26(2)]钒具有广泛用途。黏土钒矿中,钒以+3、+4、+5价的化合物
存在,还包括钾、镁的铝硅酸盐,以及 SiO 、Fe O 。采用以下工艺流程可由黏土钒矿制备
2 3 4
NH VO 。
4 3
“酸浸氧化”中,VO+和VO2+被氧化成VO,同时还有________被氧化。写出VO+转化为
VO反应的离子方程式:__________________________________________________________。
答案 Fe2+ VO++MnO +2H+===VO+Mn2++HO
2 2
解析 Fe O 与稀硫酸反应:Fe O+8H+===2Fe3++Fe2++4HO,“酸浸氧化”过程中,
3 4 3 4 2
Fe2+具有还原性,也能被MnO 氧化生成Fe3+。VO+被氧化为VO,MnO 则被还原为Mn2
2 2
+,溶液呈酸性,结合守恒规律,写出离子方程式:VO++MnO +2H+===VO+Mn2++
2
HO。
2
4.[2019·全国卷Ⅱ,26(2)①]立德粉ZnS·BaSO(也称锌钡白),是一种常用白色颜料。以重
4
晶石(BaSO)为原料,可按如下工艺生产立德粉:
4
在回转炉中重晶石被过量焦炭还原为可溶性硫化钡,该过程的化学方程式为
________________________________________________________________________
________________________________________________________________________。
回转炉尾气中含有有毒气体,生产上可通过水蒸气变换反应将其转化为CO 和一种清洁能源
2气体,该反应的化学方程式为____________________________________________________
________________________________________________________________________。
答案 BaSO+4C========BaS+4CO↑ CO+HO(g)=====CO+H
4 2 2 2
解析 由流程图中经浸出槽后得到净化的BaS溶液以及回转炉尾气中含有有毒气体可知,
在回转炉中BaSO 与过量的焦炭粉反应生成可溶性的BaS和CO;生产上可通过水蒸气变换
4
反应除去回转炉中的有毒气体CO,即CO与HO反应生成CO 和H。
2 2 2
5.[2020·全国卷Ⅱ,26(3)(4)]化学工业为疫情防控提供了强有力的物质支撑。氯的许多化合
物既是重要化工原料,又是高效、广谱的灭菌消毒剂。回答下列问题:
(3)Cl O为淡棕黄色气体,是次氯酸的酸酐,可由新制的 HgO和Cl 反应来制备,该反应为
2 2
歧化反应(氧化剂和还原剂为同一种物质的反应)。上述制备 ClO 的化学方程式为
2
________________________________________________________________________
________________________________________________________________________。
(4)ClO 常温下为黄色气体,易溶于水,其水溶液是一种广谱杀菌剂。一种有效成分为
2
NaClO 、NaHSO 、NaHCO 的“二氧化氯泡腾片”,能快速溶于水,溢出大量气泡,得到
2 4 3
ClO 溶液。上述过程中,生成ClO 的反应属于歧化反应,每生成1 mol ClO 消耗NaClO 的
2 2 2 2
量 为 ________mol ; 产 生 “ 气 泡 ” 的 化 学 方 程 式 为
_____________________________________
________________________________________________________________________。
答案 (3)2Cl +HgO===HgCl +ClO
2 2 2
(4)1.25 NaHCO +NaHSO===CO↑+NaSO +HO
3 4 2 2 4 2
解析 (3)由新制的HgO和Cl 反应制备ClO,由于该反应为歧化反应,所以只有氯元素的
2 2
化合价发生变化,由 0 价变为+1 价和-1 价,所以反应的化学方程式为 2Cl +
2
HgO===HgCl +ClO。(4)由题意知,在NaClO 生成ClO 的过程中,发生歧化反应,NaClO
2 2 2 2 2
既是氧化剂,又是还原剂,4NaClO――→4ClO,NaClO――→NaCl,每生成4 mol ClO,
2 2 2 2
需消耗5 mol NaClO ,所以每生成1 mol ClO ,需消耗 mol(即1.25 mol) NaClO 。产生的气
2 2 2
泡的成分为CO,反应的化学方程式为NaHCO +NaHSO===CO↑+NaSO +HO。
2 3 4 2 2 4 2