文档内容
2024届高考化学一轮复习限时训练:《化学物质及其变化》专题16
1.下列过程中的化学反应,相应的离子方程式正确的是
A. 向碳酸钠溶液中加入过量醋酸:CO2-+2H+=H O+CO↑
3 2 2
B. 稀硝酸和过量的铁屑反应:Fe+4H++NO- =Fe3++NO↑+2HO
3 2
C. 向次氯酸钙溶液中通入少量二氧化碳气体:ClO-+CO +H O=HClO+HCO -
2 2 3
D. 向0.1mol·L-1氯化铝溶液中加入过量浓氨水:Al3++3NH·H O=A1(OH) ↓+3NH+
3 2 3 4
2.宏观辨识与微观探析是化学学科核心素养之一。下列物质的性质实验对应的反应方程式书
写正确的是
A.硫酸亚铁溶液滴入酸性高锰酸钾溶液中:5Fe2++MnO 8H+=Mn2++5Fe3++4HO
+ 2
B.足量NH 通入氯化铝溶液中:Al3++4NH +2HO=AlO+4NH
3 3 2
C.足量氯气通入碳酸钠溶液中:Cl+CO Cl-+ClO-+CO
2 = 2
D.SO 通入HS溶液中:4H++2S2-+SO =3S↓+2HO
2 2 2 2
3.大庆市某中学化学实验小组在实验室鉴定某无色溶液。已知溶液中的溶质仅由NH、K+、
Ag+、Ca2+、Al3+、AlO、MnO CO SO中的若干种组成。取该溶液进行如下实验:
、 、
(1)取适量溶液,加入过量盐酸,有气体生成,并得到无色溶液
(2)在(1)所得溶液中加入过量NH HCO 溶液,有气体生成,同时产生白色沉淀甲;
4 3
(3)在(2)所得溶液中加入过量Ba(OH) 溶液并加热也有气体生成,同时产生白色沉淀乙
2
则下列离子在原溶液中一定存在的有
A.K+、CO AlO B.SO、AlO、K+、CO
、
C.CO K+、Al3+、NH D.MnO K+、CO NH
、 、 、
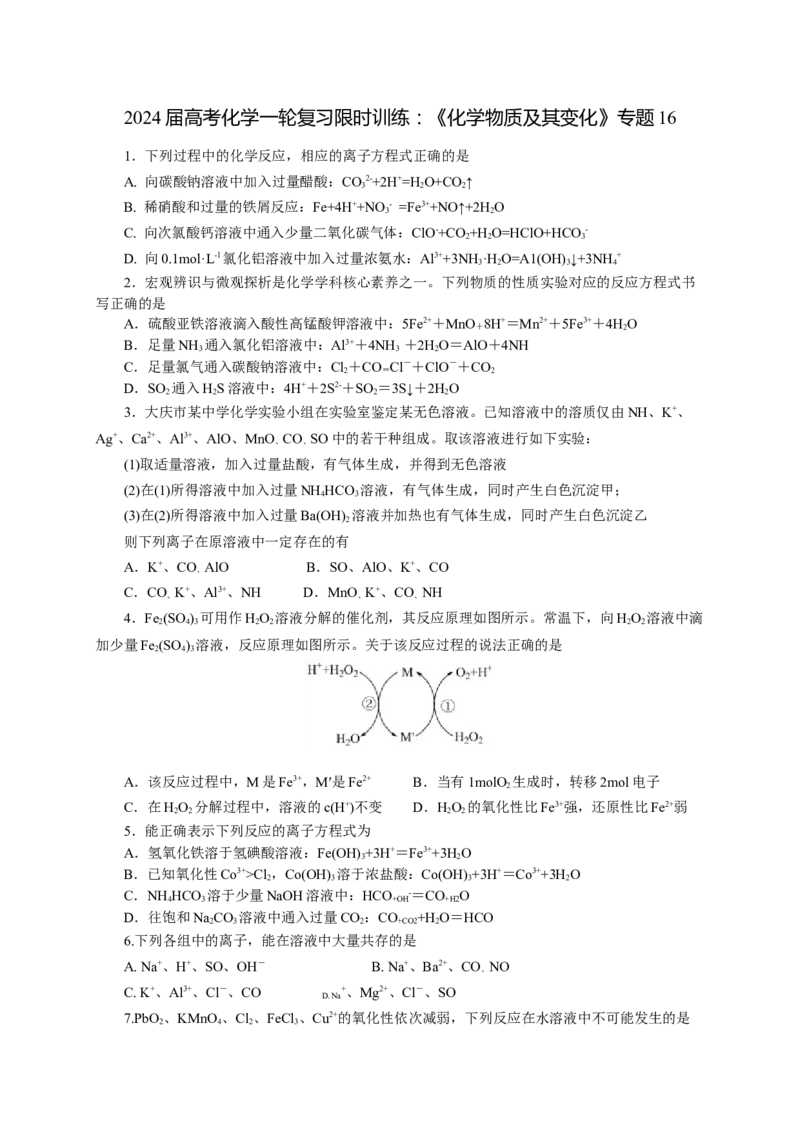
4.Fe (SO ) 可用作HO 溶液分解的催化剂,其反应原理如图所示。常温下,向HO 溶液中滴
2 4 3 2 2 2 2
加少量Fe (SO ) 溶液,反应原理如图所示。关于该反应过程的说法正确的是
2 4 3
A.该反应过程中,M是Fe3+,M′是Fe2+ B.当有1molO 生成时,转移2mol电子
2
C.在HO 分解过程中,溶液的c(H+)不变 D.HO 的氧化性比Fe3+强,还原性比Fe2+弱
2 2 2 2
5.能正确表示下列反应的离子方程式为
A.氢氧化铁溶于氢碘酸溶液:Fe(OH) +3H+=Fe3++3H O
3 2
B.已知氧化性Co3+>Cl,Co(OH) 溶于浓盐酸:Co(OH) +3H+=Co3++3H O
2 3 3 2
C.NH HCO 溶于少量NaOH溶液中:HCO -=CO O
4 3 +OH +H2
D.往饱和NaCO 溶液中通入过量CO:CO +H O=HCO
2 3 2 +CO2 2
6.下列各组中的离子,能在溶液中大量共存的是
A. Na+、H+、SO、OH- B. Na+、Ba2+、CO NO
、
C. K+、Al3+、Cl-、CO +、Mg2+、Cl-、SO
D. Na
7.PbO、KMnO 、Cl、FeCl 、Cu2+的氧化性依次减弱,下列反应在水溶液中不可能发生的是
2 4 2 3A.2Fe2++Cl=2Fe3++2Cl-
2
B.10Cl-+2MnO 16H+=2Mn2++5Cl↑+8HO
+ 2 2
C.5Pb2++2MnO 2HO=5PbO +2Mn2++4H+
+ 2 2
D. Cu+2Fe3+=Cu2++2Fe2+
8.下列对有关物质的分类不正确的是
选项 物质 分类 不同类物质
A 白磷、啤酒、漂白粉、豆腐 混合物 白磷
B 铝、铁、锌、氟气 还原剂 铁
C HgO、NaOH、KCl、金刚石 化合物 金刚石
D CaO、HO、CO、NaSO 氧化物 NaSO
2 2 2 3 2 3
9.下列反应的离子方程式书写正确的是
A.NH HCO 溶液与足量NaOH溶液混合:OH-+NH=HO+NH ↑
4 3 2 3
B. 用Fe电极电解KCl溶液:2Cl-+2HO=====H↑+Cl↑+2OH-
2 2 2
C. 用NaOH溶液加热除去试管内附着的硫粉:4OH-+2S===S2-+SO 2HO
+ 2
D.AgCl悬浊液中加入NaS溶液:2AgCl(s)+S2-(aq) Ag S(s)+2Cl-(aq)
2 2
10.常温下,下列各组离子在指定溶液中一定能大量共存的是
A. 小苏打溶液中:Ba2+、Cl-、K+、OH-
B. 通入SO 的溶液中:Cu2+、Al3+、Fe3+、Cl-
2
C. 无色透明的溶液中:SO、Na+、K+、I-
D. 由水电离的c(H+)=1×10-13mol·L-1的溶液中:K+、Na+、[Al(OH) ]-、CO
4
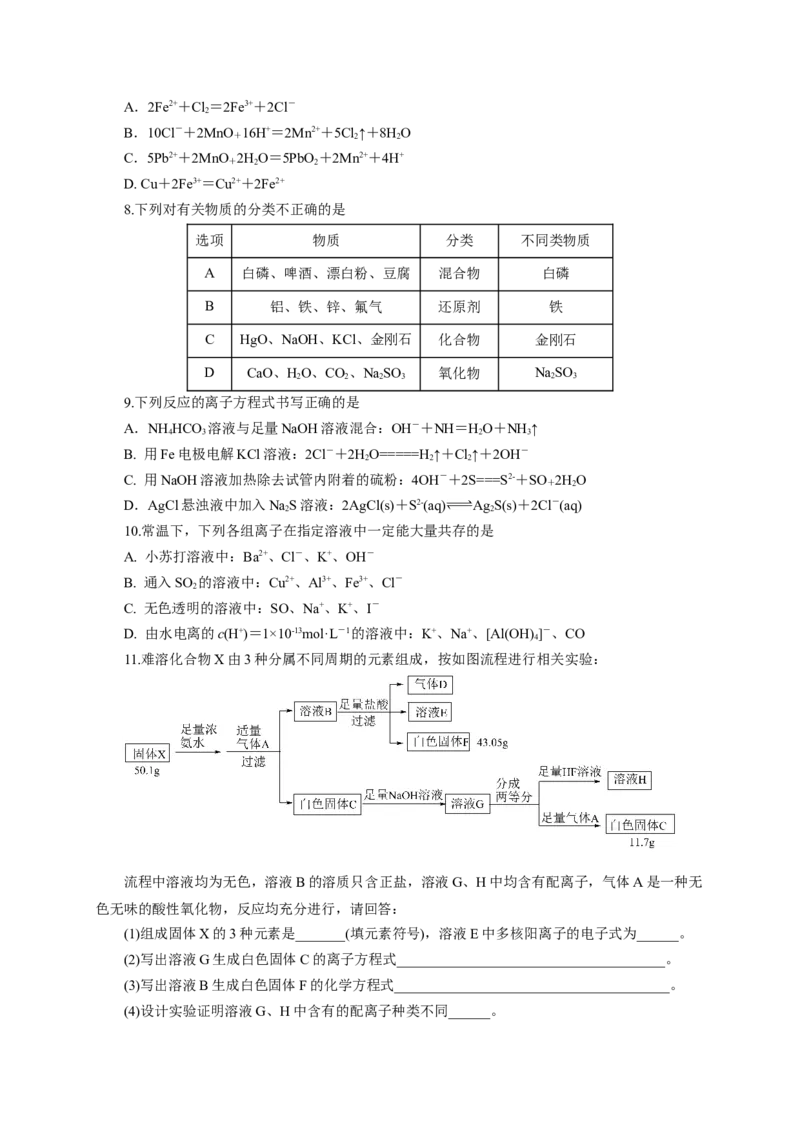
11.难溶化合物X由3种分属不同周期的元素组成,按如图流程进行相关实验:
流程中溶液均为无色,溶液B的溶质只含正盐,溶液G、H中均含有配离子,气体A是一种无
色无味的酸性氧化物,反应均充分进行,请回答:
(1)组成固体X的3种元素是_______(填元素符号),溶液E中多核阳离子的电子式为______。
(2)写出溶液G生成白色固体C的离子方程式______________________________________。
(3)写出溶液B生成白色固体F的化学方程式_______________________________________。
(4)设计实验证明溶液G、H中含有的配离子种类不同______。12.化合物X由三种元素组成,某学习小组按如下流程进行实验:
已知:黄褐色固体A的式量小于100,溶液C是单一溶质盐溶液。
(1)X的组成元素是___________,X的化学式是___________。
(2)写出B溶液与Ba(OH) 溶液恰好完全沉淀时的离子反应方程式:_______________________。
2
(3)固体A是一种良好的脱硫剂,请写出常温下固体A在HCl氛围中与HS反应的化学反应方
2
程式:_______________________________________。
(4)设计实验检验溶液B中的阳离子:___________。