文档内容
备战2024年高考化学考前手感保温训练(新高考卷)
专练03 14道选择题+主观原理题
完卷时间:40分钟
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Na-23 Ni-59 La-139
题号 1 2 3 4 5 6 7 8 9 10 11 12 13 14
答案 C A A A D B C D B D A C B A
一、选择题(只有1个正确选项)
1.中国工笔画是我国传统美术的艺术珍品,在其创作过程中要使用笔、墨、纸绢、颜料、
胶矾水等。胶矾水主要成分是明胶和明矾,用于“生宣熟化”和“三矾九染”。下列说法
错误的是
A.“生宣熟化”工艺中明矾水解得到的 胶体可促进明胶的凝聚
B.纸、绢的主要成分分别是纤维素和蛋白质,均属于天然高分子化合物
C.绘制工笔画使用的矿物颜料石青[主要成分为 ]耐酸碱腐蚀
D.绘制工笔画使用的油烟墨的主要成分炭黑具有很强的稳定性,利于绘画保存
【答案】C
【解析】A.“生宣熟化”工艺中明矾水解得到的 胶体可促进明胶的凝聚,A正确;
B.绢指丝织品,主要成分为蛋白质,纸的主要成分都是纤维素,蛋白质和纤维素属于天然
高分子,B正确;C.矿物颜料石青 能和酸反应,易被酸腐蚀,C错误;
D.油烟墨的主要成分炭黑,炭黑具有很强的稳定性,利于绘画保存,D正确;故答案选
C。
2.下列化学用语或表述正确的是
A.Ag位于元素周期表ds区
B. 的球棍模型为
C.基态Cr原子的价电子轨道表示式:D.用电子式表示 的形成过程:
【答案】A
【解析】A.银是47号元素,基态价电子排布式为: 4d105s1,位于第五周期ⅠB,则Ag位
于元素周期表ds区,A正确;B.球棍模型中,用大小不同的小球和短棍分别表示原子、
共价键,同时要体现分子的空间构型, 为四面体结构,但原子半径Cl>C>H,则
不能表示 的球棍模型,B错误;C.铬是24号元素,基态价电子排布式为:
3d54s1,基态Cr原子的价电子轨道表示式: ,C错误;D. 氯
化镁为离子化合物,用电子式表示 的形成过程:
,D错误;答案选A。
3.工业制备硝酸的重要反应之一为: 。设 为阿伏加德罗
常数的值,下列说法正确的是
A. 水中 键数目为
B. 中质子数目为
C. 氨水中,含有的 数为
D.每生成 转移电子数目为
【答案】A
【解析】A.18g水物质的量为1mol,1个水分子中有两根σ键,18g水中有2mol σ键,
数目为2N,故A正确;B.O原子中有8个质子,8个中子,则1molO 含2mol氧原子,质
A 2
子数目为16N
A
,故B错误;C.氨水为弱碱,只有小部分发生电离,1L1mol⋅L−1氨水中,含
有的铵根数目小于N,故C错误;D. 由反应可得,每生成4molNO转移20mol电子,
A
30gNO为1mol,则生成1molNO转移5mol电子,故D错误。本题选A。
4.下列解释事实的离子方程式正确的是
A.室温下pH=2的盐酸中水电离出的c(H+)=10-12mol·L-1B.0.1mol·L-1KI溶液中以下离子能大量共存:Na+、K+、ClO-、OH-
C.室温下用稀HNO 溶解铜:Cu+2NO +2H+=Cu2++2NO↑+HO
3 2 2
D.用醋酸和淀粉-KI溶液检验加碘食盐中所含的IO :
【答案】A
【解析】A.室温下pH=2的盐酸中水电离出的 ,A正确;
B.KI中碘离子具有还原性,ClO-具有氧化性,两者因发生氧化还原反应而不能大量共存,
B错误;C.稀HNO 溶解铜生成还原产物为NO,且选项的离子方程式电荷也不守恒,C错误;
3
D.醋酸是弱酸,属于弱电解质,不能将其拆开,D错误;故选A。
5.逆水煤气变换反应是一种 转化和利用的重要途径,发生的反应有
反应Ⅰ: kJ·mol
反应Ⅱ: kJ⋅mol
反应Ⅲ:
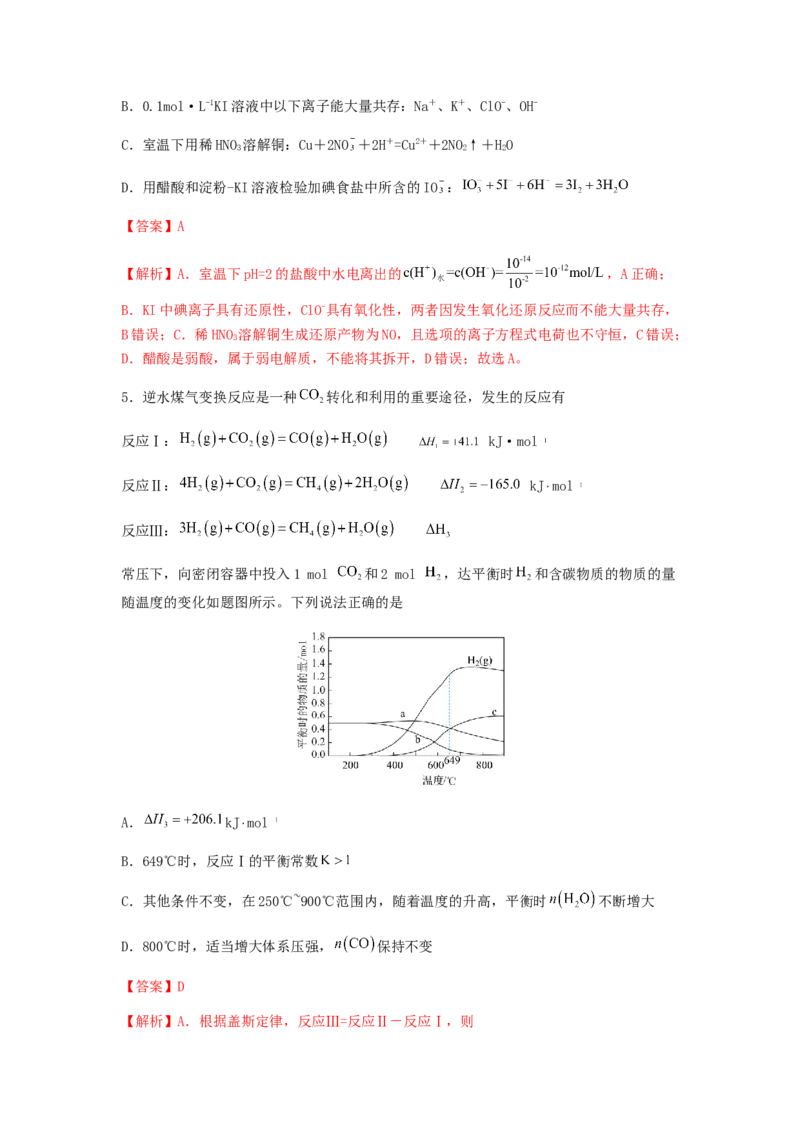
常压下,向密闭容器中投入1 mol 和2 mol ,达平衡时 和含碳物质的物质的量
随温度的变化如题图所示。下列说法正确的是
A. kJ⋅mol
B.649℃时,反应Ⅰ的平衡常数
C.其他条件不变,在250℃~900℃范围内,随着温度的升高,平衡时 不断增大
D.800℃时,适当增大体系压强, 保持不变
【答案】D
【解析】A.根据盖斯定律,反应Ⅲ=反应Ⅱ-反应Ⅰ,则,A错误;B.649℃时,反应平衡时 ,
, ,平衡常数:
,B错误;C.由图像可知,250℃~649℃范围内,随着温度的升高,平
衡时 增大,平衡逆向移动,则平衡时 不断减小;649℃~900℃范围内,随着
温度的升高,平衡时 减小,平衡正向移动,则平衡时 不断增大,C错误;
D.高温时反应I进行程度很大,反应II、III程度很小,CH 含量很少,平衡不受压强影
4
响,适当增大体系压强, 保持不变,D正确;答案选D。
6.有机物Z是化妆品成分之一,其合成路线如图。下列有关叙述正确的是
A.X和Y都属于芳香烃 B.M分子中所有的碳原子可能共面
C.X最多能与 氢气发生加成反应 D.Z的分子中含有13个碳原子
【答案】B
【解析】A.由结构简式可知,Y中有氧元素,不属于芳香烃,故A错误;B.M中含有苯环,
苯环的所有碳原子共面,另外两个碳原子可以通过碳碳单键旋转至和苯环共面,故B正确;
C.没有指明X的物质的量,无法计算与其加成的氢气的物质的量,故C错误;D.Z的分子
中含有14个碳原子,故D错误;故选B。
7.下列实验设计方案和操作正确的是C.析出
A.验证铁电极是否受到 B.分离苯酚和水 D.测定KI溶
保护 的混合物 液的浓度
晶体
A.A B.B C.C D.D
【答案】C
【解析】A.在酸化的氯化钠溶液中,可能会有少量铁与氢离子反应生成亚铁离子,所以不
能用此装置来验证铁电极是否受到保护,故A错误;B.苯酚和水形成的是乳浊液,不能用
过滤的方法分离,故B错误;C. 在乙醇中的溶解度比在水中的要小,
因此向其中加入乙醇,将析出深蓝色晶体 ,故C正确;D.溴水具有
氧化性,能腐蚀橡胶,不能用碱式滴定管盛装,应用酸式滴定管盛装,故D错误;故答案
为:C。
8.一种由短周期元素构成的洗涤剂中间体结构式如图所示,X、Q、Z、Y 、W原子序数依
次增大,X和W同主族,Q、Z、Y同周期,Q原子核外成对电子对数与未成对电子数相等,Y
可与X形成空间构型为角形的分子,下列说法正确的是
A.第一电离能:Y>Z>Q
B.简单离子半径:W>Y>Z
C.Z元素的氧化物对应水化物为强酸
D.Y的简单氢化物的中心原子的VSEPR构型为正四面体
【答案】D
【分析】由该结构图可知,X原子只形成一个键,W原子带一个正电荷,且X与W同族,则
X、W分别为H元素和Na元素;Q原子核外成对电子数与未成对电子数相等,且形成了四个
键,则Q是C元素;Z元素形成了三个键,且与碳元素同周期,原子序数比碳元素大,则Z
元素为N;Y与X形成会形成空间结构为角形的分子,且Q分别与碳元素形成了一个双键和
一个单键,则可得出Y为O元素,故X、Q、Z、Y、W分别是H、C、N、O、Na元素。
【解析】A.同周期第一电离能从左往右呈增大的趋势,但由于氮元素最外层的2p轨道为
半满,更不易失去电子,所以氮的第一电离能比相邻两元素的第一电离能大,原子半径越小的,第一电离能越大,即第一电离能:Z>Y>Q,故A错误;B.W、Y、Z为Na、O、N,这
三种元素对应的简单离子的电子层结构相同,则核电荷数越大,离子半径越小,则简单离
子半径:Z>Y>Q,故B错误;C.Z元素的氧化物NO 对应的水化物为亚硝酸,为弱酸,故C
2 3
错误;D.Y的简单氢化物为HO,其中心原子氧的杂化类型为sp3,对应的VSEPR模型为正
2
四面体,故D正确;故答案为:D。
9.氧泡泡是一种多功能新型漂白剂,其有效成分是过碳酸钠(xNaCO•yHO)。
2 3 2 2
Ⅰ.以芒硝(NaSO•10HO)、HO 等为原料制备过碳酸钠的工艺流程如图:
2 4 2 2 2
Ⅱ.测定过碳酸钠化学式的实验步骤如下(样品中杂质不参加反应):
①用电子天平称取两份质量均为mg的样品。
②将一份置于锥形瓶中,加水溶解,加催化剂使HO 充分快速分解(催化剂不参与其它反
2 2
应),然后加酚酞作指示剂,用0.0500mol•L-1HSO 溶液滴定至终点,消耗硫酸VmL。
2 4 1
③将另一份置于碘量瓶中,加入50mL蒸馏水,并立即加入6mL2.0mol•L-1HPO 溶液,再加
3 4
入过量KI固体,摇匀后于暗处放置10min,加入适量指示剂,用0.1000mol•L-1NaSO 标准
2 2 3
溶液滴定至终点,消耗NaSO 标准溶液VmL。(已知:2NaSO+I=NaSO+2NaI)
2 2 3 2 2 2 3 2 2 4 6
测定过碳酸钠化学式的步骤中,下列说法错误的是
A.步骤③样品溶于水酸化后放置一段时间,然后再加入过量KI固体,导致x:y偏大
B.该过碳酸钠样品中x:y=V:V
1 2
C.该样品的纯度为 %
D.步骤②中滴定前滴定管尖嘴处有气泡,滴定后无气泡,导致x:y偏大
【答案】B
【分析】芒硝、氧化钙、NaCrO 反应生成NaCrO 和硫酸钙沉淀,过滤滤液加入足量二氧
2 2 7 2 4
化碳,NaCrO 转化为溶解度较小的碳酸氢钠晶体和NaCrO,过滤分离出晶体煅烧精制得
2 4 2 2 7
到碳酸钠,加入稳定剂、过氧化氢在乙醇条件下抽滤、干燥得到过碳酸钠;
滴定实验的步骤是:滴定前的准备:滴定管:查漏→洗涤→润洗→装液→调液面→记录,
锥形瓶:注液体→记体积→加指示剂;滴定:眼睛注视锥形瓶溶液颜色变化;终点判断:记录数据;数据处理:通过数据进行计算;
【解析】A.步骤③样品溶于水酸化后放置一段时间,会导致过氧化氢分解,使得加入过量
KI固体后生成碘单质量减小,使得滴定过程中V 偏小,计算出y值偏小,导致x:y偏大,
2
A正确;B.②加酚酞作指示剂,酚酞变色范围为碱性,则滴定终点碳酸根离子转化为碳酸
氢根离子,则根据硫酸用量可知,碳酸钠为0.0500mol•L-1×V×10-3L×2;③中过氧化氢
1
将碘离子氧化为碘单质,碘单质被NaSO 标准溶液滴定,由电子守恒可知:
2 2 3
,可知过氧化氢为 ;故过碳酸钠样品中
,B错误;C.结合
B分析可知,该样品的纯度为
=
%,C正确;D.步骤②中滴定前滴定管尖嘴处有气泡,滴定后无气泡,使得
V 偏大,则导致x:y偏大,D正确;故选B。
1
10.物质的结构决定其性质。下列实例与解释不相符的是
选项 事实 解释
金属晶体中的自由电子在外电场作用下发生定向移
A 金属是电的良导体
动
NF 不易与Cu2+形成配位 F的电负性大,导致N原子核对其孤电子对的吸引力
3
B
键 大
C CO的沸点高于N CO的极性大于N
2 2
S的原子半径较大,其价层σ键电子对之间的斥力
D 中的键角小于
较小
A.A B.B C.C D.D
【答案】D
【解析】A.金属晶体中的自由电子在外电场作用下发生定向移动,形成电流,实例与解释
相符,故A不符合题意;B.F的电负性大,导致N原子核对其孤电子对的吸引力大,不容
易提供孤电子对,不易与Cu2+形成配位键,实例与解释相符,故B不符合题意;C.CO的沸
点高于N 均为分子晶体,相对分子质量相同,但是CO的极性大于N,导致CO沸点较高,
2 2实例与解释相符,故C不符合题意;D. 中S为sp3杂化存在1对孤电子对,而 中
碳为sp2杂化,故 中的键角小于 ,实例与解释不相符,故D符合题意;故选D。
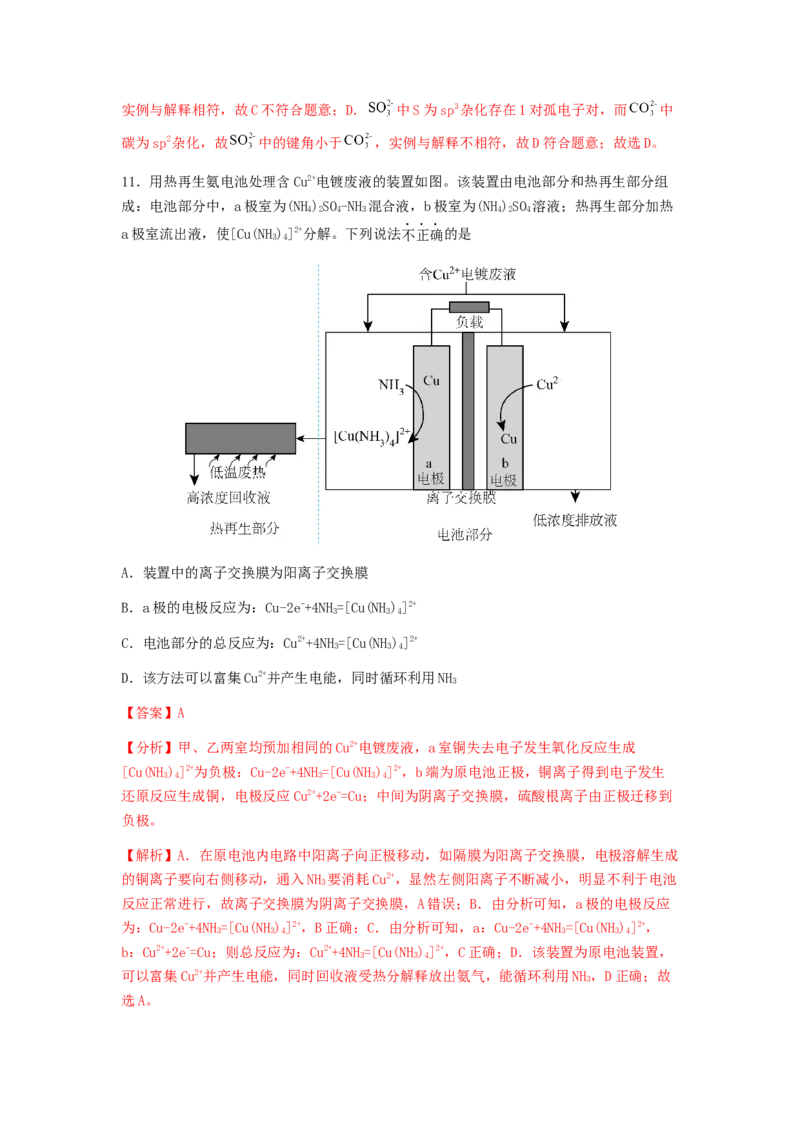
11.用热再生氨电池处理含Cu2+电镀废液的装置如图。该装置由电池部分和热再生部分组
成:电池部分中,a极室为(NH)SO-NH 混合液,b极室为(NH)SO 溶液;热再生部分加热
4 2 4 3 4 2 4
a极室流出液,使[Cu(NH)]2+分解。下列说法不正确的是
3 4
A.装置中的离子交换膜为阳离子交换膜
B.a极的电极反应为:Cu-2e-+4NH=[Cu(NH)]2+
3 3 4
C.电池部分的总反应为:Cu2++4NH=[Cu(NH)]2+
3 3 4
D.该方法可以富集Cu2+并产生电能,同时循环利用NH
3
【答案】A
【分析】甲、乙两室均预加相同的Cu2+电镀废液,a室铜失去电子发生氧化反应生成
[Cu(NH)]2+为负极:Cu-2e-+4NH=[Cu(NH)]2+,b端为原电池正极,铜离子得到电子发生
3 4 3 3 4
还原反应生成铜,电极反应Cu2++2e-=Cu;中间为阴离子交换膜,硫酸根离子由正极迁移到
负极。
【解析】A.在原电池内电路中阳离子向正极移动,如隔膜为阳离子交换膜,电极溶解生成
的铜离子要向右侧移动,通入NH 要消耗Cu2+,显然左侧阳离子不断减小,明显不利于电池
3
反应正常进行,故离子交换膜为阴离子交换膜,A错误;B.由分析可知,a极的电极反应
为:Cu-2e-+4NH=[Cu(NH)]2+,B正确;C.由分析可知,a:Cu-2e-+4NH=[Cu(NH)]2+,
3 3 4 3 3 4
b:Cu2++2e-=Cu;则总反应为:Cu2++4NH=[Cu(NH)]2+,C正确;D.该装置为原电池装置,
3 3 4
可以富集Cu2+并产生电能,同时回收液受热分解释放出氨气,能循环利用NH,D正确;故
3
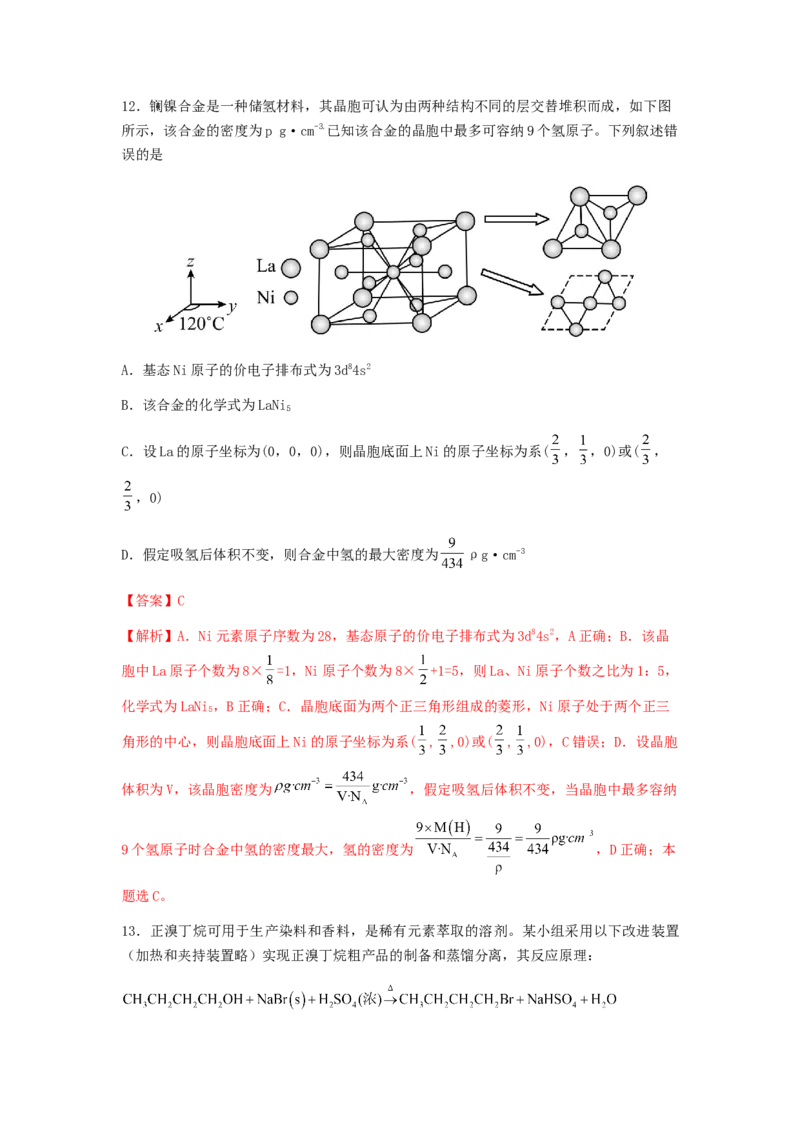
选A。12.镧镍合金是一种储氢材料,其晶胞可认为由两种结构不同的层交替堆积而成,如下图
所示,该合金的密度为p g·cm-3.已知该合金的晶胞中最多可容纳9个氢原子。下列叙述错
误的是
A.基态Ni原子的价电子排布式为3d84s2
B.该合金的化学式为LaNi
5
C.设La的原子坐标为(0,0,0),则晶胞底面上Ni的原子坐标为系( , ,0)或( ,
,0)
D.假定吸氢后体积不变,则合金中氢的最大密度为 ρg·cm-3
【答案】C
【解析】A.Ni元素原子序数为28,基态原子的价电子排布式为3d84s2,A正确;B.该晶
胞中La原子个数为8× =1,Ni原子个数为8× +1=5,则La、Ni原子个数之比为1:5,
化学式为LaNi,B正确;C.晶胞底面为两个正三角形组成的菱形,Ni原子处于两个正三
5
角形的中心,则晶胞底面上Ni的原子坐标为系( , ,0)或( , ,0),C错误;D.设晶胞
体积为V,该晶胞密度为 ,假定吸氢后体积不变,当晶胞中最多容纳
9个氢原子时合金中氢的密度最大,氢的密度为 ,D正确;本
题选C。
13.正溴丁烷可用于生产染料和香料,是稀有元素萃取的溶剂。某小组采用以下改进装置
(加热和夹持装置略)实现正溴丁烷粗产品的制备和蒸馏分离,其反应原理:下列有关说法错误的是
A.烧杯中NaOH溶液可以吸收挥发出的溴单质和溴化氢
B.恒压滴液漏斗可以用于接收蒸馏出的粗产品
C.反应开始时应先加热三颈烧瓶一段时间,再滴入浓硫酸
D.粗产品可经水洗、NaOH溶液洗涤、水洗、干燥等步骤进一步提纯
【答案】B
【解析】A.NaOH溶液具有碱性,可以与酸性的溴化氢发生中和反应,生成盐和水。同时,
溴单质也可以与NaOH溶液反应,生成相应的溴化物和次溴酸盐,故烧杯中NaOH溶液可以
吸收挥发出的溴单质和溴化氢,A正确;B.恒压滴液漏斗主要用于向反应容器中滴加液体
其特点是可以使滴加的液体与反应容器内的气体压强相等,从而使液体能够顺利滴下。然
而,恒压滴液漏斗并不适合用于接收蒸馏出的粗产品,粗产品在三颈烧瓶中,B错误;C.
加热三颈烧瓶的目的是为了预热反应体系,使其达到一个较为均匀的温度状态。这有助于
后续反应的平稳进行,避免由于温度突然升高而导致的副反应或实验事故。如果先加入浓
硫酸再进行加热,可能会因为局部温度过高而导致浓硫酸飞溅或引发其他不安全因素,故
C正确;D.正溴丁烷粗产品的制备和蒸馏分离过程中,经过水洗、氢氧化钠溶液洗涤、再
次水洗以及干燥等步骤可以去除粗产品中的杂质,提高其纯度,D正确;故选:B。
14.向AgBr饱和溶液(有足量AgBr固体)中滴加NaSO 溶液,发生反应Ag++
2 2 3
[Ag( )]-和[Ag( )]-+ [Ag( )]3-, lg[c(M)/(mol/L)、lgc(N)与
2
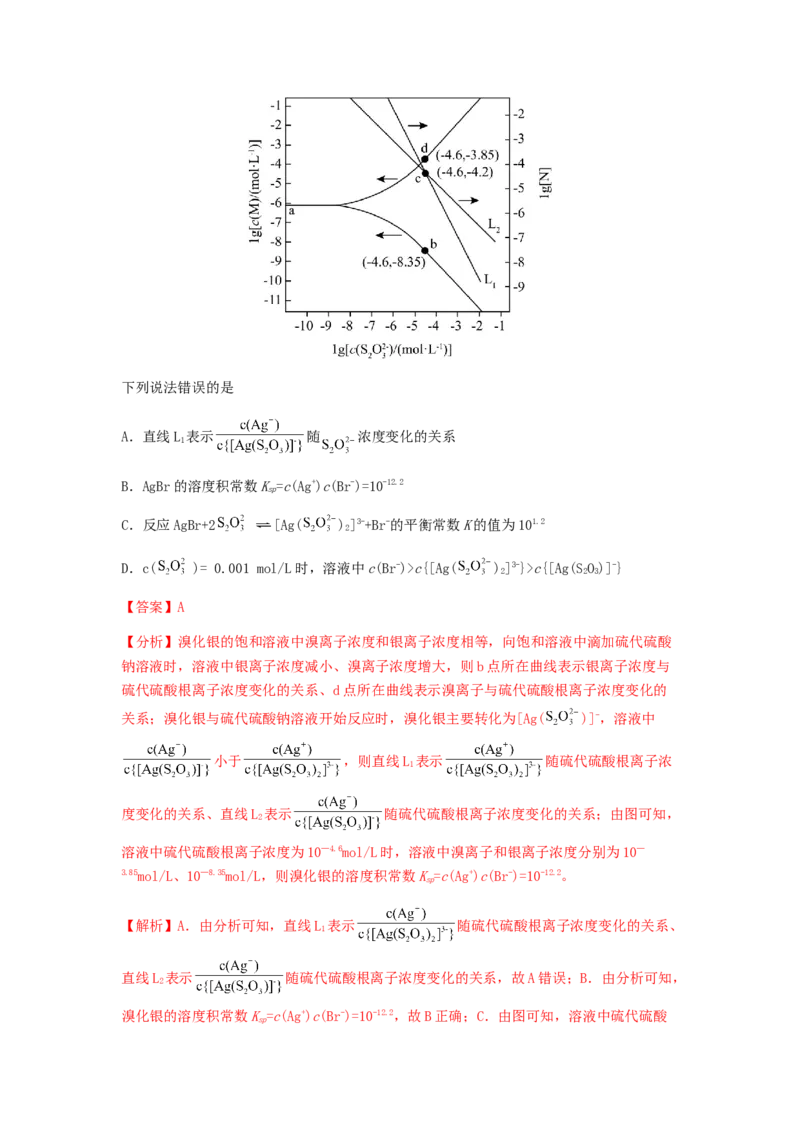
lg[c( )/mol/L)的关系如下图所示(其中M代表Ag+或Br-;N代表 或
):下列说法错误的是
A.直线L 表示 随 浓度变化的关系
1
B.AgBr的溶度积常数K=c(Ag+)c(Br-)=10-12.2
sp
C.反应AgBr+2 [Ag( )]3-+Br-的平衡常数K的值为101.2
2
D.c( )= 0.001 mol/L时,溶液中c(Br-)>c{[Ag( )]3-}>c{[Ag(SO)]-}
2 2 3
【答案】A
【分析】溴化银的饱和溶液中溴离子浓度和银离子浓度相等,向饱和溶液中滴加硫代硫酸
钠溶液时,溶液中银离子浓度减小、溴离子浓度增大,则b点所在曲线表示银离子浓度与
硫代硫酸根离子浓度变化的关系、d点所在曲线表示溴离子与硫代硫酸根离子浓度变化的
关系;溴化银与硫代硫酸钠溶液开始反应时,溴化银主要转化为[Ag( )]-,溶液中
小于 ,则直线L 表示 随硫代硫酸根离子浓
1
度变化的关系、直线L 表示 随硫代硫酸根离子浓度变化的关系;由图可知,
2
溶液中硫代硫酸根离子浓度为10—4.6mol/L时,溶液中溴离子和银离子浓度分别为10—
3.85mol/L、10—8.35mol/L,则溴化银的溶度积常数K=c(Ag+)c(Br-)=10-12.2。
sp
【解析】A.由分析可知,直线L 表示 随硫代硫酸根离子浓度变化的关系、
1
直线L 表示 随硫代硫酸根离子浓度变化的关系,故A错误;B.由分析可知,
2
溴化银的溶度积常数K=c(Ag+)c(Br-)=10-12.2,故B正确;C.由图可知,溶液中硫代硫酸
sp根离子浓度为10—4.6mol/L时,溶液中溴离子和银离子浓度分别为10—3.85mol/L、10—
8.35mol/L, 为10—4.2,则溶液中[Ag( )]3-的浓度为 =10—
2
4.15mol/L,反应的平衡常数K= = =101.2,故C正确;D.
由图可知,硫代硫酸根离子浓度为0.001 mol/L时,溶液中溴离子浓度最大,
的值大于 的值,则溶液中[Ag( )]3-的浓度大于[Ag(
2
)]-的浓度,所以溶液中离子浓度大小顺序为c(Br-)>c{[Ag( )]3-}
2
>c{[Ag(SO)]-},故D正确;故选A。
2 3
二、主观题
17.(15分)精脱硫技术主要用于煤气中羰基硫(COS)和二硫化碳(CS)的转化。回答下列
2
问题:
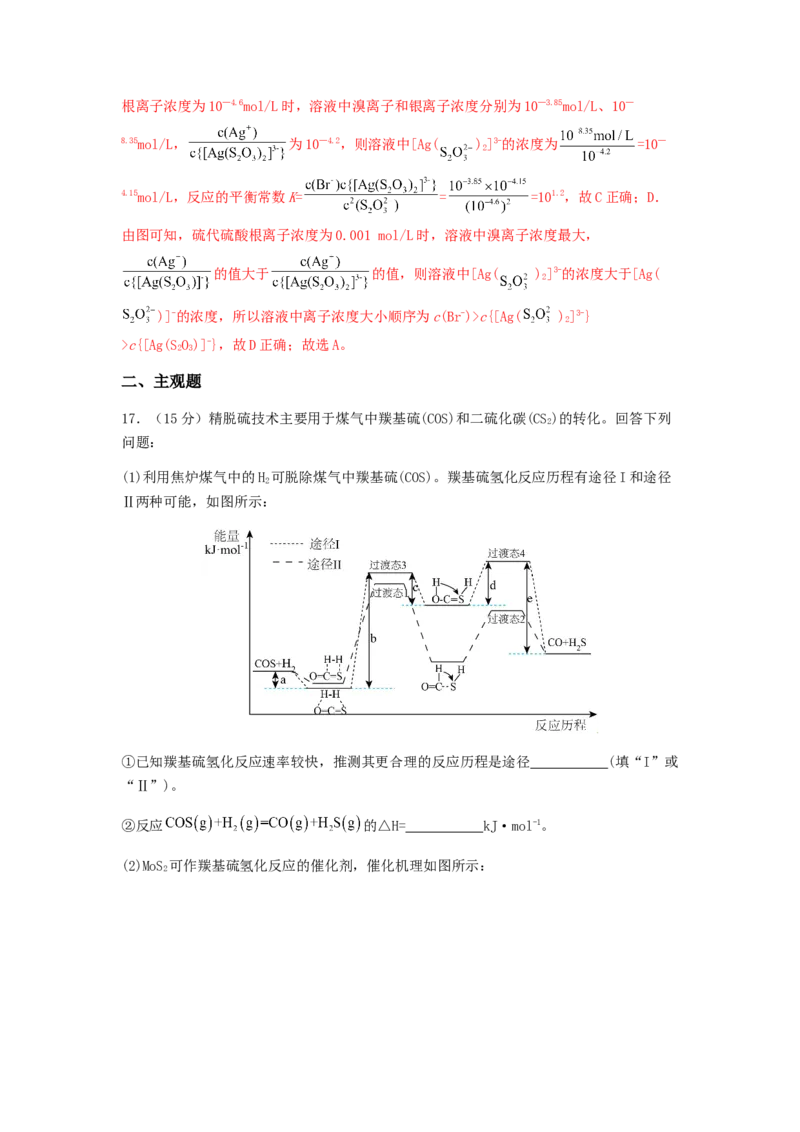
(1)利用焦炉煤气中的H 可脱除煤气中羰基硫(COS)。羰基硫氢化反应历程有途径I和途径
2
Ⅱ两种可能,如图所示:
①已知羰基硫氢化反应速率较快,推测其更合理的反应历程是途径 (填“I”或
“Ⅱ”)。
②反应 的△H= kJ·mol-1。
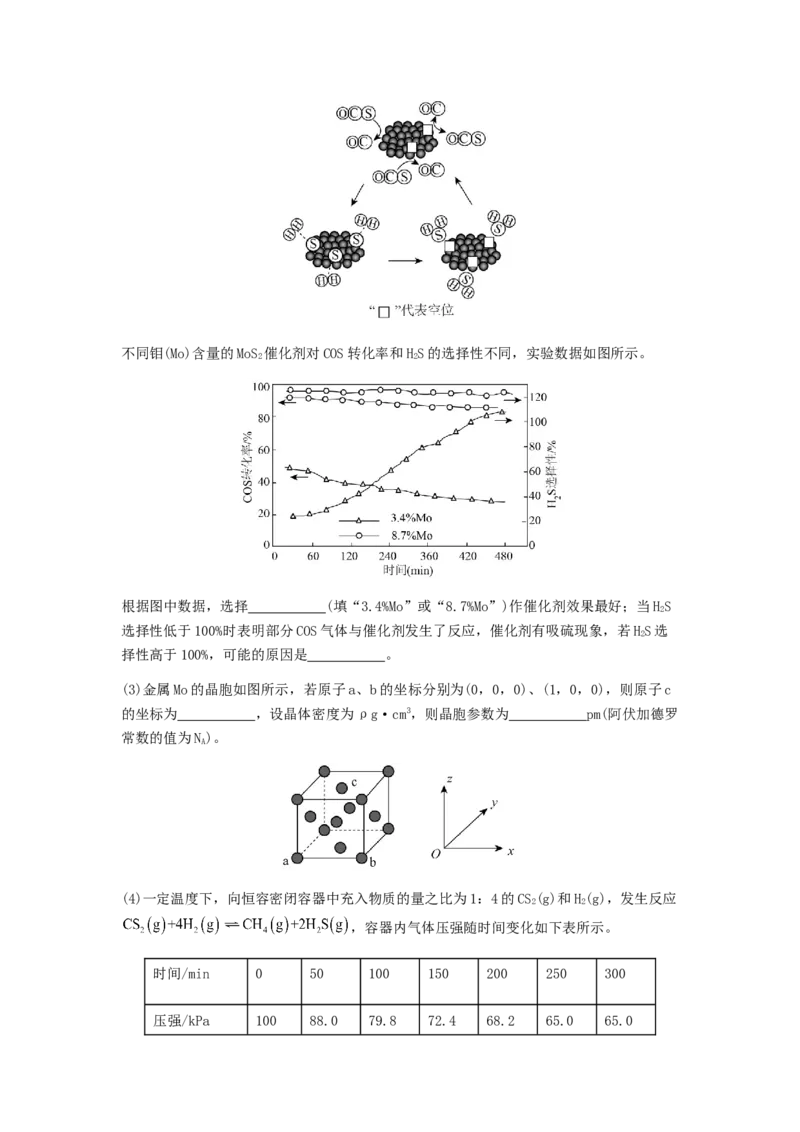
(2)MoS 可作羰基硫氢化反应的催化剂,催化机理如图所示:
2不同钼(Mo)含量的MoS 催化剂对COS转化率和HS的选择性不同,实验数据如图所示。
2 2
根据图中数据,选择 (填“3.4%Mo”或“8.7%Mo”)作催化剂效果最好;当HS
2
选择性低于100%时表明部分COS气体与催化剂发生了反应,催化剂有吸硫现象,若HS选
2
择性高于100%,可能的原因是 。
(3)金属Mo的晶胞如图所示,若原子a、b的坐标分别为(0,0,0)、(1,0,0),则原子c
的坐标为 ,设晶体密度为ρg·cm3,则晶胞参数为 pm(阿伏加德罗
常数的值为N)。
A
(4)一定温度下,向恒容密闭容器中充入物质的量之比为1:4的CS(g)和H(g),发生反应
2 2
,容器内气体压强随时间变化如下表所示。
时间/min 0 50 100 150 200 250 300
压强/kPa 100 88.0 79.8 72.4 68.2 65.0 65.0①0-250min内,H 分压的平均变化值为 kPa·min-l。
2
②该温度下,平衡常数K= (kPa)-2(列出计算式)。
p
【答案】(1)Ⅱ(1分) b‒a‒c+d‒e(2分)
(2)8.7%Mo(2分) 催化剂本身在反应过程中有失硫现象(2分)
(3) (2分) (2分)
(4)0.28(2分) (2分)
【解析】(1)①反应的活化能越大,反应速率越慢,由图可知,途径I的活化能大于途径
Ⅱ,反应速率慢于途径Ⅱ,所以应速率较快的羰基硫氢化的反应历程是途径Ⅱ,故答案为:
Ⅱ;②由图可知,该反应为反应物总能量小于生成物总能量的吸热反应,反应的△H=(b‒a‒
c)kJ/mol—(e—d)kJ/mo=( b‒a‒c+d‒e)kJ/mol,故答案为:b‒a‒c+d‒e;
(2)由图可知,时间相同时,8.7%Mo作催化剂条件下反应的羰基硫转化率和硫化氢选择
性均大于3.4%Mo作催化剂条件下,说明反应速率快于3.4%Mo作催化剂条件下,所以选择
8.7%Mo作催化剂效果最好;由题意可知,硫化氢选择性低于100%是因为部分羰基硫气体与
催化剂发生了反应,催化剂有吸硫现象所致,则硫化氢选择性高于100%是因为催化剂本身
在反应过程中有失硫现象所致,故答案为:8.7%Mo;催化剂本身在反应过程中有失硫现象;
(3)由晶胞结构可知,晶胞中位于顶点的原子a、b的坐标分别为(0,0,0)、(1,0,
0),则晶胞的边长为1,所以位于面心的原子c的坐标为 ;位于顶点和面心的钼原
子个数为8× +6× =4,设晶胞参数为apm,由晶胞的质量公式可得: =10—30aρ,
解得a= ,故答案为: ; ;
(4)由表格数据可知,起始二硫化碳、氢气的分压分别为100kPa× =20kPa、100kPa—
20kPa=80kPa,250min反应达到平衡时,容器内气体压强为65kPa,设平衡时消耗二硫化碳
的分压为akPa,由题意可建立如下三段式:由平衡时容器内气体压强为65kPa可得:100—2a=65,解得a=17.5;①由三段式所得数据
可知,0-250min内,氢气分压的平均变化值为 =0.28kPa/min,故答案为:
0.28;②由三段式所得数据可知,该温度下,平衡常数K=
p
= (kPa)-2,故答案为: 。