文档内容
专项 09 水溶液中的离子平衡
该专题分为两个板块
【1】知识清单
一、电离常数及其应用
1. 电离常数的四大应用
2. 电离常数与水解常数(K )的关系
h
3. 弱电解质电离常数的两种计算方法
二、电解质溶液中离子浓度关系
1. 电解质溶液中的“三守恒”
2. 巧抓酸碱滴定中的“五点”,判断溶液中的粒子浓度关系
三、分布系数图像与对数图像
1. 弱电解质(弱酸或弱碱)分布系数图像
2. 对数图像
【2】专项练习
【1】知识清单
一、电离常数及其应用
1. 电离常数的四大应用
(1)判断弱酸(或弱碱)的相对强弱,电离常数越大,酸性(或碱性)越强。在常温下,CHCOOH的Ka=
3
1.75×10-5,HClO的Ka=2.95×10-8,则酸性强弱为CHCOOH HClO。
3
(2)判断盐溶液的酸性(或碱性)强弱
电离常数越大,对应的盐水解程度越小,盐溶液的碱性(或酸性)越弱,如醋酸:K=1.75×10-5,次氯酸:K
=2.95×10-8,则同浓度的醋酸钠和次氯酸钠溶液的pH:醋酸钠 次氯酸钠。
(3)判断反应能否发生或者判断产物是否正确
通过强酸制弱酸来判断。如HCO :K =4.2×10-7,K =5.6×10-11,苯酚(C HOH):K=1.3×10-10,向苯
2 3 a1 a2 6 5 a
酚钠(C HONa)溶液中通入的CO 不论是少量还是过量,其化学方程式为:
6 5 2
。
(4)判断溶液微粒浓度比值的变化
利用温度不变,电离常数不变来判断。如向0.1 mol·L-1 CHCOOH溶液加水稀释,的值变大还是变小?
3
分析:首先要建立与K值的联系,再分析单一变量离子浓度。
==,稀释时,c(H+)减小,K 不变,则变大。
a
2.电离常数与水解常数(K )的关系
h
(1)对于一元弱酸HA,K 与K 的关系
a h
HA电离:HA H++A-,K=;
a
A-水解:A-+HO HA+OH-,K =;
2 h
则K·K =c(H+)·c(OH-)=K
a h w故
(2)对于二元弱酸HB,K (H B)、K (H B)与K (HB-)、K (B2-)的关系
2 a1 2 a2 2 h h
HB-水解:HB-+HO HB+OH-, ;
2 2
B2-水解:B2-+HO HB-+OH-
2
。
3.弱电解质电离常数的两种计算方法
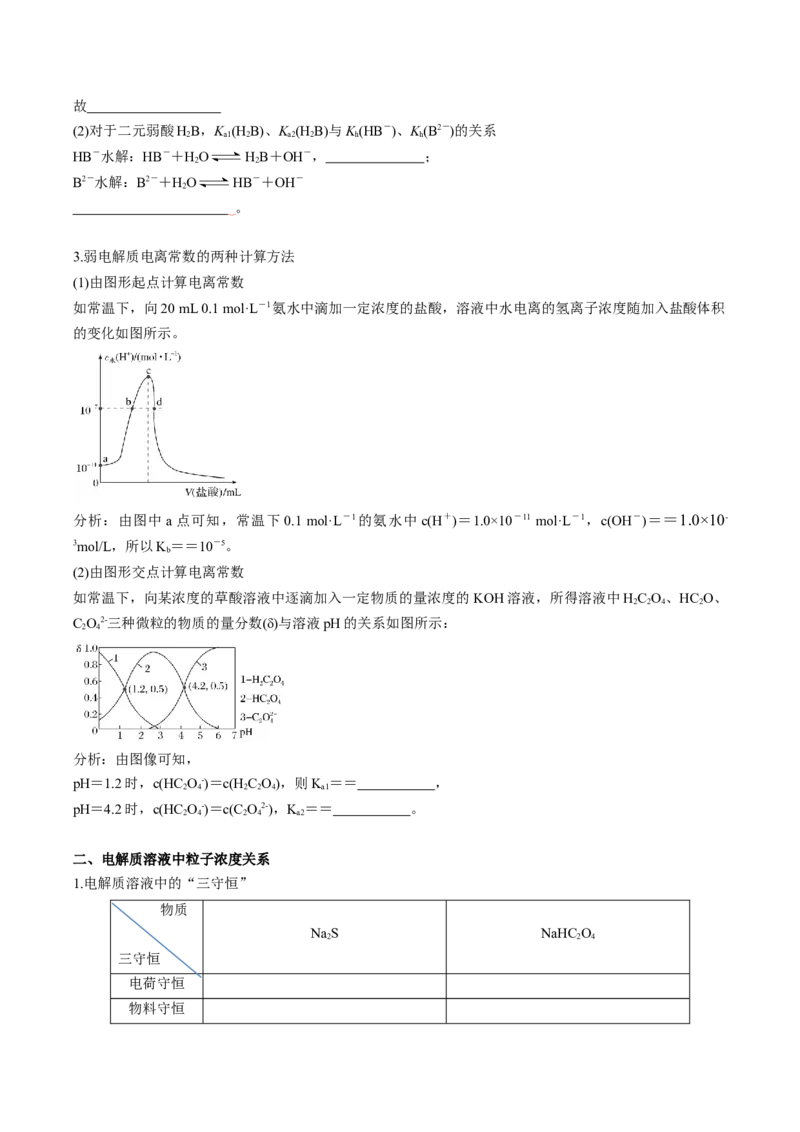
(1)由图形起点计算电离常数
如常温下,向20 mL 0.1 mol·L-1氨水中滴加一定浓度的盐酸,溶液中水电离的氢离子浓度随加入盐酸体积
的变化如图所示。
分析:由图中a点可知,常温下0.1 mol·L-1的氨水中c(H+)=1.0×10-11 mol·L-1,c(OH-)==1.0×10-
3mol/L,所以K==10-5。
b
(2)由图形交点计算电离常数
如常温下,向某浓度的草酸溶液中逐滴加入一定物质的量浓度的 KOH溶液,所得溶液中HC O 、HC O、
2 2 4 2
C O2-三种微粒的物质的量分数(δ)与溶液pH的关系如图所示:
2 4
分析:由图像可知,
pH=1.2时,c(HC O-)=c(HC O),则K == ,
2 4 2 2 4 a1
pH=4.2时,c(HC O-)=c(C O2-),K == 。
2 4 2 4 a2
二、电解质溶液中粒子浓度关系
1.电解质溶液中的“三守恒”
物质
NaS NaHC O
2 2 4
三守恒
电荷守恒
物料守恒质子守恒
说明:质子守恒可以用电荷守恒与物料守恒推出,也可以用图示法推出。如:
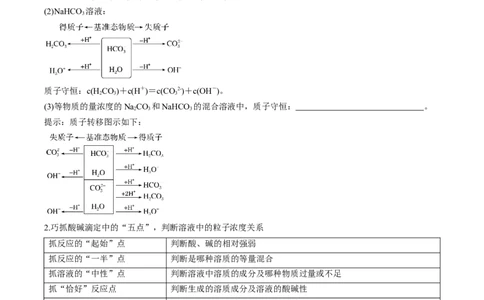
(1)Na CO 溶液:
2 3
质子守恒:c(OH-)=c(H+)+c(HCO -)+2c(HCO)。
3 2 3
(2)NaHCO 溶液:
3
质子守恒:c(HCO)+c(H+)=c(CO2-)+c(OH-)。
2 3 3
(3)等物质的量浓度的NaCO 和NaHCO 的混合溶液中,质子守恒: 。
2 3 3
提示:质子转移图示如下:
2.巧抓酸碱滴定中的“五点”,判断溶液中的粒子浓度关系
抓反应的“起始”点 判断酸、碱的相对强弱
抓反应的“一半”点 判断是哪种溶质的等量混合
抓溶液的“中性”点 判断溶液中溶质的成分及哪种物质过量或不足
抓“恰好”反应点 判断生成的溶质成分及溶液的酸碱性
抓反应的“过量”点 判断溶液中的溶质,判断哪种物质过量
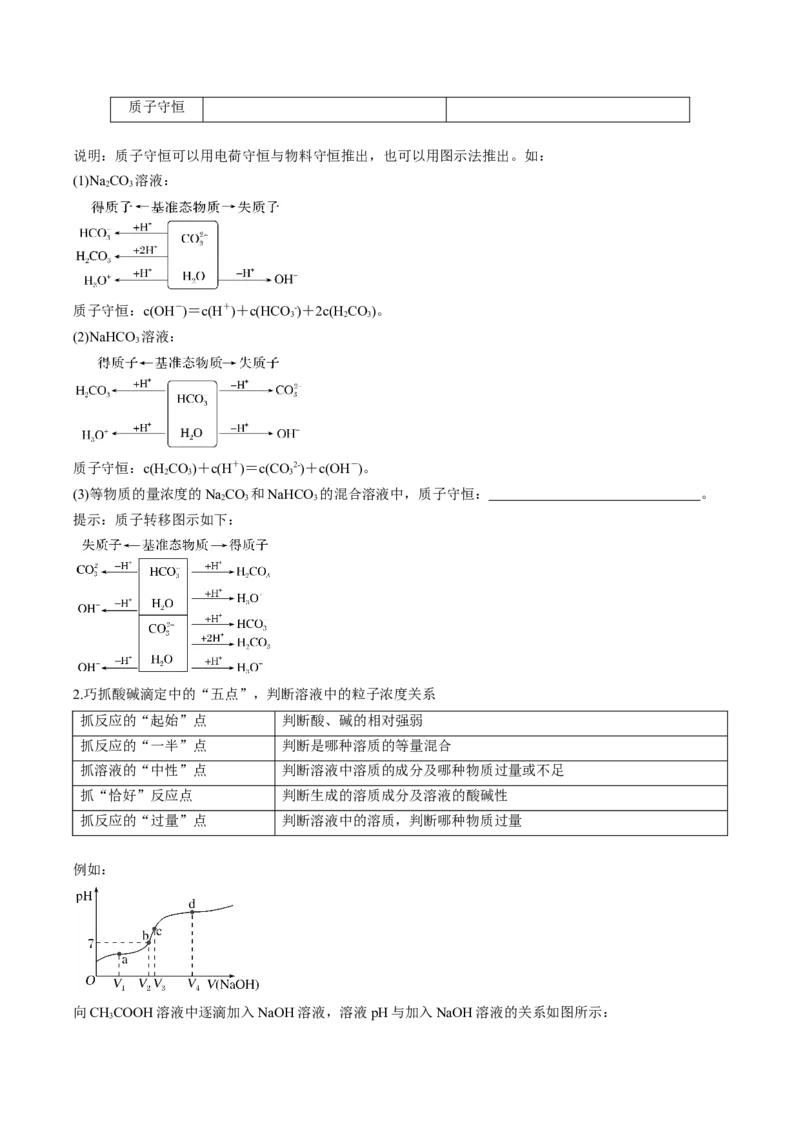
例如:
向CHCOOH溶液中逐滴加入NaOH溶液,溶液pH与加入NaOH溶液的关系如图所示:
3(注:a点为反应一半点,b点为中性点,c点为恰好反应点,d点NaOH过量一倍)
分析:
a点,溶质为:CHCOONa、CHCOOH,离子浓度关系: ;
3 3
b点,溶质为:CHCOONa、CHCOOH,离子浓度关系: ;
3 3
c点,溶质为:CHCOONa,离子浓度关系: ;
3
d点,溶质为:CHCOONa、NaOH,离子浓度关系: 。
3
其中a点是等物质的量浓度CHCOOH和CHCOONa的混合溶液,此混合液的“三守恒”“一比较”的分
3 3
析方法如下:
三、分布系数图像与对数图像
1.弱电解质(弱酸或弱碱)分布系数图像
一元弱酸(以 CHCOOH 二元弱酸(以 HC O 为
3 2 2 4
举例 三元弱酸(以HPO 为例)
3 4
为例) 例)
弱电解
质分布
系数图
弱酸溶液中加入强碱,发生中和反应,溶液的pH不断增大,各成分粒子的含量不
原因
断动态变化
δ 为 CHCOOH 、 δ 为 δ 为 HC O 、 δ 为 δ 为HPO 、δ 为HPO、
0 3 1 0 2 2 4 1 0 3 4 1 2
δn
CHCOO- HC O、δ 为C O δ 为HPO、δ 为PO
3 2 2 2 2 3
交叉点的含义[图中pH= 交叉点的含义(二元酸有 交叉点的含义:
4.76时,曲线相交, 两个交叉点): (1)pH=2时,由图可知:
利用交 c(CHCOO-)= (1)当pH=1.2时,由图 c(H PO )=c(H PO)
3 3 4 2
点求K c(CHCOOH)]: 可知:
3
K= c(H 2 C 2 O 4 )=c(HC 2 O)
a
所以,K=c(H+)=10-4.76, K 1 = K 1 =c(H+)=10-2。
a(2)pH=7.1时,由图可
知:
所以,K =c(H+)=10-
1
c(HPO)=c(H PO)
1.2。 2
(2)当pH=4.2时,由图
可知:
K =c(H+)=10-7.1。
lg K=-4.76,pK=4.76 2
a a
c(C O)=c(HC O)
2 2 (3)pH=12.2时,由图可
K =
2 知:
所以,K =c(H+)=10-
2 c(HPO)=c(PO)
4.2
K =
3
K =c(H+)=10-12.2
3
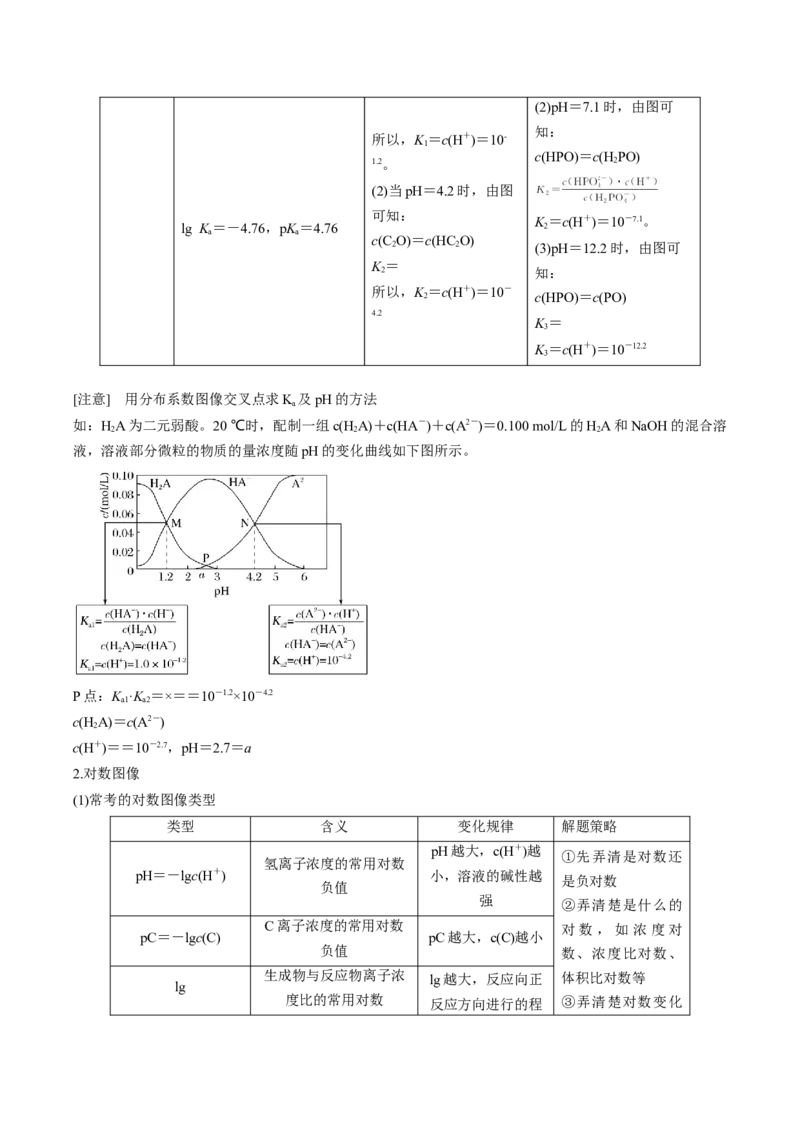
[注意] 用分布系数图像交叉点求K 及pH的方法
a
如:HA为二元弱酸。20 ℃时,配制一组c(HA)+c(HA-)+c(A2-)=0.100 mol/L的HA和NaOH的混合溶
2 2 2
液,溶液部分微粒的物质的量浓度随pH的变化曲线如下图所示。
P点:K ·K =×==10-1.2×10-4.2
a1 a2
c(H A)=c(A2-)
2
c(H+)==10-2.7,pH=2.7=a
2.对数图像
(1)常考的对数图像类型
类型 含义 变化规律 解题策略
pH越大,c(H+)越
①先弄清是对数还
氢离子浓度的常用对数
pH=-lgc(H+) 小,溶液的碱性越
是负对数
负值
强
②弄清楚是什么的
C离子浓度的常用对数 对数,如浓度对
pC=-lgc(C) pC越大,c(C)越小
负值 数、浓度比对数、
生成物与反应物离子浓 lg越大,反应向正 体积比对数等
lg
度比的常用对数 反应方向进行的程 ③弄清楚对数变化度越大
稀释后与稀释前体积比 lg越大,稀释程度
lg
的常用对数 越大
AG越大,酸性越 所表示的意义
氢离子与氢氧根离子浓
AG=lg 强,中性时,=1,
度比的常用对数
AG=0
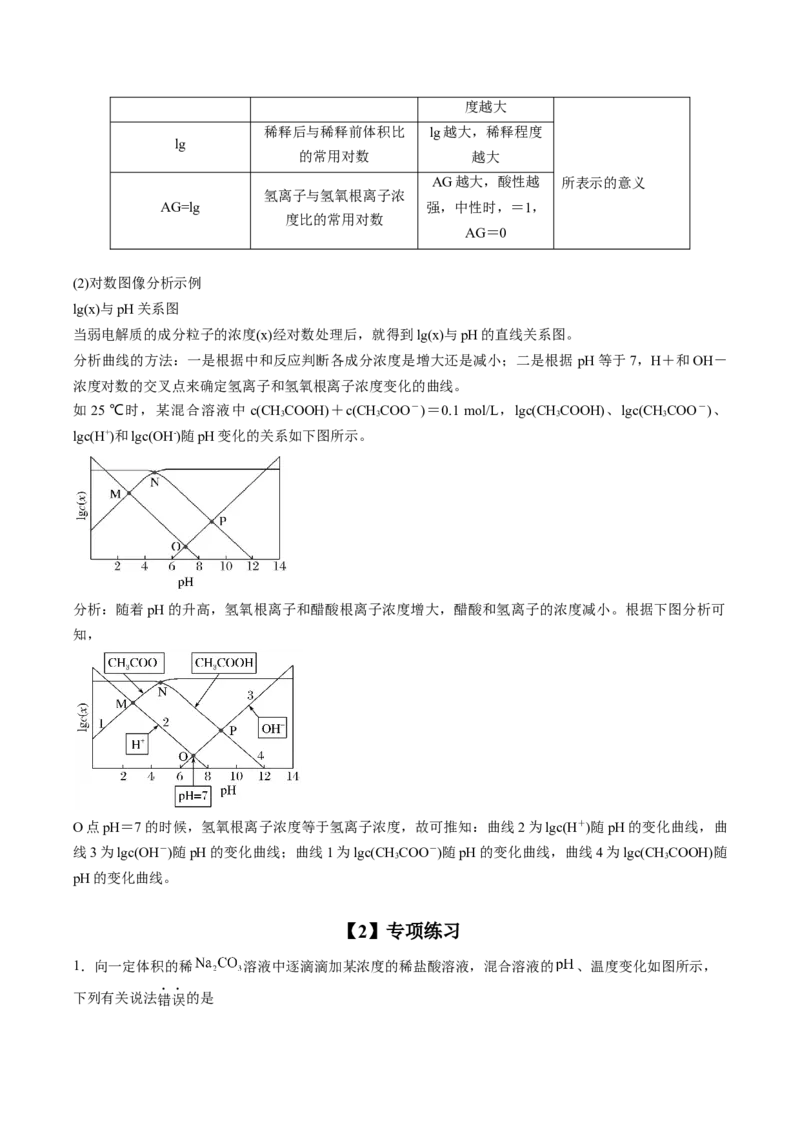
(2)对数图像分析示例
lg(x)与pH关系图
当弱电解质的成分粒子的浓度(x)经对数处理后,就得到lg(x)与pH的直线关系图。
分析曲线的方法:一是根据中和反应判断各成分浓度是增大还是减小;二是根据 pH等于7,H+和OH-
浓度对数的交叉点来确定氢离子和氢氧根离子浓度变化的曲线。
如25 ℃时,某混合溶液中 c(CHCOOH)+c(CHCOO-)=0.1 mol/L,lgc(CH COOH)、lgc(CH COO-)、
3 3 3 3
lgc(H+)和lgc(OH-)随pH变化的关系如下图所示。
分析:随着pH的升高,氢氧根离子和醋酸根离子浓度增大,醋酸和氢离子的浓度减小。根据下图分析可
知,
O点pH=7的时候,氢氧根离子浓度等于氢离子浓度,故可推知:曲线2为lgc(H+)随pH的变化曲线,曲
线3为lgc(OH-)随pH的变化曲线;曲线1为lgc(CH COO-)随pH的变化曲线,曲线4为lgc(CH COOH)随
3 3
pH的变化曲线。
【2】专项练习
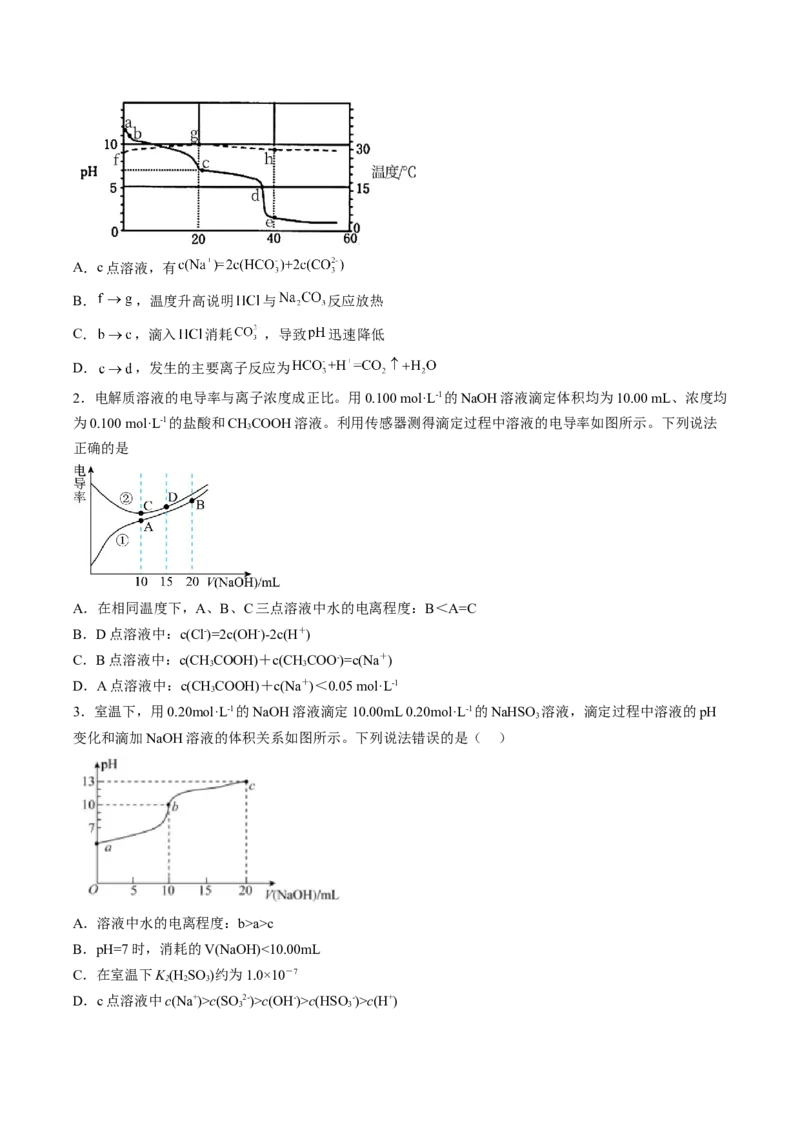
1.向一定体积的稀 溶液中逐滴滴加某浓度的稀盐酸溶液,混合溶液的 、温度变化如图所示,
下列有关说法错误的是A.c点溶液,有
B. ,温度升高说明 与 反应放热
C. ,滴入 消耗 ,导致 迅速降低
D. ,发生的主要离子反应为
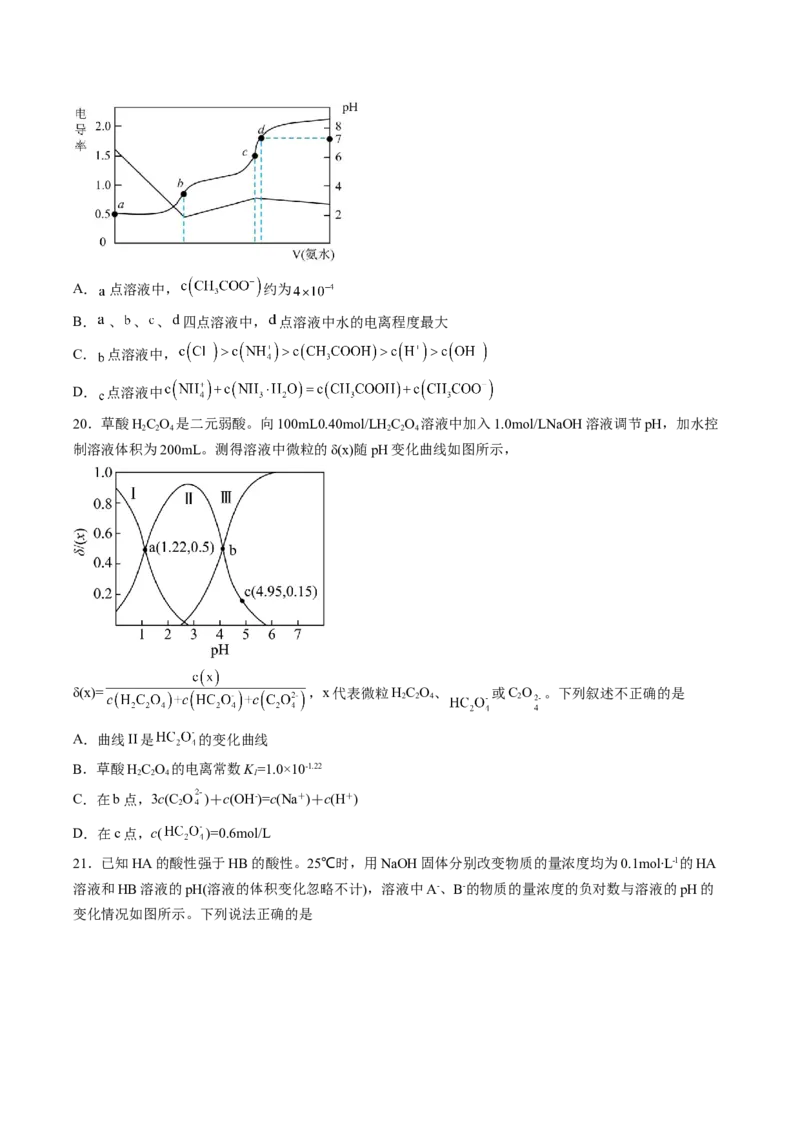
2.电解质溶液的电导率与离子浓度成正比。用0.100 mol·L-1的NaOH溶液滴定体积均为10.00 mL、浓度均
为0.100 mol·L-1的盐酸和CHCOOH溶液。利用传感器测得滴定过程中溶液的电导率如图所示。下列说法
3
正确的是
A.在相同温度下,A、B、C三点溶液中水的电离程度:B<A=C
B.D点溶液中:c(Cl-)=2c(OH-)-2c(H+)
C.B点溶液中:c(CHCOOH)+c(CHCOO-)=c(Na+)
3 3
D.A点溶液中:c(CHCOOH)+c(Na+)<0.05 mol·L-1
3
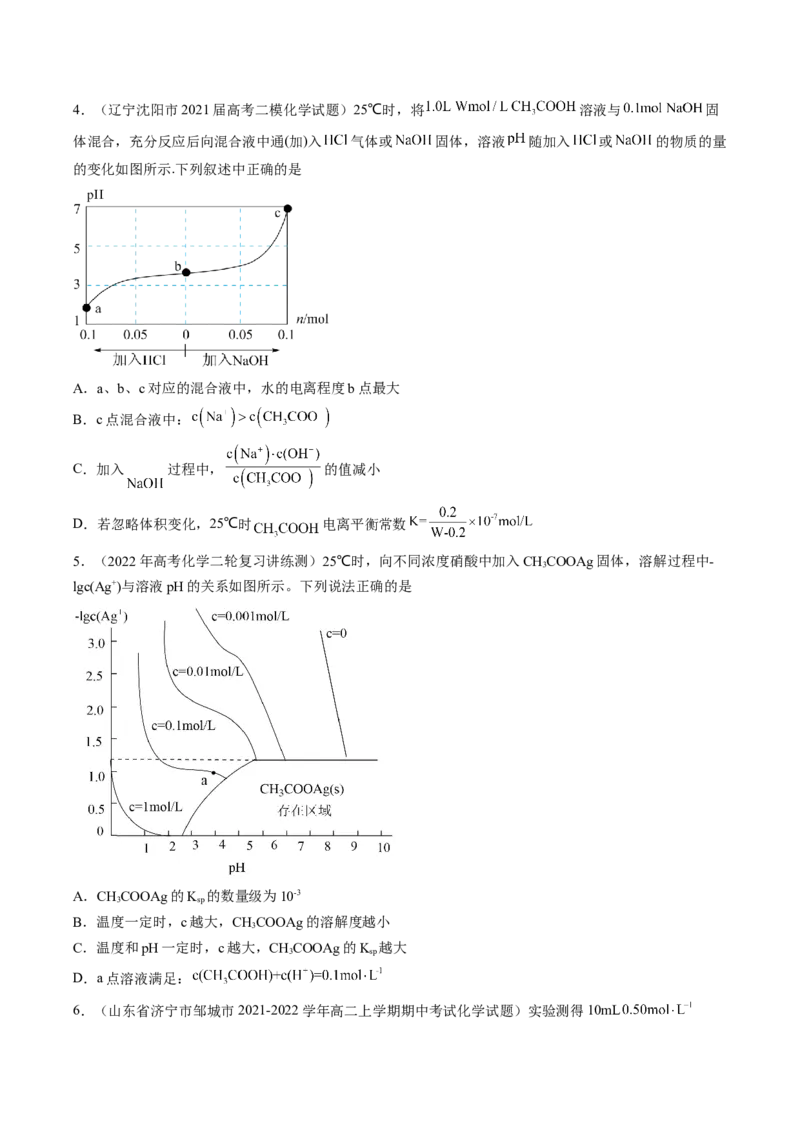
3.室温下,用0.20mol·L-1的NaOH溶液滴定10.00mL 0.20mol·L-1的NaHSO 溶液,滴定过程中溶液的pH
3
变化和滴加NaOH溶液的体积关系如图所示。下列说法错误的是( )
A.溶液中水的电离程度:b>a>c
B.pH=7时,消耗的V(NaOH)<10.00mL
C.在室温下K (H SO )约为1.0×10-7
2 2 3
D.c点溶液中c(Na+)>c(SO 2-)>c(OH-)>c(HSO -)>c(H+)
3 34.(辽宁沈阳市2021届高考二模化学试题)25℃时,将 溶液与 固
体混合,充分反应后向混合液中通(加)入 气体或 固体,溶液 随加入 或 的物质的量
的变化如图所示.下列叙述中正确的是
A.a、b、c对应的混合液中,水的电离程度b点最大
B.c点混合液中:
C.加入 过程中, 的值减小
D.若忽略体积变化,25℃时 电离平衡常数
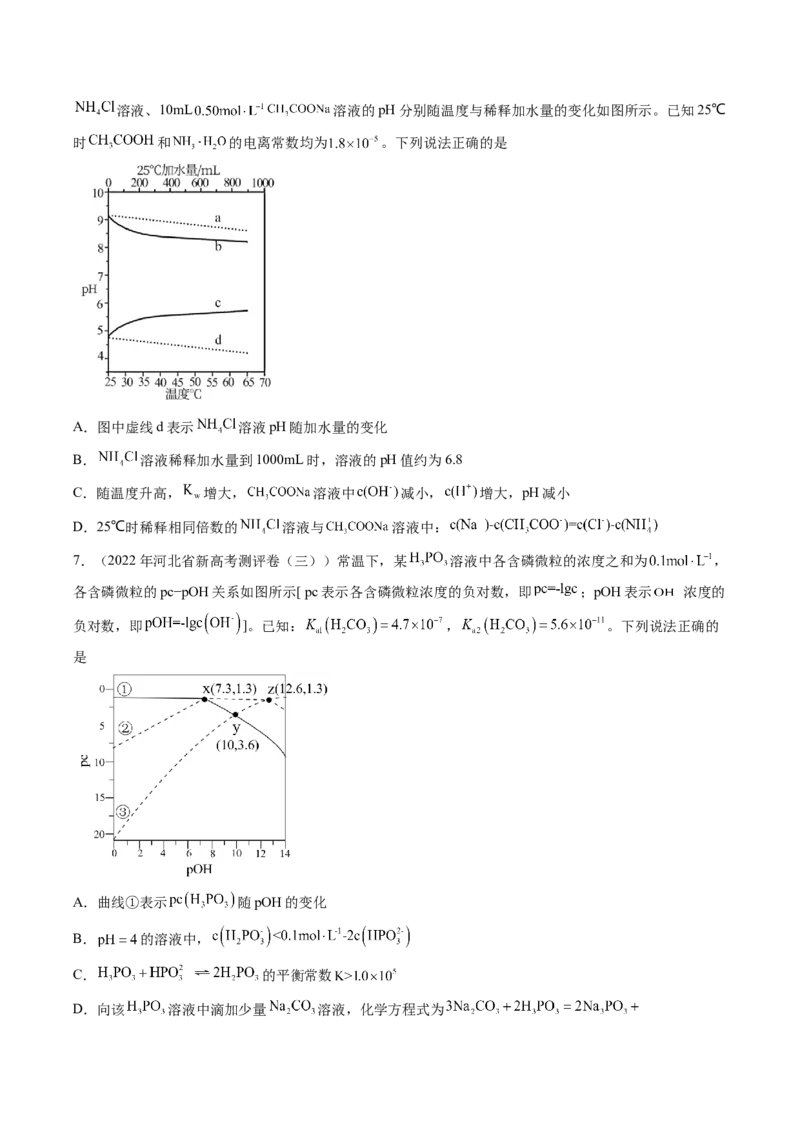
5.(2022年高考化学二轮复习讲练测)25℃时,向不同浓度硝酸中加入CHCOOAg固体,溶解过程中-
3
lgc(Ag+)与溶液pH的关系如图所示。下列说法正确的是
A.CHCOOAg的K 的数量级为10-3
3 sp
B.温度一定时,c越大,CHCOOAg的溶解度越小
3
C.温度和pH一定时,c越大,CHCOOAg的K 越大
3 sp
D.a点溶液满足:
6.(山东省济宁市邹城市2021-2022学年高二上学期期中考试化学试题)实验测得10mL溶液、10mL 溶液的pH分别随温度与稀释加水量的变化如图所示。已知25℃
时 和 的电离常数均为 。下列说法正确的是
A.图中虚线d表示 溶液pH随加水量的变化
B. 溶液稀释加水量到1000mL时,溶液的pH值约为6.8
C.随温度升高, 增大, 溶液中 减小, 增大,pH减小
D.25℃时稀释相同倍数的 溶液与 溶液中:
7.(2022年河北省新高考测评卷(三))常温下,某 溶液中各含磷微粒的浓度之和为 ,
各含磷微粒的pc−pOH关系如图所示[ pc表示各含磷微粒浓度的负对数,即 ;pOH表示 浓度的
负对数,即 ]。已知: , 。下列说法正确的
是
A.曲线①表示 随pOH的变化
B. 的溶液中,
C. 的平衡常数
D.向该 溶液中滴加少量 溶液,化学方程式为8.常温下,现有 的 溶液, 已知含氮 或含碳 各微粒的分布分数 平衡时某
种微粒的浓度占各种微粒浓度之和的分数 与pH的关系如图所示。下列说法不正确的是
A.常温下
B.向 的上述溶液中逐滴滴加NaOH溶液时, 和 浓度都逐渐减小
C. 溶液中存在下列守恒关系:
D.当溶液的 时,溶液中存在下列关系:
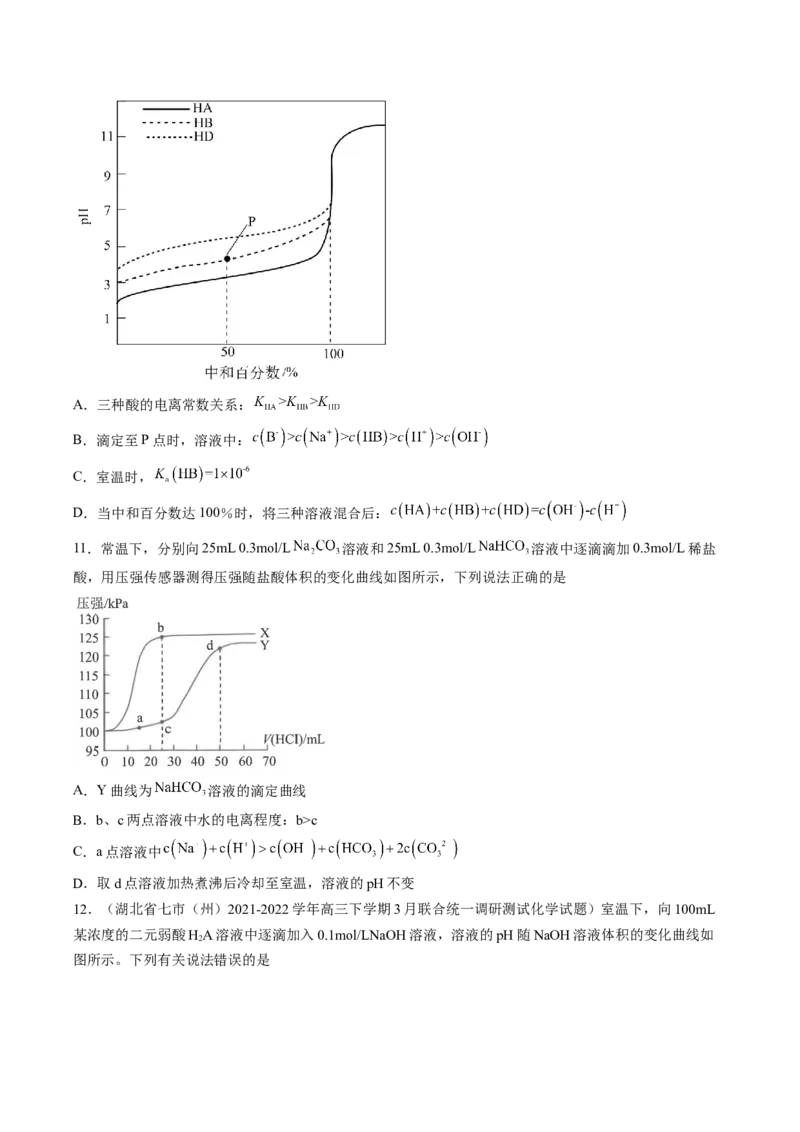
9.(重庆市第一中学2021-2022学年高三上学期第三次月考化学试题)酒石酸是一种存在于某些植物中的
二元有机弱酸.一定温度下,向 酒石酸溶液( 表示)中滴加 溶液,混合
溶液 随 变化的关系如下图所示,下列说法正确的是
A.a点表示第一滴定终点,可用石蕊溶液作为指示剂
B.a点时:
C.b点时:
D.c点时:
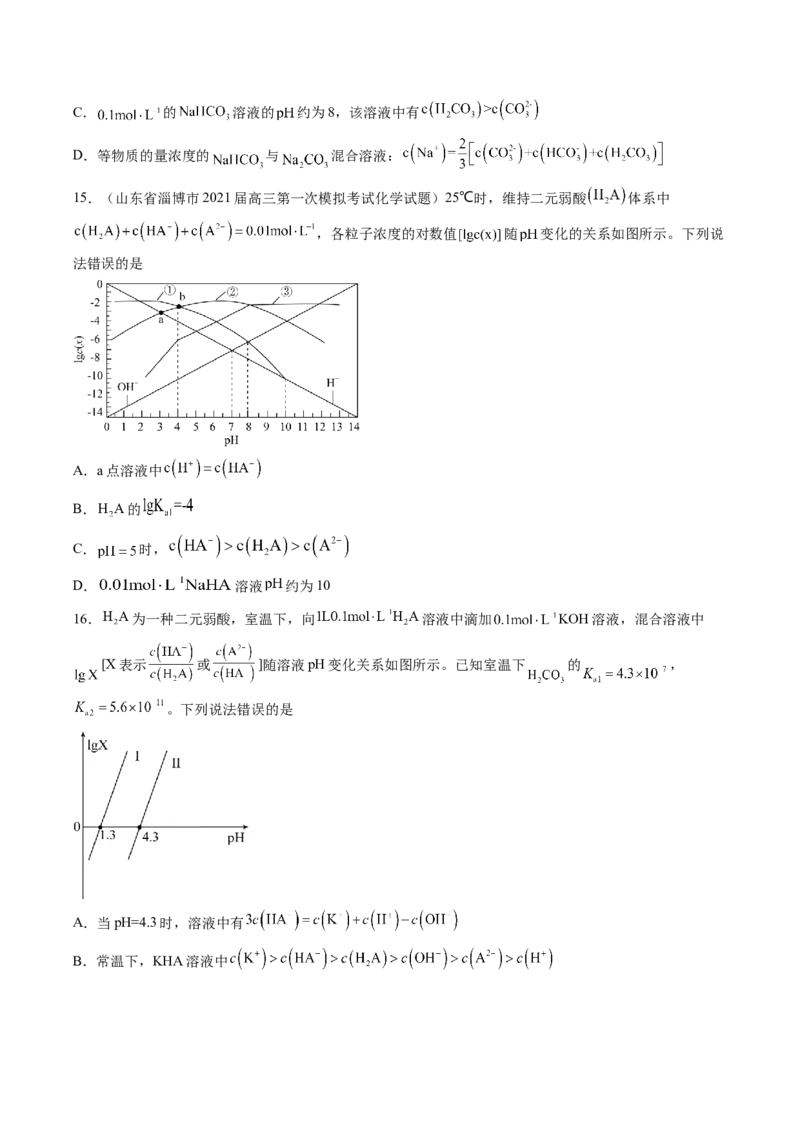
10.(湖北省重点中学2021-2022学年高二下学期3月联考化学试题)室温下,用相同浓度的NaOH溶液,
分别滴定浓度均为 的三种酸(HA、HB和HD)溶液,滴定曲线如图所示,下列判断错误的是A.三种酸的电离常数关系:
B.滴定至P点时,溶液中:
C.室温时,
D.当中和百分数达100%时,将三种溶液混合后:
11.常温下,分别向25mL 0.3mol/L 溶液和25mL 0.3mol/L 溶液中逐滴滴加0.3mol/L稀盐
酸,用压强传感器测得压强随盐酸体积的变化曲线如图所示,下列说法正确的是
A.Y曲线为 溶液的滴定曲线
B.b、c两点溶液中水的电离程度:b>c
C.a点溶液中
D.取d点溶液加热煮沸后冷却至室温,溶液的pH不变
12.(湖北省七市(州)2021-2022学年高三下学期3月联合统一调研测试化学试题)室温下,向100mL
某浓度的二元弱酸HA溶液中逐滴加入0.1mol/LNaOH溶液,溶液的pH随NaOH溶液体积的变化曲线如
2
图所示。下列有关说法错误的是A.K (H A)数量级为10-3
a1 2
B.b点时:c(Na+)>c(HA—)>c(H+)>c(A2—)>c(OH—)
C.水的电离程度:d>c>b>a
D.b→c段,反应的离子方程式为HA—+OH—=A2—+H O
2
13.(湖北部分重点学校联考2021届高三2月新高考质量检测化学试题)温度为T时,用NaOH调节草酸
( 表示,电离常数为 、 )溶液,使其满足 ,溶液中 、
、 、 及 的对数值与pH关系如图所示。下列说法错误的是
A.温度T可能为25℃ B.X点对应的
C.Z点溶液中: D.该温度下, 的 数量级为
14.下列说法错误的是
A.将 的 溶液加水稀释, 变大
B.常温下,向氨水溶液中滴入 溶液至 时:C. 的 溶液的 约为8,该溶液中有
D.等物质的量浓度的 与 混合溶液:
15.(山东省淄博市2021届高三第一次模拟考试化学试题)25℃时,维持二元弱酸 体系中
,各粒子浓度的对数值 随 变化的关系如图所示。下列说
法错误的是
A.a点溶液中
B. 的
C. 时,
D. 溶液 约为10
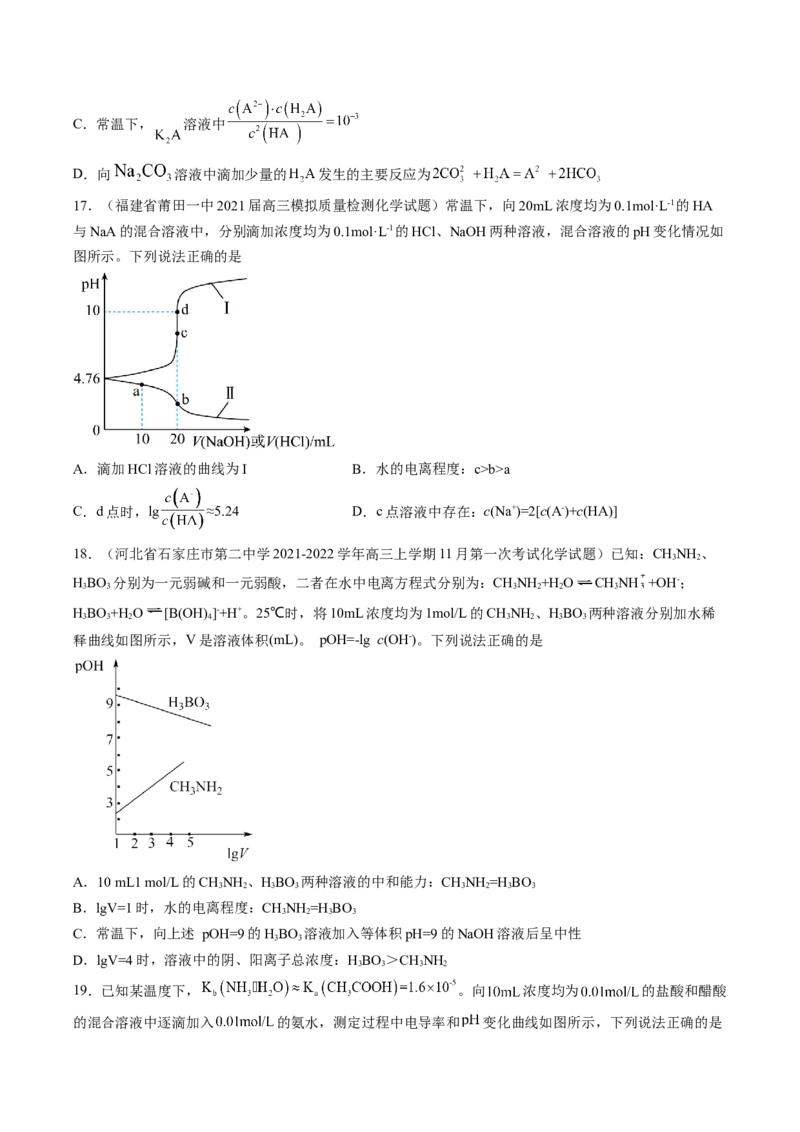
16. 为一种二元弱酸,室温下,向 溶液中滴加 KOH溶液,混合溶液中
[X表示 或 ]随溶液pH变化关系如图所示。已知室温下 的 ,
。下列说法错误的是
A.当pH=4.3时,溶液中有
B.常温下,KHA溶液中C.常温下, 溶液中
D.向 溶液中滴加少量的 发生的主要反应为
17.(福建省莆田一中2021届高三模拟质量检测化学试题)常温下,向20mL浓度均为0.1mol·L-1的HA
与NaA的混合溶液中,分别滴加浓度均为0.1mol·L-1的HCl、NaOH两种溶液,混合溶液的pH变化情况如
图所示。下列说法正确的是
A.滴加HCl溶液的曲线为I B.水的电离程度:c>b>a
C.d点时,lg ≈5.24 D.c点溶液中存在:c(Na+)=2[c(A-)+c(HA)]
18.(河北省石家庄市第二中学2021-2022学年高三上学期11月第一次考试化学试题)已知:CHNH 、
3 2
HBO 分别为一元弱碱和一元弱酸,二者在水中电离方程式分别为:CHNH +H O CHNH +OH-;
3 3 3 2 2 3
HBO+H O [B(OH) ]-+H+。25℃时,将10mL浓度均为1mol/L的CHNH 、HBO 两种溶液分别加水稀
3 3 2 4 3 2 3 3
释曲线如图所示,V是溶液体积(mL)。 pOH=-lg c(OH-)。下列说法正确的是
A.10 mL1 mol/L的CHNH 、HBO 两种溶液的中和能力:CHNH =H BO
3 2 3 3 3 2 3 3
B.lgV=1时,水的电离程度:CHNH =H BO
3 2 3 3
C.常温下,向上述 pOH=9的HBO 溶液加入等体积pH=9的NaOH溶液后呈中性
3 3
D.lgV=4时,溶液中的阴、阳离子总浓度:HBO>CHNH
3 3 3 2
19.已知某温度下, 。向 浓度均为 的盐酸和醋酸
的混合溶液中逐滴加入 的氨水,测定过程中电导率和 变化曲线如图所示,下列说法正确的是A. 点溶液中, 约为
B. 、 、 、 四点溶液中, 点溶液中水的电离程度最大
C. 点溶液中,
D. 点溶液中
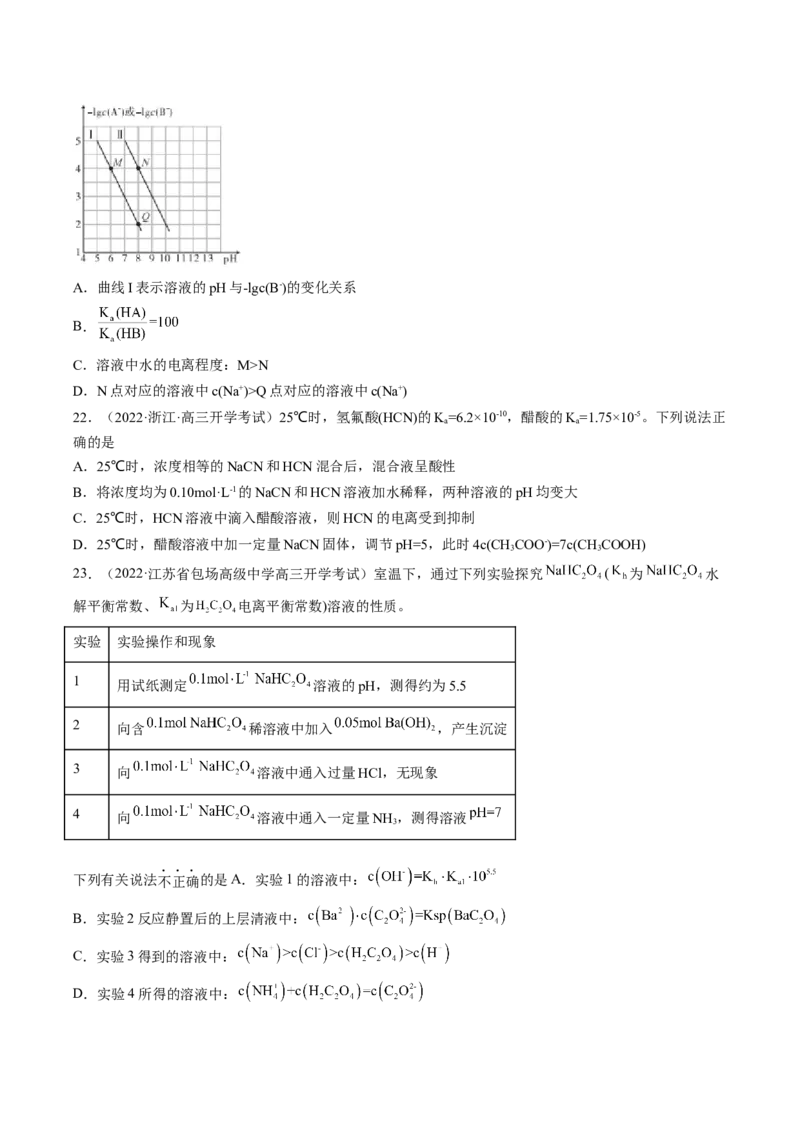
20.草酸HC O 是二元弱酸。向100mL0.40mol/LH C O 溶液中加入1.0mol/LNaOH溶液调节pH,加水控
2 2 4 2 2 4
制溶液体积为200mL。测得溶液中微粒的δ(x)随pH变化曲线如图所示,
δ(x)= ,x代表微粒HC O、 或C O 。下列叙述不正确的是
2 2 4 2
A.曲线II是 的变化曲线
B.草酸HC O 的电离常数K =1.0×10-1.22
2 2 4 1
C.在b点,3c(C O )+c(OH-)=c(Na+)+c(H+)
2
D.在c点,c( )=0.6mol/L
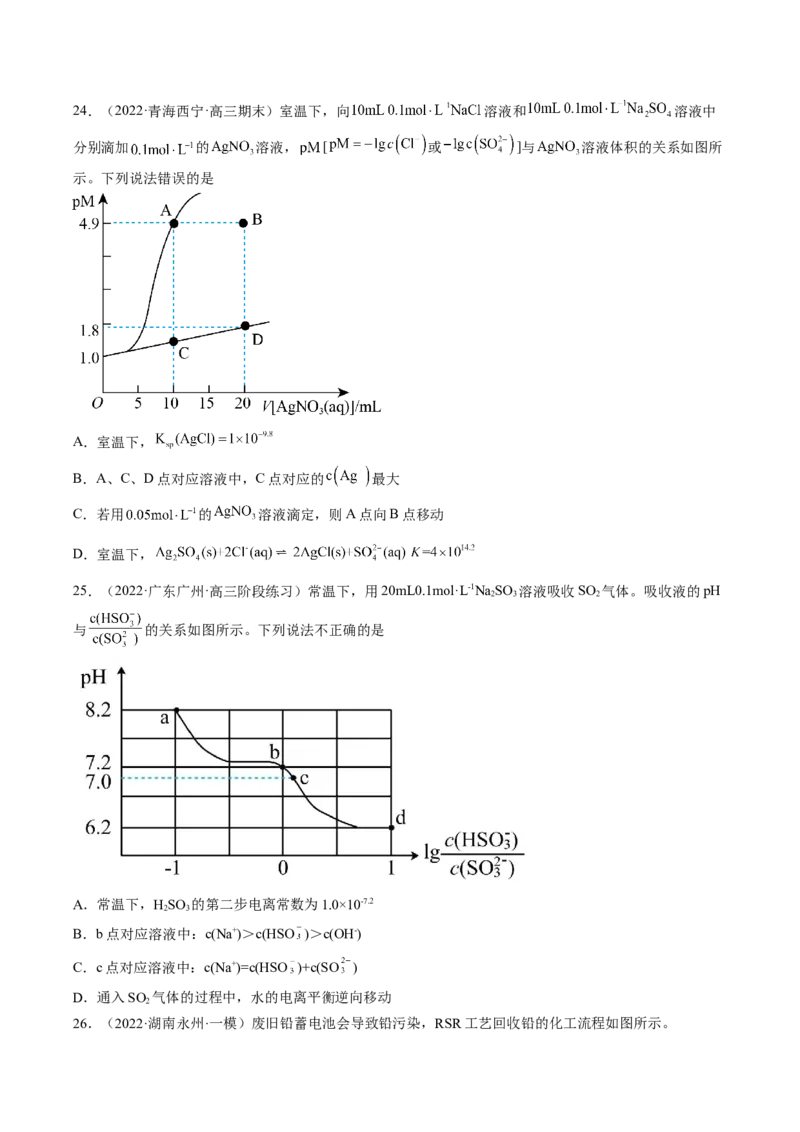
21.已知HA的酸性强于HB的酸性。25℃时,用NaOH固体分别改变物质的量浓度均为0.1mol∙L-l的HA
溶液和HB溶液的pH(溶液的体积变化忽略不计),溶液中A-、B-的物质的量浓度的负对数与溶液的pH的
变化情况如图所示。下列说法正确的是A.曲线I表示溶液的pH与-lgc(B-)的变化关系
B.
C.溶液中水的电离程度:M>N
D.N点对应的溶液中c(Na+)>Q点对应的溶液中c(Na+)
22.(2022·浙江·高三开学考试)25℃时,氢氟酸(HCN)的K=6.2×10-10,醋酸的K=1.75×10-5。下列说法正
a a
确的是
A.25℃时,浓度相等的NaCN和HCN混合后,混合液呈酸性
B.将浓度均为0.10mol·L-1的NaCN和HCN溶液加水稀释,两种溶液的pH均变大
C.25℃时,HCN溶液中滴入醋酸溶液,则HCN的电离受到抑制
D.25℃时,醋酸溶液中加一定量NaCN固体,调节pH=5,此时4c(CHCOO-)=7c(CH COOH)
3 3
23.(2022·江苏省包场高级中学高三开学考试)室温下,通过下列实验探究 ( 为 水
解平衡常数、 为 电离平衡常数)溶液的性质。
实验 实验操作和现象
1 用试纸测定 溶液的pH,测得约为5.5
2 向含 稀溶液中加入 ,产生沉淀
3 向 溶液中通入过量HCl,无现象
4 向 溶液中通入一定量NH ,测得溶液
3
下列有关说法不正确的是A.实验1的溶液中:
B.实验2反应静置后的上层清液中:
C.实验3得到的溶液中:
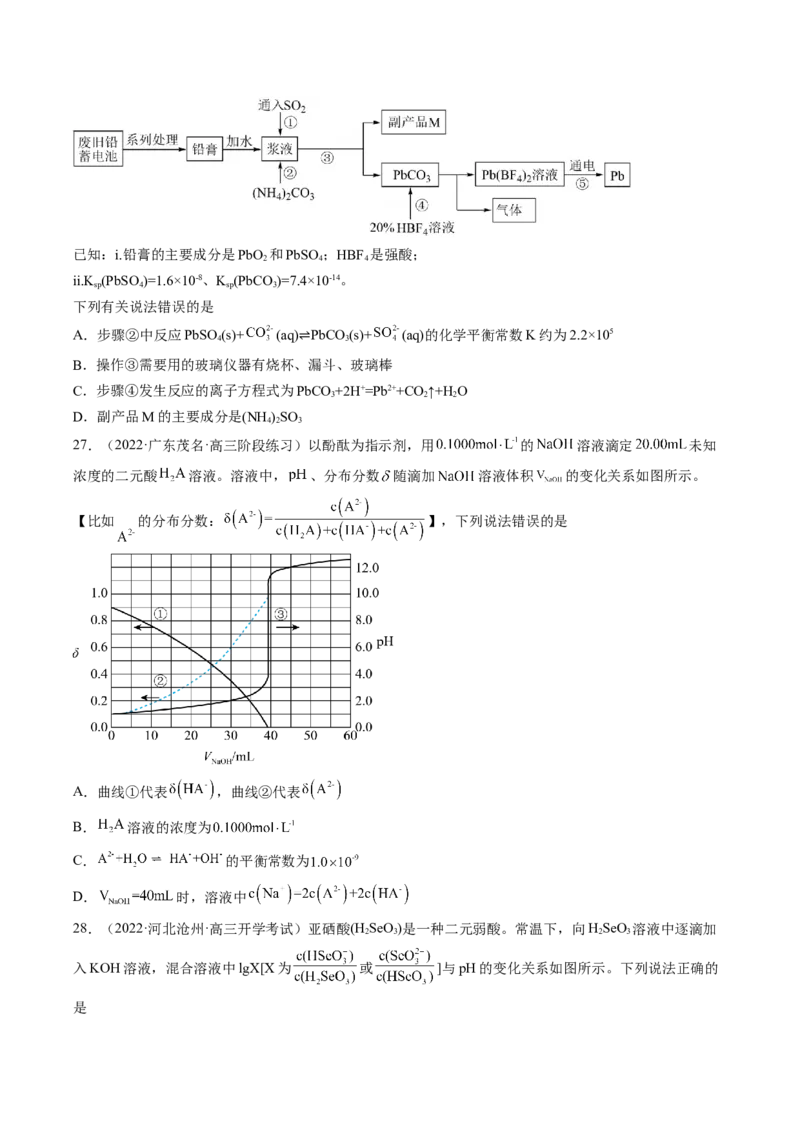
D.实验4所得的溶液中:24.(2022·青海西宁·高三期末)室温下,向 溶液和 溶液中
分别滴加 的 溶液, [ 或 ]与 溶液体积的关系如图所
示。下列说法错误的是
A.室温下,
B.A、C、D点对应溶液中,C点对应的 最大
C.若用 的 溶液滴定,则A点向B点移动
D.室温下,
25.(2022·广东广州·高三阶段练习)常温下,用20mL0.1mol·L-1NaSO 溶液吸收SO 气体。吸收液的pH
2 3 2
与 的关系如图所示。下列说法不正确的是
A.常温下,HSO 的第二步电离常数为1.0×10-7.2
2 3
B.b点对应溶液中:c(Na+)>c(HSO )>c(OH-)
C.c点对应溶液中:c(Na+)=c(HSO )+c(SO )
D.通入SO 气体的过程中,水的电离平衡逆向移动
2
26.(2022·湖南永州·一模)废旧铅蓄电池会导致铅污染,RSR工艺回收铅的化工流程如图所示。已知:i.铅膏的主要成分是PbO 和PbSO ;HBF 是强酸;
2 4 4
ii.K (PbSO )=1.6×10-8、K (PbCO )=7.4×10-14。
sp 4 sp 3
下列有关说法错误的是
A.步骤②中反应PbSO (s)+ (aq) PbCO (s)+ (aq)的化学平衡常数K约为2.2×105
4 3
B.操作③需要用的玻璃仪器有烧杯、⇌漏斗、玻璃棒
C.步骤④发生反应的离子方程式为PbCO +2H+=Pb2++CO ↑+H O
3 2 2
D.副产品M的主要成分是(NH )SO
4 2 3
27.(2022·广东茂名·高三阶段练习)以酚酞为指示剂,用 的 溶液滴定 未知
浓度的二元酸 溶液。溶液中, 、分布分数 随滴加 溶液体积 的变化关系如图所示。
【比如 的分布分数: 】,下列说法错误的是
A.曲线①代表 ,曲线②代表
B. 溶液的浓度为
C. 的平衡常数为
D. 时,溶液中
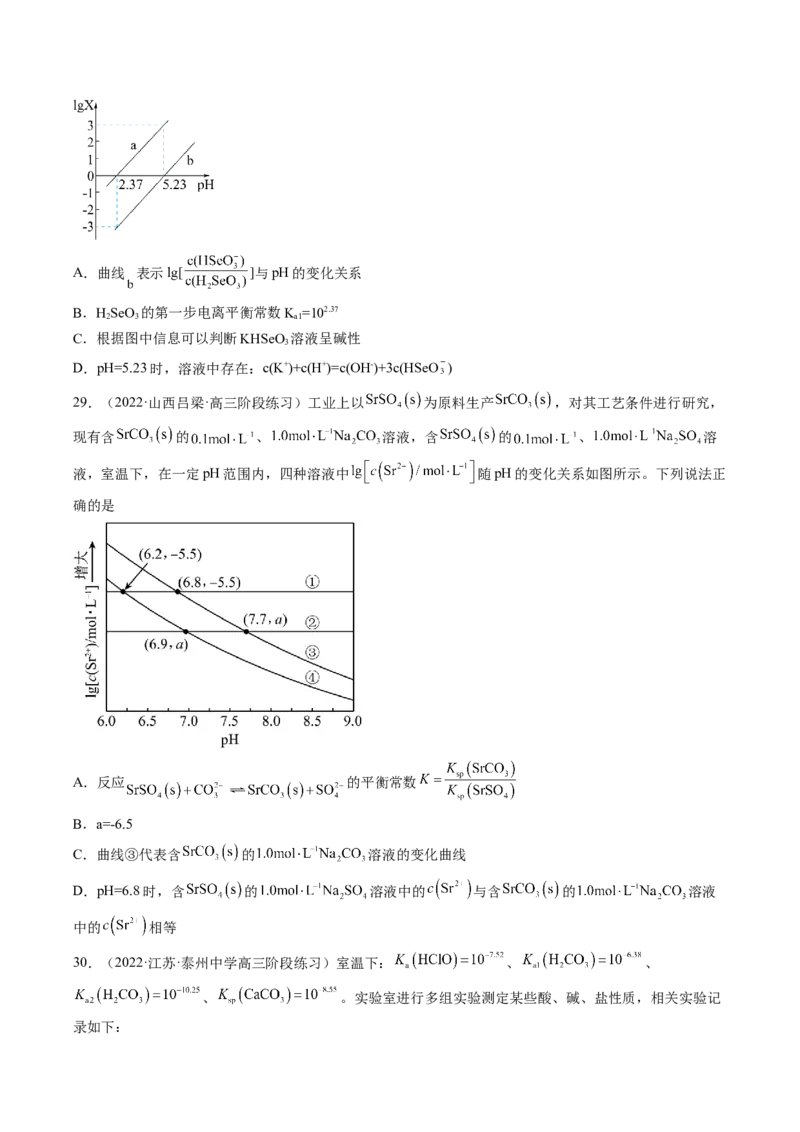
28.(2022·河北沧州·高三开学考试)亚硒酸(H SeO)是一种二元弱酸。常温下,向HSeO 溶液中逐滴加
2 3 2 3
入KOH溶液,混合溶液中lgX[X为 或 ]与pH的变化关系如图所示。下列说法正确的
是A.曲线 表示lg[ ]与pH的变化关系
B.HSeO 的第一步电离平衡常数K =102.37
2 3 a1
C.根据图中信息可以判断KHSeO 溶液呈碱性
3
D.pH=5.23时,溶液中存在:c(K+)+c(H+)=c(OH-)+3c(HSeO )
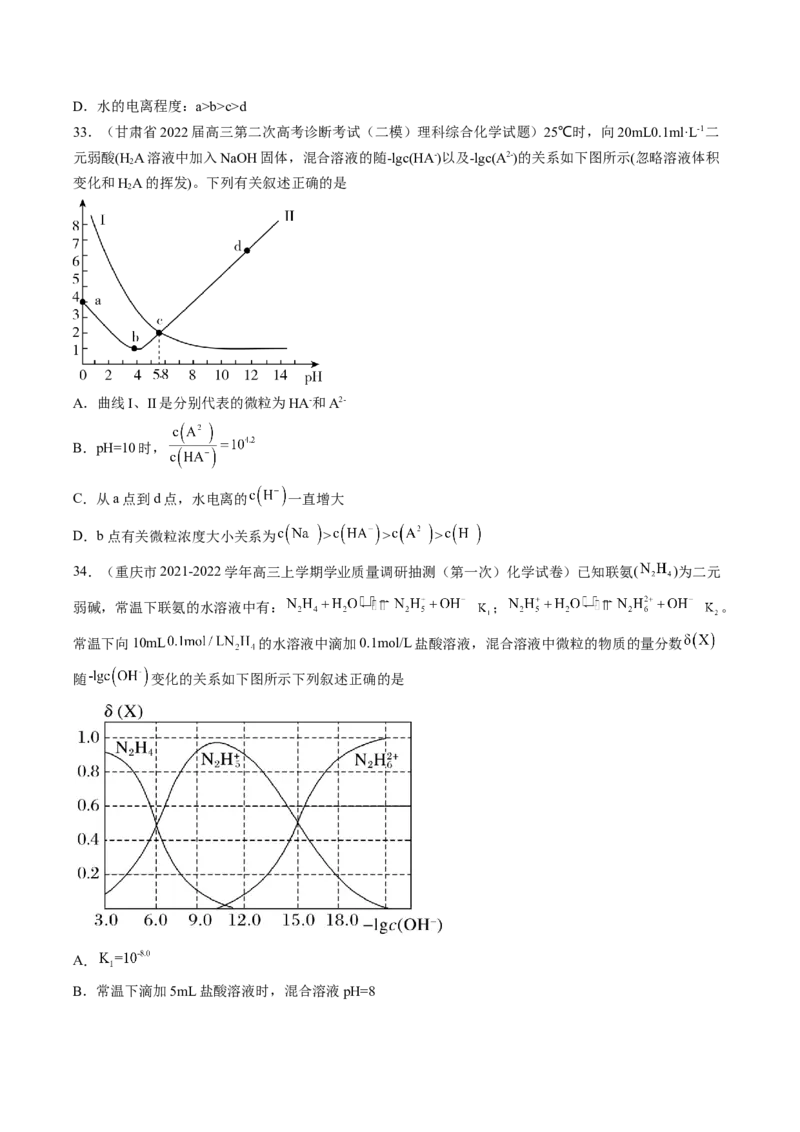
29.(2022·山西吕梁·高三阶段练习)工业上以 为原料生产 ,对其工艺条件进行研究,
现有含 的 、 溶液,含 的 、 溶
液,室温下,在一定pH范围内,四种溶液中 随pH的变化关系如图所示。下列说法正
确的是
A.反应 的平衡常数
B.a=-6.5
C.曲线③代表含 的 溶液的变化曲线
D.pH=6.8时,含 的 溶液中的 与含 的 溶液
中的 相等
30.(2022·江苏·泰州中学高三阶段练习)室温下: 、 、
、 。实验室进行多组实验测定某些酸、碱、盐性质,相关实验记
录如下:实
实验操作和现象
验
1 测定 溶液的pH约为8
2 测定 HCN与 NaOH溶液等体积混合,测得混合溶液的pH>7
3 向NaClO溶液中通入少量的 ,测得pH降低
4
向 溶液中加入等体积 溶液,产生白色沉淀
下列所得结论正确的是A.实验1溶液中存在:
B.由实验2可得
C.实验3反应的离子方程式:
D.实验4所得上层清液中的
31.(2022·浙江·高三阶段练习) 时, ,下列说法不正确的是
A. 时, 溶液中加入少量 (恢复到原温度),水的电离程度减小
B.将浓度均为 的 和 溶液加热,两种溶液的 均变大
C.相同温度下,等 的 和 溶液中,
D. 时 的 和 的混合溶液中,
32.(重庆市主城区2022届高三第二次学业教学质量抽测化学试题)我国硒含量居世界首位,HSeO 为
2 3
二元弱酸溶液,25°C时,用0.1mol·L-1 NaOH溶液滴定20mL 0.1mol·L-1 HSeO 溶液的滴定曲线如图所示
2 3
(已知:25°C时,pKa=-lgKa,HSeO 的pK =1.34,pK =7.34)
2 3 a1 a2
下列说法正确的是
A.a点对应消耗NaOH溶液的体积为10mL
B.b点溶液中:c(H SeO)>c(SeO )
2 3
C.c点溶液中:c(Na+)+c(H+)=3c(HSeO )+c(OH-)D.水的电离程度:a>b>c>d
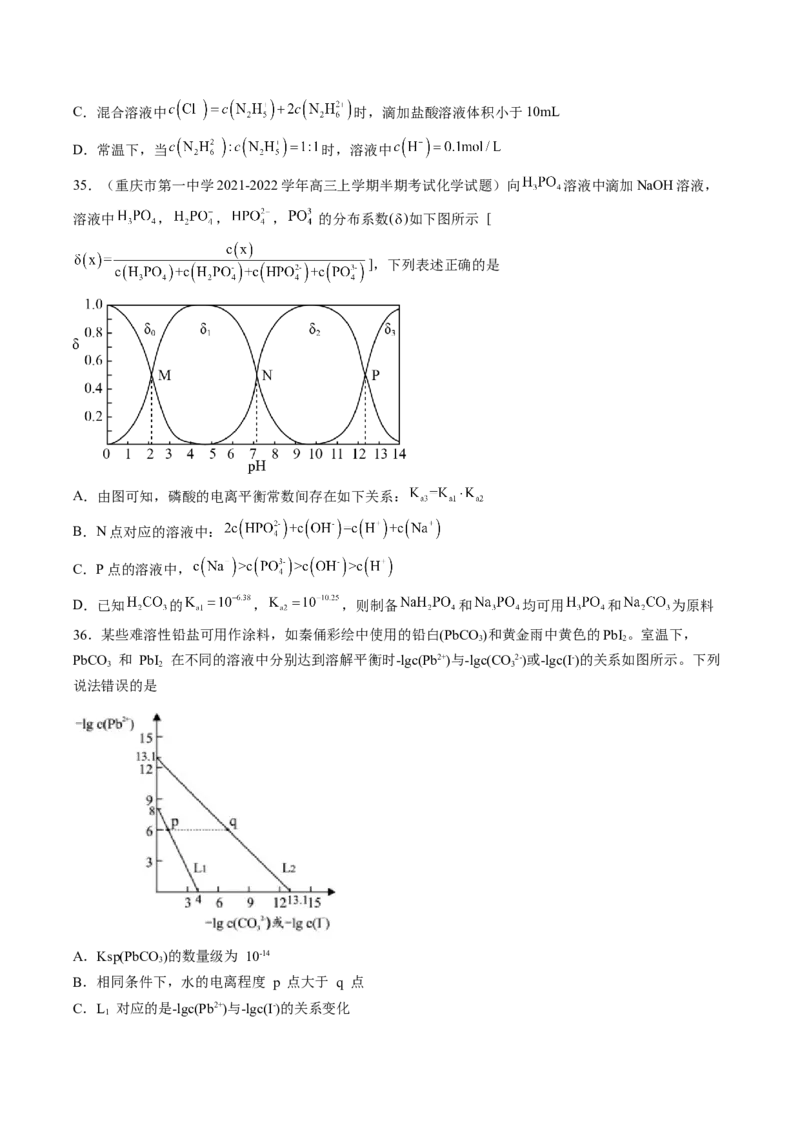
33.(甘肃省2022届高三第二次高考诊断考试(二模)理科综合化学试题)25℃时,向20mL0.1ml·L-1二
元弱酸(H A溶液中加入NaOH固体,混合溶液的随-lgc(HA-)以及-lgc(A2-)的关系如下图所示(忽略溶液体积
2
变化和HA的挥发)。下列有关叙述正确的是
2
A.曲线I、II是分别代表的微粒为HA-和A2-
B.pH=10时,
C.从a点到d点,水电离的 一直增大
D.b点有关微粒浓度大小关系为 > > >
34.(重庆市2021-2022学年高三上学期学业质量调研抽测(第一次)化学试卷)已知联氨( )为二元
弱碱,常温下联氨的水溶液中有: ; 。
常温下向10mL 的水溶液中滴加0.1mol/L盐酸溶液,混合溶液中微粒的物质的量分数
随 变化的关系如下图所示下列叙述正确的是
A.
B.常温下滴加5mL盐酸溶液时,混合溶液pH=8C.混合溶液中 时,滴加盐酸溶液体积小于10mL
D.常温下,当 时,溶液中
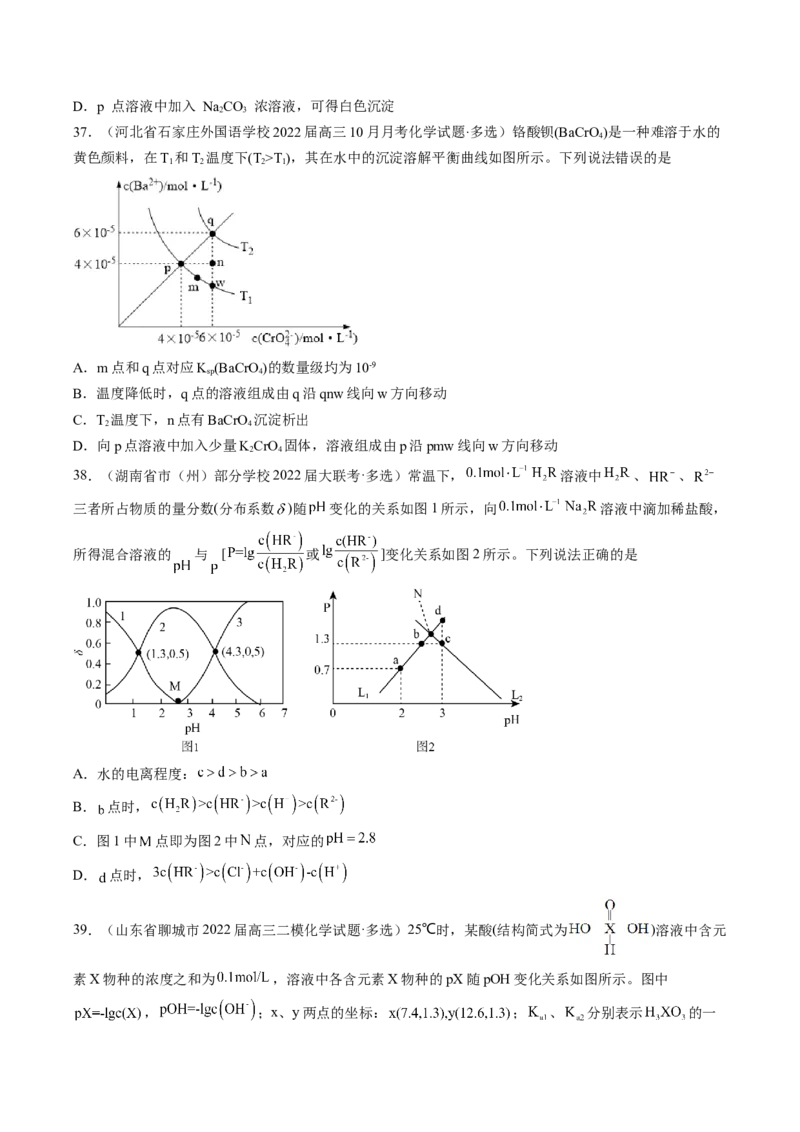
35.(重庆市第一中学2021-2022学年高三上学期半期考试化学试题)向 溶液中滴加NaOH溶液,
溶液中 , , , 的分布系数( )如下图所示 [
],下列表述正确的是
A.由图可知,磷酸的电离平衡常数间存在如下关系:
B.N点对应的溶液中:
C.P点的溶液中,
D.已知 的 , ,则制备 和 均可用 和 为原料
36.某些难溶性铅盐可用作涂料,如秦俑彩绘中使用的铅白(PbCO )和黄金雨中黄色的PbI 。室温下,
3 2
PbCO 和 PbI 在不同的溶液中分别达到溶解平衡时-lgc(Pb2+)与-lgc(CO 2-)或-lgc(I-)的关系如图所示。下列
3 2 3
说法错误的是
A.Ksp(PbCO )的数量级为 10-14
3
B.相同条件下,水的电离程度 p 点大于 q 点
C.L 对应的是-lgc(Pb2+)与-lgc(I-)的关系变化
1D.p 点溶液中加入 NaCO 浓溶液,可得白色沉淀
2 3
37.(河北省石家庄外国语学校2022届高三10月月考化学试题·多选)铬酸钡(BaCrO)是一种难溶于水的
4
黄色颜料,在T 和T 温度下(T >T),其在水中的沉淀溶解平衡曲线如图所示。下列说法错误的是
1 2 2 1
A.m点和q点对应K (BaCrO)的数量级圴为10-9
sp 4
B.温度降低时,q点的溶液组成由q沿qnw线向w方向移动
C.T 温度下,n点有BaCrO 沉淀析出
2 4
D.向p点溶液中加入少量KCrO 固体,溶液组成由p沿pmw线向w方向移动
2 4
38.(湖南省市(州)部分学校2022届大联考·多选)常温下, 溶液中 、 、
三者所占物质的量分数(分布系数 )随 变化的关系如图1所示,向 溶液中滴加稀盐酸,
所得混合溶液的 与 [ 或 ]变化关系如图2所示。下列说法正确的是
A.水的电离程度:
B. 点时,
C.图1中 点即为图2中 点,对应的
D. 点时,
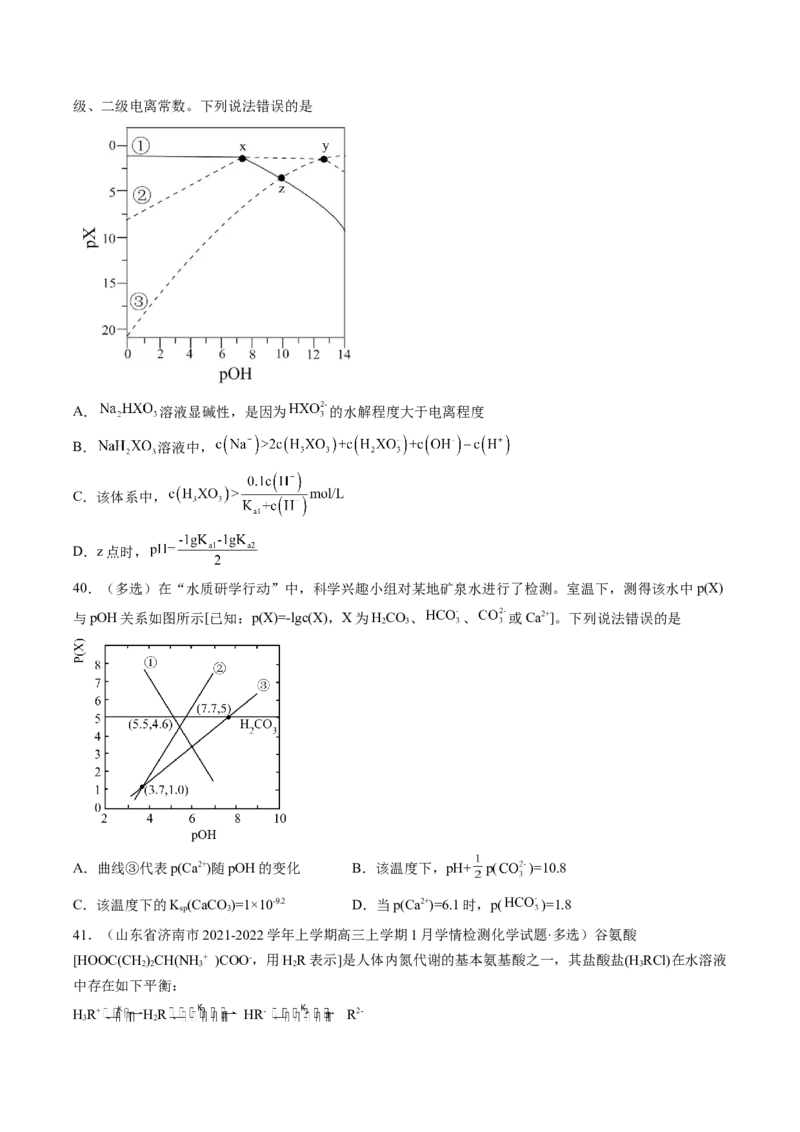
39.(山东省聊城市2022届高三二模化学试题·多选)25℃时,某酸(结构简式为 )溶液中含元
素X物种的浓度之和为 ,溶液中各含元素X物种的pX随pOH变化关系如图所示。图中
, ;x、y两点的坐标: ; 、 分别表示 的一级、二级电离常数。下列说法错误的是
A. 溶液显碱性,是因为 的水解程度大于电离程度
B. 溶液中,
C.该体系中,
D.z点时,
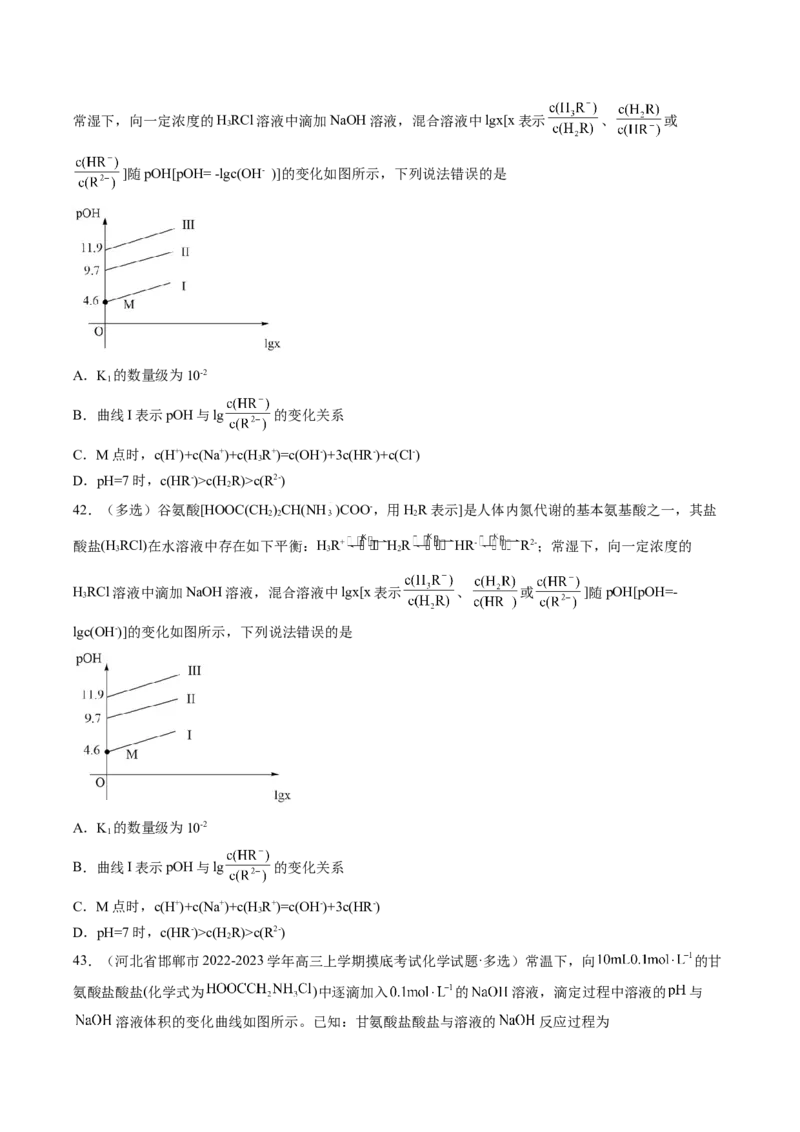
40.(多选)在“水质研学行动”中,科学兴趣小组对某地矿泉水进行了检测。室温下,测得该水中p(X)
与pOH关系如图所示[已知:p(X)=-lgc(X),X为HCO、 、 或Ca2+]。下列说法错误的是
2 3
A.曲线③代表p(Ca2+)随pOH的变化 B.该温度下,pH+ p( )=10.8
C.该温度下的K (CaCO)=1×10-9.2 D.当p(Ca2+)=6.1时,p( )=1.8
sp 3
41.(山东省济南市2021-2022学年上学期高三上学期1月学情检测化学试题·多选)谷氨酸
[HOOC(CH )CH(NH+ )COO-,用HR表示]是人体内氮代谢的基本氨基酸之一,其盐酸盐(H RCl)在水溶液
2 2 3 2 3
中存在如下平衡:
HR+ HR HR- R2-
3 2常湿下,向一定浓度的HRCl溶液中滴加NaOH溶液,混合溶液中lgx[x表示 、 或
3
]随pOH[pOH= -lgc(OH- )]的变化如图所示,下列说法错误的是
A.K 的数量级为10-2
1
B.曲线I表示pOH与lg 的变化关系
C.M点时,c(H+)+c(Na+)+c(H R+)=c(OH-)+3c(HR-)+c(Cl-)
3
D.pH=7时,c(HR-)>c(H R)>c(R2-)
2
42.(多选)谷氨酸[HOOC(CH )CH(NH )COO-,用HR表示]是人体内氮代谢的基本氨基酸之一,其盐
2 2 2
酸盐(H RCl)在水溶液中存在如下平衡:HR+ HR HR- R2-;常湿下,向一定浓度的
3 3 2
HRCl溶液中滴加NaOH溶液,混合溶液中lgx[x表示 、 或 ]随pOH[pOH=-
3
lgc(OH-)]的变化如图所示,下列说法错误的是
A.K 的数量级为10-2
1
B.曲线I表示pOH与lg 的变化关系
C.M点时,c(H+)+c(Na+)+c(H R+)=c(OH-)+3c(HR-)
3
D.pH=7时,c(HR-)>c(H R)>c(R2-)
2
43.(河北省邯郸市2022-2023学年高三上学期摸底考试化学试题·多选)常温下,向 的甘
氨酸盐酸盐(化学式为 )中逐滴加入 的 溶液,滴定过程中溶液的 与
溶液体积的变化曲线如图所示。已知:甘氨酸盐酸盐与溶液的 反应过程为,下列有关说法错误的是
A. 的电离平衡常数的数量级为
B. 溶液显酸性
C. 时,
D. 时,溶液满足