文档内容
第六篇 物质结构与性质
专项 42 晶胞确定化学式
由晶胞确定化学式是《物质结构与性质》必考知识,一般出现于晶胞的计算之中。晶体中微粒的排列
具有周期性,晶体中最小的结构重复单元称为晶胞,利用“均摊法”可以计算一个晶胞中的粒子数,从而
确定晶体的化学式。
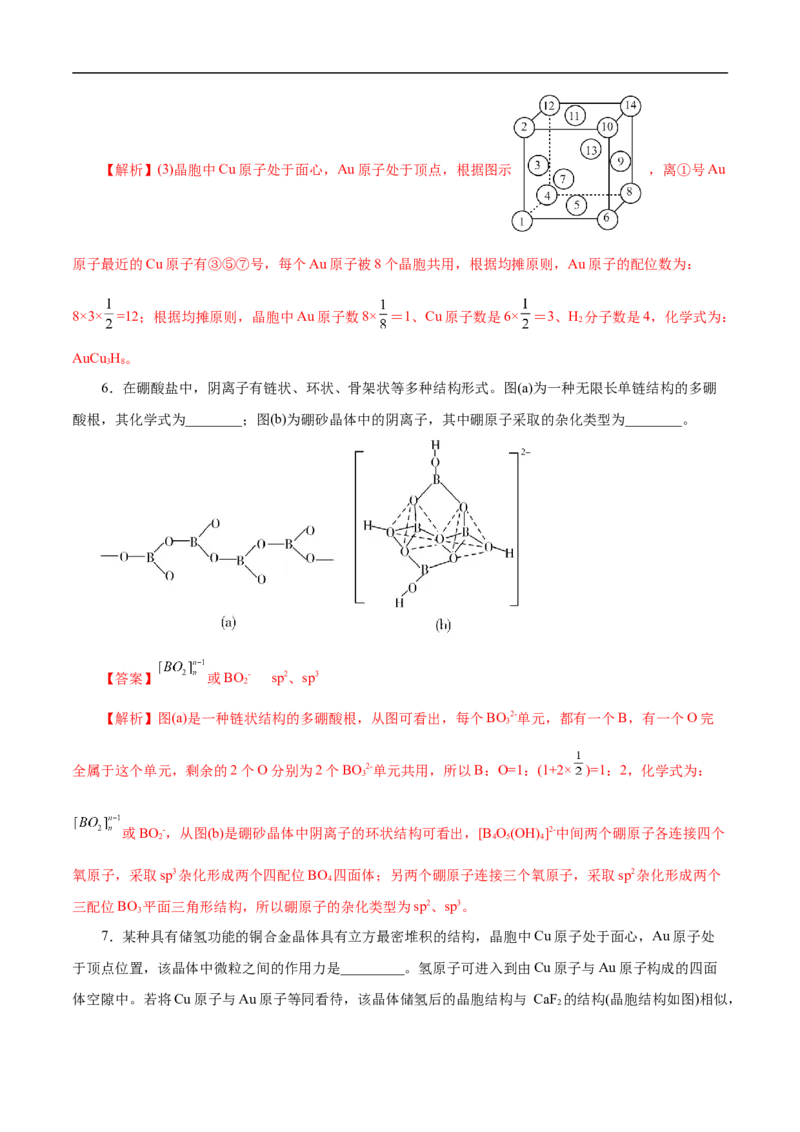
1.(2022•湖北省选择性考试)某立方卤化物可用于制作光电材料,其晶胞结构如图所示。下列说法错
误的是( )
A.Ca2+的配位数为6 B.与 距离最近的是K+
C.该物质的化学式为KCaF D.若 换为Cl-,则晶胞棱长将改变
3
【答案】B
【解析】A项,Ca2+配位数为与其距离最近且等距离的F-的个数,如图所示,Ca2+位于体心,F-位于面
心,所以Ca2+配位数为6,A正确;B项,F-与K+的最近距离为棱长的 ,F-与Ca2+的最近距离为棱长的
,所以与F-距离最近的是Ca2+,B错误;C项,K+位于顶点,所以K+个数= =1,F-位于面心,F-个数= =3,Ca2+位于体心,所以Ca2+个数=1,综上,该物质的化学式为KCaF ,C正确;D项,F-与Cl-半径
3
不同,替换后晶胞棱长将改变,D正确;故选B。
2.(2021•辽宁选择性考试)单质硫和氢气在低温高压下可形成一种新型超导材料,其晶胞如图。下列
说法错误的是( )
A.S位于元素周期表p区 B.该物质的化学式为HS
3
C.S位于H构成的八面体空隙中 D.该晶体属于分子晶体
【答案】D
【解析】A项,S的价电子排布式为:3s23p4,故S位于元素周期表p区,A正确;B项,由该物质形
成晶体的晶胞可知:S个数为8×+1=2,H个数为:12×+6×=6,故H、S原子个数比为3:1,故该物质的化
学式为HS,B正确;C项,S位于H构成的八面体空隙中,如图所示 ,C正确;D项,
3
由于该晶体是一种新型超导材料,说明其是由阴、阳离子构成的,故该晶体属于离子晶体,D错误;故选
D。
3.(2021•湖南选择性考试节选)如图是Mg、Ge、O三种元素形成的某化合物的晶胞示意图。①已知化合物中Ge和O的原子个数比为1:4,图中Z表示 原子(填元素符号),
该化合物的化学式为 ;
②已知该晶胞的晶胞参数分别为 anm、bnm、cnm,α=β=γ=90°,则该晶体的密度 ρ=
g•cm﹣3(设阿伏加德罗常数的值为N ,用含a、b、c、N 的代数式表示)。
A A
【答案】①O Mg GeO ② ×1021
2 4
【解析】①根据如图所示晶胞,根据均摊法,Z球位于晶胞内,位于晶胞的内部,含有 4+4+4+4=16
个;Y球有4个位于晶胞内,X球位于顶点的有8个,位于4条棱心的有4个,上下面心上各有2个,晶胞
1 1 1
内有5个,则晶胞中共含有的 X为8× +4× +4× +5=8个;已知化合物中Ge和O的原子个数比为
8 4 2
1:4,则为1:4比例的为X:Z,所以图中Z表示O原子,Y表示Ge原子,X表示Mg原子,则该化合物
的 化 学 式 为 MgGeO ; ② 晶 胞 的 总 质 量 为 m
2 4
4×70g⋅mol−1+8×24g⋅mol−1+16×16g⋅mol−1 728g,晶胞的体积为 V=abcnm3=abc×10﹣
= =
N mol−1 N
A A
21cm3,代入根据晶体的密度ρ= m
=
728g 。
V N ⋅abc×10−21cm3
A
1.晶胞中微粒数目的计算方法——均摊法找晶胞中的微粒数时,要找到这个晶胞中处于不同位置(顶定、棱上、面上、体内)的粒子数,然后确
定这些不同位置的粒子(以该粒子为中心)确定周围有多少个晶胞来分摊它,从而确定这些不同位置上的粒
子所需要乘的分摊系数,最后把这些乘了分摊系数的不同位置的粒子数加起来。
2.熟记几种常见的晶胞结构及晶胞含有的粒子数目
A.NaCl(含4个Na+,4个Cl-) B.干冰(含4个CO)
2
C.CaF (含4个Ca2+,8个F-) D.金刚石(含8个C)
2
E.体心立方(含2个原子) F.面心立方(含4个原子)
3.晶体中化学式计算思路
(1)运用均摊法计算出一个晶胞中的微粒数目。
(2)求出不同微粒数目的比较,得化学式。
4.晶胞中粒子配位数的计算
一个粒子周围最邻近的粒子的数目称为配位数。
(1)晶体中原子(或分子)的配位数:若晶体中的微粒为同种原子或同种分子,则某原子(或分子)的配位数
指的是该原子(或分子)最近且等距离的原(或分子)的数目。
(2)离子晶体的配位数:指一个离子周围最接近且等距离的异种电性离子的数目。1.(2022·辽宁·抚顺市第二中学高三模拟)由金、氯、铯三种元素组成的晶体M的晶胞结构如图所示(
为铯, 为氯, 为金),其中金原子有两种不同的化学环境,形成2种−1价的配离子。设阿伏加德罗常数
的值为N ,下列说法错误的是( )
A
A.M的化学式为CsAuCl
B.金原子形成的两种配离子分别为AuCl -、AuCl -
2 4
C.位于体心的Au处于由Au构成的八面体空隙中
D.金晶体(Au)是面心立方堆积,其晶胞参数为408pm,金晶体密度为 g∙cm−3
【答案】A
【解析】A项,根据晶胞结构知,金和氯形成的2种配离子分别为AuCl -、AuCl -,金元素分别显+1
2 4
价和+3价,1个晶胞中有8个AuCl -位于顶点和1个AuCl -位于体内,则AuCl 个数 ,4个
4 4
AuCl -位于棱上,2个AuCl -位于面心,AuCl -个数 ,8个Cs位于面上,则Cs有4个,因此
2 2 2
M的化学式为CsAuCl ,故A错误;B项,根据图中信息金原子形成的两种配离子分别为AuCl -、AuCl -,
3 2 4
故B正确;C项,由晶胞结构可知位于体心的Au周围有6个Au,这6个Au构成八面体,则位于体心的
Au处于由Au构成的八面体空隙中,故C正确;D项,金晶体(Au)是面心立方堆积,所以每个晶胞中含有
金原子个数为 ,其晶胞参数为408pm,金晶体密度为,故D正确。故选A。
2.已知NiMg O晶体属立方晶系,晶胞边长a。将Li+掺杂到该晶胞中,可得到一种高性能的p型太
x 1-x
阳能电池材料,其结构单元如图所示。假定掺杂后的晶胞参数不发生变化,下列说法正确的是( )。
A.该结构单元中O原子数为3
√2
B.Ni和Mg间最短距离是 a
2
C.Ni的配位数为4
D.该物质的化学式为Li Mg Ni O
0.5 1.12 2.38 4
【答案】B
【解析】该晶胞的棱上氧原子数是12,体心氧原子数是1,由均摊法可知,该结构单元中O原子数为
1
1+12× =4,A 项错误;由图可知,Ni 原子和 Mg 原子间的最短距离为晶胞面对角线的一半,即
4
1 √2
√(a2+a2)= a,B项正确;由晶胞结构单元可知,Ni位于晶胞顶点,Ni原子的配位数为6,C项错误;
2 2
1 1
1 个晶胞中 Li 原子的个数为 1×0.5=0.5,Mg 原子的个数为 2×0.5+1× =1.125,Ni 原子的个数为 7×
8 8
+3×0.5=2.375,O原子的个数为4,因此该物质的化学式为Li Mg Ni O,D项错误。
0.5 1.125 2.375 4
3.我国科学家合成了富集11B的非碳导热材料立方氮化硼晶体,晶胞结构如图。下列说法正确的是(
)。
A.11BN和10BN的性质无差异
B.该晶体具有良好的导电性
C.该晶胞中含有14个B原子,4个N原子D.N原子周围等距且最近的N原子数为12
【答案】D
【解析】11B和10B互为同位素,形成的化合物在化学性质上无差异,物理性质不同,A项错误;该晶
体中无自由移动的电子,不能导电,B项错误;该晶胞含4个N原子,B原子位于晶胞的顶点和面心上,
1 1
故B原子的数量为8× +6× =4个,C项错误;1个N原子与4个B原子成键,1个B原子可以和3个N原
8 2
子成键,N原子周围等距且最近的N原子数为12个,D项正确。
4.普鲁士蓝俗称铁蓝,结构如图甲所示(K+未画出),平均每两个立方体中含有一个K+,该晶体的化
学式为_______。又知该晶体中铁元素有+2价和+3价两种,则Fe3+与Fe2+的个数比为_______。
【答案】KFe (CN) 1∶1
2 6
【解析】每隔一个立方体中心有一个钾离子,所以一个晶胞中钾离子个数为: ,该立方体中铁
原子个数为: ,CN-位于每条棱中点,该立方体中含有CN-个数为: ,所以晶体化学式为
;Fe平均化合价2.5,所以亚铁离子与铁离子之比是1:1。
5.一种铜金合金具有储氢功能。其晶体为面心立方最密堆积结构,晶胞中Cu原子处于面心,Au原
子处于顶点,则Au原子的配位数为____。该储氢材料储氢时,氢分子可进入到由Cu原子与Au原子构成
的四面体空隙中。若将Cu原子与Au原子等同看待,该晶体储氢后的晶胞结构与ZnS的结构相似(如图
1),该晶体储氢后的化学式为____。
【答案】12 AuCu H
3 8【解析】(3)晶胞中Cu原子处于面心,Au原子处于顶点,根据图示 ,离①号Au
原子最近的Cu原子有③⑤⑦号,每个Au原子被8个晶胞共用,根据均摊原则,Au原子的配位数为:
8×3× =12;根据均摊原则,晶胞中Au原子数8× =1、Cu原子数是6× =3、H 分子数是4,化学式为:
2
AuCu H。
3 8
6.在硼酸盐中,阴离子有链状、环状、骨架状等多种结构形式。图(a)为一种无限长单链结构的多硼
酸根,其化学式为________;图(b)为硼砂晶体中的阴离子,其中硼原子采取的杂化类型为________。
【答案】 或BO- sp2、sp3
2
【解析】图(a)是一种链状结构的多硼酸根,从图可看出,每个BO2-单元,都有一个B,有一个O完
3
全属于这个单元,剩余的2个O分别为2个BO2-单元共用,所以B:O=1:(1+2× )=1:2,化学式为:
3
或BO-,从图(b)是硼砂晶体中阴离子的环状结构可看出,[B O(OH) ]2-中间两个硼原子各连接四个
2 4 5 4
氧原子,采取sp3杂化形成两个四配位BO 四面体;另两个硼原子连接三个氧原子,采取sp2杂化形成两个
4
三配位BO 平面三角形结构,所以硼原子的杂化类型为sp2、sp3。
3
7.某种具有储氢功能的铜合金晶体具有立方最密堆积的结构,晶胞中Cu原子处于面心,Au原子处
于顶点位置,该晶体中微粒之间的作用力是_________。氢原子可进入到由Cu原子与Au原子构成的四面
体空隙中。若将Cu原子与Au原子等同看待,该晶体储氢后的晶胞结构与 CaF 的结构(晶胞结构如图)相似,
2该晶体储氢后的化学式为_______________。
【答案】 金属键 Cu AuH
3 8
【解析】金属原子间形成金属键;氢原子可进入到由Cu原子与Au原子构成的四面体空隙中,则H原
子应位于晶胞内部,则应含有8个H,则化学式为Cu AuH 。
3 8
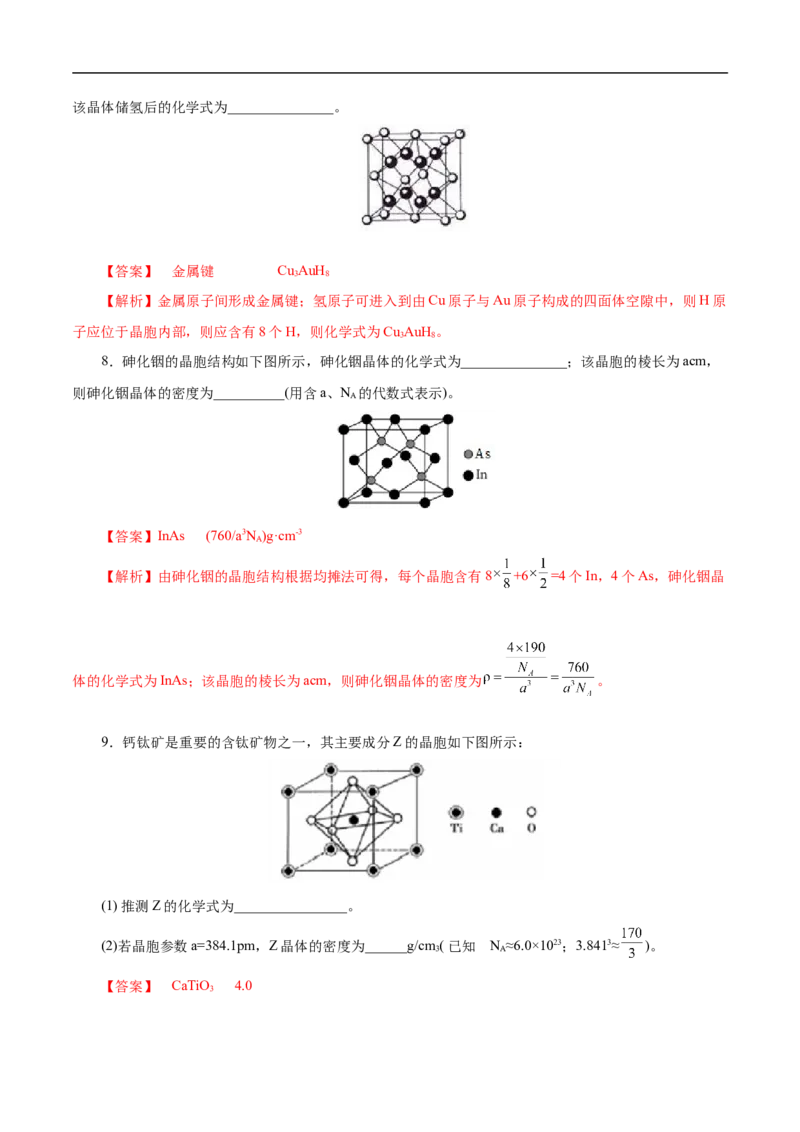
8.砷化铟的晶胞结构如下图所示,砷化铟晶体的化学式为_______________;该晶胞的棱长为acm,
则砷化铟晶体的密度为__________(用含a、N 的代数式表示)。
A
【答案】InAs (760/a3N )g·cm-3
A
【解析】由砷化铟的晶胞结构根据均摊法可得,每个晶胞含有8 +6 =4个In,4个As,砷化铟晶
体的化学式为InAs;该晶胞的棱长为acm,则砷化铟晶体的密度为 。
9.钙钛矿是重要的含钛矿物之一,其主要成分Z的晶胞如下图所示:
(1) 推测Z的化学式为________________。
(2)若晶胞参数a=384.1pm,Z晶体的密度为______g/cm( 已知 N ≈6.0×1023;3.8413≈ )。
3 A
【答案】 CaTiO 4.0
3【解析】(1)根据均摊原则,每个晶胞含有Ti原子数是 =1,含有Ca原子数1,含有O原子数是
,所Z的化学式是CaTiO ;(2)根据化学式可知Z的摩尔质量是136g/mol;晶胞的体积是
3
;则 g/cm。
3
10.一种铁氮化合物具有高磁导率,其结构如图所示:
已知:晶体的密度为 ,阿伏加德罗常数为 。该铁氮化合物的化学式为_______。;计算
Fe(Ⅱ)构成正八面体的体积为_______ 。
【答案】Fe (Ⅱ)Fe(Ⅲ)N或Fe N
3 4
【解析】一个小立方体为一个晶胞,则晶胞中N原子数目为1,Fe(Ⅱ)数目为6× =3,Fe(Ⅲ)数目为
1,故晶胞化学式为Fe (Ⅱ)Fe(Ⅲ)N或Fe N,氮化铁的化学式为Fe N,晶胞质量为 g,若晶胞的边
3 4 4
长为acm,则晶胞的密度为ρ= g•cm-3,则a3= ,Fe(Ⅱ)构成正八面体相当于2个正四棱锥,
底面为正方形,对角线为晶胞的边长并且两对角线互相垂直,S = a2cm2,正四棱锥的高为: acm,根
底据V = S h= × a2× acm3= cm3,所以八面体体积=2V =2× cm3= cm3。
锥 底 锥
11.(2023届·北京十四中高三开学考试节选)钒的某种氧化物晶胞结构如图所示(O原子2个位于体内,
4个位于面上)。该氧化物的化学式为_______,若它的晶胞棱长为x nm(假设为正六面体),则该晶体的密度
为_______ g·cm-3。(原子量:V 51,O 16; ;阿伏伽德罗常数为N )
A
【答案】VO
2
【解析】根据晶胞结构图可知,O原子2个位于体内,4个位于面上在立方晶胞的面心,V原子8个在
立方晶胞的顶点上,1个位于体心,利用均摊法可确定1个晶胞中含O原子个数: ,含有V原
子 个 数 : , 故 化 学 式 为 VO ; 该 晶 体 的 密 度 为
2
。
12.锑酸亚铁晶胞如图所示,其晶胞参数分别为anm、bnm、cnm, ,则:(1)锑酸亚铁的化学式为_______。
(2)晶体的密度为_______ (设N 为阿伏加德罗常数的值)。
A
【答案】(1) Fe(SbO ) (2)
3 2
【解析】(1)根据均摊原则,一个晶胞中含有Sb的个数为 ,含有O的个数为 ,
含有Fe的个数为 ,所以锑酸亚铁的化学式为Fe(SbO );(2)一个晶胞中含有Sb的个数为4,含
3 2
有O的个数为12,含有Fe的个数为2,晶胞的质量为 ,晶体的体积为
,所以晶体的密度为 。