文档内容
专题 05 化学能与电能的转化
内容 原电池原理及其应用 电解原理及其应用
课
1. 理解原电池的构成、工作原理及应用,能书写电极反应
标 和总反应方程式 理解电解池的构成、工
作原理及应用,能书写
解 解读 2.了解金属发生电化学腐蚀的原因、金属腐蚀的危害以及防
电极反应和总反应方程
止金属腐蚀的措施
读 式
3.了解常见化学电源的种类及其工作原理
电化学是氧化还原反应知识的应用和延伸,是热点考查内容。通常会以新型二次电
池为载体考查原电池原理与电解原理。试题难度中等,预计今后以新型电源及含有
考情分析 离子交换膜的原电池、电解池为背景,以选择题、填空题形式考查工作原理、离
子、电子移动方向、电极反应的书写和判断、电解质溶液的判断和计算、交换膜的
应用。考查考生的核心素养和探究能力。
本专题命题往往以可充电电池的工作原理及电解原理的应用为背景,考查电极反应
式的书写、离子移动方向、金属的电化学腐蚀及防护等知识。同时也对信息提取、
备考策略
应用能力进行考查。备考时要侧重原电池与电解池工作原理中基础考点的复习和电
极反应式书写技巧的掌握。
核心素养 变化观念与平衡思想 证据推理与模型认知
高频考点一 新型电池的工作原理分析
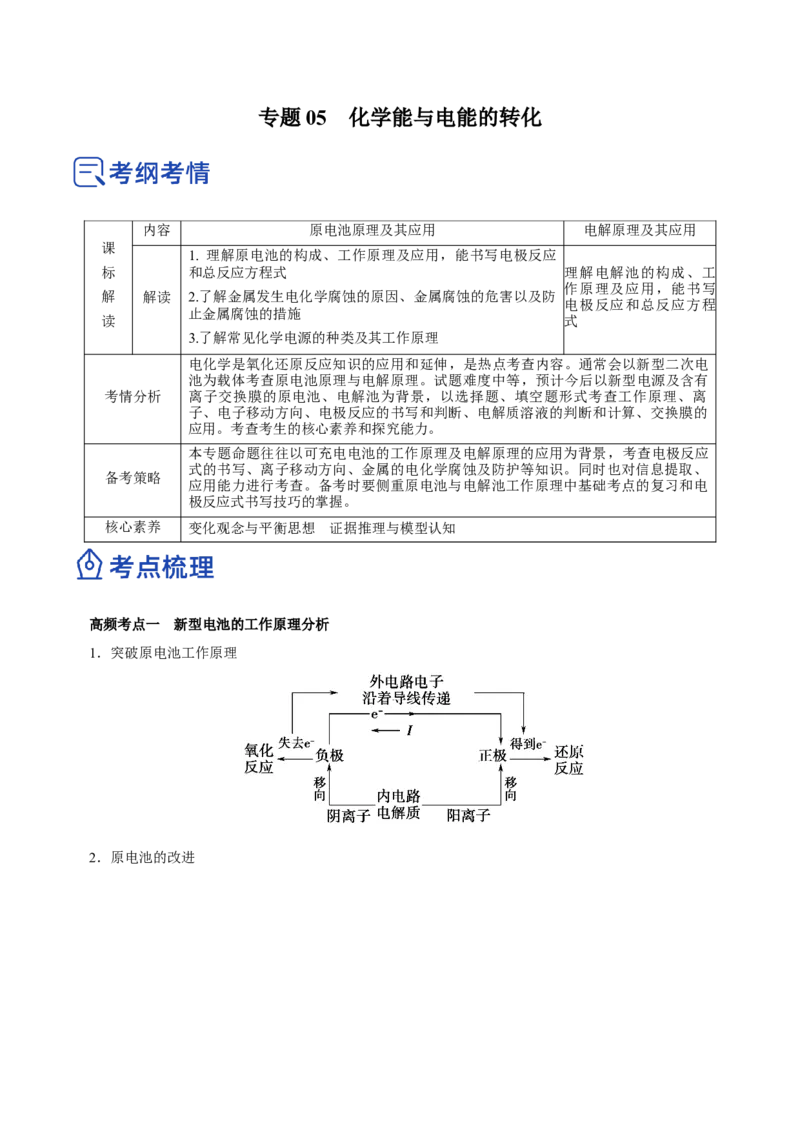
1.突破原电池工作原理
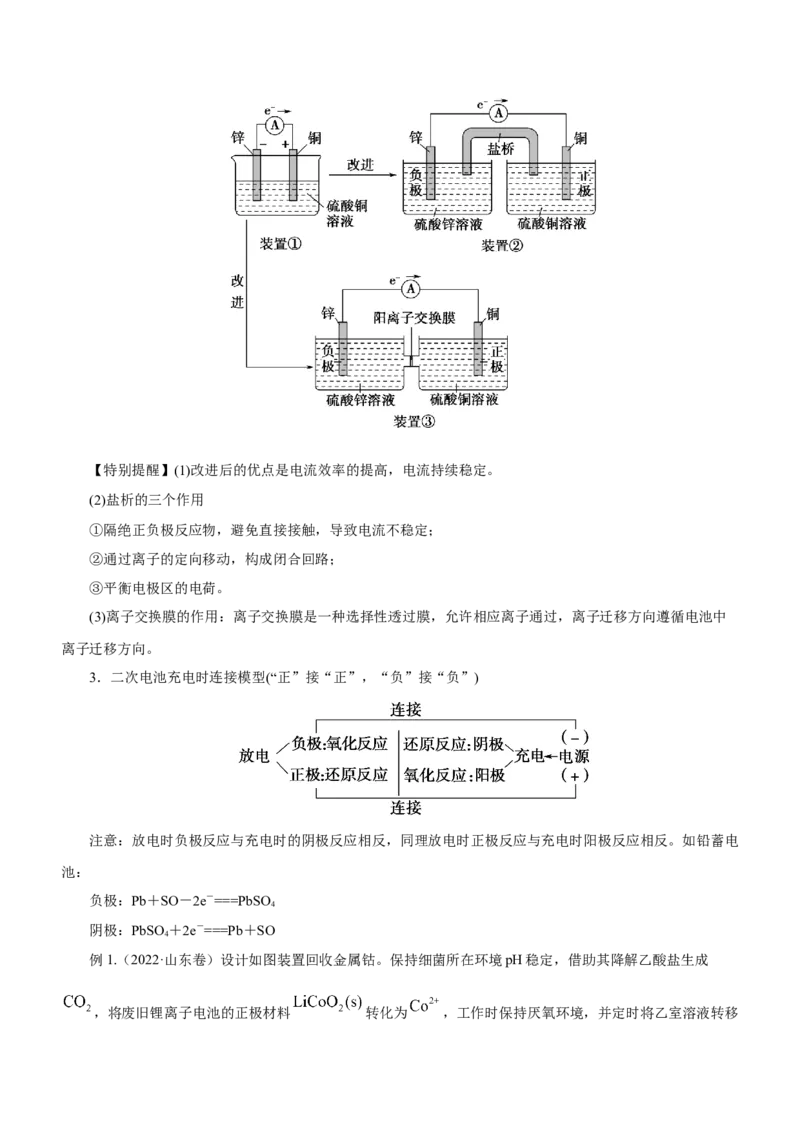
2.原电池的改进【特别提醒】(1)改进后的优点是电流效率的提高,电流持续稳定。
(2)盐析的三个作用
①隔绝正负极反应物,避免直接接触,导致电流不稳定;
②通过离子的定向移动,构成闭合回路;
③平衡电极区的电荷。
(3)离子交换膜的作用:离子交换膜是一种选择性透过膜,允许相应离子通过,离子迁移方向遵循电池中
离子迁移方向。
3.二次电池充电时连接模型(“正”接“正”,“负”接“负”)
注意:放电时负极反应与充电时的阴极反应相反,同理放电时正极反应与充电时阳极反应相反。如铅蓄电
池:
负极:Pb+SO-2e-===PbSO
4
阴极:PbSO +2e-===Pb+SO
4
例1.(2022·山东卷)设计如图装置回收金属钴。保持细菌所在环境pH稳定,借助其降解乙酸盐生成
,将废旧锂离子电池的正极材料 转化为 ,工作时保持厌氧环境,并定时将乙室溶液转移至甲室。已知电极材料均为石墨材质,右侧装置为原电池。下列说法正确的是
A. 装置工作时,甲室溶液pH逐渐增大
B. 装置工作一段时间后,乙室应补充盐酸
C. 乙室电极反应式为
D. 若甲室 减少 ,乙室 增加 ,则此时已进行过溶液转移
【答案】BD
【解析】由于乙室中两个电极的电势差比甲室大,所以乙室是原电池,甲室是电解池,然后根据原电池、
电解池反应原理分析解答。电池工作时,甲室中细菌上乙酸盐的阴离子失去电子被氧化为CO 气体,Co2+在另
2
一个电极上得到电子,被还原产生Co单质,CHCOO-失去电子后,Na+通过阳膜进入阴极室,溶液变为NaCl
3
溶液,溶液由碱性变为中性,溶液pH减小,A错误;对于乙室,正极上LiCoO 得到电子,被还原为Co2+,同
2
时得到Li+,其中的O与溶液中的H+结合HO,因此电池工作一段时间后应该补充盐酸,B正确;电解质溶液
2
为酸性,不可能大量存在OH-,乙室电极反应式为:LiCoO +e-+4H+=Li++Co2++2H O,C错误;若甲室Co2+减少
2 2
200 mg,电子转移物质的量为n(e-)= ,乙室Co2+增加300 mg,转移电子的物质的量
为n(e-)= ,说明此时已进行过溶液转移,D正确;故选BD。
【方法技巧】
(1)放电时,正、负极的判断。
(2)充、放电时两极反应式书写判断。
(3)充、放电时,电子、离子的移动方向。
(4)电极附近溶液性质的变化。
(5)充、放电两极反应类型判断。(6)充电连接判断。
(7)基本电化学计算。
【变式探究】(2022·辽宁卷)某储能电池原理如图。下列说法正确的是
A. 放电时负极反应:
B. 放电时 透过多孔活性炭电极向 中迁移
C. 放电时每转移 电子,理论上 吸收
D. 充电过程中, 溶液浓度增大
【答案】A
【解析】放电时负极反应: ,正极反应:Cl+2e-=2Cl-,消耗
2
氯气,放电时,阴离子移向负极,充电时阳极:2Cl--2e-=Cl ,由此解析 。放电时负极失电子,发生氧化反应,
2
电极反应: ,故A正确;放电时,阴离子移向负极,放电时 透
过多孔活性炭电极向NaCl中迁移,故B错误;放电时每转移 电子,正极:Cl+2e-=2Cl-,理论上 释
2
放 ,故C错误;充电过程中,阳极:2Cl--2e-=Cl ,消耗氯离子, 溶液浓度减小,故D错
2
误;故选A。
【举一反三】(2022·全国乙卷) 电池比能量高,在汽车、航天等领域具有良好的应用前景。近年来
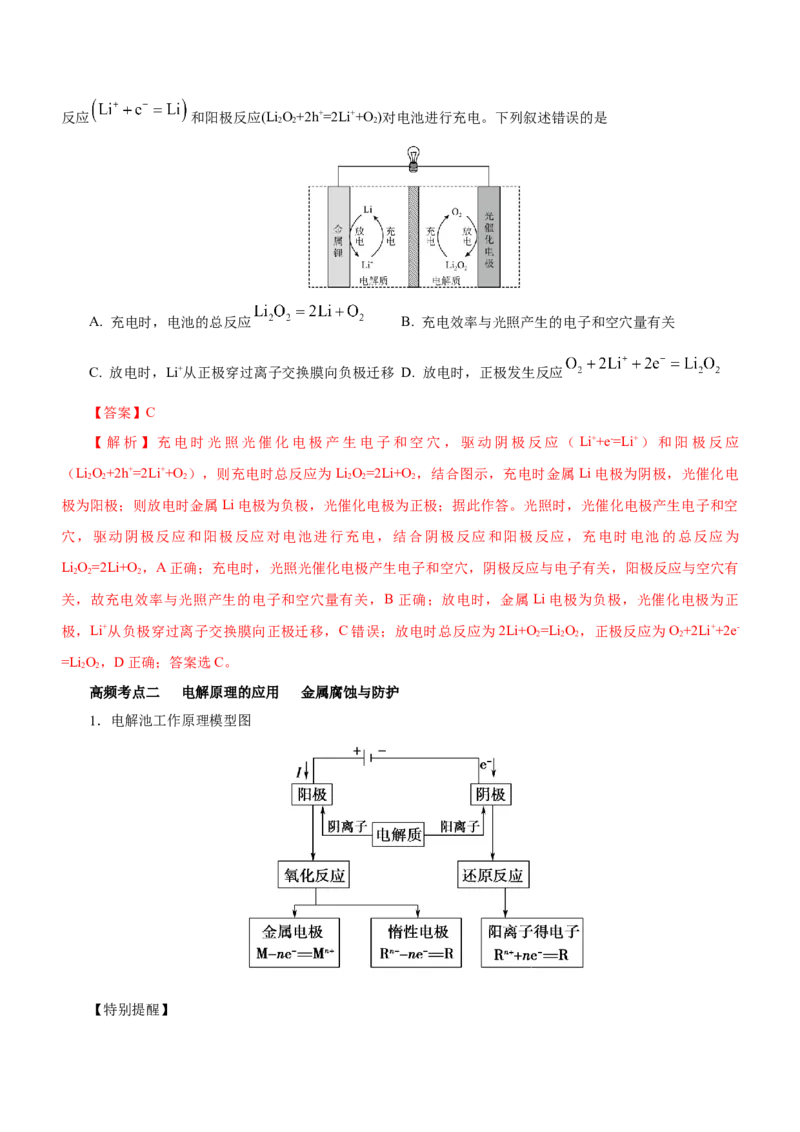
科学家研究了一种光照充电 电池(如图所示)。光照时,光催化电极产生电子 和空穴 ,驱动阴极反应 和阳极反应(Li O+2h+=2Li++O )对电池进行充电。下列叙述错误的是
2 2 2
A. 充电时,电池的总反应 B. 充电效率与光照产生的电子和空穴量有关
C. 放电时,Li+从正极穿过离子交换膜向负极迁移 D. 放电时,正极发生反应
【答案】C
【解析】充电时光照光催化电极产生电子和空穴,驱动阴极反应(Li++e-=Li+)和阳极反应
(LiO+2h+=2Li++O ),则充电时总反应为LiO=2Li+O ,结合图示,充电时金属Li电极为阴极,光催化电
2 2 2 2 2 2
极为阳极;则放电时金属Li电极为负极,光催化电极为正极;据此作答。光照时,光催化电极产生电子和空
穴,驱动阴极反应和阳极反应对电池进行充电,结合阴极反应和阳极反应,充电时电池的总反应为
LiO=2Li+O ,A正确;充电时,光照光催化电极产生电子和空穴,阴极反应与电子有关,阳极反应与空穴有
2 2 2
关,故充电效率与光照产生的电子和空穴量有关,B正确;放电时,金属Li电极为负极,光催化电极为正
极,Li+从负极穿过离子交换膜向正极迁移,C错误;放电时总反应为2Li+O=Li O ,正极反应为O+2Li++2e-
2 2 2 2
=Li O,D正确;答案选C。
2 2
高频考点二 电解原理的应用 金属腐蚀与防护
1.电解池工作原理模型图
【特别提醒】①阳离子在阴极上的放电顺序:Ag+>Fe3+>Cu2+>H+>……
②阴离子在阳极上的放电顺序:S2->I->Br->Cl->OH->含氧酸根离子>……
③当阳极是金属(Au、Pt除外)电极时,溶液中的离子不再放电而是金属失电子生成金属阳离子。
④微粒的放电顺序受温度、浓度、电压、电极材料等因素的影响。
2.电化学计算的两种常用方法
(1)根据电子守恒计算
①用于串联电路中阴阳两极产物、正负两极产物、相同电量等类型的计算,其依据是电路中转移的电子数
相等。
②用于混合溶液中电解的分阶段计算。
(2)根据关系式计算
根据得失电子守恒定律建立起已知量与未知量之间的桥梁,构建计算所需的关系式。
如以通过4 mol e-为桥梁可构建如下关系式:
(式中M为金属,n为其离子的化合价数值)
例2.(2022·广东卷)以熔融盐为电解液,以含 和 等的铝合金废料为阳极进行电解,实现
的再生。该过程中
A. 阴极发生的反应为 B. 阴极上 被氧化
C. 在电解槽底部产生含 的阳极泥 D. 阳极和阴极的质量变化相等
【答案】C
【解析】根据电解原理可知,电解池中阳极发生失电子的氧化反应,阴极发生得电子的还原反应,该题中
以熔融盐为电解液,含Cu、Mg和Si等的铝合金废料为阳极进行电解,通过控制一定的条件,从而可使阳极
区Mg和Al发生失电子的氧化反应,分别生成Mg2+和Al3+,Cu和Si不参与反应,阴极区Al3+得电子生成Al单
质,从而实现Al的再生,据此分析解答。阴极应该发生得电子的还原反应,实际上Mg在阳极失电子生成
Mg2+,A错误;Al在阳极上被氧化生成Al3+,B错误;阳极材料中Cu和Si不参与氧化反应,在电解槽底部可
形成阳极泥,C正确;因为阳极除了铝参与电子转移,镁也参与了电子转移,且还会形成阳极泥,而阴极只有
铝离子得电子生成铝单质,根据电子转移数守恒及元素守恒可知,阳极与阴极的质量变化不相等,D错误;故
选C。
【变式探究】(2022·海南卷)一种采用 和 为原料制备 的装置示意图如下。下列有关说法正确的是
A. 在b电极上, 被还原 B. 金属Ag可作为a电极的材料
C. 改变工作电源电压,反应速率不变 D. 电解过程中,固体氧化物电解质中 不断减少
【答案】A
【解析】由装置可知,b电极的N 转化为NH ,N元素的化合价降低,得到电子发生还原反应,因此b为
2 3
阴极,电极反应式为N+3H O+6e-=2NH+3O2-,a为阳极,电极反应式为2O2-+4e-=O ,据此分析解答;由分析
2 2 3 2
可得,b电极上N 转化为NH ,N元素的化合价降低,得到电子发生还原反应,即N 被还原,A正确;a为阳
2 3 2
极,若金属Ag作a的电极材料,则金属Ag优先失去电子,B错误;改变工作电源的电压,反应速率会加快,
C错误;电解过程中,阴极电极反应式为N+3H O+6e-=2NH+3O2-,阳极电极反应式为2O2-+4e-=O ,因此固体
2 2 3 2
氧化物电解质中O2-不会改变,D错误;故选A。
【举一反三】(2022·湖北卷)含磷有机物应用广泛。电解法可实现由白磷直接制备 ,过程
如图所示( 为甲基)。下列说法正确的是
A. 生成 ,理论上外电路需要转移 电子B. 阴极上的电极反应为:
C. 在电解过程中 向铂电极移动
D. 电解产生的 中的氢元素来自于
【答案】D
【解析】石墨电极发生反应的物质:P→ 化合价升高发生氧化反应,所以石墨电极为阳
4
极,对应的电极反应式为: ,则生成 ,理论上外电路需要转
移 电子,A错误;阴极上发生还原反应,应该得电子, 为阳极发生 的反
应, B错误;石墨电极:P→ 发生氧化反应,为阳极,铂电极为阴极, 应该向阳极移动,
4
即移向石墨电极,C错误;由所给图示可知HCN在阴极放电,产生 和 ,而HCN中的H来自 ,
则电解产生的 中的氢元素来自于 ,D正确;故选D。
3.金属电化学腐蚀与防护
(1)金属腐蚀快慢的三个规律
①金属腐蚀类型的差异
电解原理引起的腐蚀>原电池原理引起的腐蚀>化学腐蚀>有防护腐蚀措施的腐蚀。
②电解质溶液的影响
a.对同一金属来说,腐蚀的快慢(浓度相同):强电解质溶液>弱电解质溶液>非电解质溶液。
b.对同一种电解质溶液来说,电解质浓度越大,腐蚀越快。
③活泼性不同的两金属,活泼性差别越大,腐蚀越快。
(2)两种腐蚀与三种保护
①两种腐蚀:析氢腐蚀、吸氧腐蚀(关键在于电解液的pH)。
②三种保护:电镀保护、牺牲阳极的阴极保护法、外加电流的阴极保护法。
例3. (2022·广东卷)为检验牺牲阳极的阴极保护法对钢铁防腐的效果,将镀层有破损的镀锌铁片放入酸
化的 溶液中。一段时间后,取溶液分别实验,能说明铁片没有被腐蚀的是A. 加入 溶液产生沉淀 B. 加入淀粉碘化钾溶液无蓝色出现
C. 加入 溶液无红色出现 D. 加入 溶液无蓝色沉淀生成
【答案】D
【解析】镀层有破损的镀锌铁片被腐蚀,则将其放入到酸化的3%NaCl溶液中,会构成原电池,由于锌比
铁活泼,作原电池的负极,而铁片作正极,溶液中破损的位置会变大,铁也会继续和酸化的氯化钠溶液反应产
生氢气,溶液中会有亚铁离子生成,据此分析解答。氯化钠溶液中始终存在氯离子,所以加入硝酸银溶液后,
不管铁片是否被腐蚀,均会出现白色沉淀,故A不符合题意;淀粉碘化钾溶液可检测氧化性物质,但不论铁
片是否被腐蚀,均无氧化性物质可碘化钾发生反应,故B不符合题意;KSCN溶液可检测铁离子的存在,上述
现象中不会出现铁离子,所以无论铁片是否被腐蚀,加入KSCN溶液后,均无红色出现,故C不符合题意;
K[Fe(CN) ]是用于检测Fe2+的试剂,若铁片没有被腐蚀,则溶液中不会生成亚铁离子,则加入K[Fe(CN) ]溶液
3 6 3 6
就不会出现蓝色沉淀,故D符合题意。综上所述,答案为D。
【变式探究】(2020·江苏卷)将金属M连接在钢铁设施表面,可减缓水体中钢铁设施的腐蚀。在题图所
示的情境中,下列有关说法正确的是
A. 阴极的电极反应式为
B. 金属M的活动性比Fe的活动性弱
C. 钢铁设施表面因积累大量电子而被保护
D. 钢铁设施在河水中的腐蚀速率比在海水中的快
【答案】C
【解析】该装置为原电池原理的金属防护措施,为牺牲阳极的阴极保护法,金属M作负极,钢铁设备作
正极,据此分析解答。阴极的钢铁设施实际作原电池的正极,正极金属被保护不失电子,故A错误;阳极金
属M实际为原电池装置的负极,电子流出,原电池中负极金属比正极活泼,因此M活动性比Fe的活动性强,
故B错误;金属M失电子,电子经导线流入钢铁设备,从而使钢铁设施表面积累大量电子,自身金属不再失
电子从而被保护,故C正确;海水中的离子浓度大于河水中的离子浓度,离子浓度越大,溶液的导电性越
强,因此钢铁设施在海水中的腐蚀速率比在河水中快,故D错误;故选C。高频考点三 离子交换膜在电化学中的综合应用
1.离子交换膜的作用
(1)防止副反应的发生,避免影响所制取产品的质量;防止引发不安全因素(如在电解饱和食盐水中,利用
阳离子交换膜,防止阳极产生的Cl 进入阴极室与氢氧化钠反应,导致所制产品不纯;防止与阴极产生的H 混
2 2
合发生爆炸)。
(2)用于物质的分离、提纯等。
(3)用于物质的制备。
2.离子交换膜的类型
根据透过的微粒,离子交换膜可以分为多种,在高考试题中主要出现过阳离子交换膜、阴离子交换膜和质
子交换膜三种。阳离子交换膜只允许阳离子通过,阻止阴离子和气体通过,阴离子交换膜只允许阴离子通过,
质子交换膜只允许质子(H+)通过。
3.离子交换膜类型的判断
根据电解质溶液呈电中性的原则,判断膜的类型:
(1)首先写出阴、阳两极上的电极反应,依据电极反应式确定该电极附近哪种离子剩余。
(2)根据溶液呈电中性,判断出离子移动的方向,从而确定离子交换膜的类型。
4.定量关系
外电路电子转移数=通过隔膜的阴、阳离子带的负或正电荷数。
例4.(2022·湖南卷)海水电池在海洋能源领域备受关注,一种锂-海水电池构造示意图如下。下列说法错
误的是
A. 海水起电解质溶液作用 B. N极仅发生的电极反应:
C. 玻璃陶瓷具有传导离子和防水的功能 D. 该锂-海水电池属于一次电池
【答案】B
【解析】锂海水电池的总反应为4Li+2HO+O═4LiOH, M极上Li失去电子发生氧化反应,则M电极为
2 2
负极,电极反应为Li-e-=Li+,N极为正极,电极反应为O+2H O+4e-=4OH-。海水中含有丰富的电解质,如氯
2 2
化钠、氯化镁等,可作为电解质溶液,故A正确;由上述分析可知,N为正极,电极反应为O+2H O+4e-
2 2
=4OH-,故B错误;Li为活泼金属,易与水反应,玻璃陶瓷的作用是防止水和Li反应,并能传导离子,故C正确;该电池不可充电,属于一次电池,故D正确;答案选B。
【变式探究】(2022·全国甲卷)一种水性电解液Zn-MnO 离子选泽双隔膜电池如图所示(KOH溶液中,
2
Zn2+以Zn(OH) 存在)。电池放电时,下列叙述错误的是
A.Ⅱ区的K+通过隔膜向Ⅲ区迁移
B.Ⅰ区的SO 2-通过隔膜向Ⅱ区迁移
4
C. MnO 电极反应:MnO +2e-+4H+=Mn2++2H O
2 2 2
D.电池总反应:Zn+4OH-+MnO+4H+=Zn(OH) 2-+Mn2++2H O
2 4 2
【答案】A
【解析】根据图示的电池结构和题目所给信息可知,Ⅲ区Zn为电池的负极,电极反应为Zn-2e-+4OH-
=Zn(OH) 2-,Ⅰ区MnO 为电池的正极,电极反应为MnO +2e-+4H+=Mn2++2H O;电池在工作过程中,由于两个
4 2 2 2
离子选择隔膜没有指明的阳离子隔膜还是阴离子隔膜,故两个离子隔膜均可以通过阴、阳离子,因此可以得到
Ⅰ区消耗H+,生成Mn2+,Ⅱ区的K+向Ⅰ区移动或Ⅰ区的SO 2-向Ⅱ区移动,Ⅲ区消耗OH-,生成Zn(OH) 2-,Ⅱ
4 4
区的SO 2-向Ⅲ区移动或Ⅲ区的K+向Ⅱ区移动。据此分析答题。根据分析,Ⅱ区的K+只能向Ⅰ区移动,A错
4
误;根据分析,Ⅰ区的SO 2-向Ⅱ区移动,B正确;MnO 电极的电极反应式为MnO +2e-+4H+=Mn2++2H O,C
4 2 2 2
正确;电池的总反应为Zn+4OH-+MnO+4H+=Zn(OH) +Mn2++2H O,D正确;故答案选A。
2 2
【举一反三】(2022·浙江卷)通过电解废旧锂电池中的 可获得难溶性的 和 ,电
解示意图如下(其中滤布的作用是阻挡固体颗粒,但离子可自由通过。电解过程中溶液的体积变化忽略不计)。
下列说法不正确的是A.电极A为阴极,发生还原反应
B.电极B的电极发应:
C.电解一段时间后溶液中 浓度保持不变
D.电解结束,可通过调节 除去 ,再加入 溶液以获得
【答案】C
【解析】由电解示意图可知,电极B上Mn2+转化为了MnO ,锰元素化合价升高,失电子,则电极B为阳
2
极,电极A为阴极,得电子,发生还原反应,A正确;由电解示意图可知,电极B上Mn2+失电子转化为了
MnO ,电极反应式为:2HO+Mn2+-2e-=MnO+4H+,B正确;电极A为阴极,LiMn O 得电子,电极反应式
2 2 2 2 4
为:2LiMn O+6e-+16H+=2Li++4Mn2++8H O,依据得失电子守恒,电解池总反应为:2LiMn O+4H+=2Li++Mn2+
2 4 2 2 4
+3MnO+2H O,反应生成了Mn2+,Mn2+浓度增大,C错误;电解池总反应为:2LiMn O+4H+=2Li++Mn2+
2 2 2 4
+3MnO+2H O,电解结束后,可通过调节溶液pH将锰离子转化为沉淀除去,然后再加入碳酸钠溶液,从而获
2 2
得碳酸锂,D正确;故选C。