文档内容
专题 07 物质结构与元素周期律
01专题网络·思维脑图
02考情分析·解密高考
03高频考点·以考定法
考点一 原子结构与性质、元 考点二 分子结构与性质 考点三 晶体结构与性质
素周期律 【高考解密】 【高考解密】
命题点01 共价键的形成及类型 命题点01 晶体的性质与晶
【高考解密】
的判断 体类型的判断
命题点01原子结构与核外电子排
命题点02 分子的空间结构与价 命题点02 有关晶体计算
布
层电子对互斥理论、杂化轨道理
【技巧解密】
命题点02元素“位-构-性”的相
论
互推断
【考向预测】
命题点03 分子性质及微粒间的
【技巧解密】
作用力
【考向预测】 【技巧解密】
【考向预测】
04核心素养·微专题
微专题 晶胞参数、坐标参数的分析与应用
【淘宝店铺:向阳百分百】考点 考查内容 考情预测
1.原子结构与核外电子排布 1.选择题:高考命题一般是用元素周期表及元素周期
原子结构与性质、
2.元素“位-构-性”的相互推断律知识去推断元素类型,或是根据原子结构推导元素
元素周期律
类型及其在周期表中的位置,考查原子结构和元素性
质之间的关系,试题以短周期元素考查元素周期律及
1.共价键类型的判断
元素“位、构、性”三者之间的关系,考查原子半
2.分子的空间结构与价层电子
对互斥理论、杂化轨道理论 径、化合价、金属性、非金属性、单质及化合物性质
分子结构与性质
3.分子性质及微粒间的作用力 的递变规律与原子结构的关系,涉及化学键时主要考
查对概念的理解。同时也考查分子结构判断及晶体相
关计算。
2.非选择试题常以填空或简答方式考查,常涉及原子
1.晶体的性质与晶体类型的判结构与元素的性质(如基态微粒的电子排布式、电离能
断 及电负性的比较)、元素周期律;分子结构与性质(如
晶体结构与性质 化学键类型、原子的杂化方式、分子空间构型的分析
2.有关晶体计算
与判断);晶体结构与性质(如晶体类型、性质及与粒
子间作用的关系、以晶胞为单位的密度、微粒间距与
微粒质量的关系计算及化学式分析)等考点。命题侧重
考查分析能力和计算能力,需要熟练掌握晶胞结构,
具备一定的数学计算能力,综合性较强,题目难度中
【淘宝店铺:向阳百分百】等。
考点一 原子结构与性质、元素周期律
命题点01原子结构与核外电子排布
典例01(2023·海南卷)下列有关元素单质或化合物的叙述正确的是
A. 分子呈正四面体,键角为
B.NaCl焰色试验为黄色,与Cl电子跃迁有关
C.Cu基态原子核外电子排布符合构造原理
D. 是由极性键构成的极性分子
【答案】D
【解析】A. 分子呈正四面体,磷原子在正四面体的四个顶点处,键角为 ,A错误;B.NaCl焰色试
验为黄色,与Na电子跃迁有关,B错误;C.Cu基态原子核外电子排布不符合构造原理,考虑了半满规
则和全满规则,价电子排布式为3d104s1,这样能量更低更稳定,C错误;D. 的构型是V形,因此是由
极性键构成的极性分子,D正确;故选D。
典例02(2023·重庆卷)“嫦娥石”是中国首次在月球上发现的新矿物,其主要由 和
(钇,原子序数比 大13)组成,下列说法正确的是
A.Y位于元素周期表的第ⅢB族
B.基态 原子的核外电子填充在6个轨道中
C.5种元素中,第一电离能最小的是
D.5种元素中,电负性最大的是
【淘宝店铺:向阳百分百】【答案】A
【解析】A.钇原子序数比 大13,为39号元素,为元素周期表的第五周期第ⅢB族,A正确;B.钙为
20号元素,原子核外电子排布为1s22s22p63s23p64s2,基态 原子的核外电子填充在10个轨道中,B错误;
C.同一主族随原子序数变大,原子半径变大,第一电离能变小;同一周期随着原子序数变大,第一电离
能变大,5种元素中,钙第一电离能比铁小,C错误;D.同周期从左到右,金属性减弱,非金属性变强,
元素的电负性变强;同主族由上而下,金属性增强,非金属性逐渐减弱,元素电负性减弱;5种元素中,
电负性最大的是O,D错误;故选A。
命题点02元素“位-构-性”的相互推断
典例01(2023·全国卷)一种矿物由短周期元素W、X、Y组成,溶于稀盐酸有无色无味气体生成。W、
X、Y原子序数依次增大。简单离子 与 具有相同的电子结构。下列叙述正确的是
A.X的常见化合价有 、 B.原子半径大小为
C.YX的水合物具有两性 D.W单质只有4种同素异形体
【答案】A
【分析】W、X、Y为短周期元素,原子序数依次增大,简单离子X2-与Y2+具有相同的电子结构,则它们
均为10电子微粒, X为O,Y为Mg,W、X、Y组成的物质能溶于稀盐酸有无色无味的气体产生,则W
为C,产生的气体为二氧化碳。
【解析】A.X为O,氧的常见价态有-1价和-2价,如HO 和HO,A正确;B.W为C,X为O,Y为
2 2 2
Mg,同主族时电子层数越多,原子半径越大,电子层数相同时,原子序数越小,原子半径越大,所以原子
半径大小为:Y>W>X,B错误;C.Y为Mg,X为O,他们可形成MgO,水合物为Mg(OH) ,Mg(OH)
2 2
只能与酸反应生成盐和水,不能与碱反应,所以YX的水合物没有两性,C错误;D.W为C,碳的同素异
形体有:金刚石、石墨、石墨烯、富勒烯、碳纳米管等,种类不止四种,D错误;故选A。
典例02(2022·浙江卷)X、Y、Z、M、Q五种短周期主族元素,原子序数依次增大。X的核外电子数等
于其周期数, 分子呈三角锥形,Z的核外电子数等于X、Y核外电子数之和。M与X同主族,Q是同
周期中非金属性最强的元素。下列说法正确的是
A.X与Z形成的10电子微粒有2种
B.Z与Q形成的一种化合物可用于饮用水的消毒
【淘宝店铺:向阳百分百】C. 与 的晶体类型不同
D.由X、Y、Z三种元素组成的化合物的水溶液均显酸性
【答案】B
【分析】X的核外电子数等于其周期数,X为H,YX 分子呈三角锥形,Y为N,Z的核外电子数等于X、
3
Y核外电子数之和,则Z为O,M与X同主族,则M为Na,Q是同周期中非金属性最强的元素,则Q为
Cl,综合分析,X为H,Y为N,Z为O,M为Na,Q为Cl。
【解析】A.由分析可知X为H,Z为O,则其形成的10电子微粒有HO、OH-、HO+,A错误;B.由分
2 3
析可知Z为O,Q为Cl,可形成ClO ,有氧化性,可用于自来水消毒,B正确;C.由分析可知Z为O,
2
M为Na,Q为Cl,则MZ为NaO,为离子晶体,MQ为NaCl,为离子晶体,晶体类型相同,C错误;
2 2
D.由分析可知X为H,Y为N,Z为O,这三种元素可以形成NH₃·H₂O,其溶液显碱性,D错误;故选
B。
典例03(2021·江苏卷)前4周期主族元素X、Y、Z、W的原子序数依次增大,X是空气中含量最多的
元素,Y的周期序数与族序数相等,基态时Z原子3p原子轨道上有5个电子,W与Z处于同个主族。下列
说法正确的是
A.原子半径:r(X)A>B;金属性:C>A>B;非金属性:B>A>C。
(2)相似规律
同主族元素性质相似,位于对角线位置的元素性质相似,相邻元素性质差别不大。
(3)电子排布规律
原子最外层电子数大于或等于 3而又小于8的元素一定是主族元素;原子最外层电子数为 1或2的元素可
能是主族、副族或0族(He)元素;原子最外层电子数为8的元素是稀有气体元素。
(4)原子序数与元素位置的“序数差值”规律
1)同周期相邻主族元素的“序数差值”规律。
①除第ⅡA族和第ⅢA族外,其余同周期相邻元素原子序数差为1。
②同周期第ⅡA族和第ⅢA族元素,其原子序数差分别是:第二、三周期相差1,第四、五周期相差11,第六、
七周期相差25。
2)同族相邻元素的“序数差值”规律。
①第二、三周期的同族元素原子序数相差8。
②第三、四周期的同族元素原子序数相差有两种情况:第ⅠA族、ⅡA族相差8,其他族相差18。
【淘宝店铺:向阳百分百】③第四、五周期的同族元素原子序数相差18。
④第五、六周期的同族元素原子序数镧系之前的相差18,镧系之后的相差32。
⑤第六、七周期的同族元素原子序数相差32。
(5)含量或性质特殊的元素
5.元素金属性和非金属性强弱的判断方法
本质 原子越易失电子,金属性越强(与原子失电子数目无关)
①在金属活动性顺序表中越靠前,金属性越强
②单质与水或非氧化性酸反应越剧烈,金属性越强
金属性比较 ③单质还原性越强或阳离子氧化性越弱,金属性越强
判断方法
④最高价氧化物对应水化物的碱性越强,金属性越强
⑤若Xn++Y―→X+Ym+,则Y比X的金属性强
⑥元素在周期表中的位置:左边或下方元素的金属性强
本质 原子越易得电子,非金属性越强(与原子得电子数目无关)
①与H 化合越容易,气态氢化物越稳定,非金属性越强
2
非金属性比较 ②单质氧化性越强或阴离子还原性越弱,非金属性越强
判断方法
③最高价氧化物对应水化物的酸性越强,非金属性越强
④元素在周期表中的位置:右边或上方元素的非金属性强
6.第一电离能、电负性
(1)元素第一电离能的周期性变化规律。
一 同一周期,随着原子序数的增加,元素的第一电离能呈现增大的趋势,稀有气体元素的第一电离能最大,
般 碱金属元素的第一电离能最小;同一主族,随着电子层数的增加,元素的第一电离能逐渐减小
【淘宝店铺:向阳百分百】规
律
特 第一电离能的变化与元素原子的核外电子排布有关。通常情况下,当原子核外电子排布在能量相等的
殊 轨道上形成全空(p0、d0、f0)、半满(p3、d5、f7)和全满(p6、d10、f14)结构时,原子的能量较低,该元素具有
情 较大的第一电离能。如同周期主族元素,第ⅡA族元素的原子最外层s能级全充满、ⅤA族元素的原
况 子最外层p能级半充满,比较稳定,所以其第一电离能大于同周期相邻的主族元素
(2)电负性大小判断。
规
在周期表中,同周期主族元素电负性从左到右逐渐增大,同主族从上往下逐渐减小
律
方 常常应用化合价及物质类别判断电负性的大小,如O与Cl的电负性比较:①HClO中Cl为+1价、O
法 为-2价,可知O的电负性大于Cl;②Al O 是离子化合物、AlCl 是共价化合物,可知O的电负性大于Cl
2 3 3
7.元素推断题通常考查的角度及分析依据
考查角度 分析依据
①同周期元素的原子半径随原子序数的增大而减小(不考虑稀有气体元素);
原子半径
②同主族元素从上到下,原子半径随电子层数的增多而增大
①同周期元素从左到右,元素的最高正化合价由+1→+7,非金属元素的最低负化合价
由-4→-1(O、F除外);
元素化合价
②同主族元素的最高正化合价、最低负化合价均相同(适用于短周期主族元素,氧无
最高正价,氟无正价)
①元素的金属性越强,其最高价氧化物对应的水化物的碱性越强;
氧化物对应水化物 ②元素的非金属性越强,其最高价氧化物对应的水化物的酸性越强(F无正价,O无最
高正价,不考虑)
单质的氧化性、还原一般情况下,元素的金属性越强,单质的还原性越强,简单阳离子的氧化性越弱;元素
性 的非金属性越强,单质的氧化性越强,简单阴离子的还原性越弱
①一般情况下,对于组成和结构相似的物质,相对分子质量越大,分子间作用力越大,
物质的熔点、沸点 物质的熔点、沸点也越高,如沸点:I 2 >Br 2 >F 2 ;
②NH 、HO、HF的沸点反常高,是因为分子间形成氢键,使物质的沸点升高
3 2
①同周期元素从左到右,失电子能力逐渐减弱,得电子能力逐渐增强(不考虑稀有气体
得失电子能力
元素);
②同主族元素从上到下,失电子能力逐渐增强,得电子能力逐渐减弱
①同周期元素从左到右,金属性逐渐减弱,非金属性逐渐增强(不考虑稀有气体元素);
金属性与非金属性
②同主族元素从上到下,金属性逐渐增强,非金属性逐渐减弱
①同周期元素从左到右元素的第一电离能呈增大趋势;
元素的第一电离能
②同主族元素自上而下,第一电离能逐渐减小
①同周期元素从左到右元素的电负性逐渐增大(稀有气体元素除外);
电负性
②同主族元素自上而下,电负性逐渐减小
8、解答元素推断题的基本方法
(1)已知元素原子或离子的核外电子排布
――→――→――→
【淘宝店铺:向阳百分百】(2)已知元素单质或化合物的性质(特性)
――→――→――→
(3)已知元素在周期表中的位置
(4)利用周期表片断推断元素的种类
①利用H、He的特殊位置
已知X、Y、Z、W四种短周期元素的位置关系如图:
则可以推出X为He,再依次推知Y为F、Z为O、W为P。
②利用元素的位置关系与原子序数关系
a.同一周期中元素的原子序数一般比左边元素原子序数大1,比右边元素的原子序数小1。
b.同主族中相邻周期元素的原子序数关系
9、关于元素周期律、元素周期表的认识误区
(1)误认为主族元素的最高正价一定等于族序数。但是,F无正价。
(2)误认为元素的非金属性越强,其氧化物对应水化物的酸性就越强。但是,HClO、HSO 是弱酸,忽略了
2 3
关键词“最高价”。
(3)误认为同周期相邻两主族元素原子序数之差等于1。忽视了相差11(第4、5周期)和25(第6、7周期)。
(4)误认为失电子难的原子得电子的能力一定强。碳原子、稀有气体元素的原子失电子难,得电子也难。
(5)误认为得失电子多的原子,得失电子的能力一定强。
(6)误认为最高正价和最低负价绝对值相等的元素只有第ⅣA族的某些元素。忽视了第ⅠA族的H的最高
正价为+1价,最低负价为-1价。
10、通过“三看”比较微粒半径大小
在中学化学要求的范围内,可按“三看”规律来比较粒子半径的大小:
【淘宝店铺:向阳百分百】(1)“一看”电子层数:一般情况下,当电子层数不同时,电子层数越多,半径越大。
例如:r(Li)r(Na+)
(2)“二看”核电荷数:当电子层数相同时,核电荷数越大,半径越小。
例如:r(Na)>r(Mg)>r(Al)>r(Si)>r(P)>r(S)>r(Cl)、r(O2-)>r(F-)>r(Na+)>r(Mg2+)>r(Al3+)
(3)“三看”核外电子数:当电子层数和核电荷数均相同时,核外电子数越多,半径越大。
例如:r(Cl-)>r(Cl)、r(Fe2+)>r(Fe3+)
考向01 原子结构与核外电子排布
1.(2023·湖北·校联考模拟预测)硫的下列4种微粒,若失去一个电子所需要能量最多的是
A.[Ne] B.[Ne] C.[Ne] D.[Ne]
【答案】B
【解析】A、B、C、D四项中的微粒分别对应基态S、 、激发态 、激发态S,激发态上电子能量高,
不稳定,易失去,故需要能量最多的是基态的 ;答案选B。
2.(2023·上海黄浦·统考二模)电子亚层2p的三个轨道之间具有不同的
A.能量 B.形状 C.空间伸展方向 D.可容纳电子数
【答案】C
【解析】A.同一能级,能量相等,A错误;B.2p能级的三个轨道都是哑铃形,B错误;C.2p的三个轨
道分别沿着x轴、y轴、z轴三个伸展方向延伸,所以具有不同的空间伸展方向,C正确;D.2p的三个轨
道分别能容纳的电子数都是2个电子,D错误;选C。
3.(2023·重庆·统考模拟预测)三星堆遗址出土了大量的青铜器,其主要成分为Cu、Sn、Pb,还含少量
Fe、As、O等元素。对上述有关元素,下列说法正确的是
A.基态Cu原子的价层电子轨道表示式为
B.基态Fe原子最高能级的轨道形状为哑铃形
C.第一电离能最大的是As
D.电负性最大的是O
【答案】D
【解析】A.基态铜原子的价层电子排布式为3d104s1,基态Cu原子的价层电子轨道表示式为
【淘宝店铺:向阳百分百】,A错误;B.基态Fe原子的核外电子排布式为1s22s22p63s23p63d64s2,
最高能级为3d,轨道形状为花瓣形,B错误;C.Cu、Sn、Pb、Fe、As、O中O的第一电离能最大,C错
误;D.Cu、Sn、Pb、Fe、As、O中O的电负性最大,D正确;故答案选D。
4.(2023·北京门头沟·统考一模)下列表述不正确的是
A.原子轨道能量:1s<2s<3s<4s
B.M电子层存在3个能级、9个原子轨道
C.4s电子能量较高,总是在比3s电子离核更远的地方运动
D.同一周期,碱金属元素的第一电离能最小,最容易失电子
【答案】C
【解析】A.能层不同,能级相同的原子轨道,能层越大,能量越大,则原子轨道能量为1s<2s<3s<4s,故
A正确;B.M电子层存在s、p、d共3个能级,共有(1+3+5)=9个原子轨道,故B正确;C.4s电子能量
高于3s电子,4s电子在离核更远的地方的出现几率比3s电子大,不一定总是在比3s电子离核更远的地方
运动,故C错误;D.同周期元素,从左到右第一电离能呈增大的趋势,所以同一周期中碱金属元素的第
一电离能最小,最容易失电子,故D正确;故选C。
5.(2023·湖北鄂州·高三校联考)第三周期元素X,第一电离能介于Mg和S之间,关于该元素及其化合
物,下列说法正确的是
A.X与氢元素形成的化合物中,各原子均达到8电子稳定结构
B.X的原子核外电子有9种空间运动状态
C.X的单质和盐酸、 溶液均能反应放出
D.X的单质可以用于制造合金
【答案】D
【分析】第三周期元素X,第一电离能介于 和S之间,X为 。
【解析】A. 中H原子没有达到8电子稳定结构,故A错误;B. 的核外电子排布在8个原子轨道
中,有8种空间运动状态,故B错误;C. 和盐酸不反应,故C错误;D. 可用于制造硅钢,故D正
确;选D。
考向02 元素“位-构-性”的相互推断
【淘宝店铺:向阳百分百】1.(2023·广东·校联考一模)已知:X、Y、Z、W为前四周期主族元素,基态X的原子最外层有3个未成
对电子,次外层电子仅有1种空间运动状态;Y的单质在空气中的含量位居第二,Z是短周期主族元素中
原子半径最大的元素;基态W的原子最外层电子排布式为 。下列有关说法正确的是
A.第一电离能:X>Y>Z B.电负性:W>X>Y
C.氢化物的沸点:X>Y D.W与Y形成的化合物为分子晶体
【答案】A
【分析】基态X的原子最外层有3个未成对电子,次外层电子仅有1种空间运动状态,则X为N,Y的单
质在空气中的含量位居第二,则Y的单质为氧气,则Y为O,根据同周期元素“序大径小”,同主族元素
“序大径大”,Z是短周期主族元素中原子半径最大的元素,则Z为Na,基态W的原子最外层电子排布
式为 ,且为主族元素,则W为K。
【解析】A.同周期电离能呈增大趋势,同主族电离能逐渐减小,但IIA、IVA元素电离能大于IIIA、VIA
电离能。由分析可知,X为N,Y为O,Z为Na,则第一电离能X>Y>Z,A正确;B.W为K,X为N,Y
为O,同周期电负性逐渐增大,同主族电负性逐渐减小,则电负性:WY>X>W,C正确;D.元素Z为F元素,F元素无正化合价,D错误;答案选
C。
3.(2023·四川乐山·统考一模)W、X、Y、Z为原子序数依次增大的短周期主族元素,最外层电子数之和
为20, 是一种常见的耐高温材料,Y的内层电子总数是最外层电子数的2.5倍。下列说法正确的是
A.简单离子半径: B.简单氢化物的沸点:
C.Y与Z可以形成离子化合物 D.Y的最高价氧化物对应水化物可以与单质X反应
【答案】B
【分析】W、X、Y、Z为原子序数依次增大的短周期主族元素, 是一种常见的耐高温材料,应该是
,所以X是Al元素,W是O元素,Y的内层电子总数是最外层电子数的2.5倍,原子序数大于Al,
所以Y是Si元素,根据四种元素最外层电子数之和为20,可知Z元素的最外层电子数为 ,
则Z是Cl元素,综上可得,W、X、Y、Z依次为O、Al、Si、Cl元素。
【解析】A.Z、X、W对应的简单离子分别为 、 、 ,其中 电子层数最多,故半径最大,而
和 电子层数相同,所以半径 < ,则三种元素的简单离子半径关系为 ,故A错误;
B.W和Z的简单氢化物为 和 ,由于 中有氢键,所以沸点 > ,即 ,故B正确;
C.Y是Si元素,Z是Cl元素,都是非金属元素,都不太容易失去电子,因此不会形成离子化合物,故C
错误;D.Si的最高价氧化物对应水化物是硅酸,即 ,与单质 不反应,故D错误;故选B。
4.(2024·四川内江·统考一模)X、Y、Z、R、M为原子序数依次增大的短周期元素,其原子的最外层电子数
与原子半径的关系如图所示。下列说法不正确的是
【淘宝店铺:向阳百分百】A.X与Y形成的化合物只含极性共价键
B.简单离子半径比较:
C.含氧酸酸性比较可能存在:
D.X与Z、M三种元素共同形成的化合物可能是离子化合物
【答案】A
【分析】R半径最大,且最外层电子数为1,则R为Na,X的半径最小,则X为H,Y最外层为4个电子,
则Y为C,Z为N,M为S。
【解析】A.X为H、Y为C,若形成烯烃,则既含有极性共价键,也含有非极性共价键,A错误;B.R
为Na、Z为N,则 ,B正确;C.Z为N,M为S,若S形成的是HSO 弱酸,HNO 为强
2 3 3
酸,则酸性HNO>HSO ,C正确;D.X为H、Z为N、M为S,若形成(NH )S,含有离子键则为离子化
3 2 3 4 2
合物,D正确;故答案为:A。
5.(2023·海南·模拟预测)短周期主族元素X、Y、Z、R的主要化合价和原子半径的关系如图所示。基态
X原子的价层电子排布式为 。下列叙述错误的是
A.简单氢化物的沸点:
B.最高价氧化物对应水化物的酸性:
【淘宝店铺:向阳百分百】C.第一电离能:
D.化合物 为非极性分子
【答案】C
【分析】基态X原子的价层电子排布式为 ,化合价为-2价,说明最外层是6个电子第二周期元素,
X为O元素,Y和Z原子半径与氧元素相差不大,化合价为+4和+5价,说明和氧元素是同周期相邻元素,
分别为C和N元素,R的半径较大,化合价为+3价,R是Al元素。
【解析】A.简单氢化物的沸点:HO>NH >CH ,A正确;B.最高价氧化物对应水化物的酸性:
2 3 4
HNO>H CO>Al(OH) ,B正确;C.第一电离能:CHCl
C. D.
【答案】B
【解析】A.甲烷和乙烷组成结构相似,相对分子质量越大,范德华力越大,沸点越高,因此沸点
,故A错误;B.HF存在分子间氢键,因此沸点HF>HCl,故B正确;C. 组成结
构相似,相对分子质量越大,范德华力越大,沸点越高,因此沸点 ,故C错误;D.相同碳原子
的烷烃,支链越多,沸点越低,因此 ,故D错误。综上所述,答案为B。
典例03(2022·湖北卷)下列有关N、P及其化合物的说法错误的是
A.N的电负性比P的大,可推断NCl 分子的极性比PCl 的大
3 3
B.N与N的π键比P与P的强,可推断N≡N的稳定性比P≡P的高
C.NH 的成键电子对间排斥力较大,可推断NH 的键角比PH 的大
3 3 3
D.HNO 的分子间作用力较小,可推断HNO 的熔点比HPO 的低
3 3 3 4
【答案】A
【解析】A.P和Cl的电负性差值比N和Cl的电负性差值大,因此PCl 分子的极性比NCl 分子极性大,A
3 3
项错误;B.N与N的 键比P与P的强,故 的稳定性比 的高,B项正确;C.N的电负性比P
大,NH 中成键电子对距离N比PH 中成键电子对距离P近,NH 中成键电子对间的斥力大,因此NH 的
3 3 3 3
键角比PH 的大,C项正确;D.相对分子质量:HNO氢键>范德华力
组成和结构相似的物质,相对分子质
影响因素 形成氢键元素的电负性 原子半径
量越大,范德华力越大
影响物质的熔、沸点,溶解度等物理 分子间氢键使物质熔、沸点升高,溶 键能越大,稳定性
对性质的影响
性质 解度增大 越强
考向01 共价键的形成及类型的判断
1.(2024·广西北海·统考一模) (俗称铵铁蓝)是一种蓝色的无机颜料。下列有关该物质
的说法错误的是
A.电负性:
B.铵铁蓝中铁元素有两种化合价
C. 中 的键角比 中的 的键角大
D.铵铁蓝中的配体是 ,该配体中 键与 键的数目之比是
【答案】D
【解析】A.同周期从左到右电负性逐渐增大,同主族从上到下电负性逐渐减小,则电负性: ,故
A正确;B.由化合物中正、负化合价的代数和为0可知,铵铁蓝中铁元素有 和 两种化合价,故B正
【淘宝店铺:向阳百分百】确;C.根据价层电子对互斥理论可知, 的空间结构为正四面体形, 的空间结构为三角锥形,
中 的键角比 中的 的键角大,故C正确;D. 中C和N之间是三键,与氮
气互为等电子体,1个 中有1个 键和2个 键,则该配体中 键与 键的数目之比是 ,故D错误。
综上所述,答案为D。
2.(2023·辽宁大连·大连八中校考模拟预测)下列反应产物不能用反应物中键的极性解释的是
A.
B.
C.
D.
【答案】A
【解析】A.CHCH=CH 中的碳碳双键和H 中的H-H键都是非极性键,无法用键的极性解释反应产物,A
3 2 2
正确;B.羰基中的C电负性较小,共用电子对偏向于Cl,容易与极性试剂NH 中电负性较强的-NH 结合,
3 2
Cl电负性较强,容易与电负性较弱的H结合生成HCl,可用键的极性解释,B错误;C.CHCHOH与
3 2
HBr发生取代反应时,CHCHOH中C-O键中C的电负性较弱,O的电负性较强,共用电子对偏向于O,
3 2
HBr中Br电负性较强,共用电子对偏向于Br,因此CHCH-容易与电负性强的Br结合,而-H容易与电负
3 2
性强的-OH结合,可用键的极性解释,C错误;D.乙醛中醛基内C的电负性较弱,O的电负性较强,共
用电子对偏向O,HCN中的H-C键中C的电负性较强,H的电负性较弱,共用电子对偏向于C,因此醛基
中电负性弱的C容易与电负性强的-CN结合,醛基中电负性强的O容易与电负性弱的H相结合,可用键的
极性解释,D错误;故答案选A。
3.(2023·北京海淀·101中学校考三模)甲磺酸 是一种强酸。下列说法正确的是
【淘宝店铺:向阳百分百】A.推测甲磺酸难溶于水 B.该分子中心原子S的价层电子对数为6
C.分子中所有化学键均为极性共价键 D.该分子中硫氧键的键长均相同
【答案】C
【解析】A.该物质中有-OH可与水形成氢键,其溶解性较大,A项错误;B.S的价层电子对=4+0=4对,
B项错误;C.分子中有C-H、C-S、S=O、S-O、O-H均为极性键,C项正确;D.分子中S=O和S-O键键
长不同,D项错误;故选C。
4.(2023·安徽芜湖·统考二模)周期表前四周期的元素A、B、C、D、E原子序数依次增大。基态原子A
的原子轨道半充满,B的价电子层中有3个未成对电子,D的价层电子排布式为nsn-1np2n-2,C与D同族,E
的最外层只有1个电子,次外层有18个电子。这5种元素形成的一种1:1型离子化合物中,由C、D所形
成的阴离子呈正四面体结构、阳离子呈轴向狭长的八面体结构(如图所示)。下列说法正确的是
A.5种原子中第一电离能最大的是C
B.A、B所形成的化合物中只含极性键
C.1mol该阳离子中含有24molσ键
D.B、C、D所形成的简单氢化物中,沸点最低的是D
【答案】D
【分析】基态原子A的原子轨道半充满,则A的电子排布式为1s1,为H元素;D的价层电子排布式为
nsn-1np2n-2,s轨道全充满时有2个电子,则n-1=2,n=3,D的价层电子排布式为3s23p1,为S元素;C、D
同主族,原子序数CO,故A错误;B.A、B可形成NH,含有非极性键,故B错
2 4
误;C.由图可知,1mol该阳离子中含有26molσ键,故C错误;D.B、C所形成的简单氢化物HO与
2
NH 均可形成分子间氢键,沸点较高,D所形成的HS无分子间氢键,沸点最低,故D正确;故答案选
3 2
D。
【淘宝店铺:向阳百分百】5.(2023·海南海口·海南华侨中学校考模拟预测)火箭发射时可用 作燃料, 作氧化剂,其反应
为 。 为阿伏加德罗常数的值,下列说法正确的是
A.1.8 g 中氧的价层电子对数为
B.1 mol 中含有的π键数为
C.当生成6.72 L 时转移电子数为
D.1 mol 中含有的质子数为
【答案】A
【解析】A.1.8 g 为0.1mol,1个 中心O原子的价层电子对数= ,0.1mol水中氧的价
层电子对数为 ,故A正确;B. 结构简式为: ,分子中只含单键,不含π键,故B错
误;C.未指明气体所处状态,不能依据体积确定物质的量,故C错误;D.1 mol 中含有的质子数
为 ,故D错误;故选:A。
考向02 分子的空间结构与价层电子对互斥理论、杂化轨道理论
1.(2024·广西·校联考模拟预测)价层电子对互斥理论可以预测某些微粒的空间结构。下列说法错误的是
A.SO 和SO 的VSEPR模型均为平面三角形
2 3
B.PCl 、NCl 的空间构型都是三角锥形
3 3
C.BF 和NF 均为非极性分子
3 3
D.CO 与N 的键角相等
2
【答案】C
【解析】A.SO 和SO 中硫原子的价层电子对数均为3,则SO 和SO 的VSEPR模型均为平面三角形,A
2 3 2 3
正确;B.PCl 、NCl 中心原子孤电子对数都是= ×(5−3×1)=1,价层电子对数为4,所以PCl 、NH 均为
3 3 3 3
【淘宝店铺:向阳百分百】三角锥形,B正确;C.BF 中心原子B原子孤电子对数= ×(3−3×1)=0,价层电子对数为3,是平面正三角
3
形结构,为非极性分子,NF 中心原子孤电子对数都是= ×(5−3×1)=1,为三角锥形结构,为极性分子,C
3
错误;D.CO 分子中的中心C原子价层电子对数是2+ =2,故C原子采用sp杂化,分子呈直线形,
2
键角是180°,N−与CO 互为等电子体,N−也呈直线形,键角是180°,即CO 与N−的键角相等,D正确。
3 2 3 2 3
答案选C。
2.(2023·浙江宁波·统考模拟预测)磷酰氯( )是有机合成的催化剂,可用以下方法制取:
或 , 的分子空间结构模型如图所示,下列说法不正确的
是
A. 中只含有 键
B. 是非极性分子
C. 的空间构型是三角锥形
D. 可与 反应生成
【答案】A
【解析】A. 结构中含有P-O键、P=O键,故既含 键,也含 键,A符合题意;B. 为空间对
称结构,是非极性分子,B不符合题意;C. 的中心原子P的价层电子对数为 ,由
【淘宝店铺:向阳百分百】于中心P原子有一对孤对电子,其空间构型是三角锥形,C不符合题意;D. 可与 发生
反应: +3 → +3HCl,D不符合题意; 故选A。
3.(2023·江苏南通·统考模拟预测)周期表中VIA族元素及其化合物应用广泛。 、 、 是氧元素
的3种核素,可以形0成多种重要的化合物。亚硫酰氯 为黄色液体,其结构式为(
),遇水发生水解。工业上可电解HSO 与 混合溶液制备过二硫酸铵 ,过二硫酸
2 4
铵与双氧水中都含有过氧键(-O-O-)。硝化法制硫酸的主要反应为:
。SO 和SO 都是酸性氧化物,是制备硫酸的中间产物。下列说法正确的是
2 3
A. 、 、 具有相同的中子数
B.亚硫酰氯空间构型为平面三角形
C.SO 、SO 的中心原子轨道杂化类型均为sp2
2 3
D.SO 晶体中存在S和O 之间的强烈作用
2 2
【答案】C
【解析】A. 中子数为16-8=8、 的中子数为17-8=9、 的中子数为18-8=10,A错误;B.亚硫酰
氯S为sp3杂化,空间构型属于三角锥形,B错误;C.SO 中σ键为2,S的孤电子对为(6-2×2)÷2=1,
2
SO 中σ键为3,S的孤电子对为(6-2×3)÷2=0,,中心原子轨道杂化类型均为sp2,C正确;D.SO 晶体
3 2
中存在S和O之间的共价键,为强烈相互作用,D错误;故选C。
4.(2023·辽宁大连·大连八中校考模拟预测)三硫化四磷( )是黄绿色针状晶体,易燃、有毒,分子结
构如图所示。下列有关 的说法中正确的是
【淘宝店铺:向阳百分百】A. 中仅P原子最外层均满足8电子稳定结构
B.键角:
C. 中P原子为 杂化,S原子为 杂化
D. 分子中含有6mol极性共价键
【答案】D
【解析】A.P最外层5个电子,形成了3个共价键,S最外层6个电子,形成了2个键,因此都满足8电
子稳定结构,不仅仅是P原子,故A错误;B. 均采用sp3杂化,PCl 的中心原子有一对孤电子,
3
而 无孤电子对,因为孤电子对对成键电子对有排斥力,所以导致Cl-P-Cl键角更小,即键角比较:
,故B错误;C.S原子价层电子对数是4,则S原子是sp3杂化,故C错误;D.根据结构简式
可知1mol 分子中含有6mol极性共价键,3mol非极性共价键,故D正确;答案选D。
5.(2023·山西晋城·晋城市第一中学校校考模拟预测)油画创作通常需要用到多种无机颜料。研究发现,
在不同的空气湿度和光照条件下,颜料雌黄 褪色的主要原因是发生了以下两种化学反应:
下列说法正确的是
A.反应I和II中,元素 和 都被氧化
【淘宝店铺:向阳百分百】B.反应I和II中,氧化 转移的电子数之比为
C. 和 的空间结构都是正四面体形
D.反应I和II中,参加反应的 :IH—Br,则键长H—F离子晶体>分子晶体,如熔、沸点:金刚石
>NaCl>Cl2;金属晶体>分子晶体,如熔、沸点:Na>Cl2(金属晶体熔、沸点有的很高,如钨、铂等,有的则很低,如
汞等)。
(2)形成原子晶体的原子半径越小、键长越短,则键能越大,其熔、沸点就越高,如熔、沸点:金刚石>石英>碳化
硅>晶体硅。
(3)形成离子晶体的阴阳离子所带的电荷数越多,离子半径越小,则离子键越强,熔、沸点就越高,如熔、沸
点:MgO>MgCl2,NaCl>CsCl。
(4)金属晶体中金属离子半径越小,离子所带电荷数越多,其形成的金属键越强,金属单质的熔、沸点就越高,如
Al>Mg>Na。
(5)分子晶体的熔、沸点比较规律。
①组成和结构相似的分子,相对分子质量越大,其熔、沸点就越高,如:HI>HBr>HCl。
②组成和结构不相似的分子,分子极性越大,其熔、沸点就越高,如:CO>N2。
③同分异构体分子中,支链越少,其熔、沸点就越高,如:正戊烷>异戊烷>新戊烷。
④同分异构体中的芳香烃及其衍生物,邻位取代物>间位取代物>对位取代物,如熔、沸点:邻二甲苯>间二甲
苯>对二甲苯。
3、均摊法确定晶胞组成
(1)方法:晶胞中任意位置上的一个原子如果是被n个晶胞所共有,那么,每个原子对这个晶胞的贡献就是。
(2)类型
①长方体(正方体)晶胞中不同位置的粒子对晶胞的贡献:
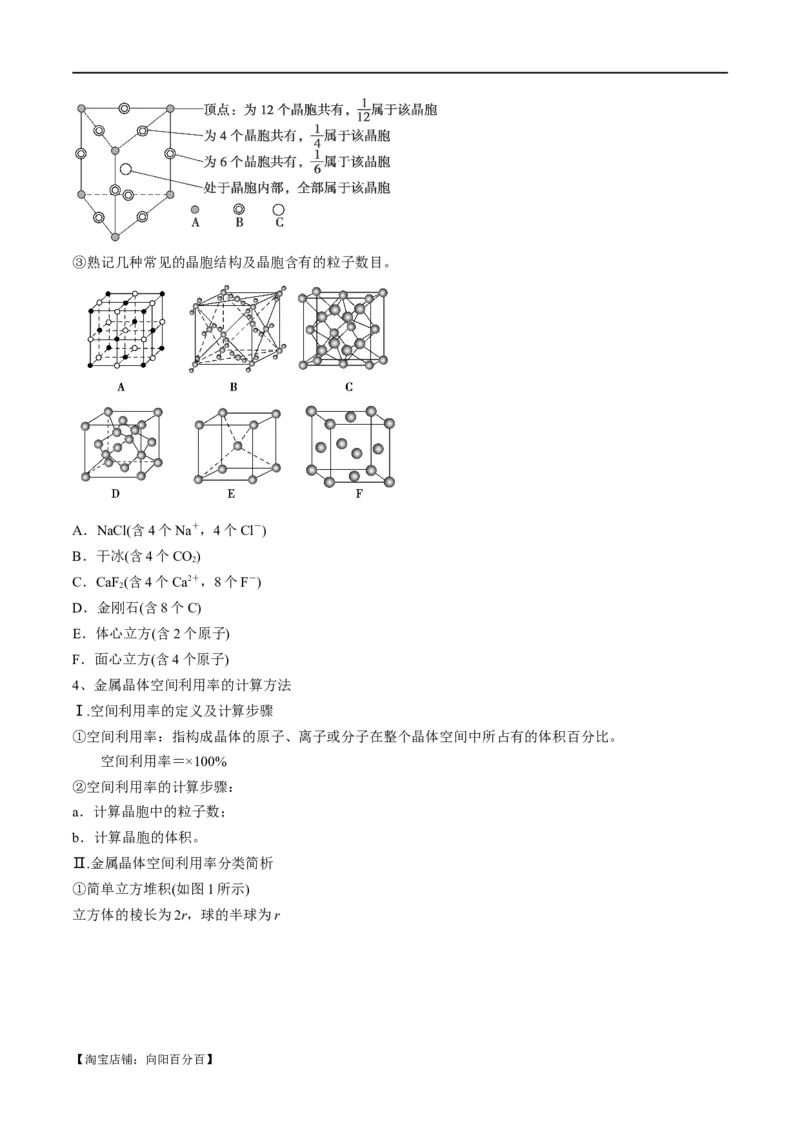
②非长方体(非正方体)晶胞中粒子对晶胞的贡献视具体情况而定。如石墨晶胞每一层内碳原子排成六边形,
其顶点(1个碳原子)对六边形的贡献为。在如图所示的正三棱柱形晶胞中:
【淘宝店铺:向阳百分百】③熟记几种常见的晶胞结构及晶胞含有的粒子数目。
A.NaCl(含4个Na+,4个Cl-)
B.干冰(含4个CO)
2
C.CaF (含4个Ca2+,8个F-)
2
D.金刚石(含8个C)
E.体心立方(含2个原子)
F.面心立方(含4个原子)
4、金属晶体空间利用率的计算方法
Ⅰ.空间利用率的定义及计算步骤
①空间利用率:指构成晶体的原子、离子或分子在整个晶体空间中所占有的体积百分比。
空间利用率=×100%
②空间利用率的计算步骤:
a.计算晶胞中的粒子数;
b.计算晶胞的体积。
Ⅱ.金属晶体空间利用率分类简析
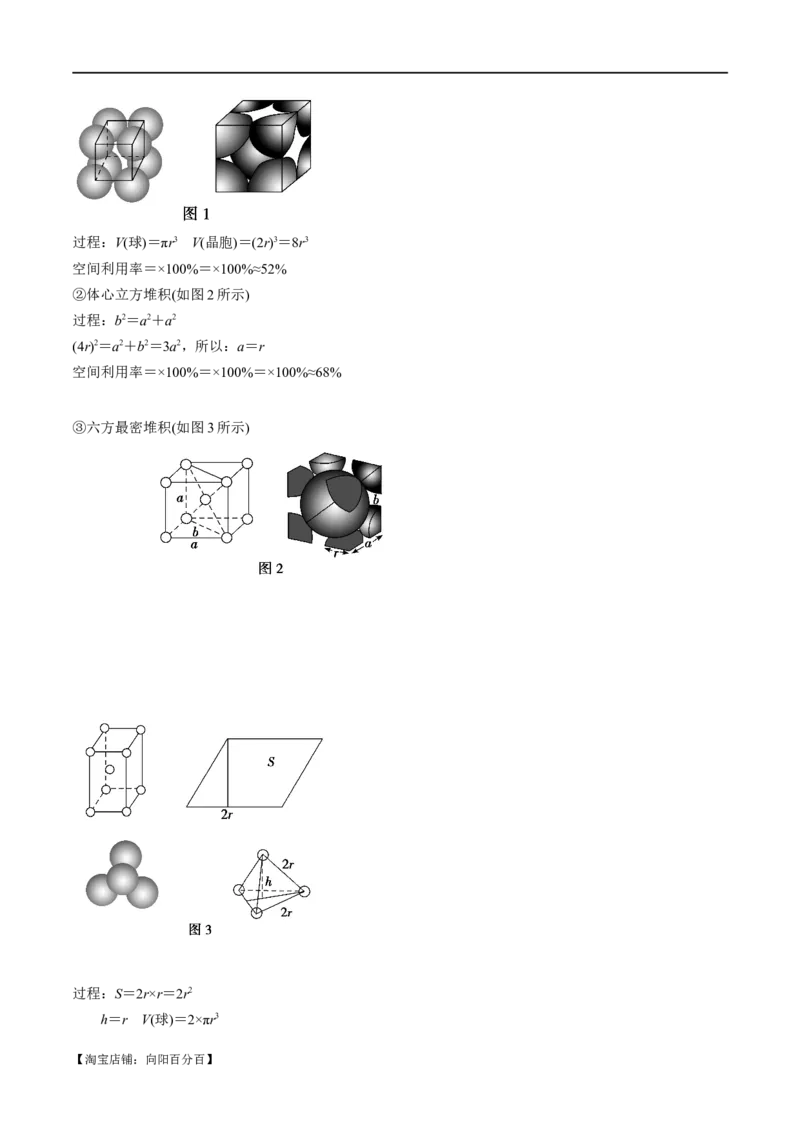
①简单立方堆积(如图1所示)
立方体的棱长为2r,球的半球为r
【淘宝店铺:向阳百分百】过程:V(球)=πr3 V(晶胞)=(2r)3=8r3
空间利用率=×100%=×100%≈52%
②体心立方堆积(如图2所示)
过程:b2=a2+a2
(4r)2=a2+b2=3a2,所以:a=r
空间利用率=×100%=×100%=×100%≈68%
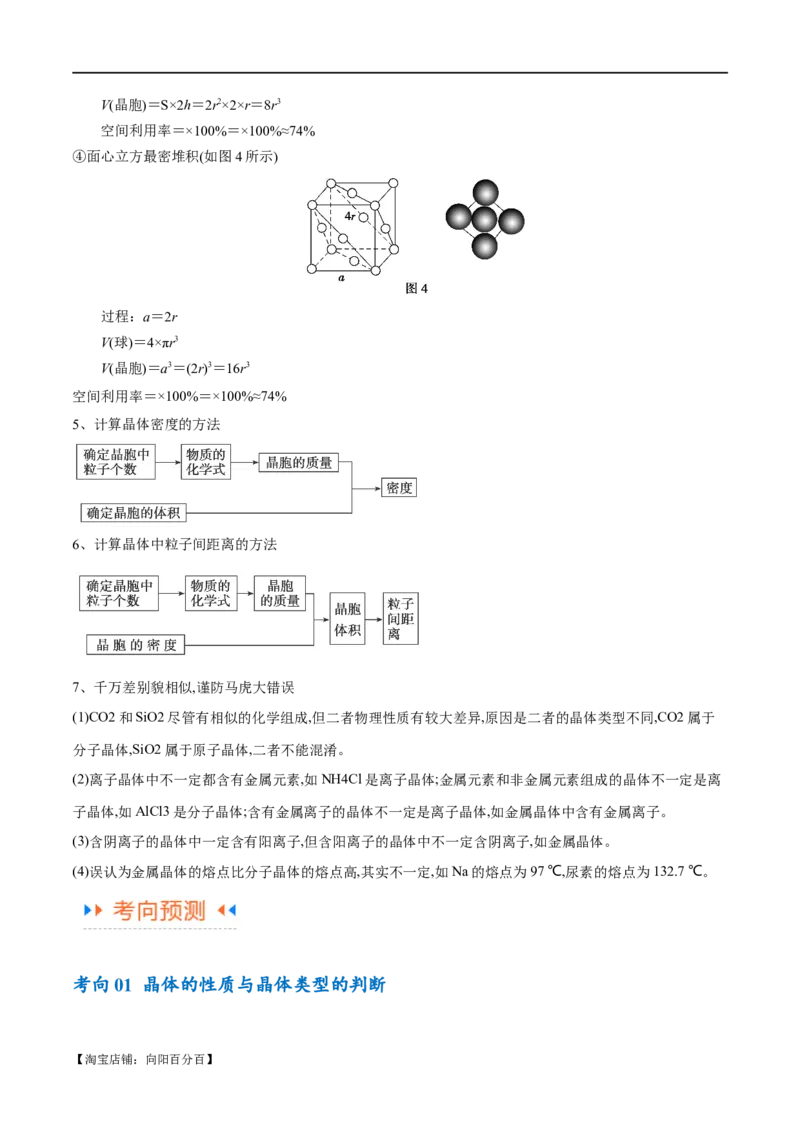
③六方最密堆积(如图3所示)
过程:S=2r×r=2r2
h=r V(球)=2×πr3
【淘宝店铺:向阳百分百】V(晶胞)=S×2h=2r2×2×r=8r3
空间利用率=×100%=×100%≈74%
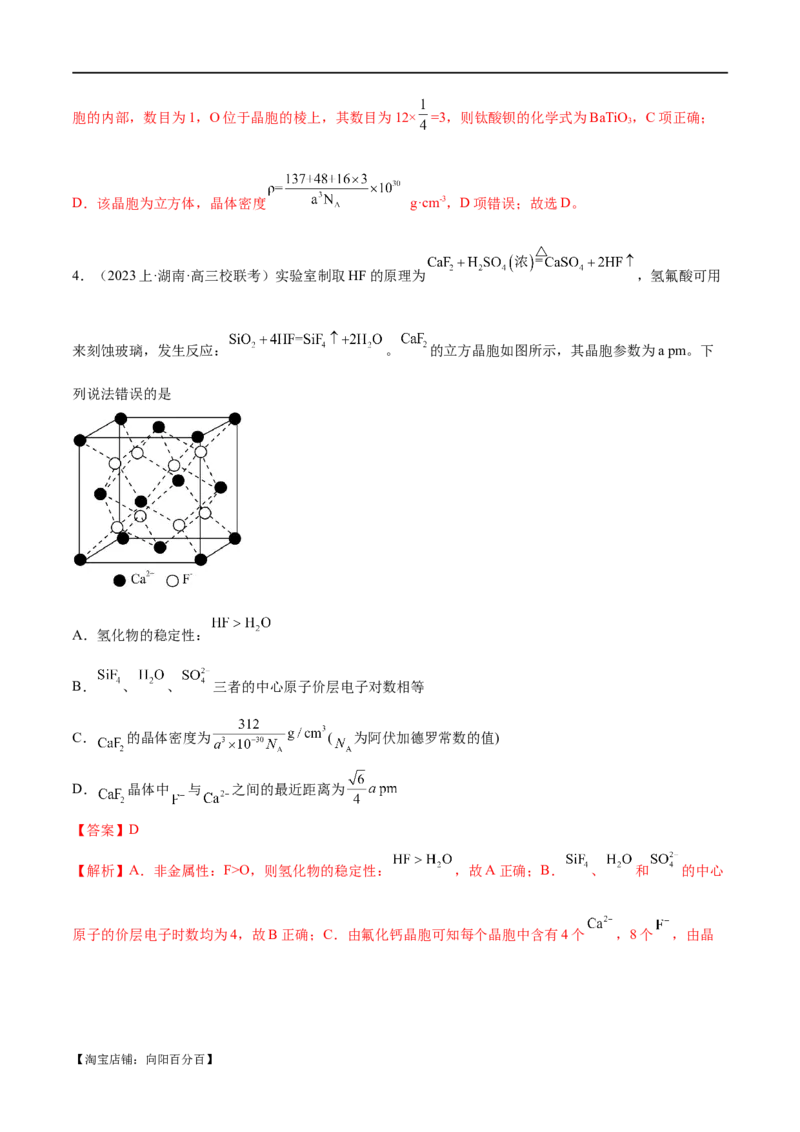
④面心立方最密堆积(如图4所示)
过程:a=2r
V(球)=4×πr3
V(晶胞)=a3=(2r)3=16r3
空间利用率=×100%=×100%≈74%
5、计算晶体密度的方法
6、计算晶体中粒子间距离的方法
7、千万差别貌相似,谨防马虎大错误
(1)CO2和SiO2尽管有相似的化学组成,但二者物理性质有较大差异,原因是二者的晶体类型不同,CO2属于
分子晶体,SiO2属于原子晶体,二者不能混淆。
(2)离子晶体中不一定都含有金属元素,如NH4Cl是离子晶体;金属元素和非金属元素组成的晶体不一定是离
子晶体,如AlCl3是分子晶体;含有金属离子的晶体不一定是离子晶体,如金属晶体中含有金属离子。
(3)含阴离子的晶体中一定含有阳离子,但含阳离子的晶体中不一定含阴离子,如金属晶体。
(4)误认为金属晶体的熔点比分子晶体的熔点高,其实不一定,如Na的熔点为97 ℃,尿素的熔点为132.7 ℃。
考向01 晶体的性质与晶体类型的判断
【淘宝店铺:向阳百分百】1.(2023·湖北·武汉二中校联考二模)纳米 为无定形(非晶态)白色粉末,颗粒尺寸小、微孔多、比表
面积大、对紫外线反射能力强等特点。下列关于纳米 的说法正确的是
A.对光有各向异性
B.熔点与晶体 相同
C.与晶体 互为同分异构体
D.可用X-射线衍射实验区分纳米 与晶体
【答案】D
【解析】A.纳米 为无定形,不是晶体,没有对光的各向异性,故A错误;B.纳米 不是晶体,
是共价晶体,因此熔点不相同,故B错误;C.具有相同分子式而结构不同的化合物互为同分异构体,
只是化学式,晶体 中没有分子,故C错误;D.纳米 不是晶体, 是共价晶体,可用X-
射线衍射实验区分纳米 与晶体 ,故D正确;故选D。
2.(2023·浙江·校联考三模)下列物质含有非极性共价键且属于分子晶体的是
A. B. C. D.
【答案】A
【解析】A.HO 结构式为H-O-O-H,属于分子晶体,含有极性共价键、非极性共价键,故A符合题意;
2 2
B.NaS属于离子晶体,含有离子键,故B不符合题意;C.CO 属于分子晶体,其结构式为O=C=O,含
2 2
有极性共价键,故C不符合题意;D.过氧化钠属于离子晶体,含有离子键和非极性共价键,故D不符合
题意;答案为A。
3.(2023·浙江宁波·统考模拟预测)2023年诺贝尔化学奖授予三位探索纳米和量子点领域的科学家。纳米
晶体具有颗粒尺寸小、微孔多、比表面积大、对紫外线反射能力强等特点。下列关于纳米 晶体的
说法正确的是
【淘宝店铺:向阳百分百】A.熔点低于大块 晶体
B.属于胶体,能产生丁达尔效应
C.与大块 晶体属于同分异构体
D.与NaOH、HF都能反应,属于两性氧化物
【答案】A
【解析】A.纳米SiO 晶体颗粒尺寸小,相对大块 晶体来说,其中有一部分共价键断裂,熔化时需要
2
克服的作用力小一些,熔点低一些,故A正确;B.纳米SiO 晶体是纯净物,而胶体是混合物,故B错误;
2
C.纳米SiO 晶体和大块SiO 晶体都是共价晶体,由原子构成,没有分子式,不属于同分异构体,故C错
2 2
误;D.SiO 能与NaOH反应生成盐硅酸钠和水,SiO 能和HF都能反应,但是SiO 不是和所有的酸都能
2 2 2
反应,只能和HF反应,和其他酸不反应,是酸性氧化物不是两性氧化物,故D 错误;故答案为:A。
4.(2023·北京朝阳·统考一模)我国科学家预言的T-碳已被合成。T-碳的晶体结构可看做将金刚石中的碳
原子用由四个碳原子组成的正四面体结构单元取代所得,T-碳和金刚石的晶胞如图所示。下列说法不正确
的是
A.T-碳与金刚石互为同素异形体
B.T-碳与金刚石均属于共价晶体
C.T-碳与金刚石中键角均为
D.T-碳晶胞中平均含有32个碳原子
【答案】C
【解析】A.T-碳与金刚石均为碳的单质,结构不同,互为同素异形体,故A正确;B.由晶胞结构可知T-
碳也是以四面体为结构单元的空间网状结构,两者均为共价晶体,故B正确;C.T-碳中4个碳原子围成
正四面体结构,该结构中键角为60°,故C错误;D.由晶胞结构可知,在T-碳晶胞中四个碳原子组成的正
【淘宝店铺:向阳百分百】四面体结构单元有8个位于顶点,6个位于面心,4个位于体内,个数为: ,则碳原子个
数为32,故D正确;故选:C。
6.(2023·广东·统考二模)六氟磷酸盐离子液体可用于有机合成的溶剂和催化剂,其结构如图所示,下列
说法错误的是
A.阳离子中碳原子有 和 两种杂化方式
B.阴、阳离子体积较大,离子之间作用力较弱,晶体的熔点较低
C.该物质中存在的化学键类型:离子键、共价键
D.所有原子均符合8电子稳定结构
【答案】D
【解析】A.阳离子中饱和碳原子为 杂化,碳碳双键两端的碳为 杂化,A正确;B.该物质为离子晶
体,但是由于阴、阳离子体积较大,离子之间作用力较弱,导致其晶体的熔点较低,B正确;C.阴阳离
子间存在离子键,阴阳离子内部存在共价键,C正确;D.氢原子不符合8电子稳定结构,D错误;故选
D。
考向02 有关晶体计算
1.(2023·广东梅州·统考三模) 晶体的晶胞结构如图所示。下列说法不正确的是
A.阴、阳离子个数比为
【淘宝店铺:向阳百分百】B. 晶体中距离 最近的 的数目为12
C.若晶胞边长均为 ,则 和 之间的最短距离为
D.阳离子位于由阴离子构成的正八面体空隙中
【答案】C
【解析】A. 位于顶点和面心,个数为 , 位于棱心和体心,个数为 ,阴、
阳离子个数比为 ,A项正确;B. 晶体的晶胞中,该晶体中距离 最近的 的数目为12,B项
正确;C. 与 之间的最短距离等于晶胞面对角线的一半,即 和 之间的最短距离为 ,C
项错误;D.由晶胞结构可知,晶胞中心的阳离子位于由阴离子构成的正八面体的中心,D项正确;故选
C。
2.(2023·辽宁阜新·阜新实验中学校考模拟预测)砷化镓是一种立方晶系如图甲所示,将Mn掺杂到晶体
中得到稀磁性半导体材料如图乙所示,砷化镓的晶胞密度为gcm-3。下列说法错误的是
A.1mol砷化镓中配位键的数目是4N
A
B.掺入Mn的晶体中Mn、Ga、As的原子个数比为5:26:32
C.沿体对角线a→b方向投影图如丙,若c在11处,则As的位置为7、9、11、13
D.该晶体中距离最近的两个镓原子之间的距离为 pm
【答案】B
【解析】A.由图甲知,1个As与4个Ga形成As-Ga共价键,即砷化镓中As的配位数为4,则1mol砷化
镓中配位键的数目是4N ,A正确;B.掺入Mn的晶体中Ga有7个位于顶点,5个位于面心,个数为:
A
【淘宝店铺:向阳百分百】;As有4个位于体内,Mn有1个位于顶点,1个位于面心,个数为: ;
Mn、Ga、As的原子个数比为 : :4=5:27:32,B错误;C.由砷化镓晶胞结构可知,c位于侧面的
面心,沿体对角线a→b方向投影图如丙,则As的位置为7、9、11、13,C正确;D.由晶胞结构可知,
距离最近的两个镓原子之间的距离为面对角线的一半,晶胞中含4个Ga和4个As,晶胞质量为 ,晶
胞体积为 ,则晶胞边长为: pm,两个镓原子之间的最近距离为 pm,
D正确;故选:B。
3.(2023上·湖南长沙·高三长郡中学校考开学考试)钛酸钡是太阳能电池材料。经X射线衍射分析测定,
钛酸钡的晶胞结构如图所示(Ti4+、Ba2+均与O2-接触),已知晶胞边长为a pm,O2-的半径为b pm,N 为阿伏
A
加德罗常数的值。下列叙述错误的是
A.8个Ti4+与Ba2+等距离且最近 B.Ti4+半径为 pm
C.钛酸钡的化学式为BaTiO D.钛酸钡的密度ρ= ×1021 g·cm-3
3
【答案】D
【解析】A.观察晶胞图示,钡离子位于体心,8个位于顶点的钛离子与钡离子最近,A项正确;B.已知
晶胞边长为apm,O2-的半径为bpm,根据图示,晶胞边长=2r(Ti4+)+2r(O2-)=apm,则r(Ti4+)=
pm,B项正确;C.根据晶胞图示,Ti位于晶胞的顶点,Ti的数目为8× =l,Ba位于晶
【淘宝店铺:向阳百分百】胞的内部,数目为1,O位于晶胞的棱上,其数目为12× =3,则钛酸钡的化学式为BaTiO ,C项正确;
3
D.该晶胞为立方体,晶体密度 g·cm-3,D项错误;故选D。
4.(2023上·湖南·高三校联考)实验室制取HF的原理为 ,氢氟酸可用
来刻蚀玻璃,发生反应: 。 的立方晶胞如图所示,其晶胞参数为a pm。下
列说法错误的是
A.氢化物的稳定性:
B. 、 、 三者的中心原子价层电子对数相等
C. 的晶体密度为 ( 为阿伏加德罗常数的值)
D. 晶体中 与 之间的最近距离为
【答案】D
【解析】A.非金属性:F>O,则氢化物的稳定性: ,故A正确;B. 、 和 的中心
原子的价层电子时数均为4,故B正确;C.由氟化钙晶胞可知每个晶胞中含有4个 ,8个 ,由晶
【淘宝店铺:向阳百分百】胞结构可知其密度为 故C正确;D. 晶体中 为面心立方最密堆积, 位于
围成的正四面体的空隙中, 与 之间的最近距离为立方晶胞体对角线长的 ,即为 ,故
D错误;答案选D。
5.(2023·辽宁·校联考三模)一种由Cu、In、Te组成的晶体属四方晶系,晶胞参数如图所示,晶胞棱边
夹角均为90°,晶体中Te原子填充在Cu、In围成的四面体空隙中,A点、B点原子的分数坐标分别为
、 ,下列说法错误的是
A.该晶体的化学式为
B.C点原子的分数坐标为
C.晶胞中四面体空隙的占有率为50%
D.晶胞中C、D间距离
【答案】D
【解析】A.晶胞中位于顶点、面上、和体内的Cu原子个数= ,位于面上、棱上的In原
子个数= ,位于体内的Te原子个数=8×1=8,则Cu、In、Te的原子个数比为4:4:8=1:1:2,晶
【淘宝店铺:向阳百分百】体的化学式为CuInTe ,A正确;B.由位于顶点A点和体心B点原子的分数坐标分别为(0,0,0)、
2
可知,晶胞边长为1,则位于体对角线 处,面对角线 处的C原子的分数坐标分别为 ,B正确;
C.由晶胞结构可知,In原子形成的四面体空隙有8个,形成的八面体空隙也有8个,则四面体空隙的占
有率为 ,C正确;D.由晶胞中C、D形成的直角三角形的边长为 pm、 pm可知,
C、D间距离d= ,D错误;答案选D。
微专题 晶胞参数、坐标参数的分析与应用
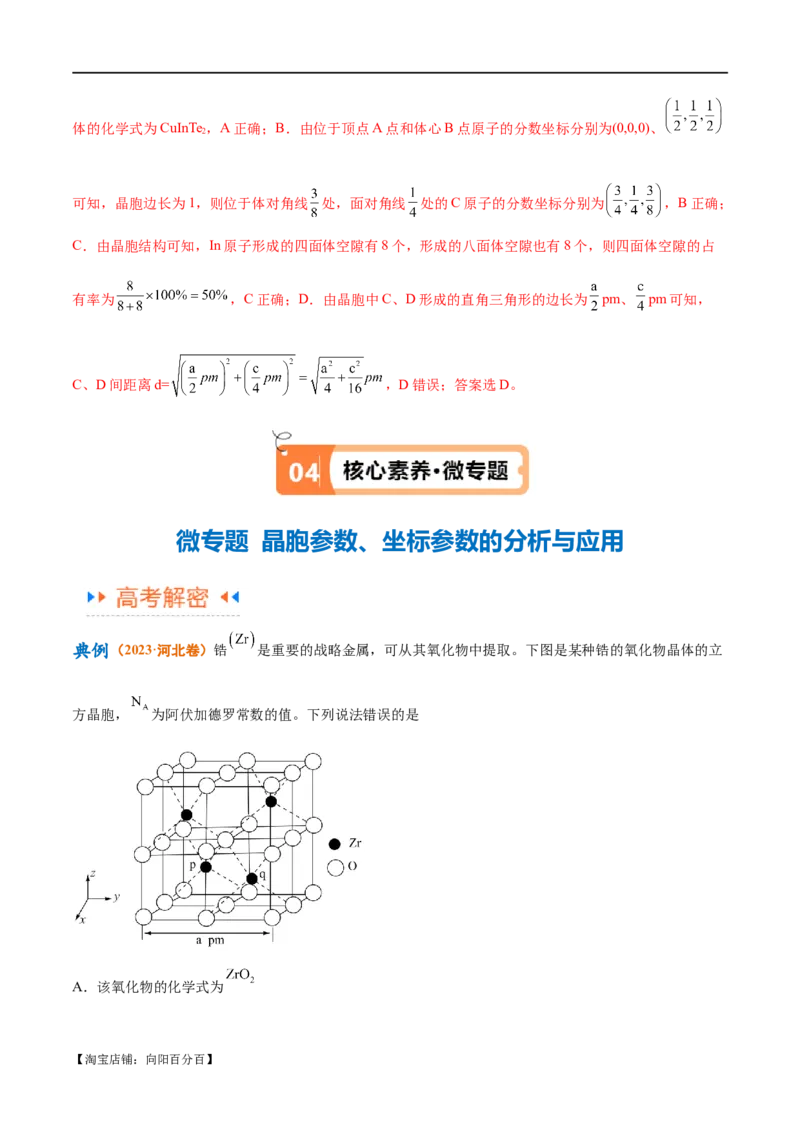
典例(2023·河北卷)锆 是重要的战略金属,可从其氧化物中提取。下图是某种锆的氧化物晶体的立
方晶胞, 为阿伏加德罗常数的值。下列说法错误的是
A.该氧化物的化学式为
【淘宝店铺:向阳百分百】B.该氧化物的密度为
C. 原子之间的最短距离为
D.若坐标取向不变,将p点 原子平移至原点,则q点 原子位于晶胞 面的面心
【答案】B
【解析】A.根据“均摊法”,晶胞中含4个Zr、 个O,则立方氧化锆的化学式为
ZrO,选项A正确;B.结合A分析可知,晶体密度为 ,选项B错
2
误;C. 原子之间的最短距离为面对角线的一般,即 ,选项C正确;D.根据晶胞的位置可知,
若坐标取向不变,将p点 原子平移至原点,则垂直向下,q点 原子位于晶胞 面的面心,选项D正
确;答案选B。
一、原子分数坐标参数
1.概念
原子分数坐标参数,表示晶胞内部各原子的相对位置。
2.原子分数坐标的确定方法
(1)依据已知原子的坐标确定坐标系取向。
(2)一般以坐标轴所在正方体的棱长为1个单位。
(3)从原子所在位置分别向x、y、z轴作垂线,所得坐标轴上的截距即为该原子的分数坐标。
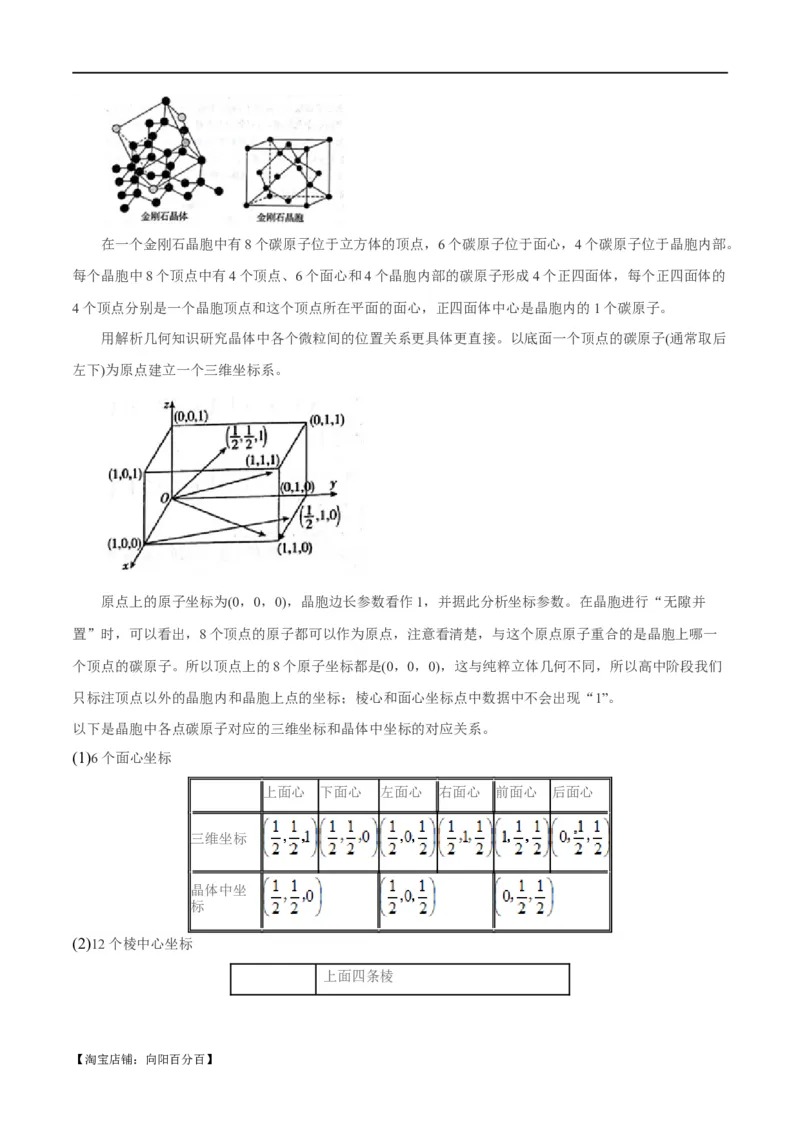
3.金刚石晶胞中碳原子坐标的确定
以金刚石晶胞结构为例,金刚石晶体整体上是正四面体立体网状结构。每个碳原子L能层的4个电子
采用sp3杂化,形成4个等同的杂化轨道,相邻的两个碳原子之间形成σ键。这样每个碳原子与周围4个碳
原子形成4个σ键,每个碳原子都是直接相连的4个碳原子的重心。
【淘宝店铺:向阳百分百】在一个金刚石晶胞中有8个碳原子位于立方体的顶点,6个碳原子位于面心,4个碳原子位于晶胞内部。
每个晶胞中8个顶点中有4个顶点、6个面心和4个晶胞内部的碳原子形成4个正四面体,每个正四面体的
4个顶点分别是一个晶胞顶点和这个顶点所在平面的面心,正四面体中心是晶胞内的1个碳原子。
用解析几何知识研究晶体中各个微粒间的位置关系更具体更直接。以底面一个顶点的碳原子(通常取后
左下)为原点建立一个三维坐标系。
原点上的原子坐标为(0,0,0),晶胞边长参数看作1,并据此分析坐标参数。在晶胞进行“无隙并
置”时,可以看出,8个顶点的原子都可以作为原点,注意看清楚,与这个原点原子重合的是晶胞上哪一
个顶点的碳原子。所以顶点上的8个原子坐标都是(0,0,0),这与纯粹立体几何不同,所以高中阶段我们
只标注顶点以外的晶胞内和晶胞上点的坐标;棱心和面心坐标点中数据中不会出现“1”。
以下是晶胞中各点碳原子对应的三维坐标和晶体中坐标的对应关系。
(1)6个面心坐标
上面心 下面心 左面心 右面心 前面心 后面心
三维坐标
晶体中坐
标
(2)12个棱中心坐标
上面四条棱
【淘宝店铺:向阳百分百】三维坐标
晶体中坐标
下面四条棱
三维坐标
晶体中坐
标
垂直底面四条棱
三维坐标
晶体中坐
标
(3)晶胞内部4个碳原子的坐标
金刚石晶胞有两种取向,由于金刚石晶胞内部有4个碳原子,在空间分布是不对称的,所以从不同方
向观察晶胞时,内部的4个碳原子的位置是不相同的。我们把左边的图叫作取向1,右边的图叫作取向2
它们各自绕竖直中心轴旋转90°,就能够变为对方。金刚石晶胞内4个碳原子坐标:
取向1:
取向2:
所以金刚石晶胞的取向不同时,晶胞内部不对称的4个原子的坐标会发生改变。
4.常见晶胞的原子坐标
【淘宝店铺:向阳百分百】1)金刚石晶胞的原子坐标
(1)取向一:
金刚石晶胞中碳原子的坐标:
8个顶点碳原子的坐标:0,0,0;
6个面中心碳原子的坐标:1/2,0,1/2;1/2,1/2,0;0,1/2,1/2;
4个内部碳原子的坐标:1/4,1/4,3/4;3/4,1/4,1/4;3/4,3/4,3/4;1/4,3/4,1/4;
(2)取向二:
金刚石晶胞中碳原子的坐标:
8个顶点碳原子的坐标:0,0,0;
6个面中心碳原子的坐标:1/2,0,1/2;1/2,1/2,0;0,1/2,1/2;
4个内部碳原子的坐标:1/4,1/4,1/4;3/4,3/4,1/4;3/4,1/4,3/4;1/4,3/4,3/4;
注:金刚石晶胞的取向不同时,即使都是取前左下的顶点原子作原点,晶胞内部不对称的4个碳原子的坐
标,也会发生改变。
2)氟化钙晶体:
每个CaF 晶胞有4个Ca2+和8个F-原子分数坐标如下:
2
【淘宝店铺:向阳百分百】Ca2+: 0,0,0 1/2,1/2,0 1/2,0,1/2 0,1/2,1/2
F-: 1/4,1/4,1/4 3/4,1/4,1/4 1/4,3/4,1/4 1/4,1/4,3/4
3/4,3/4,1/4 3/4,1/4,3/4 1/4,3/4,3/4 3/4,3/4,3/4
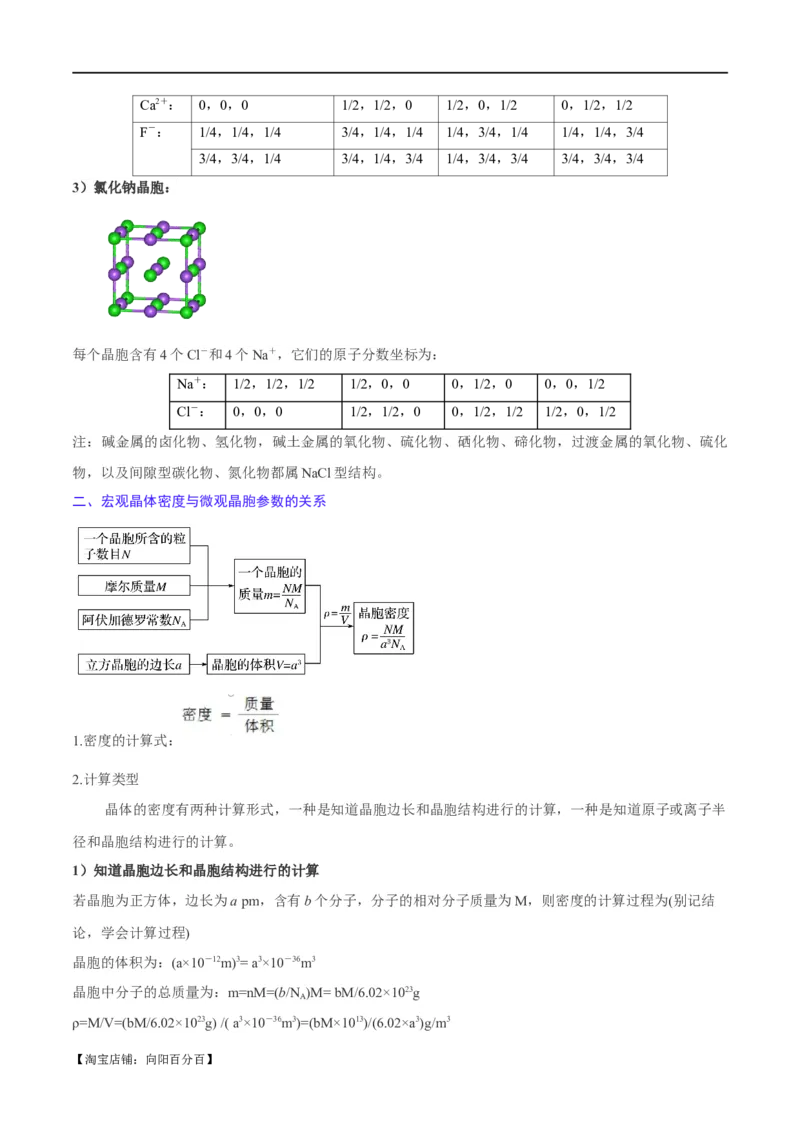
3)氯化钠晶胞:
每个晶胞含有4个Cl-和4个Na+,它们的原子分数坐标为:
Na+: 1/2,1/2,1/2 1/2,0,0 0,1/2,0 0,0,1/2
Cl-: 0,0,0 1/2,1/2,0 0,1/2,1/2 1/2,0,1/2
注:碱金属的卤化物、氢化物,碱土金属的氧化物、硫化物、硒化物、碲化物,过渡金属的氧化物、硫化
物,以及间隙型碳化物、氮化物都属NaCl型结构。
二、宏观晶体密度与微观晶胞参数的关系
1.密度的计算式:
2.计算类型
晶体的密度有两种计算形式,一种是知道晶胞边长和晶胞结构进行的计算,一种是知道原子或离子半
径和晶胞结构进行的计算。
1)知道晶胞边长和晶胞结构进行的计算
若晶胞为正方体,边长为a pm,含有b个分子,分子的相对分子质量为M,则密度的计算过程为(别记结
论,学会计算过程)
晶胞的体积为:(a×10-12m)3= a3×10-36m3
晶胞中分子的总质量为:m=nM=(b/N )M= bM/6.02×1023g
A
ρ=M/V=(bM/6.02×1023g) /( a3×10-36m3)=(bM×1013)/(6.02×a3)g/m3
【淘宝店铺:向阳百分百】(1)CO 分子晶体的密度计算:
2
已知CO 分子晶体的结构如下图(面心立方),晶胞边长为572pm(计算数据)。
2
①晶胞中的分子数目计算:8×1/8+6×1/2=4
一个晶胞中有4个CO。
2
②晶体密度计算:
m=nM=[4/(6.02×1023/mol)]×44g/mol=2.9236×10-22g
V=(572×10-12)3m3=1.8715×10-28m3
ρ=m/V=2.9236×10-22g /1.8715×10-28m3=1.562×106g/m3=1.562g/ cm3。
(2)Po(钋),相对原子质量为209,晶胞边长为336pm。
①晶胞中原子数目计算:8×1/8=1。
②密度计算:
m=nM=[1/(6.02×1023/mol)]×209g/mol=3.472×10-22g
V=(336×10-12)3m3=3.7933×10-29m3
ρ=m/V=3.472×10-22g /3.7933×10-29m3=9.153 ×106g/m3=9.153g/cm3
2)知道原子或离子半径和晶胞结构进行的计算
先用原子或离子的半径计算出晶胞的边长,然后再进行密度计算。
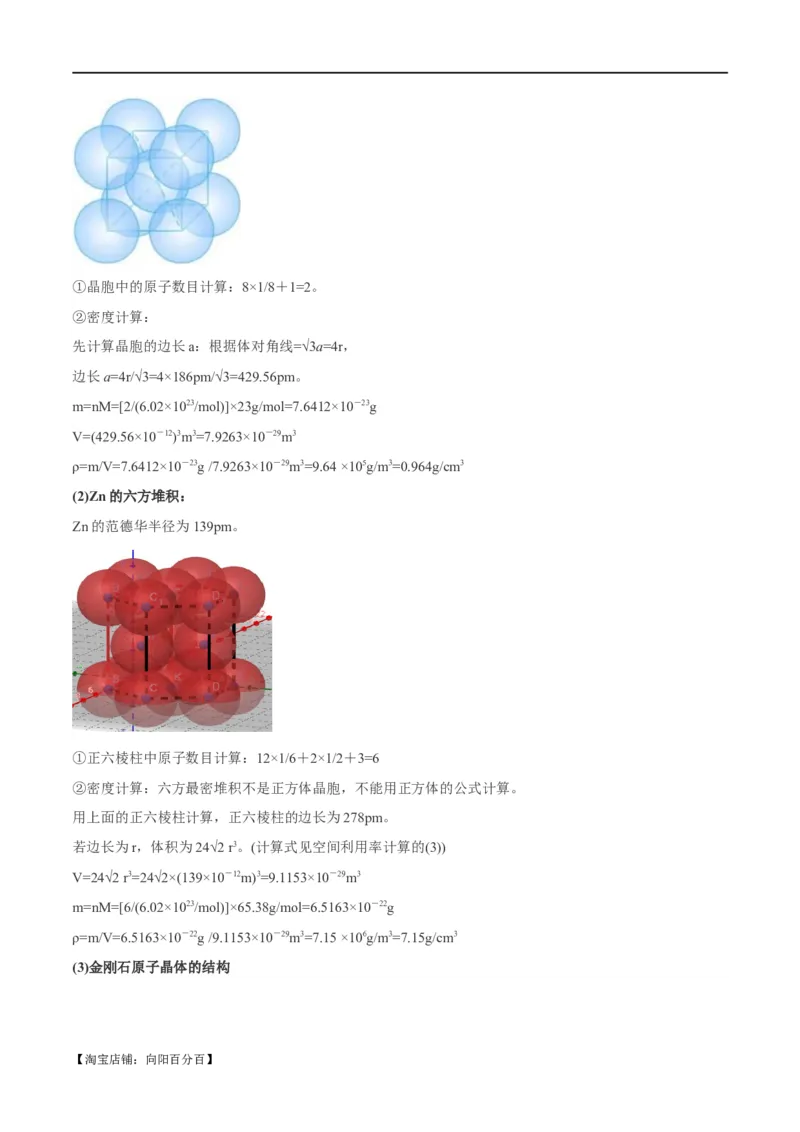
(1)Na的体心立方
Na的原子半径r=186pm。
【淘宝店铺:向阳百分百】①晶胞中的原子数目计算:8×1/8+1=2。
②密度计算:
先计算晶胞的边长a:根据体对角线=√3a=4r,
边长a=4r/√3=4×186pm/√3=429.56pm。
m=nM=[2/(6.02×1023/mol)]×23g/mol=7.6412×10-23g
V=(429.56×10-12)3m3=7.9263×10-29m3
ρ=m/V=7.6412×10-23g /7.9263×10-29m3=9.64 ×105g/m3=0.964g/cm3
(2)Zn的六方堆积:
Zn的范德华半径为139pm。
①正六棱柱中原子数目计算:12×1/6+2×1/2+3=6
②密度计算:六方最密堆积不是正方体晶胞,不能用正方体的公式计算。
用上面的正六棱柱计算,正六棱柱的边长为278pm。
若边长为r,体积为24√2 r3。(计算式见空间利用率计算的(3))
V=24√2 r3=24√2×(139×10-12m)3=9.1153×10-29m3
m=nM=[6/(6.02×1023/mol)]×65.38g/mol=6.5163×10-22g
ρ=m/V=6.5163×10-22g /9.1153×10-29m3=7.15 ×106g/m3=7.15g/cm3
(3)金刚石原子晶体的结构
【淘宝店铺:向阳百分百】①晶胞中的原子数目计算:8×1/8+6×1/2+4=8
②密度计算:以金刚石结构为例,C的共价半径为77pm。
大立方体的边长为8r/√3,即355.65 pm。(计算式见空间利用率计算的(4))
m=nM=[8/(6.02×1023/mol)]×12g/mol=1.5947×10-22g
V=(355.65×10-12)3m3=4.4985×10-29m3
ρ=m/V=1.5947×10-22g /4.4985×10-29m3=3.545 ×106g/m3=3.545g/cm3
(4)离子晶体的密度计算:
①NaCl:Na+的离子半径为95pm,Cl-的离子半径为181pm
晶胞边长的计算:2r(Na+)+2r(Cl-)=552pm。
其中含Na+4个,Cl-4个。
m=nM=[4/(6.02×1023/mol)]×23g/mol+[4/(6.02×1023/mol)]×35.45g/mol=3.8837×10-22g
V=(552×10-12)3m3=1.682×10-28m3
ρ=m/V=3.8837×10-22g /1.682×10-28m3=2.309×106g/m3=2.309g/cm3
②CsCl:Cs+的离子半径为169pm,Cl-的离子半径为181pm。
晶胞边长的计算:[2r(Cs+)+2r(Cl-)]/√3=404.15pm。
【淘宝店铺:向阳百分百】其中含Cs+1个,Cl-1个。
m=nM=[1/(6.02×1023/mol)]×132.9g/mol+[1/(6.02×1023/mol)]×35.45g/mol=2.7965×10-22g
V=(404.15×10-12)3m3=6.6013×10-29m3
ρ=m/V=2.7965×10-22g /6.6013×10-29m3=4.236×106g/m3=4.236g/cm3
③CaF :Ca2+的离子半径为99pm,F-的离子半径为136pm。
2
右侧为晶胞的八分之一
晶胞边长计算为2{[2r(Ca2+)+2r(F-)]/√3}=542.71pm。
其中含Ca2+4个,F-8个,则密度为
M=nm=[4/(6.02×1023/mol)]×40g/mol+[8/(6.02×1023/mol)]×19g/mol=5.1827×10-22g
V=(542.71×10-12)3m3=1.5985×10-28m3
ρ=m/V=5.1827×10-22g /1.5985×10-28m3=3.242×106g/m3=3.242g/cm3
1.(2023·吉林白山·统考三模)Li、Fe、Se可形成新型超导材料,晶胞如图所示(Fe原子均位于面上)。晶
胞棱边夹角均为90°,X的坐标为(0,1, ),Y的坐标为( , , ),设N 为阿伏加德罗常数的值。
A
下列说法正确的是
【淘宝店铺:向阳百分百】已知:以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标
A.基态Fe原子的核外电子排布式为[Ar]3d54s2
B.坐标为( ,1, )的原子是Li原子
C.Se原子X与Se原子Y之间的距离为 nm
D.该晶体的密度为 g·cm-3
【答案】C
【解析】A.Fe为26号元素,基态Fe原子的核外电子排布式为[Ar]3d64s2,故A错误;B.由晶胞结构可
知坐标为( ,1, )的原子是Z原子,即Fe原子,故B错误;C.Se原子X与Se原子Y,沿x轴方向的
距离为 ,沿y轴方向的距离为 ,沿z轴方向的距离为 ,两点间的距离为 nm,故C正确;
D.Li原子有8位于顶点,1个位于体心,个数为: ,Fe有8个位于面上,个数为 ,Se
原子8个位于棱上,2个位于体内,个数为: ,晶胞的质量为: g,
【淘宝店铺:向阳百分百】晶胞体积为: ×10-21 cm3,密度为: g·cm-3,故D错误;故选:C。
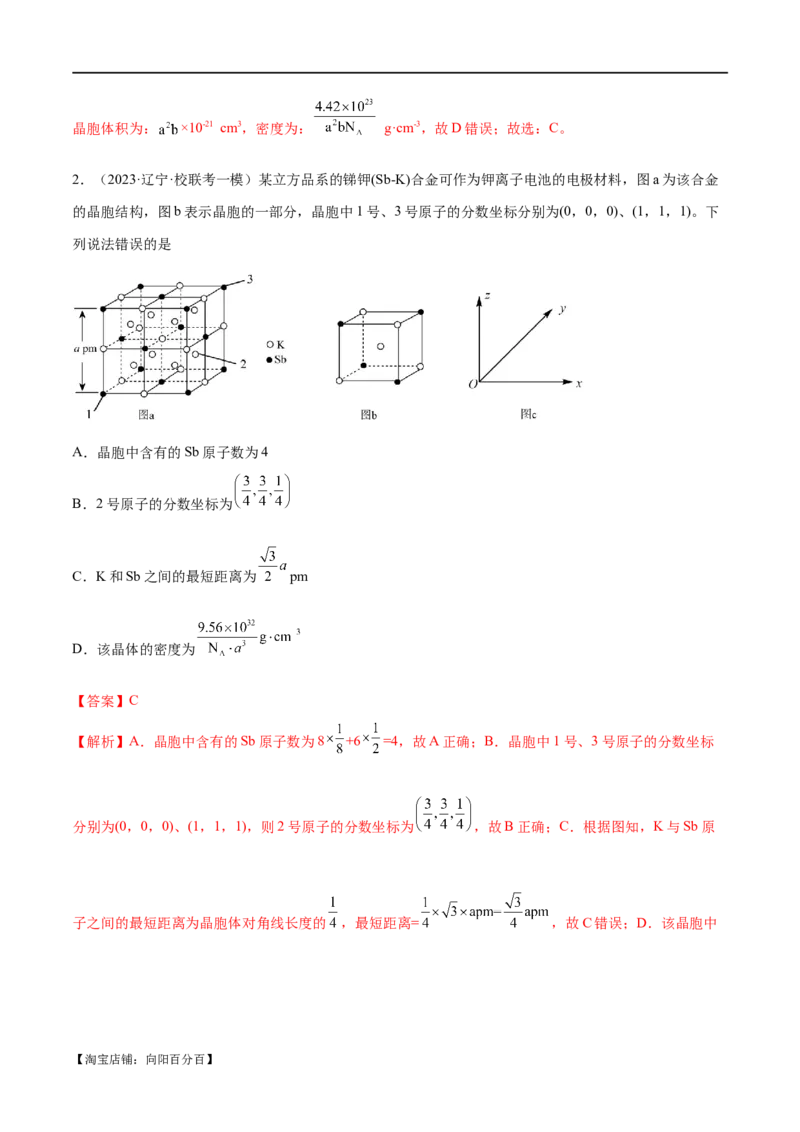
2.(2023·辽宁·校联考一模)某立方品系的锑钾(Sb-K)合金可作为钾离子电池的电极材料,图a为该合金
的晶胞结构,图b表示晶胞的一部分,晶胞中1号、3号原子的分数坐标分别为(0,0,0)、(1,1,1)。下
列说法错误的是
A.晶胞中含有的Sb原子数为4
B.2号原子的分数坐标为
C.K和Sb之间的最短距离为 pm
D.该晶体的密度为
【答案】C
【解析】A.晶胞中含有的Sb原子数为8 +6 =4,故A正确;B.晶胞中1号、3号原子的分数坐标
分别为(0,0,0)、(1,1,1),则2号原子的分数坐标为 ,故B正确;C.根据图知,K与Sb原
子之间的最短距离为晶胞体对角线长度的 ,最短距离= ,故C错误;D.该晶胞中
【淘宝店铺:向阳百分百】Sb原子数为8 +6 =4,K原子个数为12 +9=12,该晶体的密度为 =
,故D正确;故选C。
3.(2023·河北·统考模拟预测)(CHNH )PbI 的晶胞结构如图所示,其中B代表Pb2+,下列说法正确的是
3 3 3
A.Pb2+的价电子排布式为:6s26p2
B.A代表I-
C.若原子分数坐标A为(0,0,0),B为( , , ),则C的原子分数坐标为(0, , )
D.已知CHNH )PbI 的摩尔质量为Mg·mol-1,N 为阿伏加德罗常数的值,则该晶体的密度为
3 3 3 A
g•cm-3
【答案】C
【解析】A. 的价电子排布式为: ,故A错误;B.A位于顶点,个数为1,A代表 ,
故B错误;C.根据晶胞中原子的相对位置可知,若原子分数坐标A为(0,0,0),B为( , , ),则C
的原子分数坐标为(0, , ),故C正确;D. ,故晶体的密度为 ,故D错
误;故选C。
4.(2023·湖南常德·统考一模)作为储氢材料的镧镍合金被广泛应用于电动车辆,某种镧镍合金储氢后所
得晶体的化学式为LaNiH,晶胞结构如图,晶胞参数为a,下列有关表述不正确的是
5 6
【淘宝店铺:向阳百分百】A.Z表示的微粒为H
2
B.每个X原子周围最近且等距离的X原子有6个
C.若A的分数坐标为(0,0.5,0.5),B的分数坐标为(0.75,0.75,0),则C的分数坐标为(1,0.5,1)
D.若四条竖直棱的棱心位置均插入Z,则晶体的化学式为LaNiH
5 7
【答案】D
【解析】A.从晶胞中可以计算,含X原子个数为 =1,含Y原子个数为 =5,含Z个数为
=3,对照晶胞的化学式LaNiH,可得出Z表示的微粒为H,A正确;B.从图中可以看出,每
5 6 2
个X原子周围最近且等距离的X原子在顶点上,数目为6,B正确;C.若A的分数坐标为(0,0.5,0.5),
B的分数坐标为(0.75,0.75,0),则坐标原点为底面左下角的X原子,晶胞参数为1,所以C的分数坐标为
(1,0.5,1),C正确;D.若四条竖直棱的棱心位置均插入Z,则与原晶胞比,增加Z的个数为 =1,
而Z为H,所以晶体的化学式为LaNiH,D不正确;故选D。
2 5 8
5.(2023·广东·统考一模)一种锂的氧化物的晶胞结构如图所示(晶胞参数a=b=c=0.4665nm,晶胞棱边夹
角均为90°)。以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子的分数坐标。
下列有关说法不正确的是
A.该氧化物的化学式为LiO
2
B.O原子之间的最短距离为 ×466.5pm
C.与Li距离最近且相等的O有8个
【淘宝店铺:向阳百分百】D.若p原子的分数坐标为( , , ),则q原子的分数坐标为( , , )
【答案】C
【解析】A.该晶胞中,含Li+个数为8,含O2-个数为 =4,则氧化物的化学式为LiO,A正确;
2
B.从图中可以看出,O原子之间的最短距离为面对角线长度的一半,即为 ×466.5pm,B正确;C.在
晶胞中,Li+与邻近的4个O2-构成正四面体,则与Li距离最近且相等的O有4个,C不正确;D.若p原子
的分数坐标为( , , ),则q原子在x、y、z轴上的分数坐标分别为 、 、 ,从而得出q原子的分
数坐标为( , , ),D正确;故选C。
【淘宝店铺:向阳百分百】