文档内容
专题验收评价
专题 09 化学反应速率与化学平衡
内容概览
A·常考题不丢分
【考点一 化学反应速率及其影响因素和相关计算】
【考点二 化学平衡及其影响因素】
【考点三 化学平衡常数及化学平衡相关计算】
【微专题 图像、图表题的信息提取与应用】
B·综合素养拿高分/拓展培优拿高分
C·挑战真题争满分
【考点一 化学反应速率及其影响因素和相关计算】
1.(2023·辽宁·校联考二模)某温度下,在2L恒容密闭容器中4molNH COONH(s),发生如下反应
2 4
,在0-1min内,CO 的生成速率为0.4mol•L-1•min-1,0-2min内,
2
CO 的生成速率为0.3mol•L-1•min-1,0-3min内,CO 的生成速率为0.2mol•L-1•min-1,下列说法错误的是
2 2
A.当混合气体的平均摩尔质量不变时,标志此反应达到了平衡状态
B.0-1min内,NH COONH(s)的反应速率为62.4g/min
2 4
C.30秒时,CO 的浓度大于0.2mol/L
2
D.2min时,再加入2molNH ,此时反应的V >V
3 逆 正
【答案】A【解析】A.此反应开始时只加入了 ,生成的 和 始终是2∶1,所以当混合气体
的平均摩尔质量不变时,不可以标志此反应达到了平衡状态,A错误;通过三段式计算
,
1min内消耗 0.8mol,质量为62.4g,故反应速率为62.4g/min,B正确;C.由于反应速率
越来越慢,故30秒时, 的浓度大于0.2mol/L,C正确;D.由于反应2min已经达到平衡,当再加入
2mo 时,平衡逆移,故 ,D正确;故选A。
2.(2023上·安徽宣城·高三安徽省郎溪中学校考期中)在 ℃下,向2L恒容密闭容器中充入 气
体,发生反应: 。速率方程 ,
( 、 为速率常数,只与温度、活化能有关)。达到平衡时 的转化率为
50%。若升高温度,达到新平衡时 的转化率增大。下列说法正确的是
A.升高温度, 增大, 减小,
B.当混合气体的密度不变时,反应达到平衡状态
C. ℃下,反应达到平衡时
D. ℃下,平衡时再充入 , 的平衡转化率减小
【答案】D【解析】A.升高温度,正、逆反应速率都增大,正、逆反应速率常数都增大,升高温度,达到新平衡时
的转化率增大,则正反应是吸热反应 ,A错误;B.反应过程中混合气体的体积和质量均不
变,故混合气体的密度一直不变,不能作为反应达到平衡的标志,B错误;C.平衡时,
, , ,平衡时 ,
C错误;D.反应物只有一种气体,正反应是气体分子数增大的反应,充入 ,相当于对原平衡加压(不
改变反应物量),导致 的平衡转化率减小,D正确;故选D。
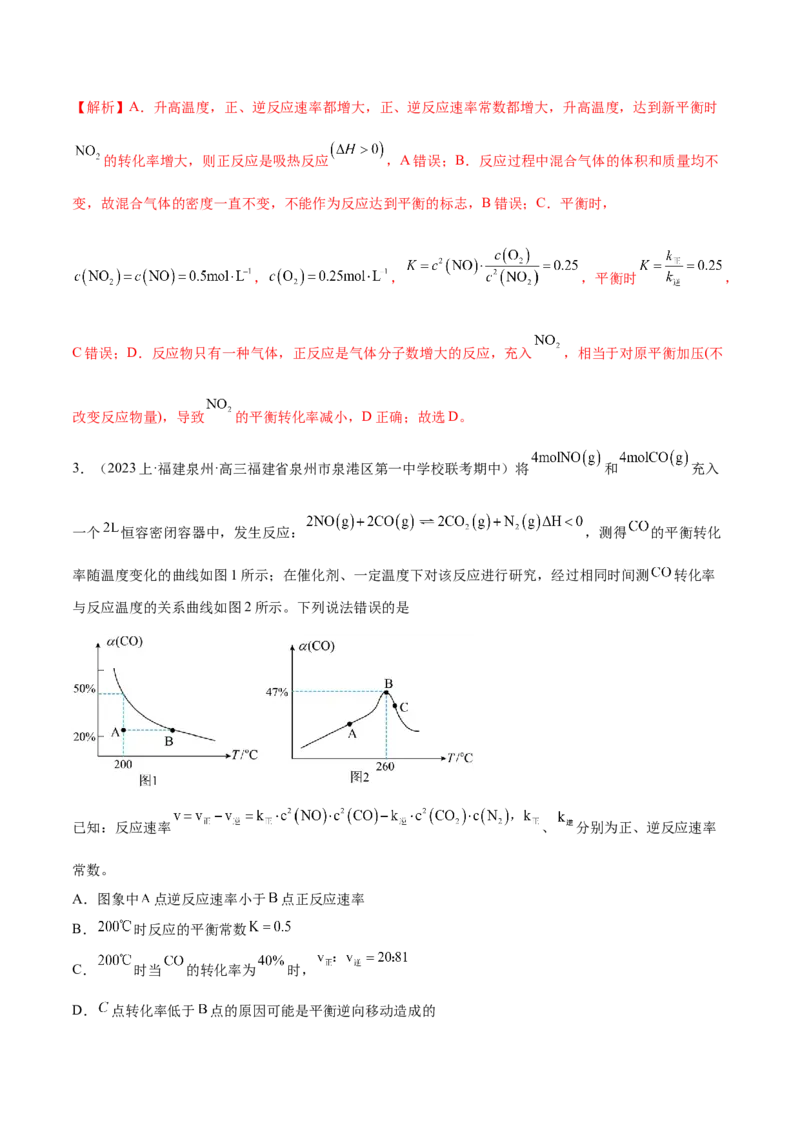
3.(2023上·福建泉州·高三福建省泉州市泉港区第一中学校联考期中)将 和 充入
一个 恒容密闭容器中,发生反应: ,测得 的平衡转化
率随温度变化的曲线如图1所示;在催化剂、一定温度下对该反应进行研究,经过相同时间测 转化率
与反应温度的关系曲线如图2所示。下列说法错误的是
已知:反应速率 、 分别为正、逆反应速率
常数。
A.图象中 点逆反应速率小于 点正反应速率
B. 时反应的平衡常数
C. 时当 的转化率为 时,
D. 点转化率低于 点的原因可能是平衡逆向移动造成的【答案】C
【解析】A. 点为平衡点, 点正反应速率等于逆反应速率,温度越高,反应速率越快, 点温度高于
点,则图象中 点逆反应速率小于 点逆反应速率,即 点逆反应速率小于 点正反应速率,故A正确;
B. 时, 的平衡转化率为 ,列化学平衡三段式,
,故B正确;C.当反应达到平衡时,正逆反应速率
相等, ,则 ,当
的转化率为 时,
起始
转化
平衡
,故C错误;D. 点 转化率最高,说明此时反应恰
好达到平衡状态,该反应为放热反应,升高温度,平衡逆向移动,相同时间 转化率减小,D正确;故
选C。
4.(2023·北京西城·统考一模)探究影响HO 分解速率的影响因素,实验方案如图。
2 2
下列说法不正确的是A.对比①②,可探究FeCl 溶液对HO 分解速率的影响
3 2 2
B.对比②③④,可探究温度对HO 分解速率的影响
2 2
C.HO 是直线形的非极性分子
2 2
D.HO 易溶于水,主要是由于HO 与HO分子之间能形成氢键
2 2 2 2 2
【答案】C
【解析】A.实验②是在实验①的溶液中加入催化剂FeCl ,与实验①做对比实验,可探究FeCl 溶液对
3 3
HO 分解速率的影响,A正确;B.实验②是参照,③、④相当于在②的基础上升高和降低温度,可探究
2 2
温度对HO 分解速率的影响,B正确;C.HO 的分子结构为 ,分子结构不对称,为极性分子,
2 2 2 2
C不正确;D.HO 为极性分子,水也为极性分子,HO 易溶于水,满足相似相溶原理,更主要是HO 与
2 2 2 2 2 2
HO分子之间能形成氢键,D正确;故选C。
2
5.(2023·福建莆田·统考模拟预测)工业上在 催化作用下生产 的反应为
,该反应可看作两步:① (快);
② (慢)。下列说法正确的是
A.该反应活化能为
B.减小 的浓度能降低 的生成速率
C. 的存在使有效碰撞次数增加,降低了该反应的焓变
D.①的活化能一定大于②的活化能
【答案】B
【解析】A. =正反应的活化能-逆反应的活化能=-198kJ/mol,所以逆反应的活化能大于198kJ/mol,故
A错误;B.慢反应是决速步, 是慢反应的反应物,减小 的浓度会降低正反应速率,降低 的生成
速率,故B正确;C. 是催化剂,催化剂不能改变反应的焓变,故C错误;D.反应①是快反应,反
应②是慢反应,活化能越小反应越快,①的活化能小于②的活化能,故D错误;故选B。【考点二 化学平衡及其影响因素】
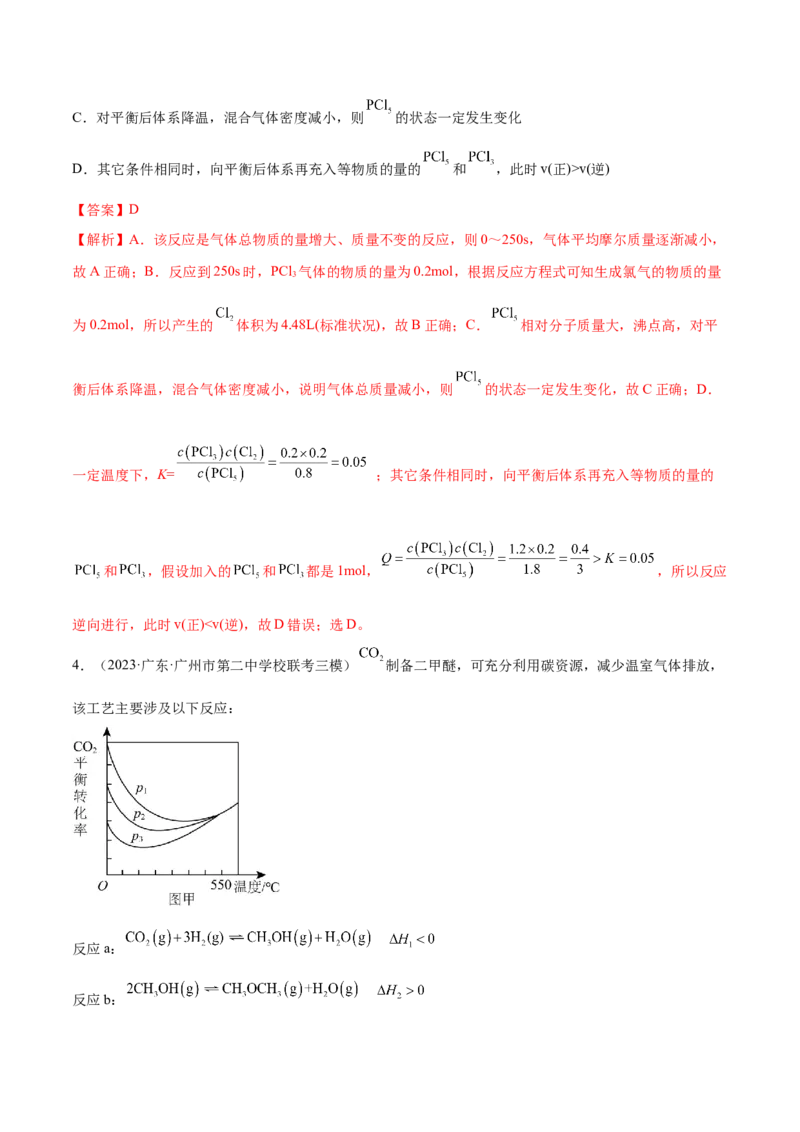
1.(2023·重庆·统考三模)甲烷是一种温室气体,将它转化为高附加值产品甲醇具有重要意义。目前工业
上的甲烷转化大多需要先通过重整生成合成气(CO、 )再转化为甲醇,涉及的反应如下:
反应Ⅰ:
反应Ⅱ:
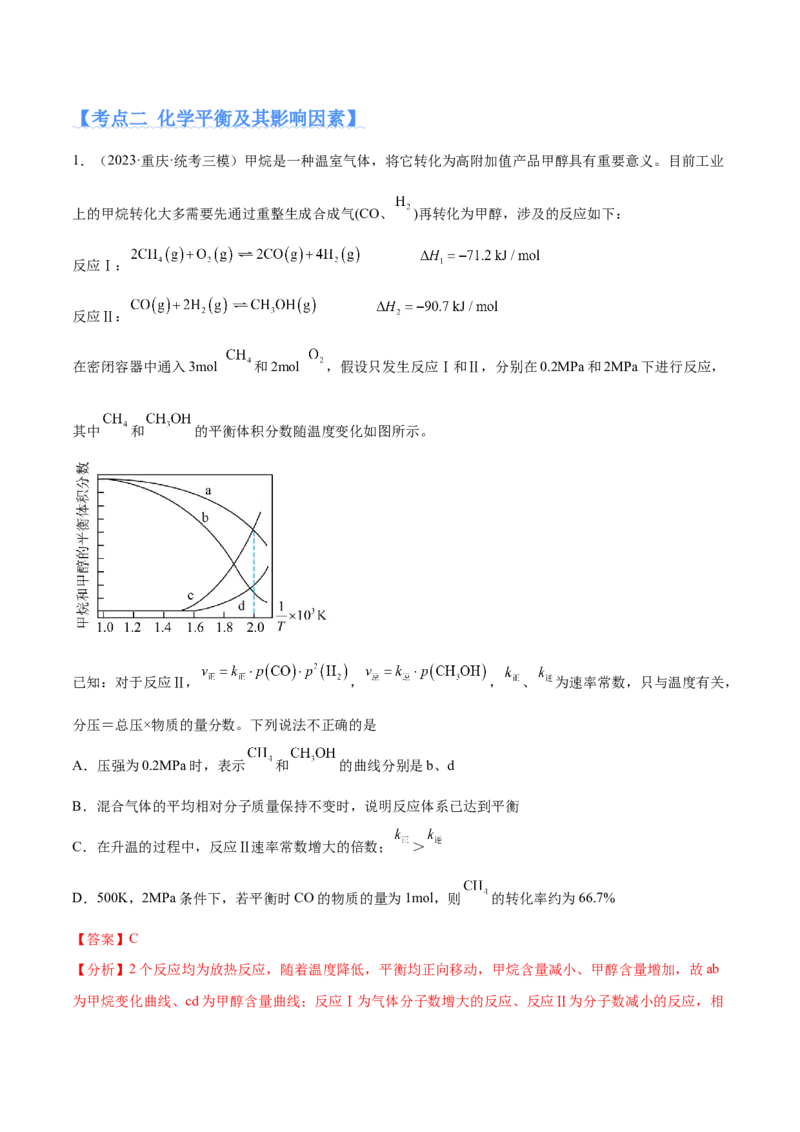
在密闭容器中通入3mol 和2mol ,假设只发生反应Ⅰ和Ⅱ,分别在0.2MPa和2MPa下进行反应,
其中 和 的平衡体积分数随温度变化如图所示。
已知:对于反应Ⅱ, , , 、 为速率常数,只与温度有关,
分压=总压×物质的量分数。下列说法不正确的是
A.压强为0.2MPa时,表示 和 的曲线分别是b、d
B.混合气体的平均相对分子质量保持不变时,说明反应体系已达到平衡
C.在升温的过程中,反应Ⅱ速率常数增大的倍数; >
D.500K,2MPa条件下,若平衡时CO的物质的量为1mol,则 的转化率约为66.7%
【答案】C
【分析】2个反应均为放热反应,随着温度降低,平衡均正向移动,甲烷含量减小、甲醇含量增加,故ab
为甲烷变化曲线、cd为甲醇含量曲线;反应Ⅰ为气体分子数增大的反应、反应Ⅱ为分子数减小的反应,相同条件下,增大压强,反应Ⅰ逆向移动、反应Ⅱ正向移动,使得甲烷含量增加、甲醇含量增大,则bd为
0.2Mpa变化曲线、ac为2Mpa变化曲线;
【解析】A.由分析可知,压强为0.2MPa时,表示 和 的曲线分别是b、d,A正确;B.混合
气体的平均相对分子质量M= m/n,气体质量不变,但是气体的总物质的量随反应进行而改变,所以M会
发生改变,当M不变时,反应达到平衡,B正确;C.已知:对于反应Ⅱ, ,
,当 时,即达到化学平衡态,此时 ,因为反应是放热反应,升温
减小,所以升高温度 变小,所以 增加的倍数更大,C错误;D.在密闭容器中通入3mol
和2mol ,只发生反应Ⅰ和Ⅱ:
由图可知,平衡时,甲烷、甲醇量相等,则3-2a=2a-1,a=1mol, 的转化率约为 66.7%,
D正确;答案选C。
2.(2023·湖南永州·统考三模)T℃,2NO (g) NO g) H<0,该反应正、逆反应速率与浓度的关系为
2 2 4(
△
v =k c2(NO ),v =k c(NO)(k 、k 为速率常数)。结合图像,下列说法错误的是
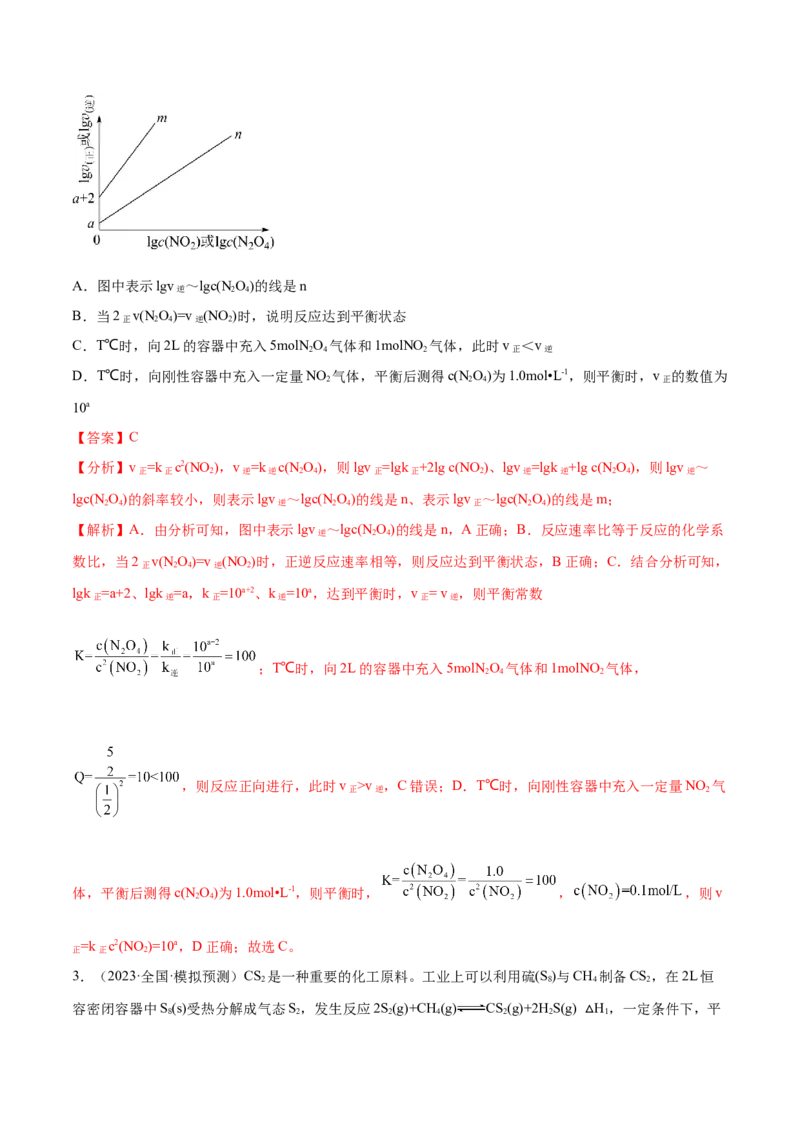
正 正 2 逆 逆 2 4 正 逆A.图中表示lgv ~lgc(N O)的线是n
逆 2 4
B.当2 v(N O)=v (NO )时,说明反应达到平衡状态
正 2 4 逆 2
C.T℃时,向2L的容器中充入5molN O 气体和1molNO 气体,此时v <v
2 4 2 正 逆
D.T℃时,向刚性容器中充入一定量NO 气体,平衡后测得c(NO)为1.0mol•L-1,则平衡时,v 的数值为
2 2 4 正
10a
【答案】C
【分析】v =k c2(NO ),v =k c(NO),则lgv =lgk +2lg c(NO)、lgv =lgk +lg c(N O),则lgv ~
正 正 2 逆 逆 2 4 正 正 2 逆 逆 2 4 逆
lgc(N O)的斜率较小,则表示lgv ~lgc(N O)的线是n、表示lgv ~lgc(N O)的线是m;
2 4 逆 2 4 正 2 4
【解析】A.由分析可知,图中表示lgv ~lgc(N O)的线是n,A正确;B.反应速率比等于反应的化学系
逆 2 4
数比,当2 v(N O)=v (NO )时,正逆反应速率相等,则反应达到平衡状态,B正确;C.结合分析可知,
正 2 4 逆 2
lgk =a+2、lgk =a,k =10a+2、k =10a,达到平衡时,v = v ,则平衡常数
正 逆 正 逆 正 逆
;T℃时,向2L的容器中充入5molN O 气体和1molNO 气体,
2 4 2
,则反应正向进行,此时v >v ,C错误;D.T℃时,向刚性容器中充入一定量NO 气
正 逆 2
体,平衡后测得c(NO)为1.0mol•L-1,则平衡时, , ,则v
2 4
=k c2(NO )=10a,D正确;故选C。
正 正 2
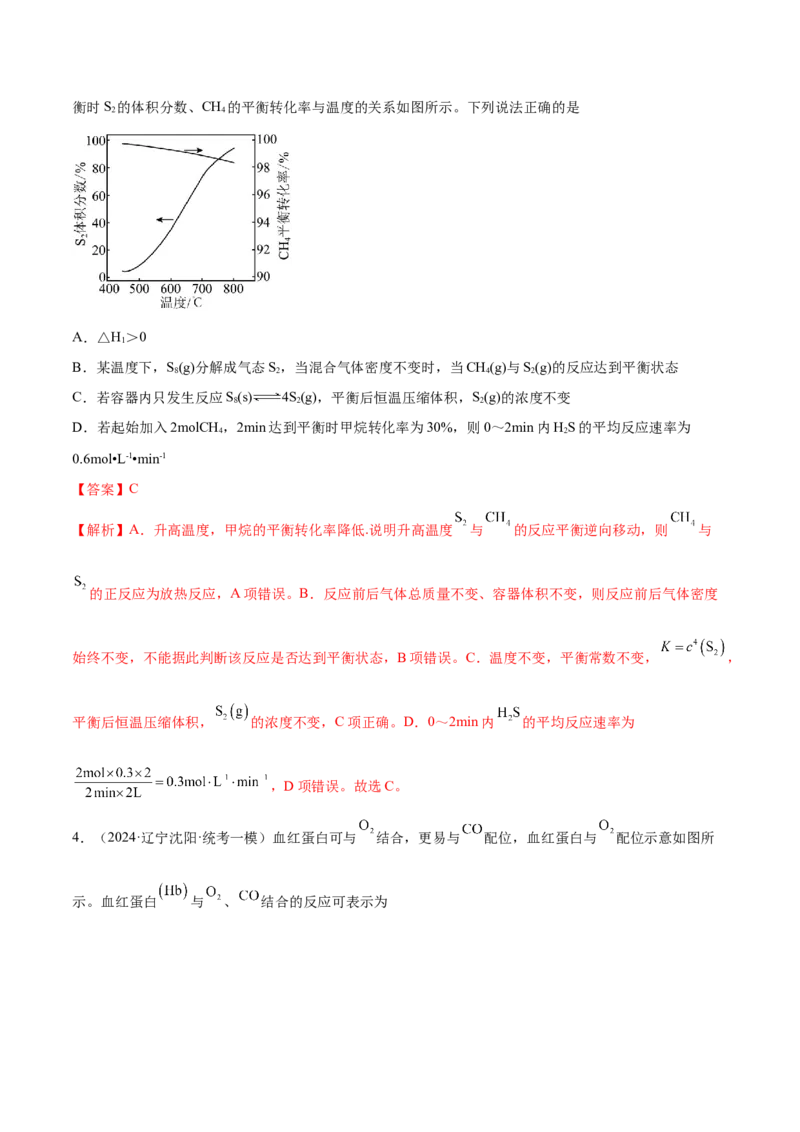
3.(2023·全国·模拟预测)CS 是一种重要的化工原料。工业上可以利用硫(S )与CH 制备CS,在2L恒
2 8 4 2
容密闭容器中S(s)受热分解成气态S,发生反应2S(g)+CH (g) CS(g)+2HS(g) H,一定条件下,平
8 2 2 4 2 2 1
△衡时S 的体积分数、CH 的平衡转化率与温度的关系如图所示。下列说法正确的是
2 4
A.△H>0
1
B.某温度下,S(g)分解成气态S,当混合气体密度不变时,当CH(g)与S(g)的反应达到平衡状态
8 2 4 2
C.若容器内只发生反应S(s) 4S(g),平衡后恒温压缩体积,S(g)的浓度不变
8 2 2
D.若起始加入2molCH ,2min达到平衡时甲烷转化率为30%,则0~2min内HS的平均反应速率为
4 2
0.6mol•L-1•min-1
【答案】C
【解析】A.升高温度,甲烷的平衡转化率降低.说明升高温度 与 的反应平衡逆向移动,则 与
的正反应为放热反应,A项错误。B.反应前后气体总质量不变、容器体积不变,则反应前后气体密度
始终不变,不能据此判断该反应是否达到平衡状态,B项错误。C.温度不变,平衡常数不变, ,
平衡后恒温压缩体积, 的浓度不变,C项正确。D.0~2min内 的平均反应速率为
,D项错误。故选C。
4.(2024·辽宁沈阳·统考一模)血红蛋白可与 结合,更易与 配位,血红蛋白与 配位示意如图所
示。血红蛋白 与 、 结合的反应可表示为①
②
下列说法中错误的是
A.相同温度下, B.反应①②的 、 均小于0
C.图中 的配位数为6 D.用高压氧舱治疗 中毒时,平衡①②均逆向移动
【答案】D
【解析】A.CO也可与血红蛋白配位,它与血红蛋白结合的能力更强,则反应②比反应①正向进行的程度
大,所以相同温度下, ,A正确;B.反应①②分别为O 和CO与血红蛋白中的Fe2+形成配位键的
2
过程,气体分子数减小、形成化学键能够释放能量,故反应反应①②的 、 均小于0,B正确;C.
图中 与周围的6个原子结合,配位数为6,C正确;D. 用高压氧舱治疗 中毒时,氧气浓度增大,
平衡①正向移动导致c(Hb)减小,所以平衡②逆向移动,D不正确;答案选D。
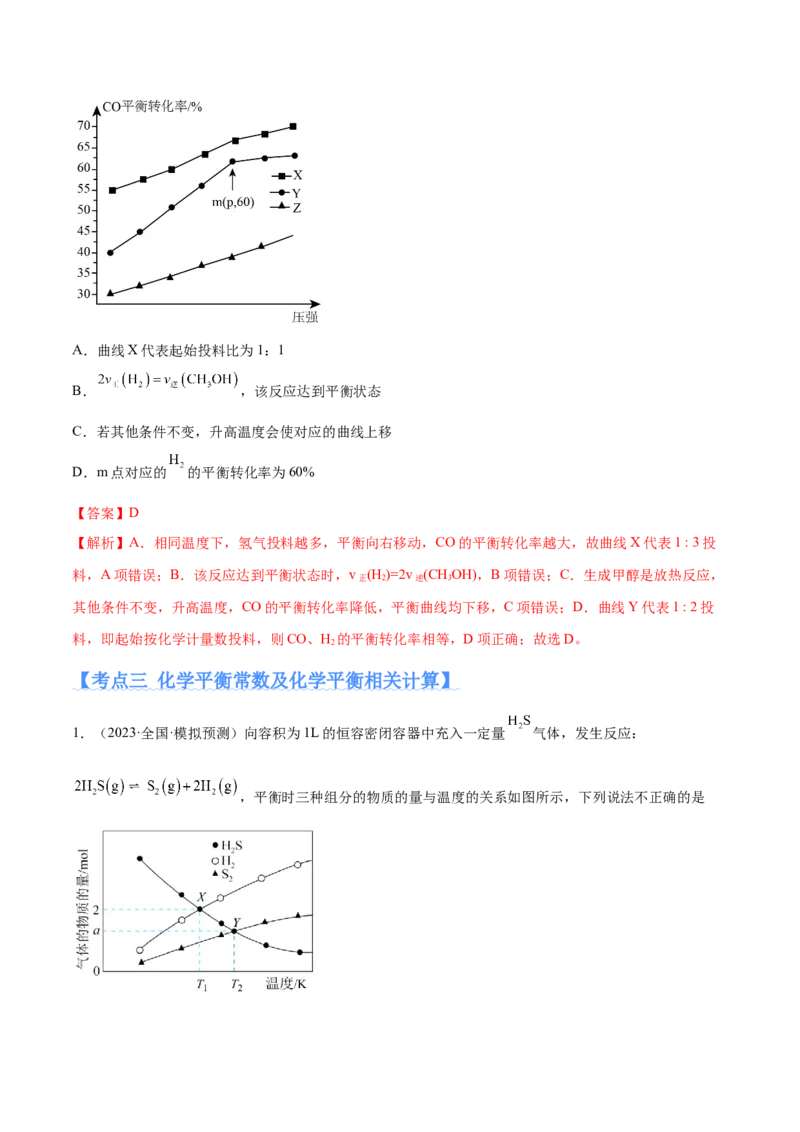
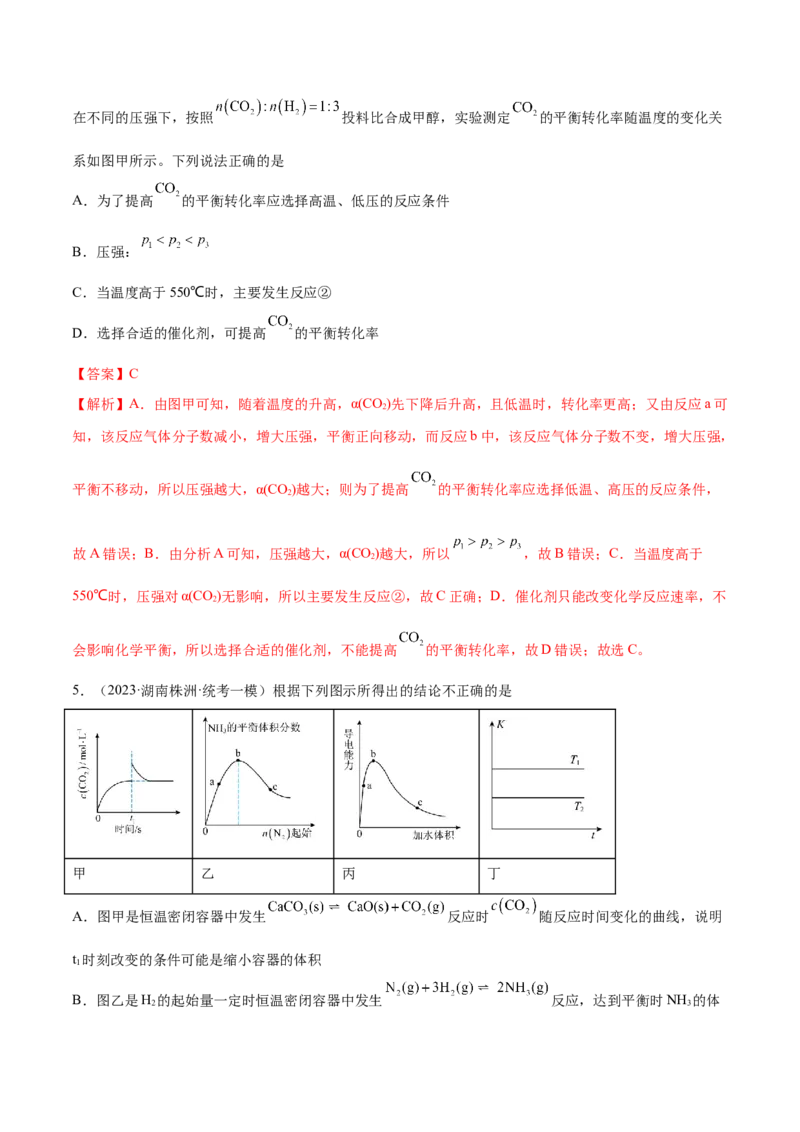
5.(2023·辽宁·校联考模拟预测)在600K下,按初始投料比 分别为1:1、1:2、1:3投料,
发生反应为 。测得不同压强下,CO平衡转化率如图所示。下列叙
述正确的是A.曲线X代表起始投料比为1:1
B. ,该反应达到平衡状态
C.若其他条件不变,升高温度会使对应的曲线上移
D.m点对应的 的平衡转化率为60%
【答案】D
【解析】A.相同温度下,氢气投料越多,平衡向右移动,CO的平衡转化率越大,故曲线X代表1 : 3投
料,A项错误;B.该反应达到平衡状态时,v (H )=2v (CHOH),B项错误;C.生成甲醇是放热反应,
正 2 逆 3
其他条件不变,升高温度,CO的平衡转化率降低,平衡曲线均下移,C项错误;D.曲线Y代表1 : 2投
料,即起始按化学计量数投料,则CO、H 的平衡转化率相等,D项正确;故选D。
2
【考点三 化学平衡常数及化学平衡相关计算】
1.(2023·全国·模拟预测)向容积为1L的恒容密闭容器中充入一定量 气体,发生反应:
,平衡时三种组分的物质的量与温度的关系如图所示,下列说法不正确的是A.该反应在温度为 时的平衡常数小于温度为 时的平衡常数
B.
C.X点时压缩容器容积, 的平衡转化率减小
D. 时,向Y点容器中再充入 和 ,此时
【答案】D
【解析】A.由题图可知,随着温度的升高,平衡体系中 和 的物质的量增大, 的物质的量减小,
即平衡正向移动,说明反应的 ,故该反应在温度为 时的平衡常数小于温度为 时的平衡常数,
A正确;B.由题图可知,X点时, ,即反应消耗了2mol ,体系中还剩余2mol
,故初始充入 的物质的量为4mol,Y点体系中生成 的物质的量为a mol,由
可知, ,解得 ,B正确;C.题给反应为气体总分子数增大的反应,
压缩容器容积相当于增大压强,平衡逆向移动, 的平衡转化率减小,C正确;D.结合B项分析可知,
Y点时, , ,容器容积为1L,则 时,反应的平衡常数
,向Y点容器中再充入 和 ,此时 ,, ,则 ,反应正向进行, ,D错
误;故答案为:D。
2.(2023·北京丰台·统考一模)下列三个化学反应焓变、平衡常数与温度的关系分别如下表所示。下列说
法正确的是
温度
化学反应 平衡常数
973K 1173K
① 1.47 2.15
② 2.38 1.67
③ a b
A.1173K时,反应①起始 ,平衡时 约为0.4
B.反应②是吸热反应,
C.反应③达平衡后,升高温度或缩小反应容器的容积平衡逆向移动
D.相同温度下, ;
【答案】D
【解析】A.1173K时,反应①起始 ,
, ,x≈0.4,平衡时
约为0.2 ,A错误;B.升温,化学平衡常数减小,说明平衡向逆反应方向移动,所以②的正反应为放热反应, ,B错误;C.根据盖斯定律可知②-①可得③,故 ,a=1.62,b=0.78,
升温,化学平衡常数减小,说明平衡向逆反应方向移动,所以 ,反应③达平衡后,升高温度平衡逆
向移动,但是由于反应两端气体的化学计量数之和相等缩小反应容器的容积化学平衡不移动,C错误;
D.相同温度下,根据盖斯定律可知②-①可得③,故 ; ,D正确;故选D。
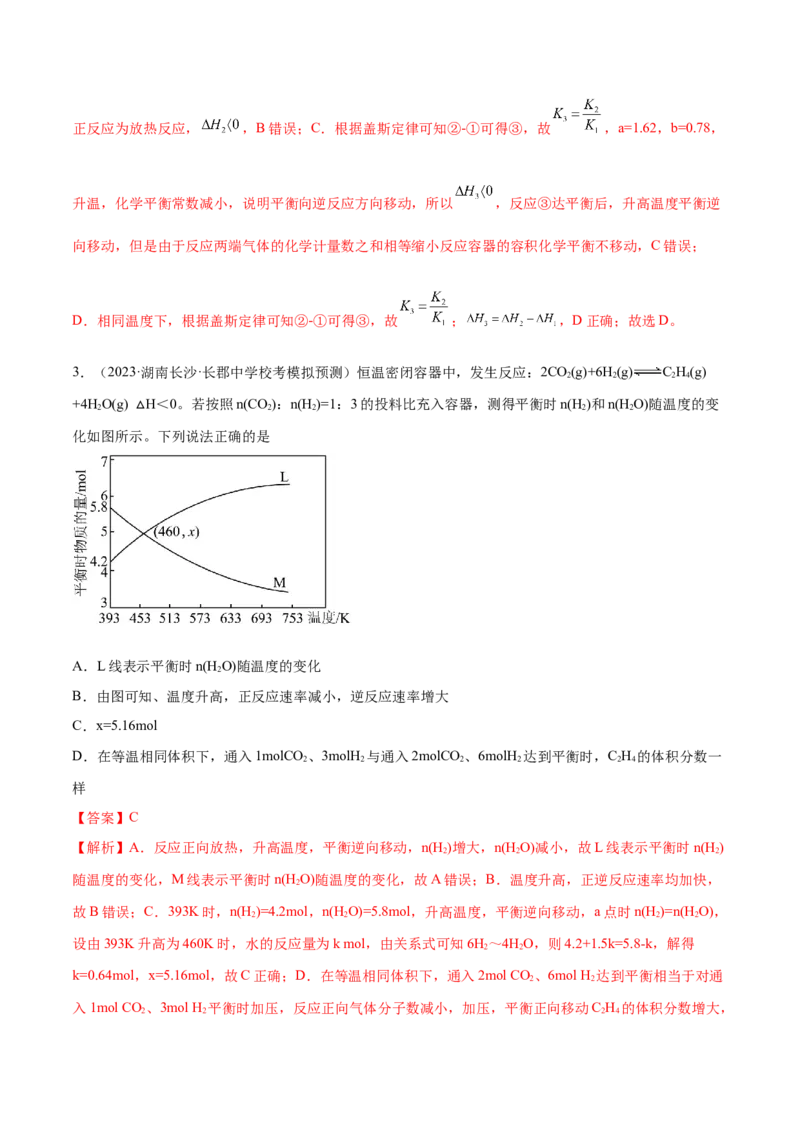
3.(2023·湖南长沙·长郡中学校考模拟预测)恒温密闭容器中,发生反应:2CO(g)+6H(g) C H(g)
2 2 2 4
+4H O(g) H<0。若按照n(CO):n(H )=1:3的投料比充入容器,测得平衡时n(H )和n(H O)随温度的变
2 2 2 2 2
化如图所示△。下列说法正确的是
A.L线表示平衡时n(H O)随温度的变化
2
B.由图可知、温度升高,正反应速率减小,逆反应速率增大
C.x=5.16mol
D.在等温相同体积下,通入1molCO 、3molH 与通入2molCO 、6molH 达到平衡时,C H 的体积分数一
2 2 2 2 2 4
样
【答案】C
【解析】A.反应正向放热,升高温度,平衡逆向移动,n(H )增大,n(H O)减小,故L线表示平衡时n(H )
2 2 2
随温度的变化,M线表示平衡时n(H O)随温度的变化,故A错误;B.温度升高,正逆反应速率均加快,
2
故B错误;C.393K时,n(H )=4.2mol,n(H O)=5.8mol,升高温度,平衡逆向移动,a点时n(H )=n(HO),
2 2 2 2
设由393K升高为460K时,水的反应量为k mol,由关系式可知6H~4HO,则4.2+1.5k=5.8-k,解得
2 2
k=0.64mol,x=5.16mol,故C正确;D.在等温相同体积下,通入2mol CO、6mol H 达到平衡相当于对通
2 2
入1mol CO、3mol H 平衡时加压,反应正向气体分子数减小,加压,平衡正向移动C H 的体积分数增大,
2 2 2 4故D错误;故选C。
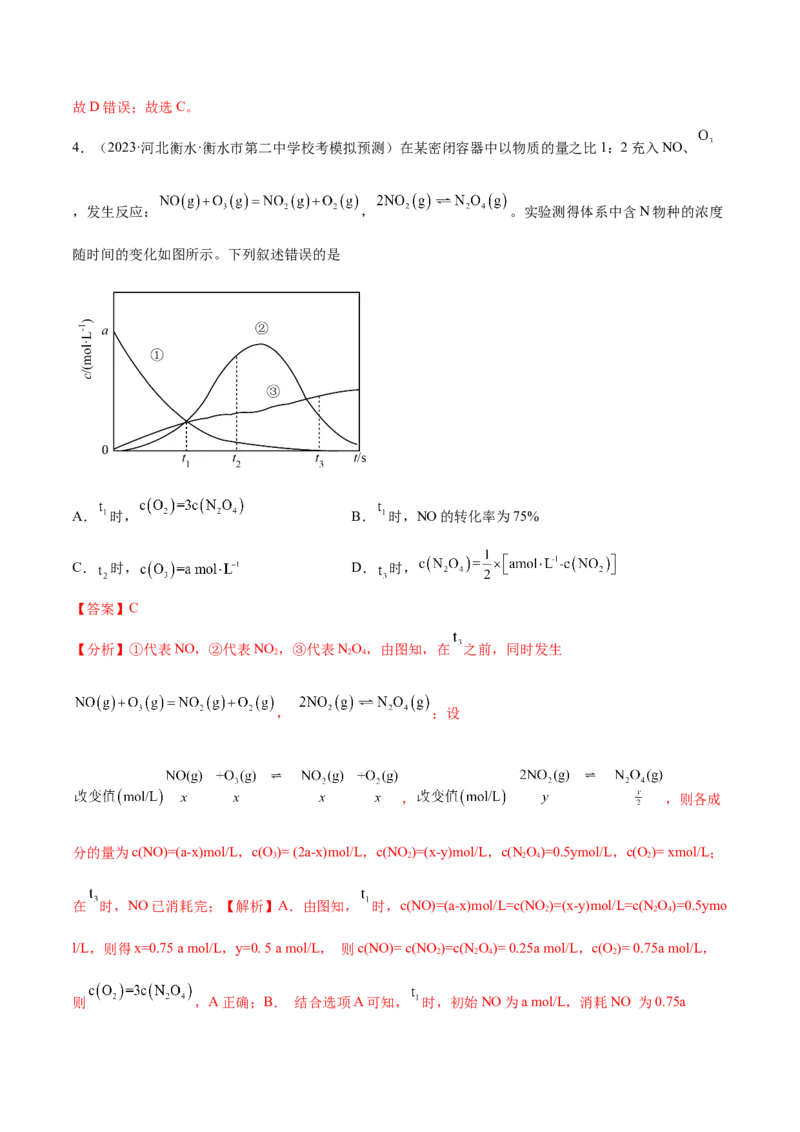
4.(2023·河北衡水·衡水市第二中学校考模拟预测)在某密闭容器中以物质的量之比1:2充入NO、
,发生反应: , 。实验测得体系中含N物种的浓度
随时间的变化如图所示。下列叙述错误的是
A. 时, B. 时,NO的转化率为75%
C. 时, D. 时,
【答案】C
【分析】①代表NO,②代表NO ,③代表NO,由图知,在 之前,同时发生
2 2 4
, ;设
, ,则各成
分的量为c(NO)=(a-x)mol/L,c(O)= (2a-x)mol/L,c(NO )=(x-y)mol/L,c(NO)=0.5ymol/L,c(O)= xmol/L;
3 2 2 4 2
在 时,NO已消耗完;【解析】A.由图知, 时,c(NO)=(a-x)mol/L=c(NO )=(x-y)mol/L=c(NO)=0.5ymo
2 2 4
l/L,则得x=0.75 a mol/L,y=0. 5 a mol/L, 则c(NO)= c(NO )=c(N O)= 0.25a mol/L,c(O)= 0.75a mol/L,
2 2 4 2
则 ,A正确;B. 结合选项A可知, 时,初始NO为a mol/L,消耗NO 为0.75amol/L,则NO的转化率为75%,B正确;C. ,由图
知, 时实际消耗NO<amol/L,则 ,C不正确;
D.氮原子为a mol/L, 时,NO不存在,按氮元素守恒 ,D正确;答案
选C。
5.(2023·湖南常德·常德市一中校考模拟预测)将一定量的 固体置于恒容密闭真空容器中(固体试
样的体积忽略不计),使其在50℃的恒温条件下分解: 。实验测得该体系的
压强如表所示:
时间/min 0 10 20 30 40 50 60 70
压强/kPa 0 0.66 1.28 1.78 2.20 2.50 2.50 2.50
已知: 为用各气体分压表示的平衡常数,分压=总压×物质的量分数。
下列有关说法正确的是
A.当混合气体的平均摩尔质量不再随时间变化时,反应达到平衡
B.0~10 min,用HS的压强变化表示该反应的平均反应速率为
2
C.50℃时, 的分解反应的压强平衡常数
D.50℃时,若在65 min时将容器的容积压缩至原来的 ,再次达到平衡时,体系的压强大于2.50 kPa
【答案】C
【解析】A.反应的平均摩尔质量为= ,与反应平衡无关,项错误;B.该时间内
压强变化了0.66kPa,又NH 和HS物质的量之比为1:1,则平均速率为 ,B项错
3 2
误;C.50min时反应达到平衡,体系压强为2.5 kPa,同时两物质的物质的量分数均为 ,则K=
p,C项正确;D.由于体系温度不变,K 不变。则K= 得出P
p p 总
=2.5 kPa,D项错误;故选C。
【微专题 图像、图表题的信息提取与应用】
1.(2023·天津南开·统考一模)已知: 现将三个相同容积的密闭容器中按
不同方式投入反应物发生反应。相关数据见下表:
容器1 容器2 容器3
反应温度(°C) 400 400 500
起始量 lmol 、1mol (g) 2mol HI lmol 、1mol (g)
平衡浓度
平衡转化率
平衡常数
下列各项关系不正确的是
A. B.
C. D.
【答案】B
【解析】A.容器1和容器2是等效平衡,因此 ,温度升高平衡逆向移动,因此 ,A正确;
B.容器1和容器2是等效平衡,因此 ,温度升高平衡逆向移动, 减小,因此 ,B错
误;C.温度升高平衡逆向移动,平衡转化率减小,因此 ,C正确;D.容器1和容器2是
等效平衡,达到平衡状态时,各物质的浓度相等, ,且两容器温度相同,则有
,D正确;故选B。2.(2023·湖北·校联考模拟预测)在恒温恒容条件下,向某容器中充入一定量的NO 气体发生下列反应:
2 5
2NO(g) 4NO (g)+O(g) ΔH>0。温度T时,部分实验数据如表所示:
2 5 2 2
t/s 0 50 100 150
c(NO)/mol·L-1 4.00 2.5 2.00 2.00
2 5
下列有关说法错误的是
A.温度T时,该反应平衡常数K=64
B.150s后再充入一定量NO,再次达到平衡NO 的转化率将增大
2 5 2 5
C.达平衡后升高温度,该容器内混合气体的密度不会改变
D.其他条件不变,若将恒容改为恒压,则平衡时NO 的转化率增大
2 5
【答案】B
【解析】A.
K= ,故A正确;B.恒容条件下,再充入一定量NO,相当于加压,再次达到平衡NO 的转化
2 5 2 5
率将降低,故B错误;C.升高温度,混合气体的总质量、容器的体积都不变,因此气体的密度不变,故
C正确;D.该反应的正反应是气体分子数增大的反应,其他条件不变时,改为在恒压密闭容器中反应,
相当于减压,平衡正向移动,平衡时NO 的转化率增大,故D正确;选B。
2 5
3.(2023·上海浦东新·统考二模)一定温度下,向1.0L恒容密闭容器中充入 ,发生如下反应:
。反应过程中测定的部分数据见下表。下列说法错误的是
0 50 150 250 350
0 0.16 0.19 0.20 0.20
A.0~250s,反应过程中气体平均摩尔质量逐渐减小
B.反应到250s时,产生的 体积为4.48L(标准状况)C.对平衡后体系降温,混合气体密度减小,则 的状态一定发生变化
D.其它条件相同时,向平衡后体系再充入等物质的量的 和 ,此时v(正)>v(逆)
【答案】D
【解析】A.该反应是气体总物质的量增大、质量不变的反应,则0~250s,气体平均摩尔质量逐渐减小,
故A正确;B.反应到250s时,PCl 气体的物质的量为0.2mol,根据反应方程式可知生成氯气的物质的量
3
为0.2mol,所以产生的 体积为4.48L(标准状况),故B正确;C. 相对分子质量大,沸点高,对平
衡后体系降温,混合气体密度减小,说明气体总质量减小,则 的状态一定发生变化,故C正确;D.
一定温度下,K= ;其它条件相同时,向平衡后体系再充入等物质的量的
和 ,假设加入的 和 都是1mol, ,所以反应
逆向进行,此时v(正)c>a
2 2
C.图丙是一定温度下,将一定质量的冰醋酸加水稀释过程中溶液的导电能力变化,则用湿润的pH试纸测
量a处溶液的pH,测量结果偏小
D.图丁表示反应 不同温度时平衡常数K随压强的变化关系图,则
【答案】B
【解析】A.恒温密闭容器中发生 ,K=c(CO),温度不变,平衡常数不变,t
2 1
时刻缩小容器体积,c(CO)迅速增大,重新达到平衡后,c(CO)与原平衡c(CO)相等,A正确;B.H 的起
2 2 2 2
始量一定时在恒温密闭容器中发生 反应,随着氮气的物质的量逐渐增大,反应
正向进行,H 的转化率逐渐增大,故H 的转化率:c>b>a ,B错误;C.在一定温度下,将一定质量的
2 2
冰醋酸加水稀释,醋酸的电离程度增大,导电能力增强,但超过b点以后,离子浓度减小,导电能力减弱,
在a点用湿润的PH试纸测量PH时,相当于醋酸被稀释,酸性增强,PH偏小,C正确;D.由于
为放热反应,升高温度平衡逆向移动,平衡常数减小,由图知T 时的
2
K值小于T 时的K值,故 ,D正确;故选B。
1
1.(2023·湖南·校联考模拟预测)在一定温度下,以 为催化剂,氯苯和 在 溶液中发生反应
反应①: (邻二氯苯)
反应②: (对二氯苯)
反应①和②存在的速率方程: 和 , 、 为速
率常数,只与温度有关,反应①和②的 曲线如图所示。下列说法错误的是A.若对二氯苯比邻二氯苯稳定,则
B.保持反应体系温度恒定,体系中两种有机产物的浓度之比保持不变
C.通过改变催化剂可以提高产物中对二氯苯的比例
D.相同时间内, (对二氯苯) (邻二氯苯)
【答案】A
【解析】A.反应①和反应②的 、 ,又知对二氯苯比邻二氯苯稳定,则反应②吸收的热量
更少,即 ,A错误;B.反应① 和反应②
,则 ,
,温度恒定时, 、 保持不变,则两种有机产物的浓度之比保持
不变,B正确;C.改变催化剂可改变选择性,可提高产物中对二氯苯的比例,C正确;D.反应①和反应
②中 转化为对二氯苯和邻二氯苯均为 进行,则 (对二氯苯) (邻二氯苯)成立,
D正确;故选A。
2.(2023·全国·模拟预测)在恒温恒容的密闭容器中,在某催化剂表面上发生分解反应:
,测得不同起始浓度和不同催化剂表面积时Z的浓度随时间的变化如表所示。下列
说法错误的是编号 0 20 40 60 80
① a 2.40 2.00 1.60 1.20 0.80
② a 1.20 0.80 0.40 x
③ 2a 2.40 1.60 0.80 0.40 0.40
A.实验①,100 min时反应达到平衡状态
B.实验②,60 min时反应处于平衡状态
C.相同条件下,增大催化剂的表面积,Z的平衡转化率不变
D.相同条件下,增加Z的浓度,反应速率增大
【答案】D
【解析】A.由实验①中数据可知,该反应的速率保持不变,对比实验①、③可知,实验①达到平衡时Z
的浓度也为 ,而实验①中100 min时Z的浓度减小到 ,即100 min时反
应达到平衡状态,选项A正确;B.由数据分析知,反应速率不变,若实验②中60 min时没有达到平衡状
态,则Z的浓度为0,与可逆反应的特点不符,所以60 min时反应已达平衡状态,选项B正确;C.增大
催化剂的表面积,能加快反应速率,但不影响化学平衡,即Z的平衡转化率不变,选项C正确;D.实验
①和②催化剂表面积相同,实验①中Z的起始浓度是实验②的2倍,实验①、②中0~20 min和20~40 min
内,∆c(Z)都是 ,则相同条件下增加Z的浓度,反应速率并未增大,选项D错误;答案选
D。
3.(2023·北京西城·统考二模)中国科学家首次用 改性铜基催化剂,将草酸二甲酯加氢制乙二醇的反
应条件从高压降至常压。草酸二甲酯加氢的主要反应有:①
②
③
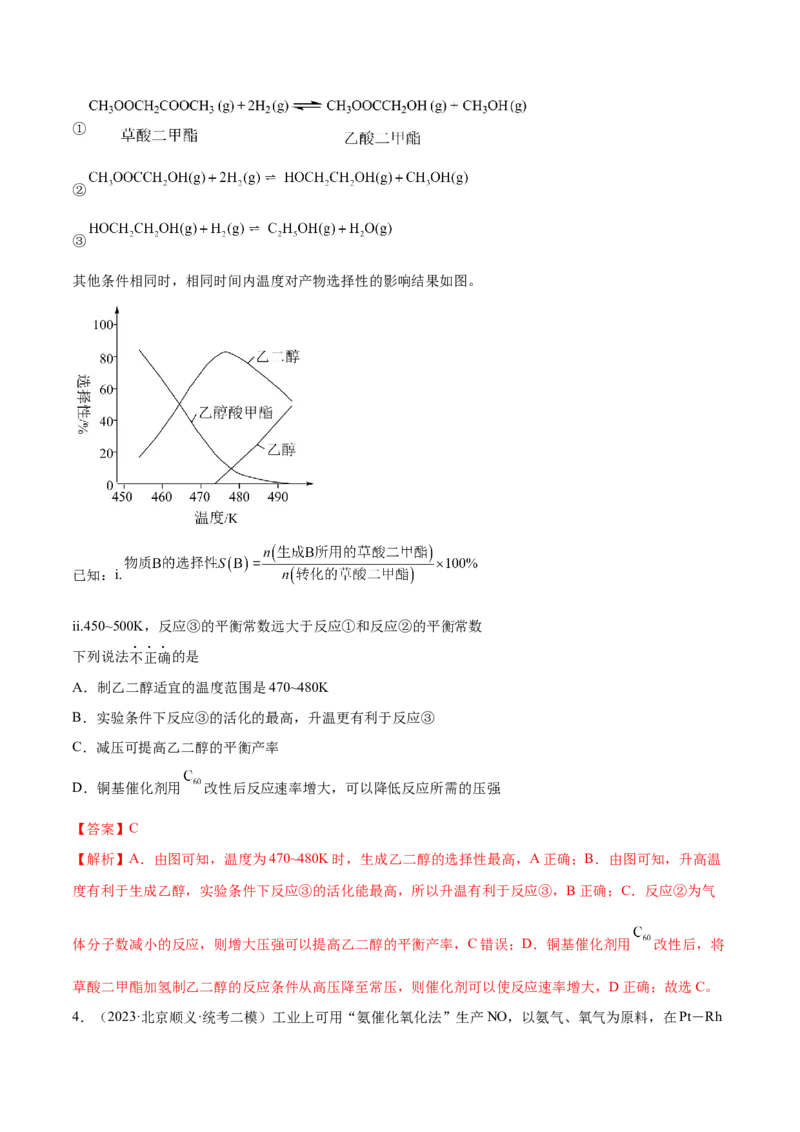
其他条件相同时,相同时间内温度对产物选择性的影响结果如图。
已知:i.
ii.450~500K,反应③的平衡常数远大于反应①和反应②的平衡常数
下列说法不正确的是
A.制乙二醇适宜的温度范围是470~480K
B.实验条件下反应③的活化的最高,升温更有利于反应③
C.减压可提高乙二醇的平衡产率
D.铜基催化剂用 改性后反应速率增大,可以降低反应所需的压强
【答案】C
【解析】A.由图可知,温度为470~480K时,生成乙二醇的选择性最高,A正确;B.由图可知,升高温
度有利于生成乙醇,实验条件下反应③的活化能最高,所以升温有利于反应③,B正确;C.反应②为气
体分子数减小的反应,则增大压强可以提高乙二醇的平衡产率,C错误;D.铜基催化剂用 改性后,将
草酸二甲酯加氢制乙二醇的反应条件从高压降至常压,则催化剂可以使反应速率增大,D正确;故选C。
4.(2023·北京顺义·统考二模)工业上可用“氨催化氧化法”生产NO,以氨气、氧气为原料,在Pt-Rh合金催化剂存在下生成NO和副产物N,两个竞争反应化学方程式如下:
2
Ⅰ.4NH(g)+5O(g) 4NO(g)+6H O(g)
3 2 2
Ⅱ.4NH(g)+3O(g) 2N(g)+6HO(g)
3 2 2 2
现将1molNH 、1.45molO 充入1L恒容密闭容器中,在上述催化剂作用下反应,相同时间内有关生成物物
3 2
质的量随温度变化曲线如图所示:
已知:有效转化率= ×100%
下列说法不正确的是
A.400℃时,主要发生反应Ⅱ
B.由图分析工业上用氨催化氧化制备HNO,最佳温度约为840℃
3
C.520℃时,NH 的有效转化率约为66.7%
3
D.840℃后,NO的物质的量下降,可能是反应I平衡逆向移动所致
【答案】C
【解析】A.400℃时,氮气的物质的量最大,说明主要发生反应Ⅱ,A正确;B.840℃时一氧化氮的产率
最高副产物氮气产率最低,则工业用氨催化氧化制备HNO,选择的最佳温度是840℃,B正确;C.由图知
3
520C时,生成氮气和一氧化氮的物质的量均为0.2mol,则反应Ⅱ消耗的氨气的物质的量为0.4mol,反应Ⅰ
消耗的氨气的物质的量为0.2mol,NH 的有效转化率为 ,C错误;D.840℃
3
后,NO的物质的量下降,可能是反应Ⅰ为放热反应,升温,反应Ⅰ平衡逆向移动所致,D正确;故选C。
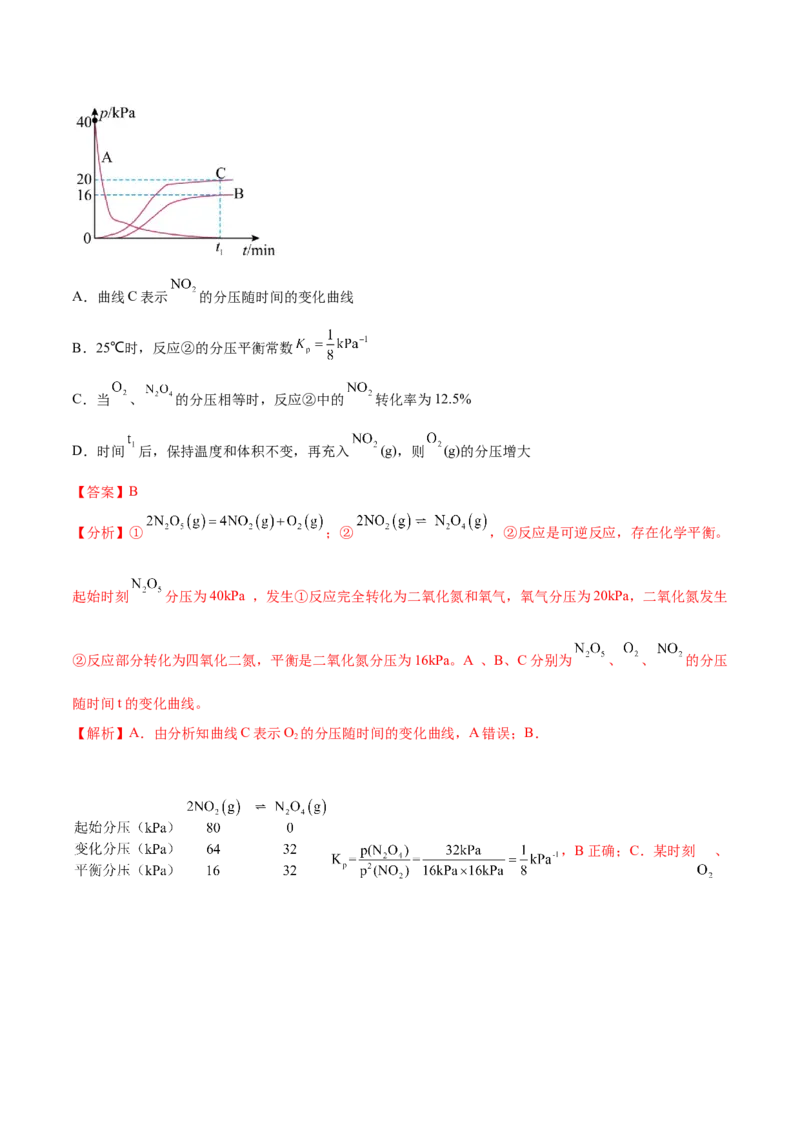
5.(2023·重庆·重庆市育才中学校考模拟预测)25℃时,向恒容容器中加入A发生反应:①
;② 。反应体系中 、 、 的分压随时间t的
变化曲线如图所示。下列说法正确的是A.曲线C表示 的分压随时间的变化曲线
B.25℃时,反应②的分压平衡常数
C.当 、 的分压相等时,反应②中的 转化率为12.5%
D.时间 后,保持温度和体积不变,再充入 (g),则 (g)的分压增大
【答案】B
【分析】① ;② ,②反应是可逆反应,存在化学平衡。
起始时刻 分压为40kPa ,发生①反应完全转化为二氧化氮和氧气,氧气分压为20kPa,二氧化氮发生
②反应部分转化为四氧化二氮,平衡是二氧化氮分压为16kPa。A 、B、C分别为 、 、 的分压
随时间t的变化曲线。
【解析】A.由分析知曲线C表示O 的分压随时间的变化曲线,A错误;B.
2
,B正确;C.某时刻 、的分压相等为20kPa时: ,二氧化氮的转化率为50%,C
错误;D.时间 后,保持温度和体积不变,再充入 (g)引起②化学平衡发生移动,由勒夏特列原理知
体系中总的物质的量依然增大, (g)的物质的量不变,氧气分压减小,D错误;故选B。
6.(2023·河北邯郸·统考二模)工业上用 和 合成甲醇涉及以下反应:
I.
II.
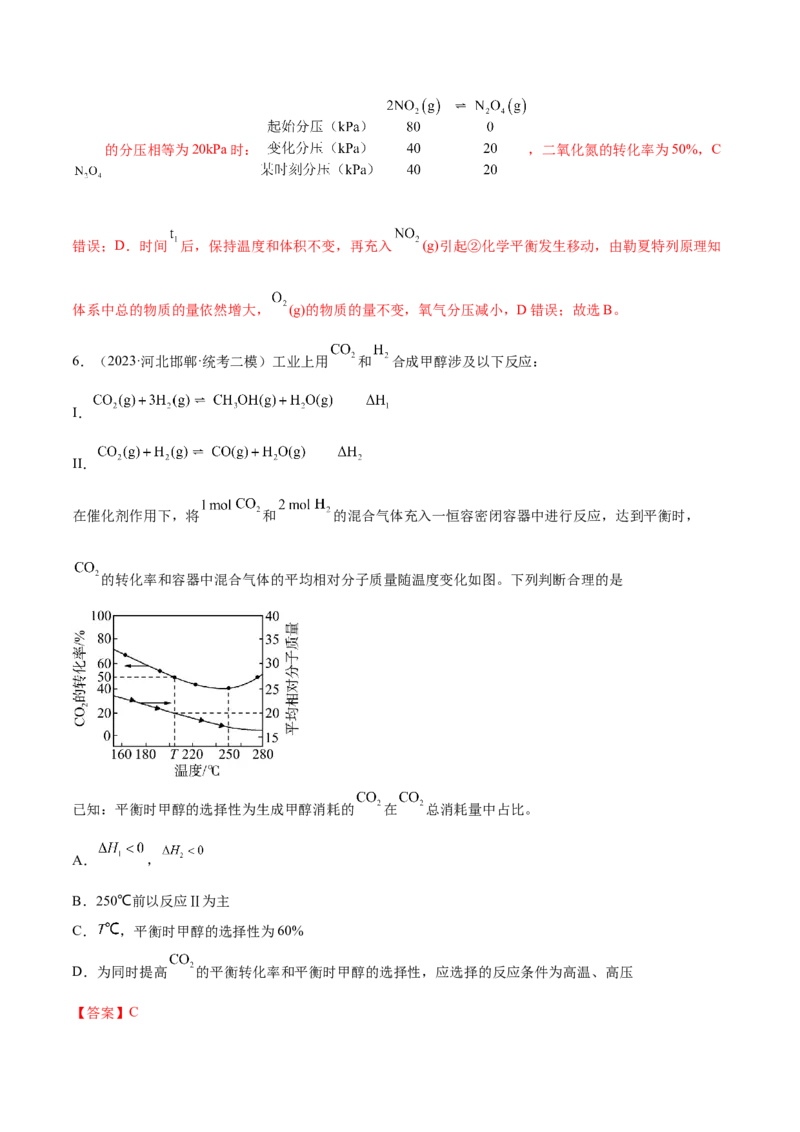
在催化剂作用下,将 和 的混合气体充入一恒容密闭容器中进行反应,达到平衡时,
的转化率和容器中混合气体的平均相对分子质量随温度变化如图。下列判断合理的是
已知:平衡时甲醇的选择性为生成甲醇消耗的 在 总消耗量中占比。
A. ,
B.250℃前以反应Ⅱ为主
C. ,平衡时甲醇的选择性为60%
D.为同时提高 的平衡转化率和平衡时甲醇的选择性,应选择的反应条件为高温、高压
【答案】C【解析】A.由图可知,温度越高, 的转化率越小,平衡逆向移动,所以反应I为放热反应,反应II
为吸热反应,A错误;B.由图可知,当温度高于250℃, 的转化率随温度的升高而增大,则250℃以
后以反应II为主,B错误;C. , 转化率为 ,平均相对分子质量为20,混合气体总物质的量
为: 则 为 ,设甲醇为 , 为 , , ,
, ,计算 , ,甲
醇的选择性为 ,C正确;D.因为反应I为放热反应,升高温度, 的平衡转化率降低,
D错误;故选C。
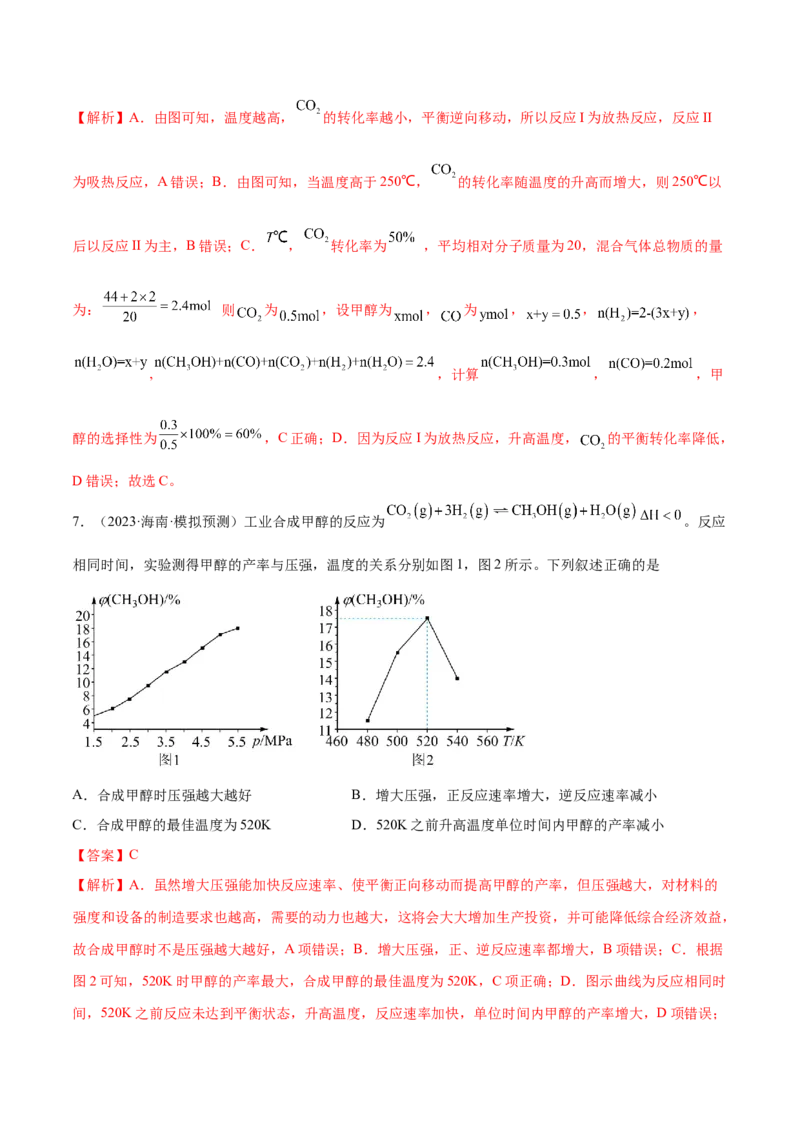
7.(2023·海南·模拟预测)工业合成甲醇的反应为 。反应
相同时间,实验测得甲醇的产率与压强,温度的关系分别如图1,图2所示。下列叙述正确的是
A.合成甲醇时压强越大越好 B.增大压强,正反应速率增大,逆反应速率减小
C.合成甲醇的最佳温度为520K D.520K之前升高温度单位时间内甲醇的产率减小
【答案】C
【解析】A.虽然增大压强能加快反应速率、使平衡正向移动而提高甲醇的产率,但压强越大,对材料的
强度和设备的制造要求也越高,需要的动力也越大,这将会大大增加生产投资,并可能降低综合经济效益,
故合成甲醇时不是压强越大越好,A项错误;B.增大压强,正、逆反应速率都增大,B项错误;C.根据
图2可知,520K时甲醇的产率最大,合成甲醇的最佳温度为520K,C项正确;D.图示曲线为反应相同时
间,520K之前反应未达到平衡状态,升高温度,反应速率加快,单位时间内甲醇的产率增大,D项错误;答案选C。
8.(2023·辽宁锦州·渤海大学附属高级中学校考模拟预测)一定温度下,在2个容积均为1 L的密闭容器
中,充入一定量的反应物,发生反应:2NO(g)+2CO(g) N(g)+2CO (g) ΔH<0,相关反应数据如下表所
2 2
示:
起始时物质的量/mol 10 s时物质的量/mol
容器编号 温度
NO CO N
2
Ⅰ T℃ 0.2 0.2 0.05
1
Ⅱ T℃(T >T) 0.2 0.2 0.05
2 2 1
下列说法正确的是
A.10 s时,容器Ⅰ中的反应处于平衡状态
B.10 s时,容器Ⅰ中的化学反应速率v(CO)=0.005mol·L-1·s-1
2
C.化学平衡常数:K >K
Ⅱ Ⅰ
D.若起始时,向容器Ⅱ中充入0.08 mol NO、0.1 mol CO、0.04 mol N 和0.1 mol CO ,反应将向逆反应方
2 2
向进行
【答案】D
【分析】由表中数据可知,T>T 容器II中反应速率快,10s两容器中氮气的物质的量相同,说明II中氮气
2 1
的量已经保持不变,容器II中反应达到平衡状态,则容器I中的反应没有达到平衡状态。
【解析】A.根据分析,10 s时,容器Ⅰ中的反应还未达到平衡状态,故A错误;B.10s时,容器Ⅰ中的
化学反应速率 ,故B错误;C.升高温度,平衡逆向移动,
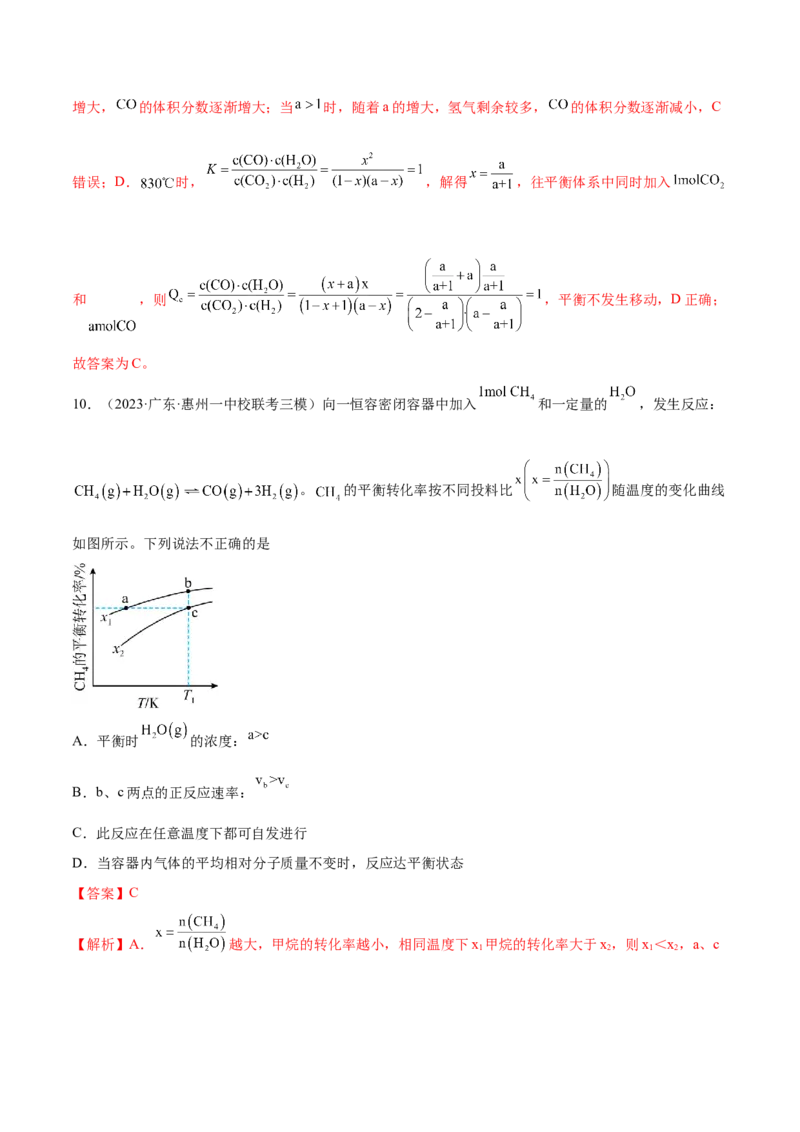
平衡常数K减小,所以化学平衡常数:K 反应Ⅱ
B.反应活化能:反应I<反应Ⅱ
C.增加 浓度可增加平衡时产物Ⅱ和产物I的比例
D.选择相对较短的反应时间,及时分离可获得高产率的产物Ⅰ【答案】C
【解析】A.反应I、Ⅲ为放热反应,相同物质的量的反应物,反应I放出的热量小于反应Ⅱ放出的热量,
反应放出的热量越多,其焓变越小,因此反应焓变:反应I>反应Ⅱ,故A正确;B.短时间里反应I得到
的产物比反应Ⅱ得到的产物多,说明反应I的速率比反应Ⅱ的速率快,速率越快,其活化能越小,则反应
活化能:反应I<反应Ⅱ,故B正确;C.产物I和产物II存在可逆反应,则产物II和产物I的比值即该可逆
反应的平衡常数K,由于平衡常数只与温度有关,所以增加HCl浓度平衡时产物II和产物I的比例不变,
故C错误;D.根据图中信息,选择相对较短的反应时间,及时分离可获得高产率的产物Ⅰ,故D正确。
综上所述,答案为C。
4.(2022·北京·高考真题)CO 捕获和转化可减少CO 排放并实现资源利用,原理如图1所示。反应①完
2 2
成之后,以N 为载气,以恒定组成的N、CH 混合气,以恒定流速通入反应器,单位时间流出气体各组分
2 2 4
的物质的量随反应时间变化如图2所示。反应过程中始终未检测到CO,在催化剂上有积碳。
2
下列说法不正确的是
A.反应①为CaO+CO =CaCO ;反应②为CaCO +CH CaO+2CO+2H
2 3 3 4 2
B.t~t,n(H )比n(CO)多,且生成H 速率不变,可能有副反应CH C+2H
1 3 2 2 4 2
C.t 时刻,副反应生成H 的速率大于反应②生成H 速率
2 2 2
D.t 之后,生成CO的速率为0,是因为反应②不再发生
3
【答案】C
【解析】A.由题干图1所示信息可知,反应①为CaO+CO =CaCO ,结合氧化还原反应配平可得反应②为
2 3
,A正确;B.由题干图2信息可知,t~t,n(H )比n(CO)多,且生成
1 3 2H 速率不变,且反应过程中始终未检测到CO,在催化剂上有积碳,故可能有副反应 ,
2 2
反应②和副反应中CH 和H 的系数比均为1:2,B正确;C.由题干反应②方程式可知,H 和CO的反应速
4 2 2
率相等,而t 时刻信息可知,H 的反应速率未变,仍然为2mmol/min,而CO变为1~2mmol/min之间,故
2 2
能够说明副反应生成H 的速率小于反应②生成H 速率,C错误;D.由题干图2信息可知,t 之后,CO的
2 2 3
速率为0,CH 的速率逐渐增大,最终恢复到1,说明生成CO的速率为0,是因为反应②不再发生,而后
4
副反应逐渐停止反应,D正确;答案选C。
5.(2022·北京·高考真题)某 的多孔材料刚好可将NO“固定”,实现了NO 与NO 分离并制备
2 4 2 2 4
HNO,如图所示:
3
已知:2NO (g) NO(g) ΔH<0
2 2 4
下列说法不正确的是
A.气体温度升高后,不利于NO 的固定
2 4
B.NO 被固定后,平衡正移,有利于NO 的去除
2 4 2
C.制备HNO 的原理为:2NO+O +2H O=4HNO
3 2 4 2 2 3
D.每制备0.4molHNO ,转移电子数约为
3
【答案】D
【解析】A.已知:2NO (g) NO(g) ΔH<0,升高温度,平衡逆向移动,NO 的浓度减小,不利于NO
2 2 4 2 4 2 4
的固定,故A正确;B.NO 被固定后,NO 浓度减小,平衡正移,有利于NO 的去除,故B正确;C.
2 4 2 4 2
被固定的四氧化二氮和氧气、水反应生成硝酸,制备HNO 的原理为:2NO+O +2H O=4HNO ,故C正确;
3 2 4 2 2 3
D.由C化学方程式可知,4HNO~4e-,每制备0.4molHNO ,转移电子数约为0.4× ,故D错误。
3 3
故选D。
6.(2022·北京·高考真题)某 多孔材料孔径大小和形状恰好将 “固定”,能高选择性吸附。废气中的 被吸附后,经处理能全部转化为 。原理示意图如下。
已知:
下列说法不正确的是
A.温度升高时不利于 吸附
B.多孔材料“固定” ,促进 平衡正向移动
C.转化为 的反应是
D.每获得 时,转移电子的数目为
【答案】D
【分析】废气经过MOFs材料之后,NO 转化成NO 被吸附,进而与氧气和水反应生成硝酸,从该过程中
2 2 4
我们知道,NO 转化为NO 的程度,决定了整个废气处理的效率。
2 2 4
【解析】A.从 可以看出,这个是一个放热反应,升高温度之后,平衡逆向移动,
导致生成的NO 减少,不利于NO 的吸附,A正确;B.多孔材料“固定” ,从而促进
2 4 2
平衡正向移动,B正确;C.NO 和氧气、水反应生成硝酸,其方程式为 ,C正
2 4
确;D.在方程式 中,转移的电子数为4e-,则每获得 ,转移的电子
数为0.4mol,即个数为 ,D错误;故选D。
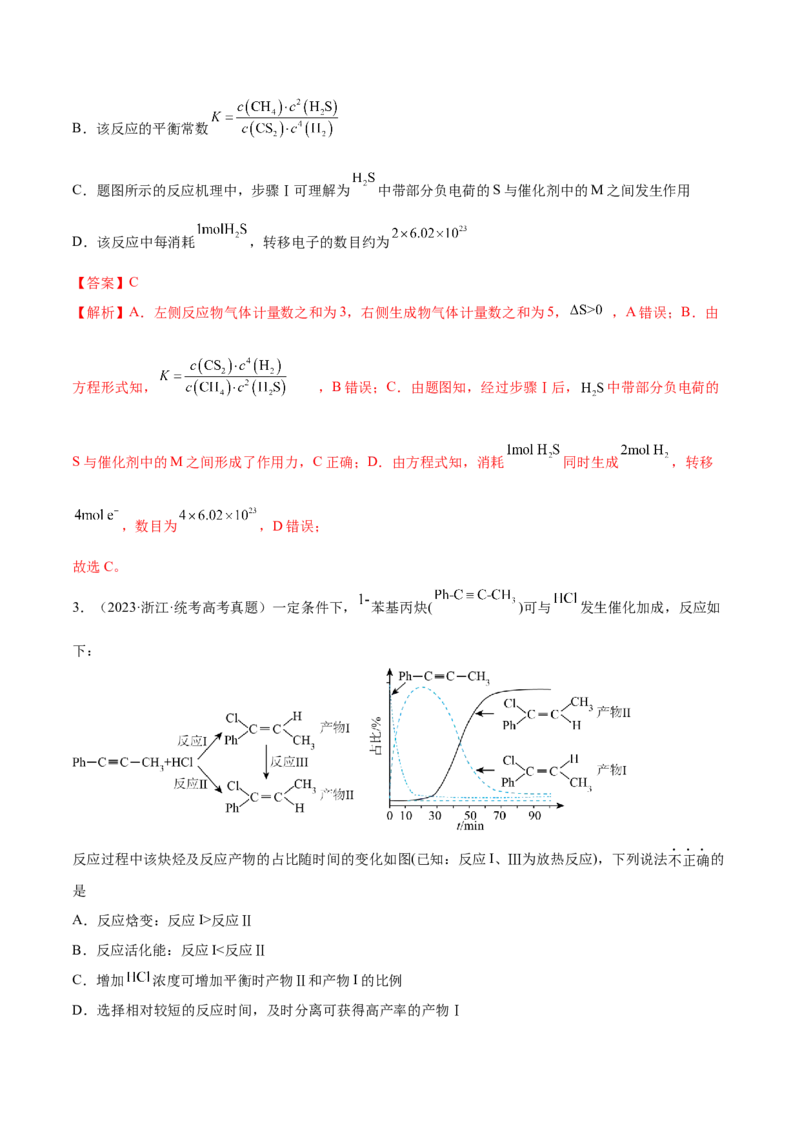
7.(2022·江苏·高考真题)乙醇-水催化重整可获得 。其主要反应为,
,在 、 时,若仅考
虑上述反应,平衡时 和CO的选择性及 的产率随温度的变化如图所示。
CO的选择性 ,下列说法正确的是
A.图中曲线①表示平衡时 产率随温度的变化
B.升高温度,平衡时CO的选择性增大
C.一定温度下,增大 可提高乙醇平衡转化率
D.一定温度下,加入 或选用高效催化剂,均能提高平衡时 产率
【答案】B
【分析】根据已知反应① ,反应②
,且反应①的热效应更大,温度升高的时候对反应①影响更
大一些,根据选择性的含义,升温时CO选择性增大,同时CO 的选择性减小,所以图中③代表CO的选
2
择性,①代表CO 的选择性,②代表H 的产率。
2 2
【解析】A.由分析可知②代表H 的产率,故A错误;B.由分析可知升高温度,平衡时CO的选择性增
2大,故B正确;C.一定温度下,增大 ,可以认为开始时水蒸气物质的量不变,增大乙醇物质
的量,乙醇的平衡转化率降低,故C错误;D.加入CaO同时吸收CO 和水蒸气,无法判断平衡如何移动,
2
无法判断如何影响平衡时 产率,故D错误;故选B。
8.(2022·海南·统考高考真题)某温度下,反应CH=CH (g)+HO(g) CHCHOH(g)在密闭容器中达到平
2 2 2 3 2
衡,下列说法正确的是
A.增大压强, ,平衡常数增大
B.加入催化剂,平衡时 的浓度增大
C.恒容下,充入一定量的 ,平衡向正反应方向移动
D.恒容下,充入一定量的 , 的平衡转化率增大
【答案】C
【解析】A.该反应是一个气体分子数减少的反应,增大压强可以加快化学反应速率,正反应速率增大的
幅度大于逆反应的,故v > v ,平衡向正反应方向移动,但是因为温度不变,故平衡常数不变,A不正
正 逆
确;B.催化剂不影响化学平衡状态,因此,加入催化剂不影响平衡时CHCHOH(g)的浓度,B不正确;
3 2
C.恒容下,充入一定量的HO(g),HO(g)的浓度增大,平衡向正反应方向移动,C正确;D.恒容下,充
2 2
入一定量的CH=CH (g),平衡向正反应方向移动,但是CH=CH (g)的平衡转化率减小,D不正确;综
2 2 2 2
上所述,本题选C。
9.(2022·湖南·高考真题)甲基丙烯酸甲酯是合成有机玻璃的单体。
旧法合成的反应:
新法合成的反应:
下列说法错误的是(阿伏加德罗常数的值为 )A. 的电子式为
B.新法没有副产物产生,原子利用率高
C. 的 溶液中 的微粒数小于
D. 的作用是降低反应的活化能,使活化分子数目增多,百分数不变
【答案】D
【解析】A.氢氰酸为共价化合物,结构式为H—C≡N,电子式为 ,故A正确;B.由方
程式可知,新法合成甲基丙烯酸甲酯的反应为没有副产物生成,原子利用率为100的化合反应,故B正确;
C.硫酸氢铵是强酸弱碱的酸式盐,铵根离子在溶液中会发生水解反应,所以1L0.05mol/L的硫酸氢铵溶液
中铵根离子的数目小于0.05mol/L×1L×N mol—1=0.05N ,故C正确;D.由方程式可知,钯为新法合成甲基
A A
丙烯酸甲酯的催化剂,能降低反应的活化能,使活化分子的数目和百分数都增大,故D错误;故选D。
10.(2021·江苏·高考真题)NH 与O 作用分别生成N、NO、NO的反应均为放热反应。工业尾气中的
3 2 2 2
NH 可通过催化氧化为N 除去。将一定比例的NH 、O 和N 的混合气体以一定流速通过装有催化剂的反
3 2 3 2 2
应管,NH 的转化率、生成N 的选择性[ 100%]与温度的关系如图所示。
3 2
下列说法正确的是
A.其他条件不变,升高温度,NH 的平衡转化率增大
3
B.其他条件不变,在175~300 ℃范围,随温度的升高,出口处N 和氮氧化物的量均不断增大
2
C.催化氧化除去尾气中的NH 应选择反应温度高于250 ℃
3
D.高效除去尾气中的NH ,需研发低温下NH 转化率高和N 选择性高的催化剂
3 3 2
【答案】D
【解析】A.NH 与O 作用分别生成N、NO、NO的反应均为放热反应,根据勒夏特列原理,升高温度,
3 2 2 2平衡向逆反应方向进行,氨气的平衡转化率降低,故A错误;B.根据图象,在175~300 ℃范围,随温度
的升高,N 的选择率降低,即产生氮气的量减少,故B错误;C.根据图象,温度高于250℃ N 的选择率
2 2
降低,且氨气的转化率变化并不大,浪费能源,根据图象,温度应略小于225℃,此时氨气的转化率、氮
气的选择率较大,故C错误;D.氮气对环境无污染,氮的氧化物污染环境,因此高效除去尾气中的
NH ,需研发低温下NH 转化率高和N 选择性高的催化剂,故D正确;答案为D。
3 3 2