文档内容
专题 11 物质结构与元素周期律
(考试时间:75分钟 试卷满分:100分)
一、选择题(本题共15小题,每小题3分,共45分。每小题只有一项是符合题目要求的)
1.科学家利用氦核 撞击氮原子,发生反应: ,下列说法正确的是( )
A. 的质子数为2 B. 的中子数为9
C. 和 互为同位素 D. 与 化学性质不同
【答案】A
【解析】A项,质子数与原子序数相等,故4He的质子数为2,A正确;B项, 的中子数为15-
7=8,H没有中子,则 的中子数为8,B错误;C项,同位素为质子数相同、中子数不同的核素,
为单质,C错误;D项,2H、1H互为同位素,2H、1H 是不同的氢分子,两者的化学性质相同,D错
2 2
误;故选A。
2.下列物质中含非极性键的盐是( )
A.NH Cl B.NaC O C.MgN D.NaO
4 2 2 4 3 2 2 2
【答案】B
【解析】A项,氯化铵的铵根离子中含有氮氢极性共价键,A不合题意;B项,NaC O 为草酸盐,草
2 2 4
酸根离子中含有碳碳非极性共价键,B符合题意;C项,氮化镁不属于盐,C不合题意;D项,过氧化钠
为氧化物,不属于盐,D不合题意;故选B。
3.下列性质的比较,不能用元素周期律解释的是( )
A.原子半径:S>Cl B.热稳定性:HCl>HS
2
C.非金属性:Cl>S D.酸性:HClO>HSO
3 2 3
【答案】D
【解析】A项,同一周期从左往右主族元素的原子半径依次减小,故原子半径:S>Cl可以用元素周
期律解释,A不合题意;B项,同一周期从左往右主族元素的非金属性增强,其简单气态氢化物的热稳定
性也依次增强,故热稳定性:HCl>HS可以用元素周期律解释,B不合题意;C项,同一周期从左往右主
2
族元素的非金属性增强,故非金属性:Cl>S符合元素周期律,C不合题意;D项,非金属元素的最高价
氧化物对应的水化物的酸性与元素的非金属性一致,但HClO、HSO 不是Cl、S的最高价氧化物对应水
3 2 3
化物,故酸性:HClO>HSO 不能用元素周期律解释,D符合题意;故选D。
3 2 3
4.下列说法正确的是( )A.ⅠA族元素全部属于金属元素,ⅦA族元素全部属于非金属元素
B.人们可以借助元素周期表,在金属与非金属的分界线附近寻找耐高温材料
C.1869年门捷列夫发现元素的性质随着元素核电荷数的递增而呈周期性变化的规律
D.2015年中、德、加科学家成功制备出了含+9价铱元素的离子(IrO +),其中n=4
n
【答案】D
【解析】A项,第IA族元素氢是非金属元素,不全是金属,ⅦA族元素全部属于非金属元素,故A
错误;B项,元素周期表的金属与非金属的分界线处的元素具有金属和非金属的性质,具有半导体性质,
可寻找半导体材料,不能用于寻找耐高温材料,故B错误;C项,1869年门捷列夫发现了元素的性质随着
相对原子质量的递增而呈周期性变化的规律,后人逐渐修正成元素的性质随着元素原子序数的递增而呈现
周期性变化的规律,故C错误;D项,若n=4,则 lrO+中氧元素显−2价,设铱元素的化合价是z,由原
4
子团中元素的化合价代数和等于原子团的化合价,可得:z+(−2)×4=+1,则z=+9价,故D正确。
5.(2024·广东梅州高三模拟)最近媒体报道了一些化学物质,如爆炸力极强的 、比黄金还贵的
、太空中的甲醇气团等。下列说法中不正确的是( )
A. 中含中子数为10N B.甲醇(CHOH)属于共价化合物
A 3
C.N 和N 互为同素异形体 D.由N 变成N 是化学变化
5 2 5 2
【答案】A
【解析】A项,1个 中所含中子数为18, 中所含中子数为9N ,A不正确;B项,
A
甲醇(CHOH)是碳原子、氢原子、氧原子间以共价键形成的共价化合物,B正确;C项,N 和N 是氮元素
3 5 2
的两种同素异形体,C正确;D项,N、N 是氮元素的同素异形体,所以2N=5N 是化学变化,D正确;
5 2 5 2
故选A。
6.(2024·江西名校高三联合测评)科学家利用 粒子(即氦核 )进行多种核反应:
、 。已知2H和3H都具有放射性,下列说法错误的是( )
1 1
A.X元素位于元素周期表的第二周期第ⅥA族
B.1H和2H互为同位素,化学性质相同
1 1
C.2H、3H都可作为示踪原子
1 1
D.核反应产生的能量可用于发电,属于化学能转化为电能
【答案】D
【解析】A项,因为核反应过程中电子数不变,由题意可推出Z=8,所以X是O,位于元素周期表中
第二周期第ⅥA族,A正确;B项,同位素的化学性质几乎相同,B正确;C项,由于2H、3H都具有放
1 1
射性,所以均可作为示踪原子,C正确;D项,核反应不属于化学反应的范畴,利用核反应产生的能量发电是将核能转化为电能,D错误;故选D。
7.(2023·安徽省阜阳市联考)活泼金属氢化物是火箭燃料的重要供氢剂,如氢化钠、氢化钙等。例
如,氢化钙的供氢原理是CaH+2H O= Ca(OH) +2H ↑,下列有关分析中正确的是( )
2 2 2 2
A.氢化钙中含共价键,水分子中含有极性键
B.水分子和氢分子中都存在非极性共价键
C.氢氧化钙只存在离子键
D.该反应过程中断裂离子键和共价键,形成离子键和共价键
【答案】D
【解析】A项,氢化钙是由Ca2+和H-构成的,不含共价键,A错误;B项,HO结构式为H-O-H,不
2
存在非极性共价键,B错误;C项,Ca(OH) 是由Ca2+和OH-构成,其中OH-含有O-H极性共价键,C错
2
误;D项,该反应过程中,有离子键Ca2+和H-的断裂、Ca2+和OH-的形成,有共价键O-H键断裂和H-H键
的形成,D正确; 故选D。
8.(2024·贵州省部分学校高三适应性联考)2023年8月24日中午12点,日本政府不顾中国等太平洋国
家的强烈反对,悍然启动核污染水排海工作,给太平洋沿岸国家人民的健康和生命财产安全造成极大隐
患。核废水中含有氚(3H)和14C等多种放射性核素。下列有关说法错误的是( )
A.氚的核内中子数是 核内中子数的2倍
B.14C可用于文物年代的鉴定,它与12C互为同位素
C. 和 都属于氢元素
D. 属于化学变化( 表示中子)
【答案】D
【解析】A项,氚(3H)的中子数为2,2H的中子数为1,因此氚的核内中子数是2H核内中子数的2
倍,A正确;B项,放射性碳测定年代法是最常用的考古方法,它所能断定的年份最久的达50000年,14C
与12C互为同位素,B正确;C项,3H、2H和1H都属于氢元素,互为同位素,C正确;D项,
中原子核发生了变化,属于核反应,不属于化学变化,D错误;故选D。
9.X、Y、Z、M、Q五种短周期元素,原子序数依次增大。Y元素的最高正价为+4价,Y元素与Z
元素相邻,且化合物ZX 的电子总数为18个;X与M元素同主族;Q元素的原子最外层电子数比次外层
2 4
少一个电子。下列说法不正确的是( )
A.最高价氧化物对应水化物的酸性:Q>Z>Y
B.原子半径:ZZ>Y,A项正确;B项,Z、
Y、M分别是N、C、Na,同周期从左到右,原子半径逐渐减小,同主族从上到下,原子半径逐渐增大,
所以原子半径:ZY>W
D.简单气态氢化物的稳定性:X>Z
【答案】A
【解析】W的原子半径在短周期主族元素中最大,W为Na;X的质子数是Z核外最外层电子数的2
倍,分情况讨论:若Z核外最外层电子数为7,则Z为Cl、X为Si,由化合物中元素化合价代数和为0可知,Y元素化合价为-3,Y为P;若Z核外最外层电子数为6,则Z为S、X为Mg,Y元素化合价为+7,不
合理;若Z核外最外层电子数为5,则X的质子数为10,不合理;可知Z为Cl、X为Si、Y为P。A项,
氢氧化钠为强碱,硅酸为弱酸,磷酸为中强酸,高氯酸为强酸,A项正确;B项,氯化钠水溶液呈中性,
B项错误;C项,核外电子排布相同的离子,原子序数大的半径小,磷离子的半径大于氯离子的,C项错
误;D项,同周期主族元素从左到右,非金属性依次增强,则简单气态氢化物的稳定性Cl>Si,D项错误;
故选A。
12.原子序数依次增大的W、X、Y、Z四种短周期主族元素,W、Y同周期且价电子数之和为10,
W、Y可形成结构如图所示的阴离子,Z原子最外层有2个电子,下列说法错误的是( )
A.常见简单氢化物沸点:
B.简单离子半径:
C.WY2-中两种元素的原子 离子 最外层均达到8电子结构
2 4
D.Z2+、WY2-均能促进水的电离
2 4
【答案】B
【解析】A项,由图可知W形成四个共价键,所以为碳,Y形成了2个共价键,再结合W、Y价电子
数关系可推出Y是氧。易推出X是氮,Z是镁。常温下水是液体、NH 易液化而CH 难液化,A项正确;
3 4
B项,简单离子半径:N3- >O2- > Mg2+,B项错误;C项,原子最外层有4个电子,通过形成四个共价键而
使自已最外层达到8个电子,O原子最外层有6个电子,形成2个键后最外层也达到8个电子,C项正确;
D项,Mg2+能水解,C O2-是弱酸的酸根,也能水解,D项正确;故选B。
2 4
13.W、X、Y、Z、M为原子序数依次增大的短周期主族元素,其原子半径和最外层电子数的关系如
图所示。下列说法正确的是( )
A.简单氢化物的沸点:X>M
B.WX 与YX 的化学键类型完全相同
2 2 2 2
C.X、Y、Z的简单离子半径:XY>Z;C项错误;D项,氢氧化钠为强碱,氢氧化铝为弱碱,故碱性:氢氧化钠>氢氧化
铝,D项错误;故选A。
14.短周期主族元素W、X、Y、Z、Q原子序数依次增大,形成的化合物是一种重要的食品添加剂,
结构如下图。下列正确的是( )
A.原子半径大小:Y>Z>Q
B.该化合物中Z原子不满足8电子稳定结构
C.Y是第ⅢA族元素
D.W和Z可形成三种10电子微粒
【答案】D
【解析】五种元素均为短周期元素,且原子序数依次增大,Q显+1价,即Q为Na,W形成一个共价
键,则W为H,Y形成三个共价键,即Y为N,X形成四个共价键,则X为C,Z形成2个共价键,则Z
为O,W为H,X为C,Y为N,Z为O,Q为Na。A项,一般电子层数越多,原子半径越大,同周期从
左向右原子半径依次减小,因此原子半径:Na>N>O,故A错误;B项,其中一个O与C形成碳氧双
键,该氧元素满足8电子稳定结构,另一个O与C形成一个C-O单键,同时该氧元素又得到Na失去的一
个电子,因此该氧元素也满足8电子稳定结构,故B错误;C项,Y为N,位于第二周期ⅤA族,故C错
误;D项,H和O形成10电子微粒分别为HO、HO+、OH-,故D正确;故选D。
2 3
15.我国科学家分析月壤成分发现含有X、Y、Z、W、M五种主族元素,其原子序数依次增大且都不
大于20,Y、Z、W同周期且Z、M同主族;X与W形成的化合物是光导纤维的基本原料,在潜水艇中
YX 可以用作供氧剂。下列说法正确的是( )
2 2
A.离子半径的大小顺序:Z>Y>X
B.最简单气态氢化物稳定性X>W
C.最高价氧化物对应水化物碱性Y>Z>M
D.工业上用电解ZX来制备Z的单质
【答案】B
【解析】光导纤维的主要成分是SiO,X与W形成的化合物是光导纤维的基本原料,则X是O,W
2是Si。YX 可以用作供氧剂则Y元素是Na,再根据原子序数依次增大且都不大于20,Y、Z、W同周期且
2 2
Z、M同主族,可推断Z元素是Mg,M元素是Ca。A项,据分析可知X、Y、Z元素分别为O、Na、
Mg,离子半径的大小顺序:O2- >Na+ > Mg2+,故A错误; B项,X、W元素分别为O、Si,最简单气态氢
化物稳定性:HO>SiH,故B正确;C项,Y、Z、M元素分别为Na、Mg、Ca,最高价氧化物对应水化物
2 4
碱性Ca (OH)> Mg (OH) ,故C错误;D项,Z是Mg元素,工业上用电解MgCl 来制备Mg的单质,故D
2 2 2
错误;故选B。
二、非选择题(本题包括4小题,共55分)
16.(12分)W、X、Y、Z、N、M六种主族元素,它们在周期表中位置如图所示,请用对应的的化学
用语回答下列问题:
(1)N元素在周期表中的位置___________,根据周期表,推测N原子序数为___________
(2)比较Y、Z、W三种元素形成简单离子的半径由大到小的顺序___________(用元素符号表示)
(3)M最高价氧化物的水化物在水中的电离方程式:___________
(4)以下说法正确的是___________
A.单质的还原性:X>Y,可以用X与YM 溶液发生反应置换出Y来证明
2
B.Y与同周期的ⅢA元素的原子序数相差1
C.硅主要用于半导体器件的研制,目前用硅研发出的太阳能光伏电池,如我校的路灯
D.元素N位于金属与非金属的分界线附近,可以推断N元素的单质可与氨水反应放出氢气
(5)由X、W元素构成的原子个数比为1:1的化合物所含化学键类型为___________,将一定量此化合
物投入到足量的水中,产生2.24L气体(标准状况下),转移电子的物质的量为________。
【答案】(1) 第四周期ⅣA族 32
(2)S2->O2->Mg2+ (3)HClO =H++ClO -
4 4
(4)BC
(5) 离子键、非极性共价键 0.2mol
【解析】(1)由周期表可知,N元素在周期表中的位置为第四周期ⅣA族,原子序数为32;(2)Y和W
的简单离子电子层数相同,而Y的原子序数大于W,所以Y的简单离子的半径小于W,Y和W的简单离
子电子层数小于Z,所以Y和W的简单离子的都半径小于Z,所以Y、Z、W三种元素形成简单离子的半
径由大到小的顺序为S2->O2->Mg2+;(3)由周期表可知,M元素为Cl,其最高价氧化物的水化物为
HClO,在水中的电离方程式为HClO=H++ClO -;(4)A.X和Y同周期,同周期元素从左往右金属性依次
4 4 4
减弱,金属性越强,其单质的还原性越强,所以X>Y,但X是元素Na,在YM (MgCl )溶液中优先与水反
2 2
应,不会置换出Mg,A错误;B.Y属于第三周,所以与同周期的ⅢA元素的原子序数相差1,B正确;C.硅主要用于半导体器件的研制,目前用硅研发出的太阳能光伏电池,可用于路灯,C正确;D.元素N
位于金属与非金属的分界线附近,其性质与Al近似,但Al只能与强碱溶液反应生成氢气,而氨水是弱碱
溶液,不能与Al反应生成氢气,D错误;故选BC。(5)由X、W元素构成的原子个数比为1:1的化合物
为NaO,所含化学键类型为离子键、非极性共价键;讲NaO 投入水中,发生反应为2 Na O+2H O=4
2 2 2 2 2 2 2
NaOH+ O↑,该反应中每生成1mol O,转移电子数为2mol e-,产生2.24L气体(标准状况下),则产生
2 2
0.1mol O ,转移电子数为0.2mol e-。
2
17.(13分)如图为元素周期表的一部分。请回答下列问题。
(1)图中阴影部分所示区域的元素称为____元素,下列元素属于该区域的是____(填字母)。
A.Ba B.Fe C.Br D.Rb
(2)已知A、B、C、D、E、F六种短周期元素的原子半径和某些化合价如表:
元素 A B C D E F
化合价 -2 +5、-3 +4、-4 +6、-2 +2 +1
原子半径/nm 0.074 0.075 0.077 0.102 0.160 0.186
写出D元素在元素周期表中的位置____。
(3)C的最高价氧化物与E的单质在点燃条件下发生反应的化学方程式为____;由F的化合物生成A的
单质的化学方程式为____。
(4)C与氢元素可组成一种气体,该气体在标准状况下的密度为1.25g•L-1,该气体的摩尔质量为____。
(5)下列说法不正确的是____。A.元素最高正价与最低负价绝对值相等的元素一定处于第ⅣA族
B.第5周期第ⅤA族元素的原子序数为65
C.②形成的最简单氢化物比①形成的最简单氢化物的稳定性高
D.周期表中当某元素的周期序数大于其族序数时,该元素可能属于金属或非金属
(6)BrCl属于卤素互化物,性质与Cl 相似。写出BrCl与氢氧化钠溶液反应的化学方程式____。
2
【答案】(1) 过渡金属 B (2)三周期第ⅥA族
(3)CO +2Mg 2MgO+C 2Na O+2H O=2NaOH+O ↑
2 2 2 2 2
(4)28g/mol (5)ABD (6)BrCl+2NaOH=NaCl+NaBrO+H O
2
【解析】(1)如图中阴影部分所示区域为副族和VIII族元素,又称为过渡金属元素;选项中Ba、Br、
Rb为主族元素,Fe为过渡金属元素,所以 B正确;(2)A、D主要化合价为-2价,其中A无正化合价,则A为0元素、D为S元素;B化合价有+5、-3价,则B位于VA族,由于B的原子半径大于O、小于S,则
B为N元素;C的化合价为+4、-4价,则C位于IVA族,C的原子半径大于O、小于S,则C为C元素;E
为+2价, E的原子半径大于S,则E为Mg元素;F的化合价为+1价,原子半径大于Mg,则F为Na元
素,根据分析可知,D为S元素,在元素周期表中的位置是第三周期第ⅥA族;(3)C为C元素,C的最高
价氧化物为二氧化碳,E为Mg,镁与二氧化碳点燃生成氧化镁和C,反应的化学方程式为:CO+2Mg
2
2MgO+C ;F为Na元素,A为氧元素,其单质为氧气,由钠的化合物生成A单质,即过氧化钠与水反应
生成氢氧化钠和氧气,反应的化学方程式为: 2NaO+2H O=2NaOH+O ↑;(4)该气体的摩尔质量为:
2 2 2 2
;(5)A项,H元素化合价范围为-1~+1,其最高正价与最低负价绝对
值相等,但处于IA,故A错误;B项,第五周期第0族,原子序数为54,第五周期第VA族,其原子序数
应为:54-3=51,故 B错误;C项,②和①同周期,且在①右边,同周期元素越往右,非金属性越强,故
非金属性更强,②形成的最简单氢化物比形成的最简单氢化物的稳定性高,故C正确;D项,周期表中当
某元素的周期序数大于其族序数时,该元素处于左下方,属于金属元素,故D错误;故选ABD;(6)BrCl
属于卤素互化物,性质与Cl 相似,氯气与氢氧化钠溶液反应的化学方程式:
2
Cl+2NaOH=NaCl+NaClO+H O,BrCl与氢氧化钠溶液反应的化学方程式:
2 2
BrCl+2NaOH=NaCl+NaBrO+H O。
2
18.(14分)A、B、C、D、E、F为短周期元素,非金属元素A最外层电子数与其周期数相同,B的最
外层电子数是其所在周期数的2倍。B单质在D单质中充分燃烧能生成B的最高价化合物 。 与
具有相同的电子数。A单质在F单质中燃烧,产物溶于水得到一种强酸M。G是应用最广泛的金属元素。
回答下列问题:
(1) 的离子结构示意图为 。
(2)G在周期表中的位置是 。
(3)B、D、E组成的一种常见盐中,D的质量分数约为 ,该盐溶液与少量M溶液反应的离子方程
式为 。
(4)由这些元素组成的物质,其组成和结构信息如下:
物质 组成和结构信息
a 含有A的二元离子化合物
b 含D且含非极性共价键的二元离子化合物,阴阳离子数之比为1∶2
c 化学式为BDF
2
①a的化学式为 。
②b的一种常见用途为 。
③已知c中所有原子均满足8电子稳定结构,该化合物的电子式为 。
(5)下列关于元素A、B、D、E、F的说法正确的是 。a.最高价含氧酸的酸性:
b.离子半径比较:
c.A、B均可与D形成直线形分子
d.可用 试纸测 溶液的
【答案】(1) (2)第四周期第Ⅷ族
(3) CO 2-+H+=HCO-
3 3
(4) NaH 供氧剂或氧化剂
(5)ab
【解析】A、B、C、D、E、F为短周期元素,非金属元素 A 最外层电子数与其周期数相同,则 A
为 H;B 的最外层电子数是其所在周期数的2 倍, 则 B 为C 或S,B 在D 中充分燃烧能生成其最高
价化合物 BD,则 D 为O,B 的最高正价为+4 价,则 B 为C,E+与 D2- 具有相同的电子数,则 E 为
2
Na ; A 在F 中燃烧,产物溶于水得到种强酸M,则 F 为 Cl,M盐酸溶液;G是应用最广泛的金属元
素,G为Fe。(1)E 为Na, E+的离子结构示意图为 ;(2)G为Fe,G在周期表中的位置是第四
周期第Ⅷ族;(3)B为C,D为O,E为Na,组成的一种常见盐中是NaCO,O的质量分数约为45%,该盐
2 3
溶液与少量盐酸溶液反应的离子方程式为CO2-+H+=HCO-;(4)①这几种元素只有 Na 能与 H 形成离子化
3 3
合物,含有A的二元离子化合物为NaH,a的化学式为NaH;②D 为O,含D且含非极性共价键的二元离
子化合物,阴阳离子数之比为1:2,b为NaO,NaO 能与水反应放出氧气,b的一种常见用途为供氧剂
2 2 2 2
或氧化剂;③已知c中所有原子均满足8电子稳定结构,BDF 为COCl ,该化合物的电子式为
2 2
;(5)a项,F 为 Cl,B 为C,Cl的非金属性强于C,故最高价含氧酸的酸性:F>B,故a正
确;b项,D 为O,E 为Na ,离子半径比较:D2->E+,故b正确;c项,A 为 H,B 为C,D 为O,
A、B均可与D形成的分子水喝二氧化碳,水是V形,故c错误;d项,D 为O,E 为Na ,F 为 Cl,组
成NaClO具有强氧化性,不能用 pH试纸测EFD溶液的 pH,故d错误;故选ab。
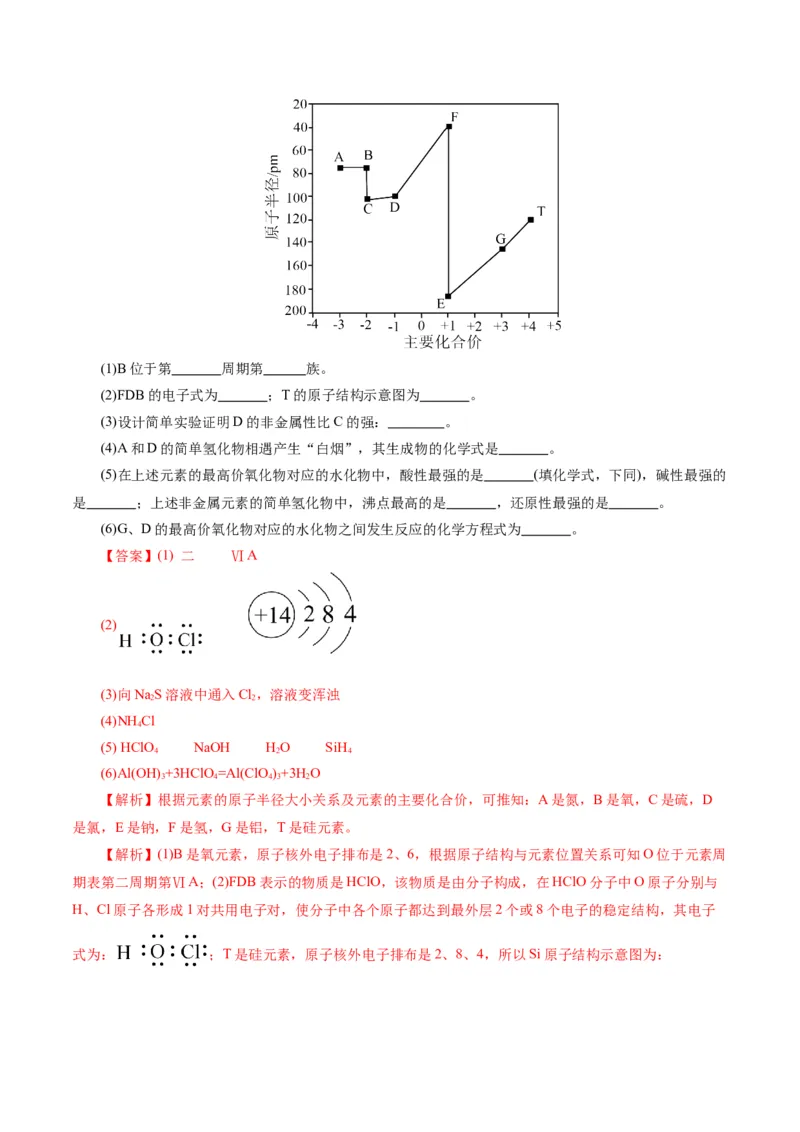
19.(16分)部分短周期主族元素的原子半径和主要化合价的关系如图所示,其中E、G、T位于同一周
期。回答下列问题:(1)B位于第 周期第 族。
(2)FDB的电子式为 ;T的原子结构示意图为 。
(3)设计简单实验证明D的非金属性比C的强: 。
(4)A和D的简单氢化物相遇产生“白烟”,其生成物的化学式是 。
(5)在上述元素的最高价氧化物对应的水化物中,酸性最强的是 (填化学式,下同),碱性最强的
是 ;上述非金属元素的简单氢化物中,沸点最高的是 ,还原性最强的是 。
(6)G、D的最高价氧化物对应的水化物之间发生反应的化学方程式为 。
【答案】(1) 二 ⅥA
(2)
(3)向NaS溶液中通入Cl,溶液变浑浊
2 2
(4)NH Cl
4
(5) HClO NaOH H O SiH
4 2 4
(6)Al(OH) +3HClO =Al(ClO )+3H O
3 4 4 3 2
【解析】根据元素的原子半径大小关系及元素的主要化合价,可推知:A是氮,B是氧,C是硫,D
是氯,E是钠,F是氢,G是铝,T是硅元素。
【解析】(1)B是氧元素,原子核外电子排布是2、6,根据原子结构与元素位置关系可知O位于元素周
期表第二周期第ⅥA;(2)FDB表示的物质是HClO,该物质是由分子构成,在HClO分子中O原子分别与
H、Cl原子各形成1对共用电子对,使分子中各个原子都达到最外层2个或8个电子的稳定结构,其电子
式为: ;T是硅元素,原子核外电子排布是2、8、4,所以Si原子结构示意图为:;(3)C是硫,D是氯,二者是同一周期元素,元素的非金属性越强,其单质的氧化性就越
强,活动性强的可以把活动性弱的从化合物中置换出来,故可以根据向NaS溶液中通入Cl,溶液变浑
2 2
浊,发生反应:Cl+Na S=2NaCl+S↓,由此可证明元素的非金属性:Cl>S;(4)A是氮,D是氯,二者的氢
2 2
化物NH 、HCl在空气中相遇,会发生反应:NH +HCl=NH Cl,NH Cl是白色固体,因此会产生白烟想
3 3 4 4
象;(5)在上述元素的最高价氧化物对应的水化物中,酸性最强的是高氯酸,其化学式是HClO;碱性最强
4
的是氢氧化钠,其化学式是NaOH;上述非金属元素的简单氢化物中,HO呈液态,其余氢化物都是气
2
态,故沸点最高的氢化物是HO;元素的非金属性越强,其简单氢化物稳定性就越强,该物质的还原性就
2
越弱;元素的非金属性越弱,形成的简单氢化物的稳定性就越弱,该物质的还原性就越强。在上述元素中
非金属性最弱的非金属元素是Si元素,则硅烷SiH 的还原性最强;(6)D是Cl,G是Al,二者的最高价氧
4
化物对应的水化物分别是HClO、Al(OH) ,前者是一元强酸,后者是两性氢氧化物,Al(OH) 能够与强酸
4 3 3
HClO 发生反应产生盐和水,该反应的化学方程式为:Al(OH) +3HClO =Al(ClO )+3H O。
4 3 4 4 3 2