文档内容
备战2025年高考化学【二轮·突破提升】专题复习讲义
专题18 新型电化学装置及其应用
讲义包含四部分:把握命题方向►精选高考真题►高效解题策略►各地最新模拟
电化学是高考的热点,试题的背景较为新颖。近年的高考通常以新型燃料电池、比能量高的新型电池
为载体,考查原电池的工作原理,电解池的原理与物质的制备、金属的提纯、金属的防护等。复习时建议
关注以下几点:
(1)电极的判断、电极反应式的书写。
(2)电解质溶液pH的判断、电化学中的计算。
(3)隔膜电池中交换膜种类的判断、隔膜的作用。
(4)新型燃料电池、新型可充电电池的工作原理。
(5)利用电化学原理进行金属的防腐。
预计2025年高考选择题中,仍然以某一个新型电池为背景考查电化学知识,结合物质的制备、废弃物
的处理等内容进行考察,电极反应方程式的书写或正误判断、离子移动的方向、电极产物种类的判断与量
的计算等仍是考察的重点。
1.(2025·浙江·高考真题)一种可充放电 电池的结构示意图如图所示。该电池放电时,产物为
和 ,随温度升高Q(消耗 转移的电子数)增大。下列说法不正确的是
A.熔融盐中 的物质的量分数影响充放电速率
B.充放电时, 优先于 通过固态电解质膜
C.放电时,随温度升高Q增大,是因为正极区 转化为
D.充电时,锂电极接电源负极
【答案】C【分析】 电池放电时,锂电极为负极,发生反应: ,多孔功能电极为正极,低温时发生
反应: ,随温度升高Q增大,正极区 转化为 ;充电时,锂电极为阴极,得到电子,多
孔功能电极为阳极, 或 失去电子。
【详解】A.由分析可知,电池总反应方程式为: 或 ,充放电时
有 参与或生成,因此熔融盐中 的物质的量分数影响充放电速率,A正确;
B. 比 的半径小,因此 优先于 通过固态电解质膜,B正确;
C.放电时,正极得到电子, 中氧原子为-1价, 中氧原子为-2价,因此随温度升高Q增大,正极区
转化为 ,C错误;
D.充电时,锂电极为阴极,连接电源负极,D正确;
答案选C。
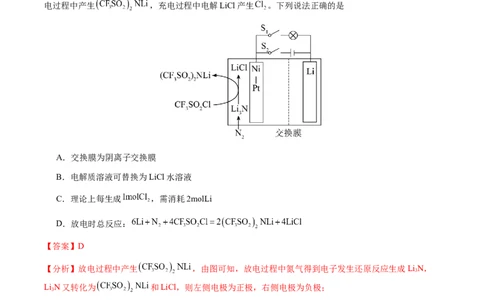
2.(2024·广西·高考真题)某新型钠离子二次电池(如图)用溶解了NaPF 的二甲氧基乙烷作电解质溶液。
6
放电时嵌入PbSe中的Na变成Na+后脱嵌。下列说法错误的是
A.外电路通过1mol电子时,理论上两电极质量变化的差值为23g
B.充电时,阳极电极反应为:
C.放电一段时间后,电解质溶液中的Na+浓度基本保持不变
D.电解质溶液不能用NaPF 的水溶液替换
6
【答案】A
【分析】放电时嵌入PbSe中的Na变成Na+后脱嵌,则右侧电极为负极,Na失电子生成Na+;Na+透过允许
Na+通过的隔膜从右侧进入左侧,则左侧为正极。
【详解】A.外电路通过1mol电子时,负极有1molNa失电子生成Na+进入右侧溶液,溶液中有1molNa+从
右侧进入左侧,并与正极的Na V(PO ) 结合,则理论上两电极质量变化的差值为2mol×23g/mol=46g,A
3-x 2 4 3
错误;
B.充电时,左侧电极为阳极,NaV(PO ) 失电子生成Na V(PO ),则阳极电极反应为:
3 2 4 3 3-x 2 4 3,B正确 ;
C.放电一段时间后,负极产生的Na+的物质的量与负极区通过隔膜进入左极区的Na+的物质的量相同,进
入左极区的Na+与参加左侧正极反应的Na+的物质的量相同,所以电解质溶液中的Na+浓度基本保持不变,
C正确 ;
D.Na能与水反应,所以电解质溶液不能用NaPF 的水溶液替换,D正确 ;
6
故选 A。
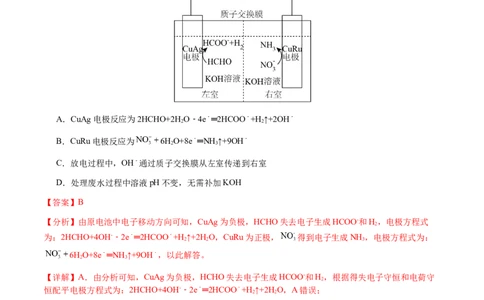
3.(2024·福建·高考真题)一种兼具合成功能的新型锂电池工作原理如图。电解质为含 有机溶液。放
电过程中产生 ,充电过程中电解LiCl产生 。下列说法正确的是
A.交换膜为阴离子交换膜
B.电解质溶液可替换为LiCl水溶液
C.理论上每生成 ,需消耗2molLi
D.放电时总反应:
【答案】D
【分析】放电过程中产生 ,由图可知,放电过程中氮气得到电子发生还原反应生成LiN,
3
LiN又转化为 和LiCl,则左侧电极为正极,右侧电极为负极;
3
【详解】A.放电过程中负极锂失去电子形成锂离子,锂离子通过阳离子交换膜进入左侧生成
,A错误;
B.锂为活泼金属,会和水反应,故电解质溶液不能为水溶液,B错误;
C.充电过程中电解LiCl失去电子发生氧化反应产生 : ,锂离子在阴极得到电子发生还
原生成锂单质: ,则每生成 ,同时生成2mol Li;放电过程中,消耗6mol Li,同时生
成4mol LiCl,则整个充放电过程来看,理论上每生成 ,需消耗1mol Li,C错误;D.由分析,放电过程中,正极氮气得到电子发生还原反应生成LiN,LiN又转化为 和
3 3
LiCl,负极锂失去电子发生氧化反应生成锂离子,总反应为
,D正确;
故选D。
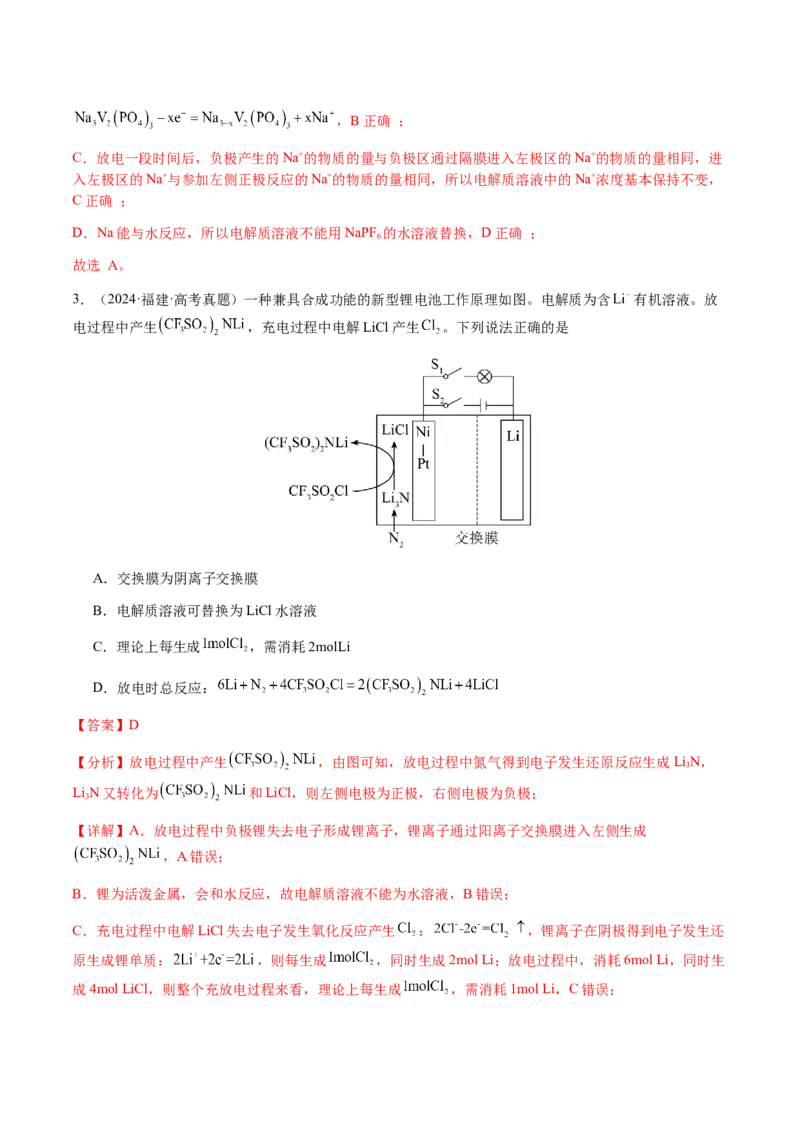
4.(2024·江西·高考真题)我国学者发明了一种新型多功能甲醛﹣硝酸盐电池,可同时处理废水中的甲醛
和硝酸根离子(如图)。下列说法正确的是
A.CuAg电极反应为2HCHO+2H O﹣4e﹣═2HCOO﹣+H ↑+2OH﹣
2 2
B.CuRu电极反应为 6HO+8e﹣═NH ↑+9OH﹣
2 3
C.放电过程中,OH﹣通过质子交换膜从左室传递到右室
D.处理废水过程中溶液pH不变,无需补加KOH
【答案】B
【分析】由原电池中电子移动方向可知,CuAg为负极,HCHO失去电子生成HCOO-和H,电极方程式
2
为:2HCHO+4OH-﹣2e﹣═2HCOO﹣+H ↑+2H O,CuRu为正极, 得到电子生成NH ,电极方程式为:
2 2 3
6HO+8e﹣═NH ↑+9OH﹣,以此解答。
2 3
【详解】A.由分析可知,CuAg为负极,HCHO失去电子生成HCOO-和H,根据得失电子守恒和电荷守
2
恒配平电极方程式为:2HCHO+4OH-﹣2e﹣═2HCOO﹣+H ↑+2H O,A错误;
2 2
B.由分析可知,CuRu为正极, 得到电子生成NH ,根据得失电子守恒和电荷守恒配平电极方程式
3
为: 6HO+8e﹣═NH ↑+9OH﹣,B正确;
2 3
C.质子交换膜只允许H+通过,C错误;
D.由分析可知,负极电极方程式为:2HCHO+4OH-﹣2e﹣═2HCOO﹣+H ↑+2H O,正极电极方程式为:
2 2
6HO+8e﹣═NH ↑+9OH﹣,总反应为8HCHO+ 7OH-=NH +8HCOO-+4 H ↑+2H O,处理废水
2 3 3 2 2
过程中消耗OH-,溶液pH减小,需补加 KOH,D错误;
故选B。5.(2024·浙江·高考真题)金属腐蚀会对设备产生严重危害,腐蚀快慢与材料种类、所处环境有关。下图
为两种对海水中钢闸门的防腐措施示意图:
下列说法正确的是
A.图1、图2中,阳极材料本身均失去电子
B.图2中,外加电压偏高时,钢闸门表面可发生反应:
C.图2中,外加电压保持恒定不变,有利于提高对钢闸门的防护效果
D.图1、图2中,当钢闸门表面的腐蚀电流为零时,钢闸门、阳极均不发生化学反应
【答案】B
【详解】A.图1为牺牲阳极的阴极保护法,牺牲阳极一般为较活泼金属,其作为原电池的负极,其失去
电子被氧化;图2为外加电流保护法,阳极材料为辅助阳极,其通常是惰性电极,本身不失去电子,电解
质溶液中的阴离子在其表面失去电子,如海水中的 ,A不正确;
B.图2中,外加电压偏高时,钢闸门表面积累的电子很多,除了海水中的 放电外,海水中溶解的 也
会竞争放电,故可发生 ,B正确;
C.图2为外加电流保护法,理论上只要能对抗钢闸门表面的腐蚀电流即可,当钢闸门表面的腐蚀电流为
零时保护效果最好;腐蚀电流会随着环境的变化而变化,若外加电压保持恒定不变,则不能保证抵消腐蚀
电流,不利于提高对钢闸门的防护效果,C不正确;
D.图1当钢闸门表面的腐蚀电流为零时,说明钢闸门被保护,钢闸门不发生化学反应,图2中当钢闸门
表面的腐蚀电流为零时,说明钢闸门被保护,辅助阳极上发生了氧化反应,D不正确;
综上所述,本题选B。
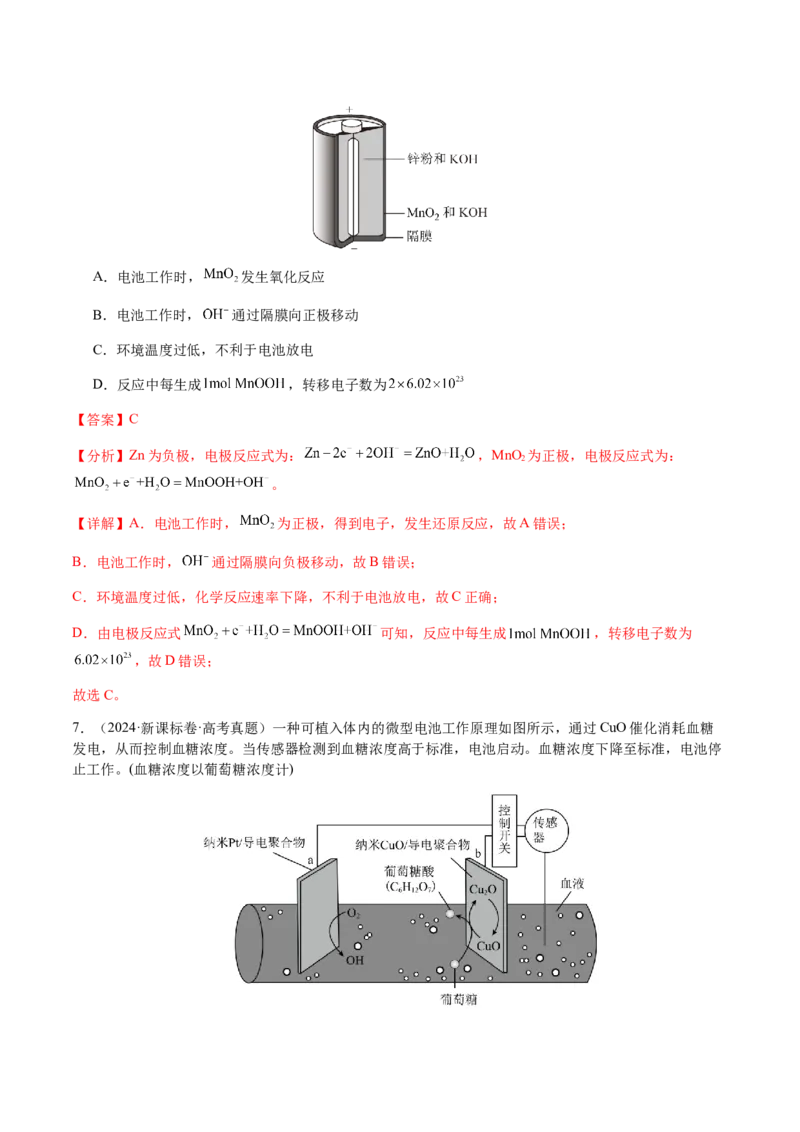
6.(2024·江苏·高考真题)碱性锌锰电池的总反应为 ,电池构造示意
图如图所示。下列有关说法正确的是A.电池工作时, 发生氧化反应
B.电池工作时, 通过隔膜向正极移动
C.环境温度过低,不利于电池放电
D.反应中每生成 ,转移电子数为
【答案】C
【分析】Zn为负极,电极反应式为: ,MnO 为正极,电极反应式为:
2
。
【详解】A.电池工作时, 为正极,得到电子,发生还原反应,故A错误;
B.电池工作时, 通过隔膜向负极移动,故B错误;
C.环境温度过低,化学反应速率下降,不利于电池放电,故C正确;
D.由电极反应式 可知,反应中每生成 ,转移电子数为
,故D错误;
故选C。
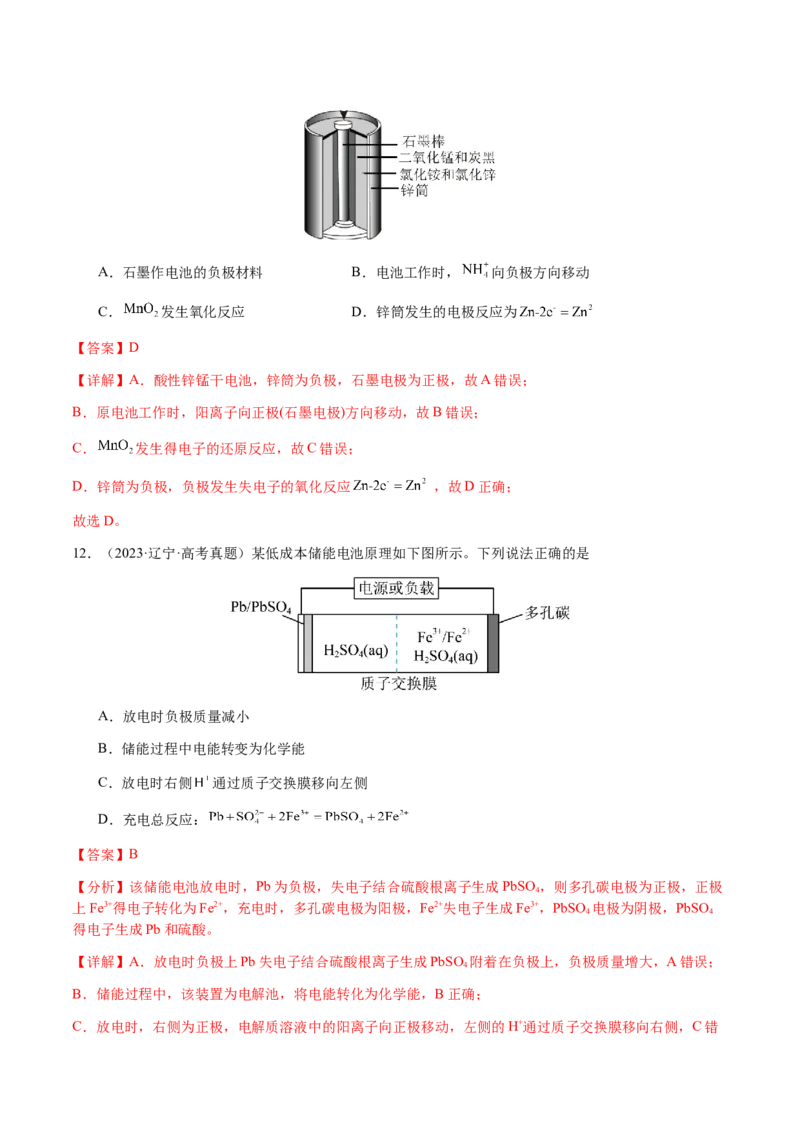
7.(2024·新课标卷·高考真题)一种可植入体内的微型电池工作原理如图所示,通过CuO催化消耗血糖
发电,从而控制血糖浓度。当传感器检测到血糖浓度高于标准,电池启动。血糖浓度下降至标准,电池停
止工作。(血糖浓度以葡萄糖浓度计)电池工作时,下列叙述错误的是
A.电池总反应为
B.b电极上CuO通过Cu(Ⅱ)和Cu(Ⅰ)相互转变起催化作用
C.消耗18mg葡萄糖,理论上a电极有0.4mmol电子流入
D.两电极间血液中的 在电场驱动下的迁移方向为b→a
【答案】C
【分析】由题中信息可知,b电极为负极,发生反应 ,然后再发生
;a电极为正极,发生反应 ,在这个过程中发生
的总反应为 。
【详解】A.由题中信息可知,当电池开始工作时,a电极为电池正极,血液中的 在a电极上得电子生
成 ,电极反应式为 ;b电极为电池负极, 在b电极上失电子转化成
CuO,电极反应式为 ,然后葡萄糖被CuO氧化为葡萄糖酸,CuO被还原
为 ,则电池总反应为 ,A正确;
B.b电极上CuO将葡萄糖被CuO氧化为葡萄糖酸后被还原为 , 在b电极上失电子转化成CuO,
在这个过程中CuO的质量和化学性质保持不变,因此,CuO通过Cu(Ⅱ)和Cu(Ⅰ)相互转变起催化作用,B
正确;
C.根据反应 可知, 参加反应时转移2 mol电子, 的
物质的量为0.1 mmol,则消耗18 mg葡萄糖时,理论上a电极有0.2 mmol电子流入,C错误;
D.原电池中阳离子从负极移向正极迁移,故 迁移方向为b→a,D正确。
综上所述,本题选C。
8.(2024·全国甲卷·高考真题)科学家使用 研制了一种 可充电电池(如图所示)。电池工
作一段时间后, 电极上检测到 和少量 。下列叙述正确的是
A.充电时, 向阳极方向迁移
B.充电时,会发生反应C.放电时,正极反应有
D.放电时, 电极质量减少 , 电极生成了
【答案】C
【分析】Zn具有比较强的还原性, 具有比较强的氧化性,自发的氧化还原反应发生在Zn与MnO 之
2
间,所以 电极为正极,Zn电极为负极,则充电时 电极为阳极、Zn电极为阴极。
【详解】A.充电时该装置为电解池,电解池中阳离子向阴极迁移,即 向阴极方向迁移,A不正确;
B.放电时,负极的电极反应为 ,则充电时阴极反应为Zn2++2e-=Zn,即充电时Zn元素化合
价应降低,而选项中Zn元素化合价升高,B不正确;
C.放电时 电极为正极,正极上检测到 和少量 ,则正极上主要发生的电极反应是
,C正确;
D.放电时,Zn电极质量减少0.65g(物质的量为0.010mol),电路中转移0.020mol电子,由正极的主要
反应 可知,若正极上只有 生成,则生成 的物质的量为
0.020mol,但是正极上还有 生成,因此, 的物质的量小于0.020mol,D不正确;
综上所述,本题选C。
9.(2024·安徽·高考真题)我国学者研发出一种新型水系锌电池,其示意图如下。该电池分别以
(局部结构如标注框内所示)形成的稳定超分子材料和 为电极,以 和 混合液为电解质溶液。下
列说法错误的是
A.标注框内所示结构中存在共价键和配位键
B.电池总反应为:
C.充电时,阴极被还原的 主要来自
D.放电时,消耗 ,理论上转移 电子
【答案】C【分析】由图中信息可知,该新型水系锌电池的负极是锌、正极是超分子材料;负极的电极反应式为
,则充电时,该电极为阴极,电极反应式为 ;正极上发生 ,则充
电时,该电极为阳极,电极反应式为 。
【详解】A.标注框内所示结构属于配合物,配位体中存在碳碳单键、碳碳双键、碳氮单键、碳氮双键和
碳氢键等多种共价键,还有由 提供孤电子对、 提供空轨道形成的配位键,A正确;
B.由以上分析可知,该电池总反应为 ,B正确;
C.充电时,阴极电极反应式为 ,被还原的Zn2+主要来自电解质溶液,C错误;
D.放电时,负极的电极反应式为 ,因此消耗0.65 g Zn(物质的量为0.01mol),理论上转移
0.02 mol电子,D正确;
综上所述,本题选C。
10.(2024·浙江·高考真题)破损的镀锌铁皮在氨水中发生电化学腐蚀,生成 和 ,下列说
法不正确的是
A.氨水浓度越大,腐蚀趋势越大
B.随着腐蚀的进行,溶液 变大
C.铁电极上的电极反应式为:
D.每生成标准状况下 ,消耗
【答案】C
【详解】A.氨水浓度越大,越容易生成 ,腐蚀趋势越大,A正确;
B.腐蚀的总反应为Zn+4NH •H O= +H ↑+2H O+2OH-,有OH-离子生成,溶液 变大,B
3 2 2 2
正确;
C.该电化学腐蚀中Zn作负极,Fe作正极,正极上氢离子得电子生成氢气,铁电极上的电极反应式为:
,C错误;
D.根据得失电子守恒,每生成标准状况下 ,转移电子数为 ,消耗
,D正确;
故选C。
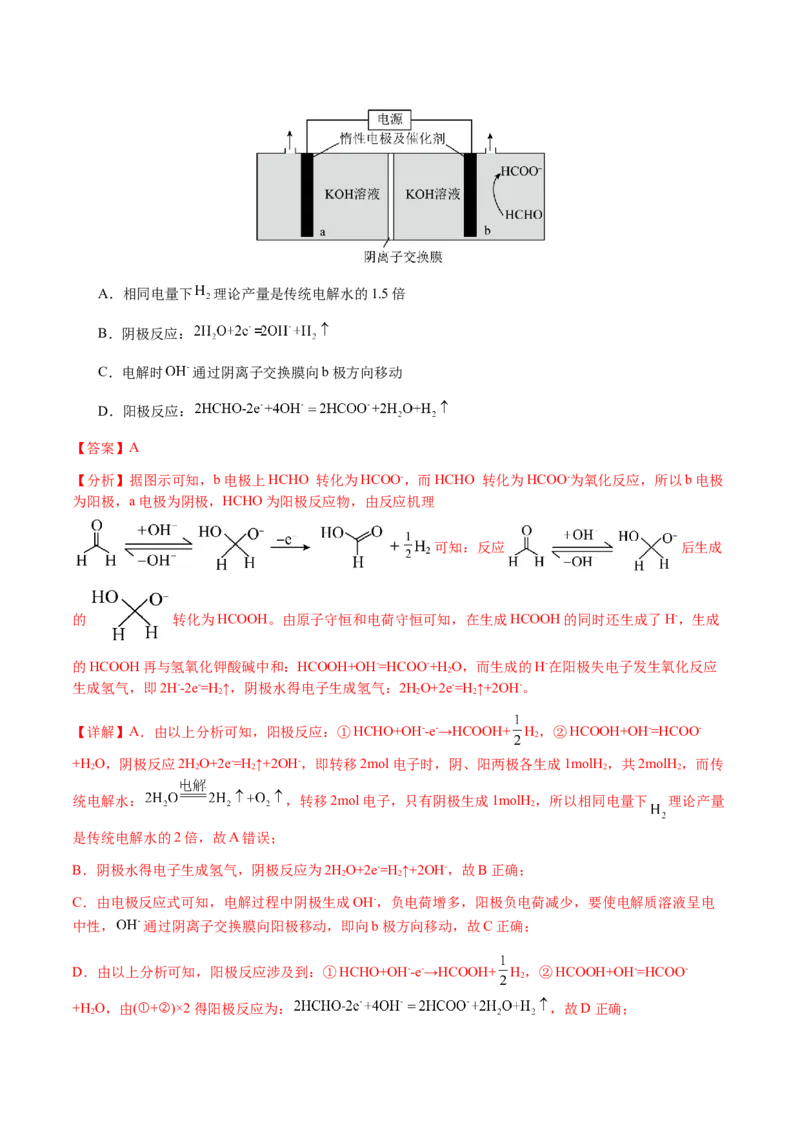
11.(2024·北京·高考真题)酸性锌锰干电池的构造示意图如下。关于该电池及其工作原理,下列说法正
确的是A.石墨作电池的负极材料 B.电池工作时, 向负极方向移动
C. 发生氧化反应 D.锌筒发生的电极反应为
【答案】D
【详解】A.酸性锌锰干电池,锌筒为负极,石墨电极为正极,故A错误;
B.原电池工作时,阳离子向正极(石墨电极)方向移动,故B错误;
C. 发生得电子的还原反应,故C错误;
D.锌筒为负极,负极发生失电子的氧化反应 ,故D正确;
故选D。
12.(2023·辽宁·高考真题)某低成本储能电池原理如下图所示。下列说法正确的是
A.放电时负极质量减小
B.储能过程中电能转变为化学能
C.放电时右侧 通过质子交换膜移向左侧
D.充电总反应:
【答案】B
【分析】该储能电池放电时,Pb为负极,失电子结合硫酸根离子生成PbSO ,则多孔碳电极为正极,正极
4
上Fe3+得电子转化为Fe2+,充电时,多孔碳电极为阳极,Fe2+失电子生成Fe3+,PbSO 电极为阴极,PbSO
4 4
得电子生成Pb和硫酸。
【详解】A.放电时负极上Pb失电子结合硫酸根离子生成PbSO 附着在负极上,负极质量增大,A错误;
4
B.储能过程中,该装置为电解池,将电能转化为化学能,B正确;
C.放电时,右侧为正极,电解质溶液中的阳离子向正极移动,左侧的H+通过质子交换膜移向右侧,C错误;
D.充电时,总反应为PbSO +2Fe2+=Pb+ +2Fe3+,D错误;
4
故答案选B。
13.(2024·重庆·高考真题)我国科研工作者研发了一种新型复合电极材料,可将 电催化转化为甲
酸,如图是电解装置示意图。下列说法正确的是
A.电解时电极N上产生 B.电解时电极M上发生氧化反应
C.阴、阳离子交换膜均有两种离子通过 D.总反应为
【答案】D
【分析】催化电极M上二氧化碳得到电子发生还原反应和水生成甲酸根离子和氢氧根离子:
,甲酸根离子和氢氧根离子通过阴离子膜加入中间室,氢氧根离子和氢离子
生成水、甲酸根离子和氢离子生成甲酸,则M是阴极,那么N是阳极,阳极水失去电子发生氧化反应生成
氧气: ,氢离子通过阳离子膜进入中间室;
【详解】A.酸性条件下,电解时电极N上水失去电子发生氧化反应生成氧气: ,A
错误;
B.催化电极M上二氧化碳得到电子发生还原反应生成甲酸,B错误;
C.由分析,阳离子交换膜有1种离子通过,C错误;
D.由分析,总反应为二氧化碳和水生成甲酸和氧气,D正确;
故选D。
14.(2024·广东·高考真题)一种基于氯碱工艺的新型电解池(下图),可用于湿法冶铁的研究。电解过程
中,下列说法不正确的是A.阳极反应:
B.阴极区溶液中 浓度逐渐升高
C.理论上每消耗 ,阳极室溶液减少
D.理论上每消耗 ,阴极室物质最多增加
【答案】C
【分析】左侧电极为阴极,发生还原反应, 在碱性条件下转化为Fe,从而实现冶铁,电极反应为:
;右侧电极为阳极,溶液为饱和食盐水, 放电产生氯气,电极反应
为: ;中间为阳离子交换膜, 由阳极向阴极移动。
【详解】A.由分析可知,阳极反应为: ,A正确;
B.由分析可知,阴极反应为: ,消耗水产生 ,阴极区溶液中 浓
度逐渐升高,B正确;
C.由分析可知,理论上每消耗 ,转移6mol电子,产生3mol ,同时有6mol 由阳极转移
至阴极,则阳极室溶液减少 ,C错误;
D.由分析可知,理论上每消耗 ,转移6mol电子,有6mol 由阳极转移至阴极,阴极室物质
最多增加 ,D正确;
故选C。
15.(2024·湖南·高考真题)在 水溶液中,电化学方法合成高能物质 时,伴随少量 生成,
电解原理如图所示,下列说法正确的是A.电解时, 向Ni电极移动
B.生成 的电极反应:
C.电解一段时间后,溶液pH升高
D.每生成 的同时,生成
【答案】B
【分析】由电解原理图可知,Ni电极产生氢气,作阴极,发生还原反应,电解质溶液为KOH水溶液,则
电极反应为: ;Pt电极 失去电子生成 ,作阳极,电极反应为:
,同时,Pt电极还伴随少量 生成,电极反应为:
。
【详解】A.由分析可知,Ni电极为阴极,Pt电极为阳极,电解过程中,阴离子向阳极移动,即 向Pt
电极移动,A错误;
B.由分析可知,Pt电极 失去电子生成 ,电解质溶液为KOH水溶液,电极反应为:
,B正确;
C.由分析可知,阳极主要反应为: ,阴极反应为:
,则电解过程中发生的总反应主要为: ,反应
消耗 ,生成 ,电解一段时间后,溶液pH降低,C错误;
D.根据电解总反应: 可知,每生成1mol ,生成0.5mol ,
但Pt电极伴随少量 生成,发生电极反应: ,则生成1molH 时得到的部分电子由
2
OH-放电产生O 提供,所以生成 小于0.5mol,D错误;
2
故选B。
16.(2024·山东·高考真题)以不同材料修饰的 为电极,一定浓度的 溶液为电解液,采用电解和催
化相结合的循环方式,可实现高效制 和 ,装置如图所示。下列说法错误的是A.电极a连接电源负极
B.加入Y的目的是补充
C.电解总反应式为
D.催化阶段反应产物物质的量之比
【答案】B
【分析】电极b上Br-发生失电子的氧化反应转化成 ,电极b为阳极,电极反应为Br- -6e-+3H O=
2
+6H+;则电极a为阴极,电极a的电极反应为2HO+2e-=H ↑+2OH-;电解总反应式为Br-+3H O
2 2 2
+3H ↑;催化循环阶段 被还原成Br-循环使用、同时生成O,实现高效制H 和O,即Z为O。
2 2 2 2 2
【详解】A.根据分析,电极a为阴极,连接电源负极,A项正确;
B.根据分析电解过程中消耗HO和Br-,而催化阶段 被还原成Br-循环使用,故加入Y的目的是补充
2
HO,维持NaBr溶液为一定浓度,B项错误;
2
C.根据分析电解总反应式为Br-+3H O +3H ↑,C项正确;
2 2
D.催化阶段,Br元素的化合价由+5价降至-1价,生成1molBr-得到6mol电子,O元素的化合价由-2价升
至0价,生成1molO 失去4mol电子,根据得失电子守恒,反应产物物质的量之比n(O ) ∶n(Br-)=6∶4=3∶2,D
2 2
项正确;
答案选B。
17.(2024·湖北·高考真题)我国科学家设计了一种双位点 电催化剂,用 和 电化学催
化合成甘氨酸,原理如图,双极膜中 解离的 和 在电场作用下向两极迁移。已知在 溶液
中,甲醛转化为 ,存在平衡 。 电极上发生的电子转移反
应为 。下列说法错误的是A.电解一段时间后阳极区 减小
B.理论上生成 双极膜中有 解离
C.阳极总反应式为
D.阴极区存在反应
【答案】B
【分析】在KOH溶液中HCHO转化为HOCH O-:HCHO+OH-→HOCH O-,存在平衡HOCH O-+OH-
2 2 2
[OCH O]2-+H O,Cu电极上发生的电子转移反应为[OCH O]2--e-=HCOO-+H∙,H∙结合成H,Cu电极为阳
2 2 2 2
极;PbCu电极为阴极,首先HOOC—COOH在Pb上发生得电子的还原反应转化为OHC—COOH:
HC O+2e-+2H+=OHC—COOH+H O,OHC—COOH与HO—N+H 反应生成HOOC—CH=N—OH:OHC—
2 2 4 2 3
COOH+HO—N+H→HOOC—CH=N—OH+H O+H+,HOOC—CH=N—OH发生得电子的还原反应转化成
3 2
HN+CHCOOH:HOOC—CH=N—OH+4e-+5H+=H N+CHCOOH+H O。
3 2 3 2 2
【详解】A.根据分析,电解过程中,阳极区消耗OH-、同时生成HO,故电解一段时间后阳极区c(OH-)减
2
小,A项正确;
B.根据分析,阴极区的总反应为HC O+HO—N+H+6e-+6H+= H N+CHCOOH+3H O,1molH O解离成
2 2 4 3 3 2 2 2
1molH+和1molOH-,故理论上生成1molH N+CHCOOH双极膜中有6molH O解离,B项错误;
3 2 2
C.根据分析,结合装置图,阳极总反应为2HCHO-2e-+4OH-=2HCOO-+H ↑+2H O,C项正确;
2 2
D.根据分析,阴极区的Pb上发生反应HC O+2e-+2H+=OHC—COOH+H O,D项正确;
2 2 4 2
答案选B。
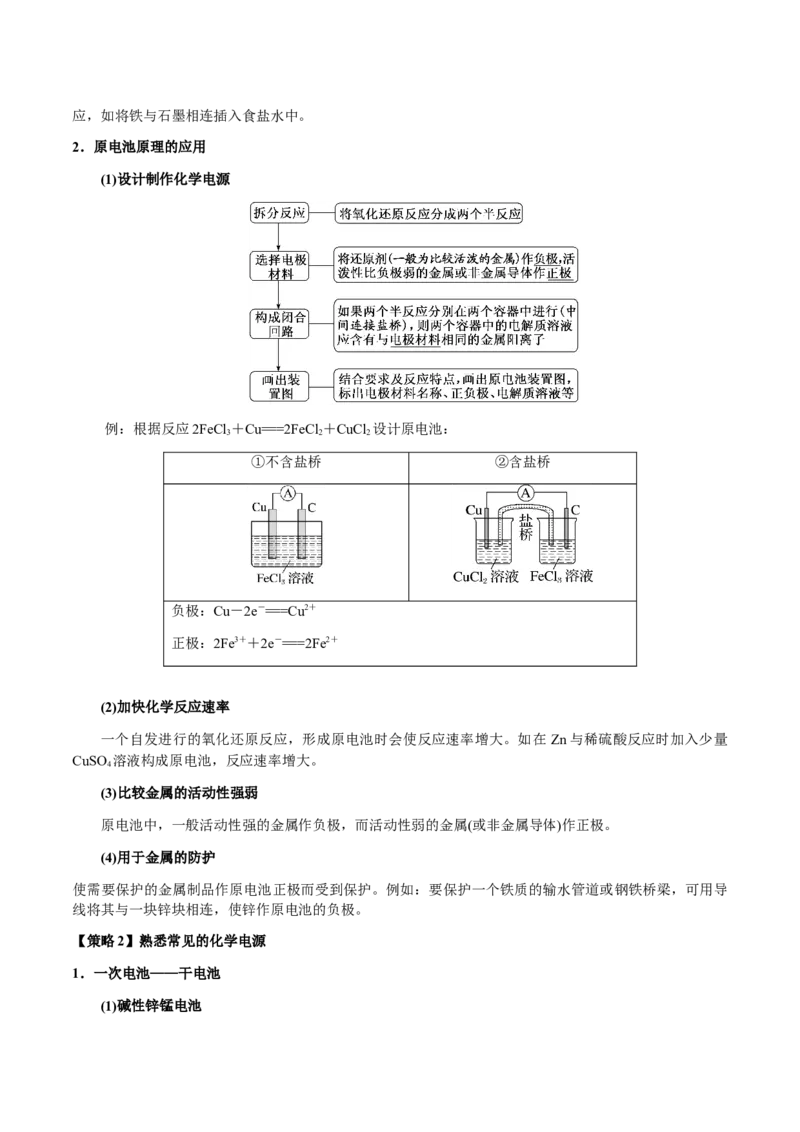
18.(2024·吉林·高考真题)“绿色零碳”氢能前景广阔。为解决传统电解水制“绿氢”阳极电势高、反
应速率缓慢的问题,科技工作者设计耦合 高效制 的方法,装置如图所示。部分反应机理为:
。下列说法错误的是A.相同电量下 理论产量是传统电解水的1.5倍
B.阴极反应:
C.电解时 通过阴离子交换膜向b极方向移动
D.阳极反应:
【答案】A
【分析】据图示可知,b电极上HCHO 转化为HCOO-,而HCHO 转化为HCOO-为氧化反应,所以b电极
为阳极,a电极为阴极,HCHO为阳极反应物,由反应机理
可知:反应 后生成
的 转化为HCOOH。由原子守恒和电荷守恒可知,在生成HCOOH的同时还生成了H-,生成
的HCOOH再与氢氧化钾酸碱中和:HCOOH+OH-=HCOO-+H O,而生成的H-在阳极失电子发生氧化反应
2
生成氢气,即2H--2e-=H ↑,阴极水得电子生成氢气:2HO+2e-=H ↑+2OH-。
2 2 2
【详解】A.由以上分析可知,阳极反应:①HCHO+OH--e-→HCOOH+ H,②HCOOH+OH-=HCOO-
2
+H O,阴极反应2HO+2e-=H ↑+2OH-,即转移2mol电子时,阴、阳两极各生成1molH ,共2molH ,而传
2 2 2 2 2
统电解水: ,转移2mol电子,只有阴极生成1molH ,所以相同电量下 理论产量
2
是传统电解水的2倍,故A错误;
B.阴极水得电子生成氢气,阴极反应为2HO+2e-=H ↑+2OH-,故B正确;
2 2
C.由电极反应式可知,电解过程中阴极生成OH-,负电荷增多,阳极负电荷减少,要使电解质溶液呈电
中性, 通过阴离子交换膜向阳极移动,即向b极方向移动,故C正确;
D.由以上分析可知,阳极反应涉及到:①HCHO+OH--e-→HCOOH+ H,②HCOOH+OH-=HCOO-
2
+H O,由(①+②)×2得阳极反应为: ,故D正确;
2答案选A。
19.(2023·辽宁·高考真题)某无隔膜流动海水电解法制 的装置如下图所示,其中高选择性催化剂
可抑制 产生。下列说法正确的是
A.b端电势高于a端电势 B.理论上转移 生成
C.电解后海水 下降 D.阳极发生:
【答案】D
【分析】根据图示,钛网上海水中Cl-、HO发生失电子的氧化反应生成HClO、O,钛网为阳极,电极反
2 2
应式为Cl-+H O-2e-=HClO+H+,钛箔上生成H,钛箔上生成H 的电极反应为2H++2e-=H ↑,钛箔为阴极,
2 2 2 2
高选择性催化剂PRT可抑制O 产生,电解的主要总反应为Cl-+2H O HClO+H↑+OH-,以此解题。
2 2 2
【详解】A.由分析可知,a为正极,b电极为负极,则a端电势高于b端电势,A错误;
B.右侧电极上产生氢气的电极方程式为:2H++2e-=H ↑,则理论上转移 生成 ,B错误;
2
C.由分析可知,电解的主要总反应为Cl-+2H O HClO+H↑+OH-,电解后海水中OH-浓度增大,pH上
2 2
升,C错误;
D.由图可知,阳极上的电极反应为: ,D正确;
故选D。
20.(2024·广东·高考真题)我国自主设计建造的浮式生产储御油装置“海葵一号”将在珠江口盆地海域
使用,其钢铁外壳镶嵌了锌块,以利用电化学原理延缓外壳的腐蚀。下列有关说法正确的是
A.钢铁外壳为负极 B.镶嵌的锌块可永久使用
C.该法为外加电流法 D.锌发生反应:
【答案】D
【分析】钢铁外壳镶嵌了锌块,由于金属活动性Zn>Fe,即锌块为负极,钢铁为正极,形成原电池,Zn
失去电子,发生还原反应, ,从而保护钢铁,延缓其腐蚀。【详解】A.由于金属活动性Zn>Fe,钢铁外壳为正极,锌块为负极,故A错误;
B.Zn失去电子,发生氧化反应, ,镶嵌的锌块会被逐渐消耗,需根据腐蚀情况进行维护
和更换,不能永久使用,故B错误;
C.由分析得,该方法为牺牲阳极的阴极保护法,故C错误;
D.Zn失去电子,发生氧化反应: ,故D正确;
故选D。
【策略1】掌握原电池的原理及应用
1.原电池正、负极的判断方法
【注意】
①活泼性强的金属不一定作负极,对于某些原电池,如镁、铝和 NaOH溶液组成的原电池,Al作负
极,Mg作正极。原电池的正极和负极与电极材料的性质有关,也与电解质溶液有关,不要形成思维定式
——活泼金属一定是负极,但负极一定发生氧化反应。
总反应 Cu+4H++2NO===Cu2++2NO ↑+2HO
2 2
Al——Cu (浓硝酸) 负极反应 Cu-2e-===Cu2+
正极反应 4H++2NO+2e-===2NO ↑+2HO
2 2
总反应 2Al+2HO+2OH-===2AlO-+3H↑
2 2 2
Al——Mg (NaOH溶液) 负极反应 2Al-6e-+8OH-===2AlO-+4HO
2 2
正极反应 6HO+6e-===3H↑+6OH-
2 2
②电子不能通过电解质溶液,溶液中的离子不能通过盐桥和导线(即电子不下水,离子不上岸)。
③自发发生的氧化还原反应并不一定是电极与电解质溶液反应,也可以是电极与溶解的 O 等发生反
2应,如将铁与石墨相连插入食盐水中。
2.原电池原理的应用
(1)设计制作化学电源
例:根据反应2FeCl +Cu===2FeCl +CuCl 设计原电池:
3 2 2
①不含盐桥 ②含盐桥
负极:Cu-2e-===Cu2+
正极:2Fe3++2e-===2Fe2+
(2)加快化学反应速率
一个自发进行的氧化还原反应,形成原电池时会使反应速率增大。如在 Zn与稀硫酸反应时加入少量
CuSO 溶液构成原电池,反应速率增大。
4
(3)比较金属的活动性强弱
原电池中,一般活动性强的金属作负极,而活动性弱的金属(或非金属导体)作正极。
(4)用于金属的防护
使需要保护的金属制品作原电池正极而受到保护。例如:要保护一个铁质的输水管道或钢铁桥梁,可用导
线将其与一块锌块相连,使锌作原电池的负极。
【策略2】熟悉常见的化学电源
1.一次电池——干电池
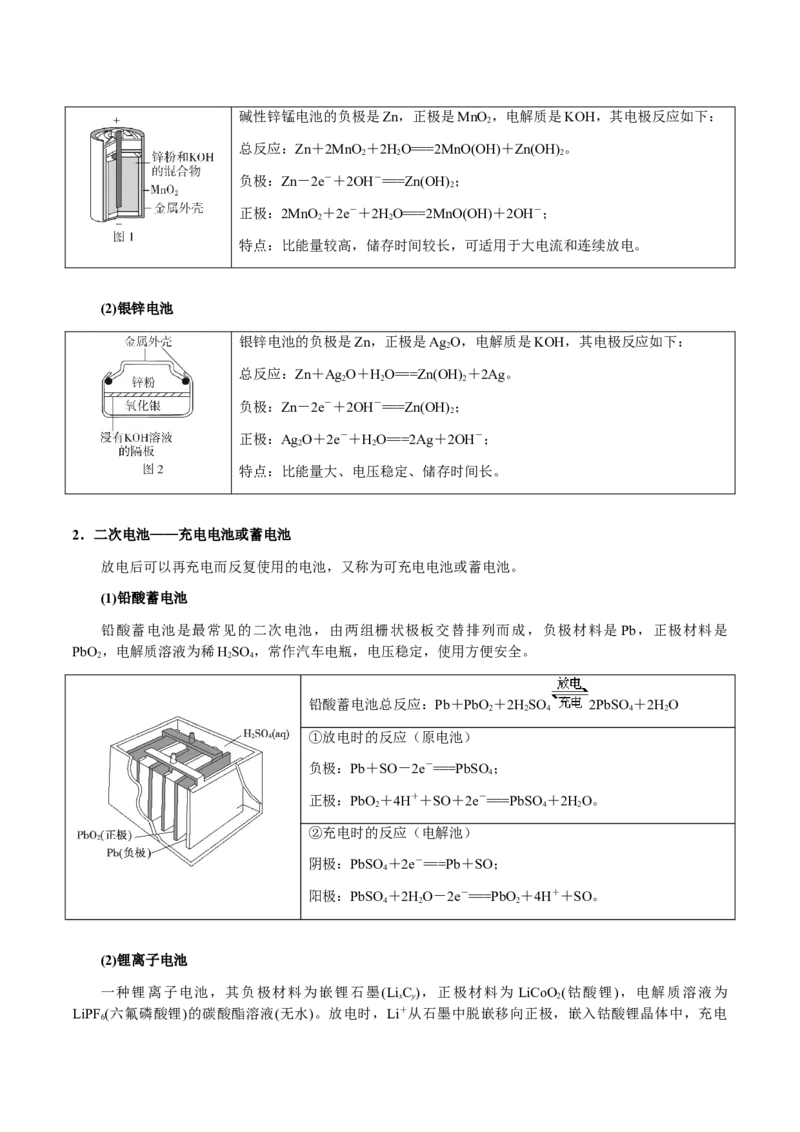
(1)碱性锌锰电池碱性锌锰电池的负极是Zn,正极是MnO ,电解质是KOH,其电极反应如下:
2
总反应:Zn+2MnO +2HO===2MnO(OH)+Zn(OH) 。
2 2 2
负极:Zn-2e-+2OH-===Zn(OH) ;
2
正极:2MnO +2e-+2HO===2MnO(OH)+2OH-;
2 2
特点:比能量较高,储存时间较长,可适用于大电流和连续放电。
(2)银锌电池
银锌电池的负极是Zn,正极是Ag O,电解质是KOH,其电极反应如下:
2
总反应:Zn+Ag O+HO===Zn(OH) +2Ag。
2 2 2
负极:Zn-2e-+2OH-===Zn(OH) ;
2
正极:Ag O+2e-+HO===2Ag+2OH-;
2 2
特点:比能量大、电压稳定、储存时间长。
2.二次电池——充电电池或蓄电池
放电后可以再充电而反复使用的电池,又称为可充电电池或蓄电池。
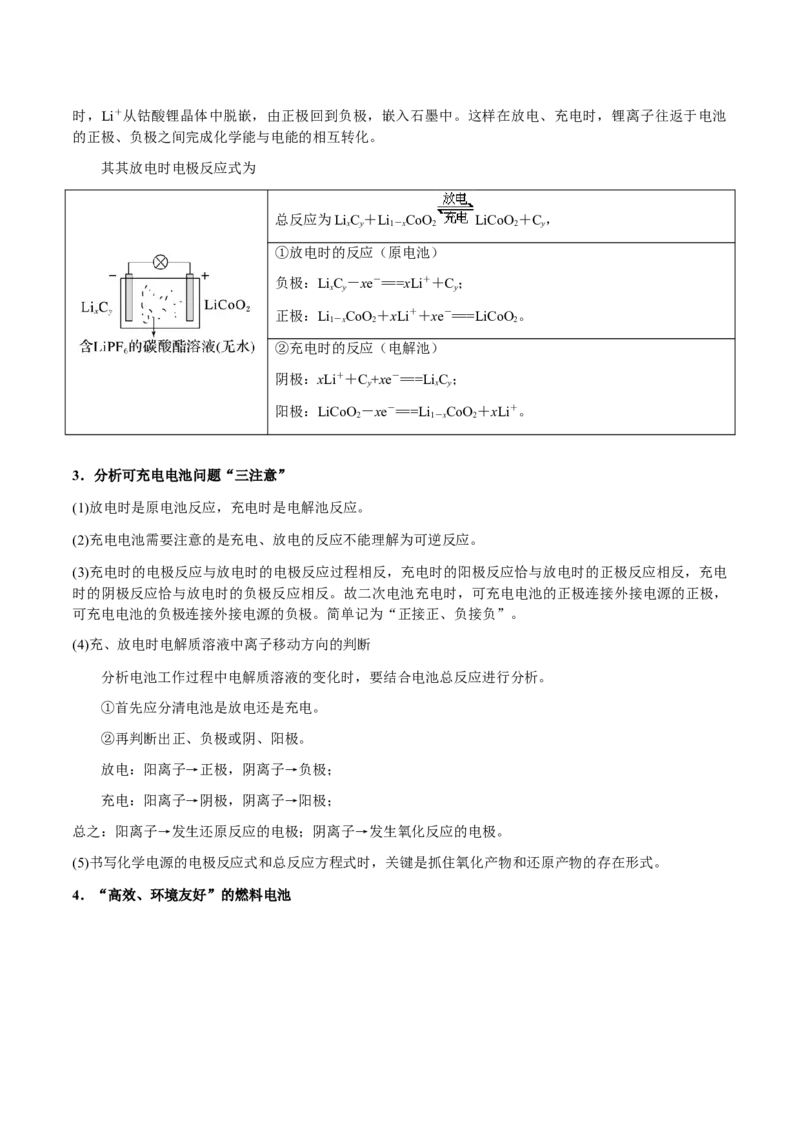
(1)铅酸蓄电池
铅酸蓄电池是最常见的二次电池,由两组栅状极板交替排列而成,负极材料是 Pb,正极材料是
PbO ,电解质溶液为稀HSO ,常作汽车电瓶,电压稳定,使用方便安全。
2 2 4
铅酸蓄电池总反应:Pb+PbO +2HSO 2PbSO +2HO
2 2 4 4 2
①放电时的反应(原电池)
负极:Pb+SO-2e-===PbSO;
4
正极:PbO +4H++SO+2e-===PbSO+2HO。
2 4 2
②充电时的反应(电解池)
阴极:PbSO +2e-===Pb+SO;
4
阳极:PbSO +2HO-2e-===PbO+4H++SO。
4 2 2
(2)锂离子电池
一种锂离子电池,其负极材料为嵌锂石墨(LiC),正极材料为 LiCoO (钴酸锂),电解质溶液为
x y 2
LiPF (六氟磷酸锂)的碳酸酯溶液(无水)。放电时,Li+从石墨中脱嵌移向正极,嵌入钴酸锂晶体中,充电
6时,Li+从钴酸锂晶体中脱嵌,由正极回到负极,嵌入石墨中。这样在放电、充电时,锂离子往返于电池
的正极、负极之间完成化学能与电能的相互转化。
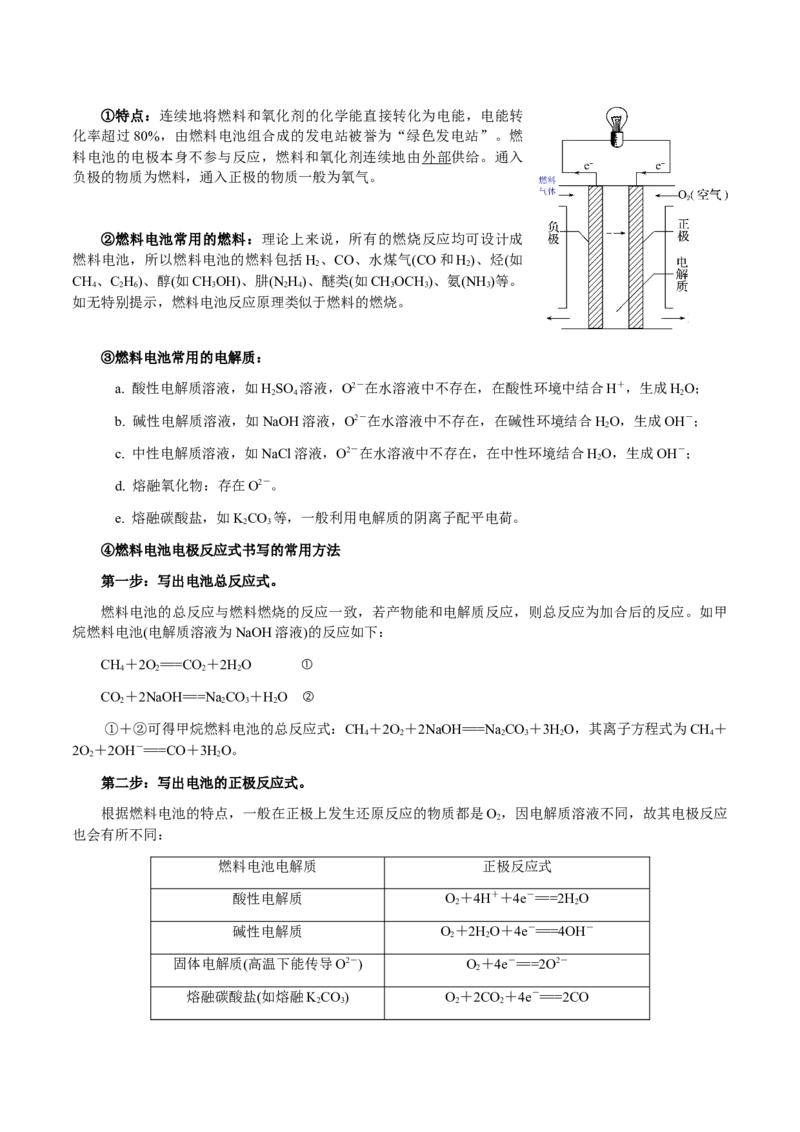
其其放电时电极反应式为
总反应为LiC+Li CoO LiCoO +C,
x y 1-x 2 2 y
①放电时的反应(原电池)
负极:LiC-xe-===xLi++C;
x y y
正极:Li CoO+xLi++xe-===LiCoO。
1-x 2 2
②充电时的反应(电解池)
阴极:xLi++C+xe-===LiC;
y x y
阳极:LiCoO -xe-===Li CoO+xLi+。
2 1-x 2
3.分析可充电电池问题“三注意”
(1)放电时是原电池反应,充电时是电解池反应。
(2)充电电池需要注意的是充电、放电的反应不能理解为可逆反应。
(3)充电时的电极反应与放电时的电极反应过程相反,充电时的阳极反应恰与放电时的正极反应相反,充电
时的阴极反应恰与放电时的负极反应相反。故二次电池充电时,可充电电池的正极连接外接电源的正极,
可充电电池的负极连接外接电源的负极。简单记为“正接正、负接负”。
(4)充、放电时电解质溶液中离子移动方向的判断
分析电池工作过程中电解质溶液的变化时,要结合电池总反应进行分析。
①首先应分清电池是放电还是充电。
②再判断出正、负极或阴、阳极。
放电:阳离子→正极,阴离子→负极;
充电:阳离子→阴极,阴离子→阳极;
总之:阳离子→发生还原反应的电极;阴离子→发生氧化反应的电极。
(5)书写化学电源的电极反应式和总反应方程式时,关键是抓住氧化产物和还原产物的存在形式。
4.“高效、环境友好”的燃料电池①特点:连续地将燃料和氧化剂的化学能直接转化为电能,电能转
化率超过80%,由燃料电池组合成的发电站被誉为“绿色发电站”。燃
料电池的电极本身不参与反应,燃料和氧化剂连续地由外部供给。通入
负极的物质为燃料,通入正极的物质一般为氧气。
②燃料电池常用的燃料:理论上来说,所有的燃烧反应均可设计成
燃料电池,所以燃料电池的燃料包括H 、CO、水煤气(CO和H)、烃(如
2 2
CH、C H)、醇(如CHOH)、肼(N H)、醚类(如CHOCH )、氨(NH )等。
4 2 6 3 2 4 3 3 3
如无特别提示,燃料电池反应原理类似于燃料的燃烧。
③燃料电池常用的电解质:
a. 酸性电解质溶液,如HSO 溶液,O2-在水溶液中不存在,在酸性环境中结合H+,生成HO;
2 4 2
b. 碱性电解质溶液,如NaOH溶液,O2-在水溶液中不存在,在碱性环境结合HO,生成OH-;
2
c. 中性电解质溶液,如NaCl溶液,O2-在水溶液中不存在,在中性环境结合HO,生成OH-;
2
d. 熔融氧化物:存在O2-。
e. 熔融碳酸盐,如KCO 等,一般利用电解质的阴离子配平电荷。
2 3
④燃料电池电极反应式书写的常用方法
第一步:写出电池总反应式。
燃料电池的总反应与燃料燃烧的反应一致,若产物能和电解质反应,则总反应为加合后的反应。如甲
烷燃料电池(电解质溶液为NaOH溶液)的反应如下:
CH+2O===CO +2HO ①
4 2 2 2
CO+2NaOH===Na CO+HO ②
2 2 3 2
①+②可得甲烷燃料电池的总反应式:CH+2O+2NaOH===Na CO+3HO,其离子方程式为CH+
4 2 2 3 2 4
2O+2OH-===CO+3HO。
2 2
第二步:写出电池的正极反应式。
根据燃料电池的特点,一般在正极上发生还原反应的物质都是O ,因电解质溶液不同,故其电极反应
2
也会有所不同:
燃料电池电解质 正极反应式
酸性电解质 O+4H++4e-===2H O
2 2
碱性电解质 O+2HO+4e-===4OH-
2 2
固体电解质(高温下能传导O2-) O+4e-===2O2-
2
熔融碳酸盐(如熔融KCO) O+2CO+4e-===2CO
2 3 2 2第三步:电池的总反应式-电池的正极反应式=电池的负极反应式,注意在将两个反应式相减时,要
约去正极的反应物O。
2
【策略3】掌握常考的新型化学电源
1.锂电池与锂离子电池
(1)锂电池
锂电池是一类由金属锂或锂合金为负极材料、使用非水电解质溶液的电池。工作时金属锂失去电子被
氧化为Li+,负极反应均为Li-e-===Li+,负极生成的Li+经过电解质定向移动到正极。
(2)锂离子二次电池
①锂离子电池基于电化学“嵌入/脱嵌”反应原理,替代了传统的“氧化—还原”原理;在两极形成的
电压降的驱动下,Li+可以从电极材料提供的“空间”中“嵌入”或“脱嵌”。
②锂离子电池充电时阴极反应式一般为C +xLi++xe-===LiC ;放电时负极反应是充电时阴极反应的
6 x 6
逆过程:LiC -xe-===C +xLi+。
x 6 6
③锂离子电池的正极材料一般为含 Li+的化合物,目前已商业化的正极材料有 LiFePO 、LiCoO 、
4 2
LiMn O 等。
2 4
总反应
Li CoO+LiC LiCoO +C (x<1)
1-x 2 x 6 2 6
钴酸锂电池
负极反应 LiC -xe-===xLi++C
x 6 6
正极反应 Li CoO+xe-+xLi+===LiCoO
1-x 2 2
总反应
FePO +Li LiFePO
4 4
磷酸铁锂电
池 负极反应 Li-e-===Li+
正极反应 FePO +Li++e-===LiFePO
4 4
总反应
LixC6+Li3-xNiCoMnO6 C6+Li3NiCoMnO6
锰酸锂电池
负极反应 LiC -xe-===xLi++C
x 6 6
正极反应 Li3-xNiCoMnO6 +xe-+xLi+===Li3NiCoMnO6
总反应 xLi+LiV O===Li VO
3 8 1+x 3 8
锂钒氧化物
负极反应 xLi-xe-=== xLi+
电池
正极反应 xLi++LiV O+xe-===Li VO
3 8 1+x 3 8
2.微生物燃料电池
微生物燃料电池是一种利用微生物将有机物中的化学能直接转化成电能的装置。其基本工作原理是在
负极室厌氧环境下,有机物在微生物作用下分解并释放出电子和质子,电子依靠合适的电子传递介体在生物组分和负极之间进行有效传递,并通过外电路传递到正极形成电流,而质子通过质子交换膜传递到正
极,氧化剂(如氧气)在正极得到电子被还原。
3.物质循环转化型电池
根据物质转化中,元素化合价的变化或离子的移动(阳离子移向正极区域,阴离子移向负极区域)判断
电池的正、负极,是分析该电池的关键。
4.浓差电池
(1)在浓差电池中,为了限定某些离子的移动,常涉及到“离子交换膜”。
①常见的离子交换膜
阳离子交换膜 只允许阳离子(包括H+)通过
阴离子交换膜 只允许阴离子通过
质子交换膜 只允许H+通过
②离子交换膜的作用
a. 能将两极区隔离,阻止两极物质发生化学反应。
b. 能选择性地允许离子通过,起到平衡电荷、形成闭合回路的作用。
③离子交换膜的选择依据:离子的定向移动。
(2)“浓差电池”的分析方法
浓差电池是利用物质的浓度差产生电势的一种装置。两侧半电池中的特定物质有浓度差,离子均是由“高
浓度”移向“低浓度”,依据阴离子移向负极区域,阳离子移向正极区域判断电池的正、负极,这是解题
的关键。
【策略4】熟练掌握电解池的原理及应用
1.电解过程的三个流向
①电子流向:电源负极→电解池阴极;电解池的阳极→电源的正极;
②离子流向:阳离子→电解池的阴极,阴离子→电解池的阳极。
③电流方向:电源正极→电解池阳极→电解质溶液→阴极→负极。
2.阴、阳两极上的放电顺序
在阳极上阴离子失去电子发生氧化反应,在阴极上阳离子得到电子发生还原反应的过程叫放电。离子
的放电顺序取决于离子本身的性质即离子得失电子的能力,另外也与离子的浓度及电极材料有关。
(1)阴极:阴极上放电的总是溶液中的阳离子,与电极材料无关。
阳 离 子 放 电 顺 序 为 Ag+>Hg2+>Fe3+>Cu2+>H+( 指 酸 电 离 的 )>Pb2+>Sn2+>Fe2+>Zn2+>H+( 指 水 电 离
的)>Al3+>Mg2+>Na+>Ca2+>K+。(在溶液中Al3+、Mg2+、Na+、Ca2+、K+等是不会在阴极上放电的,但在熔
融状态下的物质中会放电)(2)阳极:
①若是活性电极(银以前包括银在内的金属)作阳极,则活性电极首先失电子,发生氧化反应,电极被
溶解变成离子而进入溶液,溶液中的阴离子不能失电子;
②若是惰性电极(如:Pt、石墨、Au等)作阳极,则仅是溶液中的阴离子放电,常见阴离子的放电顺序
为:金属(Au、Pt除外)电极>S2->SO2->I->Br->Cl->OH->含氧酸根离子。
3
(3)阴、阳极放电后的产物
S2 I Br Cl
反应物 阴极金属阳离子(H+) 阳极活性金属电极 OH-
- - - -
产物 金属(H ) 金属离子 S I Br Cl O、HO
2 2 2 2 2 2
3.电解后电解质溶液的复原
电解后电解质溶液复原遵循“少什么补什么”原则,先让析出的产物(气体或沉淀)恰好完全反应,再
将其化合物投入电解后的溶液中即可。如:
①NaCl溶液:通HCl气体(不能加盐酸);
②AgNO 溶液:加Ag O固体;
3 2
③CuCl 溶液:加CuCl 固体;
2 2
④KNO 溶液:加HO;
3 2
⑤CuSO 溶液:加CuO或CuCO[不能加Cu O、Cu(OH) 、Cu (OH) CO]。
4 3 2 2 2 2 3
4.电镀:电镀是利用电解原理在某些金属表面镀上一薄层其他金属或合金的过程。
电镀是一种特殊的电解,要求镀件必须作阴极,镀层金属作阳极,含镀层金属离子的可溶性盐溶液作
电解质溶液(作为电镀液)。在直流电的作用下,阳极金属溶解在溶液中成为阳离子,移向阴极,在阴极
获得电子被还原成金属,在镀件表面覆盖上一层均匀光洁而致密的镀层。
特征:①阳极本身放电被氧化,不断溶解;
②宏观上看无新物质生成;
③电解液的总量、浓度、pH均不变。
④阳极减少的质量和阴极增加的质量相等。
电镀
示意图
电极反应 阳极 Cu-2e-===Cu2+阴极 Cu2++2e-===Cu
电解质溶液的浓度变化 CuSO 溶液的浓度不变
4
5.电解精炼粗铜:
① 阳极材料是粗铜,阴极材料是精铜,电解质溶液是 CuSO 溶液 ( 或 Cu(NO ) 溶液 ) 。
4 3 2
②粗铜中往往含有锌、铁、镍、银、金等多种杂质,当含杂质的铜在阳极不断溶解时,位于金属活动
性顺序铜以前的金属杂质如Zn、Fe、Ni等,也会同时放电:
Zn-2e-= Zn2+、Fe-2e-= Fe2+、Ni-2e-= Ni2+、Cu-2e-= Cu2+,
位于金属活动性顺序铜之后的金、银等金属杂质,因为失去电子能力比Cu弱,难以在阳极失去电子
变成阳离子溶解下来,而以 阳极泥的形式沉积下来, 阳极泥可作为提炼金、银等贵重金属的原料 ,这样可
得符合电气工业要求的纯度达99.95%~99.98%的铜。
在阴极,由于溶液中的Zn2+、Fe2+、Ni2+、H+等离子得到电子的能力均比Cu2+弱,且物质的量浓度均比
Cu2+小,所以只有Cu2+在阴极获得电子而析出Cu,这样,在阴极就得到了纯铜。
③长时间电解后,CuSO 溶液的浓度变小 , 电解质溶液必须补充。
4
④阳极减少的质量和阴极增加的质量不相等;
电解精炼铜
示意图
Zn-2e-= Zn2+、Fe-2e-= Fe2+、
阳极
电极反应 Ni-2e-= Ni2+、Cu-2e-= Cu2+。
阴极 Cu2++2e-===Cu
电解质溶液的浓度变化 CuSO 溶液的浓度变小
4
【微点拨】电解精炼中,比需要精炼的金属活泼的杂质溶解,而不比需要精炼的金属活泼的杂质会沉积
(如:精炼镍时Cu也会沉积)。
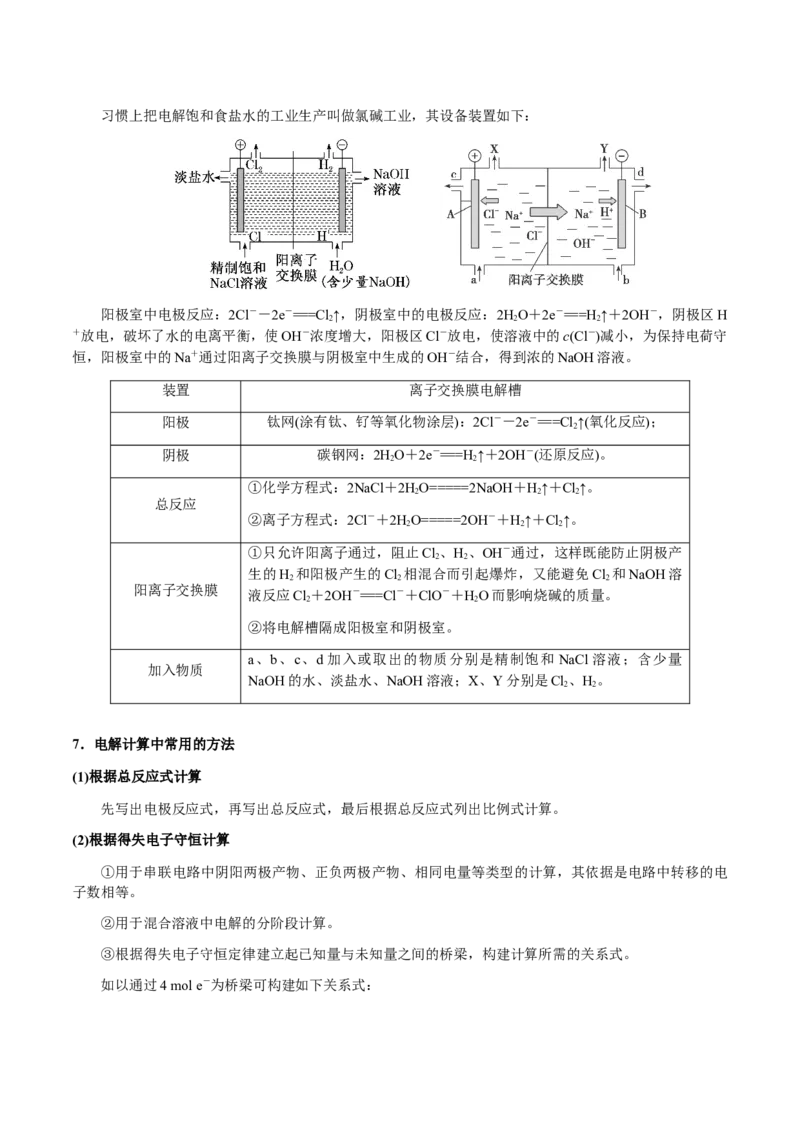
6.氯碱工业——电解饱和食盐水制烧碱、氯气和氢气习惯上把电解饱和食盐水的工业生产叫做氯碱工业,其设备装置如下:
阳极室中电极反应:2Cl--2e-===Cl↑,阴极室中的电极反应:2HO+2e-===H ↑+2OH-,阴极区H
2 2 2
+放电,破坏了水的电离平衡,使OH-浓度增大,阳极区Cl-放电,使溶液中的c(Cl-)减小,为保持电荷守
恒,阳极室中的Na+通过阳离子交换膜与阴极室中生成的OH-结合,得到浓的NaOH溶液。
装置 离子交换膜电解槽
阳极 钛网(涂有钛、钌等氧化物涂层):2Cl--2e-===Cl↑(氧化反应);
2
阴极 碳钢网:2HO+2e-===H ↑+2OH-(还原反应)。
2 2
①化学方程式:2NaCl+2HO=====2NaOH+H↑+Cl↑。
2 2 2
总反应
②离子方程式:2Cl-+2HO=====2OH-+H↑+Cl↑。
2 2 2
①只允许阳离子通过,阻止Cl 、H 、OH-通过,这样既能防止阴极产
2 2
生的H 和阳极产生的Cl 相混合而引起爆炸,又能避免Cl 和NaOH溶
2 2 2
阳离子交换膜
液反应Cl+2OH-===Cl-+ClO-+HO而影响烧碱的质量。
2 2
②将电解槽隔成阳极室和阴极室。
a、b、c、d加入或取出的物质分别是精制饱和 NaCl溶液;含少量
加入物质
NaOH的水、淡盐水、NaOH溶液;X、Y分别是Cl、H。
2 2
7.电解计算中常用的方法
(1)根据总反应式计算
先写出电极反应式,再写出总反应式,最后根据总反应式列出比例式计算。
(2)根据得失电子守恒计算
①用于串联电路中阴阳两极产物、正负两极产物、相同电量等类型的计算,其依据是电路中转移的电
子数相等。
②用于混合溶液中电解的分阶段计算。
③根据得失电子守恒定律建立起已知量与未知量之间的桥梁,构建计算所需的关系式。
如以通过4 mol e-为桥梁可构建如下关系式:该关系式具有总揽电化学计算的作用和价值,熟记电极反应式,灵活运用关系式便能快速解答常见的
电化学计算问题。
【策略5】牢记金属的腐蚀与防护方法
1.化学腐蚀与电化学腐蚀的比较
类型 化学腐蚀 电化学腐蚀
金属与其表面接触的一些物质(如O、 不纯金属与电解质溶液接触发生原
2
条件
Cl、SO 等)直接反应而引起的腐蚀 电池反应
2 2
现象 电流产生 有微弱电流产生
本质 金属被氧化 较活泼金属被氧化
联系 两者往往同时发生,电化学腐蚀更普遍
2.析氢腐蚀与吸氧腐蚀的比较
以钢铁的腐蚀为例进行分析:
类型 析氢腐蚀(腐蚀过程中不断有氢气放出) 吸氧腐蚀(反应过程吸收氧气)
水膜酸性较强(pH≤4.3),如:NH Cl溶 水膜酸性很弱或呈中性,且溶有一定
4
条件
液、稀HSO 等 量氧气
2 4
负极 Fe-2e-===Fe2+
电极
反应
正极 2H++2e-===H ↑ O+2HO+4e-===4OH-
2 2 2
总反应式 Fe+2H+===Fe2++H↑ 2Fe+O+2HO===2Fe(OH)
2 2 2 2
①钢铁暴露在潮湿空气中主要发生的是吸氧腐蚀,铁锈的形成过程中主要发生的
反应为:
4Fe(OH) +O+2HO===4Fe(OH) ,
2 2 2 3
2Fe(OH) ===Fe O·xHO(铁锈)+(3-x)H O。
3 2 3 2 2
易错提醒
②纯度越高的金属,腐蚀得越慢。
③不纯的金属或合金,在潮湿空气中的腐蚀速率远大于在干燥、隔绝空气条件下
的腐蚀速率。
④两种腐蚀正极的现象不同:析氢腐蚀正极产生H,气体压强变大,pH增大;
2
吸氧腐蚀正极吸收O,气体压强变小,pH增大。
2联系 吸氧腐蚀更普遍
3.金属的防护
(1)电化学保护法
①牺牲阳极法——原电池原理
a.负极:比被保护金属活泼的金属;
b.正极:被保护的金属设备。
②外加电流法——电解原理
a.阴极:被保护的金属设备;
b.阳极:惰性金属。
【策略6】能进行隔膜多室电池装置的分析
1.电化学中的离子交换膜
(1)离子交换膜的种类及作用
阳离子交换膜 只允许阳离子透过,不允许阴离子或某些分子透过
阴离子交换膜 只允许阴离子透过,不允许阳离子或某些分子透过
质子交换膜 只允许H+透过,不允许其他阳离子和阴离子透过
由一张阳膜和一张阴膜复合制成。该膜特点是在直流电的作用下,阴、阳
双极膜 膜复合层间的HO解离成H+和OH-并通过阳膜和阴膜分别向两极区移
2
动,作为H+和OH-的离子源
(2)离子交换膜的功能:选择性透过离子,平衡电荷,形成闭合回路。
(3)离子交换膜的应用
①隔离某些物质,防止发生反应。
②用于物质的制备(电解后溶液阴极区或阳极区得到所制备的物质)。
③物质分离、提纯。
2.含膜电解池装置分析
(1)两室电解池:
例如,工业上利用如图两室电解装置制备烧碱:阳极室中电极反应:2Cl--2e-===Cl↑,
2
阴极室中的电极反应:2HO+2e-===H ↑+2OH-,
2 2
阴极区H+放电,破坏了水的电离平衡,使OH-浓度增大,阳极区Cl-放电,使溶液中的c(Cl-)减
小,为保持电荷守恒,阳极室中的Na+通过阳离子交换膜与阴极室中生成的OH-结合,得到浓的NaOH溶
液。利用这种方法制备物质,纯度较高,基本没有杂质。
阳离子交换膜的作用:只允许Na+通过,而阻止阴离子(Cl-)和气体(Cl )通过。这样既防止了两极产生
2
的H 和Cl 混合爆炸,又避免了Cl 和阴极产生的NaOH反应生成NaClO而影响烧碱的质量。
2 2 2
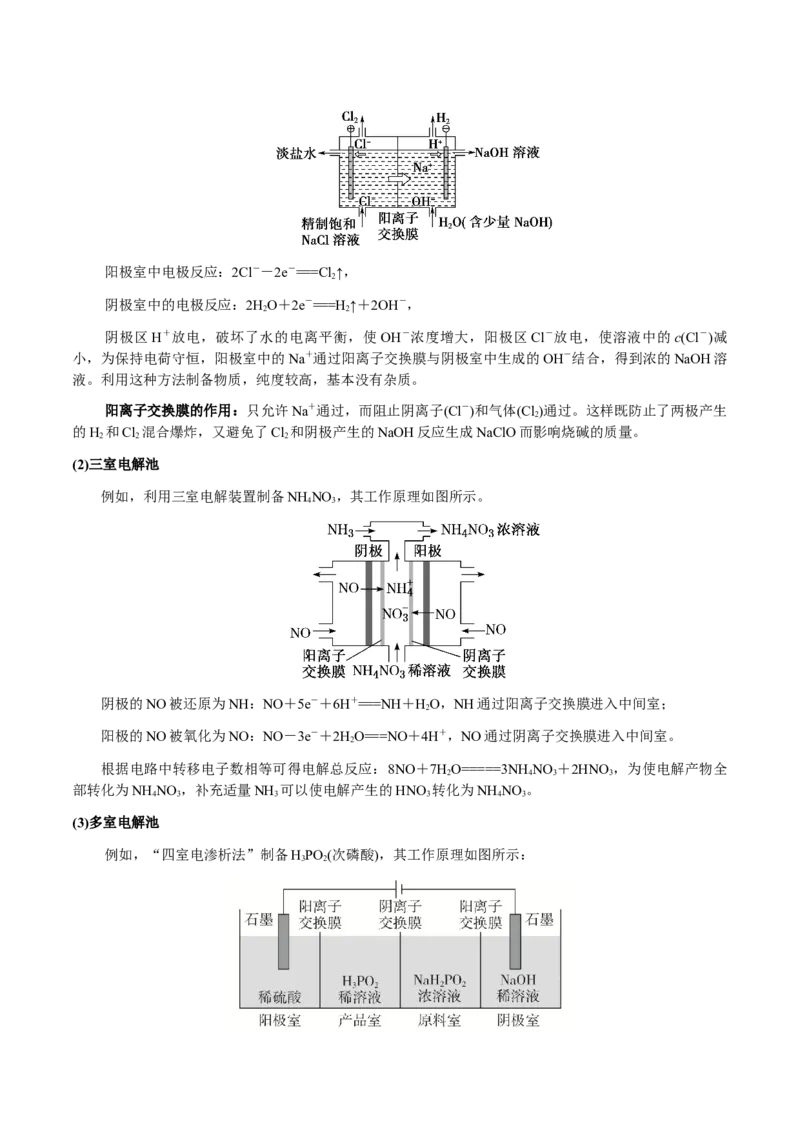
(2)三室电解池
例如,利用三室电解装置制备NH NO ,其工作原理如图所示。
4 3
阴极的NO被还原为NH:NO+5e-+6H+===NH+HO,NH通过阳离子交换膜进入中间室;
2
阳极的NO被氧化为NO:NO-3e-+2HO===NO+4H+,NO通过阴离子交换膜进入中间室。
2
根据电路中转移电子数相等可得电解总反应:8NO+7HO=====3NH NO +2HNO ,为使电解产物全
2 4 3 3
部转化为NH NO ,补充适量NH 可以使电解产生的HNO 转化为NH NO 。
4 3 3 3 4 3
(3)多室电解池
例如,“四室电渗析法”制备HPO (次磷酸),其工作原理如图所示:
3 2电解稀硫酸的阳极反应:2HO-4e-===O ↑+4H+,产生的H+通过阳离子交换膜进入产品室,原料室
2 2
中的HPO穿过阴离子交换膜进入产品室,与H+结合生成弱电解质HPO ;
2 3 2
电解NaOH稀溶液的阴极反应:4HO+4e-===2H ↑+4OH-,原料室中的Na+通过阳离子交换膜进入
2 2
阴极室,可得副产品NaOH。
(4)电渗析法
将含AB 的废水再生为HB和A(OH) 的原
n m n m
理:已知A为金属活动顺序表H之前的金
属,Bn-为含氧酸根离子。
1.(2024·广东湛江·一模)镁合金中添加稀土元素会形成一种长周期堆垛有序( )结构,这种特殊结
构可以显著提高镁合金的耐腐蚀性能。下列说法正确的是
A.该防腐蚀保护法为外加电流法
B.镁合金被腐蚀时, 发生氧化反应
C.负极反应可能为:
D.添加 、 等金属一定也能提升镁合金的耐腐蚀性
【答案】B
【详解】A.该方法通过改变金属材料的组成来达到金属防护的目的,不属于外加电流法,A错误;
B.镁合金被腐蚀时, 作负极,发生氧化反应,B正确;
C.负极发生失电子的氧化反应,C错误;
D. 、 不如镁活泼,添加 、 等金属后会加速镁合金的腐蚀,D错误;故选B。
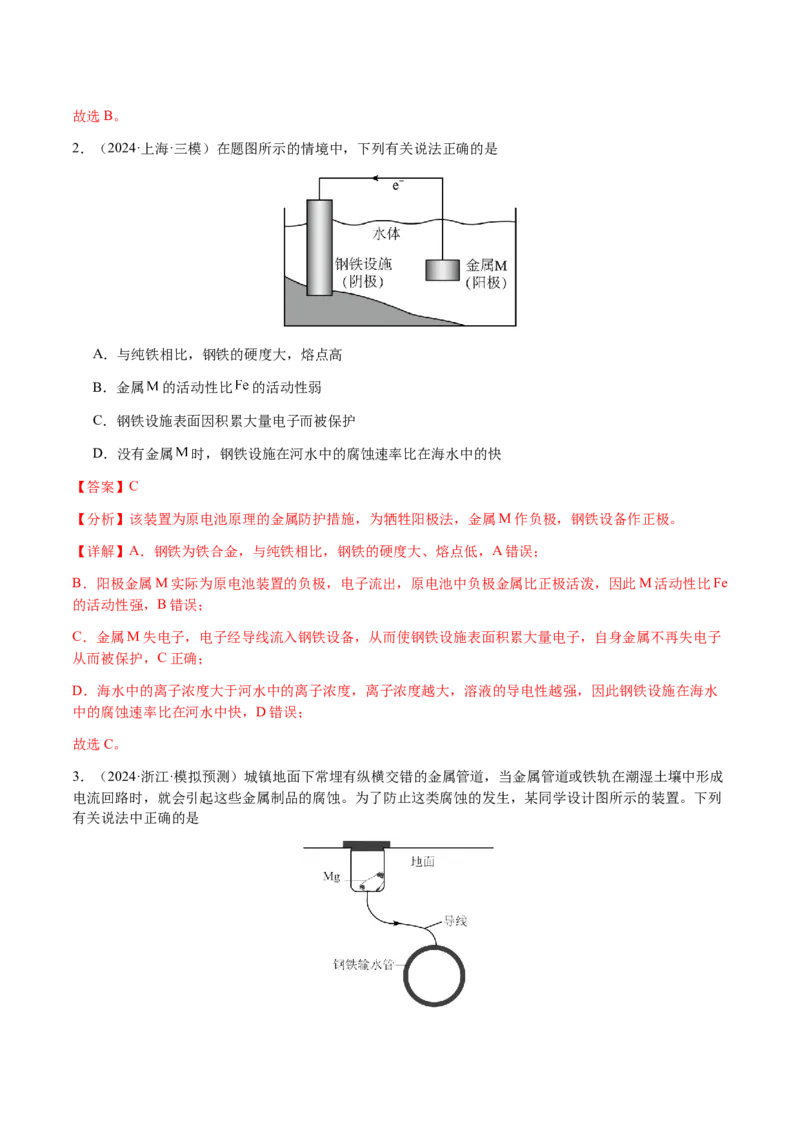
2.(2024·上海·三模)在题图所示的情境中,下列有关说法正确的是
A.与纯铁相比,钢铁的硬度大,熔点高
B.金属 的活动性比 的活动性弱
C.钢铁设施表面因积累大量电子而被保护
D.没有金属 时,钢铁设施在河水中的腐蚀速率比在海水中的快
【答案】C
【分析】该装置为原电池原理的金属防护措施,为牺牲阳极法,金属M作负极,钢铁设备作正极。
【详解】A.钢铁为铁合金,与纯铁相比,钢铁的硬度大、熔点低,A错误;
B.阳极金属M实际为原电池装置的负极,电子流出,原电池中负极金属比正极活泼,因此M活动性比Fe
的活动性强,B错误;
C.金属M失电子,电子经导线流入钢铁设备,从而使钢铁设施表面积累大量电子,自身金属不再失电子
从而被保护,C正确;
D.海水中的离子浓度大于河水中的离子浓度,离子浓度越大,溶液的导电性越强,因此钢铁设施在海水
中的腐蚀速率比在河水中快,D错误;
故选C。
3.(2024·浙江·模拟预测)城镇地面下常埋有纵横交错的金属管道,当金属管道或铁轨在潮湿土壤中形成
电流回路时,就会引起这些金属制品的腐蚀。为了防止这类腐蚀的发生,某同学设计图所示的装置。下列
有关说法中正确的是A.电流由 经过导线流向钢铁制品
B. 块表面随着时间的进行,会有 产生
C.钢铁管道与电源正极相连的保护法是外加电流保护法
D.应选用电阻率小的导体,比如 来避免能量损耗
【答案】B
【分析】钢铁输水管与镁块相连形成原电池,镁作负极,发生氧化反应被腐蚀,钢铁输水管作正极,受到
保护。
【详解】A.钢铁输水管与镁块相连形成原电池,镁作负极,发生氧化反应被腐蚀,钢铁输水管作正极,
电流由钢铁制品经过导线流向 ,A错误;
B.由分可知,镁作负极,Mg失去电子生成Mg2+,Mg2+在潮湿的环境中会水解转化为 ,B正
确;
C.Mg为活泼金属,可作为牺牲阳极,则将Mg与钢铁输水管相连是用牺牲阳极法保护钢铁输水管,C错
误;
D.Fe比Ag活泼,若选用 作为导体,Ag与钢铁制品形成原电池,钢铁制品作负极会被腐蚀,D错
误;
故选B。
4.(2024·湖北·一模)港珠澳大桥的设计使用寿命高达120年,主要的防腐方法有:①钢梁上安装铝片;
②使用高性能富锌(富含锌粉)底漆;③使用高附着性防腐涂料;④预留钢铁腐蚀量。下列分析不合理的是
A.若将钢梁与直流负极相连,也可减慢腐蚀速率
B.防腐过程中铝和锌均作为负极,失去电子
C.方法①②③只能减缓钢铁腐蚀,未能完全消除
D.钢梁在水下部分比在空气与水交界处更容易腐蚀
【答案】D
【分析】钢是铁碳合金,潮湿的环境中易形成原电池发生吸氧腐蚀被损耗。
【详解】A.将钢梁与直流负极相连,铁做电解池的阴极被保护,可减慢铁的腐蚀速率,该保护方法为外
加电流法,故A正确;
B.铝和锌的金属活动性均大于铁,防腐过程中铝和锌均作为负极,失去电子发生氧化反应被损耗,铁作
正极被保护,该保护方法为牺牲阳极法,故B正确;
C.钢梁上安装铝片、使用高性能富锌(富含锌粉)底漆、使用高附着性防腐涂料可以减缓钢铁腐蚀,但不能
完全消除铁的腐蚀,故C正确;
D.空气与水交界处的氧气浓度大于水下部分,氧气浓度越大,铁越容易发生吸氧腐蚀,所以钢梁在水下部分比在空气与水交界处更难腐蚀,故D错误;
故选D。
5.(2024·河南·模拟预测)利用如图电化学装置可将 转化为 ,同时获得 。下列说法错误的
是
A.催化电极Ⅱ与电源的正极相连
B.工作时,质子通过交换膜由催化电极Ⅱ室移向催化电极Ⅰ室
C.催化电极Ⅰ的电极反应式:
D.理论上每消耗 ,生成
【答案】D
【分析】由图示可知,催化电极Ⅰ通入CO,生成CO,化合价降低,得到电子,为阴极,电极反应式为
2
CO+2e−+2H+=CO+H O,催化电极Ⅱ为阳极,电极反应式为Cl--2e-+H O=ClO-+2H+,以此解题。
2 2 2
【详解】A.催化电极Ⅱ为阳极,与电源正极相连,故A正确;
B.电解池中,质子移向阴极,质子通过交换膜由催化电极Ⅱ室移向催化电极Ⅰ室,故B正确;
C.催化电极Ⅰ通入CO,生成CO,化合价降低,得到电子,为阴极,电极反应为CO+2e−
2 2
+2H+=CO+H O,C正确;
2
D.根据电子得失守恒,消耗1molCO ,转移2mol电子,生成1molNaClO,故D错误;
2
故答案选D。
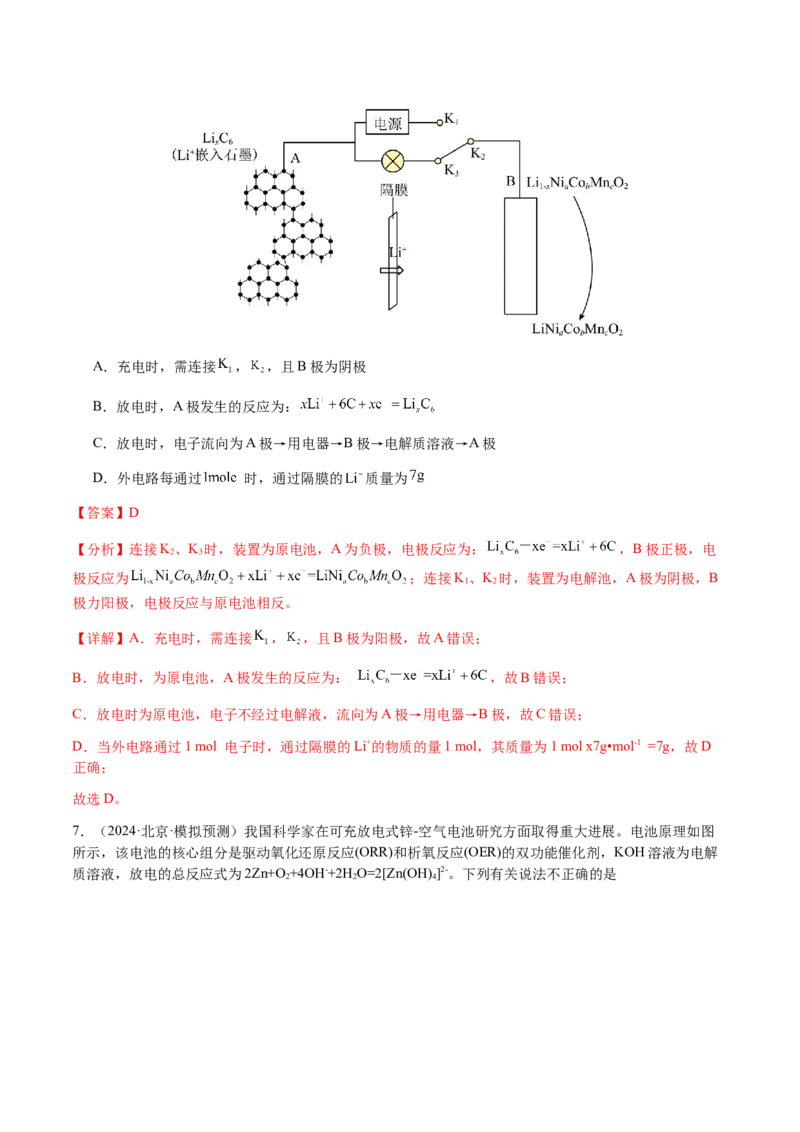
6.(2024·浙江·模拟预测)目前新能源汽车多采用三元锂电池,某三元锂电池的工作原理如图所示,下列
说法正确的是A.充电时,需连接 , ,且B极为阴极
B.放电时,A极发生的反应为:
C.放电时,电子流向为A极→用电器→B极→电解质溶液→A极
D.外电路每通过 时,通过隔膜的 质量为
【答案】D
【分析】连接K、K 时,装置为原电池,A为负极,电极反应为: ,B极正极,电
2 3
极反应为 ;连接K、K 时,装置为电解池,A极为阴极,B
1 2
极力阳极,电极反应与原电池相反。
【详解】A.充电时,需连接 , ,且B极为阳极,故A错误;
B.放电时,为原电池,A极发生的反应为: ,故B错误;
C.放电时为原电池,电子不经过电解液,流向为A极→用电器→B极,故C错误;
D.当外电路通过1 mol 电子时,通过隔膜的Li+的物质的量1 mol,其质量为1 mol x7g•mol-1 =7g,故D
正确;
故选D。
7.(2024·北京·模拟预测)我国科学家在可充放电式锌-空气电池研究方面取得重大进展。电池原理如图
所示,该电池的核心组分是驱动氧化还原反应(ORR)和析氧反应(OER)的双功能催化剂,KOH溶液为电解
质溶液,放电的总反应式为2Zn+O +4OH-+2H O=2[Zn(OH) ]2-。下列有关说法不正确的是
2 2 4A.放电时电解质溶液中K+向正极移动
B.放电时锌电池负极反应为Zn-2e-+4OH-=[Zn(OH) ]2-
4
C.充电时催化剂降低析氧反应(OER)的活化能
D.充电时阴极生成6.5gZn的同时阳极产生2.24LO (标准状况)
2
【答案】D
【分析】根据2Zn+O +4OH-+2H O=2[Zn(OH) ]2-可知,O元素的化合价降低,被还原,应为原电池正极,
2 2 4
Zn元素化合价升高,被氧化,应为原电池负极,负极反应式为Zn-2e-+4OH-=[Zn(OH) ]2-,放电时阳离
4
子向正极移动,据此分析解答。
【详解】A.放电时电解质溶液中带正电荷的K+向正极移动,故A正确;
B.由总反应式知,放电时负极是活泼金属锌失去电子被氧化为Zn2+,Zn2+与OH-反应结合为[Zn(OH) ]2
4
-:Zn-2e-+4OH-=[Zn(OH) ]2-,故B正确;
4
C.由总反应式和原理图知,放电时发生“氧化还原反应(ORR)”,充电时发生“析氧反应(OER)”,“双功
能催化剂”意味着无论放电还是充电均能降低反应活化能,起到催化作用,故C正确;
D.充电时阴极生成6.5 g Zn转移0.2 mol e-,而阳极产生2.24 L O (标准状况),转移0.4 mol e-,故D错
2
误;
答案选D。
8.(2024·湖南永州·模拟预测)利用电解原理,采用中性红试剂直接捕获空气中的二氧化碳的装置图如
下:已知:中性红NR: , :
下列说法不正确的是
A.若用铅蓄电池进行电解,a极接铅蓄电池的Pb极
B.电解时,b极的电极反应式为:
C.装置中离子交换膜为阳离子交换膜
D.左储液罐发生反应的离子方程式为:
【答案】A
【分析】根据题目所给图示分析,b电极上: ,得氢发生还原反应,则b电极作阴极,a电极
作阳极,b电极的电极反应式为: ,则a电极的电极反应式为:
,据此解答。
【详解】A.根据分析,若用铅蓄电池进行电解, 极是负极, 极是正极,故a电极应连接正极,
即 极,A错误;
B.根据分析,b电极上发生还原反应,其电极反应式为: ,B正确;
C.由b电极的电极反应式可知,氢氧根浓度增大,要保持溶液中电荷守恒,故需要将a电极产生的氢离子
转移到b极区,则装置中离子交换膜为阳离子交换膜,C正确;
D.由a电极的电极反应式可知,反应物需要碳酸氢根,左储液罐需要产生碳酸氢根供给,则左储液罐发
生反应的离子方程式为: ,D正确;
故选A。
9.(2024·江西·一模)水系电池具有成本低廉、安全性高等优点,某水系碱性镍-锌二次电池的工作原理
如图所示。
下列叙述错误的是
A.放电时,a极为负极B.放电时,b极反应式为
C.充电时,b极与电源正极连接
D.充电时,a极生成 时转移 电子
【答案】D
【分析】根据题干中水系碱性镍-锌二次电池的工作原理图可得,放电时a极为负极,发生氧化反应:
,b极为正极,发生还原反应: ;充电时a极为阴
极,发生还原反应: ,b极为阳极,发生氧化反应:
。
【详解】A.根据分析,放电时a极为负极,发生氧化反应: ,A正确;
B.根据分析,放电时b极为正极,发生还原反应: ,B正确;
C.根据分析,充电时,b极为阳极,与电源正极连接,C正确;
D.根据分析,充电时,a极反应式为 ,
,D错误;
故选D。
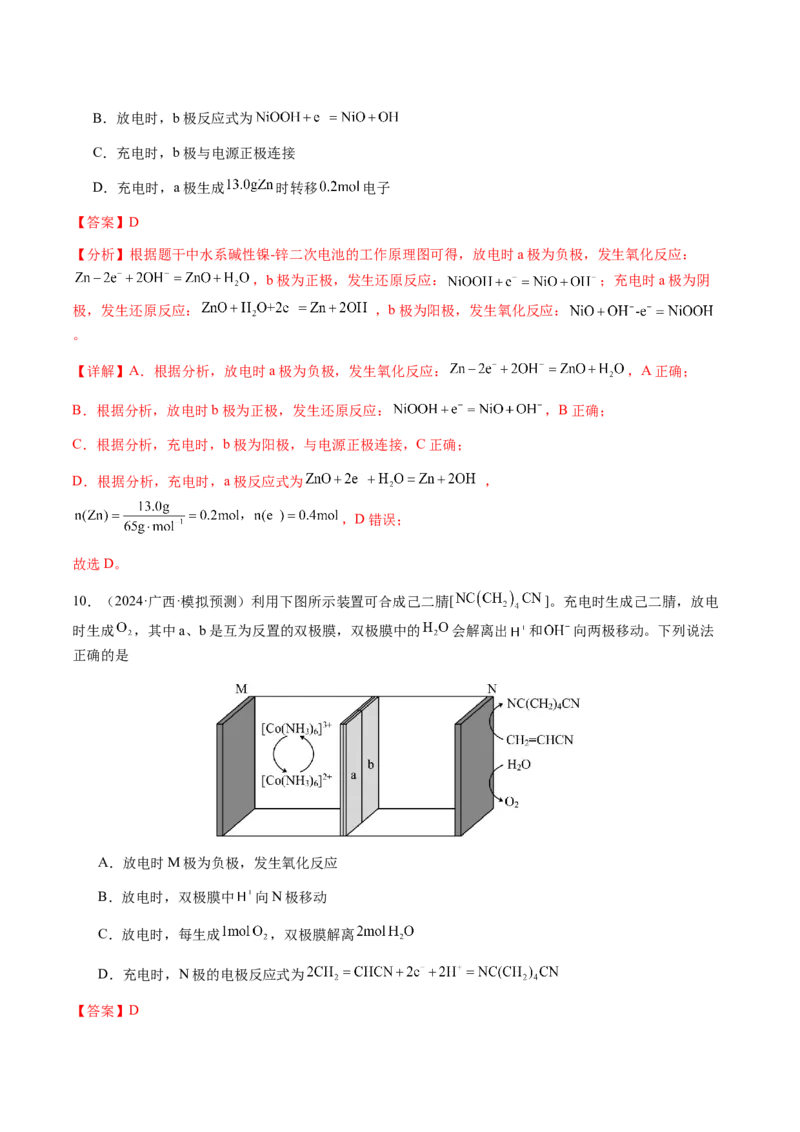
10.(2024·广西·模拟预测)利用下图所示装置可合成己二腈[ ]。充电时生成己二腈,放电
时生成 ,其中a、b是互为反置的双极膜,双极膜中的 会解离出 和 向两极移动。下列说法
正确的是
A.放电时M极为负极,发生氧化反应
B.放电时,双极膜中 向N极移动
C.放电时,每生成 ,双极膜解离
D.充电时,N极的电极反应式为
【答案】D【分析】放电时为原电池,N极上HO失电子生成O,则M极为正极,N极为负极,正极反应式为
2 2
[Co(NH )]3++e−=[Co(NH)]2+,负极反应式为2HO−4e−=O ↑+4H+,放电时,双极膜中OH−向负极移动,
3 6 3 6 2 2
H+向正极移动;充电时为电解池,M极为阳极,N极为阴极,阳极反应式为[Co(NH )]2+−e−=[Co(NH)]3+,
3 6 3 6
阴极反应式为2CH=CHCN+2e−+2H+=NC(CH)CN。
2 2 4
【详解】A.放电时为原电池,N极上HO失电子生成O,则M极为正极,电极反应式为[Co(NH )]3++e-
2 2 3 4
=[Co(NH)]2+,发生还原反应,故A错误;
3 4
B.放电时为原电池,M极为正极,N极为负极,双极膜中OH−向负极移动,H+向正极移动,即OH−向N
极移动,H+向M极移动,故B错误;
C.放电时,N电极为负极,水在负极失去电子发生氧化反应生成氧气和氢离子,电极反应式为
解离2mol水,因为a、b是互为反置的双极膜,所以共解离4mol水,故C错误;
D.充电时,N极是阴极,反应式为2CH=CHCN+2e−+2H+=NC(CH)CN,故D正确;
2 2 4
故答案选D。
11.(2024·吉林长春·一模)我国学者研发出一种新型水系锌电池,其示意图如下。该电池分别以
Zn−TCPP(局部结构如标注框内所示)形成的稳定超分子材料和Zn为电极,以ZnSO 和KI混合液为电解质
4
溶液。下列说法错误的是
A.标注框内所示结构中存在共价键和配位键
B.电池总反应为: +Zn Zn2++3I−
C.充电时,阴极被还原的Zn2+主要来自电解质溶液
D.放电时,外电路转移0.2mol电子,理论上电池负极消耗6.5gZn
【答案】B
【分析】由图可知,锌电极是原电池的负极,锌失去电子发生氧化反应生成锌离子;超分子材料是正极,
在正极得到电子发生还原反应生成碘离子,总反应为: 。据此分析作答。
【详解】A.标注框内所示结构属于配合物,配位体中存在碳碳单键、碳碳双键等多种共价键,还有由N
提供孤电子对、Zn2+提供空轨道形成的配位键,A正确;B.锌电极是原电池的负极,锌失去电子发生氧化反应生成锌离子;超分子材料是正极, 在正极得到电
子发生还原反应生成碘离子,总反应为: ,B错误;
C.充电时溶液中的 优先在阴极被还原,电极反应为 , 主要来源于电解质溶液,C
正确;
D.放电时,负极的电极反应式为 ,外电路转移0.2mol电子,理论上电池负极消耗
0.1mol×65g/mol=6.5gZn,D正确;
故选B。
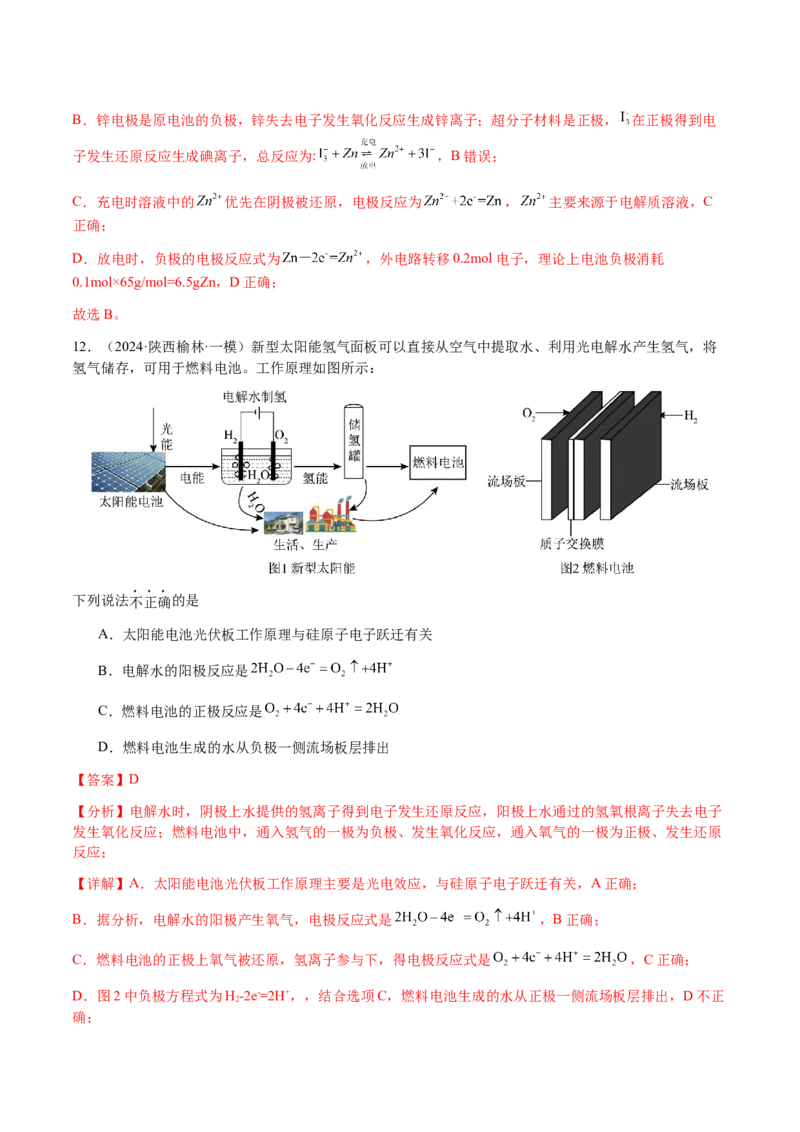
12.(2024·陕西榆林·一模)新型太阳能氢气面板可以直接从空气中提取水、利用光电解水产生氢气,将
氢气储存,可用于燃料电池。工作原理如图所示:
下列说法不正确的是
A.太阳能电池光伏板工作原理与硅原子电子跃迁有关
B.电解水的阳极反应是
C.燃料电池的正极反应是
D.燃料电池生成的水从负极一侧流场板层排出
【答案】D
【分析】电解水时,阴极上水提供的氢离子得到电子发生还原反应,阳极上水通过的氢氧根离子失去电子
发生氧化反应;燃料电池中,通入氢气的一极为负极、发生氧化反应,通入氧气的一极为正极、发生还原
反应;
【详解】A.太阳能电池光伏板工作原理主要是光电效应,与硅原子电子跃迁有关,A正确;
B.据分析,电解水的阳极产生氧气,电极反应式是 ,B正确;
C.燃料电池的正极上氧气被还原,氢离子参与下,得电极反应式是 ,C正确;
D.图2中负极方程式为H-2e-=2H+,,结合选项C,燃料电池生成的水从正极一侧流场板层排出,D不正
2
确;选D。
13.(2024·江西上饶·模拟预测)科学家成功研制出一种可在一分钟内完成充放电的超常性能铝离子电
池。该电池内部的 和有机阳离子构成电解质溶液,其放电工作原理如图所示。下列说法不正确的是
A.放电时,铝为负极,石墨为正极
B.充电时, 向石墨电极移动
C.放电时,负极的电极反应式为
D.充电时,电子从石墨电极直接经导线流入铝电极,然后再经电解质溶液流回石墨电极
【答案】D
【分析】根据电池原理图可知,放电时铝电极为负极,石墨为正极;电解时铝电极为阴极,石墨为阳极。
【详解】A.放电时, 向负极移动,故铝为负极,石墨为正极,A项正确;
B.充电时,铝为阴极,石墨为阳极,阴离子向阳极移动,B项正确;
C.放电时,负极上铝失电子结合 生成 ,发生反应: ,C项正确;
D.根据“电子不下水,离子不上岸”,电子不进入电解质溶液,电解质溶液中是自由移动的离子导电,
故充电时电子移动方向为:石墨电极→外加电源正极,外加电源负极→铝电极,D项错误;
答案选D。
14.(2024·浙江·模拟预测)一种清洁、低成本的氯碱工业双联装置工作原理如图所示,浓缩海水可以造
成溶液中离子浓度差异,使离子从高浓度区域向低浓度区域迁移,从而产生离子电流。下列说法不正确的
是A.电极Y为负极,可以在X、Z电极上收集到H
2
B.与传统氯碱工业相比,该双联装置的优点是可避免使用离子交换膜
C.装置Ⅱ中的电极质量每变化mg,装置I中可制得 LiCl
D.随着装置的运行,电极Z附近溶液的pH增大,电极W附近有白色沉淀出现
【答案】C
【分析】结合题干信息,装置Ⅰ为原电池,装置Ⅱ为电解池,装置Ⅰ中,Li+移向X电极,故X为正极,Y
为负极;Z为阴极,W为阳极,X电极反应为2H++2e-=H ↑,W电极反应为Ag-e-=Ag+,生成的银离子再发
2
生Ag++Cl-=AgCl↓,Z电极反应为2HO+2e-=H ↑+2OH-,据此分析解答。
2 2
【详解】A.根据分析,电极Y为负极,可以在X、Z电极上收集到H,故A正确;
2
B.反应中,氯离子生成氯化银,可以不使用离子交换膜,故与传统氯碱工业相比,该双联装置可避免使
用离子交换膜,故B正确;
C.W电极反应为Ag-e-=Ag+,装置Ⅱ中的W电极质量每变化mg,该电极减少mg银,转移电子的物质的
量为 ,结合得失电子守恒,故装置I中X电极生成 LiCl,则装置I中可制得 LiCl,
故C错误;
D.Z电极反应为2HO+2e-=H ↑+2OH-,随着装置的运行,电极Z附近溶液的pH增大,电极W反应为Ag-
2 2
e-=Ag+,生成的银离子再发生Ag++Cl-=AgCl↓,故附近有白色沉淀出现,故D正确;
故选C。
15.(2024·全国·模拟预测)我国科学家发明了一种新型短路膜电池,利用 分离 的装置如图所示。
下列说法中正确的是A.正极反应为
B.正极反应消耗22.4L ,理论上需要转移2mol电子
C.该装置用于空气中 的捕获, 最终由出口A流出
D.该电池中电子由负极经短路膜流向正极
【答案】D
【分析】通入氧气的一极为正极,电极反应式为 , 与 反应得到 ,通
入氢气的一极为负极,电极反应式为 , 与 反应生成 ,实现 的分离。
【详解】A.由分析可知,正极的电极反应式为 ,A错误;
B.未指明是否处在标准状况下,无法计算22.4L 的物质的量,则无法计算反应中需要转移的电子数,
B错误;
C.由题图可知,负极生成 ,则 最终由出口B流出,C错误;
D.由题图可知,电子可以在短路膜中移动,该电池中负极上失去的电子经短路膜流向正极,D正确;
故选D。
16.(2024·四川达州·一模)碱性锌锰干电池的总反应为: ,电池构
造示意图如图所示。下列有关说法正确的是A. 电极电势高
B.电池工作时, 被氧化
C.电池工作时, 通过隔膜向正极移动
D.反应中每生成 ,消耗
【答案】D
【分析】根据电池总反应方程式可知:Zn为负极,发生氧化反应,电极反应式为:Zn-2e-+2OH-
=ZnO+H O,MnO 为正极,发生还原反应,电极反应式为:MnO +e-+H O=MnOOH+OH-。电池工作时,阳
2 2 2 2
离子向正极定向移动,阴离子向负极定向移动。
【详解】A.根据反应总方程式可知,电池工作时,锌为负极,则 电极电势低,A错误;
B.根据电池反应方程式可知:电池工作时,Mn元素化合价降低,得到电子被还原,所以MnO 发生还原
2
反应,B错误;
C.电池工作时,OH-会向正电荷较多的负极定向移动,即OH-通过隔膜向负极移动,C错误;
D.根据 ,故每生成l mol MnOOH,消耗0.5mol锌,
即65g/mol×0.5mol=32.5g,D正确;
故合理选项是D。
17.(2025·河北·模拟预测)清华大学尹斓副教授、熊巍博士提出了一种可完全生物降解的锌-钼( )
原电池,是实现生物可吸收电子药物的重要电源,结构如图所示。已知电池使用过程中在 表面形成一
层 薄膜,下列说法正确的是
A. 作原电池负极,其质量逐渐减小
B.该电池在放电过程中,水凝胶的 不变
C. 表面发生的电极反应:
D.电路中转移 电子时,理论上消耗【答案】B
【分析】锌为活泼金属,失去电子发生氧化反应,是负极,电极反应式为 ,Mo为
正极,电极反应式为 。
【详解】A.Zn为原电池负极发生氧化还原反应生成ZnO,电极质量增大,A错误;
B.负极反应式为 ,正极电极反应式为 ,则总反应式为:
,水凝胶的 不变,故B正确;
C.锌失去电子发生氧化反应,电极反应式为 ,C错误;
D.正极电极反应式为 ,电路中转移 电子时,理论上消耗 ,则D
错误;
故选B。
18.(2025·河南·模拟预测)我国科学家设计了一种水系 可充电电池,其工作原理如图所示。
下列说法正确的是
A.充电时,电极b为阳极
B.充电时,阳极附近溶液的pH增大
C.放电时,负极的电极反应:
D.放电时,溶液中 向电极b方向迁移
【答案】C
【分析】由图可知,放电时,电极a上MnO 转化为Mn2+,发生还原反应,电极b上Cu S转化为S,发生
2 2
氧化反应,则电极a为正极,电极b为负极;充电时,电极a上Mn2+转化为MnO ,发生氧化反应,电极b
2
上S转化为Cu S,发生还原反应,此时电极a为阳极,电极b为阴极。
2
【详解】A.充电时,S转化为Cu S,发生还原反应,则电极b为阴极,A错误;
2
B.根据分析,充电时,电极b为阴极,则电极a为阳极,电极a的电极反应为Mn2++2H O-2e-
2=MnO+4H+,阳极附近溶液的pH减小,B错误;
2
C.放电时,电极b为负极,负极的电极反应为Cu S−4e−=S+2Cu2+,C正确;
2
D.放电时,溶液中 向正极移动,即向电极a方向迁移,D错误;
故选C。
19.(2025·福建泉州·模拟预测)一种 打印机的柔性电池以碳纳米管作电极材料,以吸收 溶液的
有机高聚物为固态电解质,电池总反应为:
。下列说法不正确的是
A.放电时,含有锌膜的碳纳米管纤维作电池负极
B.充电时, 移向锌膜,锌元素发生还原反应
C.充电时,阴极反应:
D.该有机高聚物可通过加聚反应制得
【答案】C
【分析】电池总反应为:
,放电时,Zn为负极,电极反应式为:
,正极反应式为:MnO +e-
2
+H O=MnOOH+OH-,充电时,与电源负极相连的是阴极,与正极相连的是阳极;
2
【详解】A.Zn所在电极为负极,即放电时,含有锌膜的碳纳米管纤维作电池负极,故A正确;
B.由分析可知,放电时Zn所在电极为负极,充电时,Zn所在电极为阴极,Zn2+移向锌膜,锌元素发生还
原反应,故B正确;
C.由分析可知,充电时,与电源负极相连的是阴极,则阴极反应:
,故C错误;D.有机高聚物的结构片段发现可知,是加成聚合产物,合成有机高聚物的单体是:
,该有机高聚物可通过加聚反应制得,故D正确;
故选C。
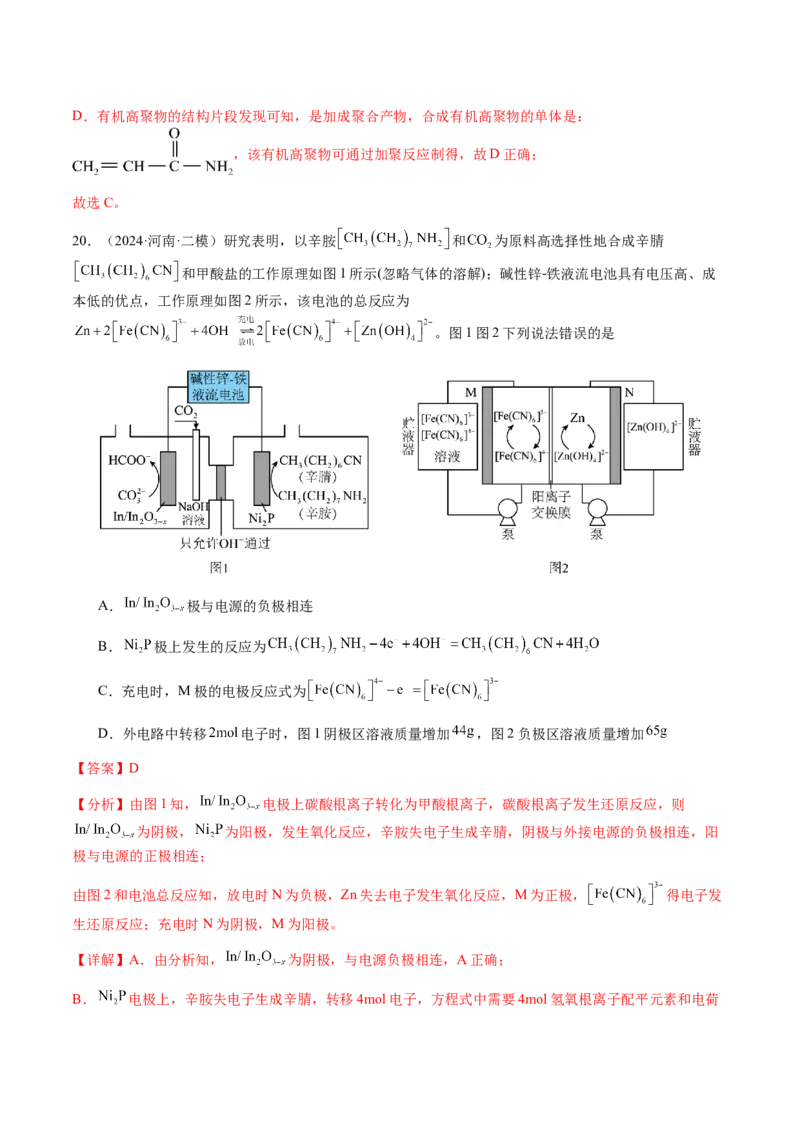
20.(2024·河南·二模)研究表明,以辛胺 和 为原料高选择性地合成辛腈
和甲酸盐的工作原理如图1所示(忽略气体的溶解);碱性锌-铁液流电池具有电压高、成
本低的优点,工作原理如图2所示,该电池的总反应为
。图1图2下列说法错误的是
A. 极与电源的负极相连
B. 极上发生的反应为
C.充电时,M极的电极反应式为
D.外电路中转移 电子时,图1阴极区溶液质量增加 ,图2负极区溶液质量增加
【答案】D
【分析】由图1知, 电极上碳酸根离子转化为甲酸根离子,碳酸根离子发生还原反应,则
为阴极, 为阳极,发生氧化反应,辛胺失电子生成辛腈,阴极与外接电源的负极相连,阳
极与电源的正极相连;
由图2和电池总反应知,放电时N为负极,Zn失去电子发生氧化反应,M为正极, 得电子发
生还原反应;充电时N为阴极,M为阳极。
【详解】A.由分析知, 为阴极,与电源负极相连,A正确;
B. 电极上,辛胺失电子生成辛腈,转移4mol电子,方程式中需要4mol氢氧根离子配平元素和电荷守恒,电极反应式为: ,B正确;
C.充电时,M电极为阳极,发生氧化反应,M极的电极反应式为 ,C正
确;
D.外电路中转移 电子时,图1阴极吸收1mol二氧化碳,增加44g,但是同时有2mol氢氧根离子移
出阴极区,增加的质量只有10g;外电路中转移 电子时,图2中,锌失电子后与氢氧根离子生成
,溶液增加的质量为1mol锌和2mol氢氧根质量之和,大于65g,D错误;
故选D。