文档内容
临考押题卷 02(黑吉辽通用)
满分100分 考试时间75分钟
可能用到的相对原子质量:H-1 C-12 N-14 O-16 S-32 K-39 Fe-56 Ga-70
一、选择题:本题共15小题,每小题3分,共45分。在每小题给出的四个选项中,只有一项符合题目
要求。
1.化学与生活、科技、社会发展息息相关。下列有关说法正确的是
A.大规模开发可燃冰有利于实现碳达峰、碳中和
B.铁磁流体液态机器人中驱动机器人运动的磁铁的主要成分是 Fe O
2 3
C.“天问一号”火星车使用热控保温材料——纳米气凝胶,可产生丁达尔效应
D.“天和”核心舱电推进系统中使用的氮化硼陶瓷基复合材料属于新型有机高分子材料
【答案】C
【解析】A.大规模开发可燃冰会增加二氧化碳的排放量,不利于实现碳达峰、碳中和,A 错误;B.
铁磁流体液态机器人中驱动机器人运动的磁铁的主要成分是 Fe3O4,B 错误;C.纳米气凝胶为胶体,
可产生丁达尔效应,C 正确;D.“天和”核心舱电推进系统中使用的氮化硼陶瓷基复合材料属于新型
无机高分子材料,D 错误;故选 C。
2.下列化学用语或图示表达错误的是
A. 的电子式:
B. 的球棍模型:
C.苯的空间填充模型:
D. 的离子结构示意图:
【答案】B
【解析】A.铵根离子带1个单位正电荷,中心原子为N,N原子与每个H原子共用1对电子,A正确;
B.CO 是共价化合物,直线形分子,中心原子是C,含有C=O双键,且氧原子半径小于碳原子,B错
2
误;C.苯为正六边形结构,C正确;D.Ca2+的质子数为20,核外电子数为18,核外各层上电子数分别
为2、8、8,D正确;故选B。
3.下列有关物质的工业制备方法不合理的是
A.用蒸发结晶法提取海水中的食盐
B.氯气与澄清石灰水制取漂白粉
C.用“吹出法”从海水中提取溴
D.催化裂化将重油转化为汽油等物质
【答案】B
【解析】A.海水中氯化钠溶解度随温度变化不大,工业上是通过蒸发溶剂的方法得到氯化钠晶体,故A正确;B.工业上用氯气与石灰乳反应制取漂白粉,故B错误;C.Br 易挥发,通入热空气吹出Br ,
2 2
可以起到富集溴元素的作用,故C正确;D.通过催化裂化,将长链的重油转化为短链的汽油等物质,
故D正确。答案选B。
4.下列装置能用于相应实验的是
A.粗盐水的过滤 B.制备 C.乙酸乙酯的制备与收集 D.铁制镀件镀铜
【答案】D
【解析】A.过滤操作中漏斗末端应紧扣接液烧杯内壁,选项A错误;B.浓盐酸与二氧化锰反应制备
氯气时应该加热,选项B错误;C.乙酸乙酯在氢氧化钠溶液中能发生水解,收集时应用饱和碳酸钠溶
液接收,选项C错误;D.在铁制品表面镀铜时应将铁制品连接在电源的负极作为阴极,铜连接在电源
的正极,电解质溶液为可溶性铜盐溶液,选项D正确;答案选D。
5.中国科学院金属研究所发现采用 和NaOH混合促进剂,可明显提高铝与水反应制氢系统的
性能,制氢机理如图。主要反应为: ↑;
。 溶液显碱性,N 代表阿伏加德罗常数的值。下
A
列说法正确的是
A.1L 0.1 mol∙L−1 溶液中阴离子数目等于
B.上述反应中的氧化产物为Sn和H
2
C.标准状况下,反应过程中生成33.6L H ,转移电子数目为9N
2 A
D.Al-Sn 原电池的形成,能提高产氢速率,析氢反应主要发生在 Sn上
【答案】D
【分析】Al与NaSnO 可以发生反应6Al+3Na SnO +15H O=3Sn+6NaAl(OH)+3H ↑(1),和NaOH
2 3 2 3 2 4 2
也可发生反应2Al+2NaOH+6H O=2NaAl(OH)+3H ↑(2),图示中Al与NaSnO 和NaOH反应,随着
2 4 2 2 3
反应的进行,生成的Sn和氢气的量也逐渐增多。
【解析】A.NaSnO 溶液显碱性,是强碱弱酸盐, 会发生水解导致阴离子个数增多,大于0.1N
2 3 A
个,故A错误;B.根据分析该过程存在6Al+3Na SnO +15H O=3Sn+6NaAl(OH)+3H ↑,还原产物为
2 3 2 4 2
Sn和H,故B错误;C.在整个过程中生成故氢气的反应有两个,当氢气全部是反应(1)生成的,
233.6LH转移的电子数为9N ,当氢气全部是反应(2)生成的,转移的电子数为3N ,两个反应同时发生,
A A
故转移电子数目为介于3N 与9N 之间,故C错误;D.形成Al-Sn原电池可以加快反应速率,Al活泼
A A
作负极,故Sn作正极,析氢反应主要发生在Sn上,故D正确,故选:D。
6.1908年意大利化学家Ciamician发现,当物质M暴露于阳光下一年后,会产生物质N,该反应为:
下列有关叙述错误的是
A.M和N互为同分异构体
B.N中有3个手性碳原子
C.M与H₂的加成产物还能发生消去反应
D.M中所有碳原子不可能共平面
【答案】B
【解析】A.M和N的分子式均为C H O,互为同分异构体,故A正确;B.手性碳原子是指C的四个
10 14
化学键连接的基团均不同,N中有4个手性碳原子,故B错误;C.M与H₂的加成后碳氧双键打开,生
成-OH,可发生消去反应,故C正确;D. 如图,M中该C与其所连接的三个C不可能共
平面,故D正确;故选B。
7.W、X、Y、Z、Q是核电荷数依次增大的五种短周期元素。 的半径在所有离子中最小,X、Y、Z
同周期且相邻,Z、Q位于同一主族且Z的核电荷数是Q的一半。下列说法正确的是
A.Z、Q元素的最高正价相同
B.W、X、Y、Z四种元素不能形成离子化合物
C.X、Q的最高价氧化物对应水化物的酸性:
D.X、Y、Z分别与W形成的简单化合物的沸点:
【答案】C
【分析】W、X、Y、Z、Q是核电荷数依次增大的五种短周期元素。 的半径在所有离子中最小,则
W为H,Z、Q位于同一主族且Z的核电荷数是Q的一半,则Z为O,Q为S,X、Y、Z同周期且相邻,
故X为C,Y为N;
【解析】A.Z为O,Q为S,Z一般没有正价,Q元素的最高正价为+6价,选项A错误;B.W、X、
Y、Z四种元素能形成离子化合物NH HCO 或(NH )CO,选项B错误;C.元素非金属性S>C,故X、
4 3 4 2 3
Q的最高价氧化物对应水化物的酸性: ,选项C正确;D.X、Y、Z分别与W形成的简
单化合物中HO、NH 存在氢键,沸点: ,选项D错误;答案选C。
2 3
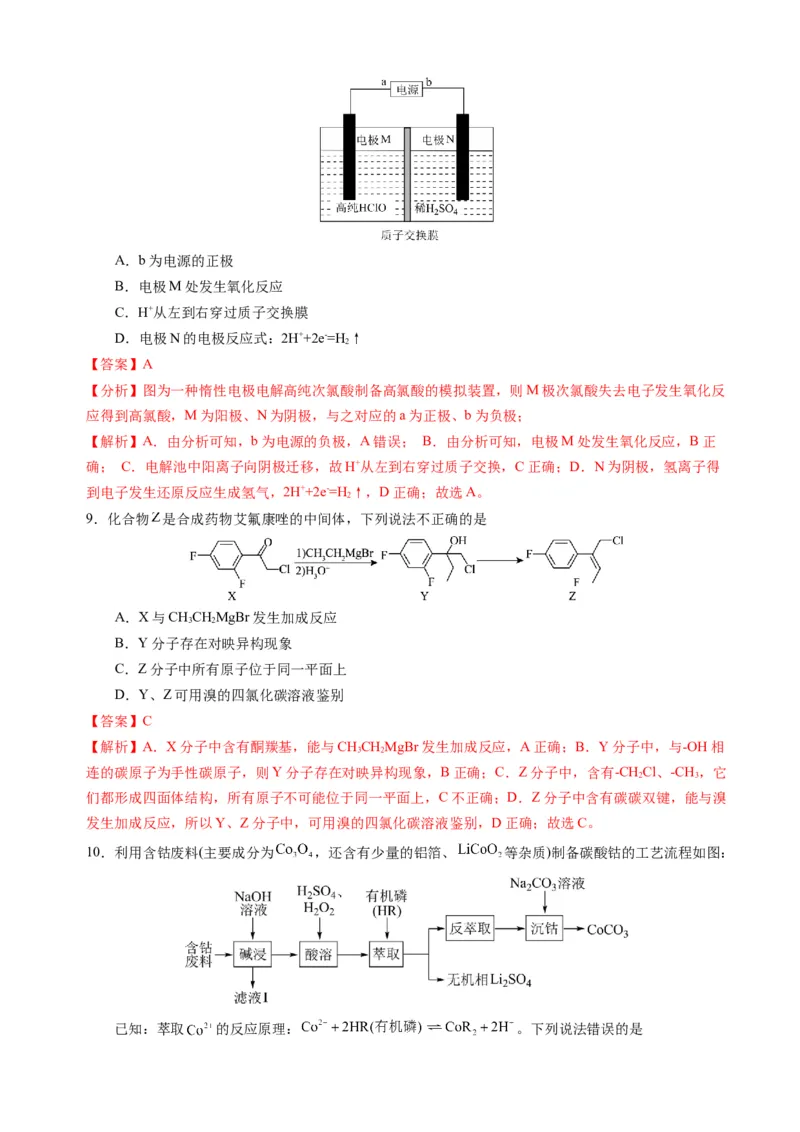
8.高氯酸(HClO)是制备导弹和火箭的固体推进剂高氯酸铵(NH ClO )的原料之一,下图为一种惰
4 4 4
性电极电解高纯次氯酸制备高氯酸的模拟装置。下列有关说法不正确的是A.b为电源的正极
B.电极M处发生氧化反应
C.H+从左到右穿过质子交换膜
D.电极N的电极反应式:2H++2e-=H ↑
2
【答案】A
【分析】图为一种惰性电极电解高纯次氯酸制备高氯酸的模拟装置,则M极次氯酸失去电子发生氧化反
应得到高氯酸,M为阳极、N为阴极,与之对应的a为正极、b为负极;
【解析】A.由分析可知,b为电源的负极,A错误; B.由分析可知,电极M处发生氧化反应,B正
确; C.电解池中阳离子向阴极迁移,故H+从左到右穿过质子交换,C正确;D.N为阴极,氢离子得
到电子发生还原反应生成氢气,2H++2e-=H ↑,D正确;故选A。
2
9.化合物 是合成药物艾氟康唑的中间体,下列说法不正确的是
A.X与CHCHMgBr发生加成反应
3 2
B.Y分子存在对映异构现象
C.Z分子中所有原子位于同一平面上
D.Y、Z可用溴的四氯化碳溶液鉴别
【答案】C
【解析】A.X分子中含有酮羰基,能与CHCHMgBr发生加成反应,A正确;B.Y分子中,与-OH相
3 2
连的碳原子为手性碳原子,则Y分子存在对映异构现象,B正确;C.Z分子中,含有-CHCl、-CH,它
2 3
们都形成四面体结构,所有原子不可能位于同一平面上,C不正确;D.Z分子中含有碳碳双键,能与溴
发生加成反应,所以Y、Z分子中,可用溴的四氯化碳溶液鉴别,D正确;故选C。
10.利用含钴废料(主要成分为 ,还含有少量的铝箔、 等杂质)制备碳酸钴的工艺流程如图:
已知:萃取 的反应原理: 。下列说法错误的是A.“滤液Ⅰ”中溶质的主要成分是
B.“酸溶”反应中 做氧化剂
C.“反萃取”中可加入 分离出
D.“沉钴”时 溶液滴加速率不宜过快,目的是防止生成
【答案】B
【分析】
含钴废料(主要成分为 ,还含有少量的铝箔、 等杂质)中加入NaOH溶液碱浸,铝箔溶解
转化为 (滤液Ⅰ)除去,滤渣主要含 和 ,根据实验目的可知后续需要萃取
Co2+,说明经过酸溶之后,+3价Co元素转化为Co2+,即在酸溶步骤中Co元素被还原,则加入的HO 作
2 2
还原剂,过滤,所得滤液中主要含CoSO 和LiSO ,滤液中加入有机磷萃取,分液后得到含有LiSO 的
4 2 4 2 4
无机相及含有CoR 的有机相,有机相中可加入HSO 进行反萃取分离出Co2+,最后加入NaCO 溶液沉
2 2 4 2 3
钴获得CoCO,以此分析解答。
3
【解析】A.由分析知,滤液Ⅰ”主要成分是 ,故A正确;B.由分析知,“酸溶”反应中
HO 作还原剂,故B错误;C.根据分析,“反萃取”中可加入HSO 分离出Co2+,故C正确;D.
2 2 2 4
“沉钴”时NaCO 的滴速过快或浓度太大溶液碱性增强会产生 杂质,将导致产品不纯,溶液滴
2 3
加速率不宜过快,故D正确;故选B。
11.我国科学家研发了一种由废水(含 、 等)提铀并同步产电的工艺,其工作原理和相关物
质转化关系如图所示,下列有关该过程的说法不正确的是
A.电子从 电极经导线流向CCF电极
B.CCF电极上发生的反应有:
C.生成( 的反应中,
D.利用电解法再次获得含 溶液,需将附着 、 的电极置于阳极
【答案】C
【分析】由图可知,铁电极为原电池的负极,铁失去电子发生氧化反应生成亚铁离子,电极反应式为Fe
—2e—=Fe2+,CCF电极为正极,水分子作用下氧气在正极得到电子发生还原反应生成过氧化氢和氢氧根
离子、UO 在正极得到电子发生还原反应生成UO ,电极反应式为 、UO
2
+2e—=UO,放电生成的UO 与过氧化氢反应生成(UO )O ·H O,反应的化学方程式为
2 2 2 2 2
UO +2H O=(UO)O ·H O。
2 2 2 2 2 2
【解析】A.由分析可知,铁电极为原电池的负极,CCF电极为正极,则电子从Fe电极经导线流向CCF电极,故A正确;B.由分析可知,CCF电极为正极,水分子作用下氧气在正极得到电子发生还原反应
生成过氧化氢和氢氧根离子、UO 在正极得到电子发生还原反应生成UO ,电极反应式为
2
、UO +2e—=UO,故B正确;C.由分析可知,生成(UO )O ·H O的化
2 2 2 2
学方程式为UO +2H O=(UO)O ·H O,则反应中氧化剂HO 与还原剂UO 的物质的量之比为1:1,故C
2 2 2 2 2 2 2 2 2
错误;D.利用电解法再次获得含 溶液时,与直流电源的正极相连的CCF电极为阳极,UO 、
2
(UO )O ·H O在阳极失去电子发生氧化反应生成UO ,故D正确;故选C。
2 2 2
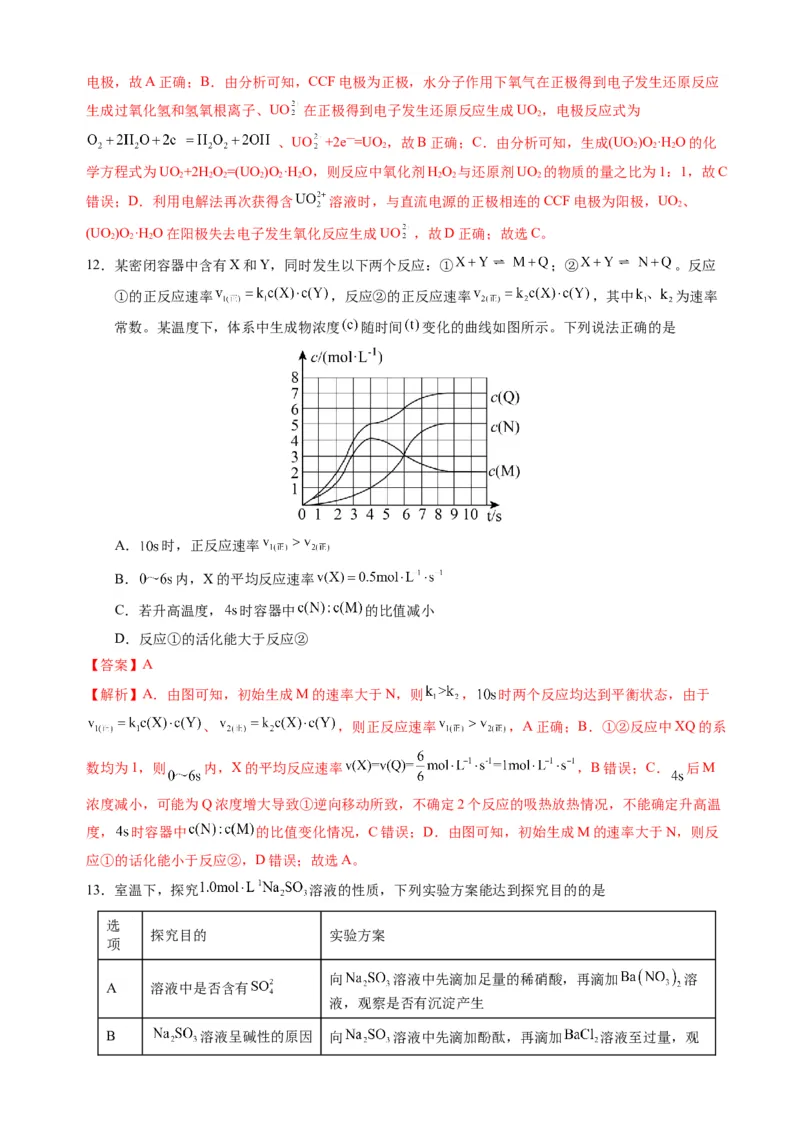
12.某密闭容器中含有X和Y,同时发生以下两个反应:① ;② 。反应
①的正反应速率 ,反应②的正反应速率 ,其中 为速率
常数。某温度下,体系中生成物浓度 随时间 变化的曲线如图所示。下列说法正确的是
A. 时,正反应速率
B. 内,X的平均反应速率
C.若升高温度, 时容器中 的比值减小
D.反应①的活化能大于反应②
【答案】A
【解析】A.由图可知,初始生成M的速率大于N,则 , 时两个反应均达到平衡状态,由于
、 ,则正反应速率 ,A正确;B.①②反应中XQ的系
数均为1,则 内,X的平均反应速率 ,B错误;C. 后M
浓度减小,可能为Q浓度增大导致①逆向移动所致,不确定2个反应的吸热放热情况,不能确定升高温
度, 时容器中 的比值变化情况,C错误;D.由图可知,初始生成M的速率大于N,则反
应①的话化能小于反应②,D错误;故选A。
13.室温下,探究 溶液的性质,下列实验方案能达到探究目的的是
选
探究目的 实验方案
项
向 溶液中先滴加足量的稀硝酸,再滴加 溶
A 溶液中是否含有
液,观察是否有沉淀产生
B 溶液呈碱性的原因 向 溶液中先滴加酚酞,再滴加 溶液至过量,观察溶液颜色变化
C 是否具有漂白性 向溴水中滴加足量 溶液,观察溶液颜色
向 溶液中先滴加几滴 溶液,无明显现象,再滴
D 是否具有还原性
加适量稀盐酸,观察是否有沉淀产生
【答案】B
【解析】A.硝酸具有氧化性,能氧化亚硫酸根生成硫酸根,和钡离子生成硫酸钡沉淀,不能检验溶液
中是否含有亚硫酸根离子,A不符合题意;B.亚硫酸根离子水解生成氢氧根离子,使得溶液显碱性,
滴加酚酞溶液变红色,再滴加 溶液至过量,钡离子和亚硫酸根离子生成沉淀,导致亚硫酸根离子
浓度减小,其水解逆向移动,氢氧根离子浓度减小,红色变浅,能达到实验目的,B符合题意;C.溴
水具有强氧化性,向溴水中滴加足量 溶液,两者发生氧化还原反应使得溴水褪色,不体现亚硫
酸根离子的漂白性,C不符合题意;D. 溶液中先滴加几滴 溶液,加入盐酸,两者在酸性
条件下,发生氧化还原反应生成硫单质黄色沉淀,亚硫酸根离子发生还原反应,体现氧化性,D不符合
题意;故选B。
14.为维护国家安全和利益,2023年7月3日,我国决定对镓、锗相关物项实施出口管制。氮化镓的晶
胞结构如下图所示(晶胞参数为apm)。下列说法不正确的是
A.该物质的化学式为GaN
B.晶体结构中Ga的配位数为4
C.该晶体的密度为
D.第二周期基态原子第一电离能大于N的元素有2种
【答案】C
【解析】A.该晶胞中含4个Ga原子、4个N原子,该物质的化学式为GaN,A正确;
B.与N原子最近且等距离的Ga原子有4个,N的配位数为4,Ga的配位数也为4,B正确;
C.GaN晶体的密度为 ,C错误;
D.与N元素位于同一周期且基态原子第一电能比N大的有F和Ne,D正确;
故选C。
15.常温下,用0.100 mol/L的NaOH溶液滴定20.00 mL未知浓度的次磷酸HPO 溶液。溶液pH、所有
3 2
含磷微粒的分布系数 [比如 的分布系数:[ ]随滴加NaOH溶液体
积V(NaOH)的变化关系如图所示。下列说法不正确的是A.HPO 是一种一元弱酸
3 2
B.常温下,HPO 的电离常数
3 2
C.V(NaOH)=10 mL时,c(Na+)<c( )
D.pH=7时,溶液中c(Na+)<0.05 mol/L
【答案】B
【分析】左侧纵坐标是含磷微粒的分布系数,根据图示可知:随着NaOH溶液的加入,溶液的pH值逐
渐增大,则曲线②为pH变化;含磷微粒只有2种,说明次磷酸为一元弱酸,且溶液的pH值越小,①、
③为含磷微粒,δ(H PO )越大,溶液的pH值越大,δ( )越大,故曲线③为δ(H PO ),曲线①为δ(
3 2 3 2
),然后根据问题分析解答。
【解析】A.随着NaOH溶液的加入,溶液的pH值逐渐增大,则②为pH变化;①、③为含磷微粒,且
含磷微粒只有2种,说明次磷酸为一元弱酸,A正确;B.左侧纵坐标是含磷微粒的分布系数,而溶液
pH随所加NaOH溶液体积V变化曲线(滴定曲线)是右侧的纵坐标,当 (H PO )= ( )时,即
3 2
c(H PO )=c( ),溶液的pH<4,所以K = <1.0×10-3,B错误;C.根据图像
3 2 a
可知:当V(NaOH)=10 mL时,c( )>c(H PO ),溶液为HPO 与NaHPO 的混合溶液,溶液中存在
3 2 3 2 2
电荷守恒:c(Na+)+c(H+)=c(OH-)+c( ),此时溶液pH<7,溶液显酸性,则c(H+)>c(OH-),故c(Na+)
<c( ),C正确;D.溶液中存在电荷守恒:c(Na+)+c(H+)=c(OH-)+c( ),当溶液pH=7,溶液
显中性,则c(H+)=c(OH-),故c(Na+)=c( ),此时溶液为HPO 与NaHPO 的混合溶液,HPO 过量,
3 2 2 3 2
此时加入NaOH溶液的体积小于20 mL,故c(Na+)=c( )< =0.05 mol/L,即c(Na+)
<0.05 mol/L,D正确;故合理选项是B。
二、非选择题:本题共4小题,共55分。
16.(14分)
锰废渣的硫酸浸出液含有大量 、 、 以及少量的 、 、 、 。通过沉
淀-萃取法可以回收其中的锰、钴、镍,流程如图所示。已知:萃取剂a和b均为有机物,可用通式 表示,萃取金属离子时,发生反应:
( 代表被萃取的金属)。
(1) 的作用是 。
(2)该流程中涉及的实验操作有___________(填字母标号)。
A.过滤 B.蒸发结晶 C.分液 D.蒸馏
(3)加入 调 的目的是 。
(4)已知: , ,向除铁后的溶液中加入 ,当溶液中
时, 。(保留1位有效数字)
(5)写出反萃取出 的离子方程式 。
(6) 、 利用萃取剂b进行分离,二者萃取率随无机相 变化如图所示。无机相的 控制
在 左右为宜。
(7)回收液中 浓度的测定:取 回收液,滴入几滴紫脲酸胺指示剂(遇 显橙黄色),
用浓度为 的 溶液进行滴定( ),达到滴定终点时消耗
溶液的体积 。 物质的量浓度为 。
【答案】(1)氧化
(2)AC
(3)使Fe3+转化成Fe(OH) 沉淀除去
3
(4)0.001
(5)
(6)5.4
(7)0.0250mol/L
【分析】锰废渣的硫酸浸出液首先用二氧化锰将二价铁氧化为三价铁,加入碳酸钙后调节pH使三价铁
转化为氢氧化铁除去三价铁离子,再用氟化锰除去钙离子、镁离子,随后再用萃取剂a萃取滤液中的
,所得有机相中加入反萃取剂得到含Mn2+的溶液,无机相用萃取剂b萃取 ,无机相中为含的溶液,有机相加入反萃取剂得到含Co2+的溶液,以此解题。
【解析】(1)根据题意可知,浸出液中含有二价铁, 的作用是氧化 ;
(2)根据流程图可知,该流程涉及的实验过程有过滤,分液,故选AC;
(3)在用二氧化锰将二价铁氧化为三价铁后,加入碳酸钙调节pH使三价铁形成氢氧化铁沉淀,故目的
是:使Fe3+转化成Fe(OH) 沉淀除去;
3
(4)当溶液中 时, ,
;
(5)根据信息可知,反萃取剂为酸,则反萃取出 是加入适量的酸将锰离子反萃取出来,相应的方
程式为: ;
(6)根据图中信息可知,pH为5.4左右时, 、 的萃取率相差较大,故无机相的 控制在5.4
左右;
(7)根据滴定原理可知,Ni2+与HY2-的物质的量之比为1∶1,则Ni2+的物质的量为0.1000mol/
2
L×0.0125L =0.00125mol,则Ni2+的物质的量浓度为 。
17.(13分)
三草酸合铁(Ⅲ)酸钾晶体{ , },为翠绿色单斜晶体,溶于水,
难溶于乙醇,是一些有机反应的催化剂。实验室制备该晶体具体步骤如下:
Ⅰ.制备
ⅰ.称 摩尔盐[ , ]放入 水中。再加入
溶液,搅拌,微热。
ⅱ.继续加入 氨水(过量),加热,不断搅拌,煮沸后静置,倾去上层清液,抽滤得 沉
淀。
Ⅱ.制备
ⅲ.称取 和 加入盛有 水的烧杯中,加热使其完全溶解后,搅拌,将
步骤ⅱ制取的 加入此溶液中。加热,使 溶解,溶液呈翠绿色。
ⅳ.过滤,将滤液浓缩。浓缩液转移至 烧杯中,后进行操作a。将得到的晶体分别用少量水和
乙醇洗涤,干燥,称量晶体质量为 。
回答下列问题:
(1)微热时,温度不能过高的原因是 。
(2)已知:二价铁在碱性介质中比酸性介质中更易氧化。摩尔盐相比硫酸亚铁不易变质的原因是
。
(3)步骤ⅱ中,制备 加热煮沸的目的是 。(4)步骤ⅲ中,写出将氢氧化铁加入溶液的离子方程式 。
(5)已知三草酸合铁(Ⅲ)酸钾与氢氧化钾溶解性曲线如下图所示,步骤ⅰ中操作 为 。
(6)用95%乙醇洗涤晶体的目的为 。
(7)该实验的产率为 (保留1位小数)。
【答案】(1)防止过氧化氢分解
(2)摩尔盐溶液酸性更强,亚铁离子不容易被氧化变质
(3)使氢氧化铁完全沉淀
(4)
(5)冷却结晶,过滤
(6)减少晶体的溶解损失,并易于干燥
(7)79.8
【分析】由题意可知, 溶解,加入 溶液氧化二价铁为三价铁,搅拌
微热,继续加入氨水(过量),加热不断搅拌,煮沸后静置,倾去上层清液,抽滤得 沉淀;
和 加入水,加热溶解,搅拌,将 加入此溶液中,加热,使 溶
解,过滤,将滤液浓缩、冷却结晶、过滤得到 晶体;
【解析】(1)步骤ⅰ为加热溶解 操作,需要使用烧杯、玻璃棒、酒精灯,A为
烧杯,由于过氧化氢不稳定受热易分解,故需微热,温度不能过高;
(2)已知:二价铁在碱性介质中比酸性介质中更易氧化;摩尔盐溶液中铵根离子水解使得溶液酸性更
强,导致亚铁离子不容易被氧化变质;
(3)加热煮沸可以使得氢氧化铁胶体小颗粒发生聚沉,得到氢氧化铁沉淀,利于分离;
(4)已知:三草酸合铁(Ⅲ)酸钾晶体{ }为翠绿色单斜晶体,溶于水,则碱性条件
下,氢氧化铁和草酸反应生成 和氢氧根离子,反应为:
;
(5)由曲线可知,三草酸合铁(Ⅲ)酸钾溶解度受温度影响较大,且低温时溶解度较小,故操作 为冷却
结晶、过滤得到 晶体;
(6)三草酸合铁(Ⅲ)酸钾晶体{ }溶于水,难溶于乙醇,且乙醇易挥发,故95%乙
醇洗涤晶体的目的为减少晶体的溶解损失,并易于干燥晶体;
(7)9.80g摩尔盐[ , ]为0.025mol,根据铁守恒可知,理论生成0.025mol ,则该实验的产率为 =79.8%。
18.(14分)
甲烷是一种清洁能源,也是一种重要的化工原料,常用作合成甲醇。
(1)已知甲烷、碳单质、氢气的燃烧热分别为 、 、 。则甲烷裂解
制备炭黑的热化学方程式为 。
(2)科学家们曾尝试用甲烷催化法消除汽车尾气中的NO,反应的热化学方程式为
。
①该反应 (填“能”或“不能”)自发进行。
②向绝热、恒容密闭容器中加入一定量的 和 发生反应,下列能判断该反应到达
平衡状态的是 (填字母)。
a.体系中混合气体的压强不变
b.体系中
c.体系的温度不变
d.混合气体的平均相对分子质量不变
e.混合气体的密度不变
(3)以甲烷为原料通过以下反应合成甲醇: 。
现将 和 充入恒容密闭容器中,在不同温度和压强下进行上述反应。测得平衡时
甲醇的物质的量随温度、压强的变化如图所示:
①结合反应原理及图像分析可知: 时降低温度, (填“增大”、“减小”或
“不变”); (填“>”、“<”或“=”)。
②E、F、N点对应的化学平衡常数大小关系为 (用 、 、 表示)。
③ ,若F点对应的平衡时 ,总压强为4MPa,则用分压代替浓度表示F点
的平衡常数 (分压 总压 物质的量分数)。
(4) 加氢制甲醇也具有重要的经济价值,其热化学方程式为
,已知m为起始时 和 的投料比。下图中其中投料比最大的是 (填“ ”、
“ ”或“ ”),理由是 。【答案】(1)
(2)能 ac
(3)减小 > 1.25
(4) 保持 不变,增大 ,平衡正向移动, 的平衡转化率增大
【解析】(1)根据燃烧热分别写出热化学方程式,
①
②
③
根据盖斯定律计算③-①-2 ②得 ,
故答案为+73.5kJ/mol;
(2)①该反应为熵增焓减的反应, ,反应能自发进行;
②向绝热、恒容密闭容器中加入一定量的 和 发生反应
;
a.反应为气体体积不变的反应,根据理想气体状态方程pV=nRT,温度变化,故压强也是变量,根据
“变量不变达平衡”,体系中混合气体的压强不变能说明反应达平衡状态,选项a正确;
b.随着反应的进行,根据物质计量数关系,反应后体系中保持 ,无法说明反应达
平衡状态,选项b错误;
c.反应为放热反应,随着反应的进行温度发生变化,当体系的温度不变时反应达平衡,选项c正确;
d.反应为气体体积不变的反应,气体总质量、总物质的量不变,混合气体的平均相对分子质量始终不
变,无法说明反应达平衡,选项d错误;
e.反应为气体体积不变的反应,气体总质量、总体积不变,混合气体的密度始终不变,无法说明反应达
平衡,选项e错误;
答案选ac;
(3)①正反应为放热反应,降低温度,平衡正向移动,则P 时降低温度,n(CH)减小,增大压强,平衡
1 4
正向移动,CH 的物质的量减小,则p>p;
4 1 2
②升高温度,平衡正向移动,平衡常数增大,相同温度平衡常数相同,则有 ;
③根据数据列三段式:此时总压强为4MPa,则P(CH )= ×4 MPa=1.6MPa,P(O )=0.8MPa,P(CH OH)=1.6MPa,则Kp=
4 2 3
=1.25MPa-1;
(4)根据图中信息可知,保持 不变,增大 ,平衡正向移动, 的平衡转化率增大,故
其中投料比最大的是 。
19.(14分)
雷诺嗪 是一种安全性比较高的药物,主要用于治疗慢性心绞痛。该物质的合成路线如下图所示。
回答下列问题:
(1) 中含有的官能团名称为 。
(2) 的分子式为 。
(3)利用质谱法测得 的相对分子质量为113,则 D的结构简式为 。
(4) 的化学方程式为 。
(5) 与 F生成 的过程中, 断键的位置为下图中 处。
(6)H为A的同分异构体,符合下列条件的 有 种。(已知:同一个碳原子上连两个
不稳定)
①属于芳香族化合物;
② 该物质与足量的 发生反应,可生成标准状况下 。
写出其中 谱上峰面积之比为 的结构简式: 。
【答案】(1)醚键和酚羟基
(2)C H N
8 11
(3)(4) + +HCl
(5)c
(6)9 或
【分析】A和 在一定条件下发生取代反应生成B,C和D发生取代反应生成E,利用质谱法
测得D的相对分子质量为113,结合C和E的结构简式可以推知D为 ,E和 发生取
代反应生成F,B、F和CHCH(OH)CH 发生反应生成G;
3 3
【解析】(1)由图可知,A含有醚键和酚羟基;
(2)由C结构可知, 的分子式为C H N;
8 11
(3)由分析可知,D为: ;
(4)E和 发生取代反应生成F, +
+HCl;
(5)结合B、F的结构简式可以推知B与F生成G的过程中,B断键的位置为图中的c,断裂后生成羟
基且碳链得到增长;
(6)H为A的同分异构体,符合条件:①属于芳香族化合物,含有苯环;②1mol该物质与足量的Na
发生反应,可生成标准状况下 22.4LH ,则分子中含有 2个-OH;综上所述,苯环上的取代基为:-
2
CHOH和-OH(存在邻间对3种);-CH、-OH、-OH(苯环上3个取代基且2个相同,则有6种);共有9种,
2 3
谱上峰面积之比为 的结构中存在 1 个甲基且结构对称,为 或
。