文档内容
绝密★启用前
2025 年高考考前信息必刷卷 03(北京专用)
化 学
考情速递
高考·新动向:近年来高考化学试卷总体呈现回归教材、回归课标的特点,2025年可能会继续延续这一
趋势。这意味着每一道题在考纲上都会有相应的考点对应,不管题型、考法、侧重点如何变化,都会
基于教材本身展开。
高考·新考法:对中学化学基础知识能正确复述、再现、识别,并能融会贯通;将实际问题分解,通过
运用有关知识,采用分析、综合的方法,处理简单化学问题;对常规考点的新设问或知识融合,对非
常规考点的创新糅合等。
高考·新情境:继续考查高中化学主干内容,强调化学与科技、生产、生活的亲密联系。高考化学学科
的改革旨在贴近社会与生活,强调课程标准的教育理念。改革后,试题将更加紧密地结合生活生产环
境,体现教育与实践的融合。命题会精选试题情境,发挥学科育人价值。情境素材可能来源于生活实
际、科研成果、社会热点等
命题·大预测:化学试题将继续体现综合性,即一道试题可能涉及多个知识点的综合考查。例如,在一
道工业流程题中,可能同时考查化学反应原理、元素化合物知识、化学实验操作等多个方面的内容,
要求考生能够将所学的化学知识融会贯通。题目的呈现方式可能会有创新,例如采用图表、数据等多
种形式呈现信息,增加信息的密度,测试考生在阅读理解、知识提炼、信息整合及书面表达等方面的
综合能力。考生需要能够快速捕捉关键信息、精准分析并有效传达信息,像根据图表中的数据变化趋
势分析化学平衡的移动方向等。
(考试时间:90分钟 试卷满分:100分)
注意事项:
1.答卷前,考生务必将自己的姓名、考生号等填写在答题卡和试卷指定位置上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡对应题目的答案标号涂黑。如需改动,用橡
皮擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上。写在本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H-1 Li-7 C-12 N-14 O-16 F-19 Na-23 Mg-24 Al-27 Si-28
S-32 Cl-35.5 K-39 Mn-55 Fe-56 Cu-64 Zn-65 Br-80 I-127 Ba-137 Ce-140 Pb-207
第一部分
一、选择题(本部分共14题,每题3分,共42分。在每题列出的四个选项中,选出最符合题目要求的
一项。)
1.我国在可控核聚变研究上处于世界领先水平。核聚变原料的制备与核聚变的产物如图。已知: 、 、 中仅 具有放射性。下列说法不正确的是( )
A.元素的第一电离能:H>He>Li B.可用质谱区分 、 和
C. 具有放射性 D. 、 的化学性质基本相同
2.下列化学用语或图示表达正确的是( )
A.SO 的VSEPR模型: B.NaOH的电子式:
3
C.葡萄糖的结构简式:C H O D.乙烯分子中的π键:
6 12 6
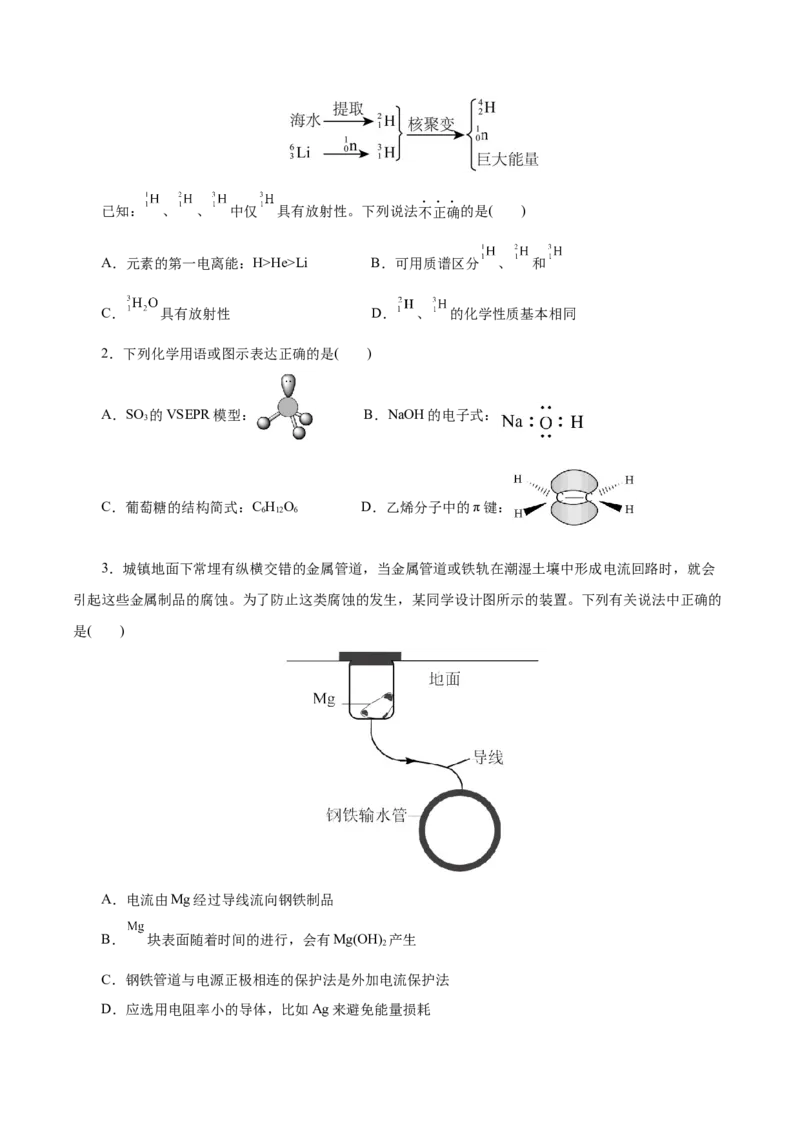
3.城镇地面下常埋有纵横交错的金属管道,当金属管道或铁轨在潮湿土壤中形成电流回路时,就会
引起这些金属制品的腐蚀。为了防止这类腐蚀的发生,某同学设计图所示的装置。下列有关说法中正确的
是( )
A.电流由Mg经过导线流向钢铁制品
B. 块表面随着时间的进行,会有Mg(OH) 产生
2
C.钢铁管道与电源正极相连的保护法是外加电流保护法
D.应选用电阻率小的导体,比如Ag来避免能量损耗4.下列说法不正确的是( )
A.采用多次盐析和溶解,可以分离提纯蛋白质
B.油脂的氢化也称油脂的硬化,得到的硬化油可作为制造肥皂和人造奶油的原料
C.苯甲酸钠是常用的食品防腐剂
D.高压法聚乙烯支链较少,密度和软化温度较高,属于高密度聚乙烯
5.下列离子方程式书写正确的是
A.NaHCO 溶液的水解:HCO -+H O CO2-+H O+
3 3 2 3 3
B.向Al (SO ) 溶液中滴加NaCO 溶液:2Al3++3CO 2-=Al(CO)↓
2 4 3 2 3 3 2 3 3
C.向Fe (SO ) 溶液中通入足量HS:2Fe3++S2-=2Fe2++S↓
2 4 3 2
D.向Ca(ClO) 溶液中通入少量SO :Ca2++3ClO-+SO+H O=Cl-+CaSO↓+2HClO
2 2 2 2 4
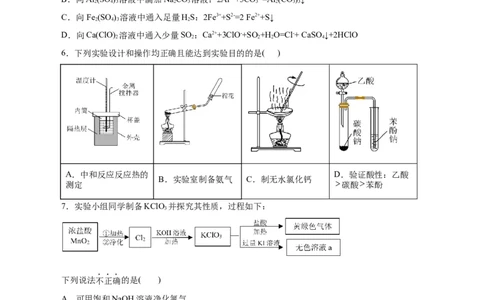
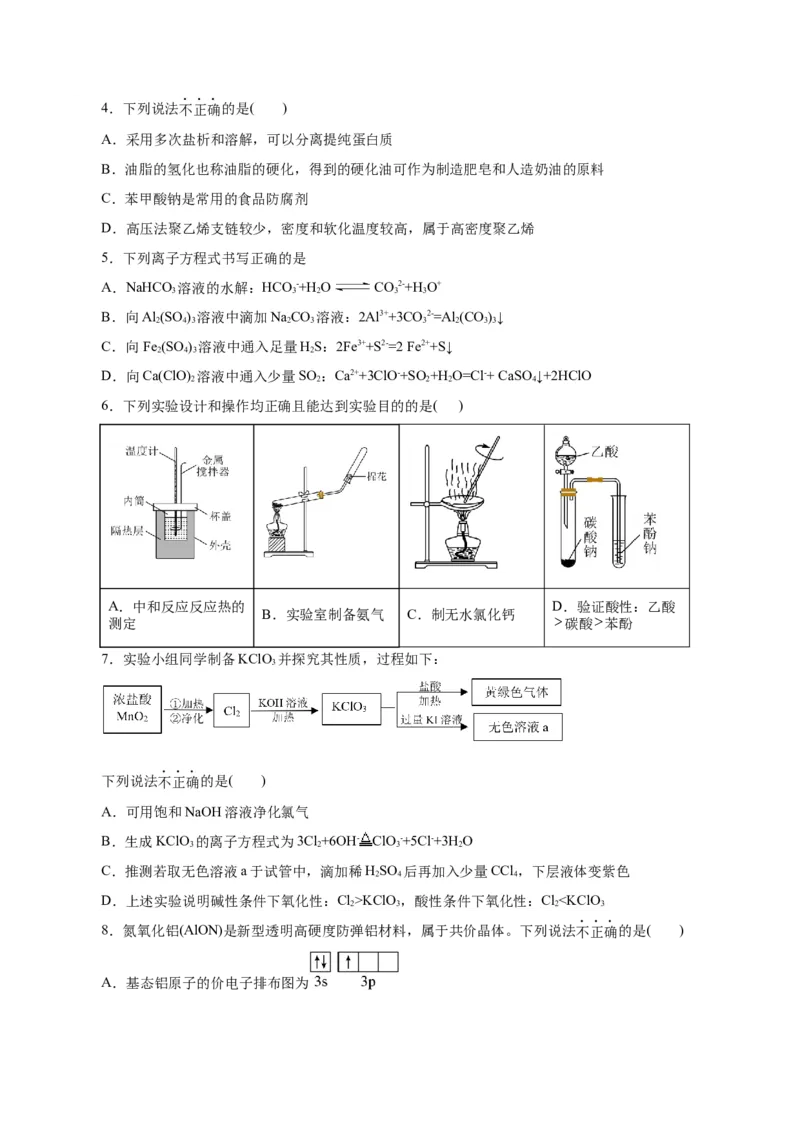
6.下列实验设计和操作均正确且能达到实验目的的是( )
A.中和反应反应热的 D.验证酸性:乙酸
B.实验室制备氨气 C.制无水氯化钙
测定 碳酸 苯酚
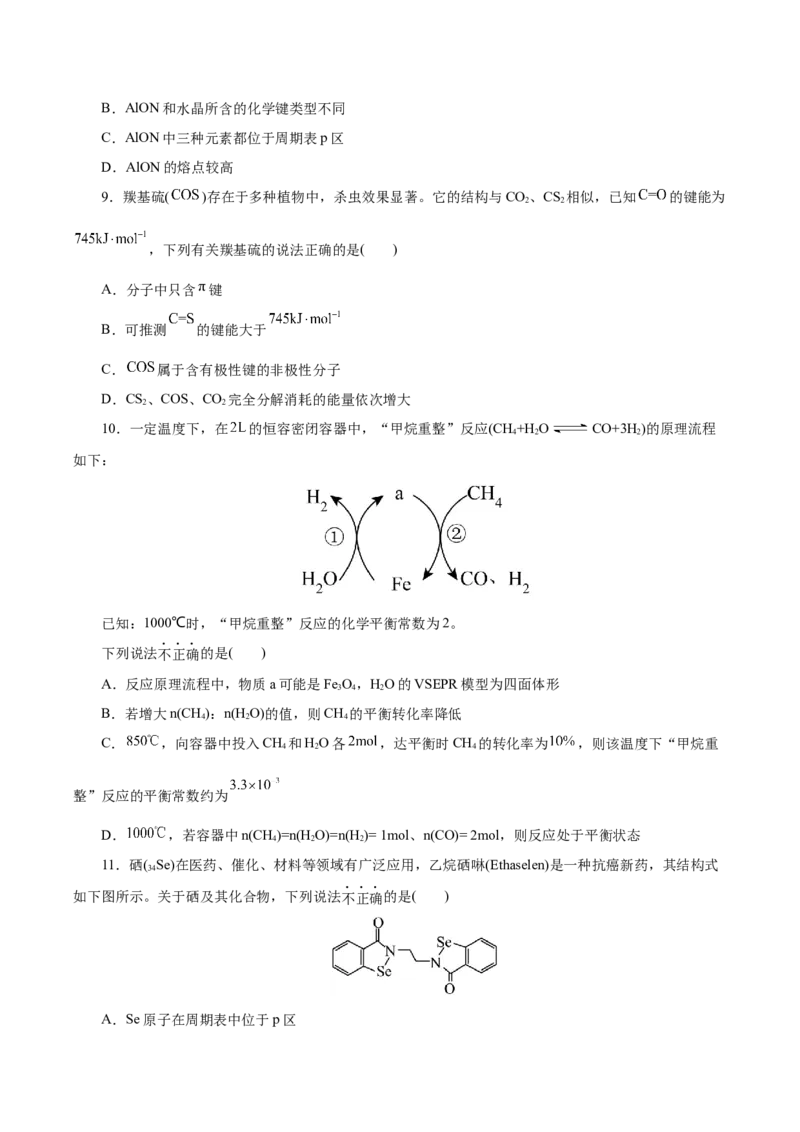
7.实验小组同学制备KClO 并探究其性质,过程如下:
3
下列说法不正确的是( )
A.可用饱和NaOH溶液净化氯气
B.生成KClO 的离子方程式为3Cl+6OH- ClO -+5Cl-+3H O
3 2 3 2
C.推测若取无色溶液a于试管中,滴加稀HSO 后再加入少量CCl ,下层液体变紫色
2 4 4
D.上述实验说明碱性条件下氧化性:Cl>KClO ,酸性条件下氧化性:ClNH+
3 4
D.在实验④的试剂中,逐滴加入浓NaOH溶液,可观察到溶液褪色
第二部分
二、非选择题(本部分共5题,共58分。)
15.(10分)某钙钛矿CHNH PbI 是一种新型半导体材料,用于制造太阳能电池。可用CHOH、NH 、
3 3 3 3 3
I、PbI 制备钙钛矿。
2 2
(1)Pb位于元素周期表第6周期ⅣA族,写出基态Pb原子价层电子轨道表示式 。
(2) NH 分子的VSEPR模型名称是 ,NH 的N—H键是由N的 轨道与H的
3 3
轨道重叠形成 键。
(3)制备CHNH PbI 的过程如下所示:
3 3 3
①Ⅰ中,CHOH的沸点高于CHI的沸点,原因是 。
3 3
②Ⅱ中,由于NH 分子中的 具有孤电子对,容易与CHI反应生成盐CHNH I。
3 3 3 3
(4)钙钛矿晶体的晶胞形状为立方体,边长为a nm,结构如图:
①距离CHNH +最近的I-有 个。
3 3
②CH NH PbI 的摩尔质量为620 g·molˉ1,阿伏加德罗常数为N ,则该晶体密度为 g·
3 3 3 A
cm-3。(1nm=10-7cm)
(5)钙钛矿的稳定性受空气中HO、O、紫外线等因素的影响。
2 2
ⅰ.
ⅱ.研究发现,一旦生成HI,钙钛矿的分解程度就会增大,请结合化学平衡移动原理解释: ,
我国研究人员利用聚乙二醇有效地解决了该问题。
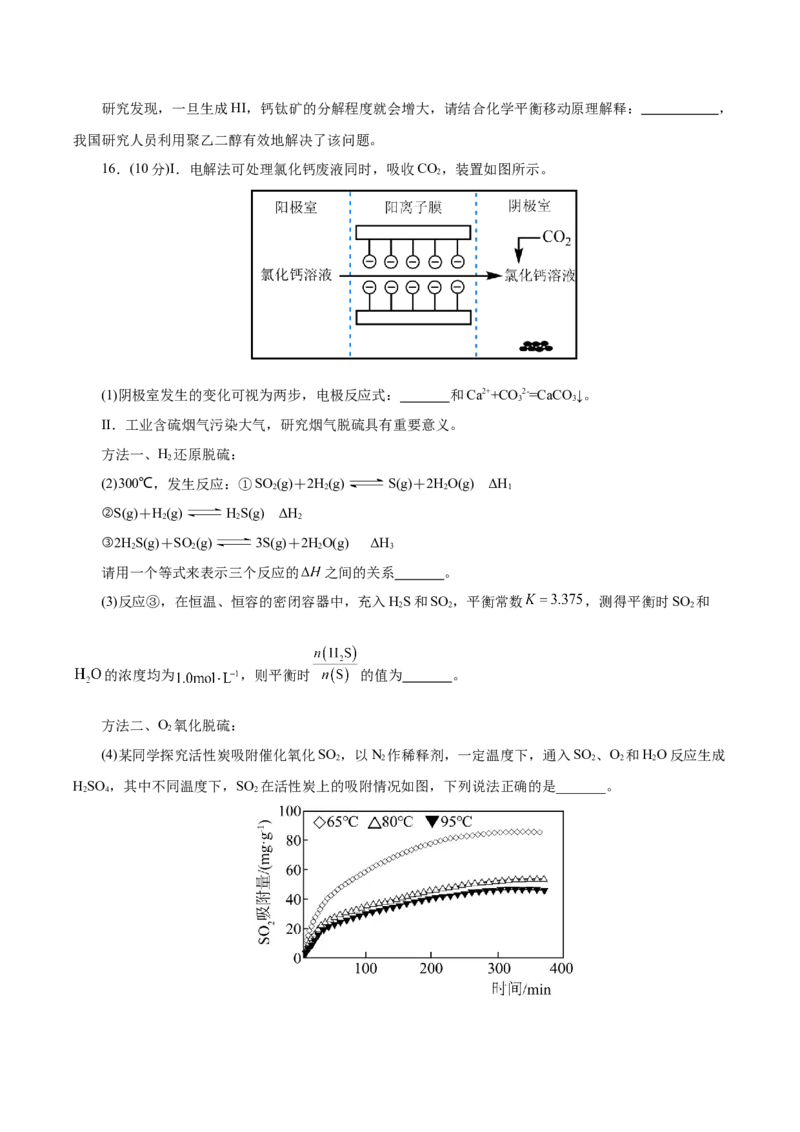
16.(10分)I.电解法可处理氯化钙废液同时,吸收CO,装置如图所示。
2
(1)阴极室发生的变化可视为两步,电极反应式: 和Ca2++CO 2-=CaCO↓。
3 3
II.工业含硫烟气污染大气,研究烟气脱硫具有重要意义。
方法一、H 还原脱硫:
2
(2)300℃,发生反应:①SO (g)+2H(g) S(g)+2HO(g) ΔH
2 2 2 1
②S(g)+H(g) HS(g) ΔH
2 2 2
③2HS(g)+SO (g) 3S(g)+2HO(g) ΔH
2 2 2 3
请用一个等式来表示三个反应的 之间的关系 。
(3)反应③,在恒温、恒容的密闭容器中,充入HS和SO ,平衡常数 ,测得平衡时SO 和
2 2 2
的浓度均为 ,则平衡时 的值为 。
方法二、O 氧化脱硫:
2
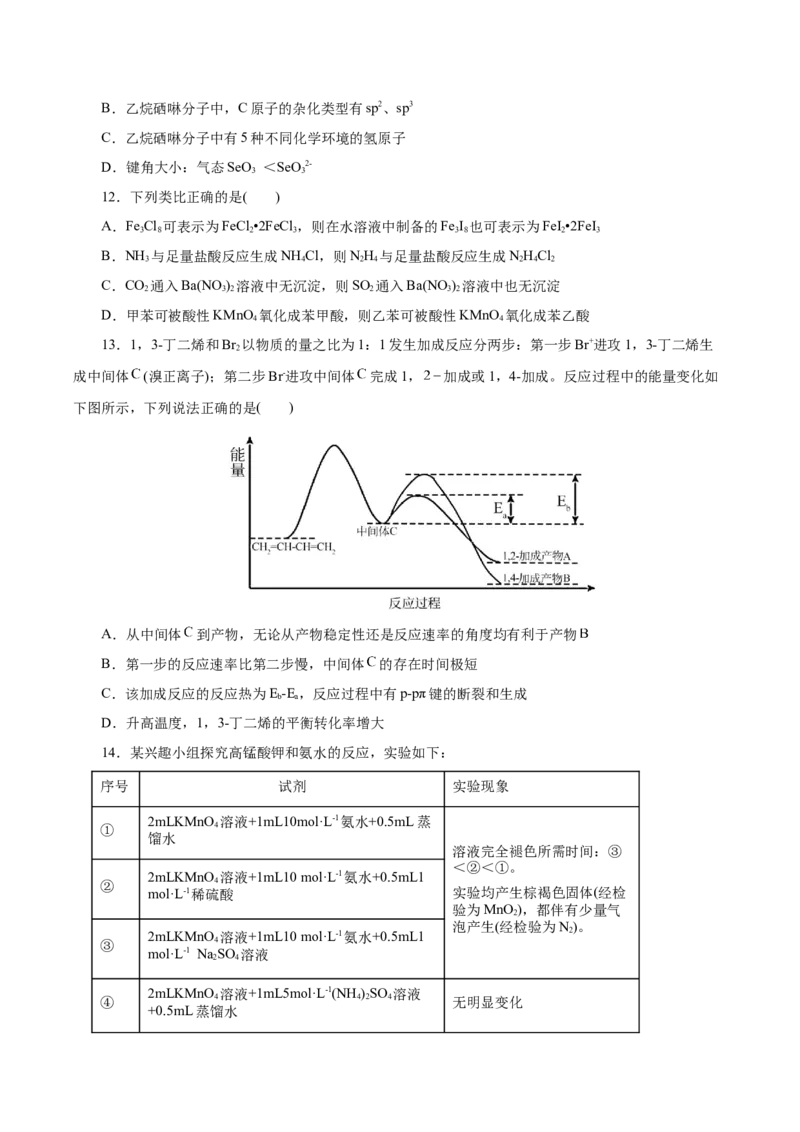
(4)某同学探究活性炭吸附催化氧化SO ,以N 作稀释剂,一定温度下,通入SO 、O 和HO反应生成
2 2 2 2 2
HSO ,其中不同温度下,SO 在活性炭上的吸附情况如图,下列说法正确的是_______。
2 4 2A.温度越低,SO 的吸附量越高,SO 氧化反应速率越快
2 2
B.已知:SO 的物理吸附过程能自发进行,可推断该过程是熵减、放热的过程,温度过高不利
2
C.原料中水蒸气的含量越大,脱硫速率一定越快
D.随着时间的推移,SO 吸附速率降低,可能是由于生成的HSO 占据了吸附位点没及时脱出导致
2 2 4
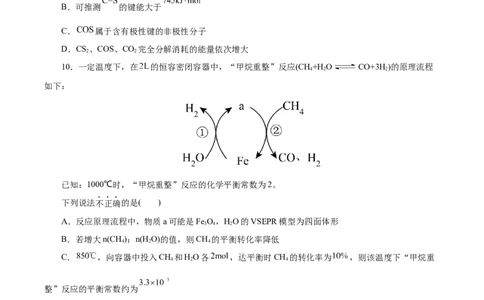
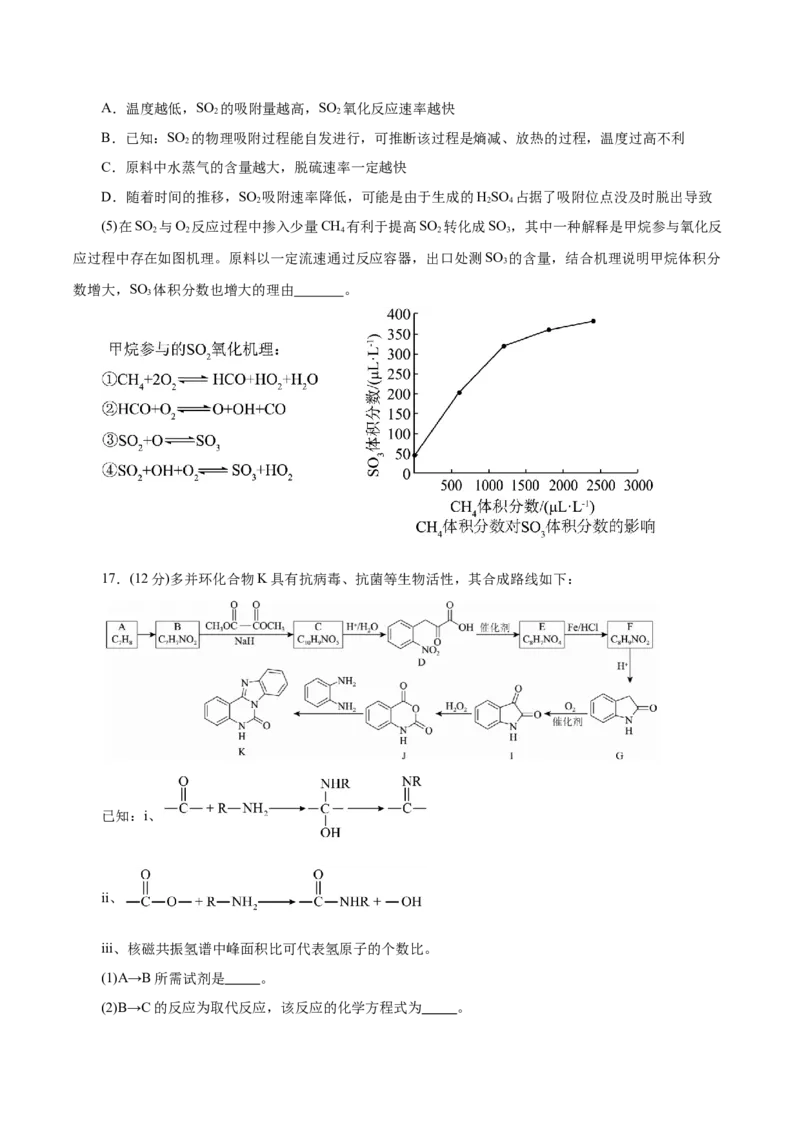
(5)在SO 与O 反应过程中掺入少量CH 有利于提高SO 转化成SO ,其中一种解释是甲烷参与氧化反
2 2 4 2 3
应过程中存在如图机理。原料以一定流速通过反应容器,出口处测SO 的含量,结合机理说明甲烷体积分
3
数增大,SO 体积分数也增大的理由 。
3
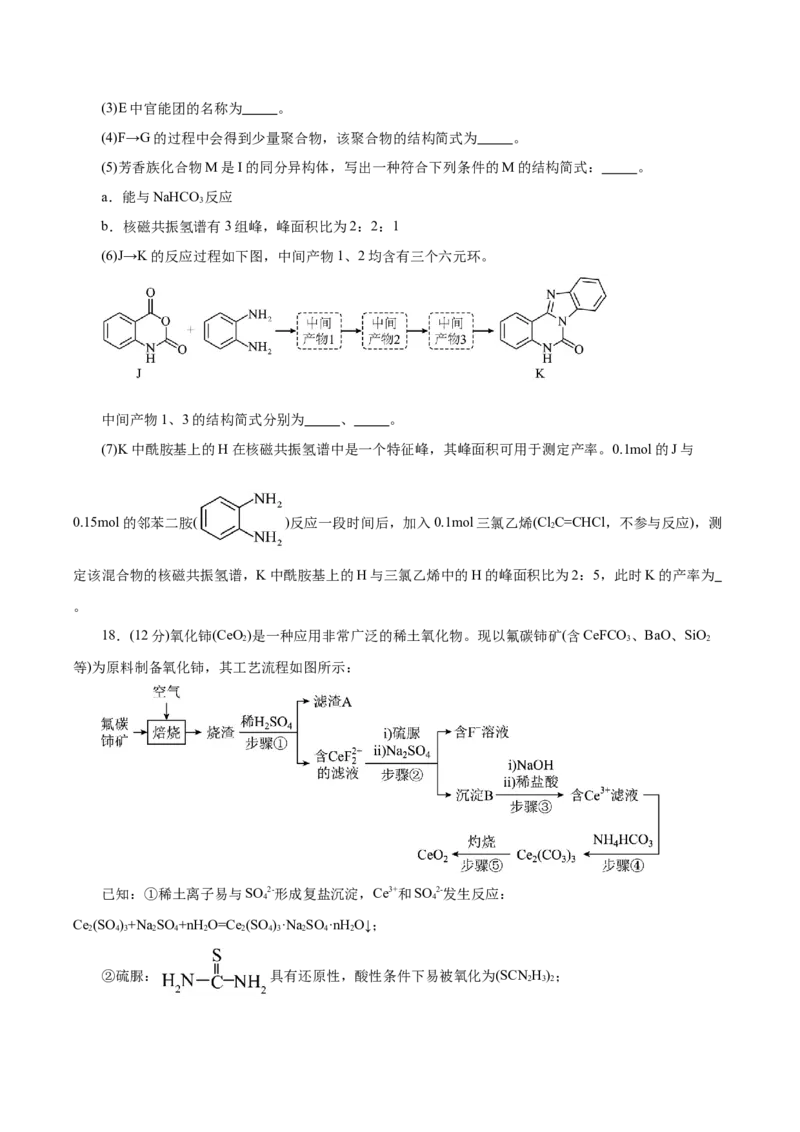
17.(12分)多并环化合物K具有抗病毒、抗菌等生物活性,其合成路线如下:
已知:i、
ii、
iii、核磁共振氢谱中峰面积比可代表氢原子的个数比。
(1)A→B所需试剂是 。
(2)B→C的反应为取代反应,该反应的化学方程式为 。(3)E中官能团的名称为 。
(4)F→G的过程中会得到少量聚合物,该聚合物的结构简式为 。
(5)芳香族化合物M是I的同分异构体,写出一种符合下列条件的M的结构简式: 。
a.能与NaHCO 反应
3
b.核磁共振氢谱有3组峰,峰面积比为2:2:1
(6)J→K的反应过程如下图,中间产物1、2均含有三个六元环。
中间产物1、3的结构简式分别为 、 。
(7)K中酰胺基上的H在核磁共振氢谱中是一个特征峰,其峰面积可用于测定产率。0.1mol的J与
0.15mol的邻苯二胺( )反应一段时间后,加入0.1mol三氯乙烯(Cl C=CHCl,不参与反应),测
2
定该混合物的核磁共振氢谱,K中酰胺基上的H与三氯乙烯中的H的峰面积比为2:5,此时K的产率为
。
18.(12分)氧化铈(CeO)是一种应用非常广泛的稀土氧化物。现以氟碳铈矿(含CeFCO、BaO、SiO
2 3 2
等)为原料制备氧化铈,其工艺流程如图所示:
已知:①稀土离子易与SO 2-形成复盐沉淀,Ce3+和SO 2-发生反应:
4 4
Ce (SO )+Na SO +nH O=Ce (SO )·Na SO ·nH O↓;
2 4 3 2 4 2 2 4 3 2 4 2
②硫脲: 具有还原性,酸性条件下易被氧化为(SCN H);
2 3 2③Ce3+在空气中易被氧化为Ce4+,两者均能形成氢氧化物沉淀;
④Ce (CO) 为白色粉末,难溶于水。
2 3 3
回答下列问题:
(1)滤渣A的主要成分是 (填写化学式)。
(2)在另一种生产工艺中,在氟碳铈矿矿石粉中加入碳酸氢钠同时通入氧气焙烧,焙烧得到NaF和
CeO 两种固体以及两种高温下的气态物质,请写出焙烧过程中相应的化学方程式 。
2
(3)加入硫脲的目的是将CeF 2+还原为Ce3+,反应的离子方程式为 。
2
(4)步骤③加入盐酸后,通常还需加入另一种化学试剂X,根据题中信息推测,加入X的作用为 。
(5)下列关于步骤④的说法正确的是_____(填字母)。
A.过滤后的滤液中仍含有较多Ce3+,需要将滤液循环以提高产率
B.可以用NaCO 溶液代替NH HCO 溶液,不影响产品纯度
2 3 4 3
C.过滤时选择减压过滤能够大大提高过滤效率
D.该步骤发生的反应是2Ce3++6 HCO -=Ce (CO)↓+3CO ↑+3H O
3 2 3 3 2 2
(6)若常温下,K (H CO)=5.0×10−11,K [Ce (CO)]=1.0×10−28,Ce3+恰好沉淀完全
a2 2 3 sp 2 3 3
c(Ce3+)=1.0×10−5mol∙L−1,此时测得溶液的pH=5,则溶液中c(HCO -)= mol∙L−1。
3
19.(14分)以NaSO 溶液和不同金属的硫酸盐溶液作为实验对象,探究盐的性质和盐溶液间反应的多
2 3
样性。
试剂
实验 现象
滴管 试管
饱和Ag SO 溶液 Ⅰ.产生白色沉淀
2 4
0.2mol·L-1CuSO Ⅱ.溶液变绿,继续滴加产生棕黄色沉淀
0.2mol·L-1NaSO 4
2 3
溶液
0.1mol·L-1Al (SO ) 溶液 Ⅲ.开始无明显变化,继续滴加产生白色沉淀
2 4 3
(1)经验检,现象Ⅰ中的白色沉淀是Ag SO 。用离子方程式解释现象Ⅰ: 。
2 3
(2)经检验,现象Ⅱ的棕黄色沉淀中不含SO 2-,含有Cu+、Cu2+和SO 2-。
4 3
已知:Cu+ Cu+Cu2+,Cu2+ CuI↓(白色)+I 。
2
①用稀硫酸证实沉淀中含有Cu+的实验现象是 。
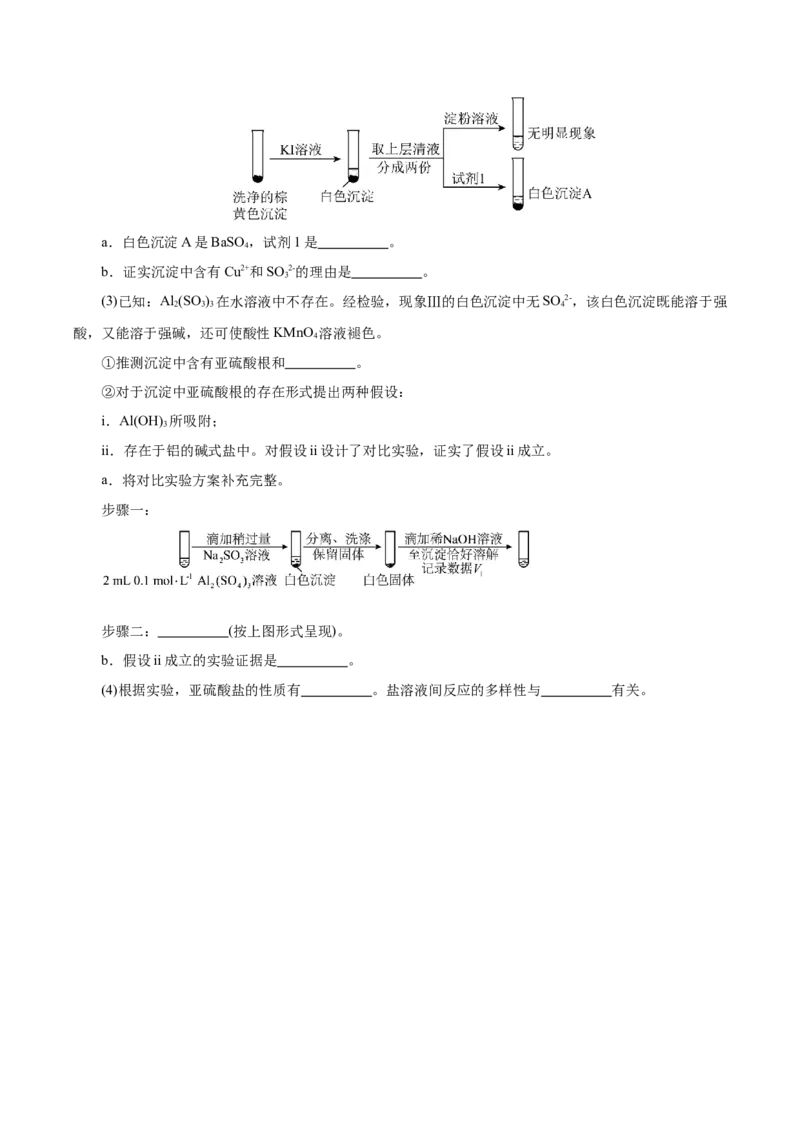
②通过下列实验证实,沉淀中含有Cu2+和SO 2-。
3a.白色沉淀A是BaSO,试剂1是 。
4
b.证实沉淀中含有Cu2+和SO 2-的理由是 。
3
(3)已知:Al (SO ) 在水溶液中不存在。经检验,现象Ⅲ的白色沉淀中无SO 2-,该白色沉淀既能溶于强
2 3 3 4
酸,又能溶于强碱,还可使酸性KMnO 溶液褪色。
4
①推测沉淀中含有亚硫酸根和 。
②对于沉淀中亚硫酸根的存在形式提出两种假设:
i.Al(OH) 所吸附;
3
ii.存在于铝的碱式盐中。对假设ii设计了对比实验,证实了假设ii成立。
a.将对比实验方案补充完整。
步骤一:
步骤二: (按上图形式呈现)。
b.假设ii成立的实验证据是 。
(4)根据实验,亚硫酸盐的性质有 。盐溶液间反应的多样性与 有关。