文档内容
绝密★启用前
2025 年高考考前信息必刷卷 04(云南专用)
化 学
考情速递
高考·新动向:2025年云南八省联考化学科目考试就是云南省自主命题的体现,单项选择题本大题有16
小题,每小题3分,共48分;非选择题本大题有4小题,每小题13分,共52分。新高考下的化学试
卷在结构上可能会与其他新高考省份有更多的一致性或者相互借鉴之处,朝着体现高考公平性、普适
性和人才选拔准确性的方向完善结构设置。
高考·新考法:2025年高考化学题型向着更加综合化、融合多知识模块方向发展,这对于考生来说首先
在知识整合方面带来了巨大挑战。化学试题会打破化学学科内各知识板块的界限,如无机化学、有机
化学、物理化学等板块不再孤立考查。在一道题目中可能同时融合多方面知识进行综合考查。。
高考·新情境:新高考体系基本形成,云南从老高考转为新高考。这使得化学学科在整个高考体系中的
定位发生了变化,其教学方式和学生的学习策略也需要相应调整。例如,在新高考模式下,化学学科
的学习可能更注重与其他学科的联系,以及在实际生活中的应用。学生需要培养综合运用知识的能力,
而不仅仅是对化学知识的死记硬背。
命题·大预测:2025年高考人数可能增多,考生增多意味着竞争加剧,在化学学科上也不例外。学生需
要更加努力提高化学成绩,以在众多考生中脱颖而出。这就要求学生在日常学习中提高学习效率,注
重知识的掌握和应用能力的提升。云南省在借鉴其他省份新高考经验的过程中,可能会在题型的创新、
题目情境的设置等方面有所借鉴。比如一些先行新高考改革省份中出现的开放性化学试题(如实验方案
设计与评价的开放性问题)、以真实科研成果或工业生产流程为背景的综合应用题等题型,有可能会逐
渐出现在云南高考化学试卷中。这有助于选拔具有创新思维和实际应用能力的学生,适应现代社会对
人才的需求。
(考试时间:75分钟 试卷满分:100分)
注意事项:
1.答卷前,考生务必将自己的姓名、考生号等填写在答题卡和试卷指定位置上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡对应题目的答案标号涂黑。如需改动,用橡
皮擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上。写在本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H-1 C-12 N-14 O-16 F-19 Na-23 Mg-24 Al-27 S-32 Cl-35.5
K-39 Ca-40 V-51 Mn-55 Fe-56 Cu-64 Zn-65 As-75 Br-80 Y-89 I-127 Ag-108 Ba-137
W-184
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一项符合题目要求。
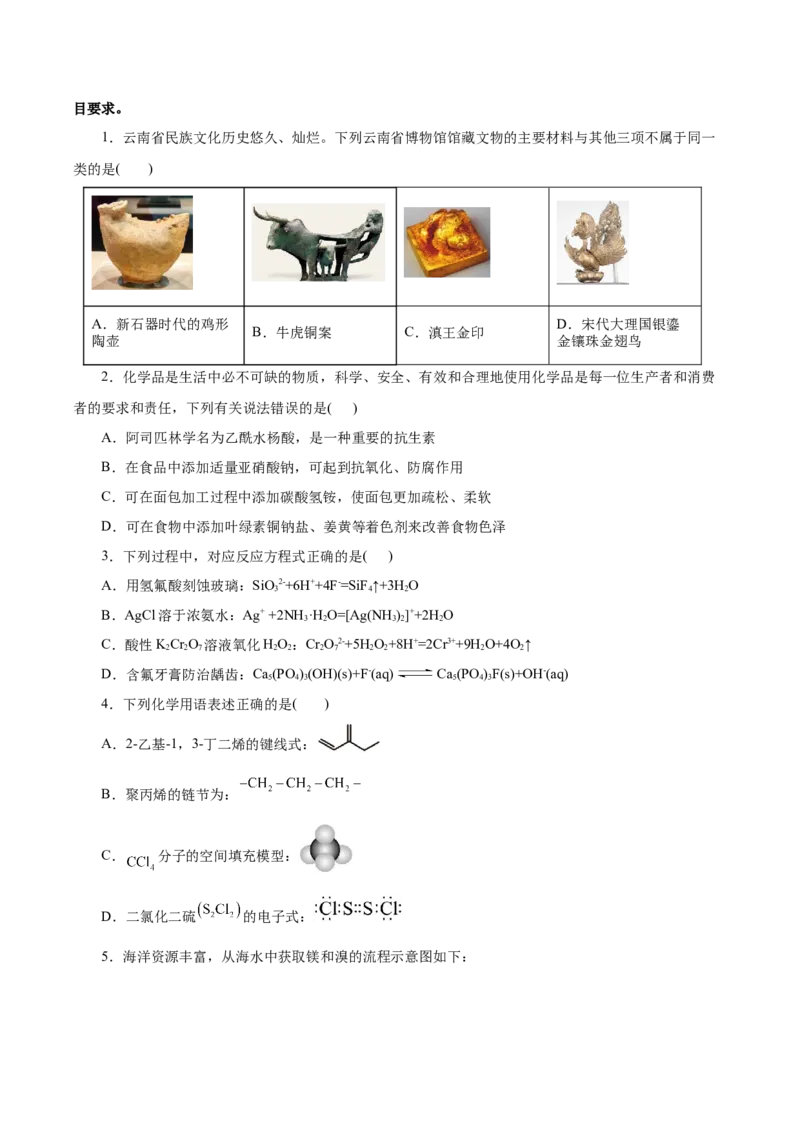
1.云南省民族文化历史悠久、灿烂。下列云南省博物馆馆藏文物的主要材料与其他三项不属于同一
类的是( )
A.新石器时代的鸡形 D.宋代大理国银鎏
B.牛虎铜案 C.滇王金印
陶壶 金镶珠金翅鸟
2.化学品是生活中必不可缺的物质,科学、安全、有效和合理地使用化学品是每一位生产者和消费
者的要求和责任,下列有关说法错误的是( )
A.阿司匹林学名为乙酰水杨酸,是一种重要的抗生素
B.在食品中添加适量亚硝酸钠,可起到抗氧化、防腐作用
C.可在面包加工过程中添加碳酸氢铵,使面包更加疏松、柔软
D.可在食物中添加叶绿素铜钠盐、姜黄等着色剂来改善食物色泽
3.下列过程中,对应反应方程式正确的是( )
A.用氢氟酸刻蚀玻璃:SiO2-+6H++4F-=SiF ↑+3H O
3 4 2
B.AgCl溶于浓氨水:Ag+ +2NH ·H O=[Ag(NH )]++2H O
3 2 3 2 2
C.酸性KCr O 溶液氧化HO:Cr O2-+5H O+8H+=2Cr3++9H O+4O↑
2 2 7 2 2 2 7 2 2 2 2
D.含氟牙膏防治龋齿:Ca (PO )(OH)(s)+F-(aq) Ca (PO )F(s)+OH-(aq)
5 4 3 5 4 3
4.下列化学用语表述正确的是( )
A.2-乙基-1,3-丁二烯的键线式:
B.聚丙烯的链节为:
C. 分子的空间填充模型:
D.二氯化二硫 的电子式:
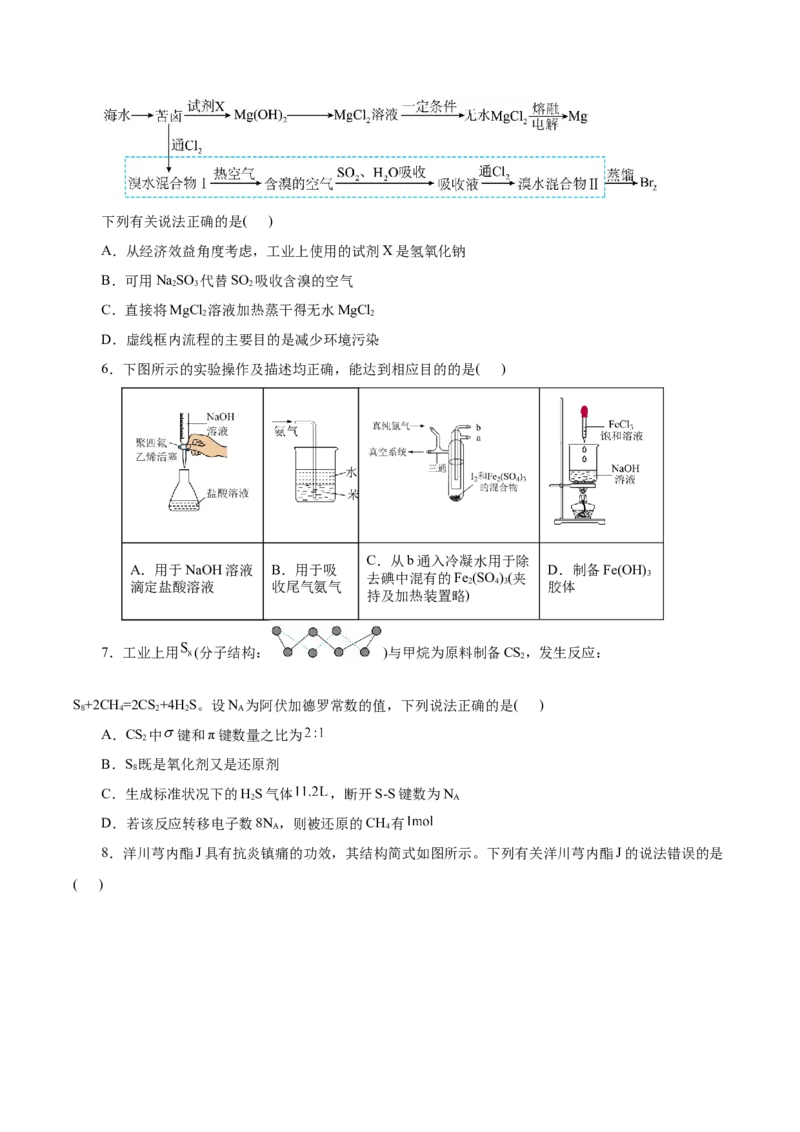
5.海洋资源丰富,从海水中获取镁和溴的流程示意图如下:下列有关说法正确的是( )
A.从经济效益角度考虑,工业上使用的试剂X是氢氧化钠
B.可用NaSO 代替SO 吸收含溴的空气
2 3 2
C.直接将MgCl 溶液加热蒸干得无水MgCl
2 2
D.虚线框内流程的主要目的是减少环境污染
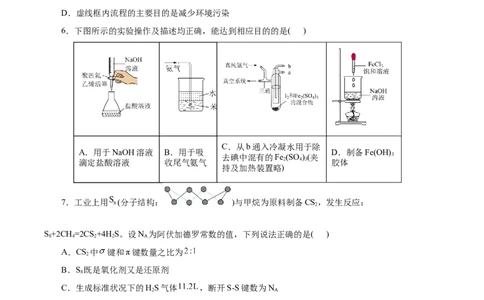
6.下图所示的实验操作及描述均正确,能达到相应目的的是( )
C.从b通入冷凝水用于除
A.用于NaOH溶液 B.用于吸 D.制备Fe(OH)
去碘中混有的Fe (SO )(夹 3
滴定盐酸溶液 收尾气氨气 2 4 3 胶体
持及加热装置略)
7.工业上用 (分子结构: )与甲烷为原料制备CS,发生反应:
2
S+2CH =2CS +4H S。设N 为阿伏加德罗常数的值,下列说法正确的是( )
8 4 2 2 A
A.CS 中 键和π键数量之比为
2
B.S 既是氧化剂又是还原剂
8
C.生成标准状况下的HS气体 ,断开S-S键数为N
2 A
D.若该反应转移电子数8N ,则被还原的CH 有
A 4
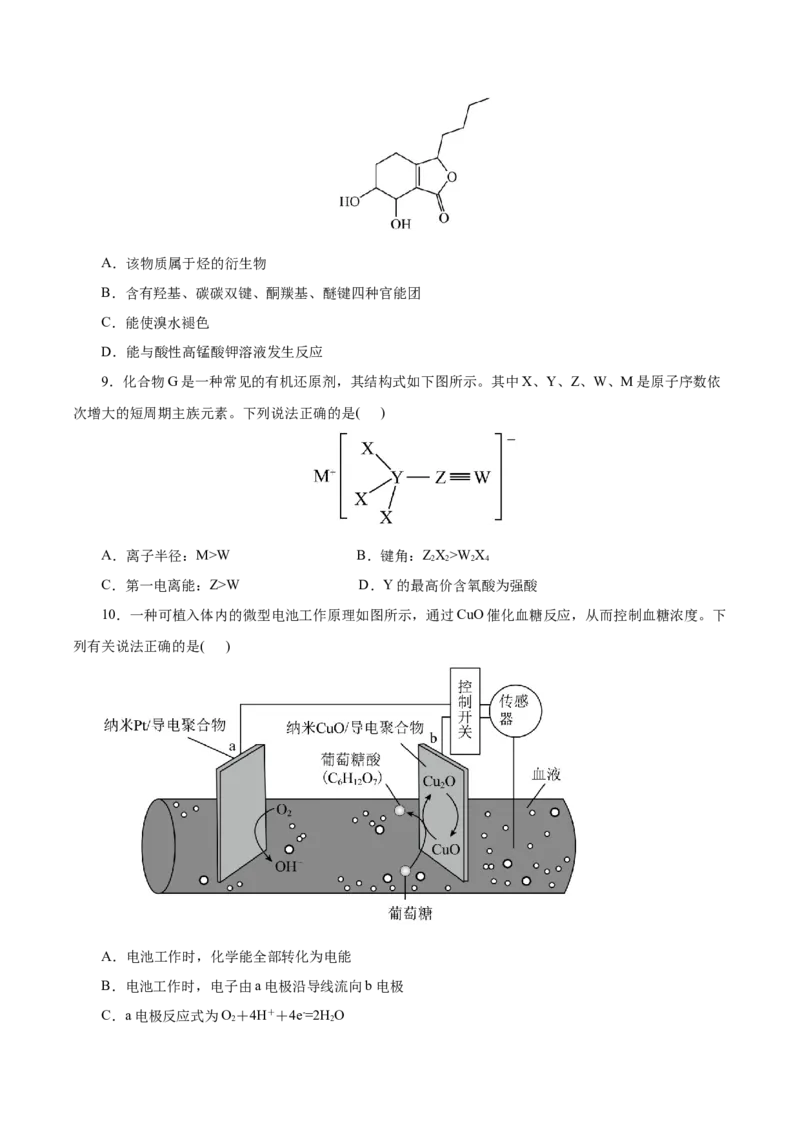
8.洋川芎内酯J具有抗炎镇痛的功效,其结构简式如图所示。下列有关洋川芎内酯J的说法错误的是
( )A.该物质属于烃的衍生物
B.含有羟基、碳碳双键、酮羰基、醚键四种官能团
C.能使溴水褪色
D.能与酸性高锰酸钾溶液发生反应
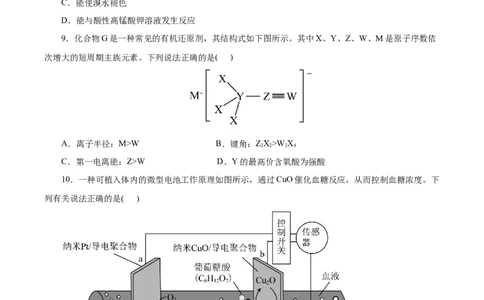
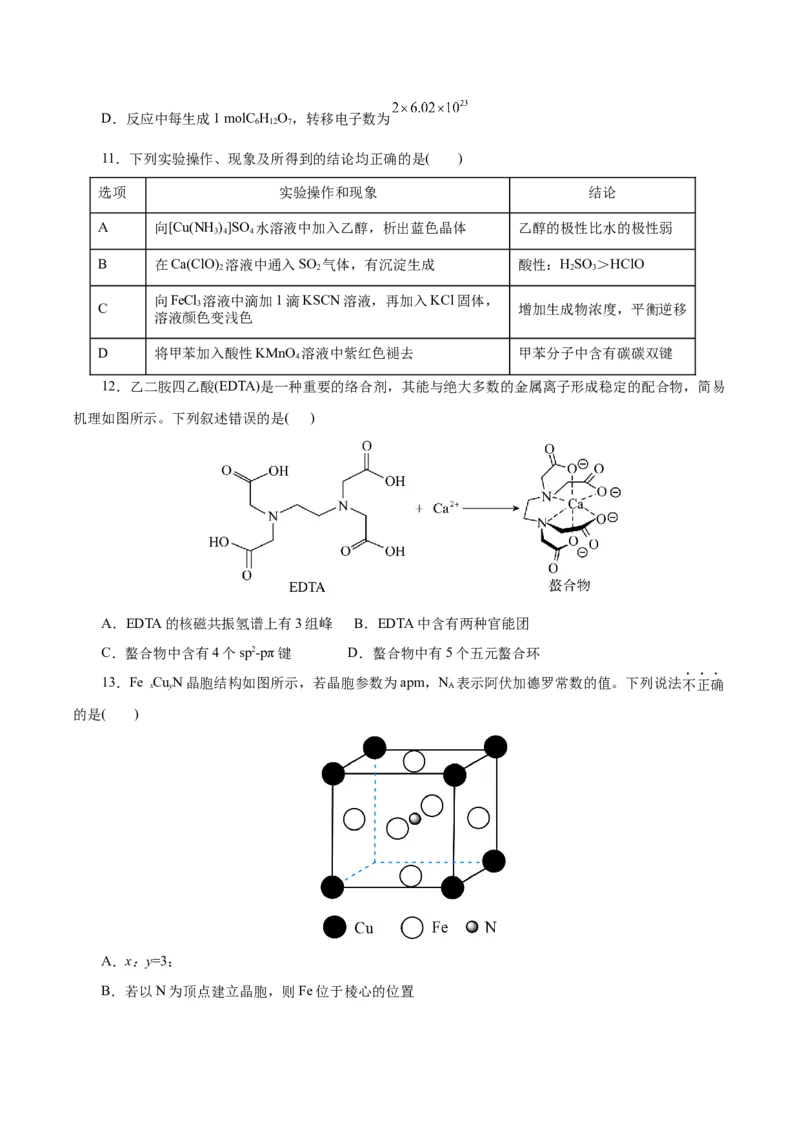
9.化合物G是一种常见的有机还原剂,其结构式如下图所示。其中X、Y、Z、W、M是原子序数依
次增大的短周期主族元素。下列说法正确的是( )
A.离子半径:M>W B.键角:ZX>WX
2 2 2 4
C.第一电离能:Z>W D.Y的最高价含氧酸为强酸
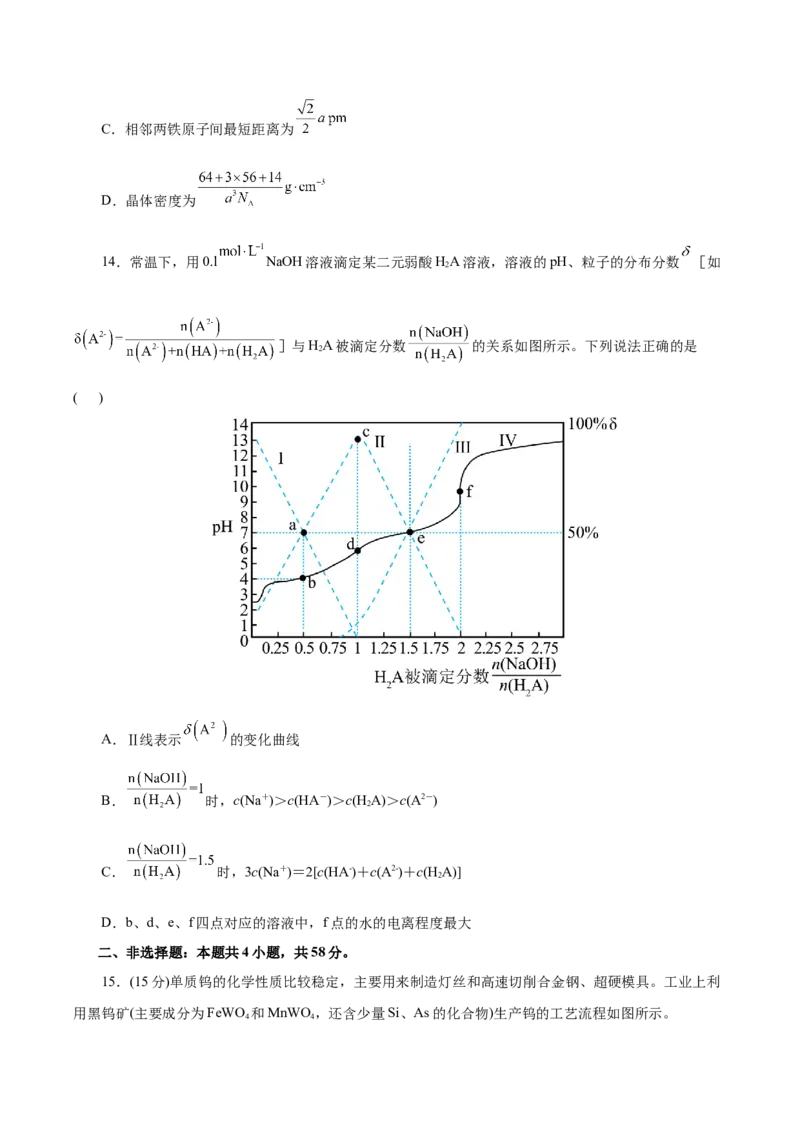
10.一种可植入体内的微型电池工作原理如图所示,通过CuO催化血糖反应,从而控制血糖浓度。下
列有关说法正确的是( )
A.电池工作时,化学能全部转化为电能
B.电池工作时,电子由a电极沿导线流向b电极
C.a电极反应式为O+4H++4e-=2H O
2 2D.反应中每生成1 molC H O,转移电子数为
6 12 7
11.下列实验操作、现象及所得到的结论均正确的是( )
选项 实验操作和现象 结论
A 向[Cu(NH )]SO 水溶液中加入乙醇,析出蓝色晶体 乙醇的极性比水的极性弱
3 4 4
B 在Ca(ClO) 溶液中通入SO 气体,有沉淀生成 酸性:HSO >HClO
2 2 2 3
向FeCl 溶液中滴加1滴KSCN溶液,再加入KCl固体,
C 3 增加生成物浓度,平衡逆移
溶液颜色变浅色
D 将甲苯加入酸性KMnO 溶液中紫红色褪去 甲苯分子中含有碳碳双键
4
12.乙二胺四乙酸(EDTA)是一种重要的络合剂,其能与绝大多数的金属离子形成稳定的配合物,简易
机理如图所示。下列叙述错误的是( )
A.EDTA的核磁共振氢谱上有3组峰 B.EDTA中含有两种官能团
C.螯合物中含有4个sp2-pπ键 D.螯合物中有5个五元螯合环
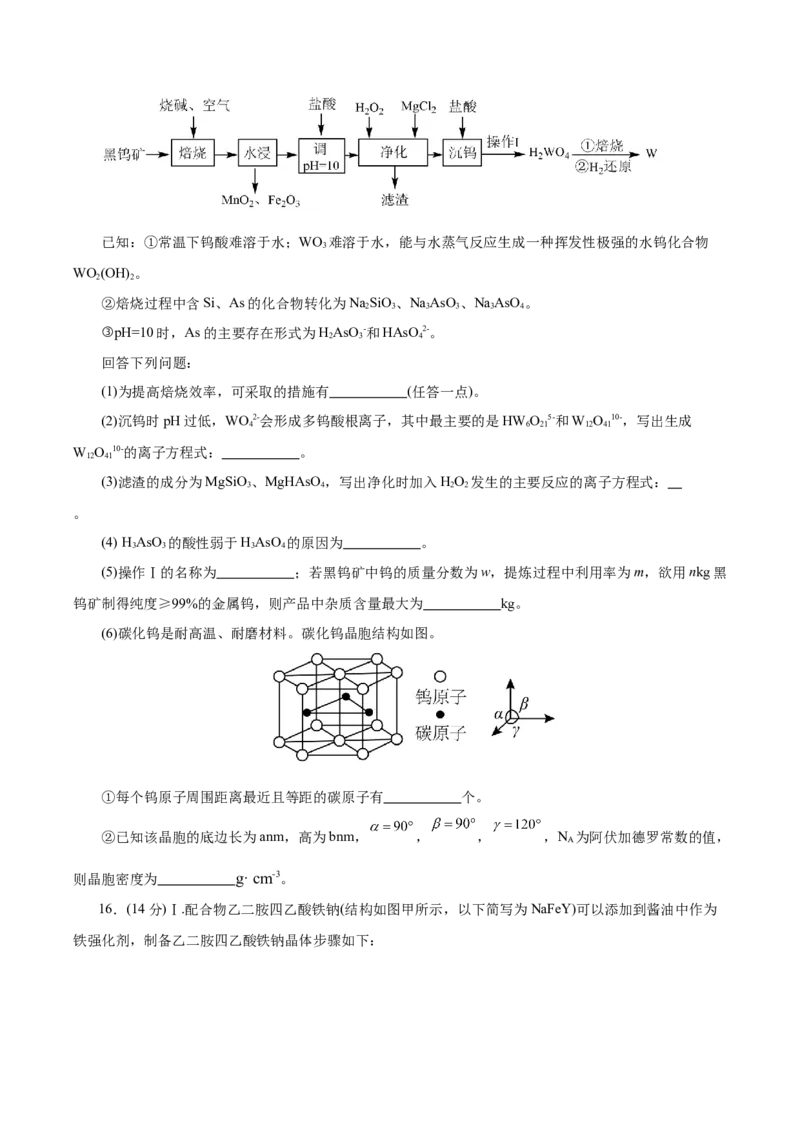
13.Fe CuN晶胞结构如图所示,若晶胞参数为apm,N 表示阿伏加德罗常数的值。下列说法不正确
x y A
的是( )
A.x:y=3:
B.若以N为顶点建立晶胞,则Fe位于棱心的位置C.相邻两铁原子间最短距离为
D.晶体密度为
14.常温下,用0.l NaOH溶液滴定某二元弱酸HA溶液,溶液的pH、粒子的分布分数 [如
2
]与HA被滴定分数 的关系如图所示。下列说法正确的是
2
( )
A.Ⅱ线表示 的变化曲线
B. 时,c(Na+)>c(HA-)>c(HA)>c(A2-)
2
C. 时,3cNa+=2[cHA-+cA2-+cHA]
2
D.b、d、e、f四点对应的溶液中,f点的水的电离程度最大
二、非选择题:本题共4小题,共58分。
15.(15分)单质钨的化学性质比较稳定,主要用来制造灯丝和高速切削合金钢、超硬模具。工业上利
用黑钨矿(主要成分为FeWO 和MnWO,还含少量Si、As的化合物)生产钨的工艺流程如图所示。
4 4已知:①常温下钨酸难溶于水;WO 难溶于水,能与水蒸气反应生成一种挥发性极强的水钨化合物
3
WO(OH) 。
2 2
②焙烧过程中含Si、As的化合物转化为NaSiO、NaAsO 、NaAsO 。
2 3 3 3 3 4
③pH=10时,As的主要存在形式为HAsO -和HAsO2-。
2 3 4
回答下列问题:
(1)为提高焙烧效率,可采取的措施有 (任答一点)。
(2)沉钨时pH过低,WO2-会形成多钨酸根离子,其中最主要的是HWO 5-和W O 10-,写出生成
4 6 21 12 41
W O 10-的离子方程式: 。
12 41
(3)滤渣的成分为MgSiO 、MgHAsO,写出净化时加入HO 发生的主要反应的离子方程式:
3 4 2 2
。
(4)HAsO 的酸性弱于HAsO 的原因为 。
3 3 3 4
(5)操作Ⅰ的名称为 ;若黑钨矿中钨的质量分数为w,提炼过程中利用率为m,欲用nkg黑
钨矿制得纯度≥99%的金属钨,则产品中杂质含量最大为 kg。
(6)碳化钨是耐高温、耐磨材料。碳化钨晶胞结构如图。
①每个钨原子周围距离最近且等距的碳原子有 个。
②已知该晶胞的底边长为anm,高为bnm, , , ,N 为阿伏加德罗常数的值,
A
则晶胞密度为 g· cm-3。
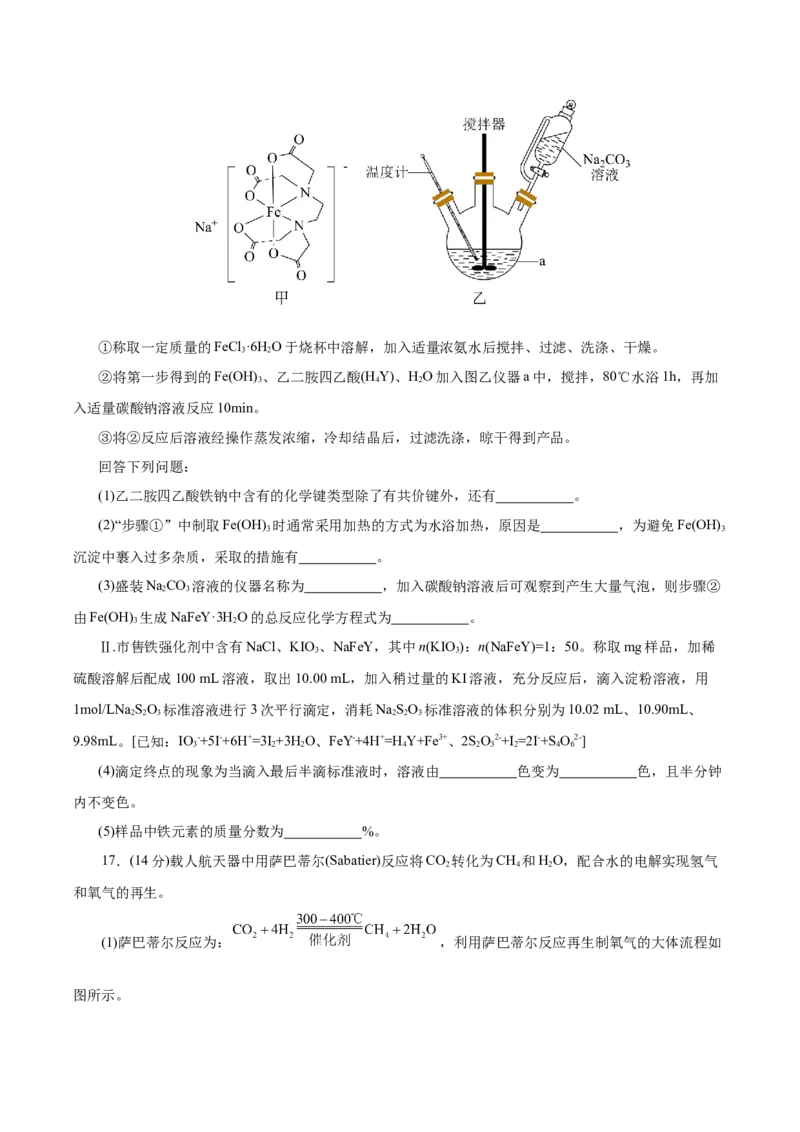
16.(14分)Ⅰ.配合物乙二胺四乙酸铁钠(结构如图甲所示,以下简写为NaFeY)可以添加到酱油中作为
铁强化剂,制备乙二胺四乙酸铁钠晶体步骤如下:①称取一定质量的FeCl ·6H O于烧杯中溶解,加入适量浓氨水后搅拌、过滤、洗涤、干燥。
3 2
②将第一步得到的Fe(OH) 、乙二胺四乙酸(H Y)、HO加入图乙仪器a中,搅拌,80℃水浴1h,再加
3 4 2
入适量碳酸钠溶液反应10min。
③将②反应后溶液经操作蒸发浓缩,冷却结晶后,过滤洗涤,晾干得到产品。
回答下列问题:
(1)乙二胺四乙酸铁钠中含有的化学键类型除了有共价键外,还有 。
(2)“步骤①”中制取Fe(OH) 时通常采用加热的方式为水浴加热,原因是 ,为避免Fe(OH)
3 3
沉淀中裹入过多杂质,采取的措施有 。
(3)盛装NaCO 溶液的仪器名称为 ,加入碳酸钠溶液后可观察到产生大量气泡,则步骤②
2 3
由Fe(OH) 生成NaFeY·3H O的总反应化学方程式为 。
3 2
Ⅱ.市售铁强化剂中含有NaCl、KIO 、NaFeY,其中n(KIO ):n(NaFeY)=1:50。称取mg样品,加稀
3 3
硫酸溶解后配成100 mL溶液,取出10.00 mL,加入稍过量的KI溶液,充分反应后,滴入淀粉溶液,用
1mol/LNa SO 标准溶液进行3次平行滴定,消耗NaSO 标准溶液的体积分别为10.02 mL、10.90mL、
2 2 3 2 2 3
9.98mL。[已知:IO -+5I-+6H+=3I +3H O、FeY-+4H+=H Y+Fe3+、2SO2-+I =2I-+S O2-]
3 2 2 4 2 3 2 4 6
(4)滴定终点的现象为当滴入最后半滴标准液时,溶液由 色变为 色,且半分钟
内不变色。
(5)样品中铁元素的质量分数为 %。
17.(14分)载人航天器中用萨巴蒂尔(Sabatier)反应将CO 转化为CH 和HO,配合水的电解实现氢气
2 4 2
和氧气的再生。
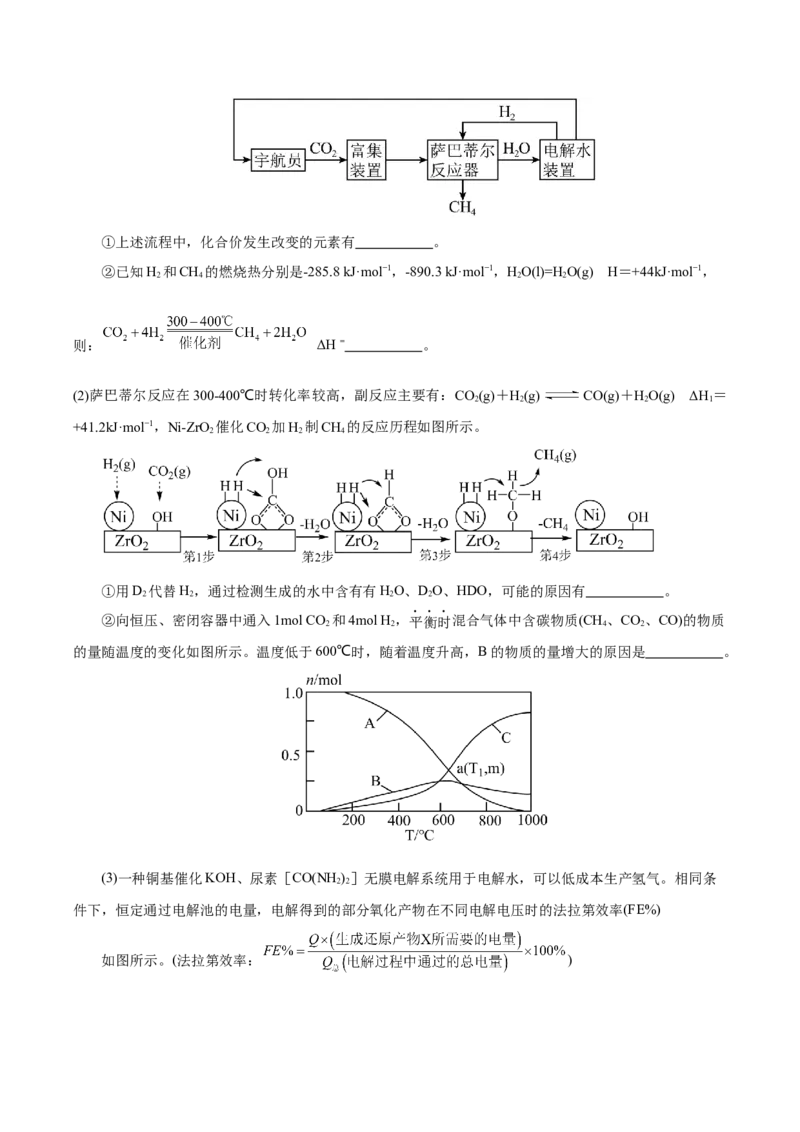
(1)萨巴蒂尔反应为: ,利用萨巴蒂尔反应再生制氧气的大体流程如
图所示。①上述流程中,化合价发生改变的元素有 。
②已知H 和CH 的燃烧热分别是-285.8 kJ·mol−1,-890.3 kJ·mol−1,HO(l)=HO(g) H=+44kJ·mol−1,
2 4 2 2
则: ΔH = 。
(2)萨巴蒂尔反应在300-400℃时转化率较高,副反应主要有:CO(g)+H(g) CO(g)+HO(g) ΔH =
2 2 2 1
+41.2kJ·mol−1,Ni-ZrO 催化CO 加H 制CH 的反应历程如图所示。
2 2 2 4
①用D 代替H,通过检测生成的水中含有有HO、DO、HDO,可能的原因有 。
2 2 2 2
②向恒压、密闭容器中通入1mol CO 和4mol H,平衡时混合气体中含碳物质(CH、CO、CO)的物质
2 2 4 2
的量随温度的变化如图所示。温度低于600℃时,随着温度升高,B的物质的量增大的原因是 。
(3)一种铜基催化KOH、尿素[CO(NH)]无膜电解系统用于电解水,可以低成本生产氢气。相同条
2 2
件下,恒定通过电解池的电量,电解得到的部分氧化产物在不同电解电压时的法拉第效率(FE%)
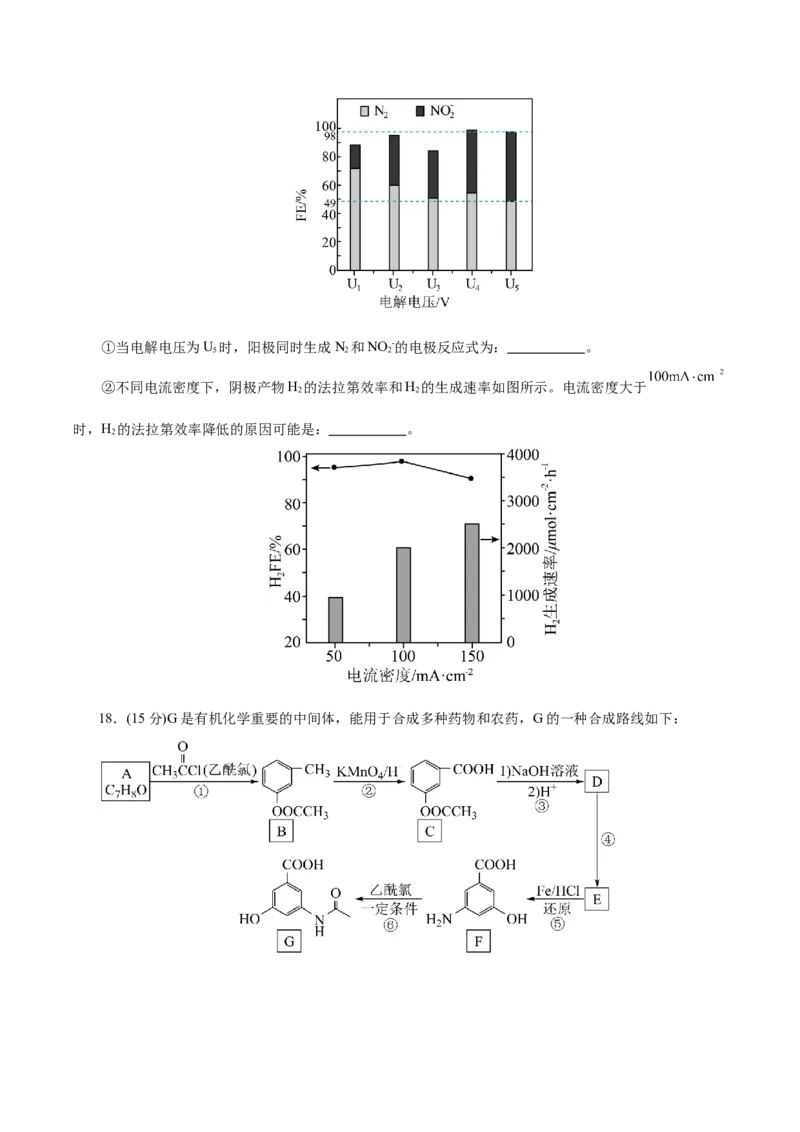
如图所示。(法拉第效率: )①当电解电压为U 时,阳极同时生成N 和NO -的电极反应式为: 。
5 2 2
②不同电流密度下,阴极产物H 的法拉第效率和H 的生成速率如图所示。电流密度大于
2 2
时,H 的法拉第效率降低的原因可能是: 。
2
18.(15分)G是有机化学重要的中间体,能用于合成多种药物和农药,G的一种合成路线如下:已知: (呈碱性,易被氧化)。
回答下列问题:
(1)A→B除生成B外,还有HCl生成,则A的名称为 。
(2)C中官能团名称为 。
(3)⑥的反应类型为 。
(4)设置反应①的目的是 。
(5)D的结构简式为 ;写出D→E反应的化学方程式: 。
(6)M是G的一种同分异构体,满足下列条件的M有 种。
①分子结构中含苯环,且环上有四个支链
②1mol该物质与足量NaHCO 反应生成2molCO
3 2
写出其中环上一氯代物只有一种的同分异构体的结构简式: (任写一种)。