文档内容
微专题31 元素推断的破解
1.(2023·全国·统考高考真题)一种矿物由短周期元素W、X、Y组成,溶于稀盐酸有无色无味气体生成。
W、X、Y原子序数依次增大。简单离子 与 具有相同的电子结构。下列叙述正确的是
A.X的常见化合价有 、 B.原子半径大小为
C.YX的水合物具有两性 D.W单质只有4种同素异形体
2.(2023·全国·统考高考真题)W、X、Y、Z为短周期主族元素,原子序数依次增大,最外层电子数之和
为19。Y的最外层电子数与其K层电子数相等,WX 是形成酸雨的物质之一。下列说法正确的是
2
A.原子半径: B.简单氢化物的沸点:
C. 与 可形成离子化合物 D. 的最高价含氧酸是弱酸
3.(2023·浙江·高考真题)X、Y、Z、M、Q五种短周期元素,原子序数依次增大。X的 轨道全充满,Y
的s能级电子数量是p能级的两倍,M是地壳中含量最多的元素,Q是纯碱中的一种元素。下列说法不正
确的是
A.电负性:
B.最高正价:
C.Q与M的化合物中可能含有非极性共价键D.最高价氧化物对应水化物的酸性:
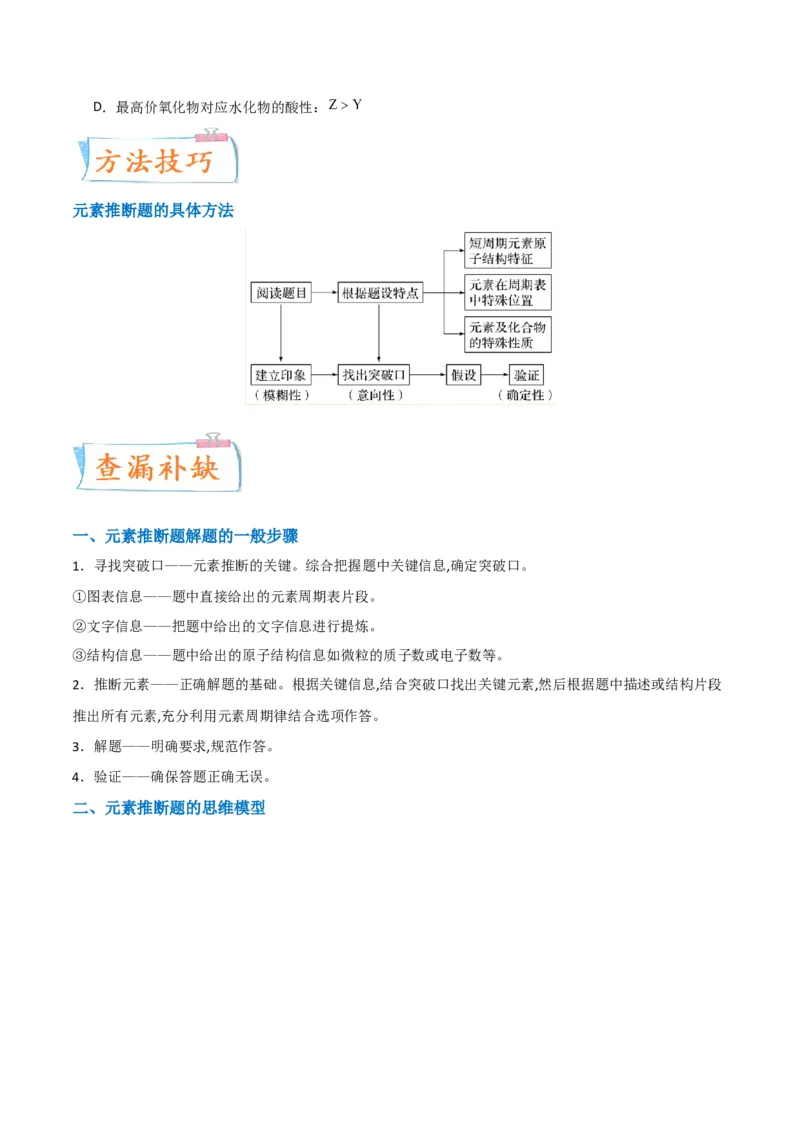
元素推断题的具体方法
一、元素推断题解题的一般步骤
1.寻找突破口——元素推断的关键。综合把握题中关键信息,确定突破口。
①图表信息——题中直接给出的元素周期表片段。
②文字信息——把题中给出的文字信息进行提炼。
③结构信息——题中给出的原子结构信息如微粒的质子数或电子数等。
2.推断元素——正确解题的基础。根据关键信息,结合突破口找出关键元素,然后根据题中描述或结构片段
推出所有元素,充分利用元素周期律结合选项作答。
3.解题——明确要求,规范作答。
4.验证——确保答题正确无误。
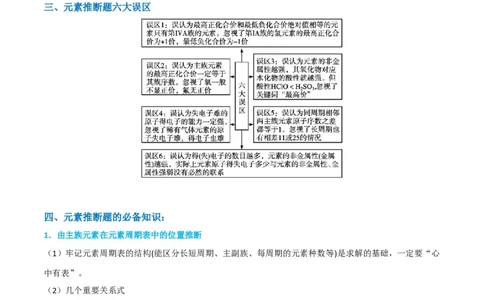
二、元素推断题的思维模型三、元素推断题六大误区
四、元素推断题的必备知识:
1.由主族元素在元素周期表中的位置推断
(1)牢记元素周期表的结构(能区分长短周期、主副族、每周期的元素种数等)是求解的基础,一定要“心
中有表”。
(2)几个重要关系式
①原子核外电子层数=周期数;
②主族序数=最外层电子数=最高正价=8-|最低负价|;
③|最高正价|-|最低负价|=0、2、4、6的主族序数依次为第Ⅳ族、第Ⅴ族、第Ⅵ族、第Ⅶ族。
(3)熟悉主族元素在元素周期表中的特殊位置
①族序数等于周期数的元素:H、Be、Al。
②族序数等于周期数2倍的元素:C、S。
③族序数等于周期数3倍的元素:O。④周期数是族序数2倍的元素:Li、Ca。
⑤周期数是族序数3倍的元素:Na、Ba。
⑥最高正价与最低负价代数和为零的短周期元素:H、C、Si。
⑦最高正价是最低负价绝对值3倍的短周期元素:S。
⑧除H外,原子半径最小的元素:F。
⑨最高正价不等于族序数的短周期元素:O(F无正价)。
2.由元素原子的核外电子排布推断
(1)最外层有1个电子的元素:H、Li、Na、K。
(2)最外层电子数等于次外层电子数的元素:Be、Ar。
(3)最外层电子数是次外层电子数2倍的元素:C;最外层电子数是次外层电子数3倍的元素:O;最外
层电子数是次外层电子数4倍的元素:Ne。
(4)最外层电子数是内层电子数总数一半的元素:Li、P。
(5)次外层电子数是最外层电子数2倍的元素:Li、Si。
(6)次外层电子数是其他各层电子总数2倍的元素:Li、Mg。
(7)次外层电子数与其他各层电子总数相等的元素:Be、S。
(8)电子层数与最外层电子数相等的元素:H、Be、Al。
3.由元素及其化合物的特性推断
(1)形成化合物种类最多的元素或单质是自然界中硬度最大的物质的元素或气态氢化物中氢的质量分数
最大的元素:C。
(2)空气中含量最多的元素或气态氢化物的水溶液呈碱性的元素:N。
(3)地壳中含量最多的元素或同周期中气态氢化物的沸点最高的元素或氢化物在通常情况下呈液态的元
素:O。
(4)地壳中含量最多的金属元素:Al。
(5)最高价氧化物及其对应的水化物既能与强酸反应,又能与强碱反应的元素:Be、Al。
(6)最活泼的非金属元素或无正价的元素或无含氧酸的非金属元素或无氧酸(气态氢化物)可腐蚀玻璃的元
素或气态氢化物最稳定的元素或阴离子的还原性最弱的元素:F。
(7)最活泼的金属元素或最高价氧化物对应的水化物碱性最强的元素或阳离子的氧化性最弱的元素:Cs。
(8)常温下单质最易着火的元素:P。
(9)焰色反应呈黄色的元素:Na。
(10)焰色反应呈紫色(透过蓝色钴玻璃观察)的元素:K。
(11)单质密度最小的元素:H;密度最小的金属元素:Li。(12)常温下单质呈液态的非金属元素:Br;金属元素:Hg。
(13)元素的气态氢化物和它的最高价氧化物对应的水化物起化合反应的元素:N;能起氧化还原反应的
元素:S。
(14)元素的气态氢化物能与它的氧化物在常温下反应生成该元素单质的元素:S。
(15)元素的单质在常温下能与水反应放出气体的短周期元素:Li、Na、F。
(16)常见的能形成同素异形体的元素:C、P、O、S,其中一种同素异形体易着火的元素:P。
(17)具有漂白性的常见物质:氯水、二氧化硫、过氧化钠,双氧水(H O )等。
2 2
(18)最高价氧化物及其水化物既能与强酸反应,又能与强碱反应的元素:Al。
4.“位”、“构”、“性”规律中的特例:
1H
(1)1 中无中子。
(2)元素周期表中每一个周期一般都是从金属元素开始,但第一周期从氢元素开始。
(3)大多数元素在自然界中都有稳定的同位素,但Na、F、P、Al等20种元素未发现稳定的同位素。
(4)元素的原子序数大,相对原子质量不一定大,如 Ar的相对原子质量为39.95大于 K的39.10。
18 19
(5)一般元素性质越活泼,其单质性质也越活泼,但N与P相反,N的非金属性强于P的,但N 比白磷、
2
红磷稳定得多。
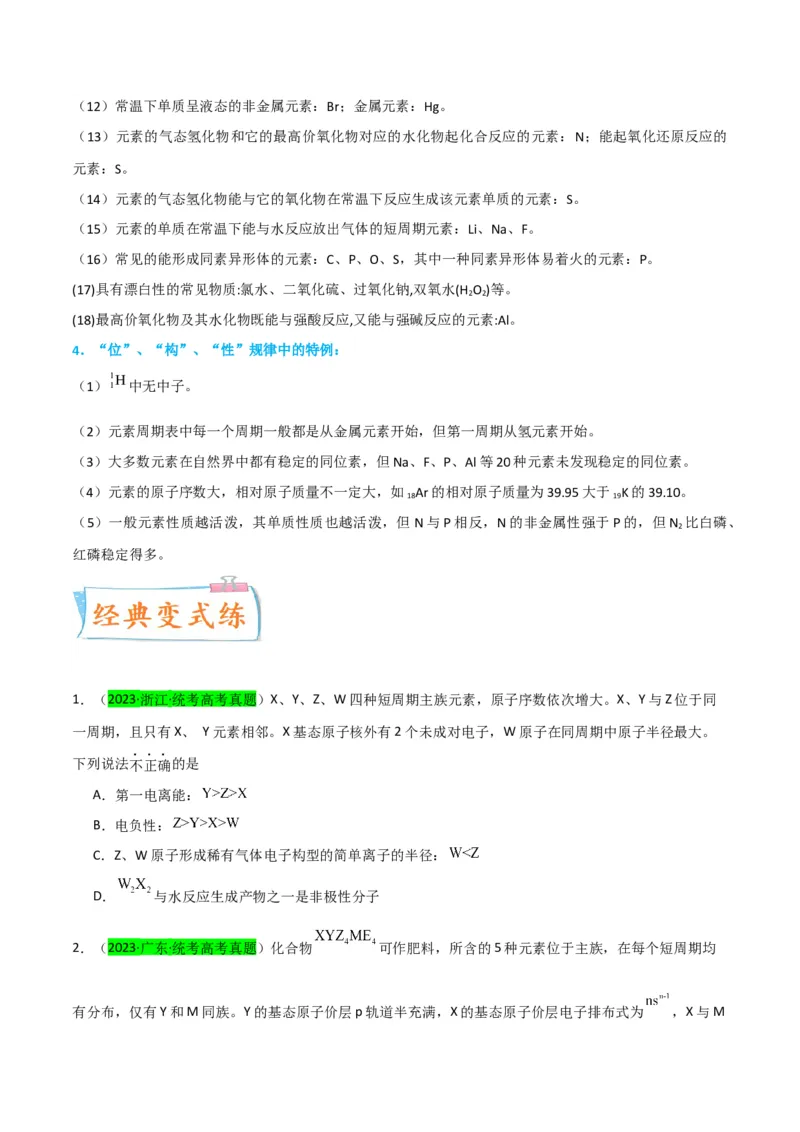
1.(2023·浙江·统考高考真题)X、Y、Z、W四种短周期主族元素,原子序数依次增大。X、Y与Z位于同
一周期,且只有X、 Y元素相邻。X基态原子核外有2个未成对电子,W原子在同周期中原子半径最大。
下列说法不正确的是
A.第一电离能:
B.电负性:
C.Z、W原子形成稀有气体电子构型的简单离子的半径:
D. 与水反应生成产物之一是非极性分子
2.(2023·广东·统考高考真题)化合物 可作肥料,所含的5种元素位于主族,在每个短周期均
有分布,仅有Y和M同族。Y的基态原子价层p轨道半充满,X的基态原子价层电子排布式为 ,X与M同周期,E在地壳中含量最多。下列说法正确的是
A.元素电负性: B.氢化物沸点:
C.第一电离能: D. 和 的空间结构均为三角锥形
3.(2023·湖南·统考高考真题)日光灯中用到的某种荧光粉的主要成分为3W (ZX ) ·WY 。已知:X、Y、Z
3 4 2 2
和W为原子序数依次增大的前20号元素,W为金属元素。基态X原子s轨道上的电子数和p轨道上的电子
数相等,基态X、Y、Z原子的未成对电子数之比为2:1:3。下列说法正确的是
A.电负性:X>Y>Z>W
B.原子半径:XW>Z
B.仅由M与X形成的化合物中不可能含非极性共价键
C.与W同周期且第一电离能介于W和Y之间的元素共有3种
D.X、Y、Z两两间均能形成双原子分子
4.(2023·河北邯郸·统考三模)2022年诺贝尔化学奖授予对点击化学和生物正交化学做出贡献的三位科学
家。我国科学家合成了一种点击化学试剂 ,X可分别与Y、M、Z形成原子个数为3、4、6的
分子, 衰变方程: 。下列说法正确的是A.X的简单离子半径一定是元素周期表中最小的
B. 和 互为同素异形体
C.同一周期中,第一电离能小于Z的有5种元素
D.Y、M形成简单氢化物的还原性:YW>ZB.仅由M与X形成的化合物中不可能含非极性共价键
C.Y的最高价氧化物对应的水化物为强酸
D.X、Y、Z两两间均能形成双原子分子
2.(2023·湖南·高三统考专题练习)日光灯中用到的某种荧光粉的主要成分为3W (ZX ) ·WY 。已知:X、
3 4 2 2
Y、Z和W为原子序数依次增大的前20号元素,W为金属元素。基态X原子s轨道上的电子数和p轨道上
的电子数相等,基态X、Y、Z原子的未成对电子数之比为2:1:3。下列说法正确的是
A.电负性:X>Y>Z>W
B.原子半径:XX>Y>Z>W
C.M的氢化物与Y的单质反应时一定有单质M生成D.最高价氧化物对应水化物酸性:Z>M>X
6.(2022·广东·统考模拟预测)X、Y、Z、W是原子序数依次增大的前三周期元素,其中X是宇宙中含量
最多的元素;Y与Z在周期表中相邻,且它们的原子最外层电子数之和等于W的原子序数;W元素原子的
最外层只有1个电子。下列说法错误的是
A.常见简单离子半径:W<Z<Y B.X、Z可形成具有强氧化性的化合物
C.Z、W形成的离子化合物只含离子键 D.Y有多种酸性氧化物
7.(2022·辽宁·统考高考真题)理论化学模拟得到一种 离子,结构如图。下列关于该离子的说法错误
的是
A.所有原子均满足8电子结构 B.N原子的杂化方式有2种
C.空间结构为四面体形 D.常温下不稳定
8.(2022·福建·统考高考真题)某非线性光学晶体由钾元素(K)和原子序数依次增大的X、Y、Z、W四种短
周期元素组成。X与Y、Z与W均为同周期相邻元素,X的核外电子总数为最外层电子数的2倍,Z为地壳
中含量最多的元素。下列说法正确的是
A.简单氢化物沸点: B. 分子的空间构型为三角锥形
C.原子半径: D.最高价氧化物对应水化物的碱性:
9.(2022·重庆·统考高考真题)R、X、Y、Z均为短周期主族元素,Y与Z同主族且Z的原子序数大于Y。R
和X的原子获得1个电子均可形成稀有气体原子的电子层结构,R的最高化合价为+1。1mol化合物RZY X
3
含58mol电子。下列说法正确的是
A.R与X形成的化合物水溶液呈碱性 B.X是四种元素中原子半径最大的
C.Y单质的氧化性比Z单质的弱 D.Z的原子最外层电子数为6
10.(2023·全国·高三专题练习)如图所示的两种化合物可应用于阻燃材料和生物材料的合成。其中W、
X、Y、Z为原子序数依次增大的短周期元素, 和 同主族, 原子序数为 原子价电子数的3倍。则
W、X、Y、Z分别为 。11.(2023·全国·高三专题练习)我国嫦娥五号探测器带回1.731kg的月球土壤,经分析发现其构成与地球
土壤类似。土壤中含有的短周期元素W、X、Y、Z原子序数依次增大,最外层电子数之和为15,X、Y、
Z为同周期相邻元素,且均不与W同族。
(1)四种元素原子半径由大到小的顺序为W>X>Y>Z ;
(2)Z的氧化物的水化物的酸性强于碳酸 。
12.(2022秋·吉林·高三校联考阶段练习)已知A、B、C、D、E、F是原子序数依次增大的六种短周期主
族元素,A与B能形成 和 两种常见共价化合物,A与C位于相邻主族,B与E位于同一主族,D
是同周期中简单离子半径最小的元素。回答下列问题:
(1)C在元素周期表中的位置是 。
(2) 的电子式为 。
(3)D的最高价氧化物对应的水化物与F的最高价氧化物对应的水化物反应的离子方程式为 。
(4) 和 是市场上较好的消毒剂,等质量的 和 分别与足量二氧化硫反应时,消耗二氧化硫
的质量之比为 。
(5)已知W、X、Y、Z四种物质中均含有上述元素中的某一种,M、X为单质,其余均为化合物,它们之间
存在如图所示的转化关系(反应条件略)。
①Z的化学式为 。
②上述五种物质所含的元素中,原子半径最大的是 (填元素符号)。
③C元素形成的单质与M在海水中可以形成原电池,其正极的电极反应式为 。