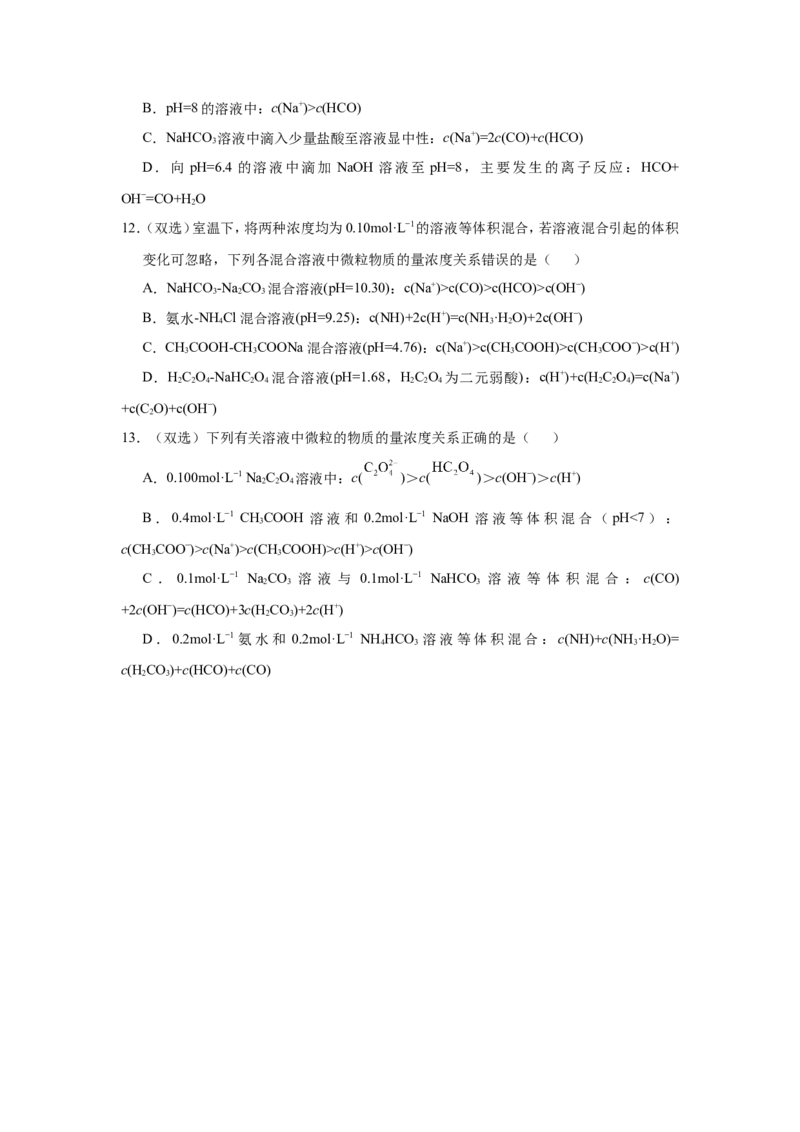文档内容
(新高考)小题必练14:盐类的水解
主要考查盐类水解的含义、影响盐类水解的主要因素、盐类水解的应用,以及运用物料守
恒、电荷守恒、质子守恒来判断和比较溶液中离子浓度大小关系。
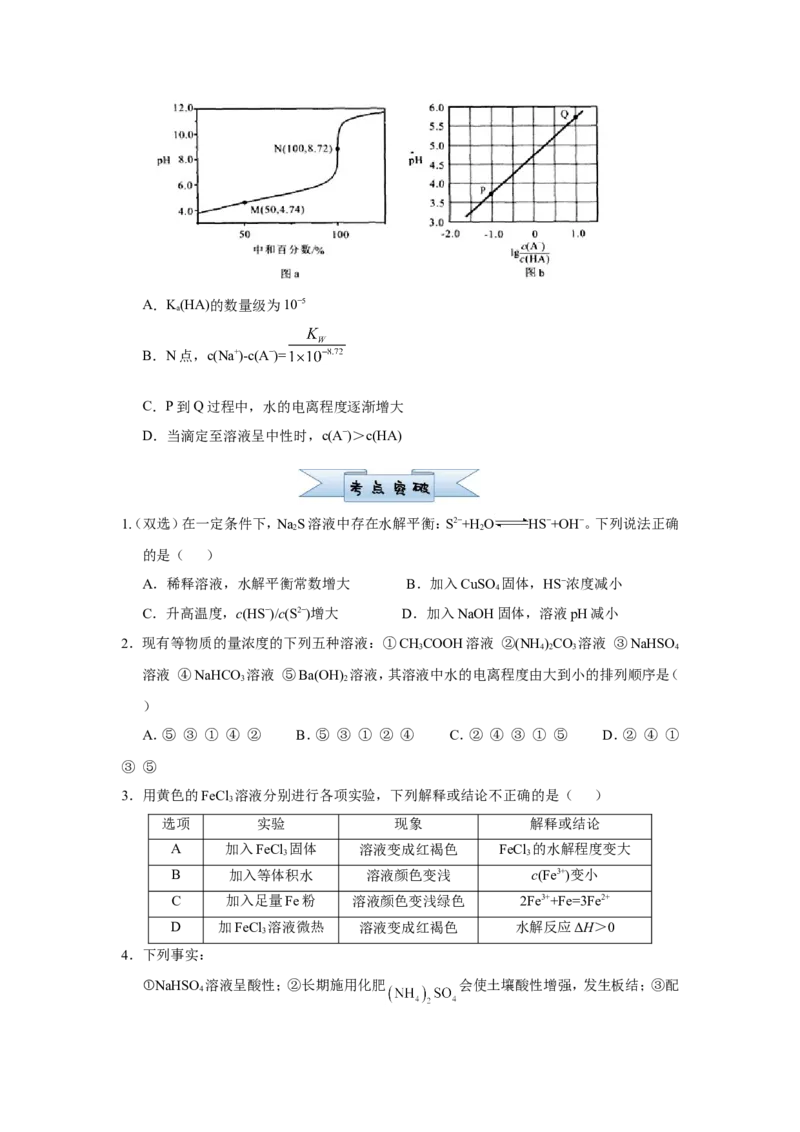
1.【2020 年山东卷】 时,HCO 的 , ,室温下向
2 3
10mL 0.1mol·L−1 NaCO 溶液中逐滴加入0.1mol·L−1 HCl溶液,如图是溶液中含碳元素微
2 3
粒物质的量分数随pH降低而变化的图象CO 因有逸出未画出 。下列说法错误的是(
2
)
A.A点所示溶液的pH<11
B.B点所示溶液:
C.A点→B点发生反应的离子方程式为
D.分步加入酚酞和甲基橙,用滴定法可测定NaCO 与NaHCO 混合物的组成
2 3 3
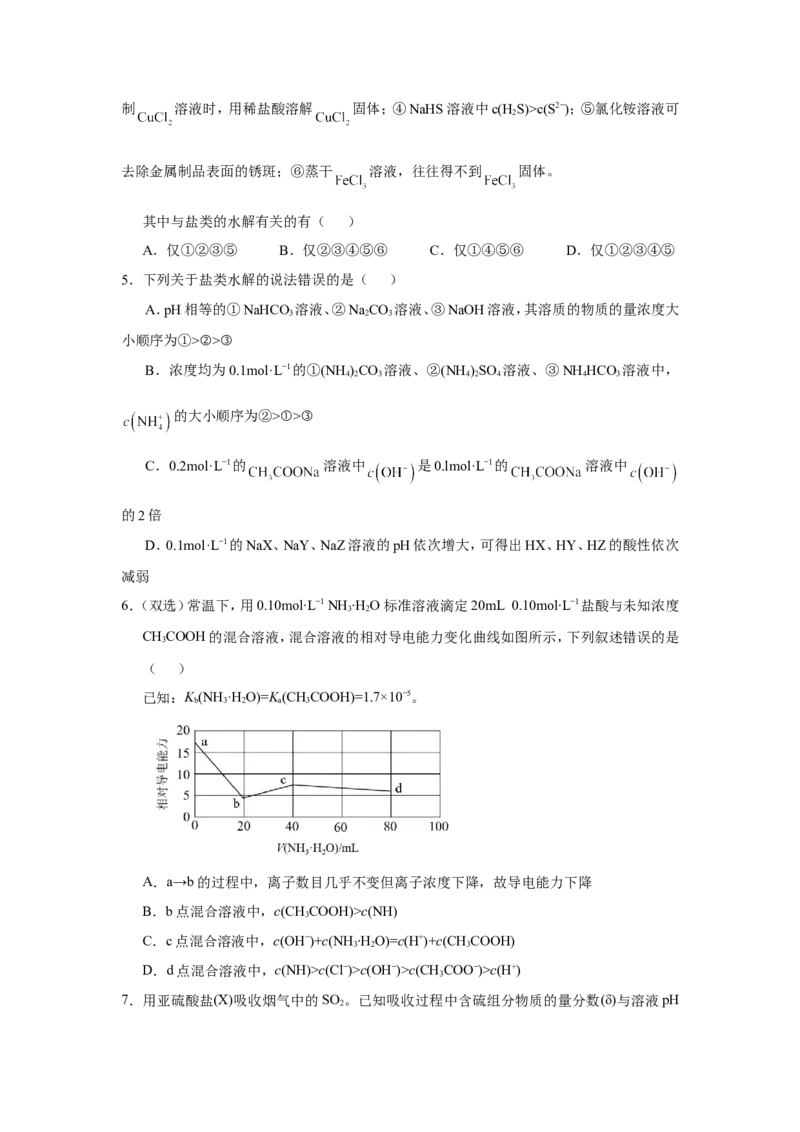
2【. 2020年江苏卷】常温下,用0.1mol·L−1 NaOH溶液滴定0.10mol·L−1 HA溶液,滴定曲线如
图a所示,混合溶液的pH与离子浓度变化的关系如图b所示。下列陈述错误的是( )A.K(HA)的数量级为10−5
a
B.N点,c(Na+)-c(A−)=
C.P到Q过程中,水的电离程度逐渐增大
D.当滴定至溶液呈中性时,c(A−)>c(HA)
1.(双选)在一定条件下,NaS溶液中存在水解平衡:S2−+HO HS−+OH−。下列说法正确
2 2
的是( )
A.稀释溶液,水解平衡常数增大 B.加入CuSO 固体,HS−浓度减小
4
C.升高温度,c(HS−)/c(S2−)增大 D.加入NaOH固体,溶液pH减小
2.现有等物质的量浓度的下列五种溶液:①CHCOOH溶液 ②(NH )CO 溶液 ③NaHSO
3 4 2 3 4
溶液 ④NaHCO 溶液 ⑤Ba(OH) 溶液,其溶液中水的电离程度由大到小的排列顺序是(
3 2
)
A.⑤ ③ ① ④ ② B.⑤ ③ ① ② ④ C.② ④ ③ ① ⑤ D.② ④ ①
③ ⑤
3.用黄色的FeCl 溶液分别进行各项实验,下列解释或结论不正确的是( )
3
选项 实验 现象 解释或结论
A 加入FeCl 固体 溶液变成红褐色 FeCl 的水解程度变大
3 3
B 加入等体积水 溶液颜色变浅 c(Fe3+)变小
C 加入足量Fe粉 溶液颜色变浅绿色 2Fe3++Fe=3Fe2+
D 加FeCl 溶液微热 溶液变成红褐色 水解反应ΔH>0
3
4.下列事实:
①NaHSO 溶液呈酸性;②长期施用化肥 会使土壤酸性增强,发生板结;③配
4制 溶液时,用稀盐酸溶解 固体;④NaHS溶液中c(HS)>c(S2−);⑤氯化铵溶液可
2
去除金属制品表面的锈斑;⑥蒸干 溶液,往往得不到 固体。
其中与盐类的水解有关的有( )
A.仅①②③⑤ B.仅②③④⑤⑥ C.仅①④⑤⑥ D.仅①②③④⑤
5.下列关于盐类水解的说法错误的是( )
A.pH相等的①NaHCO 溶液、②NaCO 溶液、③NaOH溶液,其溶质的物质的量浓度大
3 2 3
小顺序为①>②>③
B.浓度均为0.1mol·L−1的①(NH )CO 溶液、②(NH )SO 溶液、③NH HCO 溶液中,
4 2 3 4 2 4 4 3
的大小顺序为②>①>③
C.0.2mol·L−1的 溶液中 是0.lmol·L−1的 溶液中
的2倍
D.0.1mol·L−1的NaX、NaY、NaZ溶液的pH依次增大,可得出HX、HY、HZ的酸性依次
减弱
6.(双选)常温下,用0.10mol∙L−1 NH∙H O 标准溶液滴定20mL 0.10mol∙L−1盐酸与未知浓度
3 2
CHCOOH的混合溶液,混合溶液的相对导电能力变化曲线如图所示,下列叙述错误的是
3
( )
已知:K (NH ·H O)=K(CHCOOH)=1.7×10−5。
b 3 2 a 3
A.a→b的过程中,离子数目几乎不变但离子浓度下降,故导电能力下降
B.b点混合溶液中,c(CHCOOH)>c(NH)
3
C.c点混合溶液中,c(OH−)+c(NH ∙H O)=c(H+)+c(CHCOOH)
3 2 3
D.d点混合溶液中,c(NH)>c(Cl−)>c(OH−)>c(CHCOO−)>c(H+)
3
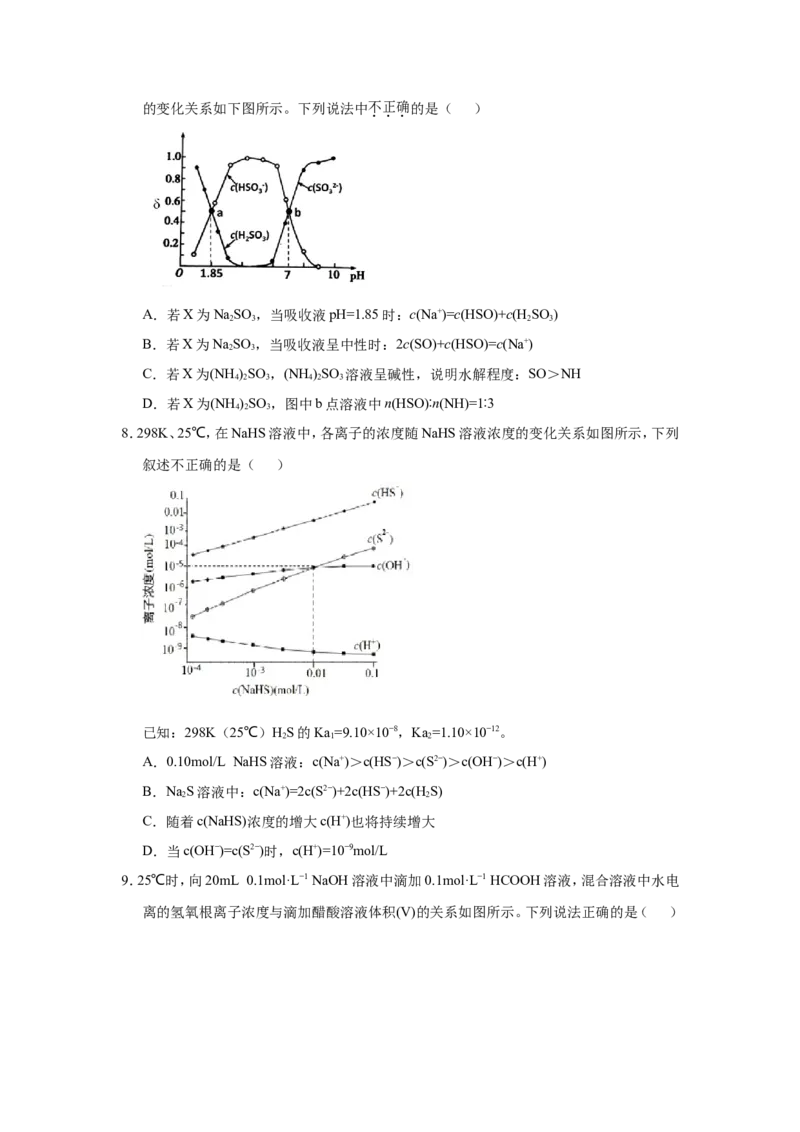
7.用亚硫酸盐(X)吸收烟气中的SO 。已知吸收过程中含硫组分物质的量分数(δ)与溶液pH
2的变化关系如下图所示。下列说法中不正确的是( )
A.若X为NaSO ,当吸收液pH=1.85时:c(Na+)=c(HSO)+c(H SO )
2 3 2 3
B.若X为NaSO ,当吸收液呈中性时:2c(SO)+c(HSO)=c(Na+)
2 3
C.若X为(NH )SO ,(NH )SO 溶液呈碱性,说明水解程度:SO>NH
4 2 3 4 2 3
D.若X为(NH )SO ,图中b点溶液中n(HSO)∶n(NH)=1∶3
4 2 3
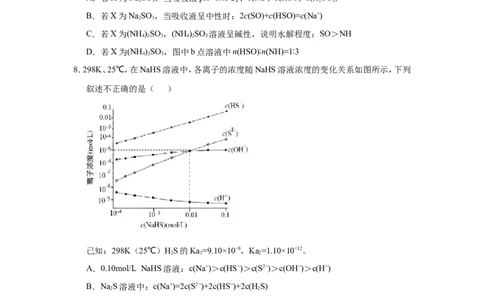
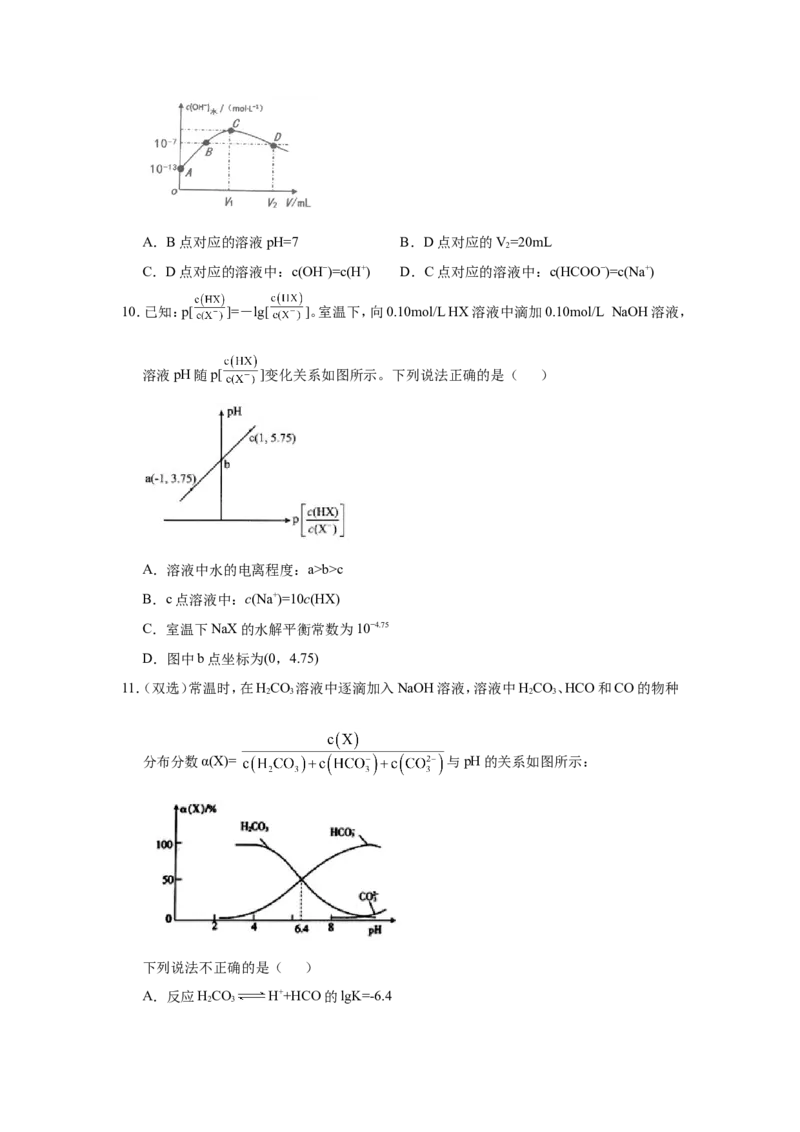
8.298K、25℃,在NaHS溶液中,各离子的浓度随NaHS溶液浓度的变化关系如图所示,下列
叙述不正确的是( )
已知:298K(25℃)HS的Ka=9.10×10−8,Ka=1.10×10−12。
2 1 2
A.0.10mol/L NaHS溶液:c(Na+)>c(HS−)>c(S2−)>c(OH−)>c(H+)
B.NaS溶液中:c(Na+)=2c(S2−)+2c(HS−)+2c(HS)
2 2
C.随着c(NaHS)浓度的增大c(H+)也将持续增大
D.当c(OH−)=c(S2−)时,c(H+)=10−9mol/L
9.25℃时,向20mL 0.1mol·L−1 NaOH溶液中滴加0.1mol·L−1 HCOOH溶液,混合溶液中水电
离的氢氧根离子浓度与滴加醋酸溶液体积(V)的关系如图所示。下列说法正确的是( )A.B点对应的溶液pH=7 B.D点对应的V=20mL
2
C.D点对应的溶液中:c(OH−)=c(H+) D.C点对应的溶液中:c(HCOO−)=c(Na+)
10.已知:p[ ]=-lg[ ]。室温下,向0.10mol/L HX溶液中滴加0.10mol/L NaOH溶液,
溶液pH随p[ ]变化关系如图所示。下列说法正确的是( )
A.溶液中水的电离程度:a>b>c
B.c点溶液中:c(Na+)=10c(HX)
C.室温下NaX的水解平衡常数为10−4.75
D.图中b点坐标为(0,4.75)
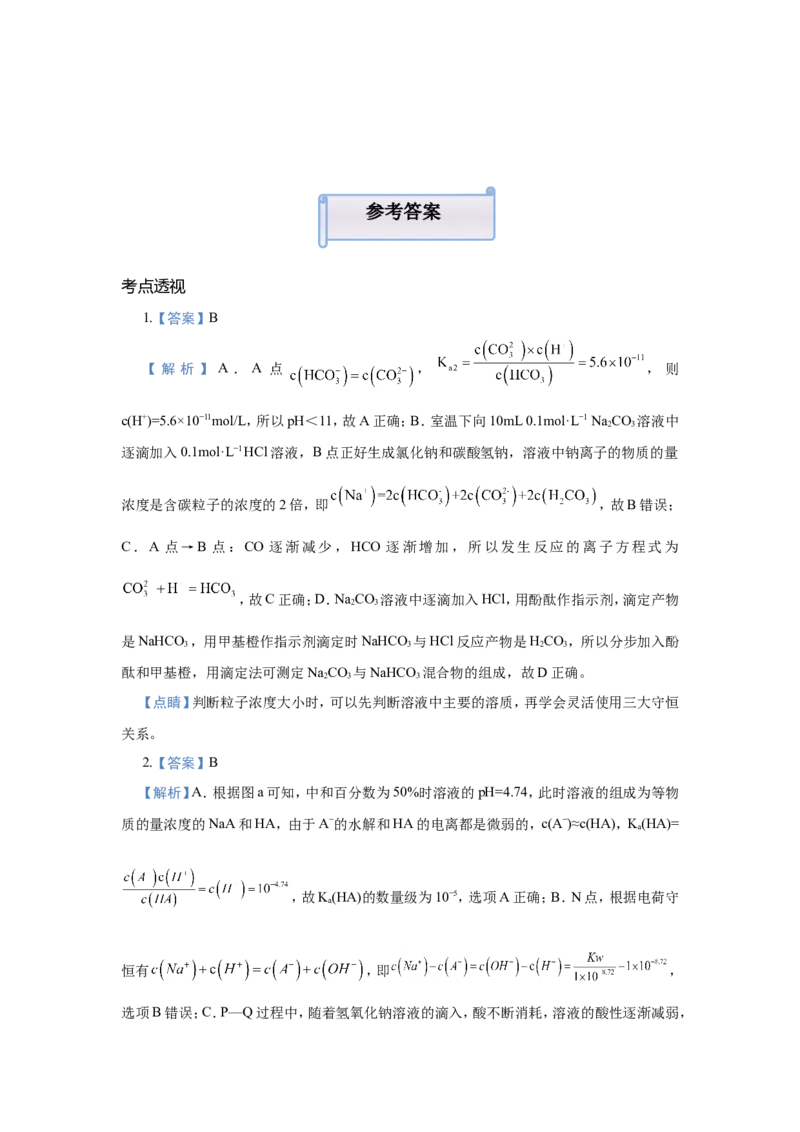
11.(双选)常温时,在HCO 溶液中逐滴加入NaOH溶液,溶液中HCO、HCO和CO的物种
2 3 2 3
分布分数α(X)= 与pH的关系如图所示:
下列说法不正确的是( )
A.反应HCO H++HCO的lgK=-6.4
2 3B.pH=8的溶液中:c(Na+)>c(HCO)
C.NaHCO 溶液中滴入少量盐酸至溶液显中性:c(Na+)=2c(CO)+c(HCO)
3
D.向 pH=6.4 的溶液中滴加 NaOH 溶液至 pH=8,主要发生的离子反应:HCO+
OH−=CO+H O
2
12.(双选)室温下,将两种浓度均为0.10mol·L−1的溶液等体积混合,若溶液混合引起的体积
变化可忽略,下列各混合溶液中微粒物质的量浓度关系错误的是( )
A.NaHCO -Na CO 混合溶液(pH=10.30):c(Na+)>c(CO)>c(HCO)>c(OH−)
3 2 3
B.氨水-NH Cl混合溶液(pH=9.25):c(NH)+2c(H+)=c(NH ·H O)+2c(OH−)
4 3 2
C.CHCOOH-CH COONa混合溶液(pH=4.76):c(Na+)>c(CH COOH)>c(CH COO−)>c(H+)
3 3 3 3
D.HC O-NaHC O 混合溶液(pH=1.68,HC O 为二元弱酸):c(H+)+c(H C O)=c(Na+)
2 2 4 2 4 2 2 4 2 2 4
+c(C O)+c(OH−)
2
13.(双选)下列有关溶液中微粒的物质的量浓度关系正确的是( )
A.0.100mol·L−1 Na C O 溶液中:c( )>c( )>c(OH−)>c(H+)
2 2 4
B.0.4mol·L−1 CH COOH 溶液和 0.2mol·L−1 NaOH 溶液等体积混合(pH<7):
3
c(CHCOO−)>c(Na+)>c(CHCOOH)>c(H+)>c(OH−)
3 3
C . 0.1mol·L−1 Na CO 溶 液 与 0.1mol·L−1 NaHCO 溶 液 等 体 积 混 合 : c(CO)
2 3 3
+2c(OH−)=c(HCO)+3c(H CO)+2c(H+)
2 3
D.0.2mol·L−1 氨水和 0.2mol·L−1 NH HCO 溶液等体积混合:c(NH)+c(NH ·H O)=
4 3 3 2
c(H CO)+c(HCO)+c(CO)
2 3参考答案
考点透视
1.【答案】B
【 解 析 】 A . A 点 , , 则
c(H+)=5.6×10−11mol/L,所以pH<11,故A正确;B.室温下向10mL 0.1mol·L−1 NaCO 溶液中
2 3
逐滴加入0.1mol·L−1 HCl溶液,B点正好生成氯化钠和碳酸氢钠,溶液中钠离子的物质的量
浓度是含碳粒子的浓度的2倍,即 ,故B错误;
C.A 点→B 点:CO 逐渐减少,HCO 逐渐增加,所以发生反应的离子方程式为
,故C正确;D.NaCO 溶液中逐滴加入HCl,用酚酞作指示剂,滴定产物
2 3
是NaHCO ,用甲基橙作指示剂滴定时NaHCO 与HCl反应产物是HCO,所以分步加入酚
3 3 2 3
酞和甲基橙,用滴定法可测定NaCO 与NaHCO 混合物的组成,故D正确。
2 3 3
【点睛】判断粒子浓度大小时,可以先判断溶液中主要的溶质,再学会灵活使用三大守恒
关系。
2.【答案】B
【解析】A.根据图a可知,中和百分数为50%时溶液的pH=4.74,此时溶液的组成为等物
质的量浓度的NaA和HA,由于A−的水解和HA的电离都是微弱的,c(A−)≈c(HA),K(HA)=
a
,故K(HA)的数量级为10−5,选项A正确;B.N点,根据电荷守
a
恒有 ,即 ,
选项B错误;C.P—Q过程中,随着氢氧化钠溶液的滴入,酸不断消耗,溶液的酸性逐渐减弱,水的电离程度逐渐增大,选项C正确;D.根据图b可知当lg (即 )时,
溶液呈酸性,当滴定至溶液呈中性时,溶液中c(A−)>c(HA),选项D正确。答案选B。
【点睛】本题考查了酸碱混合的定性判断及溶液电离平衡常数的计算,题目难度中等,明
确溶液酸碱性与溶液pH的关系为解答关键,注意掌握水的电离及其影响,试题培养了学生
的分析能力及灵活应用能力。
考点突破
1.【答案】BC
【解析】稀释溶液,水解平衡向正反应方向移动,但水解平衡常数只与温度有关,温度不变,
水解平衡常数保持不变,A项错误;加入CuSO 固体,发生沉淀反应:Cu2++S2−=CuS↓,c(S2−)减
4
小,S2−的水解平衡向逆反应方向移动,c(HS−)减小,B项正确;水解过程吸热,升高温度,水解
平衡向正反应方向移动,c(HS−)增大,c(S2−)减小,c(HS−)/c(S2−)增大,C项正确;加入NaOH固
体,c(OH−)增大,pH增大,D项错误。
2.【答案】D
【解析】设五种溶液的物质的量浓度均为c,①醋酸为弱酸,抑制了水的电离,溶液中氢离
子的浓度小于c,②(NH )CO 溶液中的铵根离子和碳酸根离子都能够水解,促进了水的电离,
4 2 3
③NaHSO 溶液为酸性溶液,溶液中氢离子的浓度为c,该溶液中水的电离程度小于①,
4
④NaHCO 为强碱弱酸盐,碳酸氢根离子水解促进了水的电离,该溶液中水的电离程度小于
3
②大于①,⑤Ba(OH) 溶液中的氢氧根离子浓度为2c,抑制了水的电离,该溶液中水的电离
2
程度小于③。综上分析,题述五种溶液中水的电离程度由大到小的顺序为② ④ ①③ ⑤,D
项正确。
3.【答案】A
【解析】FeCl 溶液中存在Fe3+的水解平衡:Fe3++3HO Fe(OH) +3H+,加入FeCl 固体
3 2 3 3
后,溶液中c(Fe3+)增大,平衡正向移动,溶液颜色加深变成红褐色,但FeCl 的水解程度减小,
3
A项错误;加入等体积水,水解平衡正向移动,溶液中c(Fe3+)减小,溶液的颜色变浅,B项正
确;加入足量铁粉,FeCl 溶液与Fe发生反应:2FeCl +Fe=3FeCl ,由于生成Fe2+,溶液变成浅
3 3 2
绿色,C项正确;加热FeCl 溶液,溶液变成红褐色,说明Fe3+的水解平衡正向移动,则有
3
FeCl 水解反应的ΔH>0,D项正确。
3
4.【答案】B【解析】①中NaHSO 为强酸强碱的酸式盐,溶液显酸性是因为NaHSO 电离出 ;②中
4 4
是NH水解使土壤酸性增强;③中HCl电离产生的 会抑制 水解;④中是因 水解
的程度大于其电离的程度;⑤中NH水解产生的 与锈斑中的 反应;⑥加热会促进
水解。
5.【答案】C
【解析】相同物质的量浓度的①NaHCO 溶液、② NaCO 溶液、③NaOH溶液碱性依次增
3 2 3
强,故 pH 相等的三种溶液中溶质的物质的量浓度大小顺序为①>②>③,A 正确;
①(NH )CO 溶液、②(NH )SO 溶液中NH浓度大于等浓度的NH HCO 溶液中NH浓度,
4 2 3 4 2 4 4 3
(NH )CO 溶液中的 、NH相互促进水解,所以c(NH)的大小顺序为②>①>③,B正确;
4 2 3
CH3COONa 溶液浓度越小其水解程度越大,水解产生氢氧根离子的浓度越大,所以
0.2mol·L−1的CH3COONa溶液中c(OH−)小于0.1mol·L−1的CH3COONa溶液中c(OH−)的2倍,
C错误;0.1mol·L−1的NaX、NaY、NaZ溶液的pH依次增大,根据“越弱越水解”可得出HX、
HY、HZ的酸性依次减弱,D正确。
6.【答案】BD
【解析】A.a→b的过程中,NH ∙H O与先与盐酸完全反应,离子数目没有变化,但体积增
3 2
加导致离子浓度下降,故导电能力下降,故A正确;B.b→c的过程中,导电能力增强,发生了
NH ∙H O与醋酸的反应,可推出醋酸的浓度为0.10mol∙L−1,b点的溶质为等浓度的NH Cl、
3 2 4
CHCOOH,因为K(CHCOOH)>K (NH),故醋酸的浓度更小,故B错误;C.c点的溶质为
3 a 3 h
NH Cl、CHCOONH,根据电荷守恒:c(OH−)+c(Cl−)+c(CHCOO−)=c(H+)+
4 3 4 3
c(NH)、物料守恒:c(NH)+c(NH ·H O)=c(Cl−)+c(CHCOO−)+c(CHCOOH),两个守恒相加即可
3 2 3 3
得出C选项中的等式,故C正确;D.d点的溶质为等浓度的NH Cl、CHCOONH 和2倍浓度
4 3 4
的 NH ∙H O , 此 时 应 该 主 要 考 虑 的 NH ∙H O 的 电 离 , 离 子 浓 度 大 小 为 :
3 2 3 2
c(NH)>c(Cl−)>c(CHCOO−)>c(OH−)>c(H+),故D错误。答案选BD。
3
7.【答案】A
【解析】图中a点当吸收液pH=1.85时,HSO 、HSO各点50%,c(HSO)=c(H SO ),b点
2 3 2 3
pH=7,c(H+)=c(OH−),利用电荷守恒、物料守恒及其变形式子进行分析。A.若X为NaSO ,存
2 3
在物料守恒,c(Na+)=2c(HSO)+2c(H SO )+2c(SO),当吸收液pH=1.85时,c(HSO)=c(H SO ),则
2 3 2 3c(Na+)=4c(H SO )+2c(SO)=4c(HSO)+2c(SO),故A错误;B.若X为NaSO ,当吸收液呈中性
2 3 2 3
时:c(H+)=c(OH−),溶液中存在电荷守恒:c(H+)+c(Na+)=c(HSO)+2c(SO)+c(OH−),得到2c(SO)
+c(HSO)=c(Na+),故B正确;C.若X为(NH )SO ,由于NH水解显酸性,SO水解显碱性,
4 2 3
(NH )SO 溶液呈碱性,说明水解程度:SO>NH,故C正确;D.若X为(NH )SO ,图中b点
4 2 3 4 2 3
溶液中,c(HSO)=c(SO),b点pH=7,c(H+)=c(OH−),根据电荷守恒:c(H+)+c(NH)=c(HSO)
+2c(SO)+c(OH−),3c(HSO)=c(NH),n(HSO)∶n(NH)=1∶3,故D正确;故选A。
8.【答案】C
【解析】A.根据图像,0.10mol/L NaHS溶液中各离子浓度的情况为c(HS−)>c(S2−)>
c(OH−)>c(H+),由于Na+不水解,浓度最大,故有c(Na+)>c(HS−)>c(S2−)>c(OH−)>c(H+),A
正确;B.NaS溶液中,由物料守恒可得:c(Na+)=2c(S2−)+2c(HS−)+2c(HS),B正确;C.由图像
2 2
可知,随着c(NaHS)浓度的增大c(H+)不断变小,C错误;D.c(OH−)=c(S2−)时,由图像可知
c(OH−)=10−5mol/L,故 mol/L,D正确;故选C。
9.【答案】C
【解析】A.B点溶质为NaOH、HCOONa,溶液呈碱性,pH>7,A错误;B.二者恰好反应时
生成醋酸钠,水的电离程度最大,所以 C点对应的V=20mL,B错误;C.D点溶质为
1
HCOONa、HCOOH,溶液呈中性,则对应的溶液中:c(OH−)=c(H+),C正确;D.C点恰好反应
生成醋酸钠,醋酸根离子水解,溶液显碱性,则对应的溶液中:c(HCOO−)<c(Na+),D错误。答
案选C。
10.【答案】D
【解析】根据图示可知,a、b、c均为酸性溶液,则溶质为HX和NaX,pH<7的溶液中,HX
的电离程度大于X−的水解程度,可只考虑H+对水的电离的抑制,溶液pH越大氢离子浓度越
小,水的电离程度越大,则溶液中水的电离程度:ac(OH−),则c(Na+)<10c(HX),B错误;C.HX在溶液中存在电离平衡:HX H++X−,K= ,则pH=pKa+p[ ],带
a
入c点坐标(1,5.75)可知,pKa=4.75,则K=10−4.75,则室温下室温下NaX的水解平衡常数K =
a h
=10−9.25,C 错误;D.HX 在溶液中存在电离平衡:HX H++X−,Ka=
,则pH=pKa+p[ ],带入c点坐标(1,5.75)可知,pKa=4.75,则b点
pH=pKa+p[ ]=0+4.75=4.75,D正确;故合理选项是D。
11.【答案】CD
【解析】由图可知,在HCO 溶液中逐滴加入NaOH溶液,溶液中HCO 含量逐渐减小;
2 3 2 3
CO、HCO 含量逐渐增多,第二步反应 HCO 逐渐变成 CO。A.pH=6.4 时,c(
)=c(H CO),反应HCO H++HCO的lgK= =lgc(H+)=-6.4,故A正确;
2 3 2 3
B.pH=8时,溶液中溶质有NaCO、NaHCO ,HCO发生水解和电离,钠离子不水解和电离,
2 3 3
所以存在c(Na+)>c(HCO),故B正确;C.中性溶液中c(H+)=c(OH−),溶液中存在电荷守恒
c(Na+)+c(H+)=c(Cl−)+c(HCO)+2c(CO)+c(OH−),则有c(Na+)=c(Cl−)+c(HCO)+2c(CO);故C错误;
pH=6.4的溶液中含有等物质的量的NaHCO 和HCO,pH=8的溶液中主要含NaHCO ,该反
3 2 3 3
应过程中主要是碳酸和NaOH的反应,所以主要发生的离子反应为HCO+OH−=HCO+H O,
2 3 2
故D错误。答案选CD。
【点睛】明确物质成分及其性质、物质之间的转化关系、电离平衡常数计算方法是解本题
关键,注意电荷守恒的灵活运用。
12.【答案】AC
【解析】氯化铵、碳酸钠等溶液会水解,充分利用电荷守恒、物料守恒关系列等式求解;A.
NaHCO 水溶液呈碱性,说明HCO的水解程度大于其电离程度,等浓度的NaHCO 和NaCO
3 3 2 3水解关系为:CO>HCO,溶液中剩余微粒浓度关系为: ,CO和HCO水解程
度微弱,生成的OH−浓度较低,由NaHCO 和NaCO 化学式可知,该混合溶液中Na+浓度最
3 2 3
大,则混合溶液中微粒浓度大小关系为: ,故A错误;
B.该混合溶液中电荷守恒为: ,物料守恒为:c(NH ·H O)
3 2
+c(NH)=2c(Cl−),两式联立消去c(Cl−)可得:c(NH)+c(H+)=2c(OH−)+c(NH ·H O),故B正确;C.
3 2
该溶液呈酸性,说明CHCOOH电离程度大于CHCOONa水解程度,则溶液中微粒浓度关系
3 3
为:c(CHCOO−)>c(Na+)>c(CHCOOH)>c(H+),故C错误;D.该混合溶液中物料守恒为:
3 3
, 电 荷 守 恒 为 :
, 两 式 相 加 可 得 :
,故D正确;答案选AC。
13.【答案】BC
【解析】A.0.100mol·L−1 Na C O 溶液中,c( )>c(OH−)>c( )>c(H+),A错误;
2 2 4
B.0.4mol·L−1 CH COOH溶液和0.2mol·L−1 NaOH溶液等体积混合后,溶液中CHCOOH和
3 3
CHCOONa 浓度相等,pH<7 说明 CHCOOH 电离程度大于 CHCOO−水解程度,因此
3 3 3
c(CHCOO−)>c(Na+)>c(CHCOOH)>c(H+)>c(OH−),B正确;C.0.1mol·L−1 Na CO 溶液与0.1
3 3 2 3
mol·L−1 NaHCO 溶液等体积混合,根据电荷守恒和物料守恒可得c(CO)+2c(OH−)=c(HCO)
3
+3c(H CO)+2c(H+),C正确;D.0.2mol·L−1氨水和0.2mol·L−1 NH HCO 溶液等体积混合生成
2 3 4 3
(NH )CO,根据物料守恒可得c(NH)+c(NH ·H O)=2c(H CO)+2c(HCO)+2c(CO),D错误;故
4 2 3 3 2 2 3
选BC。