文档内容
(新高考)小题必练13:酸碱中和滴定及应用
酸碱中和滴定是高中化学最重要的定量实验之一,是帮助学生养成科学态度和接受科学
教育极好的实验课题,常常结合溶液中的水解平衡,物质定量测定,高考再现率高,而且考察
角度不断创新,对学习化学有良好的导向作用。
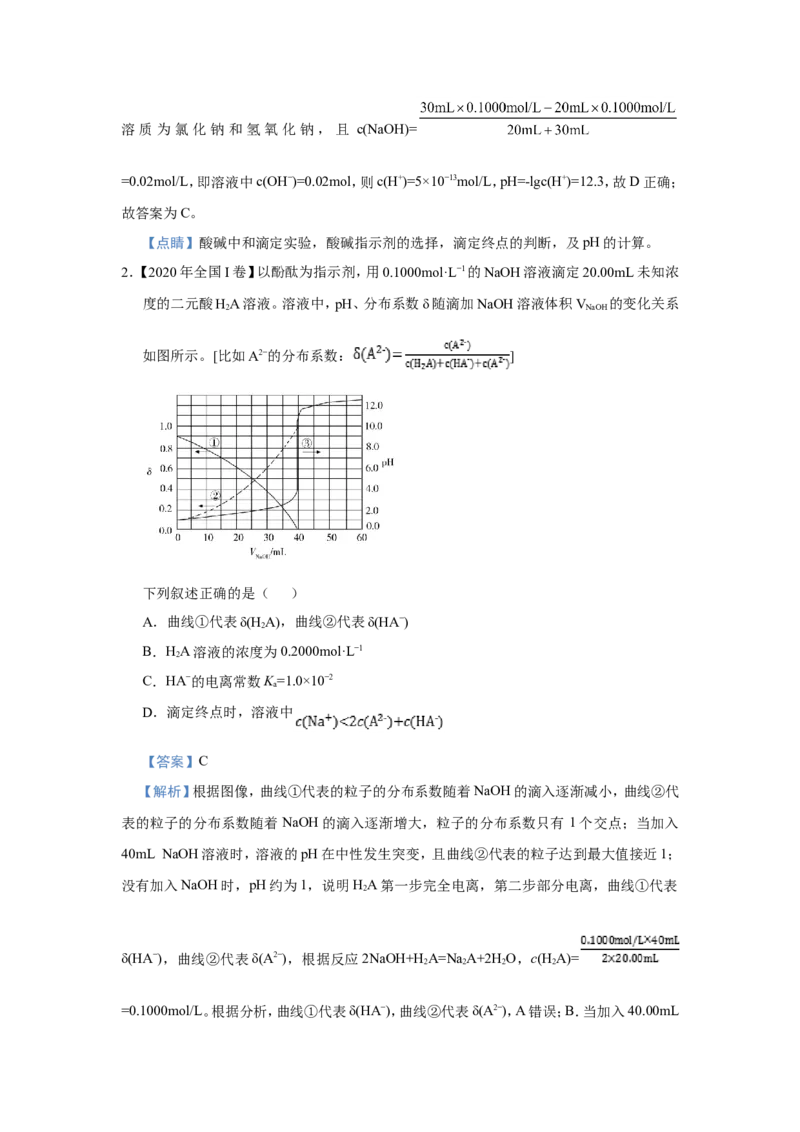
1【. 2020年浙江选考】室温下,向 盐酸中滴加0.1000mol/L NaOH
溶液,溶液的pH随NaOH溶液体积的变化如图。已知 。下列说法不正确的是(
)
A.NaOH与盐酸恰好完全反应时,pH=7
B.选择变色范围在pH突变范围内的指示剂,可减小实验误差
C.选择甲基红指示反应终点,误差比甲基橙的大
D. 时,pH=12.3
【答案】C
【解析】A.NaOH与盐酸恰好完全反应时溶液中的溶质为NaCl,呈中性,室温下pH=7,故
A正确;B.选择变色范围在pH突变范围内的指示剂,可减小实验误差,B正确;C.甲基橙的
变色范围在pH突变范围外,误差更大,故C错误;D. 时,溶液中的溶质为氯化钠和氢氧化钠,且 c(NaOH)=
=0.02mol/L,即溶液中c(OH−)=0.02mol,则c(H+)=5×10−13mol/L,pH=-lgc(H+)=12.3,故D正确;
故答案为C。
【点睛】酸碱中和滴定实验,酸碱指示剂的选择,滴定终点的判断,及pH的计算。
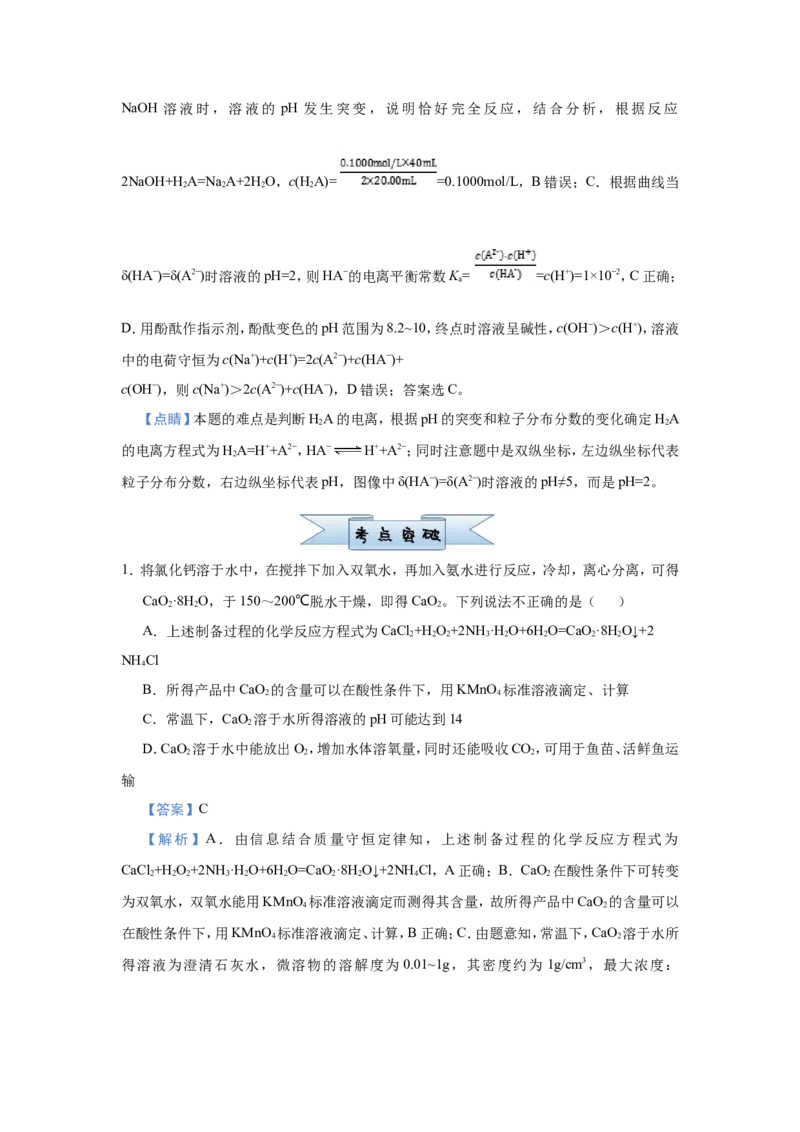
2.【2020年全国I卷】以酚酞为指示剂,用0.1000mol·L−1的NaOH溶液滴定20.00mL未知浓
度的二元酸HA溶液。溶液中,pH、分布系数δ随滴加NaOH溶液体积V 的变化关系
2 NaOH
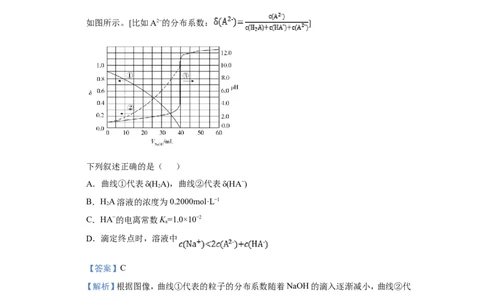
如图所示。[比如A2−的分布系数: ]
下列叙述正确的是( )
A.曲线①代表δ(H A),曲线②代表δ(HA−)
2
B.HA溶液的浓度为0.2000mol·L−1
2
C.HA−的电离常数K=1.0×10−2
a
D.滴定终点时,溶液中
【答案】C
【解析】根据图像,曲线①代表的粒子的分布系数随着NaOH的滴入逐渐减小,曲线②代
表的粒子的分布系数随着NaOH的滴入逐渐增大,粒子的分布系数只有 1个交点;当加入
40mL NaOH溶液时,溶液的pH在中性发生突变,且曲线②代表的粒子达到最大值接近1;
没有加入NaOH时,pH约为1,说明HA第一步完全电离,第二步部分电离,曲线①代表
2
δ(HA−),曲线②代表δ(A2−),根据反应2NaOH+H A=Na A+2HO,c(H A)=
2 2 2 2
=0.1000mol/L。根据分析,曲线①代表δ(HA−),曲线②代表δ(A2−),A错误;B.当加入40.00mLNaOH 溶液时,溶液的 pH 发生突变,说明恰好完全反应,结合分析,根据反应
2NaOH+H A=Na A+2HO,c(H A)= =0.1000mol/L,B错误;C.根据曲线当
2 2 2 2
δ(HA−)=δ(A2−)时溶液的pH=2,则HA−的电离平衡常数K= =c(H+)=1×10−2,C正确;
a
D.用酚酞作指示剂,酚酞变色的pH范围为8.2~10,终点时溶液呈碱性,c(OH−)>c(H+),溶液
中的电荷守恒为c(Na+)+c(H+)=2c(A2−)+c(HA−)+
c(OH−),则c(Na+)>2c(A2−)+c(HA−),D错误;答案选C。
【点睛】本题的难点是判断HA的电离,根据pH的突变和粒子分布分数的变化确定HA
2 2
的电离方程式为HA=H++A2−,HA− H++A2−;同时注意题中是双纵坐标,左边纵坐标代表
2
粒子分布分数,右边纵坐标代表pH,图像中δ(HA−)=δ(A2−)时溶液的pH≠5,而是pH=2。
1.将氯化钙溶于水中,在搅拌下加入双氧水,再加入氨水进行反应,冷却,离心分离,可得
CaO·8H O,于150~200℃脱水干燥,即得CaO。下列说法不正确的是( )
2 2 2
A.上述制备过程的化学反应方程式为CaCl +HO+2NH ·H O+6HO=CaO·8H O↓+2
2 2 2 3 2 2 2 2
NH Cl
4
B.所得产品中CaO 的含量可以在酸性条件下,用KMnO 标准溶液滴定、计算
2 4
C.常温下,CaO 溶于水所得溶液的pH可能达到14
2
D.CaO 溶于水中能放出O,增加水体溶氧量,同时还能吸收CO,可用于鱼苗、活鲜鱼运
2 2 2
输
【答案】C
【解析】A.由信息结合质量守恒定律知,上述制备过程的化学反应方程式为
CaCl +HO+2NH ·H O+6HO=CaO·8H O↓+2NH Cl,A正确;B.CaO 在酸性条件下可转变
2 2 2 3 2 2 2 2 4 2
为双氧水,双氧水能用KMnO 标准溶液滴定而测得其含量,故所得产品中CaO 的含量可以
4 2
在酸性条件下,用KMnO 标准溶液滴定、计算,B正确;C.由题意知,常温下,CaO 溶于水所
4 2
得溶液为澄清石灰水,微溶物的溶解度为 0.01~1g,其密度约为 1g/cm3,最大浓度:,氢氧根离子浓度最大为0.27mol/L,pH不可能达到14,C
错误;D.由题意知,过氧化钙晶体在水中溶解度不大,故CaO 溶于水中能平缓反应缓慢放出
2
O,增加水体溶氧量,同时还能吸收CO,可用于鱼苗、活鲜鱼运输,D正确;答案选C。
2 2
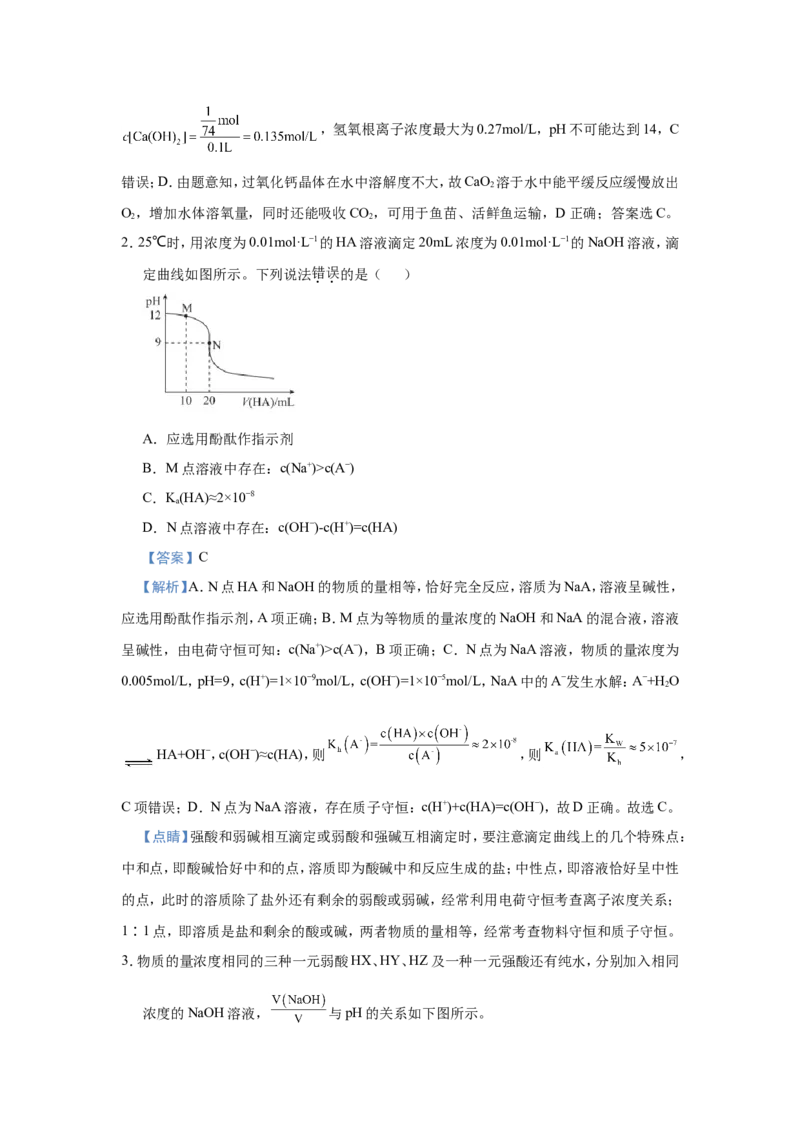
2.25℃时,用浓度为0.01mol·L−1的HA溶液滴定20mL浓度为0.01mol·L−1的NaOH溶液,滴
定曲线如图所示。下列说法错误的是( )
A.应选用酚酞作指示剂
B.M点溶液中存在:c(Na+)>c(A−)
C.K(HA)≈2×10−8
a
D.N点溶液中存在:c(OH−)-c(H+)=c(HA)
【答案】C
【解析】A.N点HA和NaOH的物质的量相等,恰好完全反应,溶质为NaA,溶液呈碱性,
应选用酚酞作指示剂,A项正确;B.M点为等物质的量浓度的NaOH和NaA的混合液,溶液
呈碱性,由电荷守恒可知:c(Na+)>c(A−),B项正确;C.N点为NaA溶液,物质的量浓度为
0.005mol/L,pH=9,c(H+)=1×10−9mol/L,c(OH−)=1×10−5mol/L,NaA中的A−发生水解:A−+H O
2
HA+OH−,c(OH−)≈c(HA),则 ,则 ,
C项错误;D.N点为NaA溶液,存在质子守恒:c(H+)+c(HA)=c(OH−),故D正确。故选C。
【点睛】强酸和弱碱相互滴定或弱酸和强碱互相滴定时,要注意滴定曲线上的几个特殊点:
中和点,即酸碱恰好中和的点,溶质即为酸碱中和反应生成的盐;中性点,即溶液恰好呈中性
的点,此时的溶质除了盐外还有剩余的弱酸或弱碱,经常利用电荷守恒考查离子浓度关系;
1∶1点,即溶质是盐和剩余的酸或碱,两者物质的量相等,经常考查物料守恒和质子守恒。
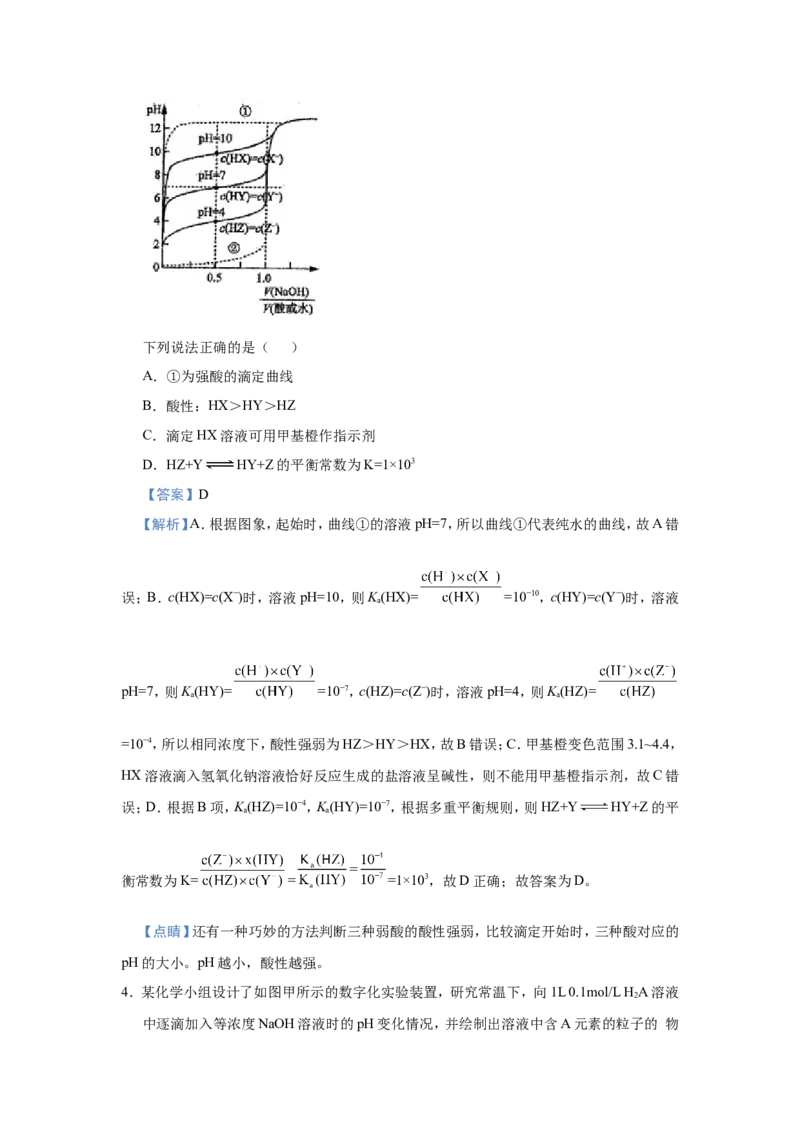
3.物质的量浓度相同的三种一元弱酸HX、HY、HZ及一种一元强酸还有纯水,分别加入相同
浓度的NaOH溶液, 与pH的关系如下图所示。下列说法正确的是( )
A.①为强酸的滴定曲线
B.酸性:HX>HY>HZ
C.滴定HX溶液可用甲基橙作指示剂
D.HZ+Y HY+Z的平衡常数为K=1×103
【答案】D
【解析】A.根据图象,起始时,曲线①的溶液pH=7,所以曲线①代表纯水的曲线,故A错
误;B.c(HX)=c(X−)时,溶液pH=10,则K(HX)= =10−10,c(HY)=c(Y−)时,溶液
a
pH=7,则K(HY)= =10−7,c(HZ)=c(Z−)时,溶液pH=4,则K(HZ)=
a a
=10−4,所以相同浓度下,酸性强弱为HZ>HY>HX,故B错误;C.甲基橙变色范围3.1~4.4,
HX溶液滴入氢氧化钠溶液恰好反应生成的盐溶液呈碱性,则不能用甲基橙指示剂,故C错
误;D.根据B项,K(HZ)=10−4,K(HY)=10−7,根据多重平衡规则,则HZ+Y HY+Z的平
a a
衡常数为K= = =1×103,故D正确;故答案为D。
【点睛】还有一种巧妙的方法判断三种弱酸的酸性强弱,比较滴定开始时,三种酸对应的
pH的大小。pH越小,酸性越强。
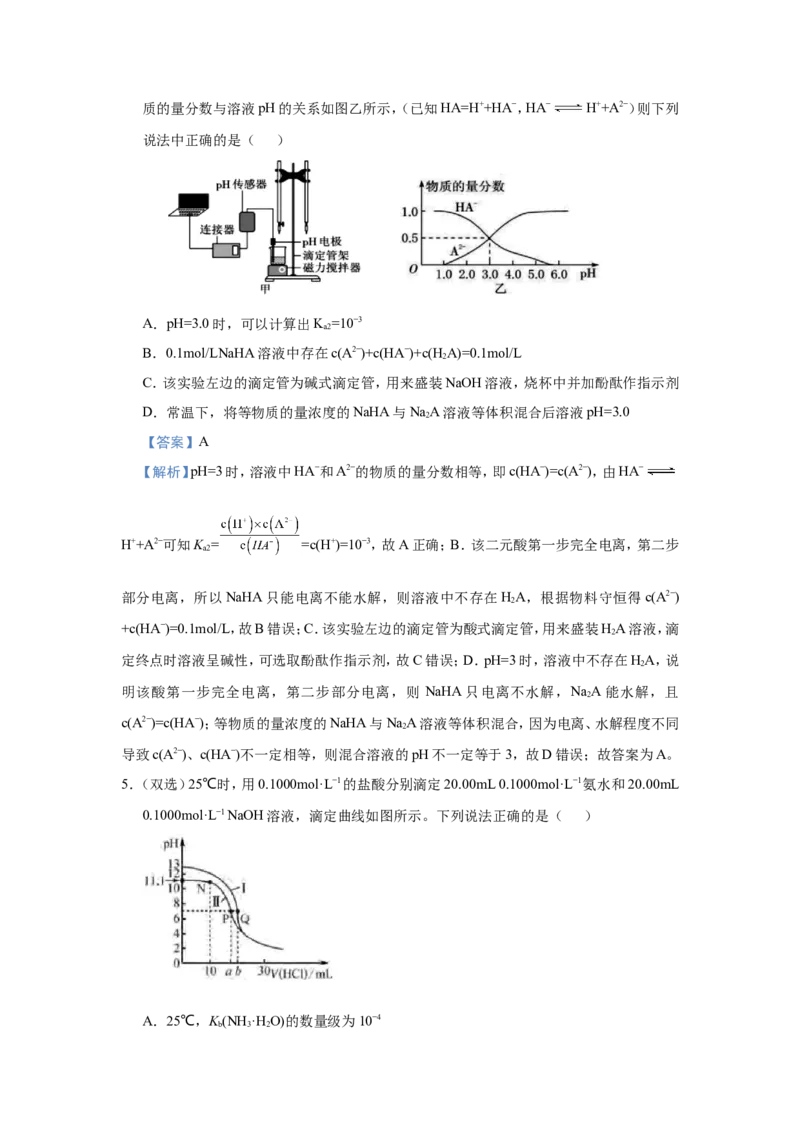
4.某化学小组设计了如图甲所示的数字化实验装置,研究常温下,向1L 0.1mol/L H A溶液
2
中逐滴加入等浓度NaOH溶液时的pH变化情况,并绘制出溶液中含A元素的粒子的 物质的量分数与溶液pH的关系如图乙所示,(已知HA=H++HA−,HA− H++A2−)则下列
说法中正确的是( )
A.pH=3.0时,可以计算出K =10−3
a2
B.0.1mol/LNaHA溶液中存在c(A2−)+c(HA−)+c(H A)=0.1mol/L
2
C.该实验左边的滴定管为碱式滴定管,用来盛装NaOH溶液,烧杯中并加酚酞作指示剂
D.常温下,将等物质的量浓度的NaHA与NaA溶液等体积混合后溶液pH=3.0
2
【答案】A
【解析】pH=3时,溶液中HA−和A2−的物质的量分数相等,即c(HA−)=c(A2−),由HA−
H++A2−可知K = =c(H+)=10−3,故A正确;B.该二元酸第一步完全电离,第二步
a2
部分电离,所以NaHA只能电离不能水解,则溶液中不存在HA,根据物料守恒得c(A2−)
2
+c(HA−)=0.1mol/L,故B错误;C.该实验左边的滴定管为酸式滴定管,用来盛装HA溶液,滴
2
定终点时溶液呈碱性,可选取酚酞作指示剂,故C错误;D.pH=3时,溶液中不存在HA,说
2
明该酸第一步完全电离,第二步部分电离,则 NaHA只电离不水解,NaA能水解,且
2
c(A2−)=c(HA−);等物质的量浓度的NaHA与NaA溶液等体积混合,因为电离、水解程度不同
2
导致c(A2−)、c(HA−)不一定相等,则混合溶液的pH不一定等于3,故D错误;故答案为A。
5.(双选)25℃时,用0.1000mol·L−1的盐酸分别滴定20.00mL 0.1000mol·L−1氨水和20.00mL
0.1000mol·L−1 NaOH溶液,滴定曲线如图所示。下列说法正确的是( )
A.25℃,K (NH ·H O)的数量级为10−4
b 3 2B.N点处的溶液中:c(NH)>c(NH ·H O)
3 2
C.曲线II滴定终点时所选的指示剂为酚酞
D.Q点所加盐酸的体积为b mL,则b=20
【答案】BD
【解析】根据起点分析,曲线I是pH=13,则为盐酸溶液滴定NaOH溶液图像,曲线II是盐
酸滴定氨水溶液图像。A.25℃,根据起点pH=11.1得到
=10-4.8,因此K (NH ·H O)的数量级为10−5,故A错误;B.N点溶质的NH Cl和NH ·H O且浓
b 3 2 4 3 2
度相等,溶液显碱性,电离占主要,因此溶液中:c(NH)>c(NH ·H O),故B正确;C.曲线II滴
3 2
定终点时溶液显酸性,因此所选的指示剂为甲基橙,故C错误;D.Q点是NaOH溶液加盐酸
进行滴定,所加盐酸的体积为b mL,溶液呈中性,则b=20,故D正确;综上所述,答案为BD。
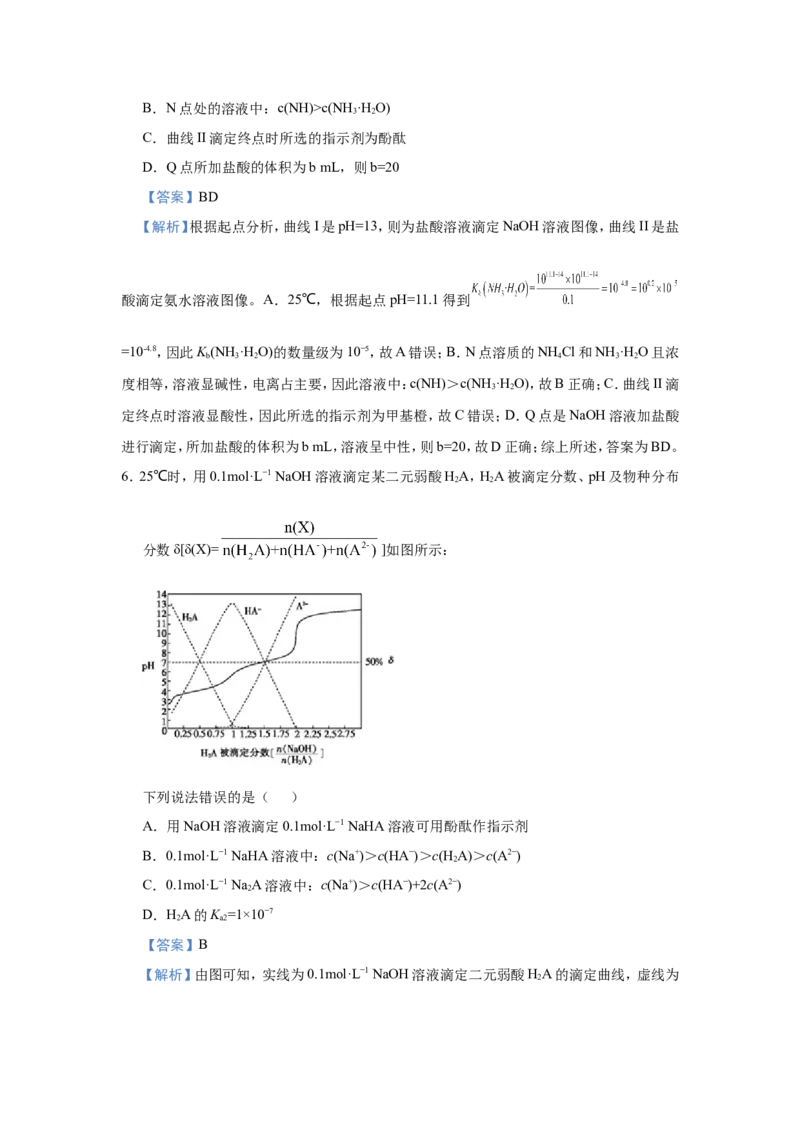
6.25℃时,用0.1mol·L−1 NaOH溶液滴定某二元弱酸HA,HA被滴定分数、pH及物种分布
2 2
分数δ[δ(X)= ]如图所示:
下列说法错误的是( )
A.用NaOH溶液滴定0.1mol·L−1 NaHA溶液可用酚酞作指示剂
B.0.1mol·L−1 NaHA溶液中:c(Na+)>c(HA−)>c(H A)>c(A2−)
2
C.0.1mol·L−1 NaA溶液中:c(Na+)>c(HA−)+2c(A2−)
2
D.HA的K =1×10−7
2 a2
【答案】B
【解析】由图可知,实线为0.1mol·L−1 NaOH溶液滴定二元弱酸HA的滴定曲线,虚线为
20.1mol·L−1 NaOH溶液滴定二元弱酸HA的物种分布分数曲线。当 =1时,反应生成
2
NaHA,NaHA溶液显酸性,当 =2时,反应生成NaA,NaA溶液显碱性。A.强碱滴
2 2
定弱酸时,滴定终点,溶液呈碱性,应选用酚酞做指示剂,则用NaOH溶液滴定0.1mol·L−1
NaHA溶液应用酚酞作指示剂,故A正确;B.由图可知,当 =1时,反应生成
NaHA,NaHA溶液显酸性,说明HA−的电离程度大于水解程度,则溶液中c(A2−)>c(H A),故
2
B错误;C.0.1mol·L−1 NaA溶液中存在电荷守恒关系c(Na+)+c(H+)=c(HA−)+2c(A2−)+c(OH−),
2
因NaA溶液显碱性,c(OH−)>c(H+),则:c(Na+)>c(HA−)+2c(A2−),故C正确;D.由图可知,当
2
δ(X)为50%时,溶液中c(HA−)=c(A2−),pH=7,由Ka= =c(H+)=1×10−7,故D正确;
2
故选:B。
【点睛】本题考查弱电解质的电离,为高频考点,侧重考查学生的分析能力和计算能力,本
题注意把握弱电解质的电离特点以及题给图象的曲线变化,难度中等。
7.某废水中含有Cr O,为了处理有毒的Cr O,需要先测定其浓度:取20mL废水,加入适量
2 2
稀硫酸,再加入过量的V mL c mol·L−1 (NH )Fe(SO ) 溶液,充分反应(还原产物为Cr3+)。
1 1 4 2 4 2
用c mol·L−1 KMnO 溶液滴定过量的Fe2+至终点,消耗KMnO 溶液V mL。则原废水中
2 4 4 2
c(CrO)为(用代数式表示)( )
2
A. mol·L−1 B. mol·L−1
C. mol·L−1 D. mol·L−1
【答案】A
【解析】KMnO 溶液滴定过量的Fe2+至终点,发生反应的关系式为KMnO ~5Fe2+,
4 4
n(KMnO)=c mol·L−1×V×10−3L=cV×10−3mol,则与它反应的 Fe2+的物质的量为 n(Fe2+)=5
4 2 2 2 2
cV×10−3mol。与Cr O反应的Fe2+的物质的量为c mol·L−1×V×10−3L-5cV×10−3mol=(cV×10-
2 2 2 1 1 2 2 1 13-5cV×10−3)mol。Cr O与的Fe2+的关系式为Cr O~6Fe2+,由此可得出n(CrO)=
2 2 2 2 2
,c(CrO)= = mol·L−1,答案为A。
2
【点睛】在废水中Cr O含量的测定实验中,Fe2+表现两个性质,一个是还原Cr O,另一个
2 2
是还原KMnO ,如果我们不能理顺两种氧化剂的作用,则可能会出现错误的结果。
4
8.室温下,依次进行如下实验:
①取一定量冰醋酸,配制成100mL 0.1mol/L醋酸溶液;
②取20mL①中所配溶液,加入20mL 0.1mol/L NaOH溶液;
③继续滴加a mL 0.1mol/L稀盐酸,至溶液的pH=7。
下列说法正确的是( )
A.①中溶液的pH=1
B.②中反应后溶液:c(Na+)>c(CHCOO−)>c(H+)>c(OH−)
3
C.③中,a=20
D.③中,反应后溶液:c(Na+)=c(CHCOO−)+c(Cl−)
3
【答案】D
【解析】A.由于醋酸为弱酸,无法完全电离,所以取一定量冰醋酸,配制成 100mL
0.1mol/L醋酸溶液,溶液pH>1,A错误;B.操作②得到的溶液为醋酸钠溶液,醋酸钠溶液显
碱性,c(H+)c(NH)>c(CH COO−)>c(H+)
3
【答案】AC
【解析】A.盐酸和CHCOONH 溶液反应生成醋酸和氯化铵,反应终点溶液为酸性,用甲
3 4
基橙作滴定指示剂,A正确;B.滴定过程中CHCOO−的浓度减小,对水的电离促进作用减弱,
3
水的电离程度减小,B错误;C.P点溶液中①电荷守恒:c(CHCOO−)+c(OH−)
3
+c(Cl−)=c(NH+)+c(H+),②物料守恒:c(CHCOO−)+c(CH COOH)=2c(Cl−),①式乘以2,和②式
4 3 3
相加,得到:2c(H+)+2c(NH)=3c(CH COO−)+c(CH COOH)+2c(OH−),P 点溶液呈酸性,
3 3
c(H+)>c(OH−),所以2c(NH)<3c(CH COO−)+c(CH COOH),C正确;D.Q点溶液中溶质为物质
3 3
的量之比为1∶1的醋酸和氯化铵,铵根离子水解,则c(Cl−)>c(NH),因醋酸电离程度小且水
也电离出氢离子,则c(NH)>c(H+)>c(CH COO−),所以c(Cl−)>c(NH)>c(H+)>c(CH COO−),D错
3 3
误;故选AC。
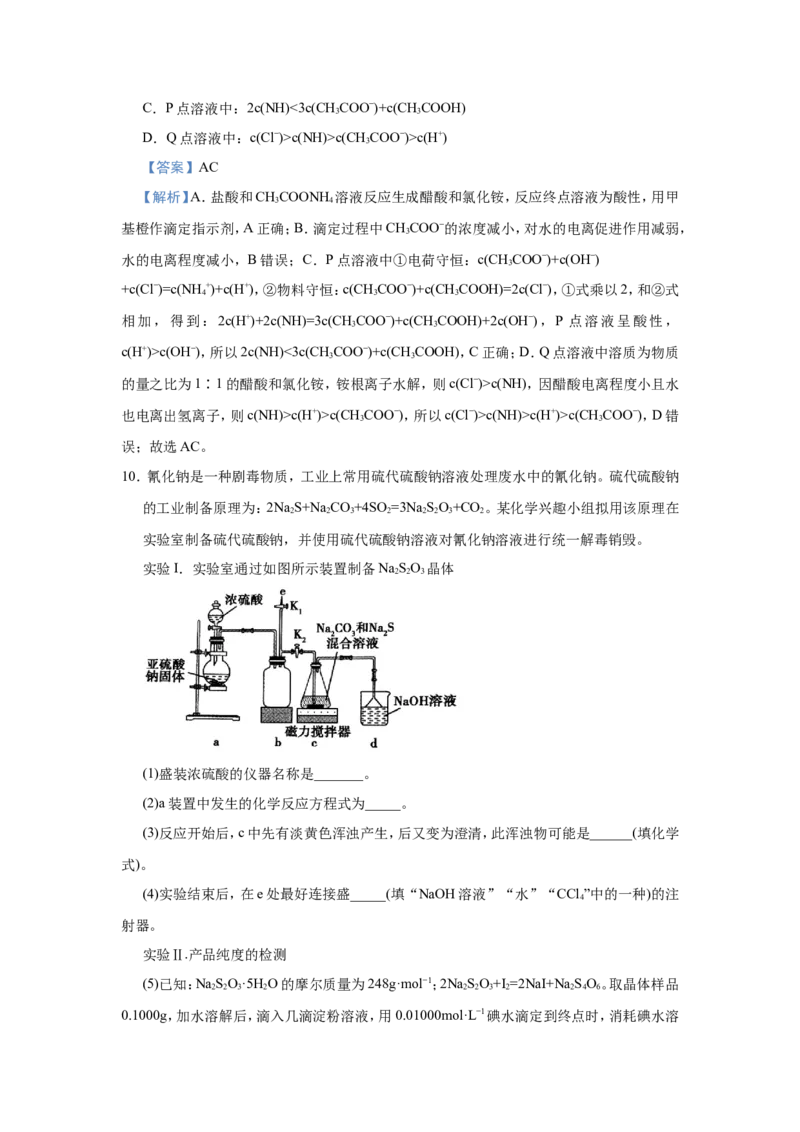
10.氰化钠是一种剧毒物质,工业上常用硫代硫酸钠溶液处理废水中的氰化钠。硫代硫酸钠
的工业制备原理为:2NaS+Na CO+4SO=3Na SO+CO 。某化学兴趣小组拟用该原理在
2 2 3 2 2 2 3 2
实验室制备硫代硫酸钠,并使用硫代硫酸钠溶液对氰化钠溶液进行统一解毒销毁。
实验I.实验室通过如图所示装置制备NaSO 晶体
2 2 3
(1)盛装浓硫酸的仪器名称是_______。
(2)a装置中发生的化学反应方程式为_____。
(3)反应开始后,c中先有淡黄色浑浊产生,后又变为澄清,此浑浊物可能是______(填化学
式)。
(4)实验结束后,在e处最好连接盛_____(填“NaOH溶液”“水”“CCl ”中的一种)的注
4
射器。
实验Ⅱ.产品纯度的检测
(5)已知:NaSO·5H O的摩尔质量为248g·mol−1;2NaSO+I =2NaI+Na SO。取晶体样品
2 2 3 2 2 2 3 2 2 4 6
0.1000g,加水溶解后,滴入几滴淀粉溶液,用0.01000mol·L−1碘水滴定到终点时,消耗碘水溶液15.00mL,则该样品的纯度是______。(保留三位有效数字)
(6)滴定过程中可能造成实验结果偏高的是_____(填字母)。
A.锥形瓶未用NaSO 溶液润洗
2 2 3
B.锥形瓶中溶液变蓝后立刻停止滴定,进行读数
C.滴定到终点时仰视读数
D.滴定管尖嘴内滴定前无气泡,滴定到终点出现气泡
【答案】(1)分液漏斗
(2)HSO (浓)+Na SO =Na SO +SO↑+H O
2 4 2 3 2 4 2 2
(3)S
(4)NaOH溶液
(5)74.4%
(6)C
【解析】a装置制备二氧化硫,c装置制备NaSO,反应导致装置内气压减小,所以b为安
2 2 3
全瓶,防止溶液倒吸,d装置吸收多余的二氧化硫,防止污染空气。I.(1)盛装浓硫酸的仪器名
称是分液漏斗;(2)a装置中浓硫酸和亚硫酸钠固体反应制备二氧化硫,化学反应方程式为
HSO (浓)+Na SO =Na SO +SO↑+H O;(3)二氧化硫与水反应生成亚硫酸,类似二氧化硫与
2 4 2 3 2 4 2 2
硫化氢的反应,酸性条件下,亚硫酸氧化硫离子生成S单质,所以此浑浊物是S;(4)实验结束
后,装置b中还有残留的二氧化硫,尾气中有未反应的二氧化硫,为防止污染空气,应用
NaOH溶液吸收,则在e处最好连接盛NaOH溶液的注射器;Ⅱ.(5)滴定所用单质碘的物质
的 量 为 n(I)=0.01000mol·L−1×0.01500L=0.00015mol , 根 据 反 应 方 程 式
2
2NaSO+I =2NaI+Na SO 可 知 , n(Na SO)=2n(I )=0.00030mol , 则 m(Na SO·5H O)=
2 2 3 2 2 4 6 2 2 3 2 2 2 3 2
0.00030mol×248g·mol−1=0.0744g,该样品的纯度为 ×100%=74.4%;(6)A.锥形瓶未用
NaSO 溶液润洗,对实验结果无影响,故A不选;B.锥形瓶中溶液变蓝后立刻停止滴定,进
2 2 3
行读数,消耗碘水的体积偏小,造成实验结果偏低,故B不选;C.滴定到终点时仰视读数,读
取的碘水体积偏大,造成实验结果偏高,故C选;D.滴定管尖嘴内滴定前无气泡,滴定到终
点出现气泡,碘水体积偏小,造成实验结果偏低,故D不选;答案选C。
11.二氧化氯(ClO )很不稳定,是一种在水处理等方面有广泛应用的高效安全消毒剂。实验
2
室以NH Cl、盐酸、NaClO(亚氯酸钠)为原料制备ClO ,制备的ClO 用水吸收得到ClO
4 2 2 2 2
溶液。为测定所得溶液中ClO 的含量,进行了下列实验:
2步骤1:准确量取ClO 溶液10.00mL,稀释成100.0mL试样;
2
步骤2:量取10.00mL试样加入到碘量瓶中,用适量的稀硫酸调节试样的pH≤2.0,加入足
量的KI晶体,摇匀,在暗处静置30min。
步骤3:用0.01000mol·L−1 Na SO 标准溶液滴定至溶液呈微黄色,加入淀粉溶液作指示
2 2 3
剂,继续滴定至终点,消耗NaSO 溶液20.00mL(已知I+2SO=2I−+SO)。
2 2 3 2 2 4
(1)若步骤2中未将锥形瓶“在暗处静置30min”,立即进行步骤3,则测定的结果可能
____(选填“偏大”、“偏小”或“无影响”)。
(2)上述步骤3中滴定终点的现象是______。
(3)请根据上述步骤计算出原ClO 溶液的浓度(用g·L−1表示)________。
2
【答案】(1)偏小
(2)滴入最后一滴标准液,溶液由蓝色变为无色,且半分钟内不褪色
(3)2.7
【解析】(1)在暗处静置是为了使ClO 与KI充分反应,若不静置,ClO 反应不完全,生成
2 2
的碘偏小,故测得的结果就偏小,故答案为:偏小;(2)由于碘遇淀粉显蓝色,所以步骤3中滴
定终点的现象是滴入最后一滴标准液,溶液由蓝色变为无色,且半分钟内不褪色;(3)ClO 溶
2
液与碘化钾反应的离子方程式:2ClO +10I−+8H+=5I +2Cl−+4H O,由I+2SO=2I−+SO,可得
2 2 2 2 2 4
ClO ~5SO,所以原 ClO 溶液的浓度为:
2 2 2
=2.7g/L。
12.Ⅰ.某工厂废水中含游离态氯,通过下列实验测定其浓度。
①取水样10.0mL于锥形瓶中,加入10.0mL的KI溶液(足量),发生反应,滴入指示剂2~
3滴。
②取一滴定管依次用自来水、蒸馏水洗净后,再用0.01mol·L−1 NaSO 溶液润洗,然后装
2 2 3
入0.01mol·L−1 NaSO 溶液到0刻度以上,排出下端尖嘴内的气泡,调整液面至0刻度或0刻
2 2 3
度下某一位置,记下读数。
③将锥形瓶置于滴定管下进行滴定,发生的反应为:I+2Na SO=2NaI+Na SO。试回答
2 2 2 3 2 4 6
下列问答:
(1)步骤①中涉及的离子反应方程式_____________________加入的指示剂是________。
(2)步骤②应使用________式滴定管。Ⅱ.(3)若用0.1032mol/L HCl溶液滴定未知浓度的NaOH溶液,下列情况对实验结果无影
响的是____________。
A.酸式滴定管未用标准盐酸溶液润洗
B.锥形瓶未用待测液润洗
C.滴定前滴定管尖嘴中有一气泡,滴定后气泡消失了
D.滴定时将标准液溅出锥形瓶外
(4)碳酸HCO :K =4.3×10−7,K =5.6×10−11,草酸HC O :K =5.9×10−2,K =6.4×10−5。
2 3 1 2 2 2 4 1 2
0.1mol/L Na CO 溶液的pH____________0.1mol/L Na C O 溶液的pH(选填“大于”、“小
2 3 2 2 4
于”或“等于”)。若将等浓度的草酸溶液和碳酸溶液等体积混合,溶液中各种离子浓度大小
的顺序正确的是_____________(填选项字母代号)。
A.c(H+)>c(HC O)>c(HCO)>c(CO)
2
B.c(HCO)>c(HC O)>c(C O)>c(CO)
2 2
C.c(H+)>c(HC O)>c(C O)>c(CO)
2 2
D.c(H CO)>c(HCO)>c(HC O)>c(CO)
2 3 2
【答案】(1)Cl+2I−=2Cl−+I 淀粉溶液
2 2
(2)碱
(3)B
(4)大于 AC
【解析】氧化还原滴定法是以氧化还原反应为基础的滴定分析方法,工厂废水中含游离态
氯,和KI反应生成碘单质和氯离子,离子方程式为:Cl+2I−=2Cl−+I ;溶液中有单质碘,加入
2 2
淀粉溶液呈蓝色,碘与 NaSO 发生氧化还原反应,当反应终点时,蓝色褪去,根据
2 2 3
计算待测液浓度和进行误差分析。(1)工厂废水中含游离态氯,和
KI反应生成碘单质和氯离子,离子方程式为:Cl+2I−=2Cl−+I ;溶液中有单质碘,加入淀粉溶
2 2
液呈蓝色,碘与 NaSO 发生氧化还原反应,当反应终点时,蓝色褪去。故答案为:
2 2 3
Cl+2I−=2Cl−+I ;淀粉溶液;(2)硫代硫酸钠溶液显碱性,应选择碱式滴定管。故答案为:碱;
2 2
(3)A.酸式滴定管未用标准盐酸溶液润洗,标准盐酸的浓度偏小,造成V(标准)偏大,根据可知,测定c(待测)偏大,故A错误; B.锥形瓶未用待测液润洗,
对V(标准)无影响,根据 可知,测定c(待测)无影响,故B正确;
C.滴定前滴定管尖嘴中有一气泡,滴定后气泡消失了,造成 V(标准)偏大,根据
可知,测定c(待测)偏大,故C错误;D.滴定时将标准液溅出锥形瓶
外,造成V(标准)偏大,根据 可知,测定c(待测)偏大,故D错误;故
选:B;(5)草酸的二级电离常数等于碳酸的二级电离常数,说明草酸氢根的酸性比碳酸氢根
的强,则0.1mol/L Na CO 溶液中碳酸根的水解程度大于0.1mol/L Na C O 溶液中草酸根的水
2 3 2 2 4
解程度,故0.1mol/L Na CO 溶液碱性更强,即0.1mol/L Na CO 溶液的pH大于0.1mol/L
2 3 2 3
NaC O 溶液的pH,草酸的一级、二级电离常数均大于碳酸的一级电离常数,草酸、碳酸的一
2 2 4
级电离远大于二级电离,第一步电离为主,因此溶液中c(H+)>c(HC O)>c(HCO)>c(CO);
2
c(H+)>c(HC O)>c(C O)>c(CO),则AC正确,BD错误。故答案为:大于;AC。
2 2
13.炼铁的矿物主要有赤铁矿、磁铁矿和菱铁矿等。目前主要采用以下流程测定铁矿石中铁
元素的含量,流程分为两个环节:铁矿石预处理和重铬酸钾滴定。
滴定过程:向预处理结束的溶液中加入适量蒸馏水和硫酸磷酸混合酸,滴加数滴二苯胺
磺酸钠,用重铬酸钾标准溶液滴定,记录终点体积V。
已知:i.钨酸钠(NaWO)可用作指示剂,若钨由+6价变为+5价,则溶液变为蓝色。
2 4
ii.Sn2+和Ti3+均具有还原性。
iii.氧化性顺序为Cr O>Fe3+>WO。
2
iV.二苯胺磺酸钠可用作氧化还原指示剂,本身无色,被氧化后呈现紫红色。
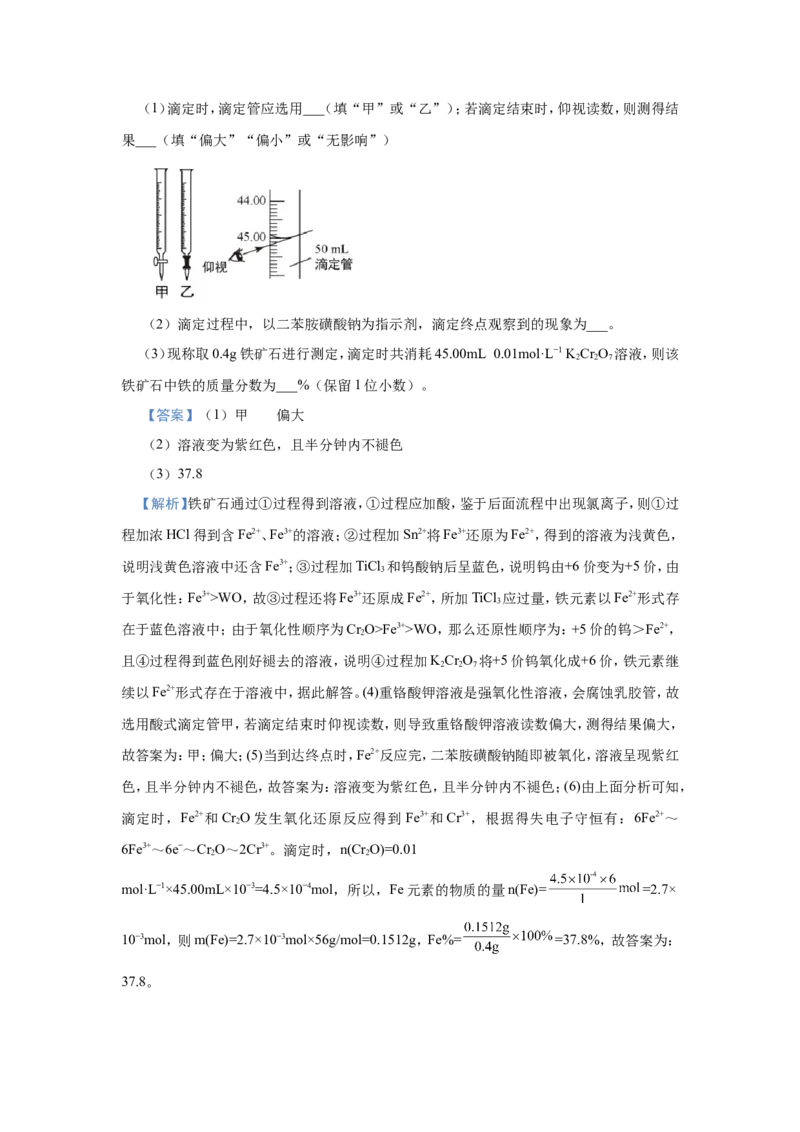
请回答下列问题:(1)滴定时,滴定管应选用___(填“甲”或“乙”);若滴定结束时,仰视读数,则测得结
果___(填“偏大”“偏小”或“无影响”)
(2)滴定过程中,以二苯胺磺酸钠为指示剂,滴定终点观察到的现象为___。
(3)现称取0.4g铁矿石进行测定,滴定时共消耗45.00mL 0.01mol·L−1 KCr O 溶液,则该
2 2 7
铁矿石中铁的质量分数为___%(保留1位小数)。
【答案】(1)甲 偏大
(2)溶液变为紫红色,且半分钟内不褪色
(3)37.8
【解析】铁矿石通过①过程得到溶液,①过程应加酸,鉴于后面流程中出现氯离子,则①过
程加浓HCl得到含Fe2+、Fe3+的溶液;②过程加Sn2+将Fe3+还原为Fe2+,得到的溶液为浅黄色,
说明浅黄色溶液中还含Fe3+;③过程加TiCl 和钨酸钠后呈蓝色,说明钨由+6价变为+5价,由
3
于氧化性:Fe3+>WO,故③过程还将Fe3+还原成Fe2+,所加TiCl 应过量,铁元素以Fe2+形式存
3
在于蓝色溶液中;由于氧化性顺序为Cr O>Fe3+>WO,那么还原性顺序为:+5价的钨>Fe2+,
2
且④过程得到蓝色刚好褪去的溶液,说明④过程加KCr O 将+5价钨氧化成+6价,铁元素继
2 2 7
续以Fe2+形式存在于溶液中,据此解答。(4)重铬酸钾溶液是强氧化性溶液,会腐蚀乳胶管,故
选用酸式滴定管甲,若滴定结束时仰视读数,则导致重铬酸钾溶液读数偏大,测得结果偏大,
故答案为:甲;偏大;(5)当到达终点时,Fe2+反应完,二苯胺磺酸钠随即被氧化,溶液呈现紫红
色,且半分钟内不褪色,故答案为:溶液变为紫红色,且半分钟内不褪色;(6)由上面分析可知,
滴定时,Fe2+和Cr O发生氧化还原反应得到 Fe3+和Cr3+,根据得失电子守恒有:6Fe2+~
2
6Fe3+~6e−~Cr O~2Cr3+。滴定时,n(CrO)=0.01
2 2
mol·L−1×45.00mL×10−3=4.5×10−4mol,所以,Fe元素的物质的量n(Fe)= =2.7×
10−3mol,则m(Fe)=2.7×10−3mol×56g/mol=0.1512g,Fe%= =37.8%,故答案为:
37.8。