文档内容
(新高考)小题必练15:难溶电解质的电离平衡
主要考查沉淀溶解平衡的特点和影响因素,溶度积常数及其计算,沉淀的生成、溶解和转
化的应用,利用溶度积常数判断难溶电解质的溶解度,离子沉淀时应调节的pH范围等。
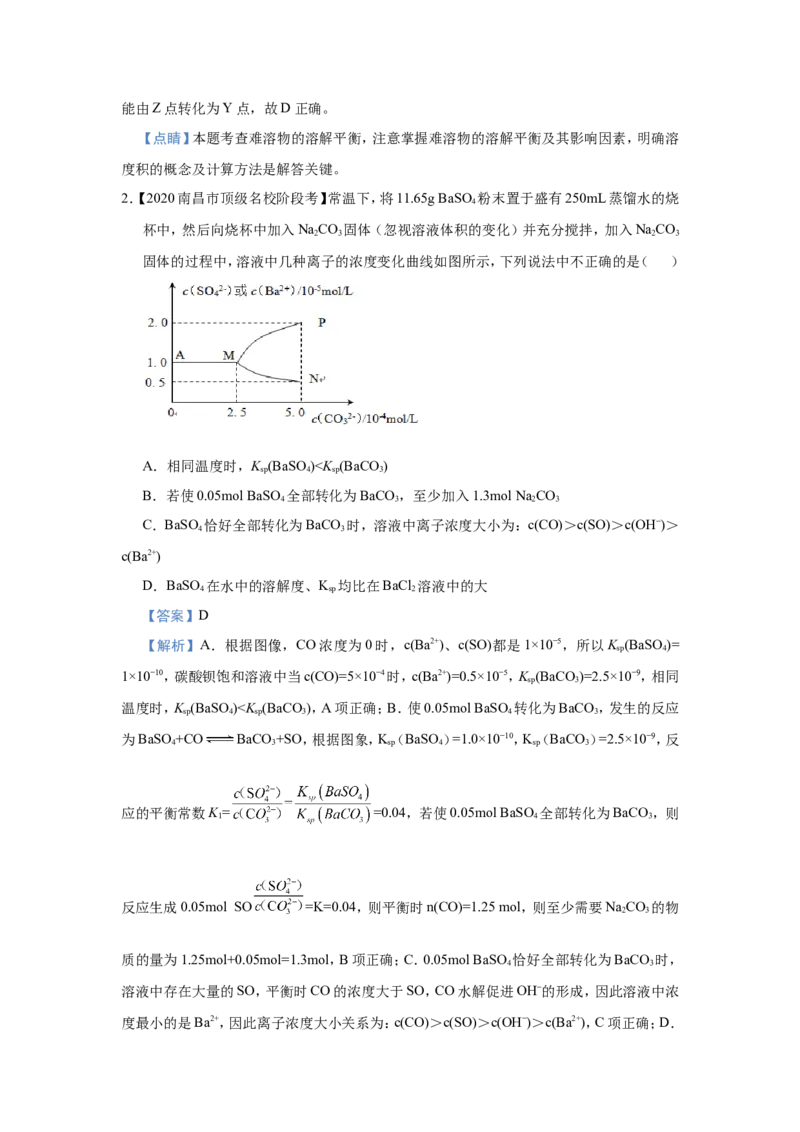
1.【2020年江苏卷】25℃时,Fe(OH) 和Cu(OH) 的饱和溶液中,金属阳离子的物质的量浓度
2 2
的负对数[-lgc(M2+)]与溶液 pH 的变化关系如图所示,已知该温度下 K [Cu(OH) ]<
sp 2
K [Fe(OH) ]。下列说法不正确的是( )
sp 2
A.K [Cu(OH) ]的数量级为10−20
sp 2
B.当Fe(OH) 和Cu(OH) 沉淀共存时,溶液中c(Fe2+)∶c(Cu2+)=104.6∶1
2 2
C.除去CuSO 溶液中含有的少量Fe2+,可加入适量CuO
4
D.向Z点对应的饱和溶液中加入少量NaOH固体,可转化为Y点对应的溶液
【答案】C
【解析】25℃时,由K [Cu(OH) ]<K [Fe(OH) ]可知溶液pH相同时,饱和溶液中c(Fe2+) >
sp 2 sp 2
c(Cu2+),则曲线a表示Cu(OH) 的饱和溶液中金属阳离子的物质的量浓度的负对数与溶液
2
pH的变化关系,曲线b表示Fe(OH) 的饱和溶液中金属阳离子的物质的量浓度的负对数与
2
溶液pH的变化关系。A项、由图可知,曲线a中pH=10时,-lgc(M2+)=11.7,则K [Cu(OH) ]=
sp 2
c(Cu2+)·c2(OH−)=10−11.7×(10−4)2=10−19.7,故A正确;B项、当Fe(OH) 和Cu(OH) 沉淀共存时,
2 2
溶液中c(OH−)相同,当pH=10时,溶液中c(Fe2+)∶c(Cu2+)=10−7.1:10−11.7=104.6∶1,故B正确;C项、
该温度下K [Cu(OH) ]<K [Fe(OH) ]可知,Cu(OH) 比Fe(OH) 更难溶,加入适量CuO调节
sp 2 sp 2 2 2
溶液pH,先沉淀的是Cu2+,无法达到除去少量Fe2+的目的,故C错误;D项、向Z点对应的饱
和溶液中加入少量NaOH固体,溶液中c(OH−)增大,温度不变K [Fe(OH) ],c(Fe2+)减小,可
sp 2能由Z点转化为Y点,故D正确。
【点睛】本题考查难溶物的溶解平衡,注意掌握难溶物的溶解平衡及其影响因素,明确溶
度积的概念及计算方法是解答关键。
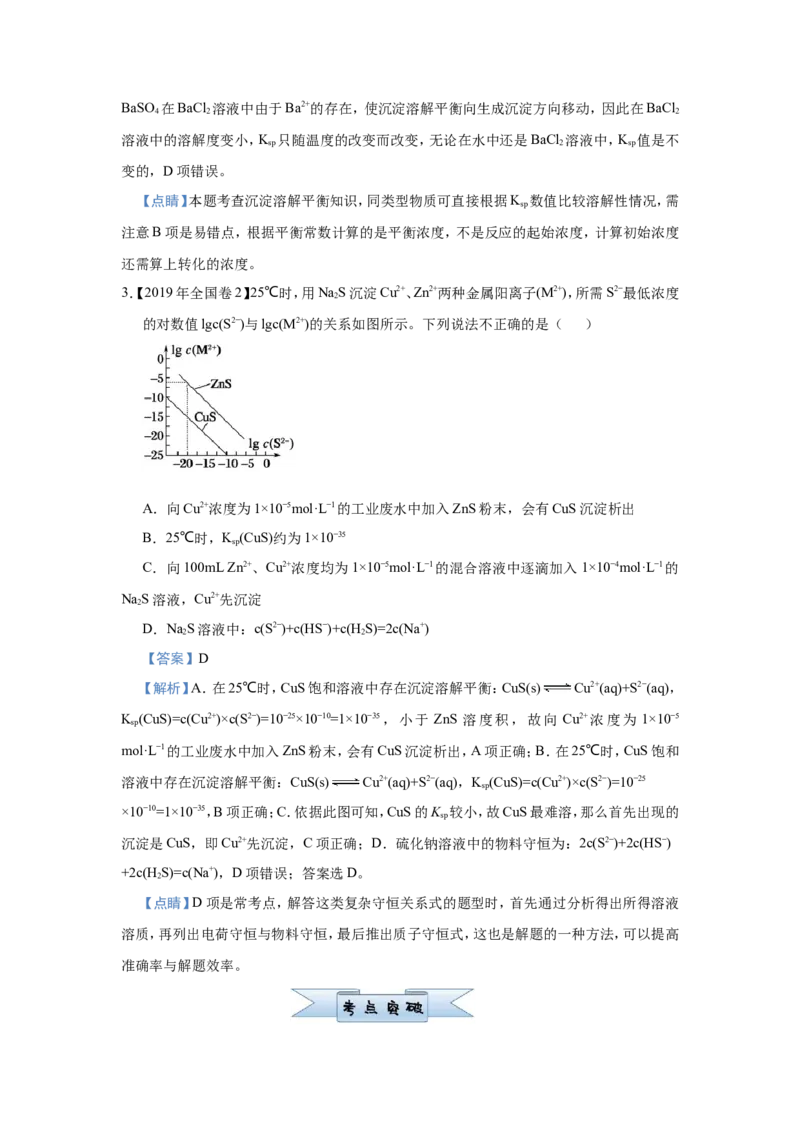
2.【2020南昌市顶级名校阶段考】常温下,将11.65g BaSO 粉末置于盛有250mL蒸馏水的烧
4
杯中,然后向烧杯中加入NaCO 固体(忽视溶液体积的变化)并充分搅拌,加入NaCO
2 3 2 3
固体的过程中,溶液中几种离子的浓度变化曲线如图所示,下列说法中不正确的是( )
A.相同温度时,K (BaSO)③>④>⑥>⑤>① B.①>⑥>⑤>②>④>③
C.①>②>③>④>⑤>⑥ D.③>②>④>⑥>①>⑤
【答案】B
【解析】AgCl在溶液中存在溶解平衡AgCl(aq) Ag+(aq)+Cl−(aq),由于c(Ag+)或c(Cl−)
对溶解平衡有抑制作用,则溶液中c(Ag+)或c(Cl−)越大,则AgCl的溶解度越小;①和⑥中铵
根离子水解生成NH ·HO,Ag+与NH ·HO结合,使溶解平衡正移,AgCl的溶解度增大,由于
3 2 3 2
(NH )CO 中NH水解程度大,则NH ·HO的浓度大,使溶解平衡正移的程度大,则①>⑥;当
4 2 3 3 2
溶 液 中 存 在 c(Ag+) 或 c(Cl−) 对 溶 解 平 衡 有 抑 制 作 用 , ② c(Cl−)=0.03mol/L ,
③c(Ag+)=0.05mol/L,④c(Cl−)=0.04mol/L,⑤c(Ag+)或c(Cl−)为0,则AgCl的溶解度由大到小
排列顺序是:⑤>②>④>③,综上可知 AgCl 的溶解度由大到小排列顺序是:
①>⑥>⑤>②>④>③;故合理选项是B。
【点睛】本题考查难溶电解质的溶解平衡,注意影响平衡移动的因素,需要理清的是离子
浓度大小与难溶电解质的溶解度的关系。
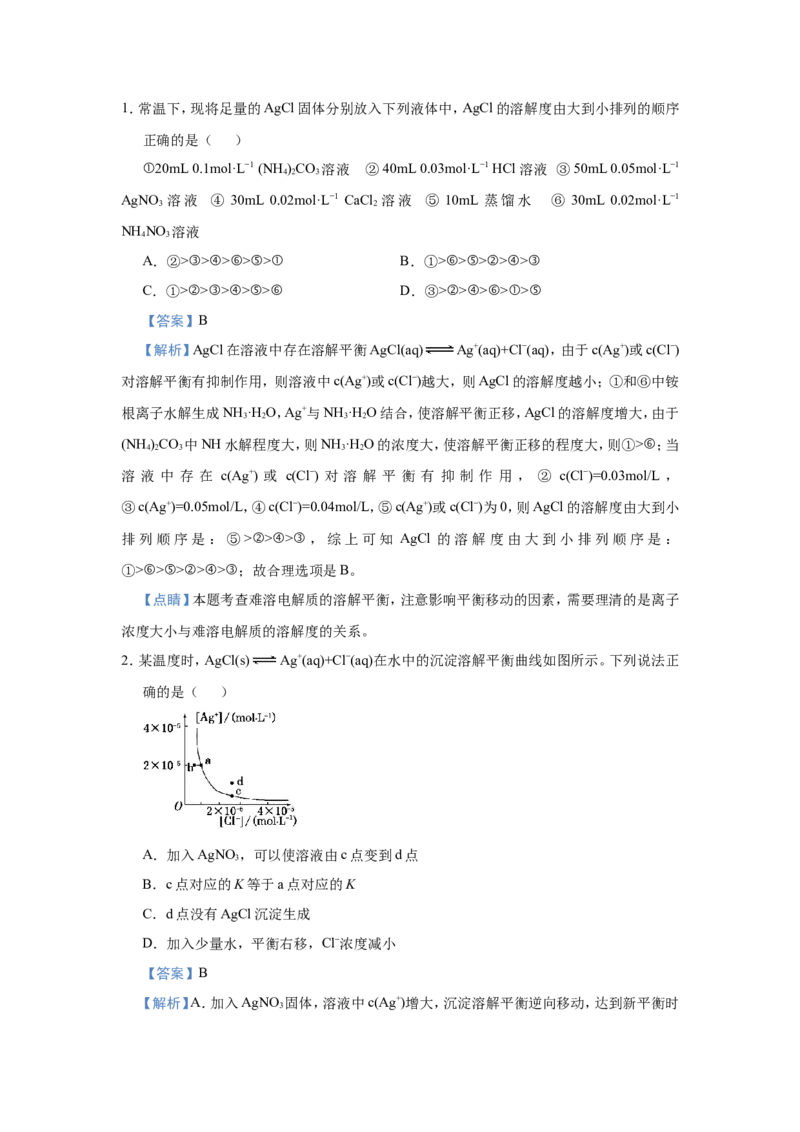
2.某温度时,AgCl(s) Ag+(aq)+Cl−(aq)在水中的沉淀溶解平衡曲线如图所示。下列说法正
确的是( )
A.加入AgNO,可以使溶液由c点变到d点
3
B.c点对应的K等于a点对应的K
C.d点没有AgCl沉淀生成
D.加入少量水,平衡右移,Cl−浓度减小
【答案】B
【解析】A.加入AgNO 固体,溶液中c(Ag+)增大,沉淀溶解平衡逆向移动,达到新平衡时
3c(Cl−)减小,而c、d两点的氯离子浓度相同,选项A错误;B.温度不变K 不变,a、c两点温度
sp
相同,所以 K 也相同,选项 B 正确;C.d 点处 c(Ag+)比平衡时的大,此时
sp
Qc=c(Ag+)·c(Cl−)>K (AgCl),所以有AgCl沉淀生成,选项C错误;D.溶液中存在着沉淀溶解
sp
溶解平衡,加入少量水,促进溶解,但是仍然为饱和溶液,因此溶液中各种离子浓度不变,选
项D错误。
【点睛】本题考查沉淀溶解平衡,注意理解难溶电解质在水中的沉淀溶解平衡特点,正确
理解和掌握溶度积K 的概念是本题解答的关键。
sp
3 . 已 知 25℃ 时 , RSO (s)+CO(aq) RCO(s)+SO(aq) 的 平 衡 常 数 K=1.75×104 ,
4 3
K (RCO)=2.80×10−9,下列叙述中正确的是( )
sp 3
A.25℃时,RSO 的K 约为4.9×10−5
4 sp
B.将浓度均为6×10−5mol/L的RCl 、NaCO 溶液等体积混合后可得到RCO 沉淀
2 2 3 3
C.向c(CO)=c(SO)的混合液中滴加RCl 溶液,首先析出RSO 沉淀
2 4
D.相同温度下,RCO 在水中的K 大于在NaCO 溶液中的K
3 sp 2 3 sp
【答案】A
【 解 析 】 25℃ 时 , RSO (s)+CO(aq) RCO(s)+SO(aq) 的 平 衡 常 数 K=
4 3
=1.75×104,K (RSO)=1.75×104×K (RCO)=1.75×
sp 4 sp 3
104×2.80×10−9=4.9×10−5。A.根据上述计算分析,25℃时,RSO 的K 约为4.9×10−5,故A正确;
4 sp
B.将浓度均为6×10−5mol/L的RCl 、NaCO 溶液等体积混合,则浓度变为原来的一半,混合
2 2 3
后 溶 液 中 c(R2+)=3×10−5mol/L , c(CO)=3×10−5mol/L , Q(RCO)=c(R2+)∙
c 3
c(CO)=3×10−5mol/L×3×10−5mol/L=9×10−10K (RCO),向c(CO)=c(SO)的混合液中滴加RCl
4 3 sp 4 sp 3 2
溶液,首先析出RCO 沉淀,故C错误;D.K 只与温度有关,与浓度无关,相同温度下RCO
3 sp 3
在水中的K 等于在NaCO 溶液中的K ,故D错误;答案选A。
sp 2 3 sp
【点睛】本题易错点在于D选项,K 也属于平衡常数,只与温度有关,与溶液中离子浓度
sp
大小无关。
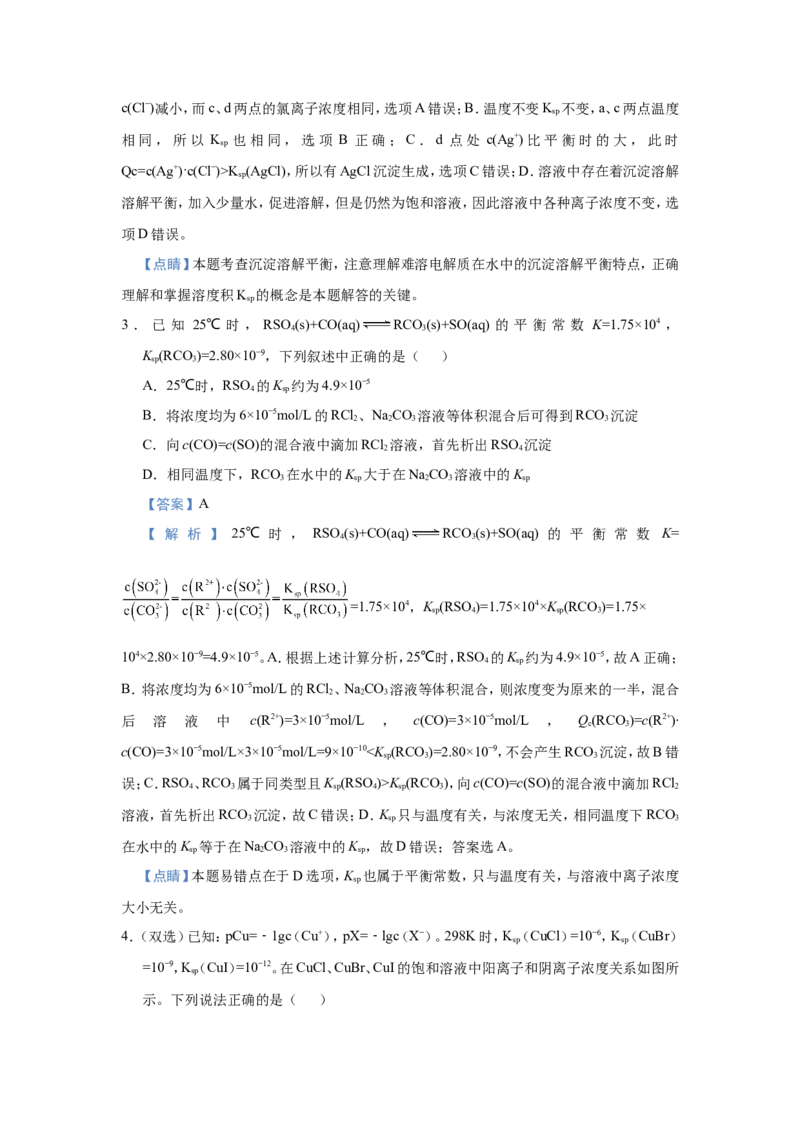
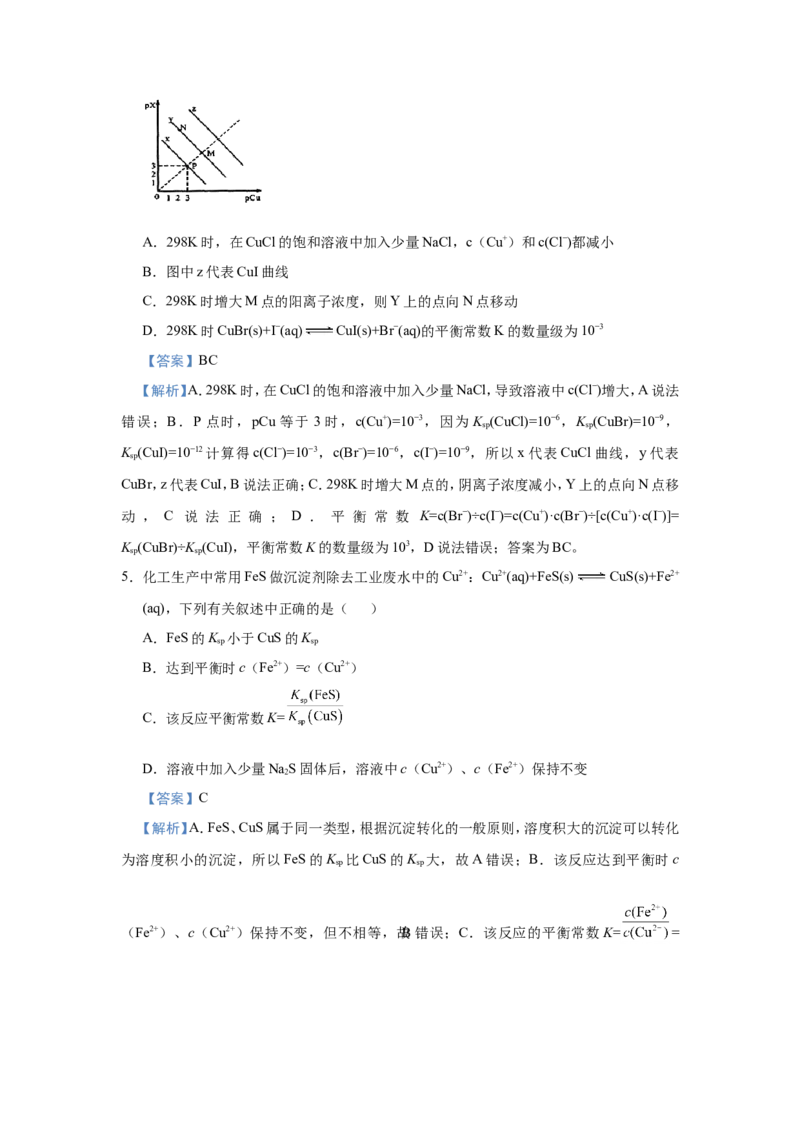
4.(双选)已知:pCu=﹣1gc(Cu+),pX=﹣lgc(X−)。298K时,K(CuCl)=10−6,K(CuBr)
sp sp
=10−9,K(CuI)=10−12。在CuCl、CuBr、CuI的饱和溶液中阳离子和阴离子浓度关系如图所
sp
示。下列说法正确的是( )A.298K时,在CuCl的饱和溶液中加入少量NaCl,c(Cu+)和c(Cl−)都减小
B.图中z代表CuI曲线
C.298K时增大M点的阳离子浓度,则Y上的点向N点移动
D.298K时CuBr(s)+I−(aq) CuI(s)+Br−(aq)的平衡常数K的数量级为10−3
【答案】BC
【解析】A.298K时,在CuCl的饱和溶液中加入少量NaCl,导致溶液中c(Cl−)增大,A说法
错误;B.P 点时,pCu 等于 3 时,c(Cu+)=10−3,因为 K (CuCl)=10−6,K (CuBr)=10−9,
sp sp
K (CuI)=10−12计算得c(Cl−)=10−3,c(Br−)=10−6,c(I−)=10−9,所以x代表CuCl曲线,y代表
sp
CuBr,z代表CuI,B说法正确;C.298K时增大M点的,阴离子浓度减小,Y上的点向N点移
动 , C 说 法 正 确 ; D . 平 衡 常 数 K=c(Br−)÷c(I−)=c(Cu+)·c(Br−)÷[c(Cu+)·c(I−)]=
K (CuBr)÷K (CuI),平衡常数K的数量级为103,D说法错误;答案为BC。
sp sp
5.化工生产中常用FeS做沉淀剂除去工业废水中的Cu2+:Cu2+(aq)+FeS(s) CuS(s)+Fe2+
(aq),下列有关叙述中正确的是( )
A.FeS的K 小于CuS的K
sp sp
B.达到平衡时c(Fe2+)=c(Cu2+)
C.该反应平衡常数K=
D.溶液中加入少量NaS固体后,溶液中c(Cu2+)、c(Fe2+)保持不变
2
【答案】C
【解析】A.FeS、CuS属于同一类型,根据沉淀转化的一般原则,溶度积大的沉淀可以转化
为溶度积小的沉淀,所以FeS的K 比CuS的K 大,故A错误;B.该反应达到平衡时c
sp sp
(Fe2+)、c(Cu2+)保持不变,但不相等,故B错误;C.该反应的平衡常数K= == ,故C正确;D.增大硫离子的浓度,平衡左向移动,所以c(Cu2+)、c
(Fe2+)均减小,故D错误;故选C。
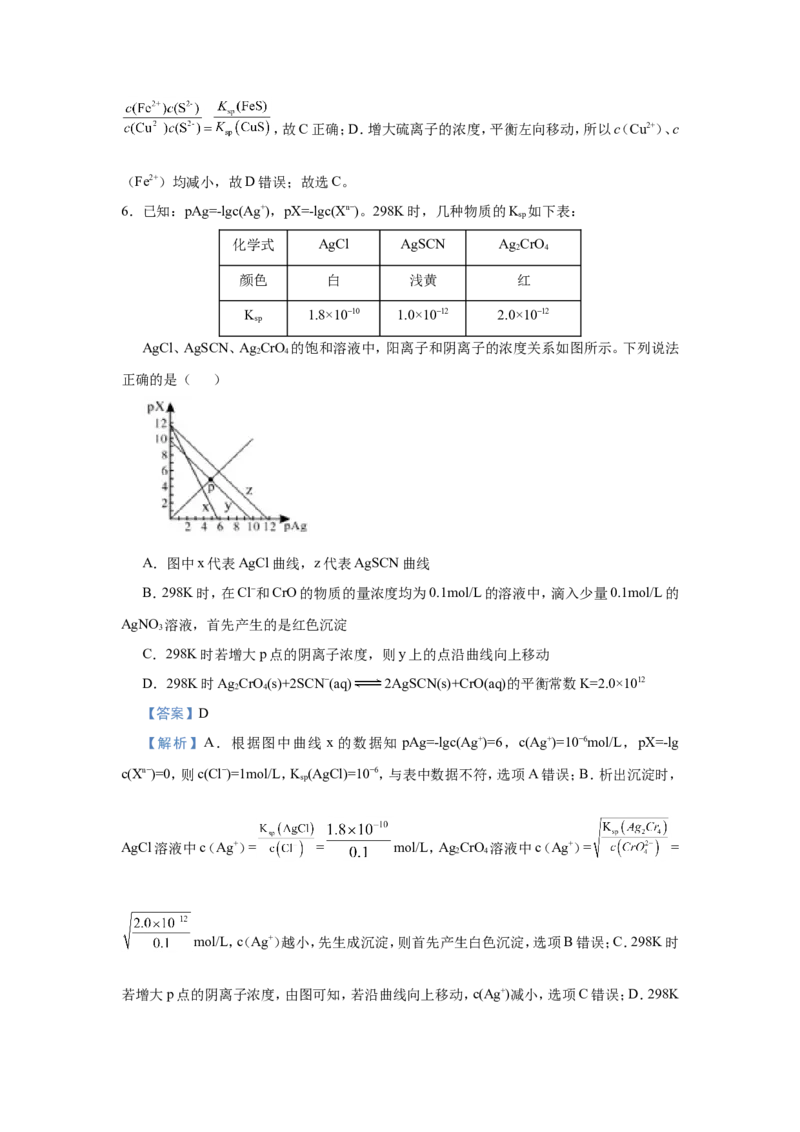
6.已知:pAg=-lgc(Ag+),pX=-lgc(Xn−)。298K时,几种物质的K 如下表:
sp
化学式 AgCl AgSCN Ag CrO
2 4
颜色 白 浅黄 红
K 1.8×10‒10 1.0×10‒12 2.0×10‒12
sp
AgCl、AgSCN、Ag CrO 的饱和溶液中,阳离子和阴离子的浓度关系如图所示。下列说法
2 4
正确的是( )
A.图中x代表AgCl曲线,z代表AgSCN曲线
B.298K时,在Cl−和CrO的物质的量浓度均为0.1mol/L的溶液中,滴入少量0.1mol/L的
AgNO 溶液,首先产生的是红色沉淀
3
C.298K时若增大p点的阴离子浓度,则y上的点沿曲线向上移动
D.298K时Ag CrO(s)+2SCN−(aq) 2AgSCN(s)+CrO(aq)的平衡常数K=2.0×1012
2 4
【答案】D
【解析】A.根据图中曲线 x 的数据知 pAg=-lgc(Ag+)=6,c(Ag+)=10−6mol/L,pX=-lg
c(Xn−)=0,则c(Cl−)=1mol/L,K (AgCl)=10−6,与表中数据不符,选项A错误;B.析出沉淀时,
sp
AgCl溶液中c(Ag+)= = mol/L,Ag CrO 溶液中c(Ag+)= =
2 4
mol/L,c(Ag+)越小,先生成沉淀,则首先产生白色沉淀,选项B错误;C.298K时
若增大p点的阴离子浓度,由图可知,若沿曲线向上移动,c(Ag+)减小,选项C错误;D.298K时 Ag CrO(s)+2SCN−(aq) 2AgSCN(s)+CrO(aq) 的 平 衡 常 数 K= =
2 4
= = =2.0×1012,选项D正确。
【点睛】本题考查沉淀的溶度积的应用,注意的含义pAg=-lgc(Ag+)、pX=-lgc(Xn−)、K ,易
sp
错点为选项D:K= = = ,结合表中数据进行计算求
解。
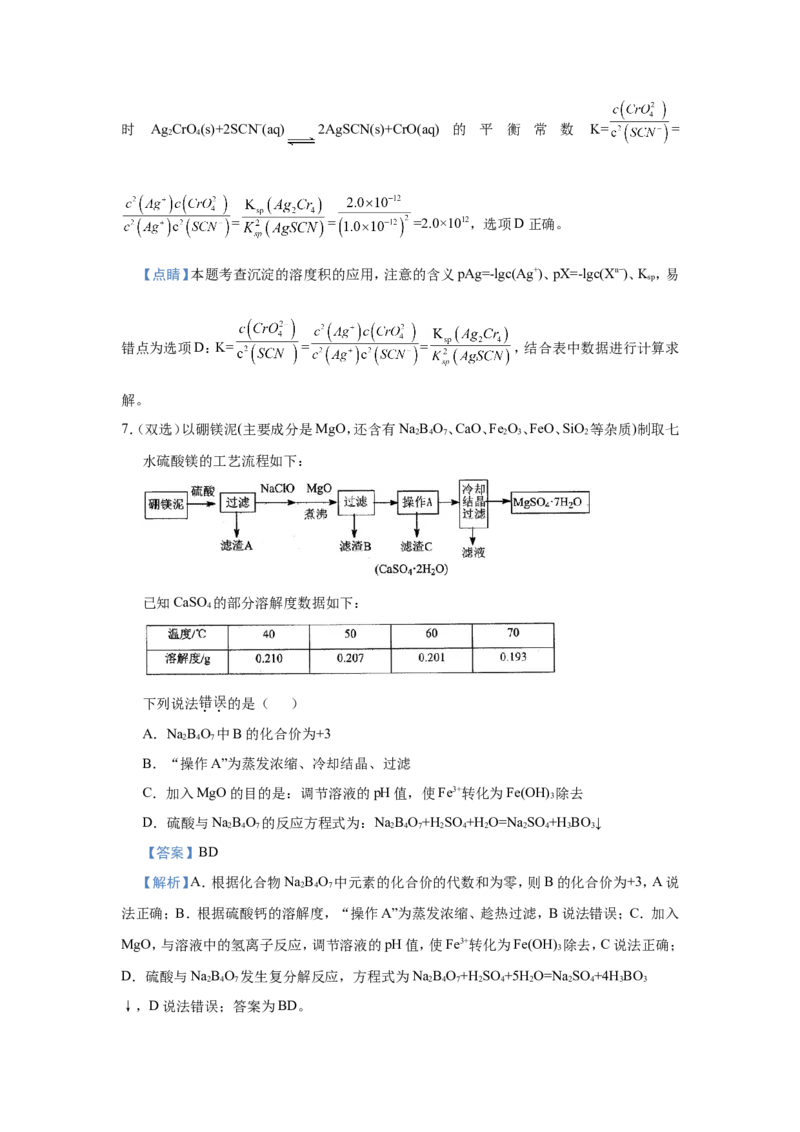
7.(双选)以硼镁泥(主要成分是MgO,还含有NaB O、CaO、Fe O、FeO、SiO 等杂质)制取七
2 4 7 2 3 2
水硫酸镁的工艺流程如下:
已知CaSO 的部分溶解度数据如下:
4
下列说法错误的是( )
A.NaB O 中B的化合价为+3
2 4 7
B.“操作A”为蒸发浓缩、冷却结晶、过滤
C.加入MgO的目的是:调节溶液的pH值,使Fe3+转化为Fe(OH) 除去
3
D.硫酸与NaB O 的反应方程式为:NaB O+HSO +HO=NaSO +HBO↓
2 4 7 2 4 7 2 4 2 2 4 3 3
【答案】BD
【解析】A.根据化合物NaB O 中元素的化合价的代数和为零,则B的化合价为+3,A说
2 4 7
法正确;B.根据硫酸钙的溶解度,“操作A”为蒸发浓缩、趁热过滤,B说法错误;C.加入
MgO,与溶液中的氢离子反应,调节溶液的pH值,使Fe3+转化为Fe(OH) 除去,C说法正确;
3
D.硫酸与NaB O 发生复分解反应,方程式为NaB O+H SO +5H O=NaSO +4H BO
2 4 7 2 4 7 2 4 2 2 4 3 3
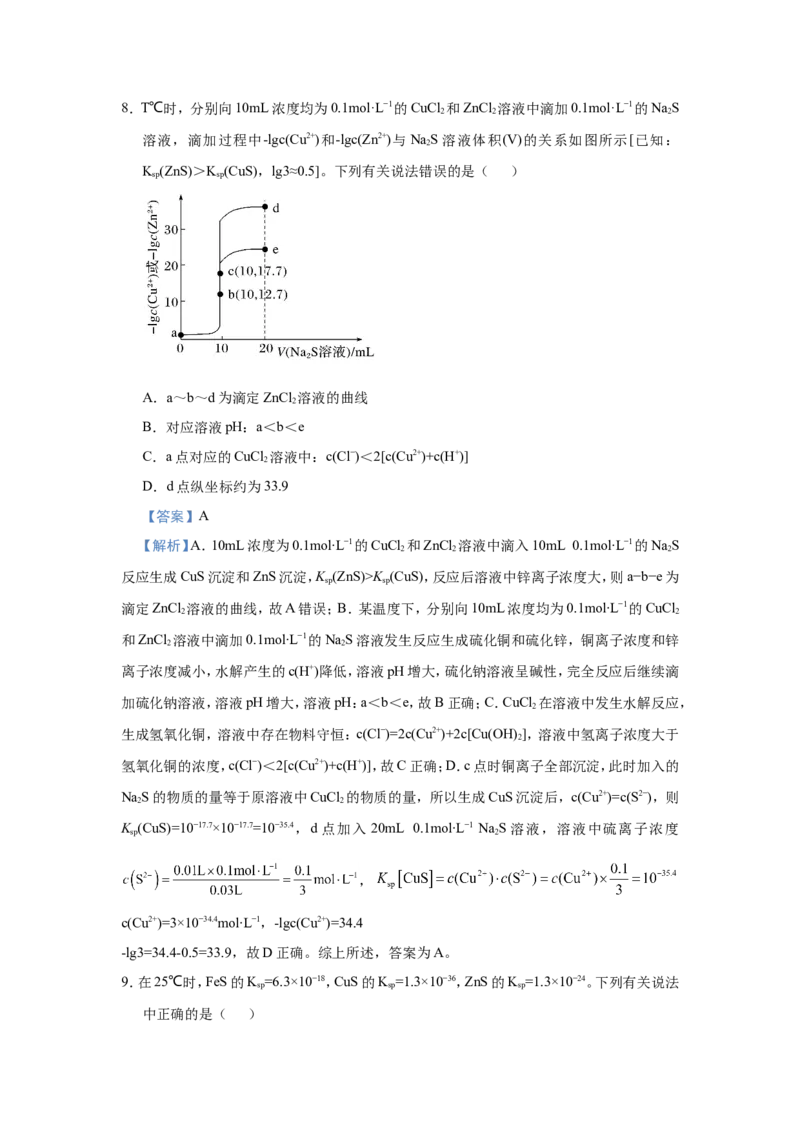
↓,D说法错误;答案为BD。8.T℃时,分别向10mL浓度均为0.1mol·L−1的CuCl 和ZnCl 溶液中滴加0.1mol·L−1的NaS
2 2 2
溶液,滴加过程中-lgc(Cu2+)和-lgc(Zn2+)与NaS溶液体积(V)的关系如图所示[已知:
2
K (ZnS)>K (CuS),lg3≈0.5]。下列有关说法错误的是( )
sp sp
A.a~b~d为滴定ZnCl 溶液的曲线
2
B.对应溶液pH:a<b<e
C.a点对应的CuCl 溶液中:c(Cl−)<2[c(Cu2+)+c(H+)]
2
D.d点纵坐标约为33.9
【答案】A
【解析】A.10mL浓度为0.1mol∙L−1的CuCl 和ZnCl 溶液中滴入10mL 0.1mol∙L−1的NaS
2 2 2
反应生成CuS沉淀和ZnS沉淀,K (ZnS)>K (CuS),反应后溶液中锌离子浓度大,则a−b−e为
sp sp
滴定ZnCl 溶液的曲线,故A错误;B.某温度下,分别向10mL浓度均为0.1mol∙L−1的CuCl
2 2
和ZnCl 溶液中滴加0.1mol∙L−1的NaS溶液发生反应生成硫化铜和硫化锌,铜离子浓度和锌
2 2
离子浓度减小,水解产生的c(H+)降低,溶液pH增大,硫化钠溶液呈碱性,完全反应后继续滴
加硫化钠溶液,溶液pH增大,溶液pH:a<b<e,故B正确;C.CuCl 在溶液中发生水解反应,
2
生成氢氧化铜,溶液中存在物料守恒:c(Cl−)=2c(Cu2+)+2c[Cu(OH) ],溶液中氢离子浓度大于
2
氢氧化铜的浓度,c(Cl−)<2[c(Cu2+)+c(H+)],故C正确;D.c点时铜离子全部沉淀,此时加入的
NaS的物质的量等于原溶液中CuCl 的物质的量,所以生成CuS沉淀后,c(Cu2+)=c(S2−),则
2 2
K (CuS)=10−17.7×10−17.7=10−35.4,d 点加入 20mL 0.1mol∙L−1 NaS 溶液,溶液中硫离子浓度
sp 2
,
c(Cu2+)=3×10−34.4mol∙L−1,-lgc(Cu2+)=34.4
-lg3=34.4-0.5=33.9,故D正确。综上所述,答案为A。
9.在25℃时,FeS的K =6.3×10−18,CuS的K =1.3×10−36,ZnS的K =1.3×10−24。下列有关说法
sp sp sp
中正确的是( )A.饱和CuS溶液中Cu2+的浓度为1.3×10−36mol·L−1
B.25℃时,FeS的溶解度大于CuS的溶解度
C.向物质的量浓度相同的FeCl 、ZnCl 的混合液中加入少量NaS,只有FeS沉淀生成
2 2 2
D.向饱和ZnS溶液中加入少量ZnCl 固体,ZnS的K 变大
2 sp
【答案】B
【解析】A.饱和CuS溶液中Cu2+的浓度为 = mol·L−1,故A错误;B.
由FeS的K =6.3×10−18、CuS的K =1.3×10−36可知,二者的组成形式相同,FeS的溶解度大于
sp sp
CuS的溶解度,故B正确;C.FeS的K =6.3×10−18、ZnS的K =1.3×10−24,向物质的量浓度相
sp sp
同的FeCl 、ZnCl 的混合液中加入少量NaS,首先生成溶解度小的沉淀,因此只有ZnS沉淀
2 2 2
生成,故C错误;D.向饱和ZnS溶液中存在ZnS的溶解平衡,加入少量ZnCl 固体,锌离子浓
2
度增大,溶解平衡逆向移动,但温度不变,ZnS的K 不变,故D错误。
sp
【点睛】比较溶解度大小的时候,应注意沉淀的类型必须相同。
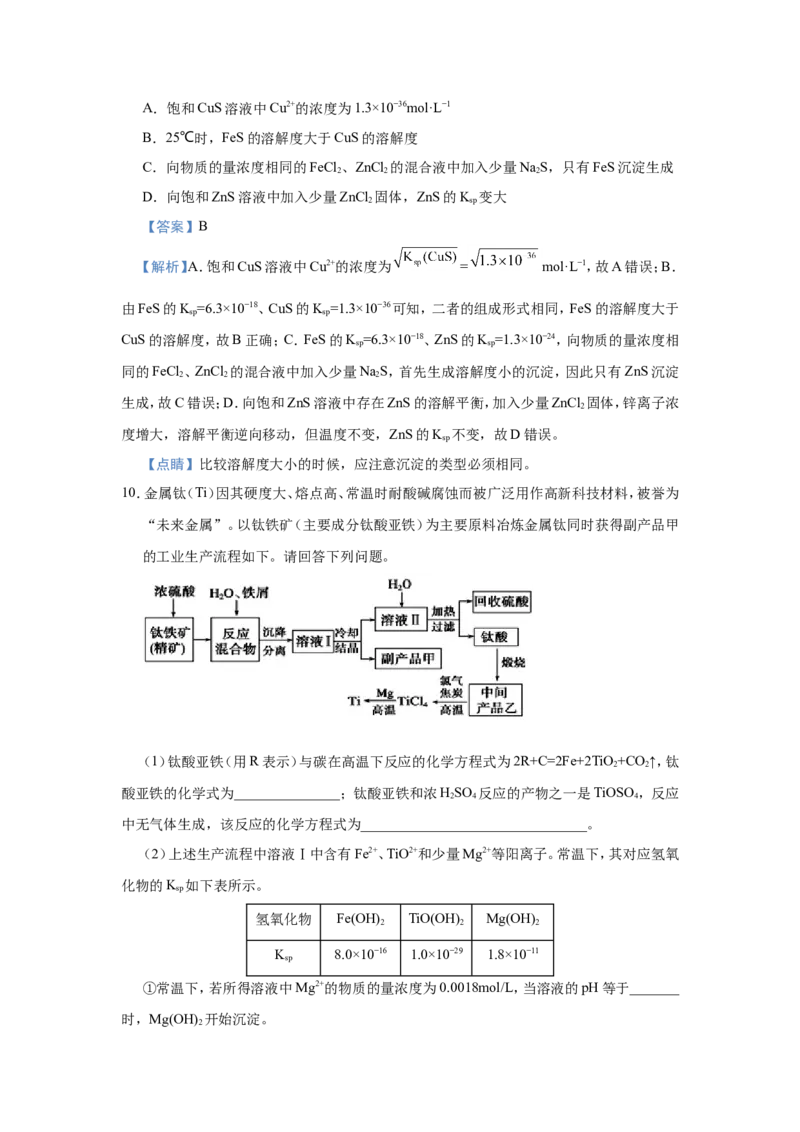
10.金属钛(Ti)因其硬度大、熔点高、常温时耐酸碱腐蚀而被广泛用作高新科技材料,被誉为
“未来金属”。以钛铁矿(主要成分钛酸亚铁)为主要原料冶炼金属钛同时获得副产品甲
的工业生产流程如下。请回答下列问题。
(1)钛酸亚铁(用R表示)与碳在高温下反应的化学方程式为2R+C=2Fe+2TiO +CO ↑,钛
2 2
酸亚铁的化学式为_______________;钛酸亚铁和浓HSO 反应的产物之一是TiOSO ,反应
2 4 4
中无气体生成,该反应的化学方程式为________________________________。
(2)上述生产流程中溶液Ⅰ中含有Fe2+、TiO2+和少量Mg2+等阳离子。常温下,其对应氢氧
化物的K 如下表所示。
sp
氢氧化物 Fe(OH) TiO(OH) Mg(OH)
2 2 2
K 8.0×10−16 1.0×10−29 1.8×10−11
sp
①常温下,若所得溶液中Mg2+的物质的量浓度为0.0018mol/L,当溶液的pH等于_______
时,Mg(OH) 开始沉淀。
2②若将含有Fe2+、TiO2+和Mg2+的溶液加水稀释,立即析出大量白色沉淀,该反应的离子方
程式为___________________________________________________________。
(3)中间产品乙与焦炭、氯气在高温下发生反应制取TiCl 的方程式为______________。
4
Mg 还原 TiCl 过程中必须在 1070K 的温度下进行,你认为还应该控制的反应条件是
4
_________。
【答案】(1)FeTiO FeTiO+2H SO =TiOSO +FeSO+2H O
3 3 2 4 4 4 2
(2)10 TiO2++2H O=TiO(OH)↓(或HTiO)+2H+
2 2 2 3
(3)TiO+2C+2Cl =TiCl +2CO 隔绝空气
2 2 4
【解析】钛铁矿用浓硫酸溶解,反应的主要产物是TiOSO 和FeSO ,向所得溶液中加入大
4 4
量水稀释后加入过量的铁粉还原铁离子,过滤得到滤液通过蒸发浓缩,冷却结晶,过滤得到
溶液中含有亚铁离子、TiO2+和少量镁离子等阳离子,冷却结晶得到副产品主要为硫酸亚铁,
滤液中加入水加热过滤得到HTiO,HTiO 加热灼烧得到TiO,加入氯气、过量碳高温下反
2 3 2 3 2
应生成四氯化钛和一氧化碳,四氯化钛和金属镁高温下反应得到氯化镁和钛金属。(1)钛酸亚
铁与碳在高温下反应的化学方程式,根据原子守恒,钛酸亚铁的化学式为FeTiO,钛酸亚铁
3
和浓硫酸反应的产物之一是TiOSO ,反应中无气体生成还生成硫酸亚铁和水,该反应的化学
4
方程式为FeTiO+2H SO =TiOSO+FeSO+2H O;(2)①加入过量的铁粉还原铁原子,防止亚
3 2 4 4 4 2
铁离子被氧化为铁离子,溶液中镁离子的物质的量浓度为0.0018mol/L,析出氢氧化镁时,溶
液中的c(OH−)= mol/L=10−4mol/L,则溶液中的氢离子浓度为10−10mol/L,则溶
液的pH=10;②TiO(OH) 的溶度积最小,溶液加水稀释析出的白色沉淀为TiO(OH),该反应
2 2
的离子方程式为TiO2++2H O=TiO(OH)↓(或HTiO)+2H+;(3)乙为TiO,与氯气和过量的碳
2 2 2 3 2
高温加热反应生成TiCl 和一氧化碳,反应方程式为:TiO+2C+2Cl =TiCl +2CO,镁能与空气
4 2 2 4
中氧气、氮气反应,需要隔绝空气进行。
11.工业制胆矾时,将粗制CuO粉末(含杂质FeO、Fe O)慢慢加入适量的稀HSO 中完全溶
2 3 2 4
解,除去杂质离子后,再蒸发结晶可得纯净的胆矾晶体。已知:pH≥9.6时,Fe2+以Fe(OH)
2
的形式完全沉淀;pH≥6.4时,Cu2+以Cu(OH) 的形式完全沉淀;pH在3~4时,Fe3+以
2
Fe(OH) 的形式完全沉淀.回答下列问题:
3
(1)为除去溶液中的Fe2+,可先加入_______,(从下面四个选项选择)将Fe2+氧化为Fe3+,反
应的离子方程式为_______________________,然后加入适量的__________,(从下面四个选项选择)调整溶液的pH为______,使Fe3+转化为Fe(OH) 沉淀。
3
A.CuO B.Cl C.Cu(OH) D.HO
2 2 2 2
(2)甲同学怀疑调整至溶液pH=4是否能达到除去Fe3+而不损失Cu2+的目的,乙同学认为
可以通过计算确定,他查阅有关资料得到如下数据,常温下Fe(OH) 的溶度积K =1×10−38,
3 sp
Cu(OH) 的溶度积K =3×10−20,通常认为残留在溶液中的离子浓度小于1×10−5mol·L−1时就认
2 sp
为沉淀完全,设溶液中CuSO 的浓度为3mol·L−1,则Cu(OH) 开始沉淀时溶液的pH为______,
4 2
Fe3+完全沉淀时溶液的pH为______,通过计算确定上述方案______(填“可行”或“不可
行”)。
【答案】(1)D Fe2++HO+2H+=2Fe3++2HO AC 3~4
2 2 2
(2)4 3 可行
【解析】将粗制CuO粉末(含杂质FeO、Fe O)慢慢加入适量的稀HSO 中完全溶解,得到
2 3 2 4
硫酸铜、硫酸铁和硫酸亚铁混合溶液,加入氧化剂,把亚铁离子氧化为铁离子,调节pH在3
~4时,Fe3+以Fe(OH) 的形式完全沉淀,过滤,蒸发结晶可得纯净的胆矾晶体。(1)由于pH
3
9.6时,Fe2+以Fe(OH) 的形式完全沉淀;pH 6.4时,Cu2+以Cu(OH) 的形式完全沉淀,故除去
2 2
溶液中的Fe2+,必须先加入氧化剂将Fe2+氧化,为了不引入杂质,加入的氧化剂选HO,即答
2 2
案选D,反应的离子方程式为2Fe2++H O+2H+=2Fe3++2H O。pH在3~4时,Fe3+以Fe(OH) 的
2 2 2 3
形式完全沉淀,为了不引入杂质,然后加入适量的CuO(或Cu(OH) 、CuCO、Cu (OH) CO),
2 3 2 2 3
即答案选AC,调整溶液的pH至3~4,使Fe3+完全转化为Fe(OH) 沉淀。(2)常温下,Cu(OH)
3 2
开始沉淀时c(Cu2+)·c2(OH-)=K [Cu(OH) ]=3 10-20,c(OH−)= =1 10−10mol/L,c(H+)=1
sp 2
10−4mol/L,Cu(OH) 开始沉淀时溶液的 pH=4。Fe3+完全沉淀时 c(Fe3+) 1 10−5mol/L,
2
c(Fe3+)·c3(OH−)=K [Fe(OH) ]=1 10−38 , c(OH−)= =1 10−11mol/L , c(H+)=1
sp 3
10−3mol/L,Fe3+完全沉淀时溶液的pH=3。根据计算结果知上述方案可行。
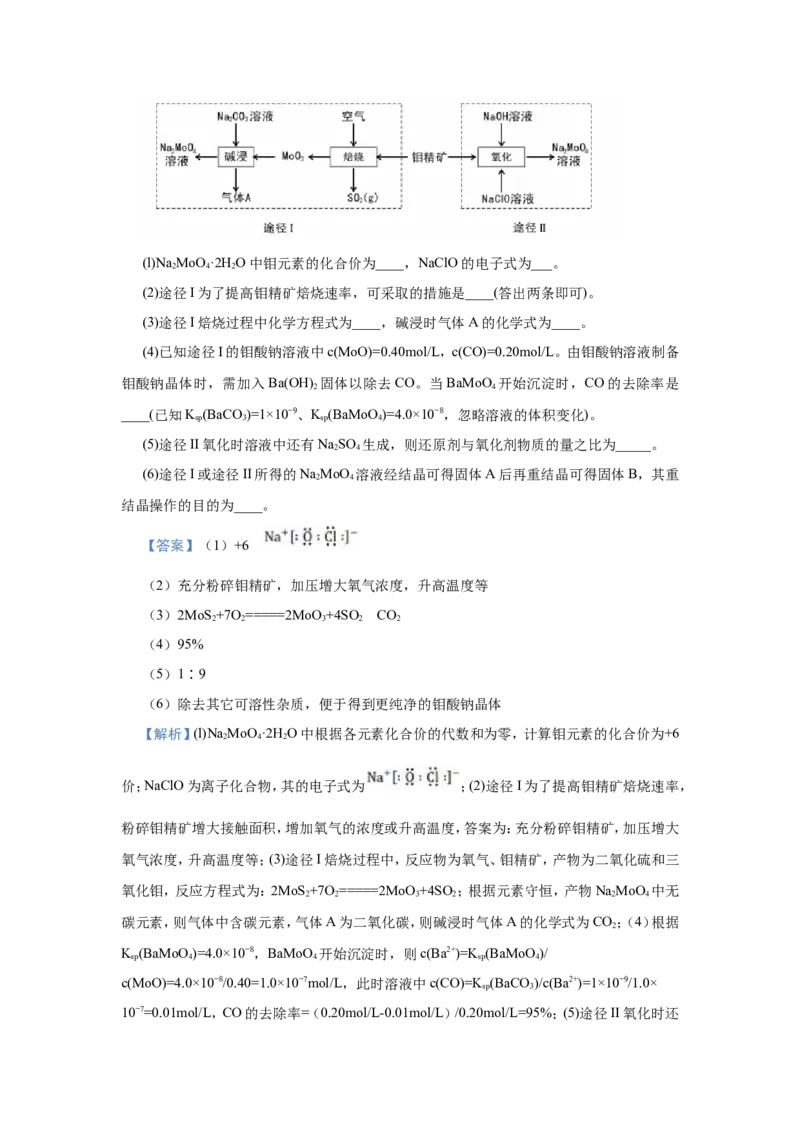
12.钼酸钠晶体(Na MoO ·2HO)是一种无公害型冷却水系统的金属缓蚀剂。工业上利用钼精
2 4 2
矿(主要成分是不溶于水的MoS )制备钼酸钠的两种途径如图所示:
2(l)Na MoO ·2HO中钼元素的化合价为____,NaClO的电子式为___。
2 4 2
(2)途径I为了提高钼精矿焙烧速率,可采取的措施是____(答出两条即可)。
(3)途径I焙烧过程中化学方程式为____,碱浸时气体A的化学式为____。
(4)已知途径I的钼酸钠溶液中c(MoO)=0.40mol/L,c(CO)=0.20mol/L。由钼酸钠溶液制备
钼酸钠晶体时,需加入Ba(OH) 固体以除去CO。当BaMoO 开始沉淀时,CO的去除率是
2 4
____(已知K (BaCO)=1×10−9、K (BaMoO)=4.0×10−8,忽略溶液的体积变化)。
sp 3 sp 4
(5)途径II氧化时溶液中还有NaSO 生成,则还原剂与氧化剂物质的量之比为_____。
2 4
(6)途径I或途径II所得的NaMoO 溶液经结晶可得固体A后再重结晶可得固体B,其重
2 4
结晶操作的目的为____。
【答案】(1)+6
(2)充分粉碎钼精矿,加压增大氧气浓度,升高温度等
(3)2MoS +7O =====2MoO +4SO CO
2 2 3 2 2
(4)95%
(5)1∶9
(6)除去其它可溶性杂质,便于得到更纯净的钼酸钠晶体
【解析】(l)Na MoO ·2HO中根据各元素化合价的代数和为零,计算钼元素的化合价为+6
2 4 2
价;NaClO为离子化合物,其的电子式为 ;(2)途径I为了提高钼精矿焙烧速率,
粉碎钼精矿增大接触面积,增加氧气的浓度或升高温度,答案为:充分粉碎钼精矿,加压增大
氧气浓度,升高温度等;(3)途径I焙烧过程中,反应物为氧气、钼精矿,产物为二氧化硫和三
氧化钼,反应方程式为:2MoS +7O =====2MoO +4SO;根据元素守恒,产物NaMoO 中无
2 2 3 2 2 4
碳元素,则气体中含碳元素,气体A为二氧化碳,则碱浸时气体A的化学式为CO;(4)根据
2
K (BaMoO)=4.0×10−8,BaMoO 开始沉淀时,则c(Ba2+)=K (BaMoO)/
sp 4 4 sp 4
c(MoO)=4.0×10−8/0.40=1.0×10−7mol/L,此时溶液中c(CO)=K (BaCO)/c(Ba2+)=1×10−9/1.0×
sp 3
10−7=0.01mol/L,CO的去除率=(0.20mol/L-0.01mol/L)/0.20mol/L=95%;(5)途径II氧化时还原剂为MoS 、氧化剂为NaClO,生成物为NaSO 和NaMoO ,反应中Mo化合价由+4价变
2 2 4 2 4
为+6价,S由-2变为+6,1mol MoS 失去16mol电子,NaClO中Cl的化合价由+1变为-1,1mol
2
得到2mol电子,则还原剂与氧化剂物质的量之比1∶9;(6)重结晶为根据可溶物的溶解度不
同,利用多次结晶得到较纯的物质,其操作的目的为除去其它可溶性杂质,便于得到更纯净
的钼酸钠晶体。
【点睛】根据元素守恒,产物NaMoO 中无碳元素,则气体中含碳元素,且为稳定的氧化
2 4
物,气体A为二氧化碳;根据还原剂失电子总数与氧化剂得电子总数的比值,可计算出还原
剂与氧化剂物质的量之比。