文档内容
微专题17 金属及其化合物制备流程(Sr)
锶:元素符号Sr,原子序数38,原子量87.62,外围电子排布式5s2,位于第五
周期第ⅡA族。
一、物理性质:
Sr是一种银白色有光泽的金属质软,容易传热导电。密度2.54克/厘米3,熔点769℃,沸
点1384℃。
二、化学性质:
Sr化学性质活泼,在空气中加热到熔点时即燃烧,呈红色火焰,生成氧化锶SrO,在加压
条件下跟氧气化合生成过氧化锶SrO 。跟卤素、硫、硒等容易化合。加热时跟氮化合生
2
成氮化锶Sr N。加热时跟氢化合生成氢化锶SrH 。跟盐酸、稀硫酸剧烈反应放出氢气。
3 2 2
常温下跟水反应生成氢氧化锶和氢气。
三、用途:
用于制造合金、光电管、照明灯。它的化合物用于制信号弹、烟火等。质量数为90的锶
是一种放射性同位素,可做β射线的放射源,半衰期为25年,在医学上有一定的应用。
在自然界主要以化合态存在,主要的矿石有天青石SrSO ,菱锶矿SrCO 。锶是碱土金属
4 3
中丰度最小的元素。1808年英国化学家戴维电解碳酸锶时发现了金属锶。工业用电解熔
融的氯化锶制取锶。
*最后附锶的化合物
四、工业制备:
工艺流程
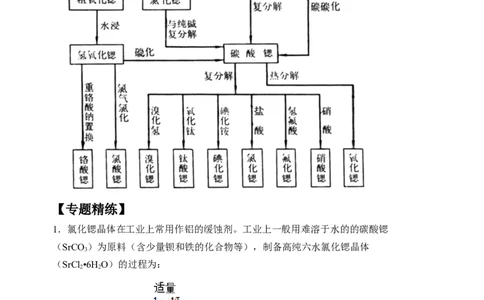
工业上将天青石加工成粗碳酸锶或硫化锶,再进一步加工成其他的锶化合物(见下图),有
两种加工方法。其中碳还原法工艺流程短、成本低,但天青石利用率低,产品质量不易
保证,并且废气污染严重。复分解法能克服碳还原法的缺点,但消耗酸、碱量较大。【专题精练】
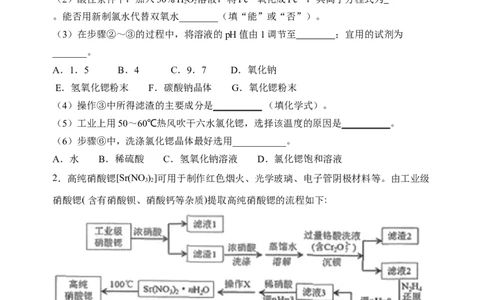
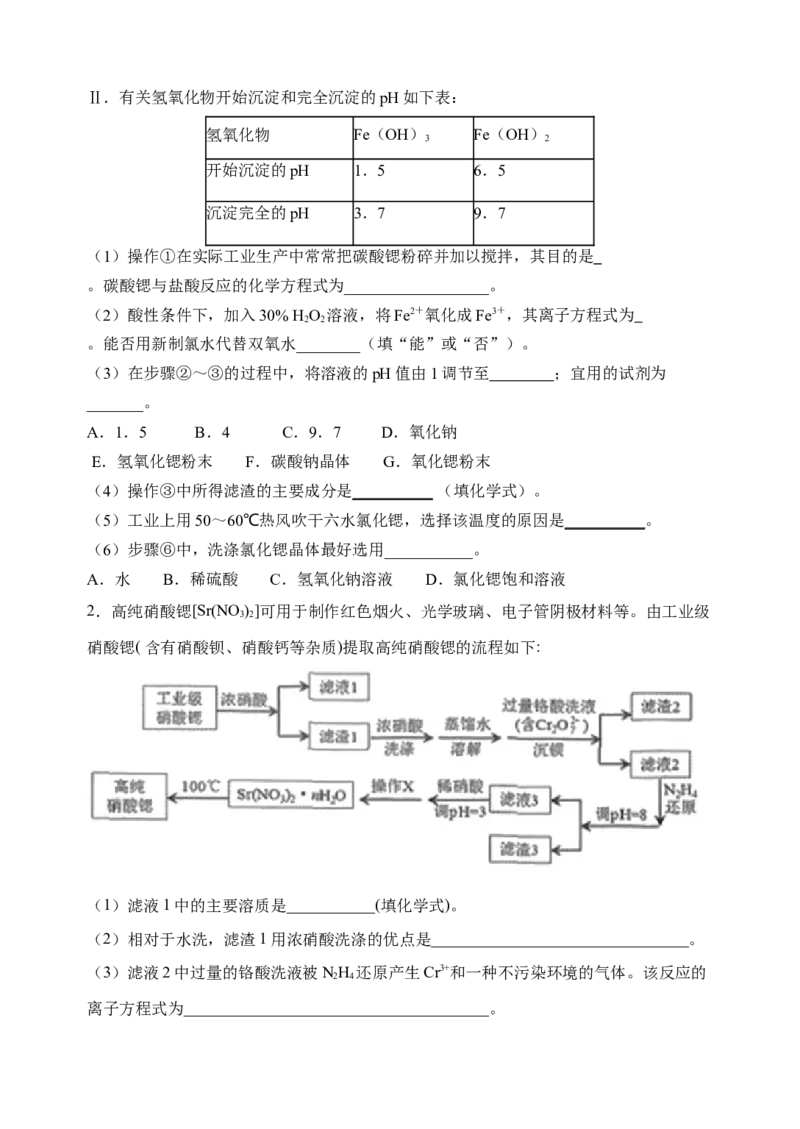
1.氯化锶晶体在工业上常用作铝的缓蚀剂。工业上一般用难溶于水的的碳酸锶
(SrCO )为原料(含少量钡和铁的化合物等),制备高纯六水氯化锶晶体
3
(SrCl •6H O)的过程为:
2 2
已知:Ⅰ.SrCl •6H O晶体在61℃时开始失去结晶水,100℃时失去全部结晶水;
2 2Ⅱ.有关氢氧化物开始沉淀和完全沉淀的pH如下表:
氢氧化物 Fe(OH) Fe(OH)
3 2
开始沉淀的pH 1.5 6.5
沉淀完全的pH 3.7 9.7
(1)操作①在实际工业生产中常常把碳酸锶粉碎并加以搅拌,其目的是
。碳酸锶与盐酸反应的化学方程式为__________________。
(2)酸性条件下,加入30% H O 溶液,将Fe2+氧化成Fe3+,其离子方程式为
2 2
。能否用新制氯水代替双氧水________(填“能”或“否”)。
(3)在步骤②~③的过程中,将溶液的pH值由1调节至 ;宜用的试剂为
_______。
A.1.5 B.4 C.9.7 D.氧化钠
E.氢氧化锶粉末 F.碳酸钠晶体 G.氧化锶粉末
(4)操作③中所得滤渣的主要成分是__________ (填化学式)。
(5)工业上用50~60℃热风吹干六水氯化锶,选择该温度的原因是__________。
(6)步骤⑥中,洗涤氯化锶晶体最好选用___________。
A.水 B.稀硫酸 C.氢氧化钠溶液 D.氯化锶饱和溶液
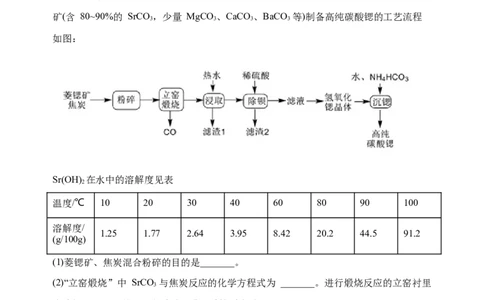
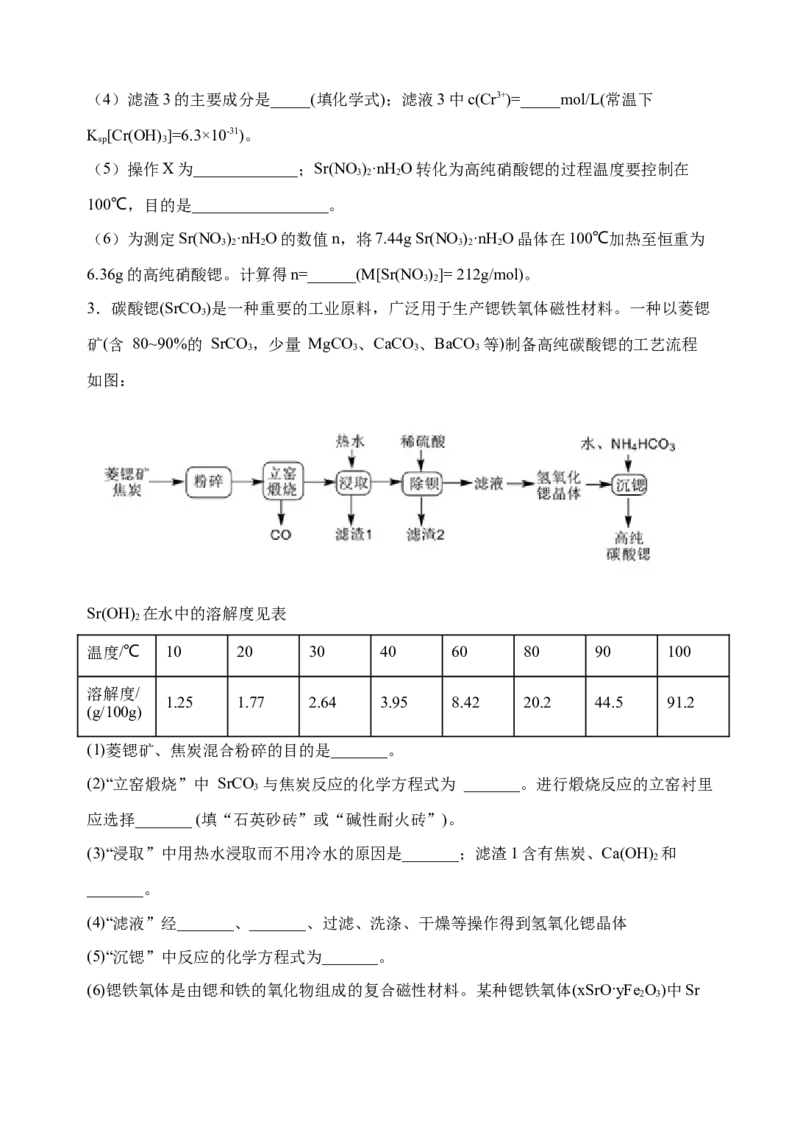
2.高纯硝酸锶[Sr(NO)]可用于制作红色烟火、光学玻璃、电子管阴极材料等。由工业级
3 2
硝酸锶( 含有硝酸钡、硝酸钙等杂质)提取高纯硝酸锶的流程如下:
(1)滤液1中的主要溶质是___________(填化学式)。
(2)相对于水洗,滤渣1用浓硝酸洗涤的优点是________________________________。
(3)滤液2中过量的铬酸洗液被NH 还原产生Cr3+和一种不污染环境的气体。该反应的
2 4
离子方程式为______________________________________。(4)滤渣3的主要成分是_____(填化学式);滤液3中c(Cr3+)=_____mol/L(常温下
K [Cr(OH) ]=6.3×10-31)。
sp 3
(5)操作X为_____________;Sr(NO)·nH O转化为高纯硝酸锶的过程温度要控制在
3 2 2
100℃,目的是_________________。
(6)为测定Sr(NO)·nH O的数值n,将7.44g Sr(NO)·nH O晶体在100℃加热至恒重为
3 2 2 3 2 2
6.36g的高纯硝酸锶。计算得n=______(M[Sr(NO )]= 212g/mol)。
3 2
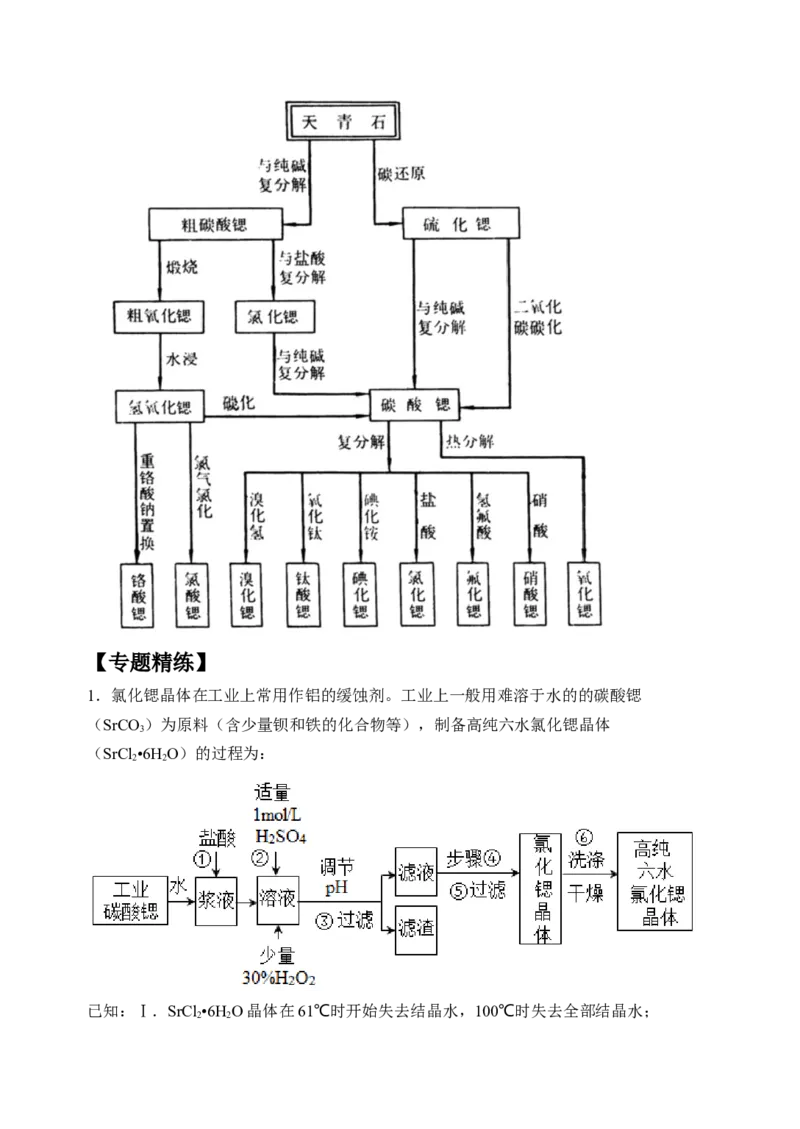
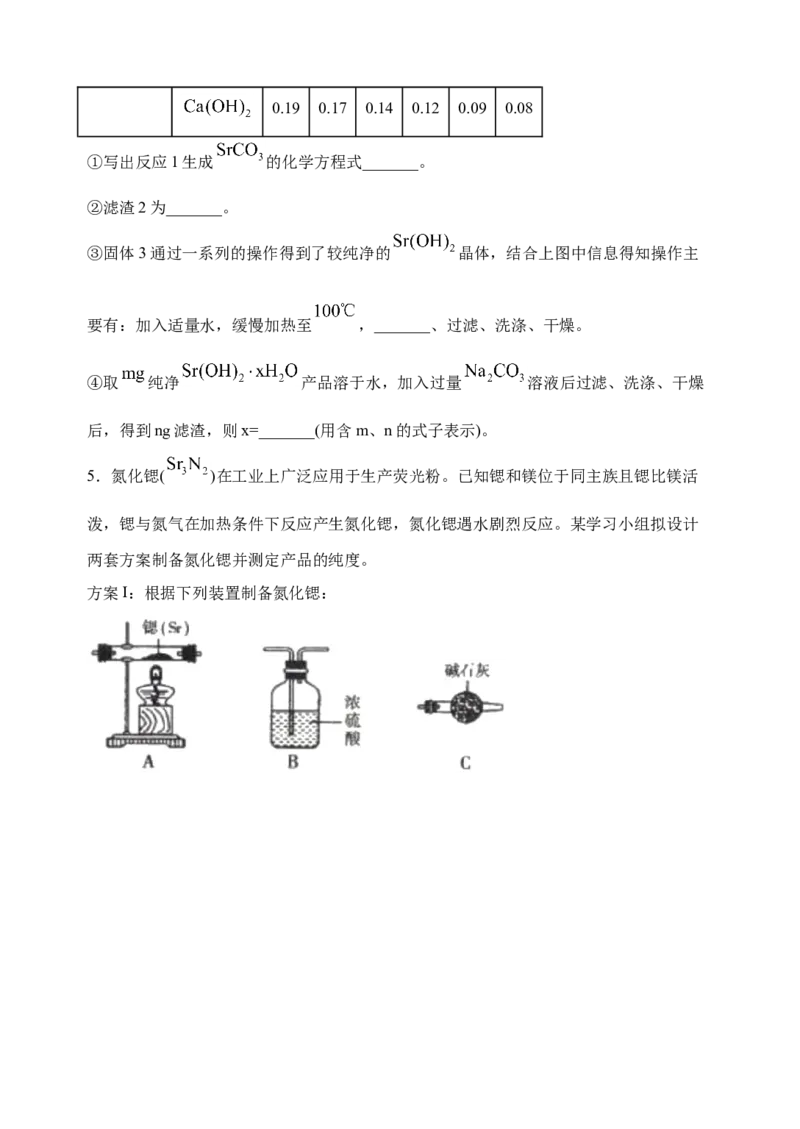
3.碳酸锶(SrCO )是一种重要的工业原料,广泛用于生产锶铁氧体磁性材料。一种以菱锶
3
矿(含 80~90%的 SrCO ,少量 MgCO 、CaCO 、BaCO 等)制备高纯碳酸锶的工艺流程
3 3 3 3
如图:
Sr(OH) 在水中的溶解度见表
2
温度/℃ 10 20 30 40 60 80 90 100
溶解度/
1.25 1.77 2.64 3.95 8.42 20.2 44.5 91.2
(g/100g)
(1)菱锶矿、焦炭混合粉碎的目的是_______。
(2)“立窑煅烧”中 SrCO 与焦炭反应的化学方程式为 _______。进行煅烧反应的立窑衬里
3
应选择_______ (填“石英砂砖”或“碱性耐火砖”)。
(3)“浸取”中用热水浸取而不用冷水的原因是_______;滤渣1含有焦炭、Ca(OH) 和
2
_______。
(4)“滤液”经_______、_______、过滤、洗涤、干燥等操作得到氢氧化锶晶体
(5)“沉锶”中反应的化学方程式为_______。
(6)锶铁氧体是由锶和铁的氧化物组成的复合磁性材料。某种锶铁氧体(xSrO·yFe O)中Sr
2 3和Fe的质量比为0.13,则 为_______ (取整数)。
4.天青石(主要含有 和少量 杂质)是获取锶元素的各种化合物的主要原料。
请回答下列问题:
(1)锶与钙在元素周期表中位于同一主族,其原子比钙多一个电子层。
①锶在元素周期表中的位置是_______。
②由元素周期律推测 属于_______(填“强碱”或“弱碱”)。
(2)硫化锶 可用作发光涂料的原料, 和碳的混合粉末在隔绝空气下高温焙烧可
生成硫化锶和一种还原性气体,该反应的化学方程式_______
(3)已知: 时, 的K =4.3×10-7;K =5.6×10-11;K (SrCO )= 5.6×10-10。在含
a1 a2 sp 3
的 的溶液中通入 至 的浓度为 时, 开始沉淀,
此时溶液的pH为_______。
(4)以天青石生产 的工艺如下:
已知: 在水中的溶解度如下表:
温度/ 0 20 40 60 80 100
溶解度 0.91 1.77 3.95 8.42 20.2 91.20.19 0.17 0.14 0.12 0.09 0.08
①写出反应1生成 的化学方程式_______。
②滤渣2为_______。
③固体3通过一系列的操作得到了较纯净的 晶体,结合上图中信息得知操作主
要有:加入适量水,缓慢加热至 ,_______、过滤、洗涤、干燥。
④取 纯净 产品溶于水,加入过量 溶液后过滤、洗涤、干燥
后,得到ng滤渣,则x=_______(用含m、n的式子表示)。
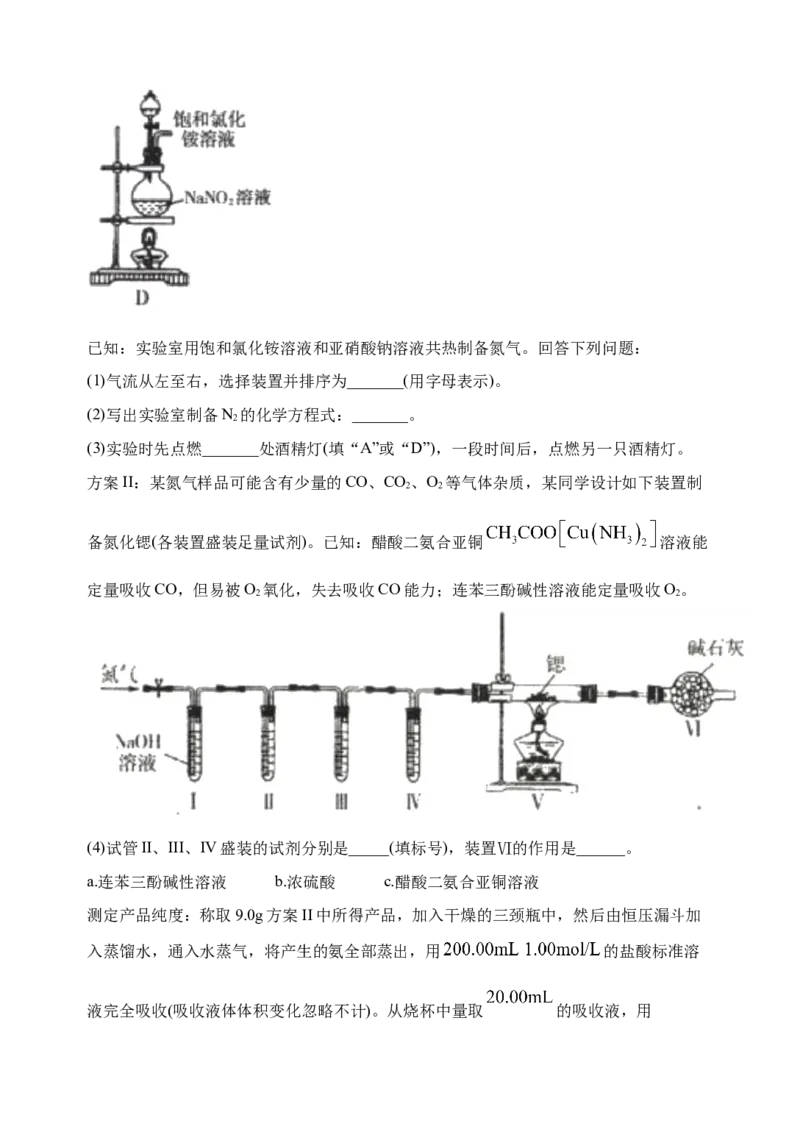
5.氮化锶( )在工业上广泛应用于生产荧光粉。已知锶和镁位于同主族且锶比镁活
泼,锶与氮气在加热条件下反应产生氮化锶,氮化锶遇水剧烈反应。某学习小组拟设计
两套方案制备氮化锶并测定产品的纯度。
方案I:根据下列装置制备氮化锶:已知:实验室用饱和氯化铵溶液和亚硝酸钠溶液共热制备氮气。回答下列问题:
(1)气流从左至右,选择装置并排序为_______(用字母表示)。
(2)写出实验室制备N 的化学方程式:_______。
2
(3)实验时先点燃_______处酒精灯(填“A”或“D”),一段时间后,点燃另一只酒精灯。
方案II:某氮气样品可能含有少量的CO、CO、O 等气体杂质,某同学设计如下装置制
2 2
备氮化锶(各装置盛装足量试剂)。已知:醋酸二氨合亚铜 溶液能
定量吸收CO,但易被O 氧化,失去吸收CO能力;连苯三酚碱性溶液能定量吸收O。
2 2
(4)试管II、III、IV盛装的试剂分别是_____(填标号),装置Ⅵ的作用是______。
a.连苯三酚碱性溶液 b.浓硫酸 c.醋酸二氨合亚铜溶液
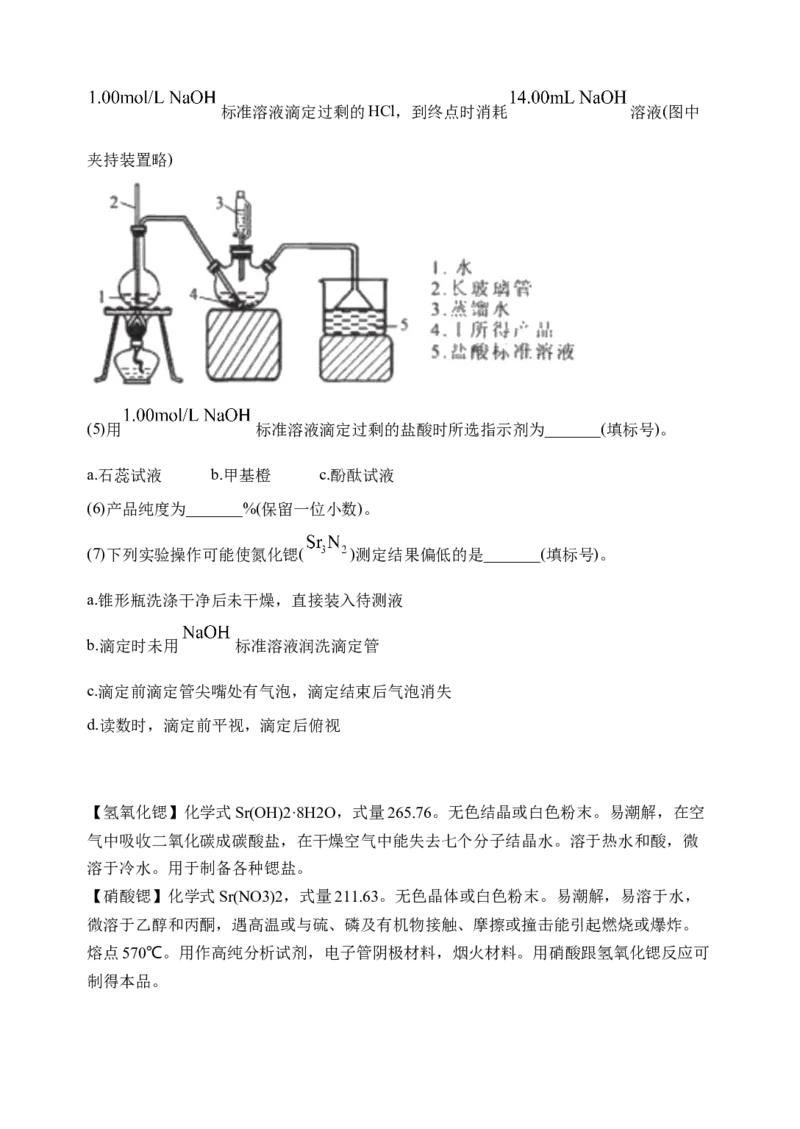
测定产品纯度:称取9.0g方案II中所得产品,加入干燥的三颈瓶中,然后由恒压漏斗加
入蒸馏水,通入水蒸气,将产生的氨全部蒸出,用 的盐酸标准溶
液完全吸收(吸收液体体积变化忽略不计)。从烧杯中量取 的吸收液,用标准溶液滴定过剩的HCl,到终点时消耗 溶液(图中
夹持装置略)
(5)用 标准溶液滴定过剩的盐酸时所选指示剂为_______(填标号)。
a.石蕊试液 b.甲基橙 c.酚酞试液
(6)产品纯度为_______%(保留一位小数)。
(7)下列实验操作可能使氮化锶( )测定结果偏低的是_______(填标号)。
a.锥形瓶洗涤干净后未干燥,直接装入待测液
b.滴定时未用 标准溶液润洗滴定管
c.滴定前滴定管尖嘴处有气泡,滴定结束后气泡消失
d.读数时,滴定前平视,滴定后俯视
【氢氧化锶】化学式Sr(OH)2·8H2O,式量265.76。无色结晶或白色粉末。易潮解,在空
气中吸收二氧化碳成碳酸盐,在干燥空气中能失去七个分子结晶水。溶于热水和酸,微
溶于冷水。用于制备各种锶盐。
【硝酸锶】化学式Sr(NO3)2,式量211.63。无色晶体或白色粉末。易潮解,易溶于水,
微溶于乙醇和丙酮,遇高温或与硫、磷及有机物接触、摩擦或撞击能引起燃烧或爆炸。
熔点570℃。用作高纯分析试剂,电子管阴极材料,烟火材料。用硝酸跟氢氧化锶反应可
制得本品。【碳酸锶】化学式SrCO3,式量147.63。白色粉末,不溶于水,微溶于含二氧化碳的水
和铵盐溶液。加热至900℃分解成氧化锶和二氧化碳,溶于稀盐酸和稀硝酸并放出二氧化
碳。熔点1497℃。用作电子元件材料、光谱试剂、烟火材料、制彩虹玻璃和其它锶盐的
制备。
【氯化锶】化学式SrCl2·6H2O,式量266.62。白色针状晶体,味苦,在干燥空气中风化,
在潮湿空气中潮解。溶于水,微溶于乙醇和丙酮。热至61.4℃失去四个分子结晶水,
100℃成为一水盐,115℃溶于结晶水中,无水盐熔点873℃。用做化学试剂、制药、制锶
盐。用盐酸跟氢氧化锶或碳酸锶反应制得。