文档内容
微专题17 金属及其化合物制备流程(Pb)
一、物质概况:
铅为化学元素,其化学符号是Pb(拉丁文Plumbum;英文lead),原子序数为82,是原子量
最大的非放射性元素。
铅是柔软和延展性强的弱金属,有毒,也是重金属。铅原本的颜色为青白色,在空气中
表面很快被一层暗灰色的氧化物覆盖。可用于建筑、铅酸蓄电池、弹头、炮弹、焊接物
料、钓鱼用具、渔业用具、防辐射物料、奖杯和部份合金,例如电子焊接用的铅锡合金。
铅是一种金属元素,可用作耐硫酸腐蚀、防电离辐射、蓄电池等的材料。其合金可作铅
字、轴承、电缆包皮等之用,还可做体育运动器材铅球。
二、物理性质:
铅是银白色的金属(与锡比较,铅略带一点浅蓝色),十分柔软,用指甲便能在它的表面划
出痕迹。用铅在纸上一划,会留下一条黑道道。在古代,人们曾用铅作笔。"铅笔"这名字,
便是从这儿来的。铅很重,一立方米的铅重达11.3吨,古代欧洲的炼金家们便用旋转迟
缓的土星来表示它,写作"h"。铅球那么沉,便是用铅做的。子弹的弹头也常灌有铅,因
为如果太轻,在前进时受风力影响会改变方向。铅的熔点也很低,为327℃,放在煤球炉
里,也会熔化成铅水。
三、化学性质:
铅很容易生锈--氧化。铅经常是呈灰色的,就是由于它在空气中,很易被空气中的氧气氧
化成灰黑色的氧化铅,使它的银白色的光泽渐渐变得暗淡无光。不过,这层氧化铅形成
一层致密的薄膜,防止内部的铅进一步被氧化。也正因为这样,再加上铅的化学性质又
比较稳定,因此铅不易被腐蚀。在化工厂里,常用铅来制造管道和反应罐。著名的制造
硫酸的铅室法,便是因为在铅制的反应器中进行化学反应而得名的.
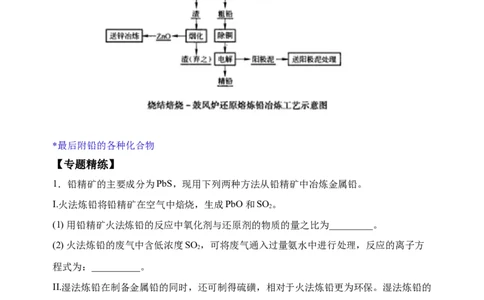
工业制备
第一种:火法炼铅
目前世界上炼铅以火法炼铅为主,火法炼铅一般包括原料准备(配料、制粒、烧结焙烧)、
还原熔炼制取粗铅和粗铅精炼三大工序。烟气制酸、烟尘综合回收以及从阳极泥回收金
银等贵金属也是火法炼铅工艺的重要组成部分。铅精烧结焙烧有两个目的:一是将原料中的硫氧化除去,并以SO 形式送去制硫酸;二是使
2
部分伴生金属氧化并与SiO 等脉石成分生成MeO.SiO 低熔点液相,使细粉状铅精矿粘结
2 2
成多孔硬块,以利还原熔炼。
(1)备料 进入烧结工序的物料包括铅精矿、石英熔剂、烧结返料,三者的配比为
30:10:60。铅精矿一般含有(%):Pb 50-60、Zn 4-6、Cu 0.2、S15-25、Fe 14、SiO 1-2。此外,
2
还伴生有Ag、Bi、Cd、In等有价金属。配好的物料,经过混合和制粒,用布料机均匀地
平铺在烧结机上进行烧结焙烧。 (2)烧结 现代烧结作业均采用带式烧结机,面积为60-
70m3。工作时,铺满炉料的烧结机在传动机械带动下向前移动,经过点火装置处炉料被
火焰点燃,并在强制通过料层吸入(或鼓出)的大量窑中氧的作用下,料层温度迅速上升到
1073-1173K,炉料中发生了一系列的烧结反应。
炉料中主要铅矿物PbS与O 反应生成PbO和SO :
2 2
3PbS+5O====2PbO+PbSO +2SO
2 4 2
3PbSO +PbS====4PbO+4SO
4 2
还有少量金属铅生成:
PbS+PbSO ====2Pb+2SO
4 2
在炉料中含量较高的黄铁矿(FeS )发生分解并进一步氧化成FeO, Fe O 和SO ,进而与
2 2 3 2
SiO, PbO化合,生成为硅酸盐(2FeO.SiO 、xPbO.SiO)和亚铁酸盐(xPbO.yFe O)。
2 2 2 2 3
影响烧结焙烧效果的因素有:①炉料配比与化学成分;②炉料水分;③炉料粒度;④料层厚度;
⑤点火温度;⑥小车运行速度;⑦吸风风量与鼓风压力、风量;⑧烟气SO 浓度等。
2
第二种:电解精炼
电解精炼。用硅氟酸和硅氟酸铅做电解液,粗铅做阳极,纯铅做阴极 ,可得纯铅 。耐
腐蚀 ,可用作水管 。铅、锑 、锡的合金熔点低(约240℃) ,凝固时膨胀,可作印刷铅
字 。铅玻璃用作X射线防护屏 。大量铅用于生产汽油抗爆剂四乙铅和蓄电池的极板。
铅电解精炼现在一般采用是1901年的柏兹所提出的,将粗铅或经过火法初步精炼的半精
炼铅,在硅氟酸与硅氟酸铅的水溶液中进行电解的过程。其目的是为了获得高品位的铅
并回收銤及稀贵金属。*最后附铅的各种化合物
【专题精练】
1.铅精矿的主要成分为PbS,现用下列两种方法从铅精矿中冶炼金属铅。
I.火法炼铅将铅精矿在空气中焙烧,生成PbO和SO 。
2
(1) 用铅精矿火法炼铅的反应中氧化剂与还原剂的物质的量之比为_________。
(2) 火法炼铅的废气中含低浓度SO ,可将废气通入过量氨水中进行处理,反应的离子方
2
程式为:__________。
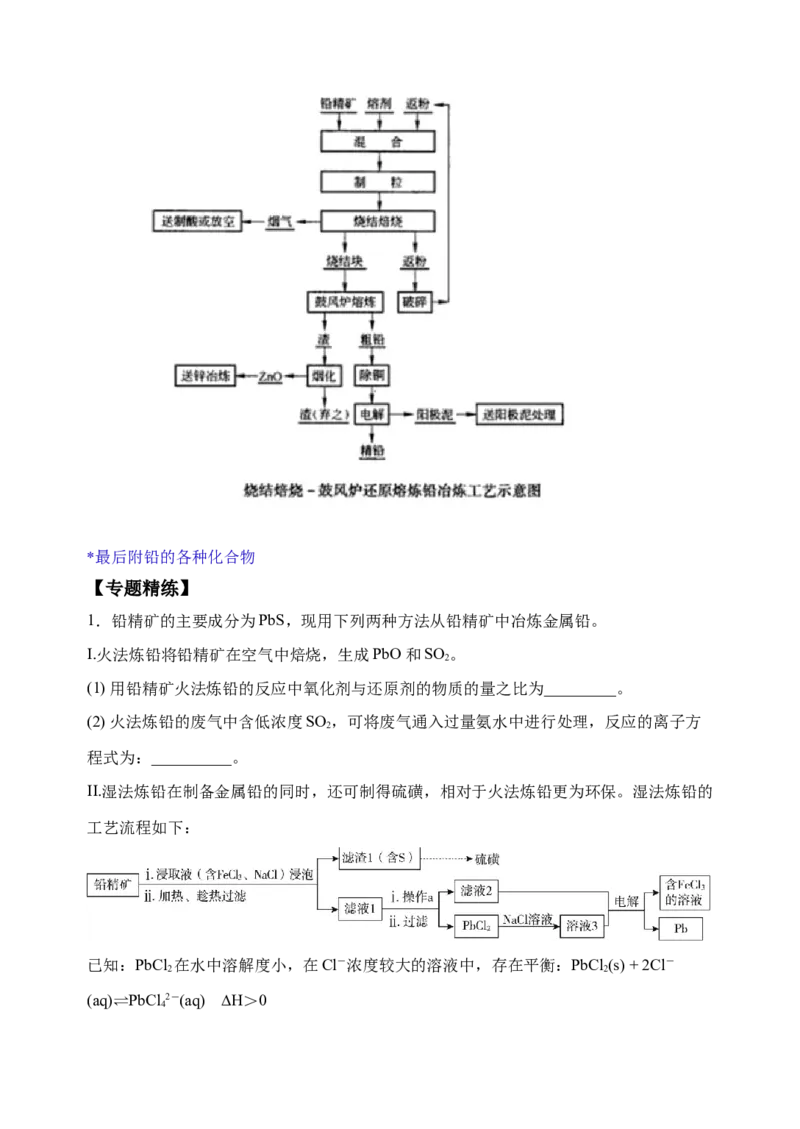
II.湿法炼铅在制备金属铅的同时,还可制得硫磺,相对于火法炼铅更为环保。湿法炼铅的
工艺流程如下:
已知:PbCl 在水中溶解度小,在Cl-浓度较大的溶液中,存在平衡:PbCl (s) + 2Cl-
2 2
(aq)⇌PbCl 2-(aq) ∆H>0
4(3) 浸取铅精矿时发生反应的离子方程式是________。
(4) 由滤液1中析出 PbCl 的操作a是_______。
2
(5) 将溶液3和滤液2分别置于如图所示电解装置的两个极室中,可制取金属铅并使浸取
液中的FeCl 再生。
3
①溶液3应置于______(填“阴极室”或“阳极室”)中。
②简述滤液2电解后再生为FeCl 的可能原理:_________
3
③若铅精矿的质量为a g,铅浸出率为b ,当电解池中通过c mol电子时,金属铅全部析
出,铅精矿中PbS的质量分数的计算式为____________
【答案】(1)3:2 (2) SO +2NH.H O= SO 2-+2NH++ H O (3) PbS+2Fe3++4Cl-= PbCl 2-+
2 3 2 3 4 2 4
2Fe2++S↓ (4) 降低温度,加水稀释 (5) ① 阴极室 ② 阳极室中Fe2+-2e-= Fe3+,阴极
室的Cl-定向移动到阳极室,实现FeCl 的再生 ③
3
【分析】
(1)硫化铅在空气中焙烧生成PbO和SO ,书写氧化还原反应方程式,然后进行分析;
2
(2)SO 为酸性气体,氨水显碱性,反应生成(NH )SO ;
2 4 2 3
(3)根据流程,PbS中S转化成S单质,利用了Fe3+的氧化性,根据信息,书写出离子方
程式;
(4)PbCl 在水中溶解度小,在Cl-浓度较大的溶液中,存在:PbCl (s) + 2Cl-(aq)⇌PbCl 2-
2 2 4
(aq) ∆H>0,获得PbCl ,让平衡向逆反应方向进行;
2
(5)①根据流程获得Pb,Pb元素的化合价降低,根据电解原理,应将溶液3置于阴极室;
②根据流程,滤液2中含有Fe2+,获得FeCl ,化合价升高,需要将滤液2放入阳极室;
3③根据Pb元素守恒进行分析和计算;
【解析】
(1)反应方程式为2PbS + 3O = 2PbO+2SO ,S元素的化合价升高,Pb元素的化合价不变,
2 2
即PbS为还原剂,氧气为氧化剂,氧化剂与还原剂的物质的量之比为3:2;
答案:3:2;
(2)由于氨水过量,反应生成正盐,离子方程式为:SO +2NH.H O= SO 2-+2NH++ H O;
2 3 2 3 4 2
答案:SO +2NH.H O= SO 2-+2NH++ H O;
2 3 2 3 4 2
(3)根据流程,滤渣1中含有硫单质,说明PbS中的S元素转化成S单质,化合价升高,
Fe3+作氧化剂,根据信息,Pb元素以PbCl 2-,因此浸取发生离子方程式为PbS+2Fe3+
4
+4Cl-= PbCl 2-+ 2Fe2++S↓;
4
答案:PbS+2Fe3++4Cl-= PbCl 2-+ 2Fe2++S↓;
4
(4)滤液1中铅元素存在的形式为PbCl 2-,由于PbCl (s) + 2Cl-(aq) PbCl 2-(aq) ∆H
4 2 4
>0,降低温度和加水稀释有利于平衡逆向移动;
答案为降低温度,加水稀释;
(5)①溶液3和滤液2中的溶质分别含有PbCl 2-和FeCl ,电解中要实现FeCl 转变为
4 2 2
FeCl ,发生氧化反应,故滤液2处于阳极室,PbCl 2-转变为Pb,发生还原反应,溶液3
3 4
处于阴极室;
答案:阴极室;
②根据①分析,获得FeCl 再生,阳极室中Fe2+-2e-= Fe3+,阴极室的Cl-定向移动到阳
3
极室,实现FeCl 的再生;
3
答案:阳极室中Fe2+-2e-= Fe3+,阴极室的Cl-定向移动到阳极室,实现FeCl 的再生;
3
③设铅精矿中PbS的质量分数为x,PbCl 2-获得2mole-生成Pb,电解池中通cmol电子时,
4
获得n(Pb)= mol,根据铅元素守恒,得出 = mol,计算出PbS的质量分数为;
答案: 。
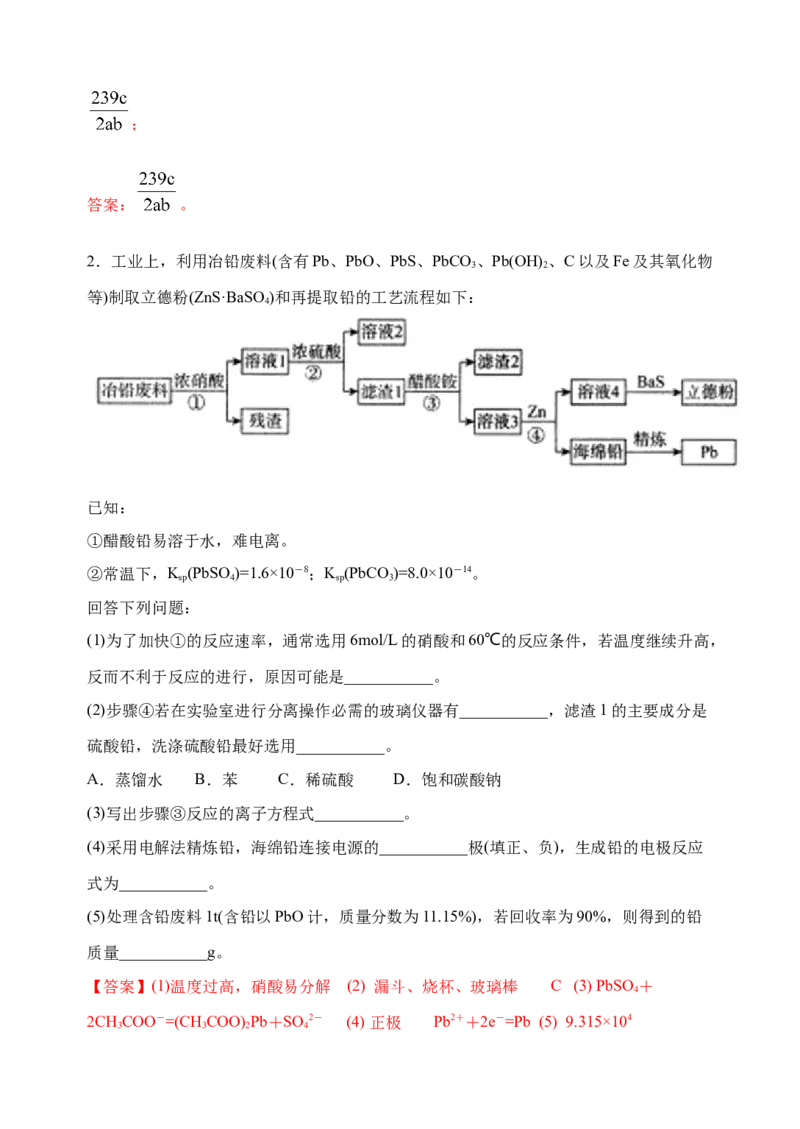
2.工业上,利用冶铅废料(含有Pb、PbO、PbS、PbCO 、Pb(OH)、C以及Fe及其氧化物
3 2
等)制取立德粉(ZnS·BaSO )和再提取铅的工艺流程如下:
4
已知:
①醋酸铅易溶于水,难电离。
②常温下,K (PbSO )=1.6×10-8;K (PbCO )=8.0×10-14。
sp 4 sp 3
回答下列问题:
(1)为了加快①的反应速率,通常选用6mol/L的硝酸和60℃的反应条件,若温度继续升高,
反而不利于反应的进行,原因可能是___________。
(2)步骤④若在实验室进行分离操作必需的玻璃仪器有___________,滤渣1的主要成分是
硫酸铅,洗涤硫酸铅最好选用___________。
A.蒸馏水 B.苯 C.稀硫酸 D.饱和碳酸钠
(3)写出步骤③反应的离子方程式___________。
(4)采用电解法精炼铅,海绵铅连接电源的___________极(填正、负),生成铅的电极反应
式为___________。
(5)处理含铅废料1t(含铅以PbO计,质量分数为11.15%),若回收率为90%,则得到的铅
质量___________g。
【答案】(1)温度过高,硝酸易分解 (2) 漏斗、烧杯、玻璃棒 C (3) PbSO +
4
2CHCOO-=(CH COO) Pb+SO 2- (4) 正极 Pb2++2e-=Pb (5) 9.315×104
3 3 2 4【分析】
(1)通常选用6mol/L的硝酸和60℃的反应条件,温度过高,硝酸易分解。
(2)步骤④反应后的分离操作是过滤,选漏斗、烧杯、玻璃棒;洗涤硫酸铅要洗去表面
吸附的杂质,还要减少损失,最好选用稀硫酸。
(3)步骤③反应的离子方程式PbSO 和CHCOO-作用生成易溶于水、难电离的
4 3
(CHCOO) Pb。
3 2
(4)采用电解法精炼铅,海绵铅连接电源的正极,铅元素化合价升高;生成铅的电极反
应式:Pb2++2e-=Pb
(5)根据铅守恒计算。
【解析】
(1)硝酸受热易分解,故温度不能太高;
(2)步骤④反应后的分离操作为过滤,过滤所需的玻璃仪器有:烧杯、漏斗和玻璃棒;
洗涤硫酸铅要洗去表面吸附的杂质,还要减少损失,故A.会造成硫酸铅部分溶解;B.可
溶性离子不能溶解,不能洗去;C.稀硫酸能够洗去杂质,同时可减少硫酸铅的溶解;
D.依题意,硫酸铅易转化为碳酸铅,引入杂质。故选C;
(3)依题意醋酸铅易溶于水、难电离,故反应的离子方程式为PbSO +2CHCOO-
4 3
=(CH COO) Pb+SO 2-。
3 2 4
(4)采用电解法精炼铅,海绵铅连接电源的正极,铅元素化合价升高;生成铅的电极反
应式:Pb2++2e-=Pb。
(5)根据铅元素守恒可得为 =9.315×104g。
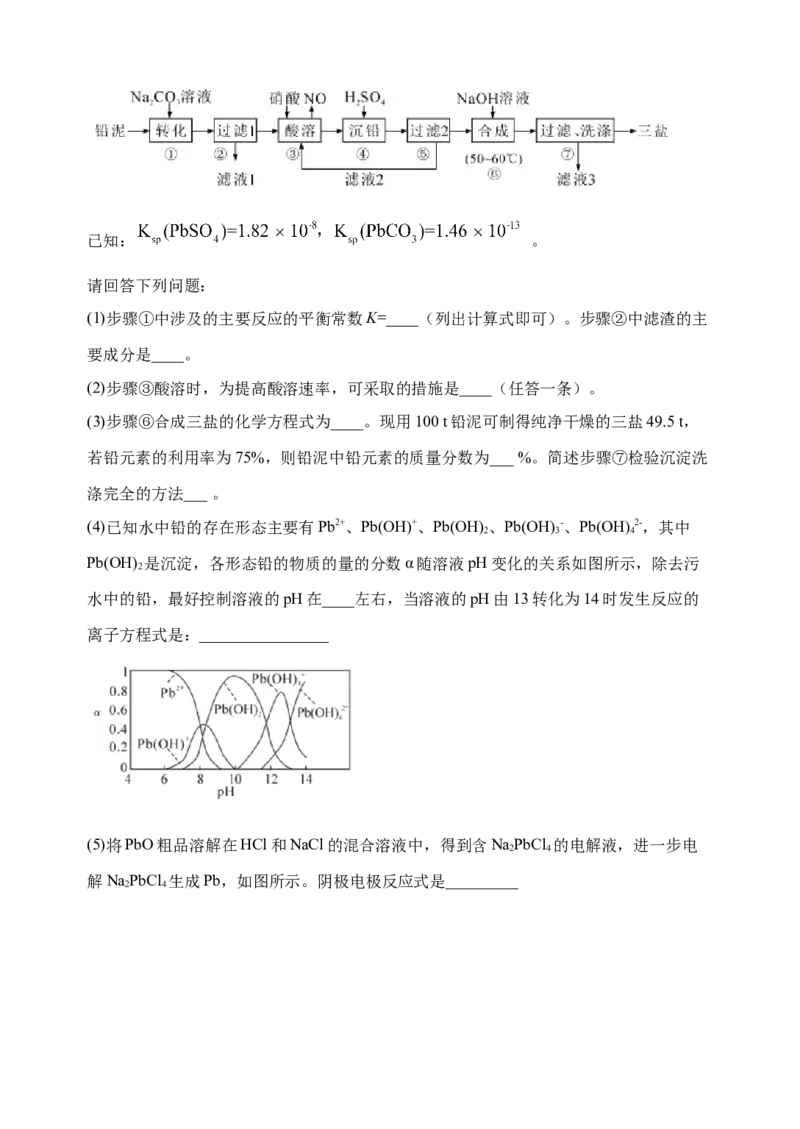
3.铅及其化合物用途广泛,三盐基硫酸铅(3PbO·PbSO ·H O,摩尔质量=990 g/mol)简
4 2
称三盐。以铅泥(主要成分为PbO、Pb及PbSO 等)为原料制备三盐的工艺流程如图所
4
示。已知: 。
请回答下列问题:
(1)步骤①中涉及的主要反应的平衡常数K=____(列出计算式即可)。步骤②中滤渣的主
要成分是____。
(2)步骤③酸溶时,为提高酸溶速率,可采取的措施是____(任答一条)。
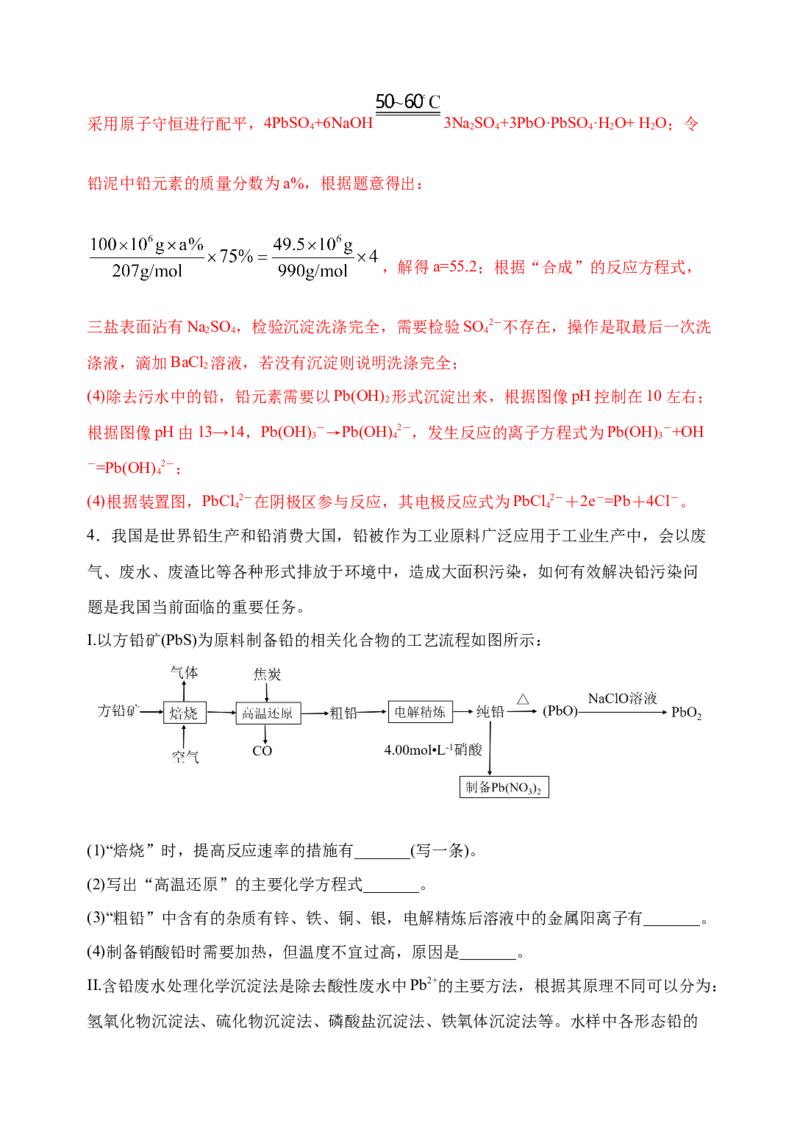
(3)步骤⑥合成三盐的化学方程式为____。现用100 t铅泥可制得纯净干燥的三盐49.5 t,
若铅元素的利用率为75%,则铅泥中铅元素的质量分数为___ %。简述步骤⑦检验沉淀洗
涤完全的方法___ 。
(4)已知水中铅的存在形态主要有Pb2+、Pb(OH)+、Pb(OH)、Pb(OH)-、Pb(OH)2-,其中
2 3 4
Pb(OH) 是沉淀,各形态铅的物质的量的分数α随溶液pH变化的关系如图所示,除去污
2
水中的铅,最好控制溶液的pH在____左右,当溶液的pH由13转化为14时发生反应的
离子方程式是:________________
(5)将PbO粗品溶解在HCl和NaCl的混合溶液中,得到含NaPbCl 的电解液,进一步电
2 4
解NaPbCl 生成Pb,如图所示。阴极电极反应式是_________
2 4【答案】(1) Pb、PbO、PbCO (2) 适当升温 (3)4PbSO +6NaOH
3 4
3NaSO +3PbO·PbSO ·H O+ H O 55.2 取少量最后一次洗涤液,滴加氯化钡溶液,若没
2 4 4 2 2
有沉淀则说明洗涤完全。 (4) 10 (5)Pb(OH) -+OH-=Pb(OH) 2- PbCl 2-+2e-=Pb+4Cl-
3 4 4
【分析】
步骤①发生中发生PbSO +CO2- PbCO +SO 2-,将PbSO 转化成PbCO ,过滤,得
4 3 3 4 4 3
到滤渣为PbO、Pb、PbCO ,在滤渣加入硝酸,PbO、Pb、PbCO 与硝酸发生反应生成
3 3
Pb(NO ),然后加硫酸发生Pb(NO )+HSO =PbSO↓+2HNO,HNO 再转移到酸溶中,
3 2 3 2 2 4 4 3 3
过滤后,向沉淀中加入NaOH溶液加热,得到三盐;
【解析】
(1)PbSO 的K 大于PbCO 的K ,因此步骤“转化”中发生PbSO +CO2- PbCO +
4 sp 3 sp 4 3 3
SO 2-,平衡常数的表达式为K = =
4 sp
;PbO、Pb不与NaCO 发生反应,步骤②中滤渣的主要成分为PbO、Pb、
2 3
PbCO ;
3
(2)提高酸溶的速率,可以采取适当升温、适当增大硝酸浓度、搅拌、粉碎固体等;
(3)“沉铅”将Pb2+转化成PbSO ,“合成”步骤中的反应物是PbSO 、NaOH,其反应方
4 4
程式为PbSO +NaOH→3PbO·PbSO ·H O+NaSO +H O,该反应属于非氧化还原反应,
4 4 2 2 4 2采用原子守恒进行配平,4PbSO +6NaOH 3NaSO +3PbO·PbSO ·H O+ H O;令
4 2 4 4 2 2
铅泥中铅元素的质量分数为a%,根据题意得出:
,解得a=55.2;根据“合成”的反应方程式,
三盐表面沾有NaSO ,检验沉淀洗涤完全,需要检验SO 2-不存在,操作是取最后一次洗
2 4 4
涤液,滴加BaCl 溶液,若没有沉淀则说明洗涤完全;
2
(4)除去污水中的铅,铅元素需要以Pb(OH) 形式沉淀出来,根据图像pH控制在10左右;
2
根据图像pH由13→14,Pb(OH)-→Pb(OH)2-,发生反应的离子方程式为Pb(OH)-+OH
3 4 3
-=Pb(OH) 2-;
4
(4)根据装置图,PbCl 2-在阴极区参与反应,其电极反应式为PbCl 2-+2e-=Pb+4Cl-。
4 4
4.我国是世界铅生产和铅消费大国,铅被作为工业原料广泛应用于工业生产中,会以废
气、废水、废渣比等各种形式排放于环境中,造成大面积污染,如何有效解决铅污染问
题是我国当前面临的重要任务。
I.以方铅矿(PbS)为原料制备铅的相关化合物的工艺流程如图所示:
(1)“焙烧”时,提高反应速率的措施有_______(写一条)。
(2)写出“高温还原”的主要化学方程式_______。
(3)“粗铅”中含有的杂质有锌、铁、铜、银,电解精炼后溶液中的金属阳离子有_______。
(4)制备销酸铅时需要加热,但温度不宜过高,原因是_______。
II.含铅废水处理化学沉淀法是除去酸性废水中Pb2+的主要方法,根据其原理不同可以分为:
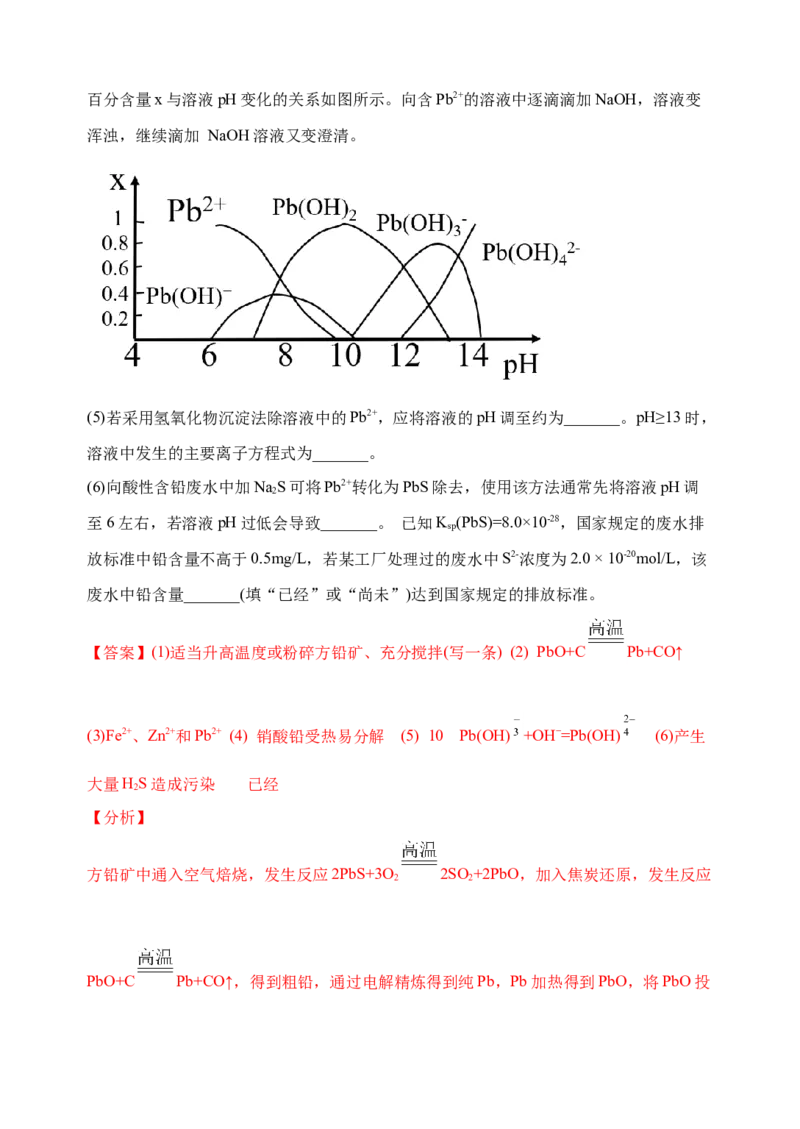
氢氧化物沉淀法、硫化物沉淀法、磷酸盐沉淀法、铁氧体沉淀法等。水样中各形态铅的百分含量x与溶液pH变化的关系如图所示。向含Pb2+的溶液中逐滴滴加NaOH,溶液变
浑浊,继续滴加 NaOH溶液又变澄清。
(5)若采用氢氧化物沉淀法除溶液中的Pb2+,应将溶液的pH调至约为_______。pH≥13 时,
溶液中发生的主要离子方程式为_______。
(6)向酸性含铅废水中加NaS可将Pb2+转化为PbS除去,使用该方法通常先将溶液pH调
2
至6左右,若溶液pH过低会导致_______。 已知K (PbS)=8.0×10-28,国家规定的废水排
sp
放标准中铅含量不高于0.5mg/L,若某工厂处理过的废水中S2-浓度为2.0 × 10-20mol/L,该
废水中铅含量_______(填“已经”或“尚未”)达到国家规定的排放标准。
【答案】(1)适当升高温度或粉碎方铅矿、充分搅拌(写一条) (2) PbO+C Pb+CO↑
(3)Fe2+、Zn2+和Pb2+ (4) 销酸铅受热易分解 (5) 10 Pb(OH) +OH−=Pb(OH) (6)产生
大量HS造成污染 已经
2
【分析】
方铅矿中通入空气焙烧,发生反应2PbS+3O 2SO +2PbO,加入焦炭还原,发生反应
2 2
PbO+C Pb+CO↑,得到粗铅,通过电解精炼得到纯Pb,Pb加热得到PbO,将PbO投入NaClO溶液中得到PbO ,发生的反应为ClO−+PbO═PbO +Cl−,以此解答。
2 2
【解析】
(1)“焙烧”时,提高反应速率的措施有:适当升高温度或粉碎方铅矿、充分搅拌(写一条);
故答案为:适当升高温度或粉碎方铅矿、充分搅拌(写一条);
(2)根据流程图可知, PbO在高温条件下能被焦炭还原生成Pb,反应方程式为PbO+C
Pb+CO↑;故答案为:PbO+C Pb+CO↑;
(3)“粗铅”中含有的杂质有锌、铁、铜、银,其中锌、铁金属的活泼性均强于金属铅,所
以在阳极上放电的金属是锌、铁、铅,电解精炼后溶液中的金属阳离子有Fe2+、Zn2+和
Pb2+,故答案为:Fe2+、Zn2+和Pb2+;
(4)销酸铅受热易分解,所以制备销酸铅时需要加热,但温度不宜过高,故答案为:销酸
铅受热易分解;
(5)由图可知,当Pb2+的浓度为0时,pH约为10,若采用氢氧化物沉淀法除溶液中的
Pb2+,应将溶液的pH调至约为10;pH 13时Pb(OH) 浓度减小,Pb(OH) 浓度增大,
⩾
Pb(OH) 与氢氧根离子反应生成Pb(OH) ,反应的离子方程式:Pb(OH) +OH−=Pb(OH)
,故答案为:10;Pb(OH) +OH−=Pb(OH) ;
(6)向酸性含铅废水中加NaS可将Pb2+转化为PbS除去,使用该方法通常先将溶液pH调
2
至6左右,若溶液pH过低会导致产生大量HS造成污染,废水中S2−浓度为
2
2.0×10−20mol/L,结合K (PbS)= 8.0×10-28可以计算出Pb2+浓度c(Pb2+)=8
sp
mol/L=4.0×10−8mol/L,铅含量=4.0×10−8mol/L×207×1000mg/mol=8.28×10−3mg/L<0.5mg/L,
因此已经达到达到国家规定的排放标准,故答案为:产生大量HS造成污染;已经。
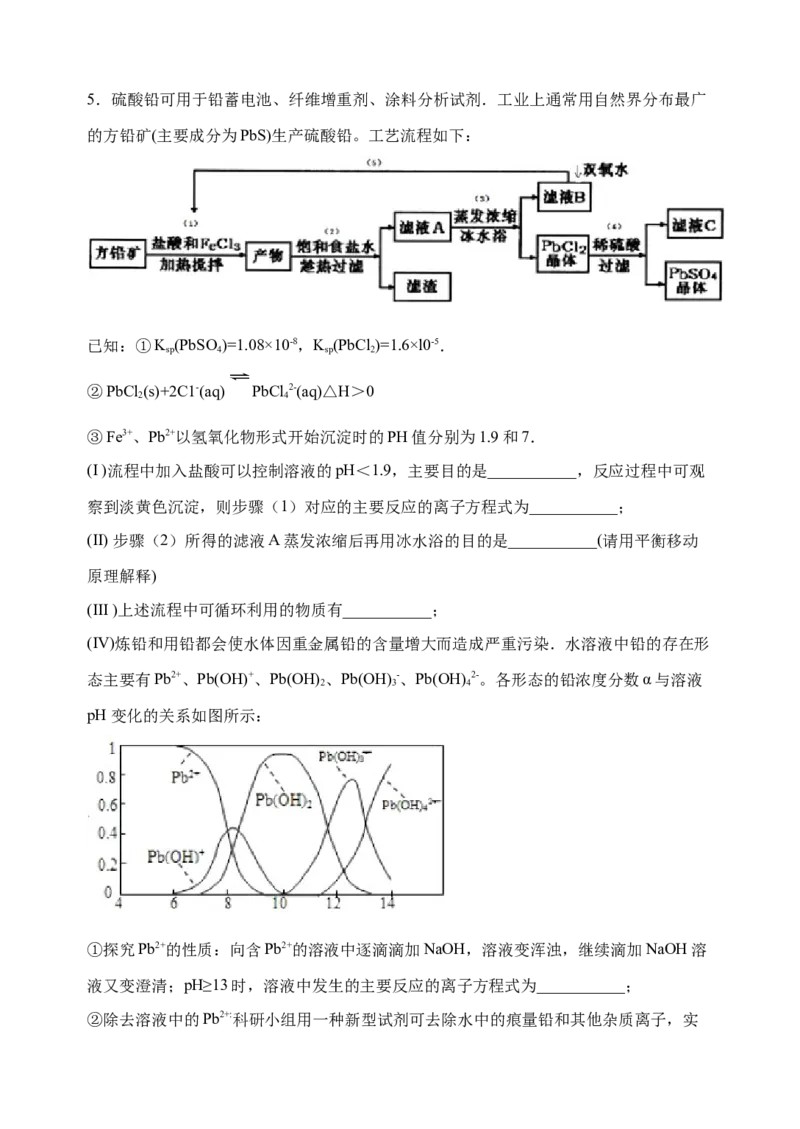
25.硫酸铅可用于铅蓄电池、纤维增重剂、涂料分析试剂.工业上通常用自然界分布最广
的方铅矿(主要成分为PbS)生产硫酸铅。工艺流程如下:
已知:①K (PbSO )=1.08×10-8,K (PbCl )=1.6×l0-5.
sp 4 sp 2
②PbCl (s)+2C1-(aq) PbCl 2-(aq)△H>0
2 4
③Fe3+、Pb2+以氢氧化物形式开始沉淀时的PH值分别为1.9和7.
(I )流程中加入盐酸可以控制溶液的pH<1.9,主要目的是___________,反应过程中可观
察到淡黄色沉淀,则步骤(1)对应的主要反应的离子方程式为___________;
(II) 步骤(2)所得的滤液A 蒸发浓缩后再用冰水浴的目的是___________(请用平衡移动
原理解释)
(III )上述流程中可循环利用的物质有___________;
(IV)炼铅和用铅都会使水体因重金属铅的含量增大而造成严重污染.水溶液中铅的存在形
态主要有Pb2+、Pb(OH)+、Pb(OH)、Pb(OH)-、Pb(OH)2-。各形态的铅浓度分数α与溶液
2 3 4
pH 变化的关系如图所示:
①探究Pb2+的性质:向含Pb2+的溶液中逐滴滴加NaOH,溶液变浑浊,继续滴加NaOH溶
液又变澄清;pH≥13时,溶液中发生的主要反应的离子方程式为___________;
②除去溶液中的Pb2+:科研小组用一种新型试剂可去除水中的痕量铅和其他杂质离子,实验结果记录如下:
Ⅰ.新型试剂处理后的水中Pb2+浓度转化率为___________;
Ⅱ.若新型试剂(DH)在脱铅过程中主要发生的反应为:2DH(s)+Pb2+ DPb(s)+2H+,则
2
脱铅时最合适的pH约为___________
A.4 B.6 C.10 D.12
【答案】(I )抑制Fe3+的水解 2Fe3++PbS+2Cl-=PbCl +S+2Fe2+ (II) 用冰水浴使PbCl (s)
2 2
+2Cl-(aq) PbCl -△H>0逆向移动,使PbCl -转化PbCl 析出 (III ) FeCl 、HCl
4 4 2 3
(IV)Pb(OH) -+HO-=Pb(OH) 2- Ⅰ. 96% Ⅱ. B
3 4
【解析】
试题分析:往方铅矿中加入FeCl 溶液和盐酸,FeCl 与PbS反应生成PbCl 和S,产物中
3 3 2
加入饱和食盐水,趁热过滤,利于PbCl (s)+2Cl-(aq) PbCl -△H>0正向进行,使
2 4
PbCl 溶解,过滤除去硫等杂质,滤液A含有PbCl -、Cl-、Fe2+、Fe3+等,滤液A蒸发浓缩,
2 4
冷水浴中冷却,利用平衡逆向进行,析出PbCl 晶体,滤液B中含有Fe2+、Fe3+,用过氧
2
化氢进行氧化后循环利用,PbCl 晶体中加入稀硫酸,转化为更难溶的硫酸铅沉淀,过滤
2
得到硫酸铅沉淀,洗涤、烘干得到硫酸铅粉末,滤液C中含有HCl。
(Ⅰ)Fe3+、Pb2+以氢氧化物形式开始沉淀时的PH值分别为1.9和7,流程中加入盐酸可
以控制溶液的pH<1.9,主要目的是:抑制Fe3+的水解,FeCl 与PbS反应生成PbCl 和
3 2
S,Pb元素化合价不变,S元素化合价升高,则铁元素的化合价降低,有FeCl 生成,反
2
应方程式为:2FeCl +PbS=PbCl +S+2FeCl ,反应离子方程式为:2Fe3+
3 2 2+PbS=PbCl +S+2Fe2+,故答案为抑制Fe3+的水解;2Fe3++PbS=PbCl +S+2Fe2+;
2 2
(Ⅱ)用冰水浴使PbCl (s)+2Cl-(aq) PbCl -△H>0逆向移动,使PbCl -转化PbCl
2 4 4 2
析出,故答案为用冰水浴使PbCl (s)+2Cl-(aq) PbCl -△H>0逆向移动,使PbCl -
2 4 4
转化PbCl 析出;
2
(Ⅲ)过氧化氢将滤液B中Fe2+氧化为Fe3+,再循环利用,C溶液中含有HCl,也可以循
环利用,故答案为FeCl 、HCl;
3
(Ⅳ)①pH≥13时,Pb(OH)-浓度减小,Pb(OH)2-浓度增大,Pb(OH)-与氢氧根
3 4 3
离子结合为Pb(OH)2-,反应离子方程式为:Pb(OH)-+HO-=Pb(OH)2-,故答案为
4 3 4
Pb(OH)-+HO-=Pb(OH)2-;
3 4
②Ⅰ.加入试剂,Pb2+的浓度转化率为 ×100%=96%,故答案为96%;
Ⅱ.反应为2EH(s)+Pb2+ EPb(s)+2H+,参加反应的是Pb2+,由图象可知,选择
2
PH要使铅全部以Pb2+形式存在,则脱铅时最合适的pH约6,故答案为B。
【一氧化铅】又称黄色氧化铅,俗名黄丹或密陀僧。化学式PbO,式量223.19。有多种
变体,四方晶体呈黄红色,密度为9.53克/厘米3;斜方正交晶体呈黄色,密度为8.0
克/厘米3;无定形者为黄色到红黄色,密度9.2~9.5克/厘米3。熔点888℃。难溶于水和
乙醇。溶于硝酸、醋酸生成相应的铅盐。溶于热的强碱溶液生成亚铅酸盐。吸收空气中
二氧化碳生成碳酸铅。在空气中加热至500℃可生成四氧化三铅。加热时可被碳、氢气、
一氧化碳还原成铅。与甘油混和生成坚硬的物质、可用作粘合剂。用作颜料、涂料油漆
的催干剂、冶金助熔剂,还用于制特种铅玻璃、搪瓷、蓄电池电极、橡胶。用空气氧化
熔融铅或加热碳酸铅、硝酸铅分解制得。【二氧化铅】又称棕色氧化铅。化学式PbO2,式量239.19,棕色细片粉末。密度9.375
克/厘米3,难溶于水和乙醇。将二氧化铅加热,它会逐步转变为铅的低氧化态氧化物并
放出氧
二氧化铅系两性氧化物,酸性比碱性强。跟强碱共热生成铅酸盐。有强氧化性。跟硫酸
共热生成硫酸铅、氧气和水。跟盐酸共热,生成二氯化铅、氯气和水。跟硫、磷等可燃
物混和研磨引起发火。用作分析试剂、氧化剂、媒染剂、蓄电池电极,还用于制火柴、
染料等。用熔融的氯酸钾或硝酸盐氧化一氧化铅,或用次氯酸钠氧化亚铅酸盐可制得二
氧化铅。
【四氧化三铅】俗称红丹或铅丹,红色氧化铅。化学式Pb3O4,式量685.57。橙红色晶
体或粉末,密度9.1克/厘米3,不溶于水和醇。四氧化三铅中,有2/3的铅氧化数为+2,
1/3的铅氧化数为+4,化学式可写作2PbO·PbO2。根据结构应属于铅酸二价铅盐
(Pb2[PbO4])。在加热至500℃以上时分解为一氧化铅和氧气。不溶于水。可溶于热碱溶液
中。有氧化性,跟盐酸反应放出氯气;跟硫酸反应放出氧气。可被稀硝酸分解,其中2/3
的铅被酸溶解,生成硝酸铅(Ⅱ),其它为不溶的二氧化铅。一氧化铅有碱性,溶于稀硝酸,
二氧化铅呈弱碱性,稍溶于酸。有毒。用于制铅玻璃、油漆、蓄电池、陶瓷、搪瓷。还
用于制钢铁涂料。将一氧化铅粉末在空气中加热至450~500℃氧化制得。
【硝酸铅】化学式Pb(NO3)2,式量331.21。无色单斜或立方晶体。密度4.53克/厘米3。
溶于水,微溶于醇。在470℃时分解为一氧化铅、二氧化氮和氧气。有强氧化性,与有机
物接触、摩擦或撞击能引起燃烧或爆炸。有剧毒。用作氧化剂、媒染剂、照像增感剂、
分析试剂、制版等。由铅跟硝酸反应制得。
【醋酸铅】亦称乙酸铅,俗称铅糖。无色晶体或白色粉末,化学式
(CH3COO)2Pb·3H2O,式量379.33,密度2.55克/厘米3。75℃失去结晶水,无水物是白
色粉末,密度3.25克/厘米3,熔点280℃。味甜,有毒!易溶于水和甘油,微溶于乙醇。
具有醋酸气味。在空气中吸收二氧化碳后变为不溶性的碱式碳酸盐。在100℃时分解出乙
酸,在200℃时完全分解。用作分析试剂、媒染剂、染发剂、医药、生物染色、有机合成,
还用于制铬酸铅颜料等。由铅粒跟醋酸反应制得。
【硫化铅】化学式PbS,式量239.25,蓝色有金属光泽立方晶体或棕黑色粉末。密度7.5
克/厘米3,熔点1114℃,在860℃时开始挥发,难溶于水和碱溶液。可溶于硝酸。在空气
中灼烧,可生成一氧化铅和二氧化硫。自然界中主要矿石为方铅矿,是炼铅的原料。高
纯度的硫化铅用作半导体。将硫化氢通入酸性硝酸铅溶液可制得。
【铬酸铅】俗名铬黄,化学式PbCrO4,式量323.18。黄色或橙黄色针状晶体或粉末,密
度6.12克/厘米3,熔点844℃。难溶于水,溶于强碱溶液或硝酸。有毒。加热到熔点以上,缓慢分解放出氧气。用作分析试剂、氧化剂、黄色颜料。由铬酸钾溶液跟硝酸铅溶液反
应制得。
【铅丹】矿物名,主要成分是Pb3O4,红色粉末状块体。硬度2~3,密度4.6克/厘米3,
常与方铅矿和白铅矿伴生。用于制红色颜料和铅玻璃。通常用的红丹即铅丹,大部分由
人工制成。
【方铅矿】主要成分为PbS,常含银。等轴晶系,晶体形状多为立方体、有时为八面体。
铅灰色,有金属光泽,立方体解理完全,硬度2~3,性脆,密度7.4~7.6克/厘米3。炼
铅的主要矿石,由于常含银,又是炼银的主要矿石。
【锡石】矿物名。化学成分为SnO2,四方晶系,晶体一般为双锥状,双锥柱状,常具膝
状双晶,集合体呈不规则颗粒。通常呈棕色至黑褐色,有金刚光泽。硬度6.0~7.0,密度
6.8~7.0克/厘米3。是炼锡的主要原料。
【白铅矿】主要成分是PbCO3。正交晶系,晶形常呈假六方双锥形状,集合体为粒状或
致密块状。白色微带浅灰。金刚光泽,硬度3.0~3.5,密度6.4~6.6克/厘米3。炼铅用矿
石。