文档内容
第二节 元素周期律
第1课时 元素性质的周期性变化规律
基础巩固
1.下列说法正确的是( )。
A.原子序数越大,原子半径一定越大
B.电子层数多的原子半径一定比电子层数少的原子半径大
C.元素性质的周期性变化不是元素性质的简单重复
D.按C、N、O、F的顺序,元素的最高正化合价依次升高
2.(2022·上海市宝山中学高一阶段练习)下列微粒半径大小关系正确的是
A. B.
C. 、 D.
3.下列不能说明钠的金属性比镁强的事实是( )。
A.钠的最高化合价为+1价,镁的最高化合价为+2价
B.NaOH的碱性比Mg(OH) 的强
2
C.钠与冷水反应剧烈,镁与冷水反应缓慢
D.在熔融状态下,钠可以从MgCl 中置换出镁
2
4.(2022·江苏徐州·高二期中)判断氮的非金属性比磷强,不可依据的事实是
A.常温下氮气是气体,磷是固体 B.稳定性:
C.酸性: D. 在空气中不能燃烧,而 可燃
5.(2022·河北·石家庄二中高二阶段练习)X、Y、Z、R、 T为短周期主族元素,其中R原子的最外层电
子数是电子层数的2倍;Y与Z能形成Z2Y、 Z2Y2型离子化合物,Y与T同主族。五种元素原子半径与原
子序数之间的关系如图所示。下列推断正确的是
A.Z Y和Z Y 的阴阳离子个数比相同 B.简单氢化物的稳定性: Y<T
2 2 2
C.最高价氧化物对应水化物的酸性: T<R D.由X、Y、Z、T四种元素组成的常见化合物溶液显酸性
6.(2022·辽宁沈阳·高三阶段练习)如图是部分短周期元素原子序数与主要化合价的关系图,X、Y、Z、
Q、W、R是其中的六种元素。下列说法不正确的是( )
学科网(北京)股份有限公司A.键能:X-H>W-H B.元素周期表中33号元素与Z同族
C.最高价氧化物对应水化物的酸性:R>W D.单质与水(或酸)反应的剧烈程度:Y>Z
7.(2022·河北·石家庄二中高二阶段练习)Q、X、Y、Z是原子序数依次增大的短周期主族元素,其最外
层电子数之和为19。Q与X、Y、Z位于不同周期,X、Y相邻,Y原子最外层电子数是Q原子内层电子数
的2倍。下列说法正确的是
A.非金属性:X>Q B.Y为铝
C.简单氢化物的沸点:Z>Q D.最高价含氧酸的酸性:Z>Y
8.已知P、S、Cl、As、Br五种元素在元素周期表中的位置如图所示。下列比较关系正确的是( )
P S Cl
As Br
A.原子半径:As>Cl>P B.热稳定性:HCl>AsH >HBr
3
C.还原性:As3->S2->Cl- D.酸性:HAsO >H SO >H PO
3 4 2 4 3 4
9.根据元素周期表中1~20号元素的性质和递变规律,填写下列空白。
(1)属于金属元素的有_____种,属于稀有气体元素的有_____(填元素符号,下同)。
(2)第三周期中,原子半径最大的元素是(稀有气体元素除外)_____。
(3)推测 、N的非金属性强弱:_____大于_____。
(4)第三周期中金属性最强的元素与氧气反应,生成的化合物有_____(写出两种化合物的化学式)。
10.(2022·河南新乡期末)某同学为了验证元素周期律相关的结论,自己设计了一套实验方案,并记
录了有关实验现象。
实验方案 实验现象
①将氯气通入NaS溶液中 有淡黄色固体(S)生成
2
②将一小块金属镁,用砂纸磨去表面的氧化膜后,放
入试管中,加入2 mL水,观察现象,记录为现象I, 现象 I :无明显变化
过一会儿,加热试管至液体沸腾,观察现象,记录为 现象II:金属镁逐渐溶解,有气体生成
现象II
③将溴水滴入NaI溶液中,充分反应后加入淀粉溶液 溶液变蓝
④将一小块金属钠放入冷水中 钠浮在水面上,熔成小球,四处游动,逐渐消失
回答下列问题:
(1)实验①相关反应的离子方程式为___________________________。由实验①可知,C1、S的非金属性
由强到弱的顺序为____________(用元素符号表示,下同)。由实验③可知,Br、I的非金属性由强到弱的
顺序为_____________。
学科网(北京)股份有限公司(2)由实验②和实验④知,碱性:NaOH________(填“>”或“<”)Mg(OH)。
2
(3)实验结论:同主族元素自上而下,元素的非金属性逐渐___________(填“增强”或“减弱”,下
同);同周期元素,原子序数逐渐增大,金属性逐渐___________,非金属性逐渐___________。由此可知:
HSiO、HPO、HSO、HClO 的酸性由强到弱的顺序为_____________________________________(填化学
2 3 3 4 2 4 4
式,下同);常见氢化物NH、HO、HF、HS中稳定性最强的是________。
3 2 2
能力提升
11.(2022·四川·邻水实验学校高一阶段练习)下列结论正确的是
①微粒半径:S2->Cl->K+>Al3+
②氢化物的稳定性:HF>HCl>H S>PH >SiH
2 3 4
③离子的还原性:S2->Cl->Br->I-
④氧化性:Cl >S>Se>Te
2
⑤酸性:HClO>H SO >H PO >H CO
2 4 3 4 2 3
⑥非金属性:O>N>P>Si
⑦金属性:Be>Mg>Ca>K
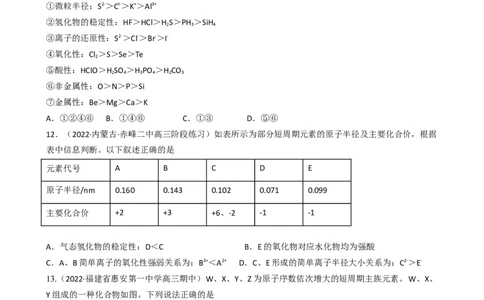
A.①②④⑥ B.①④⑥ C.①③ D.⑤⑥
12.(2022·内蒙古·赤峰二中高三阶段练习)如表所示为部分短周期元素的原子半径及主要化合价,根据
表中信息判断。以下叙述正确的是
元素代号 A B C D E
原子半径/nm 0.160 0.143 0.102 0.071 0.099
主要化合价 +2 +3 +6、-2 -1 -1
A.气态氢化物的稳定性:D<C B.E的氧化物对应水化物均为强酸
C.A、B简单离子的氧化性强弱关系为:B3+<A2+ D.C、E形成的简单离子半径大小关系为:C2->E-
13.(2022·福建省惠安第一中学高三期中)W、X、Y、Z为原子序数依次增大的短周期主族元素。W、X、
Y组成的一种化合物如图。下列说法正确的是
A.四种元素中X的原子半径最大,简单离子半径最小 B.最高化合价:Z>Y=W>X
C.氧化物对应水化物的酸性:Z>Y D.气态氢化物的稳定性:Y>Z
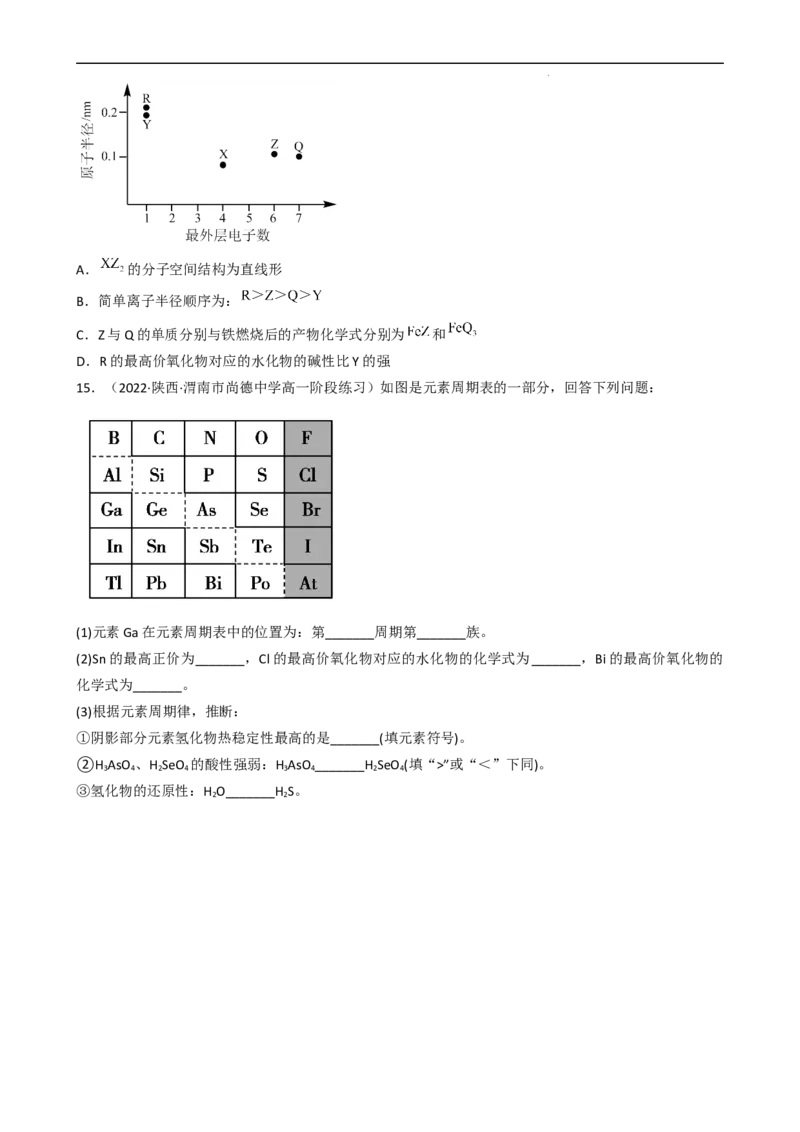
14.(2022·天津市第四十七中学高三期中)元素X、Y、Z、Q、R的原子序数依次增大且小于20,其原子
半径和最外层电子数之间的关系如图所示。下列判断不正确的是
学科网(北京)股份有限公司A. 的分子空间结构为直线形
B.简单离子半径顺序为:
C.Z与Q的单质分别与铁燃烧后的产物化学式分别为 和
D.R的最高价氧化物对应的水化物的碱性比Y的强
15.(2022·陕西·渭南市尚德中学高一阶段练习)如图是元素周期表的一部分,回答下列问题:
(1)元素Ga在元素周期表中的位置为:第_______周期第_______族。
(2)Sn的最高正价为_______,Cl的最高价氧化物对应的水化物的化学式为_______,Bi的最高价氧化物的
化学式为_______。
(3)根据元素周期律,推断:
①阴影部分元素氢化物热稳定性最高的是_______(填元素符号)。
②H AsO 、H SeO 的酸性强弱:H AsO _______H SeO (填“>”或“<”下同)。
3 4 2 4 3 4 2 4
③氢化物的还原性:H O_______H S。
2 2
学科网(北京)股份有限公司学科网(北京)股份有限公司