文档内容
第四章 物质结构 元素周期律
第一节 原子结构与元素周期表
第三课时 原子结构与元素性质—碱金属
【学习目标】1.通过观察实验现象,分析实验原理、阅读教材内容,探究认识碱金属元素性质的递变
规律,能用原子结构理论初步加以解释同主族元素性质的递变规律,初步掌握元素性质与原子结构的关
系,培养宏观辨识与微观探析的化学核心素养。
2.通过碱金属元素的相关性质的图表信息,培养分析、处理数据的能力,尝试运用比较、归纳等方法
对信息进行加工,落实证据推理与模型认知的化学核心素养。
【学习重点】碱金属元素性质的相似性和递变性
【学习难点】原子结构与碱金属元素性质的关系
【课前预习】
旧知回顾:1.元素周期表中共有 1 8 个纵列,分为 7 个主族, 7 个副族, 1个 0 族(又名 稀有气
体 元素)和1个第 Ⅷ 族(包括第 8 、 9 、 1 0 三个纵列)。其中第ⅠA族(除 氢 外)又叫 碱金属 元
素,第ⅦA族又叫 卤族 元素。
2.指出ⅠA、ⅦA族元素(除氢元素)的元素符号及名称,并分别画出原子结构示意图。其原子结构
有何特点?
【答案】 ①Ⅰ A 族:Li(锂) 、Na(钠) 、K(钾) 、Rb(铷)
、Cs(铯)
②原子结构特点:最外层均只有一各电子,由锂→铯,随原子序数递增,电子层数依次增多。
新知预习:1.在元素周期表中,同一主族元素原子结构有何特点和规律?
【温馨提示】同主族元素原子结构具有相似性和递变性。如ⅠA和ⅦA族元素具有最外层电子数都是
1和7;从上到下,随核电荷数依次增多、电子层数依次增多、原子半径依次增大。
2.碱金属元素的原子最外层有 1 个电子,化学性质 相似 ,如最高价氧化物对应水化物的化学式为
ROH ,且均呈 碱 性,都能与 氧气 等非金属单质及 水 反应等。但随核电荷数的增加,其原子的 电子
层数 逐渐增多,原子半径逐渐 增大 ,化学性质也有 差异 性,如与水反应的剧烈程度 不同 等。
【课中探究】
情景导入:在上一节课的学习中,我们知道门捷列夫绘制出了第一张元素周期表。这第一张元素周期
表实际是有很多空格的(见PPT图片),门捷列夫预言其中很多未知元素的性质。那么门捷列夫是根据什
么在预言未知元素的性质的呢?一、碱金属的概念及原子结构特点
活动一、原子结构与元素周期表的关系
任务一、根据元素周期表的结构特点,回答原子结构与元素周期表有何关系?
【答案要点】①元素周期表有七个横行,每个横行叫做一个周期,即共分为七个周期,把电子层数相
同的元素,按原子序数递增顺序从左到右排列。
②元素周期表有十八个纵行,除8、9、10三个纵行叫第Ⅷ族外,每个纵行叫做一个族,即共分十六个
族(七主七副),把最外电子层相同的元素,按电子层数递增的顺序由上而下排列。
任务二、讨论交流:结合所学知识,思考元素化学性质与原子最外层电子数有何关系?由此可得到什
么结论?
【答案要点】①元素分为金属元素和非金属元素(包括稀有气体元素)。金属性最强的元素是铯(Cs
不包括放射性元素),非金属属性最强的元素是氟(F)。
②金属元素的原子最外层电子数一般小于或等于4,容易失去电子形成稳定结构,化学性质活泼,表
现出金属性。
③非金属元素的原子最外层电子数一般大于或等于4,容易得到电子形成稳定结构,化学性质活泼,
表现出非金属性。
④稀有气体原子最外层电子数除氦为2个电子稳定结构外,都为8电子稳定结构,既不易得到电子,
也不易失去电子,化学性质稳定。
⑤结论:最外层电子数决定元素的化学性质。
【对应练习】1.下列关于碱金属元素的说法正确的是( )
①原子结构的相同点是最外层电子数相同,都为1
②原子结构的不同点是随核电荷数的增加,电子层数增多,原子半径增大
③具有相似的化学性质,都是活泼金属
④都具有强还原性,在化合物中显+1价
⑤化学性质有差别,从Li到Cs,失电子能力逐渐增强
A.①③④ B.①③⑤ C.②④⑤ D.全部
【答案】 D
【解析】 碱金属元素原子的最外层都有一个电子,都易失去一个电子,具有强还原性,在化合物中
显+1价,①③④正确;碱金属元素从Li到Cs,原子半径逐渐增大,原子核对核外电子的束缚力逐渐减
弱,失电子能力逐渐增强,②⑤正确。
2.下列叙述中,正确的是( )
A.两种粒子,若核外电子排布完全相同,则其化学性质一定相同
B.凡单原子形成的离子,一定具有稀有气体元素原子的核外电子排布
C.两原子,如果核外电子排布相同,则一定属于同种元素
D.阴离子的核外电子排布一定与比它原子序数小的稀有气体元素原子的核外电子排布相同
【答案】C【解析】两种粒子,若核外电子排布完全相同,则其化学性质不一定相同,例如钠离子和氟离子,A
项错误;凡单原子形成的离子,不一定具有稀有气体元素原子的核外电子排布,例如H+肯定不满足稀有
气体的核外电子排布,B项错误;两原子,如果核外电子排布相同,那么质子数相同,则一定属于同种元
素,C项正确;阴离子是原子得电子后的离子,则阴离子的核外电子排布与同周期的稀有气体元素原子的
核外电子排布相同,D项错误。
活动二、碱金属的概念及原子结构特点
任务一、阅读教材P98-99页第一自然段,思考什么是碱金属元素?其原子结构有何特点?可得到什么
结论?
【温馨提示】①元素周期表中第ⅠA族元素(除氢外)又称碱金属元素,包括锂(Li)、钠(Na)、钾
(K)、铷(Rb)、铯(Cs)、钫(Fr)六种元素。
②其原子结构具有相似性:最外层电子数都是1(小于4),从上到下即由Li→Cs,随着核电荷数增
加,电子层数增多。
③结论:化学性质非常活泼的金属,在自然界中都以化合态存在。
任务二、结合教材P99页“思考与讨论”,回答在周期表中,从上到下碱金属元素原子的核电荷数、
原子半径的变化有什么特点?完成表格内容。
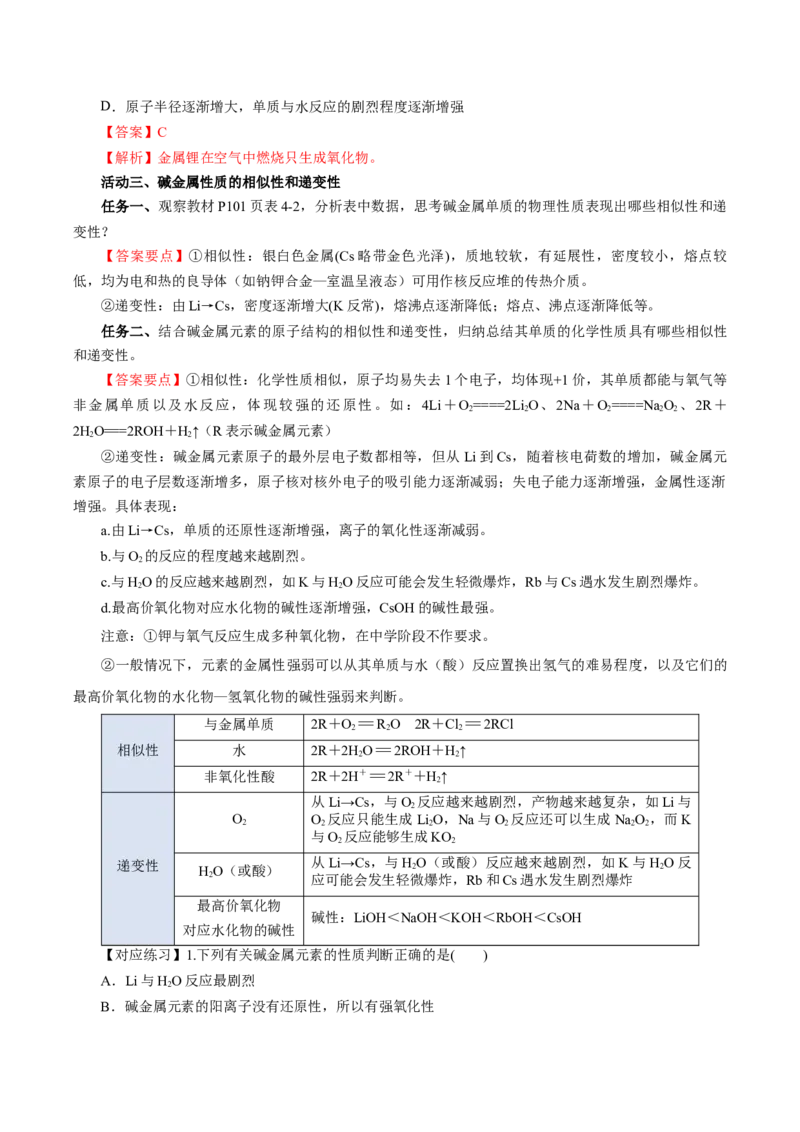
【温馨提示】
最外层电子
元素名称 元素符号 核电荷数 原子结构示意图 电子层数 原子半径/nm
数
锂 Li 3 2 0.152
钠 Na 11 3 0.186
钾 K 19 4 0.227
铷 Rb 37 5 0.248
1
铯 Cs 55 6 0.265
①最外层电子数相等(均为1);②从上到下,电子层数依次增加;③从上到下,原
结论
子半径依次增大。
【对应练习】1.以下关于锂、钠、钾、铷、铯的叙述正确的是( )
①氢氧化物中碱性最强的是CsOH ②单质熔点最高的是铯 ③它们都是热和电的良导体 ④它们的
密度依次增大,且都比水轻 ⑤它们的还原性依次增强 ⑥它们对应阳离子的氧化性依次增强
A.①③ B.②⑤ C.②④⑥ D.①③⑤【答案】D
【解析】①碱金属从上到下,金属性增强,最高价氧化物对应水化物碱性越强,因此氢氧化物中碱性
最强的是CsOH,故①正确;②从上到下,金属的熔点逐渐降低,因此单质熔点最高的是Li,故②错误;
③碱金属是是热和电的良导体,故③正确;④碱金属密度具有增大趋势,但钠的密度大于钾的密度,铷、
铯密度比水大,故④错误;⑤从上到下金属性增强,它们的还原性依次增强,故⑤正确;⑥从上到下金属
性增强,还原性增强,它们对应阳离子的氧化性依次减弱,故⑥错误;因此①③⑤正确,故D正确。故选
D。
2.已知锂及其化合物的许多性质与碱金属差异较大,却与镁相似。下面有关锂及其化合物的性质的叙
述不正确的是( )
A.锂在过量氧气中燃烧,主要产物是LiO而不是LiO
2 2 2
B.Li CO 受热很难分解
2 3
C.在相同温度下,溶解度LiCO 小于LiHCO
2 3 3
D.少量的锂保存在固体石蜡中
【答案】B
【解析】碱金属中,锂最不活泼,密度最小,比煤油还轻,能浮在煤油上,故应保存在固体石蜡中。
锂及其化合物的许多性质与镁相似,MgCO 受热易分解,LiCO 受热也易分解,B错误;MgCO 的溶解度
3 2 3 3
小于Mg(HCO ) 的溶解度,故在相同温度下,溶解度LiCO 小于LiHCO ,C正确。
3 2 2 3 3
二、碱金属元素的性质
活动一、预测碱金属的化学性质
任务一、回忆第二章学过的知识,思考金属钠具有哪些化学性质?
【温馨提示】①与非金属单质反应:
a.与氧气反应:新切开的钠具有银白色的金属光泽,在空气中很快变暗,失去金属光泽。在空气中点燃
金属钠,钠先熔化成小球,然后剧烈燃烧,火焰呈黄色,生成淡黄色固体。
反应的化学方程式:4Na+O===2Na O或2Na+O=====NaO;
2 2 2 2 2
b.与氯气反应:金属钠在氯气中燃烧,产生大量白烟,产物为氯化钠。
化学方程式:2Na+Cl ===== 2NaCl。
2
c.与硫反应:钠与硫混合研磨可发生爆炸,火星四射,产物为硫化钠。
化学方程式:2Na+S=====NaS。
2
②与水反应:浮于水面上(钠的密度小于水)、熔成一个小球(反应放热,钠的熔点低)、四处游动
(生成气体)、发出嘶嘶声(反应放热,热的钠使水蒸发)、滴有酚酞的溶液变为红色(生成NaOH)。
化学方程式:2Na + 2HO = 2NaOH + H ↑
2 2
③与盐溶液反应:先与水反应,生成的NaOH再与盐反应复分解反应。如与CuSO 溶液反应反应化学
4方程式:2Na+2HO===2NaOH+H↑、2NaOH + CuSO ===NaSO +Cu(OH) ↓,总反应式:2Na+2HO +
2 2 4 2 4 2 2
CuSO ===NaSO +Cu(OH) ↓+H↑。
4 2 4 2 2
任务二、结合碱金属的的原子结构特点,预测锂、钾可能具有哪些与钠相似的化学性质?
【温馨提示】①最外层都有1个电子→易失去1个电子→单质具有强还原性,都以化合态存在。元素
均具有较强的金属性,单质均体现较强的还原性;
②与非金属单质反应:如与O 反应生成相应的氧化物(LiO、KO)、与Cl 反应生成LiCl和KCl、与
2 2 2 2
HO反应,能置换出HO中的氢,反应通式为:2R+2HO===2ROH+H↑等。
2 2 2 2
③与非氧化性酸反应,生成H,反应通式为:2R+2H+===2R++H↑(R表示碱金属Li、K,下同)。
2 2
④与水反应生成相应的碱和氢气,其通式为2R+2HO===2ROH+H↑等。
2 2
【对应练习】1.下列关于钠的说法不正确的是( )
A.金属钠和氧气反应,条件不同,产物不同
B.钠长期置于空气中,表面不能形成致密氧化膜
C.钠与水反应时,钠熔成小球在水面四处游动
D.由于钠比较活泼,所以它能从溶液中置换出金属活动性顺序表中钠后面的金属
【答案】D
【解析】金属钠与氧气反应,常温生成氧化钠,加热生成过氧化钠,A项正确;钠长期置于空气中,
表面先生成氧化钠,会与空气中的水反应,最终生成碳酸钠,不能生成致密氧化膜,B项正确;钠是活泼
金属,熔点低,与水反应时,钠熔成小球在水面四处游动,C项正确;钠与盐溶液反应时,先与水反应,
不能从盐溶液中置换出金属,D项不正确。
2.下列叙述正确的是( )
A.Na在空气中燃烧会生成NaO,故Li在空气中燃烧也会生成LiO
2 2 2 2
B.碱金属元素是指ⅠA族的所有元素
C.在熔融状态下,钠可以从MgCl 中置换出镁
2
D.Li、Na、K都可以保存在煤油中
【答案】C
【解析】A.Li在空气中燃烧只生成LiO,故A错误;B.碱金属元素是指ⅠA族除氢外的金属元
2
素,故B错误;C.钠比镁金属性强,能在熔融状态下置换出氯化镁中的镁单质,故 C正确;D.Li的密
度比煤油小,不能保存在煤油中,故D错误;故选:C。
活动二、实验探究碱金属的化学性质
任务一、结合教材P100页实验(1)完成实验,观察比较金属钠、钾与水反应的现象,分析原理,完
成表格内容。
【温馨提示】实验操作
实验现象 在空气中燃烧,钠产生黄色火焰,钾产生紫色火焰,钾燃烧更剧烈
2Na+O====NaO
2 2 2
化学方程式
K+OΔ—\s\up 4()多种氧化物(产物中金属均为+1价)
2—→
钾原子半径比钠原子大,对最外层电子的引力弱,钾比钠更容易失去电子,
实验结论
同理,锂可以与O 反应,但不如钠剧烈:4Li+O====2LiO。
2 2 2
任务二、结合教材P100页实验(2)完成实验,观察比较金属钠、钾与水反应的现象,分析原理,完
成表格内容。
【温馨提示】
碱金属 钾 钠
实验操作
①金属浮在水面上;②金属熔化成闪亮的小球;③小球四处游动;④发出
实验 共同点
“嘶嘶”的响声;⑤反应后的溶液呈红色
现象
不同点 K与水反应更剧烈
化学方程式 2K+2HO===2KOH+H↑ 2Na+2HO===2NaOH+H↑
2 2 2 2
结论及原因分 失电子能力:K大于Na。K、Na最外层电子数目相同,但K比Na电子层
析 数多,最外层电子离核较远,故K比Na更易失电子。
【对应练习】1.下列说法错误的是( )
A.化合物中碱金属元素的化合价都为+1价
B.碱金属元素原子的次外层电子数都是8
C.碱金属元素的原子半径随核电荷数的增大而增大
D.碱金属元素都位于元素周期表的第ⅠA族
【答案】B
【解析】A项,碱金属元素的原子最外层只有 1个电子,因 此在化合物中的化合价均为+1价,正
确;B项,Li原子的次外层电子数为2,错误;C项,核电荷数越大,电子层数越多,原子半径越大,正
确;D项,碱金属元素都位于元素周期表的第ⅠA族,正确。
2.下列关于碱金属按Li、Na、K、Rb、Cs的顺序叙述中不正确的是( )
A.碱金属原子最外层都只有一个电子,在化学反应中容易失电子表现出强还原性
B.单质的熔点和沸点依次递减
C.单质都能与水反应生成碱,都能在空气中燃烧生成过氧化物D.原子半径逐渐增大,单质与水反应的剧烈程度逐渐增强
【答案】C
【解析】金属锂在空气中燃烧只生成氧化物。
活动三、碱金属性质的相似性和递变性
任务一、观察教材P101页表4-2,分析表中数据,思考碱金属单质的物理性质表现出哪些相似性和递
变性?
【答案要点】①相似性:银白色金属(Cs略带金色光泽),质地较软,有延展性,密度较小,熔点较
低,均为电和热的良导体(如钠钾合金—室温呈液态)可用作核反应堆的传热介质。
②递变性:由Li→Cs,密度逐渐增大(K反常),熔沸点逐渐降低;熔点、沸点逐渐降低等。
任务二、结合碱金属元素的原子结构的相似性和递变性,归纳总结其单质的化学性质具有哪些相似性
和递变性。
【答案要点】①相似性:化学性质相似,原子均易失去1个电子,均体现+1价,其单质都能与氧气等
非金属单质以及水反应,体现较强的还原性。如:4Li+O====2LiO、2Na+O====NaO 、2R+
2 2 2 2 2
2HO===2ROH+H↑(R表示碱金属元素)
2 2
②递变性:碱金属元素原子的最外层电子数都相等,但从 Li到Cs,随着核电荷数的增加,碱金属元
素原子的电子层数逐渐增多,原子核对核外电子的吸引能力逐渐减弱;失电子能力逐渐增强,金属性逐渐
增强。具体表现:
a.由Li→Cs,单质的还原性逐渐增强,离子的氧化性逐渐减弱。
b.与O 的反应的程度越来越剧烈。
2
c.与HO的反应越来越剧烈,如K与HO反应可能会发生轻微爆炸,Rb与Cs遇水发生剧烈爆炸。
2 2
d.最高价氧化物对应水化物的碱性逐渐增强,CsOH的碱性最强。
注意:①钾与氧气反应生成多种氧化物,在中学阶段不作要求。
②一般情况下,元素的金属性强弱可以从其单质与水(酸)反应置换出氢气的难易程度,以及它们的
最高价氧化物的水化物—氢氧化物的碱性强弱来判断。
与金属单质 2R+O=R O 2R+Cl=2RCl
2 2 2
相似性 水 2R+2HO=2ROH+H↑
2 2
非氧化性酸 2R+2H+=2R++H↑
2
从Li→Cs,与O 反应越来越剧烈,产物越来越复杂,如Li与
2
O O 反应只能生成LiO,Na与O 反应还可以生成NaO ,而K
2 2 2 2 2 2
与O 反应能够生成KO
2 2
递变性 HO(或酸) 从Li→Cs,与H 2 O(或酸)反应越来越剧烈,如K与H 2 O反
2 应可能会发生轻微爆炸,Rb和Cs遇水发生剧烈爆炸
最高价氧化物
碱性:LiOH<NaOH<KOH<RbOH<CsOH
对应水化物的碱性
【对应练习】1.下列有关碱金属元素的性质判断正确的是( )
A.Li与HO反应最剧烈
2
B.碱金属元素的阳离子没有还原性,所以有强氧化性C.Rb比Na活泼,故Rb可以从NaCl溶液中置换出Na
D.从Li到Cs都易失去最外层1个电子,且失电子能力逐渐增强
【答案】D
【解析】A项,在碱金属元素中,Li是最不活泼的元素,错误;B项,碱金属阳离子很稳定,不具有
强氧化性,错误;C项,Rb先与水反应,不会置换出Na,错误;D项,同主族元素从上到下金属性逐渐
增强,正确。
2.据报道、德国科学家实现了铷(Rb)原子气体超流体态与绝缘态的可逆转换,该成果将给量子计算机
的研究带来重大突破。已知铷在元素周期表中位于第五周期IA族。下列说法不正确的是( )
A.铷的原子序数为37 B.铷放到水中会比钠跟水反应更剧烈
C.铷的氧化物暴露在空气中易与CO 反应 D.铷的氢氧化物是弱碱
2
【答案】D
【解析】A项,铷的原子核内有37个质子,则原子序数为37,A正确;B项,铷的原子半径大于
Na,则失电子能力大于Na,故放到水中会比钠跟水反应更剧烈,B正确;C项,铷的氧化物为碱性氧化
物,则暴露在空气中易与CO 反应,C正确;D项,铷的失电子能力大于Na,则铷的氢氧化物是强碱,D
2
错误;故选D。
【课后巩固】1.下列关于同主族元素的说法错误的是( )
A.同主族元素随原子序数递增,元素原子的得电子能力逐渐增强
B.同主族元素随原子序数递增,单质氧化能力逐渐减弱
C.同主族元素原子最外层电子数都相同
D.同主族元素的原子半径,随原子序数增大而逐渐增大
【答案】A
【解析】同主族元素,最外层电子数相同,随原子序数增大,原子半径逐渐增大,得电子能力逐渐减
弱,单质氧化性逐渐减弱,故A错误,B、C、D正确。
2.下列说法中,正确的是( )
A.碱金属单质的化学性质活泼,易从盐溶液中置换其它金属
B.碱金属单质在空气中燃烧生成的都是过氧化物
C.随核电荷数增加,碱金属单质溶、沸点降低
D.碱金属的原子半径越大,越易失电子,其还原性越弱
【答案】C
【解析】A.K、Na等过于活泼的碱金属先和水反应,生成强碱,而不是与盐溶液发生置换反应,故
A错误;B.金属Li在空气中燃烧生成氧化锂,金属钾在空气中燃烧生成超氧化钾,只有金属钠在空气中
燃烧生成过氧化钠,故B错误;C.随核电荷数增加,其阳离子半径越来越大,与自由电子的作用力越来
越弱,所以碱金属单质溶、沸点降低,故C正确;D.碱金属的原子半径越大,原子核对最外层电子的吸引能力减弱,则越易失电子,其还原性越强,故D错误。答案选C。
3.下列有关碱金属的说法不正确的是( )
A.均为ⅠA族元素,最外层均有1个电子
B.单质的还原性:Li>Na>K>Rb>Cs
C.碱性:LiOH<NaOH<KOH<RbOH<CsOH
D.由Li到Cs,核电荷数依次增加,电子层数、原子半径依次增大
【答案】B
【解析】碱金属位于周期表第ⅠA族,主族序数等于原子最外层电子数,最外层电子数为1,故A正
确;同主族电子层数依次增加,失电子能力越来越强,还原性增强,单质的还原性:Li<Na<K<Rb<
Cs,故B错误;金属性越强形成的碱的碱性越强,LiOH<NaOH<KOH<RbOH<CsOH,故C正确;同一
主族,从上到下,电子层数、原子半径依次增大,故D正确。
4.下列关于碱金属的叙述中,正确的是( )
A.碱金属单质的密度随原子序数的增大而增大
B.碱金属随着原子序数增大,与水反应越剧烈
C.碱金属的原子半径越大,越易失电子,其还原性越弱
D.碱金属单质的化学性质活泼,易从盐溶液中置换其它金属
【答案】B
【解析】A.碱金属单质的密度随原子序数的增大而增大,Na,K反常,故A错误;B.碱金属随着
原子序数增大,越易失电子,与水反应越剧烈,故B正确;C.碱金属的原子半径越大,越易失电子,其
还原性越强,故C错误;D.Na,K性质活泼,先和水反应,而不是与盐溶液发生置换反应,故D错误;
故答案选B。
5.借助碱金属和卤族元素的递变性分析下面的推断,其中正确的是( )
A.已知Ca是第四周期ⅡA族的元素,故Ca(OH) 的碱性比Mg(OH) 的碱性弱
2 2
B.已知As是第四周期ⅤA族的元素,故AsH 的稳定性比NH 的稳定性强
3 3
C.已知Cs的原子半径比Na的原子半径大,故Cs与水反应不如Na与水反应剧烈
D.已知Cl的核电荷数比F的核电荷数多,故Cl的原子半径比F的原子半径大
【答案】D
【解析】由碱金属元素和卤族元素的递变性可知,同主族元素从上到下金属性递增,非金属性递减,
最高价氧化物对应的水化物碱性增强,金属活动性增强,非金属气态氢化物稳定性减弱,A、B、C错误;
同主族元素随核电荷数增大,原子半径递增,D正确。
6.下列关于碱金属的叙述中正确的是( )
A.碱金属单质与水反应都能生成碱和H
2
B.碱金属单质都是质软、电和热的良导体,焰色反应都呈现黄色
C.碱金属的密度都小于1 g/cm3,因此碱金属单质都可以保存在煤油中D.碱金属单质在空气中燃烧都生成过氧化物
【答案】A
【解析】碱金属性质较活泼,都能和水反应生成碱和氢气,故A正确;碱金属单质都是质软、电和热
的良导体,但只有钠焰色反应呈现黄色,故B错误;Li、Na、K的密度小于1 g/cm3,Rb、Cs的密度大于1
g/cm3,故C错误;Li在空气中燃烧生成氧化锂,Na在空气中燃烧生成过氧化钠,K在空气中燃烧生成超
氧化钾,故D错误。
7.下列有关铯及其化合物的说法不正确的是( )
A.CsOH的碱性比KOH的强
B.铯与水或稀盐酸反应剧烈,都生成H
2
C.Cs的还原性比Na的强,故Na+的氧化性强于Cs+
D.Li的金属性比Cs的强
【答案】D
【解析】根据元素周期律,Cs的金属性比K强,故CsOH的碱性比KOH强,A项正确;Cs的性质与
钠相似,Na能与水或稀盐酸反应产生H ,故Cs也能与水或稀盐酸反应产生H ,且反应更剧烈,B项正
2 2
确;Cs的还原性强于Na,则Na+得电子能力比Cs+强,即氧化性:Na+>Cs+,C项正确;Li、Cs均为碱金
属元素,Cs的电子层数多,更容易失去最外层电子,故金属性:Cs>Li,D项错误。
8.(1)1807年,英国化学家戴维在研究中发现:电解条件下可把水分解成H 和O。他设想用电解的方
2 2
法从KOH、NaOH中分离出K和Na。最初,戴维用饱和KOH溶液进行电解,不料还是得到H 和O 。这
2 2
时,他考虑在无水条件下继续这项实验,不料,实验中产生的金属液珠一接触空气就立即燃烧起来;这
时,他又考虑在________条件下电解熔融的KOH继续实验,最后他终于成功地得到了银白色的金属钾。
(2)最近,德国科学家实现了铷原子气体超流体态与绝缘态的可逆转换,该成果将在量子计算机研究方
面带来重大突破。已知铷是37号元素,相对原子质量是85。根据材料回答下列问题:
Ⅰ.铷位于元素周期表的第________周期________族。
Ⅱ.关于铷的下列说法中正确的是________(填序号,下同)。
①与水反应比钠更剧烈 ②Rb O在空气中易吸收水和二氧化碳 ③Rb O 与水能剧烈反应并释放出
2 2 2
O ④它是极强的还原剂 ⑤RbOH的碱性比同浓度的NaOH弱
2
Ⅲ.现有铷和另一种碱金属形成的合金5 g,与足量水反应时生成标准状况下的气体2.24 L,则另一碱
金属可能是________(填元素符号)。
【答案】(1)隔绝O
2
(2)Ⅰ.五 第ⅠA Ⅱ.①②③④ Ⅲ.Na或Li
【解析】(1)有水或氧气存在的条件下,钾会被氧化。(2)Ⅰ.Rb是碱金属的37号元素,位于K的下面,它位于第五周期ⅠA族。
Ⅱ.Rb的结构性质与Na相似,且更活泼,对应的Rb O、Rb O 、RbOH的性质分别与NaO、NaO 、
2 2 2 2 2 2
NaOH相似,所以选①②③④。
Ⅲ.从碱金属与水反应通式2R+2HO===2ROH+H↑可知,生成0.1 mol H ,碱金属的物质的量为0.2
2 2 2
mol,所以合金的平均摩尔质量==25 g·mol-1,而M(Rb)>25 g·mol-1,则另一碱金属的M必小于25 g·mol
-1,所以可能是Na或Li。