文档内容
第一节 原子结构与元素周期表
第2课时 元素周期表、核素
基础巩固
1.(2022·辽宁大连·高一期末)下列说法不正确的是
A.道尔顿提出了原子学说,为近代化学的发展奠定了坚实的基础。
B.门捷列夫将元素按原子序数由小到大的顺序依次排列,制出了第一张元素周期表
C.我国化学家侯德榜发明了侯氏制碱法,为我国的化学工业发展和技术创新做出了重要 贡献
D.我国科学家居呦呦因在研制青蒿素等抗疟药物方面的卓越贡献,被授予诺贝尔生理学-或医学奖
【答案】B
【解析】A.道尔顿提出的近代原子学说对化学的发展起着十分重要的作用,因而有“原子之父”的美
誉,故A正确;
B.门捷列夫按照相对原子质量大小制出第一张元素周期表,不是按原子序数由小到大的顺序依次排列,
故B错误;
C.我国化学家侯德榜发明了侯氏制碱法,为我国的化学工业发展和技术创新做出了重要贡献,打破了西
方的垄断,故C正确;
D.我国科学家居呦呦因在研制青蒿素等抗疟药物方面的卓越贡献,被授予诺贝尔生理学-或医学奖,被
誉为“青蒿素之母”,故D正确;
故选:B。
2.(2022·黑龙江·宾县第二中学高一期末)2018年中国化学会制作了新版周期表,包含118种元素。下
列有关元素周期表说法正确的是
A.元素周期表中含元素最多的族是第ⅢB族
B.元素周期表有18个族
C.第ⅠA族的元素全部是金属元素
D.短周期是指第一、二、三、四周期
【答案】A
【解析】A.第ⅢB族含有镧系和錒系,所以元素周期表中含元素最多的族是第ⅢB族,故A正确;
B.元素周期表有7个主族、7个副族、1个0族、1个第ⅢB族,共16个族,故B错误;
C.第ⅠA族的元素除H外,全部是金属元素,故C错误;
D.短周期是指第一、二、三周期,故D错误;
选A。
3.(2022·上海市北虹高级中学高二期末)某元素原子的第三电子层上只有 1 个电子,该元素在周期表
中的位置是
A.第二周期IA 族 B.第三周期IA 族
C.第二周期VIIA 族 D.第三周期IIA 族
学科网(北京)股份有限公司【答案】B
【解析】某元素原子的第三电子层上只有 1 个电子,说明是第三周期的元素,最外层只有1个电子,说
明是第IA 族元素,因此该元素在周期表中的位置是第三周期IA 族,故B符合题意。
综上所述,答案为B。
4.(2022·江西省万载中学高一阶段练习)根据中学化学教材所附元素周期表判断,下列叙述正确的是
A.L层电子数为奇数的所有元素都是非金属
B.第三、四、五周期元素的种数分别是8、18、32种
C.由左往右数第8、9、10三列元素中没有非金属元素
D.只有第ⅡA族元素的原子最外层有2个电子
【答案】C
【解析】A.L电子层电子数为奇数的所有元素有Li、B、N、F,其中Li是金属,其余是非金属,故A错
误;
B.第3、4、5、6周期元素的数目分别是8、18、18、32,故B错误;
C.由左至右第8、9、10三列元素是第Ⅷ族,全部是金属元素,没有非金属元素,故C正确;
D.第ⅡB族以及部分第Ⅷ族元素的原子最外层有2个电子,故D错误;
答案选C。
5.(2022·黑龙江·宾县第二中学高一开学考试)下列各图若为元素周期表的一部分(表中数字代表原子序
数),其中合理的是
A. B.
C. D.
【答案】D
【解析】A.2号元素为He,位于元素周期表最右一列,故A错误;
B.11号元素位于ⅠA族,在元素周期表最左一列,故B错误;
C.10号元素为Ne,位于元素周期表最右一列,故C错误;
D.6号C元素、14号Si元素、32号Ge元素都位于ⅣA族,故D正确;
选D。
6.(2022·甘肃·民勤县第一中学高二开学考试)已知A为ⅡA族元素,B为ⅢA族元素,它们的原子序数
分别为m和n,且A、B为同一周期的元素,下列关系式错误的是
A.n=m+1 B.n=m+11 C.n=m+25 D.n=m+18
【答案】D
【解析】A.若为短周期,ⅡA族元素、ⅢA族元素的原子序数相差1,即n=m+1,故A正确;
B.若元素在四、五周期,中间有10个纵行,ⅡA族元素、ⅢA族元素的原子序数相差11,即n=m+11,
故B正确;
学科网(北京)股份有限公司C.若元素在五、六周期,中间有10个纵行,且存在镧系(14种元素)和锕系,ⅡA族元素、ⅢA族元
素的原子序数相差25,即n=m+25,故C正确;
D.由以上分析可知,无论元素在短周期还是长周期,都不存在n=m+18,故D错误;
故答案为D。
7.(2022·上海·上外附中高一期中)在元素周期表中,应用于计算机芯片的硅元素如图所示,下列有关
硅的说法正确
A.原子核外有14个电子 B.原子个数是14
C.硅原子的相对原子质量是28.09 D.质量数是28.09
【答案】C
【解析】A.由题干图中可知,原子序数是14,每个硅原子核外有14个电子,A错误;
B.图中14是指元素的原子序数、质子数、核电荷数等,而不是原子个数,B错误;
C.由图可知,硅原子的相对原子质量是28.09,C正确;
D.质量数等于质子数和中子数之和、在数值上等于相对原子质量取整,故是28,D错误;
故选C。
8.(2022·北京·北师大实验中学高一期中) Sr(锶)的87Sr、86Sr稳定同位素在同一地域土壤中87Sr/86Sr值不
38
变。土壤生物中87Sr/86Sr值与土壤中87Sr/86Sr值有效相关。测定土壤生物中87Sr/86Sr值可进行产地溯源。下
列说法不正确的是
A.87Sr和86Sr互为同位素
B.87Sr和86Sr含有的中子数分别为49和48
C.同一地域产出的同种土壤生物中87Sr/86Sr值相同
D.87Sr和86Sr的化学性质不相同
【答案】D
【解析】A.87Sr和86Sr是质子数相同、中子数不同的原子,互为同位素,故A正确;
B.87Sr和86Sr含有的中子数分别为87-38=49和86-38=48,故B正确;
C.87Sr、86Sr是 Sr的稳定同位素,同一地域产出的同种土壤生物中87Sr/86Sr值相同,故C正确;
38
D.87Sr和86Sr核外电子排布相同,所以化学性质相同,故D错误;
选D。
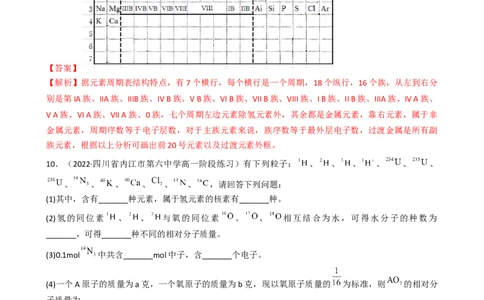
9.(2022·全国·高一)在表中用实线画出周期表的外框,写明族序数和周期序数,并在相应的空格内写
出1~20号元素的元素符号,用虚线画出过渡元素外框___。
学科网(北京)股份有限公司【答案】
【解析】据元素周期表结构特点,有7个横行,每个横行是一个周期,18个纵行,16个族,从左到右分
别是第IA族、IIA族、IIIB族、IV B族、V B族、VI B族、VII B族、VIII族、I B族、II B族、IIIA族、IV A族、
V A族、VI A族、VII A族、0族,七个周期左边元素除氢元素外,其余都是金属元素,靠右元素,属于非
金属元素,周期序数等于电子层数,对于主族元素来说,族序数等于最外层电子数,过渡金属是所有副
族元素,根据以上分析可画出前20号元素以及过渡元素外框。
10.(2022·四川省内江市第六中学高一阶段练习)有下列粒子: 、 、 、 、 、 、
、 、 、 、 、 、 ,请回答下列问题:
(1)其中,含有_______种元素,属于氢元素的核素有_______种。
(2)氢的同位素 、 、 与氧的同位素 、 、 相互结合为水,可得水分子的种数为
_______,可得_______种不同的相对分子质量。
(3)0.1mol 中共含_______mol中子,含_______个电子。
(4)一个A原子的质量为a克,一个氧原子的质量为b克,现以氧原子质量的 为标准,则 的相对分
子质量为_______。
【答案】(1) 7 3
(2) 18 7
(3) 2.1 2.2
(4)
【解析】(1)元素的种类由质子数决定,质子数不同,元素的种类就不同,有H、U、N、K、Ca、Cl、C
共7种元素,氢元素的核素有3种 、 、 ,故答案为:7;3;
学科网(北京)股份有限公司(2)由氧的同位素有16O、17O、18O,氢的同位素有 、 、 ,在1个水分子中含有2个氢原子和1
个氧原子,若水分子中的氢原子相同,则16O可分别与 、 、 构成水,即存在三种水;17O可分别
与 、 、 构成水,即存在三种水;18O可分别与 、 、 构成水,即存在三种水;若水分子
中的氢原子不同,则16O可分别与1H2H、2H3H、1H3H构成水,即存在三种水;17O可分别与1H2H、2H3H、
1H3H构成水,即存在三种水;18O可分别与1H2H、2H3H、1H3H构成水,即存在三种水;所以共形成3×6=18
种水,所以相对分子质量不同的水分子种数为18、19、20、21、22、23、24,共7种,
故答案为:18;7;
( 3 ) 0.1mol 中 共 含 中 子 物 质 的 量 =0.1mol×(14-7)×3=2.1mol , 所 含 电 子 数
=0.1mol×(7×3+1)×NA=2.2NA,故答案为:2.1;2.2NA;
(4)一个A原子的质量为a克,一个氧原子的质量为b克,现以氧原子质量的 为标准,氧原子相对原
子质量为16,则AO2的相对分子质量= ,故答案为: 。
能力提升
11.(2022·山西省大同市期末)我国拥有自主知识产权的硅衬底高光效氮化镓发光二极管(简称LED)技
术,已广泛用于照明、显像等多个领域。氮和镓的原子结构示意图及镓在元素周期表中的信息如图所示,
下列说法正确的是
A.镓的相对原子质量是69.72 g
B.镓原子核内有31个中子
C.镓元素位于第三周期、IIIA族
D.氮化镓的化学式为GaN
【答案】D
【解析】A项,相对原子质量的单位为“1”,故镓的相对原子质量是69.72,错误;B项,由图可知,镓
原子核内有31个质子,中子数目无法确定,错误;C项,根据主族元素的周期序数等于其原子的电子层
数,主族序数等于其原子的最外层电子数,故镓元素位于第四周期、IIIA族,错误;D项,由N、Ga的原
子结构示意图可知,N可显-3价,Ga显+3价,故氮化镓的化学式为GaN,正确。
12.若把元素周期表原先的主、副族及族号取消,由左至右改为18列。如碱金属元素为第1列,稀有气体元
素为第18列。按此规定,下列说法错误的是( )。
A.只有第2列元素的原子最外层有2个电子
学科网(北京)股份有限公司B.第14列元素形成的化合物种类最多
C.第3列元素种类最多
D.第17列元素都是非金属元素
【答案】A
【解析】第2列最外层2个电子,第18列的He及第3列到第12列的多数过渡元素原子的最外层也是2个
电子,故A项错误。第14列含有碳元素,形成化合物种类最多,B项正确。第3列含镧系元素和锕系元素,C
项正确。第17列全为非金属元素,D项正确。
13.(2022·全国·高一课时练习)某同学设计如下元素周期表,已知X元素的气态氢化物水溶液呈碱性,
空格中均有对应的元素填充。以下说法正确的是
A.X、Y、Z元素分别为N、P、O
B.白格中都是主族元素,灰格中都是副族元素
C.Z的氢化物只有一种
D.X、Z的简单氢化物的沸点:
【答案】A
【解析】A.根据该同学设计的元素周期表的形式和表中元素位置可知:X的原子序数为7,Z的原子序数
为8,Y的原子序数为15,因此X为N,Z为O,Y为P,A正确;
B.白格中的稀有气体元素 不属于主族元素,B错误;
C.Z的氢化物有 、 ,C错误;
D.Z的简单氢化物为水,常温下水为液态,氨气为气态,沸点: ,D错误;
故选A。
14.(2022·全国·高一课时练习)某同学在学习元素周期表后,绘制了一张“跑道式”元素周期表,结构
如图所示:
学科网(北京)股份有限公司下列有关叙述错误的是
A.元素a位于第四周期第IA族
B.元素b只能形成一种单质分子
C.元素c、d、e、f、g的原子最外层电子数相同
D.位置h和i处均各含有15种元素
【答案】B
【解析】A.根据编排原则,可知元素a为K元素,在周期表中位于第四周期第ⅠA族,A项正确;
B.元素b为O元素,可形成 等单质分子,B项错误;
C.元素c、d、e、f、g分别为 ,为第ⅦA族元素,其原子最外层均有7个电子,C项正
确;
D.位置h和i分别为镧系和锕系元素,两处均各含有15种元素,D项正确;
故选B。
15.化学上普遍应用的元素周期表已经成为化学的一种标志,这是历代化学家经过一百多年不断完
善的结果。从1869年门捷列夫制出第一个元素周期表开始,人们给出了形形色色的“元素周期表”。其
中曾出现了一种扇形元素周期表,如图是扇形元素周期表的一部分(前四周期的元素),对比中学常见元素
周期表,回答下列问题。
(1)E代表的元素处于常见周期表的位置是 ;G元素的离子结构示意图:
。
(2)A元素有多种不同的原子,写出可以用于制造氢弹的A元素的核素符号: 。
(3)C元素在自然界有多种单质存在,这些单质之间的关系是 。
(4)L 元素与 K 元素可以组成两种化合物,为了区分这两种化合物需要用到的试剂是
,其中一种化合物的水溶液与L单质反应转化为另一种化合物,其离子方程式为 。
【答案】(1)第二周期第ⅥA族
(22H、3H (3)同素异形体 (4)KSCN溶液 2Fe3++Fe=3Fe2+
1 1
【解析】由位置可知,A为H,B为Na,C为C,D为N,E为O,F为Mg,G为Al,J为S,K为
Cl,M为Br,L为Fe。(1)O元素位于第二周期第ⅥA族,Al的离子结构示意图为 。(2)可用于制造
氢弹的是2H、3H。(3)C元素在自然界有金刚石、石墨、C 等多种单质,其互为同素异形体。(4)Fe元素
1 1 60
与Cl元素可以组成FeCl 、FeCl ,检验Fe3+需要用KSCN溶液;FeCl 与Fe反应可转化为FeCl :2Fe3+
2 3 3 2
+Fe=3Fe2+。
学科网(北京)股份有限公司学科网(北京)股份有限公司学科网(北京)股份有限公司