文档内容
第四章《化学反应与电能》教学设计
第一节 原电池的工作原理
第一课时 原电池的工作原理
课题: 4.1.1 原电池的工作原理 课时 1 授课年级 高二
内容要求:认识化学能与电能相互转化的实际意义及其重要应用。从氧化还原反应的角度初
课标
步认识原电池的工作原理。了解原电池及常见化学电源的工作原理,理解原电池的构造组
要求
成。
学业要求:能分析、解释原电池的工作原理,能设计简单的原电池及创造性实验设计。
本节内容是高中化学人教版(2019版)选择性必修1第四章第一节《原电池的工作原理》
内容。电化学知识的学习,既可以为必修课程中原电池知识的学习提升高度,又可以让学生理
解、设计、掌握电化学中原电池的设计,进一步掌握化学科学的研究方法,培养学生的科学素
养。原电池原理这部分知识涉及学生对氧化还原反应、微粒观的认识发展以及分析体系中化学
反应的基本思路,但是这两块知识点在初高中必须模块已经深入学习。氧化还原反应原理,能
基本理解原电池的功能是化学能转化为电能。本册书的第一章,从物质的反应、微粒的运动、
能量的转化等各个角度,带学生又学习了化学能与热能的转化原理。
根据课标要求,本节内容分两个课时完成,由于“化学能与电能”是化学学科的重要原理
性之一,也是对氧化还原反应原理本质的拓展及应用,并在本章节要深入学习化学能与电能的
相互转化,所以本节内容有着承上启下的重要作用。让学生初步形成“原电池原理-结构-设
计”学习的基本思维模型,进一步突出本节内容的学习重点,突破进行难点,培养学生的高阶
教材 思维能力,因此,本节内容共分两个课时完成。
分析 本节课内容顺应新时代发展理念:能源与可持续发展,遵循新课标的要求,有利于培养学
生的核心素养。教材通过对单液原电池电池效率的探究,引出双液原电池,引出半电池、盐
桥、内电路、外电路等概念,对原电池工作原理的概貌有比较深入的了解。由于原电池在实际
生活、工农业生产、科学研究中应用广泛,学好本节知识,具有比较重要的理论意义和现实意
义。在化学能与电能的基础上,引入盐桥的概念,进一步巩固原电池的工作原理,在氧化还原
反应、能量转换、电解质溶液的等知识的基础上,为后面学习电解原理、金属的腐蚀与防护等
奠定基础。
(1)通过对 “Cu-Zn(CuSO 溶液)”装置的理解,观察,总结该原电池装置工作过程
4
中的实验现象(如:是否有电流产生、两电极表现产生的现象、电解质溶变化等),总结
原电池构成的条件,讨论并给出结论原电池工作原理。
(2)通过观察“Cu-Zn(盐桥)”原电池装置特点及产生电流的实验现象,分析形成电流
教学
的微观过程,了解盐桥的作用,进一步了解“氧化剂和还原剂完全隔离”的原电池装置的
目标 反应原理。
(3)通过对原电池工作原理的学习,进一步带学生完成对指定原电池的设计。
(4)单液“Cu-Zn(CuSO 溶液)”原电池装置到“Cu-Zn(盐桥)”原电池装置改进的
4
分析过程,分组讨论实验现象,总结双液原电池的工作原理。
重点 重点:原电池原理、盐桥的作用、探究能力的培养
难点 难点:原电池设计改进、探究能力的培养
核心 宏观辨识与微观探析:宏观上通过学生对锌铜原电池的实验现象的观察,得出有效实验信
息加以分析;微观角度理解原电池工作原理,拓展氧化还原反应思维。
素养科学探究与创新意识:通过实验探究,初步体验有序、全面、敏锐观察实验现象的方法,
并能准确地用语言描述,尝试对现象进行分析、归纳,培养初步的科学探究能力。
科学精神与社会责任:通过对单液电池的探究分析,改进普通原电池装置,正确理解盐桥
在电化学中的应用。理解科学认识来源于实践的科学精神,科学认识的方法之一是定性与定量
相结合。
从学生的知识认知看,高一《必修二》的学习中,已经讲解了 Zn-CuSO-Cu简单的原电
4
池,对于原电池的原理以及装置的设计学生还是有一定基础认知的。所以知识上基本要求有①
金属的性质;②电解质溶液概念;③氧化还原反应原理;④生活中常见电池的认知。但选修对
于原电池原理的难度要求是一个阶梯上升过程。选修阶段学生学习认知障碍可能是电极材料与
电极反应物的关系、电解质溶液与电极反应物的关系;如何理解双液原电池;微观角度理解原
电池中微粒的运动和反应等系列问题。
学情 学生已经具备氧化还原反应、原电池等基础知识,对简单的原电池有一定的知识贮
备,有较高的动手能力和实验操作能力的同学,但对知识运用能力有待提高,本节课将在
分析
此基础上,充分发挥学生的主动性,探究更加高效的原电池装置,让学生在探究的过程中
体验动手操作和合作的乐趣,能力上提高学生的观察能力、实验能力、思维能力,重点培养
学生对原电池的设计能力以及实验创新能力,进一步激发学生的学习兴趣。
教学过程
教学 设计意
教学活动
环节 图
【环节设计】
环 教学环节 设计意图 根据高
一必修
节
复习反应原理,电池的构成条件,为后期双 二的学
一 回顾探究单液原电池
液原电池的探究做准备。 习,回
、
生 顾并总
探究双液原电池,盐桥的工 师生通过系类问题的讨论,改进单液原电池
情 活 结原电
作原理 的方法,构建盐桥原电池。
景 情 池原
导 境 对比单液原电池和双液-盐桥 学生通过观察实验现象,进行双液原电池的 理。
入 原电池的实验现象 特点及优点讨论,给出自己的结论。
创设生
根据原电池原理的学习,引 激发学生的实验兴趣,培养学生的观察能 活中电
导学生设计原电池装置 力,加强对知识的理解。 池的应
用,激
盐桥变膜,初步了解离子交
培养学生的实验探究能力,进一步 发探究
换膜的作用
欲望。
一、知识回顾
1.原电池构成的条件有哪些?分别起到的作用是什么?
【互动提示】
装置条件:
① 构成原电池需电极,金属电极需要活泼性不同;
②电解质溶液,其中一电极可以与电解质溶液发生氧化还原反应;
③闭合的回路;将两电极深入到电解质溶液中,两电极间用导线连接构成闭合回路;
④自发的氧化还原反应。
起到作用:电极的作用是导电,有些电池中电极材料会参加反应;导线的作用是传导电子;电解
质溶液的作用是通过自由离子的移动传导电荷。
【互动试题1】下列装置能形成原电池的是( )
【答案】 C
【解析】A中酒精不是电解质溶液,所以无法发生自发的氧化还原反应;
B中装置两电极没有活泼性的差异;C装置中满足原电池构成的条件,有活泼性不同
的两级,电解质溶液,形成闭合回路同时形成自发的氧化还原反应;D装置中不能形
成闭合的回路,故本题答案选C。
2.在铜锌稀硫酸原电池中,电子是怎样移动的?电子能否通过电解质溶液?如果不
能,电流是如何形成的?
【互动提示】
由于金属锌比金属铜活泼,锌失去电子,电子通过导线流向铜片。电子不能通过电解
质溶液,在稀硫酸中H+移向铜片,SO移向锌片,阴阳离子定向移动形成电流。
二、新知预习
请画出原电池的工作原理简图,标出电子、电流、离子的移动方向,并指出有何
特点和规律?
【导入】我们生活中无处不见电池的使用,户外运动检测的电子手表;手机、笔
记本电脑很多家用电器都需要使用电池;还有近几年推行的环保交通工具,电动汽
车,它的主要核心就是在电池的技术,那么大家知道电池的能量是如何转化的吗?环活 【知识回顾】
动
环 实验演示:将锌片和铜片分别用夹子夹好与电流表串联,再同时插入到盛有CuSO 溶
一 4
节 、 液的烧杯中,如图所示:
通过实
二 原 【问题1】观察两电极的现象,电解质溶液的现象及电流表的读数如何变化? 验观
电 察、总
池 结实验
原 中现象
理 数据,
双
的 培养学
液 理 生构建
解 实验模
原
型的能
【回答】
电 力,发
①锌片逐渐溶解,铜片一级厚度再变大,颜色仍是红色; 展学生
池
模型认
②CuSO 溶液颜色逐渐变浅;
4
知的思
③电流表的指针发生偏转 维能
力。
【问题2】电流表的指针发生偏转,思考其中的能量转化?
【回答】指针发生偏转,说明产生了电流,在该装置中没有外加电源,只有两电极片
与电解质溶液间的反应,所以,可以理解为化学能转化为电能。
【问题3】将化学能转化为电能,这种装置称为原电池,那么思考,原电池构成的条
件有哪些呢?
【回答】
①活泼性不同的两级;②电解质溶液;③闭合的回路;④自发的氧化还原反应。
【问题4】思考原电池中电子流动方向和电流方向有何特点?
【回答】
①外电路:
电子的移动:由负极(Zn片)→导线→正极(Cu片)。
电流的移动:由正极(Cu片)→导线→负极(Zn片)。
②内电路:阳离子移向正极,阴离子移向负极。
【记忆小口诀】电子不下水(电子只在导线和电极移动,不可进入到溶液中);
离子不上岸(离子会在电解质溶液中定向移动,不进入导线)
【过渡】根据学生们的问题回答,继续引导问题讨论,从书写电极方程式入手。
【思考1】如何书写两极的电极反应?
【回答】从反应类型角度可以得出,负极发生氧化反应,正极发生还原反应;可以技
巧记忆“负氧正还”。电极方程式书写:
负极反应式:Zn-2e-===Zn2+;正极反应式:Cu2++2e-===Cu;电池总反应的离子
方程式是Zn+Cu2+===Zn2++Cu。
【思考2】通过原电池原理的问题分析,得出装置是两个半电池,可以分成锌半电池
和铜半电池。氧化、还原反应分别是在两级分开反应的,但是少量的Cu2+还会在Zn
表面还原的,我们如何阻止?
【引导】① 引导学生将两级分别插入不同的烧杯中;
② 引导学生思考如何将两池关联形成闭合回路,并介绍老师展示的“盐桥”,讲解
其结构及作用;
③ 引导学生两池中加入电解质溶液的设置。
活 【过渡】介绍实验台上的装置,是一个装有饱和KCl和琼脂的装置,这个装置的作用 利用已
动 有知
是起到联通两个电解质溶液,所以我们称之为盐桥。下面我们按照教材P94页实验4-
二 识,预
、 1,按下图所示装置完成实验,并回答下列问题: 测物质
双 的性
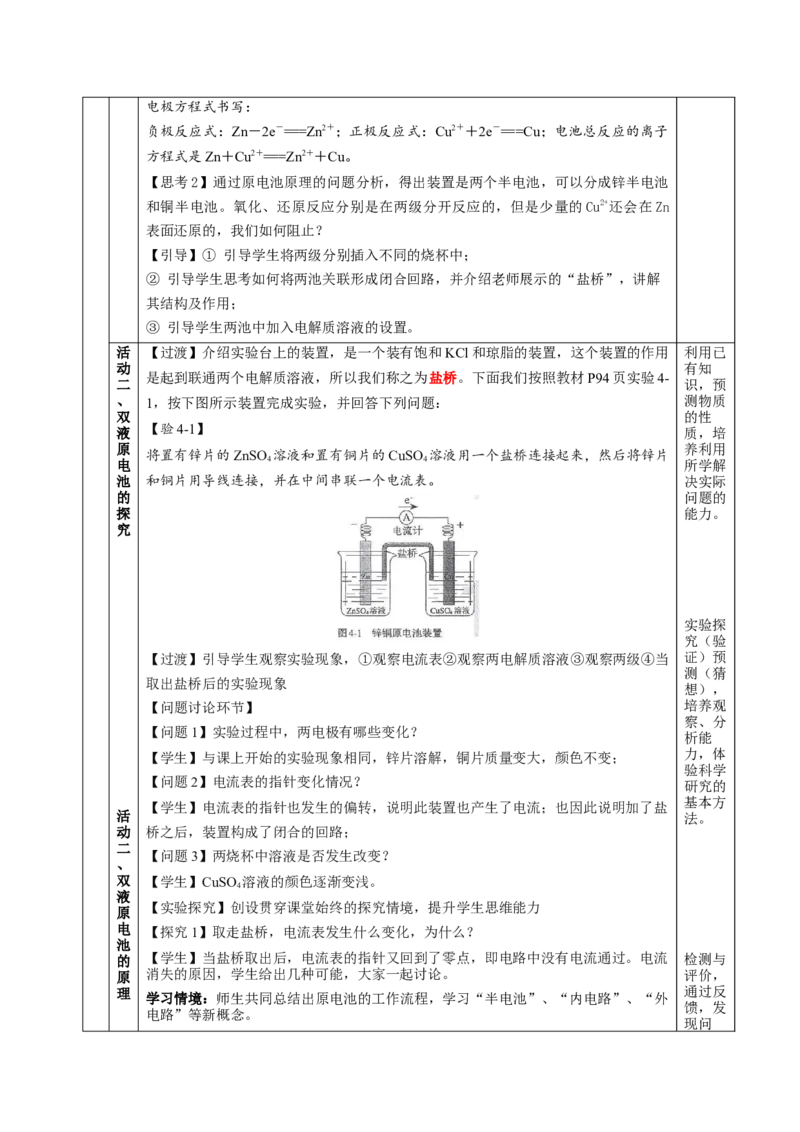
液 【验4-1】 质,培
原 养利用
将置有锌片的ZnSO 溶液和置有铜片的CuSO 溶液用一个盐桥连接起来,然后将锌片
电 4 4 所学解
池 和铜片用导线连接,并在中间串联一个电流表。 决实际
的 问题的
探 能力。
究
实验探
究(验
【过渡】引导学生观察实验现象,①观察电流表②观察两电解质溶液③观察两级④当 证)预
测(猜
取出盐桥后的实验现象
想),
【问题讨论环节】 培养观
察、分
【问题1】实验过程中,两电极有哪些变化?
析能
【学生】与课上开始的实验现象相同,锌片溶解,铜片质量变大,颜色不变; 力,体
验科学
【问题2】电流表的指针变化情况?
研究的
基本方
【学生】电流表的指针也发生的偏转,说明此装置也产生了电流;也因此说明加了盐
活 法。
动 桥之后,装置构成了闭合的回路;
二
【问题3】两烧杯中溶液是否发生改变?
、
双 【学生】CuSO 溶液的颜色逐渐变浅。
4
液
【实验探究】创设贯穿课堂始终的探究情境,提升学生思维能力
原
电 【探究1】取走盐桥,电流表发生什么变化,为什么?
池
的 【学生】当盐桥取出后,电流表的指针又回到了零点,即电路中没有电流通过。电流 检测与
原 消失的原因,学生给出几种可能,大家一起讨论。 评价,
理 通过反
学习情境:师生共同总结出原电池的工作流程,学习“半电池”、“内电路”、“外
馈,发
电路”等新概念。
现问【思考与讨论】 题,调
控课
(1)图4-1所示的铜锌原电池工作中,电子在导线的移动方向是怎样的?阴离子、
堂,提
阳子离在电解质溶液中的移动方向是怎么样的? 高效
率。
电子的移动方向:电子由Zn失去,经导线流向Cu电极。
离子的移动方向:
①硫酸锌溶液中:Zn2+向盐桥移动;
②硫酸铜溶液中:Cu2+向铜极移动;
③盐桥中:K+移向正极区(CuSO 溶液),Cl-移向负极区(ZnSO 溶液),使氧化还原反
4 4
应持续进行,不断的产生电流。
(2)铜锌原电池可以看做由两个半电池组成,一个发生氧化反应、另一发生还原反
应;分别写出两个不同电极反应方程式?
负极反应式:Zn-2e-===Zn2+,发生氧化反应;正极反应式:Cu2++2e-===Cu,发生
还原反应;电池总反应的离子方程式是Zn+Cu2+===Zn2++Cu。
【教师】我们上述的原电池,就称为“双液原电池”,思考盐桥的组成及作用是什
么?
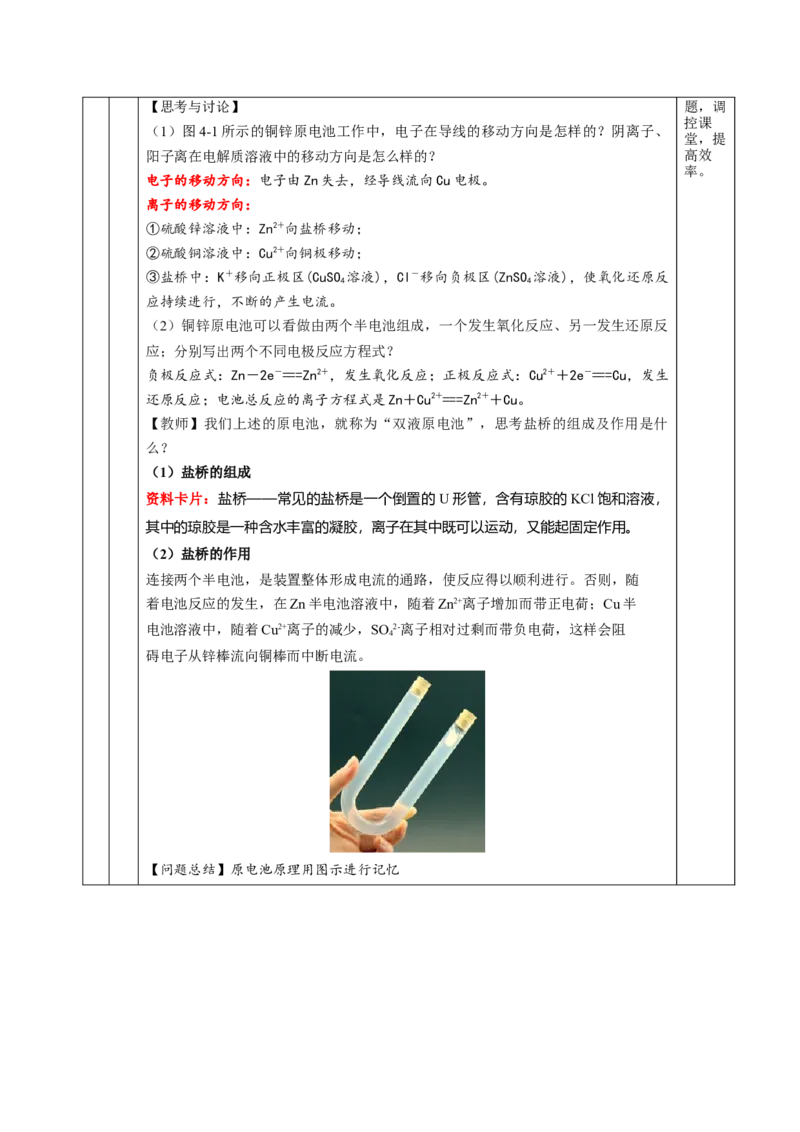
(1)盐桥的组成
资料卡片:盐桥——常见的盐桥是一个倒置的 U形管,含有琼胶的KCl饱和溶液,
其中的琼胶是一种含水丰富的凝胶,离子在其中既可以运动,又能起固定作用。
(2)盐桥的作用
连接两个半电池,是装置整体形成电流的通路,使反应得以顺利进行。否则,随
着电池反应的发生,在Zn半电池溶液中,随着Zn2+离子增加而带正电荷;Cu半
电池溶液中,随着Cu2+离子的减少,SO 2-离子相对过剩而带负电荷,这样会阻
4
碍电子从锌棒流向铜棒而中断电流。
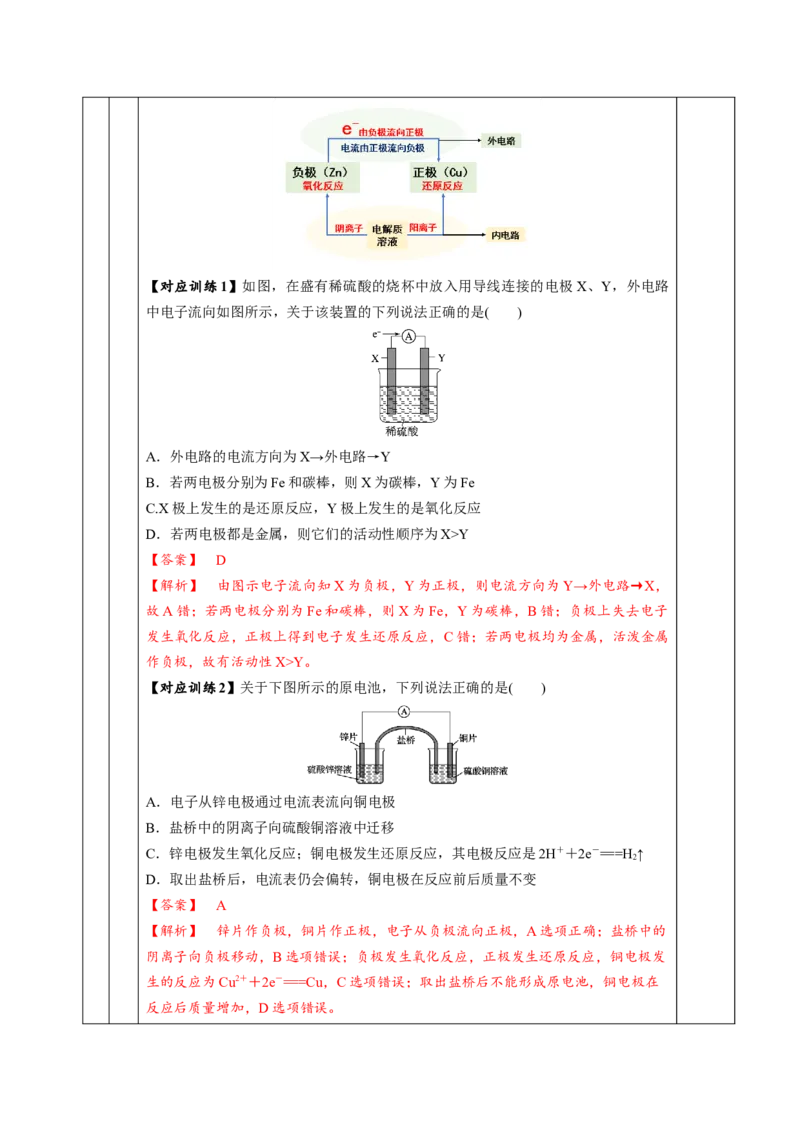
【问题总结】原电池原理用图示进行记忆【对应训练1】如图,在盛有稀硫酸的烧杯中放入用导线连接的电极X、Y,外电路
中电子流向如图所示,关于该装置的下列说法正确的是( )
A.外电路的电流方向为X→外电路→Y
B.若两电极分别为Fe和碳棒,则X为碳棒,Y为Fe
C.X极上发生的是还原反应,Y极上发生的是氧化反应
D.若两电极都是金属,则它们的活动性顺序为X>Y
【答案】 D
【解析】 由图示电子流向知X为负极,Y为正极,则电流方向为Y→外电路→X,
故A错;若两电极分别为Fe和碳棒,则X为Fe,Y为碳棒,B错;负极上失去电子
发生氧化反应,正极上得到电子发生还原反应,C错;若两电极均为金属,活泼金属
作负极,故有活动性X>Y。
【对应训练2】关于下图所示的原电池,下列说法正确的是( )
A.电子从锌电极通过电流表流向铜电极
B.盐桥中的阴离子向硫酸铜溶液中迁移
C.锌电极发生氧化反应;铜电极发生还原反应,其电极反应是2H++2e-===H ↑
2
D.取出盐桥后,电流表仍会偏转,铜电极在反应前后质量不变
【答案】 A
【解析】 锌片作负极,铜片作正极,电子从负极流向正极,A选项正确;盐桥中的
阴离子向负极移动,B选项错误;负极发生氧化反应,正极发生还原反应,铜电极发
生的反应为Cu2++2e-===Cu,C选项错误;取出盐桥后不能形成原电池,铜电极在
反应后质量增加,D选项错误。【对应练习3】用铜片、银片设计成如图所示的原电池。以下有关该原电池的叙述正
确的是( )
A.电子通过盐桥从乙池移向甲池
B.铜片是负极,发生还原反应
C.开始时,银片上发生的反应是Ag-e-=Ag+
D.将铜片浸入AgNO 溶液中发生的化学反应与该原电池总反应相同
3
【答案】D
【分析】根据题中装置,原电池的总反应为Cu+2Ag+=Cu2++2Ag,即铜片为负极,银
片为正极,根据原电池工作原理进行分析;
【详解】A.根据原电池工作原理,电子从铜片经电流计流向银片,电子不通过盐
桥,故A错误;
B.根据上述分析,铜片是负极,根据原电池工作原理,负极上失去电子,发生氧化
反应,故B错误;
C.银片为正极,电极反应式为Ag++e-=Ag,故C错误;
D.铜比银活泼,将铜片浸入AgNO 溶液中发生的化学反应方程式为
3
Cu+2AgNO =Cu(NO)+2Ag,与该原电池总反应相同,故D正确;
3 3 2
【对应练习4】铜锌原电池(如图)工作时,下列叙述正确的是( )
A.正极反应为Zn-2e-=Zn2+
B.盐桥中的K+移向ZnSO 溶液
4
C.在外电路中,电流从负极流向正极
D.Cu电极发生还原反应
【答案】D
【解析】A.铜做正极,发生还原反应,电极反应为:Cu2++2e-=Cu,A不符合题意;
B.锌作负极,发生氧化反应,电极反应为:Zn-2e-=Zn2+;硫酸锌溶液中锌离子浓度
增大,盐桥中的氯离子移向硫酸锌溶液;盐桥中的K+移向CuSO 溶液,故B不符合
4
题意;
C.原电池工作时,在外电路中,电子从电池负极经外电路流向正极,电流方向与之相反,故C不符合题意;
D.Cu电极做正极,发生还原反应,故D符合题意;
引导学生分析原电池的构造,激发学生根据原电池原理独立设计不同原电池的想法。 通过对
单液原
活
【提问1】原电池电极及电极反应有哪些特点?
电池和
动 【学生】通过点单液原电池,双液原电池的学习,对电极的观察,总结以下特点: 双液原
三 电池的
、 ①负极为电子流出极,相对活泼,通常是活动性较强的金属或某些还原剂,负极被氧 归纳总
原 化,发生氧化反应。 结,建
电 构原电
池 ②正极为电子流入极,相对不活泼,通常是活动性较差的金属或非金属导体,一般是 池 模
的 电解质溶液中的氧化性强的离子被还原或电极上附着物本身被还原,发生还原反应。 型,发
设 展学生
计 【提问2】引导学生们自己设计原电池,分小组讨论。 模型认
与 【讨论1】 知的思
改 维 方
进 同学们首先提出原电池的构成条件 法。
改
老师可以引导学生从原电池的其中一个条件出发进行设计第一步:
进
① 自发的氧化还原反应都可以设计成原电池。
② 接下来,根据选定合适氧化还原反应,进行电极,电解质溶液的选定。
【讨论2】
①电解质溶液:一般能与负极反应,或者溶解在溶液中的物质(如O)与负极反应。
2
②电极材料:一般较活泼的金属作负极,较不活泼的金属或非金属导体作正极。
【给出任务】根据原电池原理,判断该氧化还原反应 2Fe3++Cu===2Fe2++Cu2+能否
设计原电池,并写出电极方程式,同时设计单液原电池和双液原电池。
【学生】
①判断反应2Fe3++Cu===2Fe2++Cu2+是自发的氧化还原反应,可以设计为原电池;
②找出两个半反应:
还原反应:2Fe3++2e-===2Fe2+
氧化反应:Cu-2e-===Cu2+
③选电极:负极发生氧化反应—Cu,正极发生还原反应—选择活泼性弱于Cu的金属或
非金属石墨;
④电解质溶液:根据反应方程式,我们选择FeCl 溶液。
3
【教师】根据学生设计的思路,给出装置示意图,如下:
【提问】那么同学通过什么方法将单液原电池改到双液-盐桥电池呢?
【学生】讨论得出结论,电极的选择不变;需要两个电解质溶液装置,其中正极插入的电解质溶液不变,仍是FeCl 溶液。负极插入的电解质溶液选择CuCl 溶液。
3 2
【对应练习5】人们常常利用化学反应中的能量变化为人类服务。
下列化学反应在理论上可以设计成原电池的是( )
A. B.
C. D.
【答案】AC
【解析】(1)构成原电池的反应理论上应为发生电子转移的氧化还原反应,A、C选
项均为氧化还原反应,A、C选项正确;B、D选项均为非氧化还原反应,B、D选项
错误;故答案选A、C。
【引导】大家在观察盐桥原电池实现现象时,我们观察到有了盐桥的装置产生的电流
比较稳定,但是我们观察到电流强度逐渐变小,这是什么原因呢?
【思考】双液原电池电流弱的原因?
装置特点两电极分别在两池,离子通过盐桥移动,所以距离长。由于盐桥的体积有
限,所以离子容量小,那我们如何改进你呢?
【引入讲解】介绍 “离子交换膜”的定义,即:阴离子交换膜只允许阴离子通过,
阳离子交换膜只允许阳离子通过以及展现含有离子交换膜的装置。和学生介绍,离子
交换膜可以解决双液原电池电流弱的原因,本节课简单了解该装置,后期会继续深入
学习。
【互动】与学生讨论原电池装置的演变过程。
【对应练习3】锌铜原电池装置如图所示,其中阳离子交换膜只允许阳离子和水分子
通过,下列有关叙述正确的是( )
A.铜电极上发生氧化反应B.电池工作一段时间后,甲池的c(SO)减小
C.电池工作一段时间后,乙池溶液的总质量增加
D.阴、阳离子分别通过交换膜向负极和正极移动,保持溶液中电荷平衡
【答案】 C
【解析】 A项,由锌的活泼性大于铜,可知铜电极为正极,在正极上 Cu2+得电子
发生还原反应生成 Cu,错误;B项,由于阳离子交换膜只允许阳离子和水分子通
过,故甲池的c(SO)不变,错误;C项,在乙池中Cu2++2e-===Cu,同时甲池中的
Zn2+通过阳离子交换膜进入乙池中,由于M(Zn2+)>M(Cu2+),故乙池溶液的总质量增
加,正确;D项,阳离子交换膜只允许阳离子和水分子通过,电解过程中Zn2+通过阳
离子交换膜移向正极保持溶液中电荷平衡,阴离子是不能通过交换膜的,错误。
装置 原电池
实例
课堂
总结
原理 使氧化还原反应中电子作定向移动,从而形成电流。这种把化学
定义 能转变为电能的装置叫做原电池。
①电极:两种不同的导体相连;
形成条件
②电解质溶液:能与电极反应。
反应类型 自发的氧化还原反应
由电极本身性质决定:
电极名称 正极:材料性质较不活泼的电极;
负极:材料性质较活泼的电极。
负极:Zn-2e-=Zn2+ (氧化反应)
电极反应
正极:2H++2e-=H ↑(还原反应)
2
电子流向 负极→正极
电流方向 正极→负极
能量转化 化学能→电能
①抗金属的电化腐蚀;
应用
②实用电池。
第四章 化学能与电能
第一节 原电池
一、原电池的工作原理
1.原电池的构成条件
2.电极方程式的书写3.单液Cu-Zn原电池
板书 二、双液原电池
设计 1.盐桥定义及作用
2.双液原电池的构成条件
3.电极方程式的书写
三、原电池的设计
1.原电池的电极的判断方法
2.原电池的电极反应式的书写
四、含有离子交换膜电池
本节课目标是通过实际教学设计能更好的突出新课标的思想,尤其要培养学生的科学素
养、探究精神和人文精神。
本节课的设计思想主要是以学生为主的课堂,主角是学生,即期望通过学生探索欲望的热
情来激发学生学习的兴趣,进一步提升学生的自主学习能力,引导学生的思考,培养学生的实
验创作能力。
通过引导学生实验的总结、探究能力的创设,可以实现培养兴趣的同时,提升学生的思维
教学 主动性的要领;通过适时的提问、分组讨论与知识总结,还是“以训练语言为手段,贯穿实践
性”的体现。而且,在这堂课中,以小组为单位的实验安装,设计,操作,帮助了预期教学环
反思
节的创设,促使了学生的全面参与。
总之,在对新课程学习与探索的过程中,在对新的教学模式、方法的研究与实践中,本课
的教学将是一个有益的尝试。不论是对于教师还是对于学生,收获都将颇多。
课后 【练习1】原电池原理基础过关练习 难度:★★
作业
下面是四个化学反应,你认为理论上不可以用于设计原电池的化学反应是( )
A.2Al+2NaOH+2HO===2NaAlO+3H↑
2 2 2
B.2H+O=====2HO
2 2 2
C.MgN+6HO===3Mg(OH) +2NH ↑
3 2 2 2 3
D.CH+2O=====CO+2HO
4 2 2 2
【答案】C
【解析】只有自发的氧化还原反应才能用于设计原电池。C项反应前后元素化合价不变,
不属于自发的氧化还原反应,不能设计成原电池。
【练习2】双液原电池考点关练习 难度:★★★
根据下图,可判断出下列离子方程式中错误的是( )A.2Ag(s)+Cd2+(aq)===2Ag+(aq)+Cd(s)
B.Co2+(aq)+Cd(s)===Co(s)+Cd2+(aq)
C.2Ag+(aq)+Cd(s)===2Ag(s)+Cd2+(aq)
D.2Ag+(aq)+Co(s)===2Ag(s)+Co2+(aq)
【答案】 A
【解析】 根据原电池知识,金属活动性:负极>正极,可得三种金属的活动性顺序应为 Cd
>Co>Ag,则选项中符合此关系的置换反应成立。