文档内容
4.1.1 原电池的工作原理(学案)
1.以铜锌原电池为例,理解原电池的工作原理。
2.学会判断原电池的正、负极。
3.掌握原电池反应方程式和电极反应式的书写。
1.原电池正负极的判断;
2.原电池原理;
3.原电池电极反应方程式的书写。
原电池是:______________________________________________________
一、原电池的工作原理
1、理清氧化还原反应的两条线索
(1)还原剂→____________电子→元素化合价____________→被氧化→发生氧化反应。
(2)氧化剂→____________电子→元素化合价____________→被还原→发生还原反应。
2、原电池的工作原理
原电池是将化学能转化为电能的装置,原电池内发生的反应属于__________。
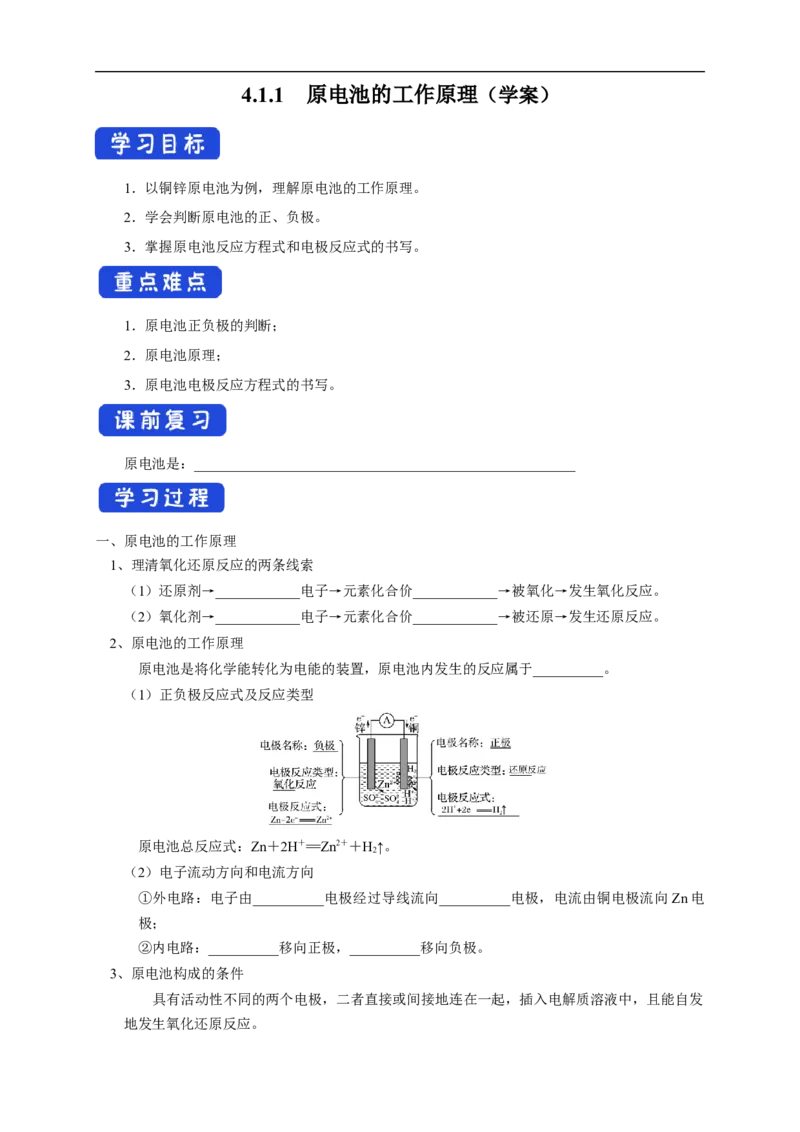
(1)正负极反应式及反应类型
原电池总反应式:Zn+2H+==Zn2++H↑。
2
(2)电子流动方向和电流方向
①外电路:电子由__________电极经过导线流向__________电极,电流由铜电极流向Zn电
极;
②内电路:__________移向正极,__________移向负极。
3、原电池构成的条件
具有活动性不同的两个电极,二者直接或间接地连在一起,插入电解质溶液中,且能自发
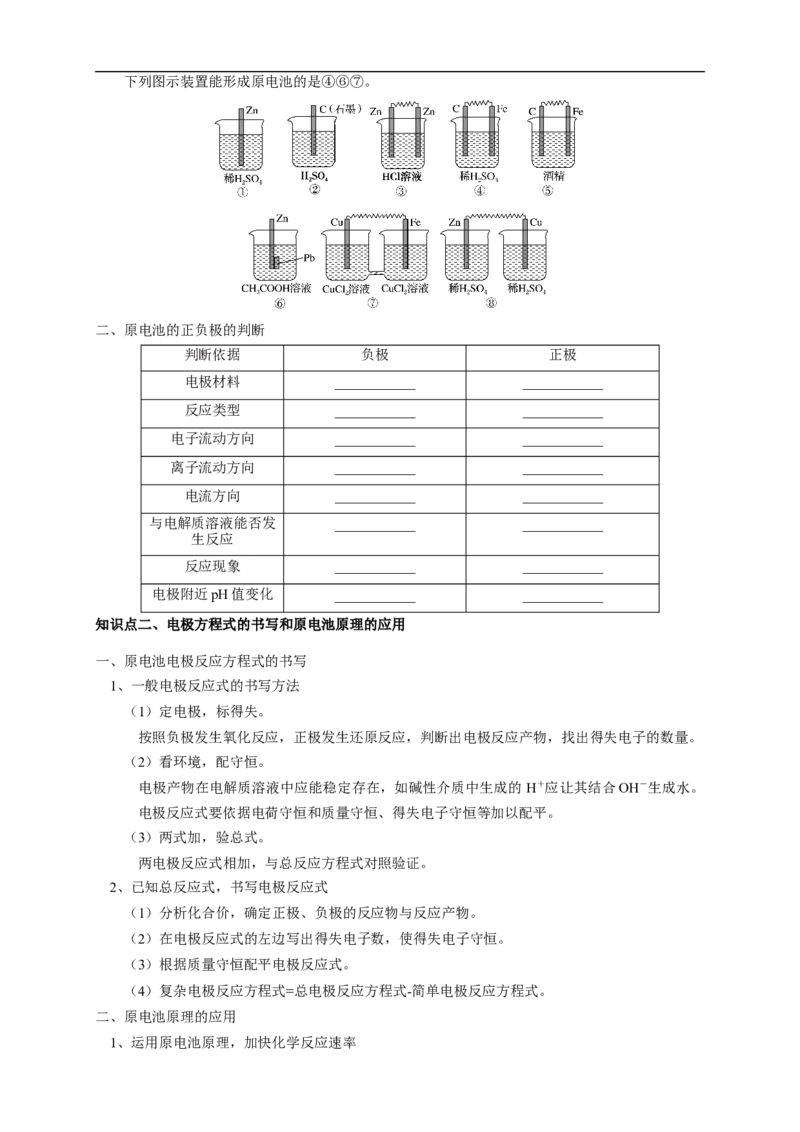
地发生氧化还原反应。下列图示装置能形成原电池的是④⑥⑦。
二、原电池的正负极的判断
判断依据 负极 正极
电极材料 __________ __________
反应类型 __________ __________
电子流动方向 __________ __________
离子流动方向 __________ __________
电流方向 __________ __________
与电解质溶液能否发 __________ __________
生反应
反应现象 __________ __________
电极附近pH值变化 __________ __________
知识点二、电极方程式的书写和原电池原理的应用
一、原电池电极反应方程式的书写
1、一般电极反应式的书写方法
(1)定电极,标得失。
按照负极发生氧化反应,正极发生还原反应,判断出电极反应产物,找出得失电子的数量。
(2)看环境,配守恒。
电极产物在电解质溶液中应能稳定存在,如碱性介质中生成的 H+应让其结合OH-生成水。
电极反应式要依据电荷守恒和质量守恒、得失电子守恒等加以配平。
(3)两式加,验总式。
两电极反应式相加,与总反应方程式对照验证。
2、已知总反应式,书写电极反应式
(1)分析化合价,确定正极、负极的反应物与反应产物。
(2)在电极反应式的左边写出得失电子数,使得失电子守恒。
(3)根据质量守恒配平电极反应式。
(4)复杂电极反应方程式=总电极反应方程式-简单电极反应方程式。
二、原电池原理的应用
1、运用原电池原理,加快化学反应速率如:实验室中用Zn与稀HSO 反应制取H 时,通常滴入几滴CuSO 溶液。这样做的原因是Zn
2 4 2 4
与置换出的Cu、稀HSO 构成Zn与置换出的Cu、稀HSO 构成了原电池,加快了反应的进行。
2 4 2 4
2、运用原电池原理,设计制造各种化学电源
3、运用原电池原理,对金属实行有效保护
例:为保护轮船船体或大坝闸门的过快腐蚀,通常在船体或闸门外壳上连接一块比船体或闸门
更活泼的金属,以保护船体或闸门。
4、运用原电池原理,判断金属的活动性大小
作为原电池负极的金属,金属活动性一般比作为正极的金属活动性强。
5、运用原电池原理,判断氧化还原进行的方向
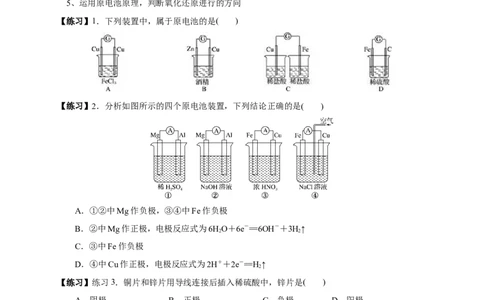
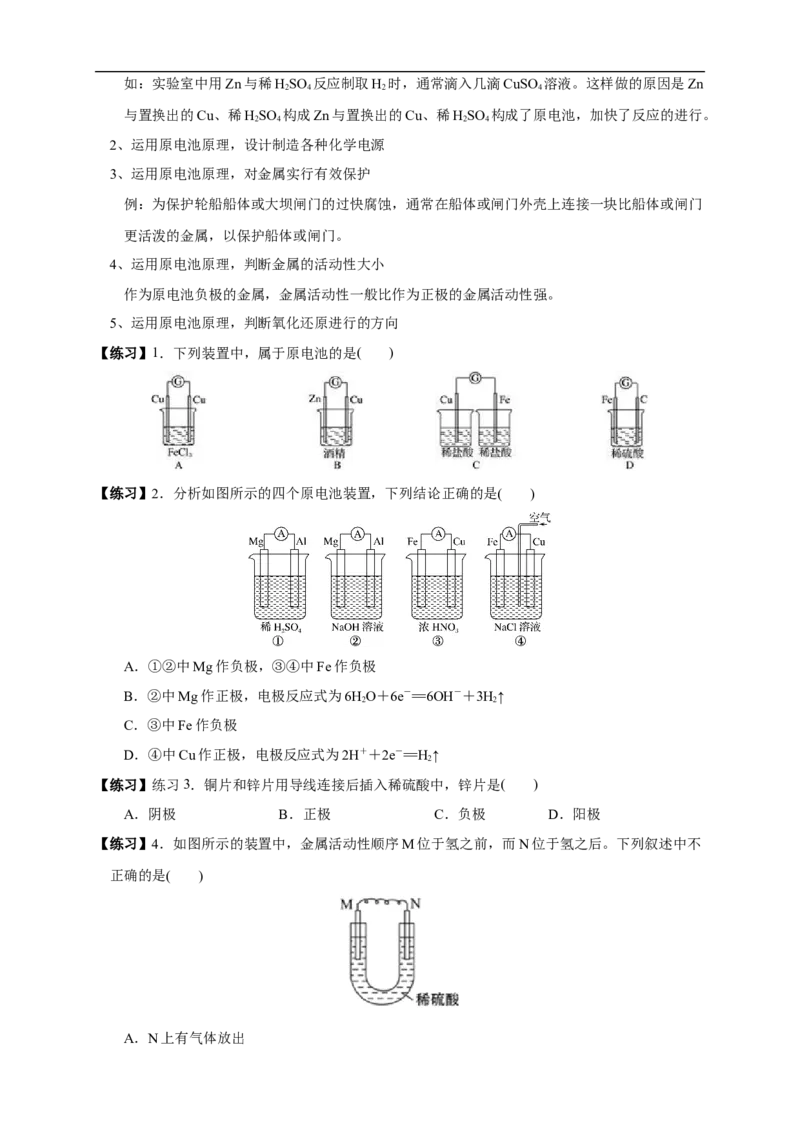
【练习】1.下列装置中,属于原电池的是( )
【练习】2.分析如图所示的四个原电池装置,下列结论正确的是( )
A.①②中Mg作负极,③④中Fe作负极
B.②中Mg作正极,电极反应式为6HO+6e-==6OH-+3H↑
2 2
C.③中Fe作负极
D.④中Cu作正极,电极反应式为2H++2e-==H↑
2
【练习】练习3.铜片和锌片用导线连接后插入稀硫酸中,锌片是( )
A.阴极 B.正极 C.负极 D.阳极
【练习】4.如图所示的装置中,金属活动性顺序M位于氢之前,而N位于氢之后。下列叙述中不
正确的是( )
A.N上有气体放出B.M为负极,N为正极
C.是化学能转变为电能的装置
D.导线中有电流通过,电流方向是由M到N
【练习】5.如图所示,两电极一为碳棒,一为铁片,若电流表的指针发生偏转,且a极上有大量
气泡生成,则以下叙述正确的是( )
A.a为负极,是铁片,烧杯中的溶液为硫酸
B.b为负极,是铁片,烧杯中的溶液为硫酸铜溶液
C.a为正极,是碳棒,烧杯中的溶液为硫酸
D.b为正极,是碳棒,烧杯中的溶液为硫酸铜溶液
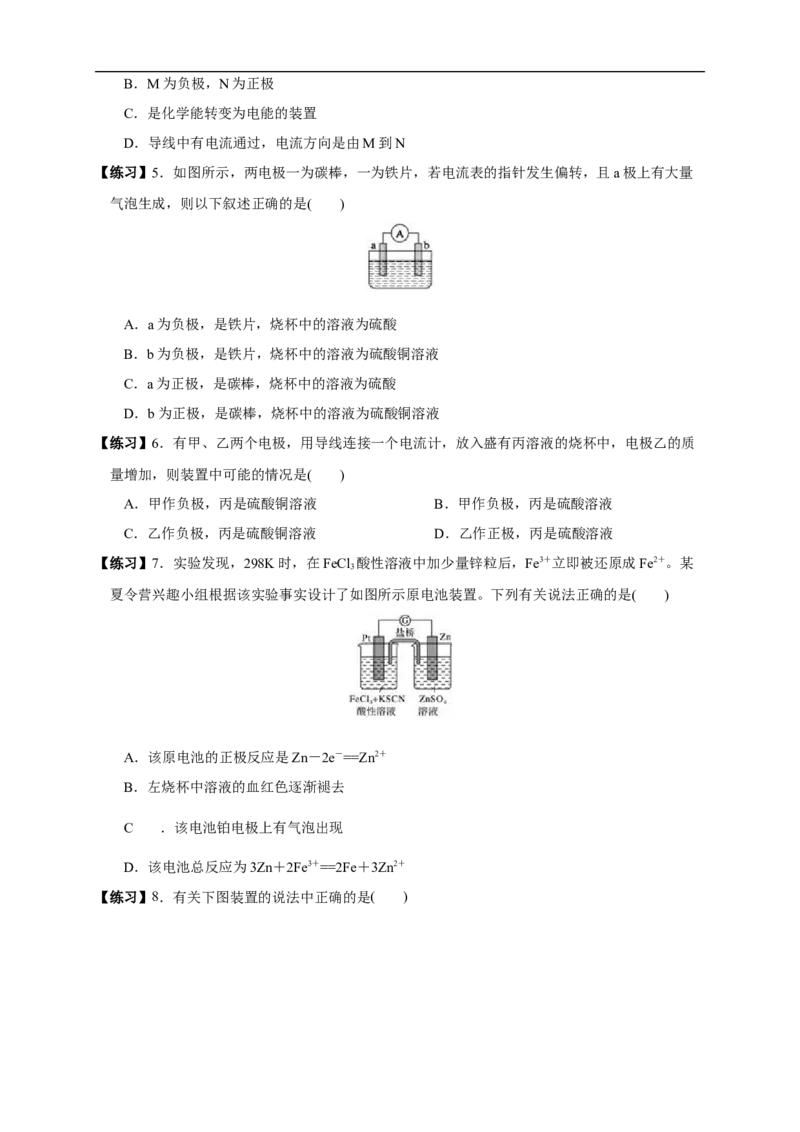
【练习】6.有甲、乙两个电极,用导线连接一个电流计,放入盛有丙溶液的烧杯中,电极乙的质
量增加,则装置中可能的情况是( )
A.甲作负极,丙是硫酸铜溶液 B.甲作负极,丙是硫酸溶液
C.乙作负极,丙是硫酸铜溶液 D.乙作正极,丙是硫酸溶液
【练习】7.实验发现,298K时,在FeCl 酸性溶液中加少量锌粒后,Fe3+立即被还原成Fe2+。某
3
夏令营兴趣小组根据该实验事实设计了如图所示原电池装置。下列有关说法正确的是( )
A.该原电池的正极反应是Zn-2e-==Zn2+
B.左烧杯中溶液的血红色逐渐褪去
C .该电池铂电极上有气泡出现
D.该电池总反应为3Zn+2Fe3+==2Fe+3Zn2+
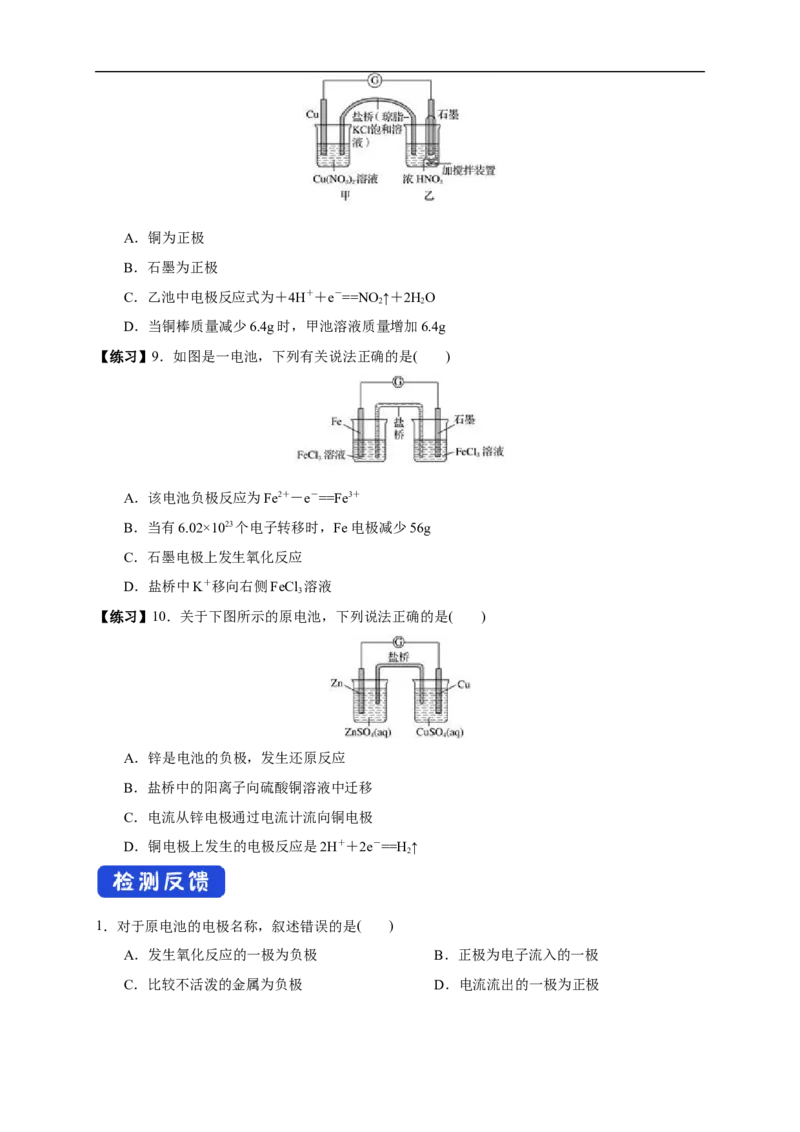
【练习】8.有关下图装置的说法中正确的是( )A.铜为正极
B.石墨为正极
C.乙池中电极反应式为+4H++e-==NO ↑+2HO
2 2
D.当铜棒质量减少6.4g时,甲池溶液质量增加6.4g
【练习】9.如图是一电池,下列有关说法正确的是( )
A.该电池负极反应为Fe2+-e-==Fe3+
B.当有6.02×1023个电子转移时,Fe电极减少56g
C.石墨电极上发生氧化反应
D.盐桥中K+移向右侧FeCl 溶液
3
【练习】10.关于下图所示的原电池,下列说法正确的是( )
A.锌是电池的负极,发生还原反应
B.盐桥中的阳离子向硫酸铜溶液中迁移
C.电流从锌电极通过电流计流向铜电极
D.铜电极上发生的电极反应是2H++2e-==H ↑
2
1.对于原电池的电极名称,叙述错误的是( )
A.发生氧化反应的一极为负极 B.正极为电子流入的一极
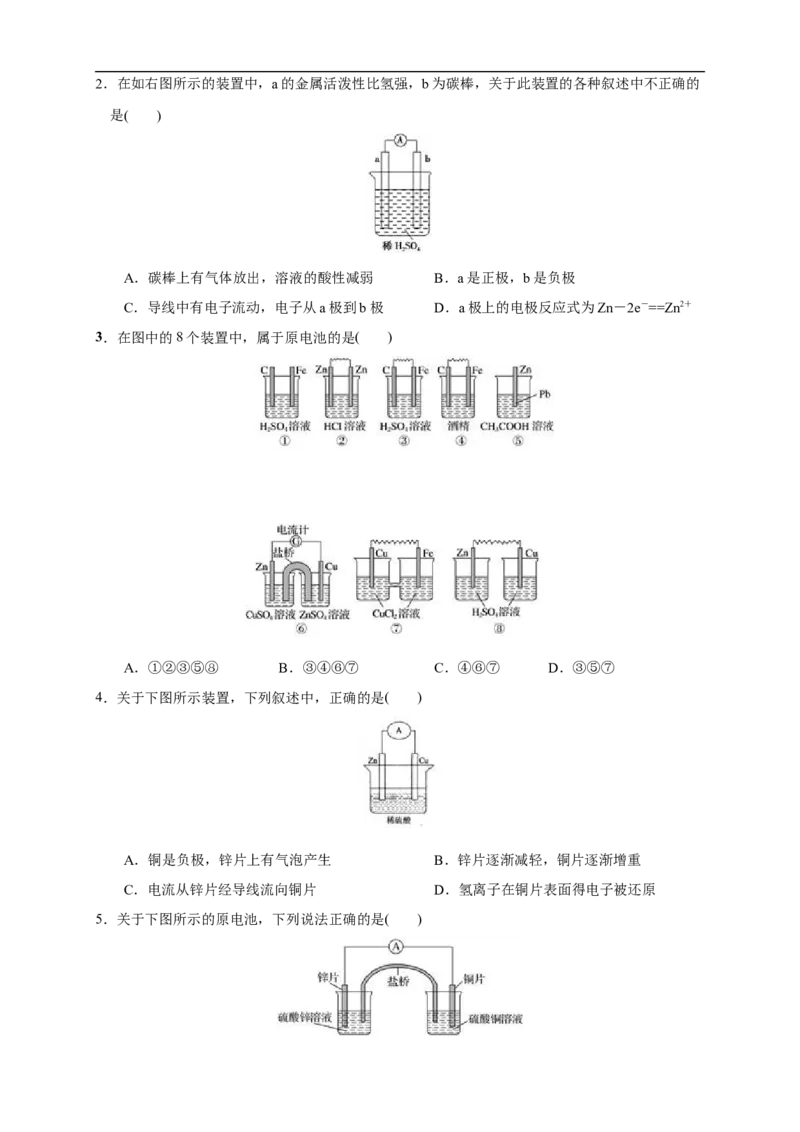
C.比较不活泼的金属为负极 D.电流流出的一极为正极2.在如右图所示的装置中,a的金属活泼性比氢强,b为碳棒,关于此装置的各种叙述中不正确的
是( )
A.碳棒上有气体放出,溶液的酸性减弱 B.a是正极,b是负极
C.导线中有电子流动,电子从a极到b极 D.a极上的电极反应式为Zn-2e-==Zn2+
3.在图中的8个装置中,属于原电池的是( )
A.①②③⑤⑧ B.③④⑥⑦ C.④⑥⑦ D.③⑤⑦
4.关于下图所示装置,下列叙述中,正确的是( )
A.铜是负极,锌片上有气泡产生 B.锌片逐渐减轻,铜片逐渐增重
C.电流从锌片经导线流向铜片 D.氢离子在铜片表面得电子被还原
5.关于下图所示的原电池,下列说法正确的是( )A.电子从锌电极通过电流表流向铜电极
B.盐桥中的阴离子向硫酸铜溶液中迁移
C.锌电极发生氧化反应;铜电极发生还原反应,其电极反应是2H++2e-==H ↑
2
D.取出盐桥后,电流表仍会偏转,铜电极在反应前后质量不变
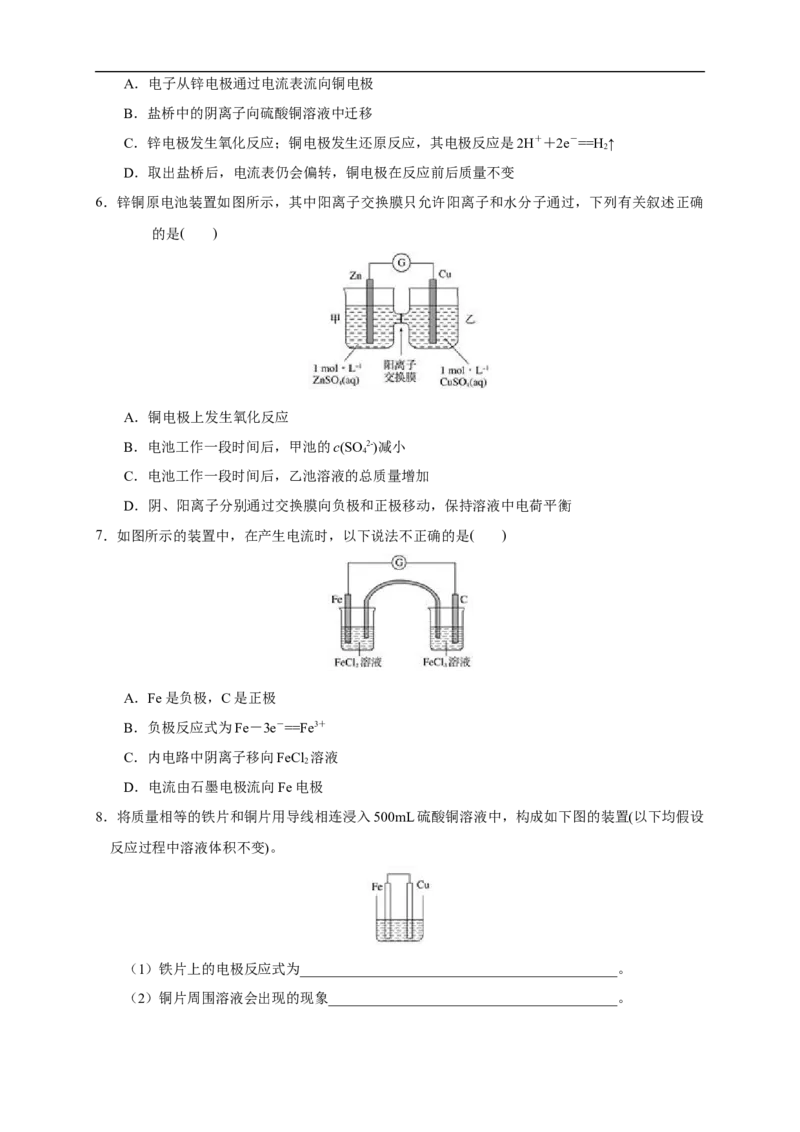
6.锌铜原电池装置如图所示,其中阳离子交换膜只允许阳离子和水分子通过,下列有关叙述正确
的是( )
A.铜电极上发生氧化反应
B.电池工作一段时间后,甲池的c(SO 2-)减小
4
C.电池工作一段时间后,乙池溶液的总质量增加
D.阴、阳离子分别通过交换膜向负极和正极移动,保持溶液中电荷平衡
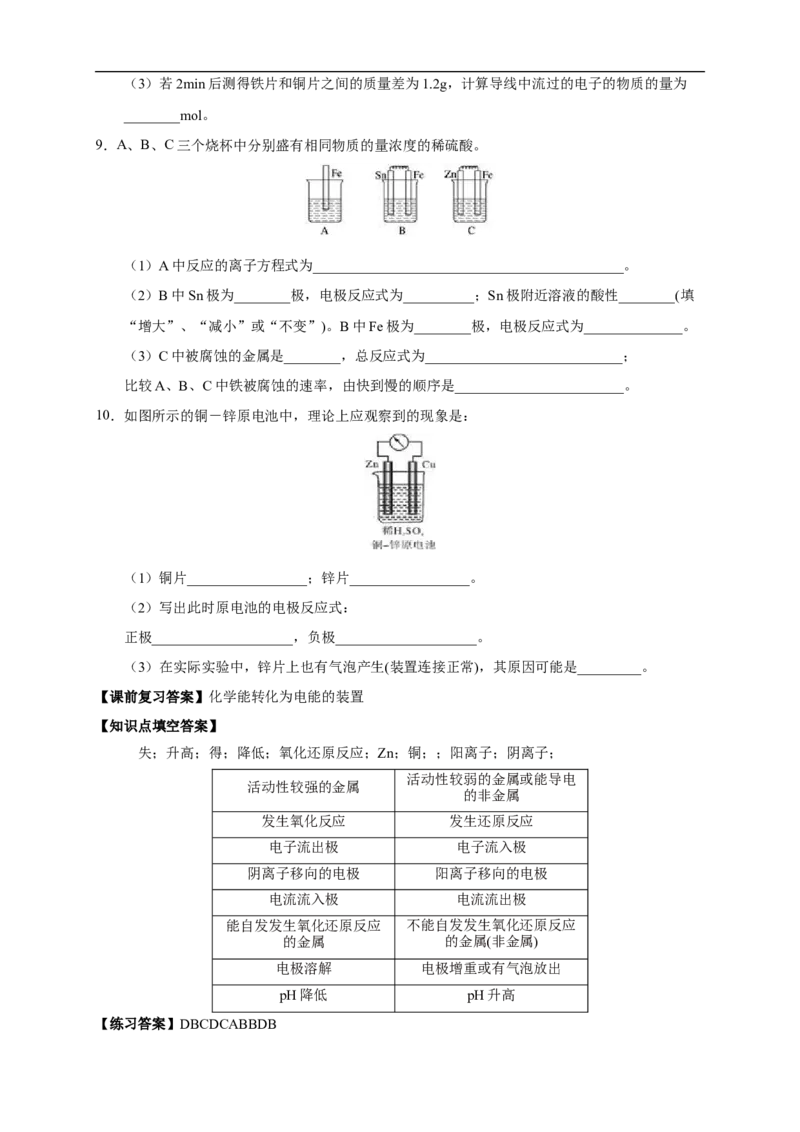
7.如图所示的装置中,在产生电流时,以下说法不正确的是( )
A.Fe是负极,C是正极
B.负极反应式为Fe-3e-==Fe3+
C.内电路中阴离子移向FeCl 溶液
2
D.电流由石墨电极流向Fe电极
8.将质量相等的铁片和铜片用导线相连浸入500mL硫酸铜溶液中,构成如下图的装置(以下均假设
反应过程中溶液体积不变)。
(1)铁片上的电极反应式为_____________________________________________。
(2)铜片周围溶液会出现的现象_________________________________________。(3)若2min后测得铁片和铜片之间的质量差为1.2g,计算导线中流过的电子的物质的量为
________mol。
9.A、B、C三个烧杯中分别盛有相同物质的量浓度的稀硫酸。
(1)A中反应的离子方程式为____________________________________________。
(2)B中Sn极为________极,电极反应式为__________;Sn极附近溶液的酸性________(填
“增大”、“减小”或“不变”)。B中Fe极为________极,电极反应式为______________。
(3)C中被腐蚀的金属是________,总反应式为____________________________;
比较A、B、C中铁被腐蚀的速率,由快到慢的顺序是________________________。
10.如图所示的铜-锌原电池中,理论上应观察到的现象是:
(1)铜片_________________;锌片_________________。
(2)写出此时原电池的电极反应式:
正极____________________,负极____________________。
(3)在实际实验中,锌片上也有气泡产生(装置连接正常),其原因可能是_________。
【课前复习答案】化学能转化为电能的装置
【知识点填空答案】
失;升高;得;降低;氧化还原反应;Zn;铜;;阳离子;阴离子;
活动性较弱的金属或能导电
活动性较强的金属
的非金属
发生氧化反应 发生还原反应
电子流出极 电子流入极
阴离子移向的电极 阳离子移向的电极
电流流入极 电流流出极
能自发发生氧化还原反应 不能自发发生氧化还原反应
的金属 的金属(非金属)
电极溶解 电极增重或有气泡放出
pH降低 pH升高
【练习答案】DBCDCABBDB【检测反馈答案】CBDDACB
8【答案】(1)Fe-2e-==Fe2+(2)溶液颜色变浅(3)0.02
9【答案】(1)Fe+2H+==Fe2++H↑(2)正;2H++2e-==H ↑;减小;负;Fe-2e-==Fe2+;
2 2
(3)Zn;Zn+HSO ==ZnSO +H↑;B、A、C。
2 4 4 2
10【答案】(1)有无色气泡产生;逐渐溶解
(2)2H++2e-==H ↑;Zn-2e-==Zn2+
2
(3)锌片含有杂质,杂质与锌形成原电池产生气泡