文档内容
4.1.1 原子结构与元素周期表
【题组一 原子结构】
1.(2020·全国课时练习)下列叙述错误的是( )
A.13C和14C属于同种元素,它们互为同位素
B.1H和2H是不同的核素,它们的质子数相等
C.14C和14N的质量数相等,它们的中子数不等
D.6Li和7Li的电子数相等,中子数也相等
【答案】D
【解析】A.13C和14C属于同种元素,由于二者质子数相同,而中子数不同,所以它们互为同位素,故A正
确;
B.1H和2H是不同的核素,由于它们都属于氢元素,所以它们的质子数相等,故B正确;
C.14C和14N的质量数相等,由于二者的质子数不同,因此它们的中子数不等,故C正确;
D.6Li和7Li的质子数相等,它们的电子数也相等,但是中子数不同,故D错误。
故选D。
2.(2019·上海市复兴高级中学月考)关于 原子说法正确的是
A.中子数等于质子数 B.质子数等于电子数
C.质子数等于质量数 D.电子数等于中子数
【答案】B
【解析】A. 的中子数=14-6=8,而质子数=6,两者不相等,A错误;
B. 的质子数=电子数=6,两者相等,B正确;
C. 的质量数=14,与其质子数不相等,C错误;
D. 的中子数=14-6=8,而电子数=质子数=6,两者不相等,D错误;
答案选B。
3(2020·黑龙江省海林林业局第一中学高一月考)已知某元素的原子序数,则不能推出该元素原子的
( )
A.质子数 B.中子数 C.电子数 D.核电荷数
【答案】B
【解析】在原子中:原子序数=质子数=电子数=核电核数。质量数=质子数+中子数,因没有质量数,故无法推出中子数。故选B。
4.(2020·全国课时练习)已知某元素的原子核外最外层电子数=最内层电子数=电子层数,则该元素是(
)
A.氦 B.锂 C.铍 D.镁
【答案】C
【解析】由元素的原子核外最外层电子数=最内层电子数=电子层数可知,该元素有两个电子层,最外层电
子数为2,内层电子数也为2,核电荷数为4,则该元素是铍元素,故选C。
5.(2020·全国高一课时练习)下列关于核外电子排布的说法中不正确的是( )
A.第二电子层最多可容纳的电子数为8
B.次外层最多可容纳的电子数为18
C.最多可容纳2个电子的电子层一定是第一电子层
D.最多可容纳8个电子的电子层一定是第二电子层
【答案】D
【解析】A.根据2n2原则,第二电子层最多可容纳8个电子,A正确;
B.最外层最多可容纳8个电子,次外层最多可容纳18个电子,B正确;
C.根据2n2原则,最多可容纳2个电子的电子层一定是第一电子层,C正确;
D.最多可容纳8个电子的电子层不一定是第二电子层,当第三电子层为最外层时,最多只可容纳8个电
子,D错误;故选D。
6.(2020·古浪县第二中学高一期中)下列有关原子核外电子的说法错误的是( )
A.在含有多个电子的原子里,电子分别在能量不同的区域内运动
B.电子总是尽可能地先从内层排起,当一层充满后再填充下一层
C.每个电子层作为最外层时,最多可容纳8个电子
D.离原子核近的电子能量低,离原子核远的电子能量高
【答案】C
【解析】A.原子含有多个电子,电子从内层排起,当一层充满后再填充下一层,电子分别在能量不同的
区域内运动,A正确;
B.电子总是从内层排起,当一层充满后再填充下一层,B正确;
C.第一个电子层作为最外层时,最多可容纳2个电子,如氦原子,故C错误;
D.原子核外的电子遵循能量最低原理排布,从第一层依次往外填充,离原子核近的电子能量低,离原子
核远的电子能量高,D正确;答案选C。
7.(2020·宁县第二中学)Na和Na+两种微粒中,不相同的是( )①核内质子数②核外电子数③最外层电子数④核外电子层数
A.①② B.②③ C.③④ D.②③④
【答案】D
【解析】Na和Na+两种微粒中,含有相同的质子数、中子数;核外电子总数、最外层电子数及层数不同,
答案为D
8.(2020·农安县万顺乡中学高一开学考试)化学的学科特征是在原子、分子水平上研究物质和创造物质。
请从微观的角度回答下列问题。
(1)物质的结构决定性质。
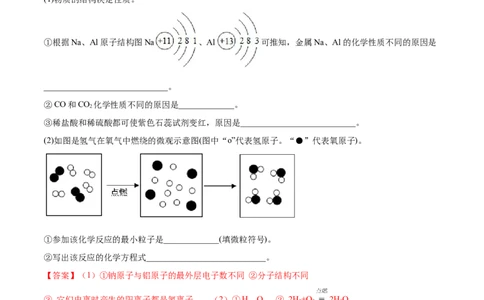
①根据Na、Al原子结构图Na 、Al 可推知,金属Na、Al的化学性质不同的原因是
_____________________________。
②CO和CO 化学性质不同的原因是_____________。
2
③稀盐酸和稀硫酸都可使紫色石蕊试剂变红,原因是___________________________。
(2)如图是氢气在氧气中燃绕的微观示意图(图中“o”代表氢原子。“●”代表氧原子)。
①参加该化学反应的最小粒子是_____________(填微粒符号)。
②写出该反应的化学方程式____________________________。
【答案】(1)①钠原子与铝原子的最外层电子数不同 ②分子结构不同
③ 它们电离时产生的阳离子都是氢离子 (2)①H、O ② 2H+O 2HO
2 2 2
【解析】(1)①在原子中,最外层电子数决定了元素的化学性质,由原子结构示意图可知,钠元素与铝原子
的最外层电子数不同,所以金属Na、Al的化学性质不同;故填:钠原子与铝原子的最外层电子数不同;
②分子是保持物质化学性质的最小粒子,一氧化碳分子与二氧化碳分子结构不同,所以二者的化学性质不
同;故填:分子结构不同;
③硫酸和盐酸都能使紫色石蕊试液变红,是因为它们电离时产生的阳离子都是氢离子;故填:它们电离时
产生的阳离子都是氢离子;(2)①由微观反应示意图可知,参加该化学反应的最小粒子是氢原子和氧原子;故填:H、O;
②由微观反应示意图可知,氢气与氧气在点燃的条件下反应生成水;故填:2H+O 2HO。
2 2 2
9.(2020·全国高一课时练习)根据下列叙述,写出微粒符号。
(1)原子核外有2个电子层,核外有10个电子的原子___________;
(2)原子核内没有中子,核外没有电子的微粒__________;
(3)质量数为24,质子数等于中子数的离子____________________;
(4)由两个原子组成的具有10个电子的分子是________;
(5)由两个原子组成的具有10个电子的阴离子是________;
(6)由三个原子组成的具有10个电子的分子是________。
【答案】(1)Ne (2) 1 H+ (3) Mg2+ (4) HF (5) OH- (6) HO
1 2
【解析】(1)原子核外有2个电子层,核外有10个电子的原子,其质子数为10,所以该原子是Ne;
(2)原子核内没有中子的原子只有氢原子,所以核外没有电子的微粒是 1 H+;
1
(3)质量数为24,质子数等于中子数的原子,可以求出其质子数为12,所以该离子是Mg2+;
(4)由两个原子组成的具有10个电子的分子是HF;
(5)由两个原子组成的具有10个电子的阴离子是OH-;
(6)由三个原子组成的具有10个电子的分子是HO。
2
【题组二 元素周期表】
1.(2020·全国课时练习)在元素周期表中横行的编排依据是( )
A.按元素的相对原子质量递增顺序从左到右排列
B.按元素的原子核外电子层数依次递增顺序从左到右排列
C.电子层相同的元素,按原子序数依次递增顺序从左到右排列
D.按元素的原子最外层电子数依次递增顺序从左到右排列
【答案】C
【解析】周期表按照原子序数的递增及原子结构的周期性变化排列,将电子层数相同的元素放在同一横行
中,然后按原子序数递增顺序排列,所以元素周期表中横行的编排依据是电子层相同的元素,按原子序数
依次递增顺序从左到右排列,故合理选项是D。
3.(2020·全国课时练习)下列各组元素中,属于同一周期的是
A.Na、P B.N、Cl C.F、Mg D.O、S
【答案】A
【解析】A. Na、P的原子结构中均有3个电子层,均位于第三周期,故A 选;B. N、Cl分别在第二周期、第三周期,故B不选;
C. F、Mg分别在第二周期、第三周期,故C不选;
D. O、S分别在第二周期、第三周期,故D不选;
故选A。
4.(2020·全国课时练习)甲、乙是元素周期表中同一主族的两种元素,若甲的原子序数为x,则乙的原
子序数不可能是 ( )
A.x+2 B.x+4 C.x+8 D.x+18
【答案】B
【解析】第一周期共有2种元素,第二、三周期各共有8种元素,第四、五周期各共有18种元素,第六、
七周期各共有32种元素,因此,相邻主族元素之间原子序数相差可能为2、8、18、32,B选项为4错误,
故选B
5.(2020·全国课时练习)下列各表中的数字代表的是元素的原子序数。表中数字所对应的元素与他们在
周期表中的位置相符的是
A. B. C. D.
【答案】D
【解析】A. 1号元素正下方应为3号元素,1号和2号元素相隔16列,A项错误;
B. 10号元素在周期表中第18列(即最后一列),B项错误;
C. 13号元素正上方应为13-8=5号元素,正下方应为13+18=31号元素,C项错误;
D. 符合元素周期表中的位置关系,D项正确;
答案选D。
6.(2020·全国课时练习)无机化学命名委员会(国际组织)在1989年作出决定:把周期表原先的主、副
族取消,从左向右按原顺序编为18列,如第ⅠA族为第1列,稀有气体为第18列。按这个规定,下列说
法正确的是( )
A.每一列都有非金属元素
B.第18列元素的原子最外层均有8个电子
C.在18列元素中,第3列所含元素种类最多
D.只有第2列元素的原子最外层有2个电子【答案】C
【解析】A.只有元素周期表的第2列到第12列都是金属元素,A错误;
B.第18列元素即稀有气体元素,其中氦原子最外层是2个电子,B错误;
C.第3列包含了镧系和锕系元素,所以该列元素的种类最多,C正确;
D.除第2列元素外,稀有气体元素He及过渡元素中的大多数元素原子的最外层电子数也是2,D错误;
故答案为:C。
7.(2020·全国课时练习)下列有关元素周期表的叙述错误的是( )
①元素周期表有18列,所以有18个族
②最外层电子数为2的元素都位于IIA族
③除0族外,短周期元素的最高正化合价的数值等于该元素的主族序数
④除短周期外,其他周期均有18种元素
⑤碱金属元素是指IA族的所有元素
⑥过渡元素没有非金属元素
A.①②③④⑤ B.②③④⑤⑥ C.①③④⑤ D.①②③⑥
【答案】A
【解析】①元素周期表中第8、9、10列为VIII族,共有16个族,①错误;
②He的最外层电子数为2,却属于0族,②错误;
③O没有最高正价,F无正价,③错误;
④第6、7周期均有32种元素,④错误;
⑤碱金属是指除H外的IA族元素,⑤错误;
⑥过渡元素是周期表中IIIB~IIB族的元素,全部是金属元素,⑥正确;
综上所诉,①②③④⑤错误,答案为A。
【题组三 核素】
1.(2020·马尾·福建师大二附中期末)下列各组微粒中,互为同位素的是( )
A. B. C.1HO 3HO D.O O
2 2 2 3
【答案】B
【解析】A. 两种元素原子的质子数不同,不是同位素,故A错误;
B. 与 质子数均为1,中子数分别为1和2,符合同位素的含义,故B正确;
C. 1HO与3HO属于分子,不是元素原子,故C错误;
2 2D. O 与O 属于同种元素组成的不同单质,属于同素异形体,故D错误;
2 3
答案选B。
2.(2020·全国课时练习)下列说法正确的是( )
A.氧气和臭氧互为同素异形体,它们的互相转化属于物理变化
B. 、 、 与 、 可组成6种不同的水分子
C. 、 和 互为同素异形体
D. 和 互为同位素
【答案】D
【解析】A. 同素异形体是由同种元素形成的不同单质,不同物质之间的转化属于化学变化,A项错误;
B. 可能组成的水分子: 、 、 、 、 、 、 、
、 、 、 、 ,共12种,B项错误;
C. 、 和 均为氢气,C项错误;
D. 和 质子数相同中子数不同,互为同位素,D正确;
答案选D。
3.(2020·全国课时练习)“玉兔”号月球车用 作为热源材料,下列关于 的说法正确的是(
)
A. 与 互为同位素 B. 与 互为同素异形体
C. 与 具有完全相同的化学性质 D. 与 具有相同的最外层电子
【答案】D
【解析】A.两者是不同元素,仅相对原子质量相等,A错误;B. 两者互为同位素,B错误;C. 两种微粒
不是同种元素,核外电子排布不同,化学性质不同,C错误;D. 两者质子数相同,所以具有相同的最外层
电子,D正确。故选择D。
4.(2020·全国课时练习)下列说法正确的是( )A. 和 互为同位素
B. 和 是具有相同质子数的不同核素
C. 与 互为同素异形体
D. 与 具有相同的最外层电子数
【答案】D
【解析】A.同位素的研究对象为原子,而 和 为单质,A错误;
B. 和 均为单质,不是核素,B错误;
C. 与 为Pu的两种不同核素,互为同位素,它们不是单质不互为同素异形体,C错误;
D. 与 的质子数相同,具有相同的最外层电子数,D正确;
答案为D。
5.(2020·防城港市防城中学期中)下列各组中属于同位素的是
A.40K与40Ca B.35Cl 和37Cl C.D与T D.金刚石与石墨
2 2
【答案】C
【解析】A.40K与40Ca是两种不同的元素,质子数不同,不能互为同位素,A错误;
B.35Cl 和37Cl 均是单质分子,不能互为同位素,B错误;
2 2
C.D与T质子数相同而中子数不同,二者互为同位素,C正确;
D.金刚石与石墨是碳元素形成的两种不同单质,互为同素异形体,错误;
答案选C。
6.(2020·东莞高级中学期中)下列有关 Tl和 Tl的说法中,不正确的是( )
A. Tl和 Tl质子数相同 B. Tl和 Tl互为同素异形体
C. Tl和 Tl互为同位素 D. Tl和 Tl是两种核素
【答案】B
【解析】 Tl和 Tl质子数相同,中子数不同,是Tl元素的两种核素,二者互为同位素。A、C、D正确,B不正确,答案选B。