文档内容
第四章 物质结构 元素周期律
第一节 原子结构与元素周期表 课时作业
第一课时 原子结构 核外电子排布
基础达标
1.随着自然科学的发展,科学家们依据实验事实,提出了各种假说和原子结构模型,
其中提出“带核原子结构模型”的科学家是( )
A.汤姆生 B.波尔
C.卢瑟福 D.道尔顿
2.以下有关原子结构的说法中,正确的是( )
A.原子核都是由质子和中子构成的
B.原子次外层电子数不一定都是8
C.原子最外层电子数一般不超过4
D.稀有气体元素原子最外层电子数都是8
3.下列有关原子核外电子的说法错误的是( )
A.每个电子层作为最外层时,最多可容纳8个电子
B.电子在核外是分层排布的
C.电子不停地做高速运动
D.离原子核近的电子能量低,离原子核远的电子能量高
4.在离子 Rn- 中,共有x个核外电子,R原子的质量数为 A,则R原子核内含有的
中子数目是( )
A.A–x+n B.A–x
C.A–x-n D.A+x-n
5.下列说法中正确的是( )
A.某单核微粒的核外电子排布为 ,则该微粒一定是氩原子
B.最外层只有3个电子的元素一定是金属元素
C. 与HO+具有相同的质子数和电子数
3
D.最外层电子数是次外层电子数2倍的元素的原子容易失去电子成为阳离子
6.中核集团原子能科学研究院团队对嫦娥五号带回的月球土壤样品进行分析研究,精确测定了40多种化学元素的含量,其中每吨月壤样品中钛的含量是地球土壤含量的六倍
多。如图是钛元素的相关信息,下列说法正确的是( )
A.钛属于非金属元素 B.钛离子的质子数为22
C.钛离子核外有22个电子 D.钛原子和钛离子属于不同的元素
7.35S是硫的一种放射性核素,可用作蛋白质代谢研究的示踪剂,还可以协助治疗软骨
肉瘤等。下列有关35S的说法正确的是( )
A.K层和M层电子数之和是核内质子数的 B.核外电子数为19
C.中子数为35,质量数为51 D.35S与35Cl互为同位素
8.下图为多电子原子的电子层模型示意图。有关描述不正确的是( )
A.K层电子的能量高于L层 B.核外电子从K层开始填充
C.L层最多能容纳8个电子 D.原子由原子核与核外电子构成
9.下列关于核外电子排布的说法中不正确的是( )
A.第二电子层最多可容纳的电子数为8
B.次外层最多可容纳的电子数为18
C.最多可容纳2个电子的电子层一定是第一电子层
D.最多可容纳8个电子的电子层一定是第二电子层
10.核电荷数为1~18的元素中,下列说法不正确的是( )
A.最外层只有1个电子的元素不一定是金属元素
B.最外层有2个电子的元素不一定是金属元素
C.原子核外各层电子数相等的元素一定是金属元素
D.最外层电子数为7的原子,最高正价为+7
能力提升11.某元素的一种同位素X的原子质量数为A,含N个中子,它与1H原子组成H X
m
分子。在ag H X中所含质子的物质的量是( )
m
A. (A—N) mol B. mol
C. (A—N+m) mol D. (A—N+m) mol
12.不列说法不正确的是( )
A.原子结构模型的演变为:希腊哲学家提出原子概念→道尔顿原子学说→汤姆生葡
萄干面包式→卢瑟福带核原子模型→玻尔原子轨道理论→量子力学
B.质量数是将原子核内所有的质子和中子的相对质量取整数值之和
C.在原子结构分层排布中,第三层(M层)容纳电子数最多为18,最少为8
D.在化学反应过程中,原子核不发生变化,但原子外层电子可能发生变化
13.空间站是一种可以提供多名航天员巡防、长期工作和生活的载人航天器。空间站
补充的一种方式是通过化学反应来生成。电解水可以生成 和 ,其中 可以直接
供人类呼吸使用。 在一定条件下与人类呼出的 反应生成 和 ,然后又可以
电解 产生 。这样就可以形成一个循环的反应链。C和O都属于元素周期表第二周期
元素,他们原子结构中相同的是( )
A.质子数 B.电子层数 C.核外电子数 D.最外层电子数
14.某简单微粒的结构示意图为 ,且x、y均为不大于20的正整数,据此回答
下列问题:
(1)若该微粒一般情况下不与其他元素的原子反应,这种微粒的符号是___________。
(2)若该微粒有很强的氧化性,且只需得到一个电子就能达到稳定结构,这种微粒的结
构示意图为__________________________。
(3)若该微粒为正一价阳离子,且对应的碱为可溶性强碱,则x=_______,y=_______。
(4)当x-y=10时,该粒子为_____________(填“原子”“阳离子”或“阴离子”)。(5)当y=8时,粒子可能为(填粒子符号)______、______、______、______、_______。
直击高考
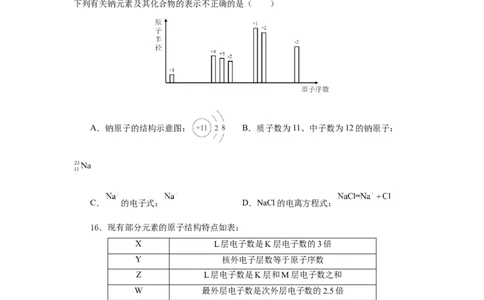
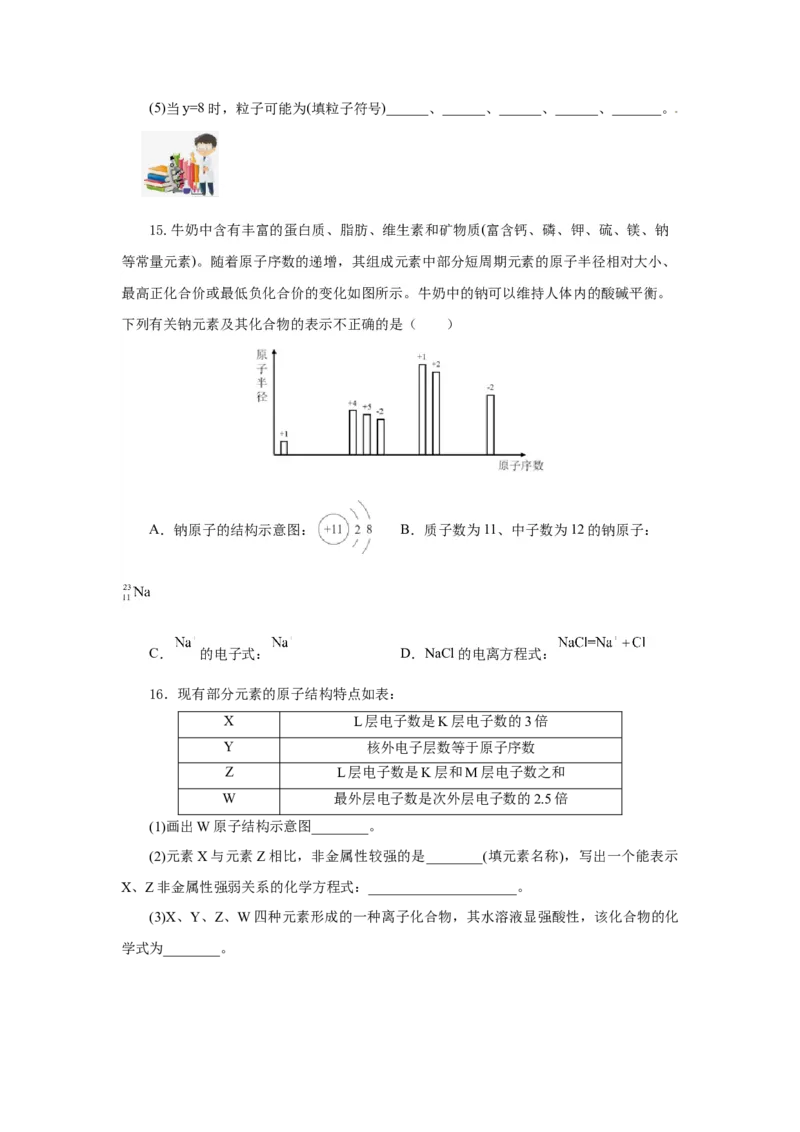
15.牛奶中含有丰富的蛋白质、脂肪、维生素和矿物质(富含钙、磷、钾、硫、镁、钠
等常量元素)。随着原子序数的递增,其组成元素中部分短周期元素的原子半径相对大小、
最高正化合价或最低负化合价的变化如图所示。牛奶中的钠可以维持人体内的酸碱平衡。
下列有关钠元素及其化合物的表示不正确的是( )
A.钠原子的结构示意图: B.质子数为11、中子数为12的钠原子:
C. 的电子式: D.NaCl的电离方程式:
16.现有部分元素的原子结构特点如表:
X L层电子数是K层电子数的3倍
Y 核外电子层数等于原子序数
Z L层电子数是K层和M层电子数之和
W 最外层电子数是次外层电子数的2.5倍
(1)画出W原子结构示意图________。
(2)元素X与元素Z相比,非金属性较强的是________(填元素名称),写出一个能表示
X、Z非金属性强弱关系的化学方程式:_____________________。
(3)X、Y、Z、W四种元素形成的一种离子化合物,其水溶液显强酸性,该化合物的化
学式为________。