文档内容
4.1.1 原子结构与元素周期表
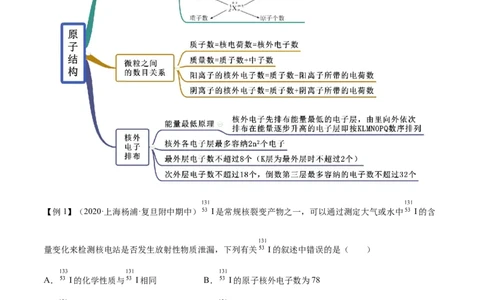
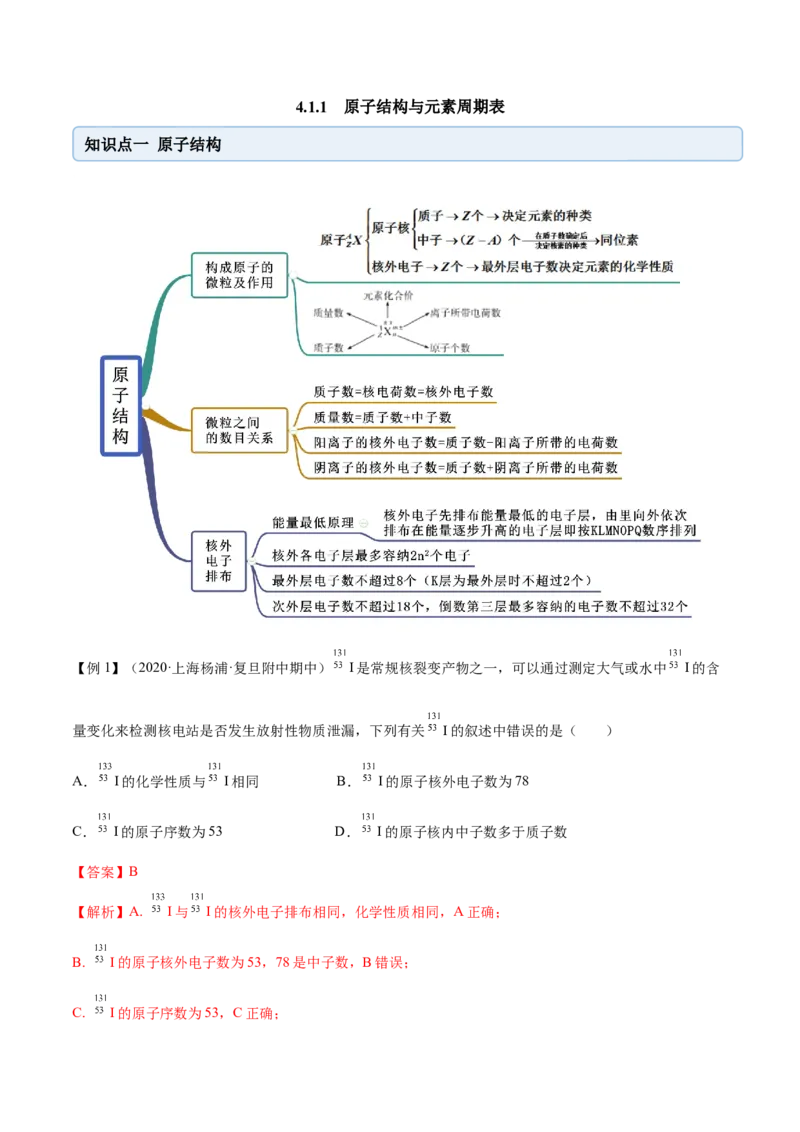
知识点一 原子结构
【例1】(2020·上海杨浦·复旦附中期中) I是常规核裂变产物之一,可以通过测定大气或水中 I的含
量变化来检测核电站是否发生放射性物质泄漏,下列有关 I的叙述中错误的是( )
A. I的化学性质与 I相同 B. I的原子核外电子数为78
C. I的原子序数为53 D. I的原子核内中子数多于质子数
【答案】B
【解析】A. I与 I的核外电子排布相同,化学性质相同,A正确;
B. I的原子核外电子数为53,78是中子数,B错误;
C. I的原子序数为53,C正确;D. I的原子核内中子数是78,质子数是53,中子数大于质子数,D正确;答案选B。
【一隅三反】
1.(2020·邵阳县第二中学月考)铀元素有多种同位素,其中 的质量数是
A.51 B.92 C.143 D.235
【答案】D
【解析】原子符号的左上角为质量数,即 的质量数是235,故D正确。综上所述,答案为D。
2.(2020·全国课时练习)某元素的二价阴离子核外有18个电子,质量数为32,该元素原子的中子数为(
)
A.2 B.14 C.18 D.16
【答案】D
【解析】原子中质子数=核外电子数,质量数=质子数+中子数;二价阴离子核外有18个电子,则该元素的
原子核外有16个电子,原子核内有16个质子,中子数=质量数-质子数 ,故选D。
3.(2020·全国课时练习)下列叙述中不正确的是( )
A.原子的核外M层电子数是L层电子数一半的元素是硅
B.原子的最外层电子数是次外层电子数1.5倍的元素是硼
C.原子的次外层电子数是最外层电子数1/3的元素是氧
D.+1价离子的电子层排布与氖原子相同的元素是氟
【答案】D
【解析】A、元素原子核外M层电子数是L层电子数的一半,说明元素原子有三个电子层,从内到外每一
个电子层上的电子数分别为2、8、4,所以原子序数为14,为硅元素,选项A正确;
B、原子的最外层电子数是次外层电子数1.5倍,说明元素原子有二个电子层,从内到外每一个电子层上的
电子数分别为2、3,所以原子序数为5,为硼元素,选项B正确;
C、原子的次外层电子数是最外层电子数1/3,说明元素原子有二个电子层,从内到外每一个电子层上的电
子数分别为2、6,所以原子序数为8,为氧元素,选项C正确;
D、+1价离子的电子层排布与氖原子相同的元素是钠,选项D不正确。
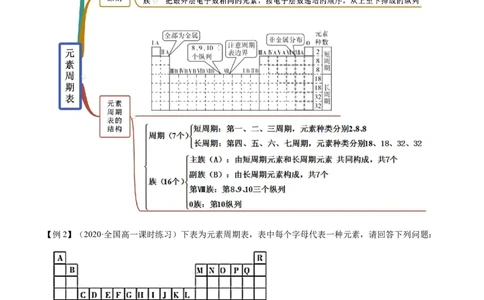
答案选D。知识点二 元素周期表
【例2】(2020·全国高一课时练习)下表为元素周期表,表中每个字母代表一种元素,请回答下列问题:
(1)属于主族元素的有_____________________(填字母)。
(2) 、 分别属于第___________族、第___________族。
(3)属于第Ⅷ族元素的有______________________(填字母)。
(4)第四周期与第三周期数目之差为______________________。【答案】(1) 、 、 、 、 、 、 (2)Ⅰ Ⅱ (3) 、 、 (4)10
【解析】(1)属于主族元素的有 、 、 、 、 、 、 ;
(2) 、 分别位于元素周期表中第Ⅰ 族、第Ⅱ 族;
(3)元素周期表中第8、9、10三个纵列统称为第Ⅷ族,故属于第Ⅷ族元素的有 、 、 ;
(4)第三周期有8种元素,第四周期有18种元素,故第四周期与第三周期所含元素的数目之差为10。
1.奇偶规律
①原子序数是奇数的主族元素,其所在主族序数及主要化合价必为奇数;
②原子序数是偶数的主族元素,其所在主族序数及主要化合价必为偶数。
2.“序、层”规律
①若一种阳离子与一种阴离子电子层数相同,则“阴上阳下”,即阴离子在上一周期,阳离子在下一周期,
【一隅三反】
1.(2020·吉林农安·期末)下列对于元素周期表结构的叙述中,正确的是
A.7个横行代表7个周期,18个纵行代表18个族
B.副族元素中没有非金属元素
C.除第一周期外,其他周期均有18种元素
D.碱金属元素是指ⅠA族的所有元素
【答案】B
【解析】A.7个横行代表7个周期,18个纵行代表16个族,7个主族、7个副族、1个0族、1个ⅤⅢ族,
A错误;
B.副族元素均在长周期,均为金属元素,只有主族元素存在非金属元素,B正确;
C.2、3周期有8种元素,6、7周期有32种元素,则只有4、5周期有18种元素,C错误;
D.碱金属元素为金属元素,而ⅠA族元素含H,碱金属元素是指ⅠA族的除H之外的所有元素,D错误。
答案选B。
2.(2020·全国课时练习)某元素的原子结构示意图为: ,则该元素在元素周期表中的位置是
A.第二周期,第ⅠA族 B.第二周期,第ⅤA族C.第三周期,第ⅣA族 D.第三周期,第ⅤA族
【答案】D
【解析】根据原子结构示意图可知质子数是15个,有3个电子层,最外层电子数是5个,则位于元素周期
表的第三周期第ⅤA族,答案选D。
3.(2020·全国课时练习)下列各图为元素周期表的一部分,则图中所示原子序数与其在元素周期表中的
位置不相符的是( )
A. B.
C. D.
【答案】C
【解析】A.2和10号元素分别为 、 ,属于同一族,并且相邻,8号元素为O,与 相隔第Ⅶ
族的 元素,原子序数与其在周期表中的位置相符,故A正确;
B.2、9、16号元素分别为 、 、 ,分别位于第一周期0族、第二周期Ⅶ 族、第5周期Ⅵ 族,
原子序数与其在周期表中的位置相符,故B正确;
C.7号和33号元素分别为 、 ,属于第Ⅴ 族元素,且相隔一个周期,12号元素为 ,位于第二
周期Ⅱ 族,但第Ⅱ 族与第Ⅴ 族相隔Ⅲ ……Ⅳ 族,故原子序数与其在周期表中的位置不相符,
故C错误;
D.1、4、12号元素分别为 、 、 ,分别位于第一周期Ⅰ 族、第二周期Ⅱ 族、第三周期Ⅱ
族,原子序数与其在周期表中的位置相符,故D正确;
答案选C。
4.(2020·全国课时练习)X、Y、Z是周期表中位置相邻的三种短周期元素,X和Y同周期,Y和Z同主
族,三种元素原子的最外层电子数之和为16,核内质子数之和为30,则X、Y、Z分别是( )
A.O、N、P B.S、P、N C.N、O、S D.Cl、S、O【答案】A
【解析】设X元素的最外层电子数为x,由X和Y同周期,Y和Z同主族可知,Y、Z最外层电子数可能
为x+1或x-1,若Y、Z元素的最外层电子数为x+1,由三种元素原子的最外层电子数之和为16可得关系式:
x+2(x+1)=16,解得x= ,不合题意舍去;若Y、Z元素的最外层电子数为x—1,由三种元素原子的最
外层电子数之和为16可得关系式:x+2(x—1)=16,解得x=6,则X为ⅥA族元素、Y为ⅤA族元素;
设X的原子序数为m,由X和Y同周期,Y和Z同主族可知,Y的原子序数为m—1,Z的原子序数可能
为m+7或m-9,若Z的原子序数为m—9,由核内质子数之和为30可得关系式:m+( m—1)+( m—9)=30,
解得m= ,不合题意舍去;若Z的原子序数为m+7,由核内质子数之和为30可得关系式:m+( m—1)+
( m+7)=30,解得m=8,则X为O元素、Y为N元素、Z为P元素,故选A。
5.(2020·全国课时练习)短周期元素 、 、 、 在元素周期表中的位置如图所示,其中 所处的
周期序数与主族序数相等,请回答下列问题:
(1) 元素的原子结构示意图为__________________; 元素在元素周期表中的位置为____________。
(2)原子序数比 小2的元素是_________(填元素符号),它的单质在氧气中燃烧的化学方程式为
______________________________。
(3)原子序数比 大4的元素是______(填元素符号),该元素最高价氧化物的水化物溶液与 元素
最高价氧化物的水化物溶液反应的离子方程式为______________________________。
【答案】(1) 第二周期ⅣA族
(2)
(3)【解析】(1)T为Al,原子核外有13个电子,原子结构示意图为 ;Q为C,原子核外有2个电子
层,最外层电子数为4,在周期表中的位置是第二周期ⅣA族;
(2)原子序数比Al小2的元素是Na,在氧气中燃烧生成过氧化钠,反应方程式为 ;
(3)原子序数比S大4的元素是Ca,该元素最高价氧化物的水化物是氢氧化钙,S元素最高价氧化物的水化
物是硫酸,氢氧化钙溶液与硫酸溶液发生中和反应生成硫酸钙和水,离子方程式为
。
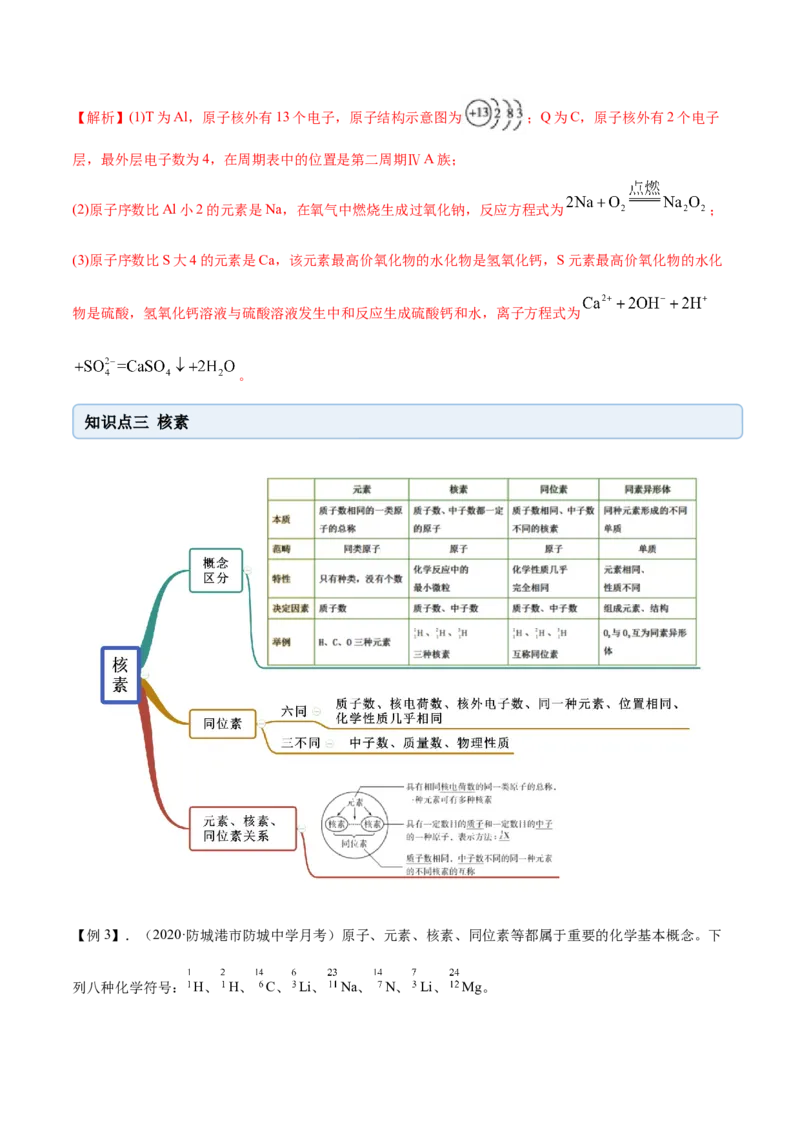
知识点三 核素
【例3】.(2020·防城港市防城中学月考)原子、元素、核素、同位素等都属于重要的化学基本概念。下
列八种化学符号: H、 H、 C、 Li、 Na、 N、 Li、 Mg。(1)涉及的核素共有__种;
(2)互为同位素的是___、___。
(3)质量数相等,但不能互称为同位素的是___;
(4)中子数相等,但质子数不相等的是___。
(5)氢的三种同位素是__。
【答案】(1)8 (2) Li和 Li H和 H (3) 和
(4) Na和 Mg (5) H、 H、 H
【解析】(1)核素是指具有一定数目质子和一定数目中子的一种原子,属于原子的有 H、 H、 C、 Li、
Na、 N、 Li、 Mg,它们都表示核素,即共有8种核素,故答案为:8;
(2)质子数相同而中子数不同的同一元素的不同原子互称同位素,在8种微粒中, Li和 Li质子数都是3,
而中子数分别为3和4,即二者互为同位素, H和 H质子数都是1,而中子数分别为0和1,即二者互为
同位素,故答案为: Li和 Li; H和 H;
(3)在8中微粒中,质量数相等的是 和 ,它们的质子数分别为6和7而不相同,它们不能互称同位
素,故答案为: 和 ;
(4)根据质量数=质子数+中子数得, H、 H、 C、 Li、 Na、 N、 Li、 Mg的中子数分别为0、
1、8、3、12、7、4、12,因此中子数相等,但质子数不相等的是 Na、 Mg,故答案为: Na和
Mg;
(5)氢原子有三种同位素: H、 H、 H,故答案为: H、 H、 H。
【一隅三反】
1.(2020·全国课时练习)在高压下氮气会发生聚合得到高聚氮。后来科学家利用 ,又制出 、 、、 及 含的化合物等。下列说法正确的是( )
A. 、 、 、 都是氮的同位素
B. 是化学变化
C.高聚氮与 、 、 、 、 互为同素异形体
D.NO和 互为同素异形体
【答案】B
【解析】A. 、 、 、 都是氮元素形成的不同种单质,互为同素异形体,故A错误;
B. 转化为 的过程中有新物质生成,属于化学变化,故B正确;
C.同素异形体是同种元素形成的不同种单质的互称, 是阳离子,不是单质,与 、 、 、 互
为同素异形体,故C错误;
D.同素异形体是同种元素形成的不同种单质的互称,NO和 是化合物,不互为同素异形体,故D错误;
故选B。
2.(2020·湖北沙区·沙市中学月考)由同一种元素所构成的不同单质被称为同素异形体,下列哪组物质不
属于同素异形体的是( )
A.钢和铁 B.金刚石和石墨 C.红磷和白磷 D.氧气和臭氧
【答案】A
【解析】A.钢和铁都是铁和碳的合金,是混合物,不是单质,不能互为同素异形体,A正确;
B.金刚石和石墨都是由碳元素形成的不同物质,都是单质,互为同素异形体,B错误;
C.红磷和白磷都是由磷元素形成的不同物质,都是单质,互为同素异形体,C错误;
D.氧气与臭氧都是由氧元素形成的不同物质,都是单质,互为同素异形体,D错误;
答案选A。
3.(2020·防城港市防城中学期中)按照要求将相应序号填入空白中:①35Cl ②金刚石 ③CO
④CO ⑤37Cl ⑥ ⑦SO ⑧ ⑨石墨。其中________互为同位素,________为酸性氧化物,
2 2
________的质量数相等,但不能互为同位素,________互称同素异形体。【答案】①⑤ ④⑦ ⑥⑧ ②⑨
【解析】同位素为同种元素的不同核素,质子数相同,质量数(或中子数)不同,所以互为同位素的为①和
⑤;和酸发生复分解反应生成盐和水的氧化物为酸性氧化物,④、⑦为酸性氧化物;原子符号左上角数字
代表质量数,⑥、⑧质子数分别为6、7,质量数都为14,质量数相等,但不能互为同位素;同种元素形成
的不同单质为同素异形体,②、⑨为碳元素的不同单质,互为同素异形体。